方案详情
文
去氧胆酸和CTAB均为弱紫外(无紫外)吸收且具有一定毒性的化合物。未经衍生的这类化合物难以用UV/Vis检测和定量。欧洲药典采用衍生-UV/Vis方法检测疫苗中去氧胆酸含量,CTAB检测方法缺乏。疫苗基质复杂,UV/Vis检测方法受基质干扰较大,灵敏度和重复性受到极大的限制。通用型检测器可用于弱紫外化合物的直接检测,无须衍生。但该类检测器灵敏度较低且受基质干扰较大,不适合疫苗基质中微量残留物质的检测。LC-MS/MS兼具LC的分离能力,又具有前体离子和产物离子双重选择性(MRM模式),可提高检测的准确性和抗基质干扰能力,适合快速检测方法的发展。
方案详情

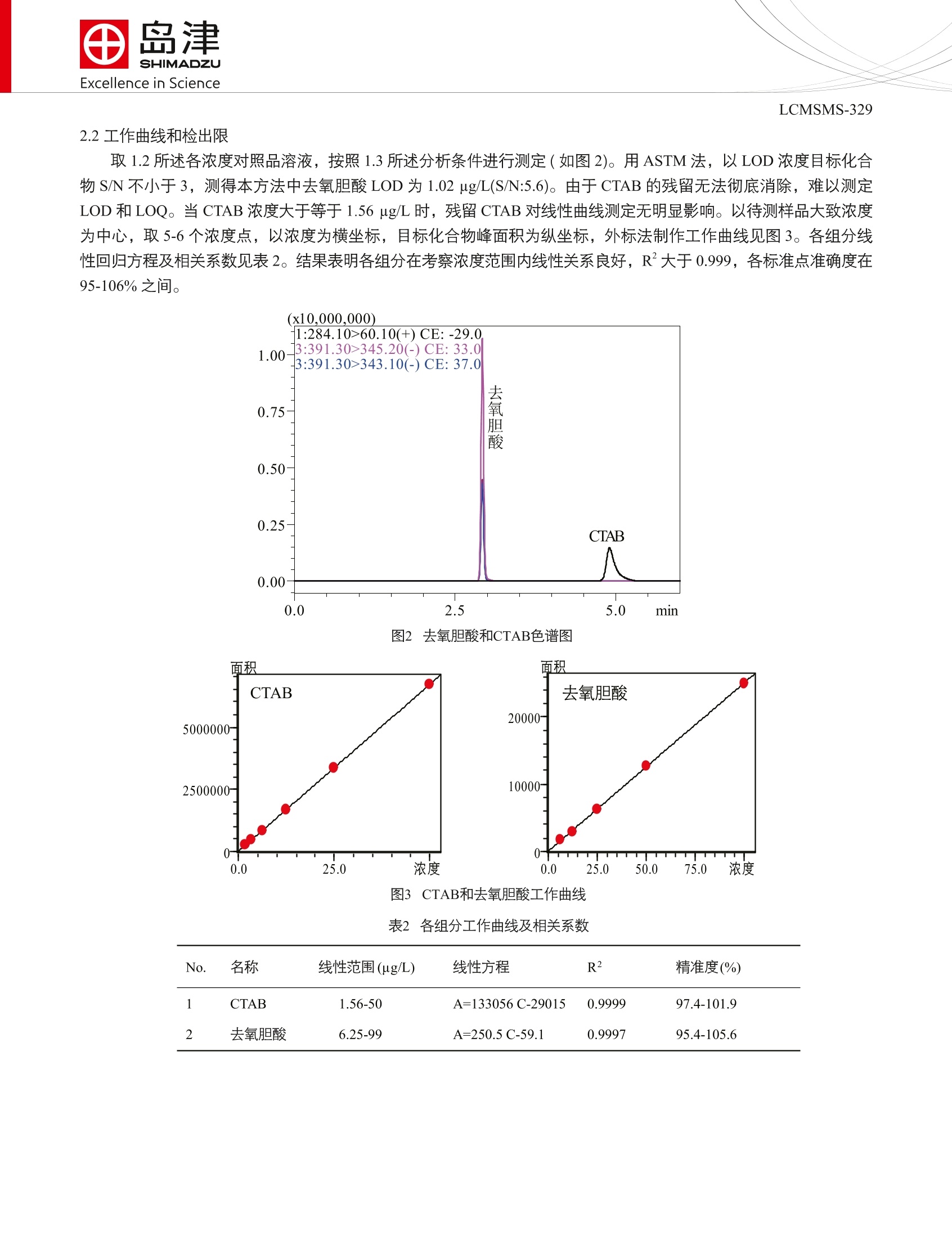
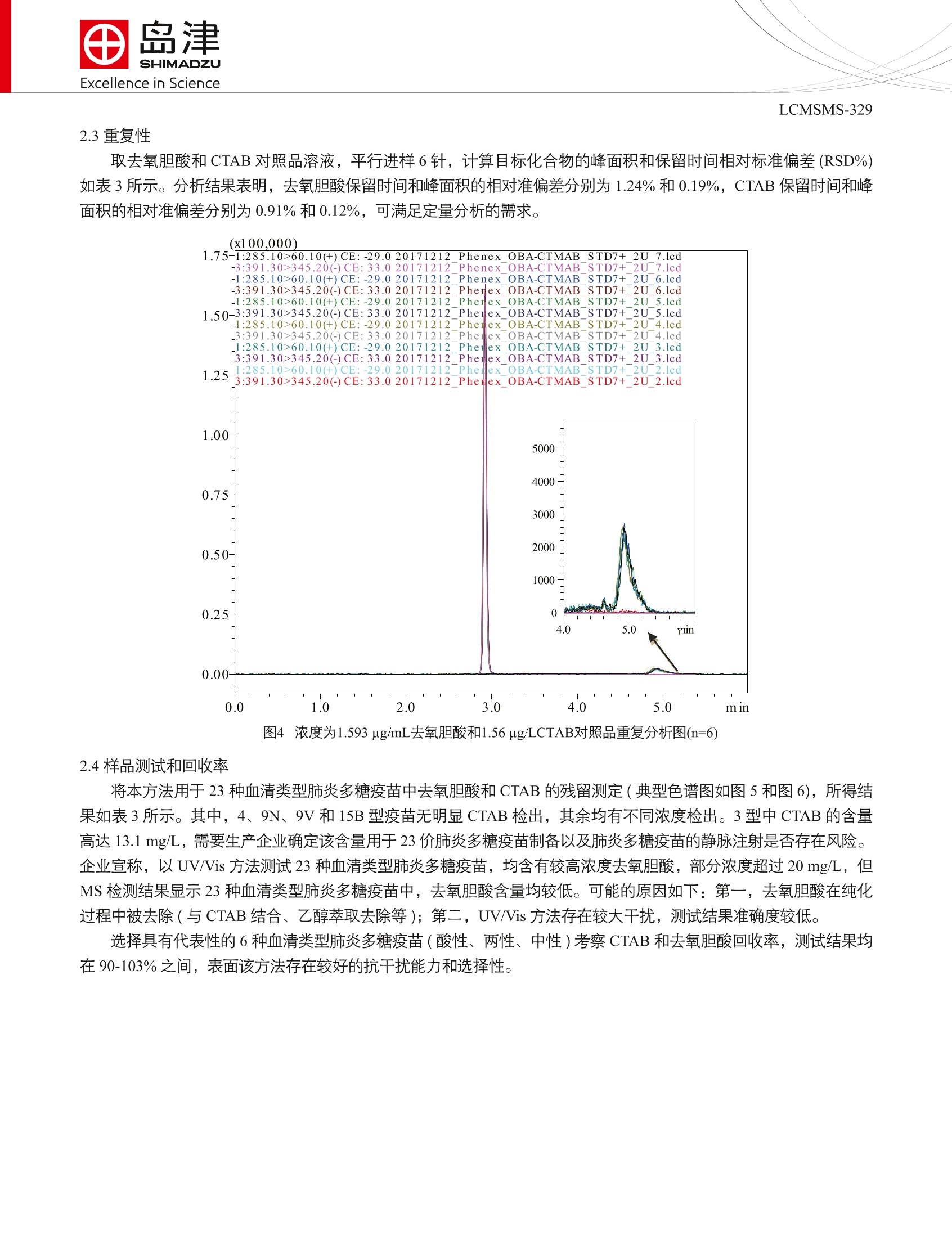
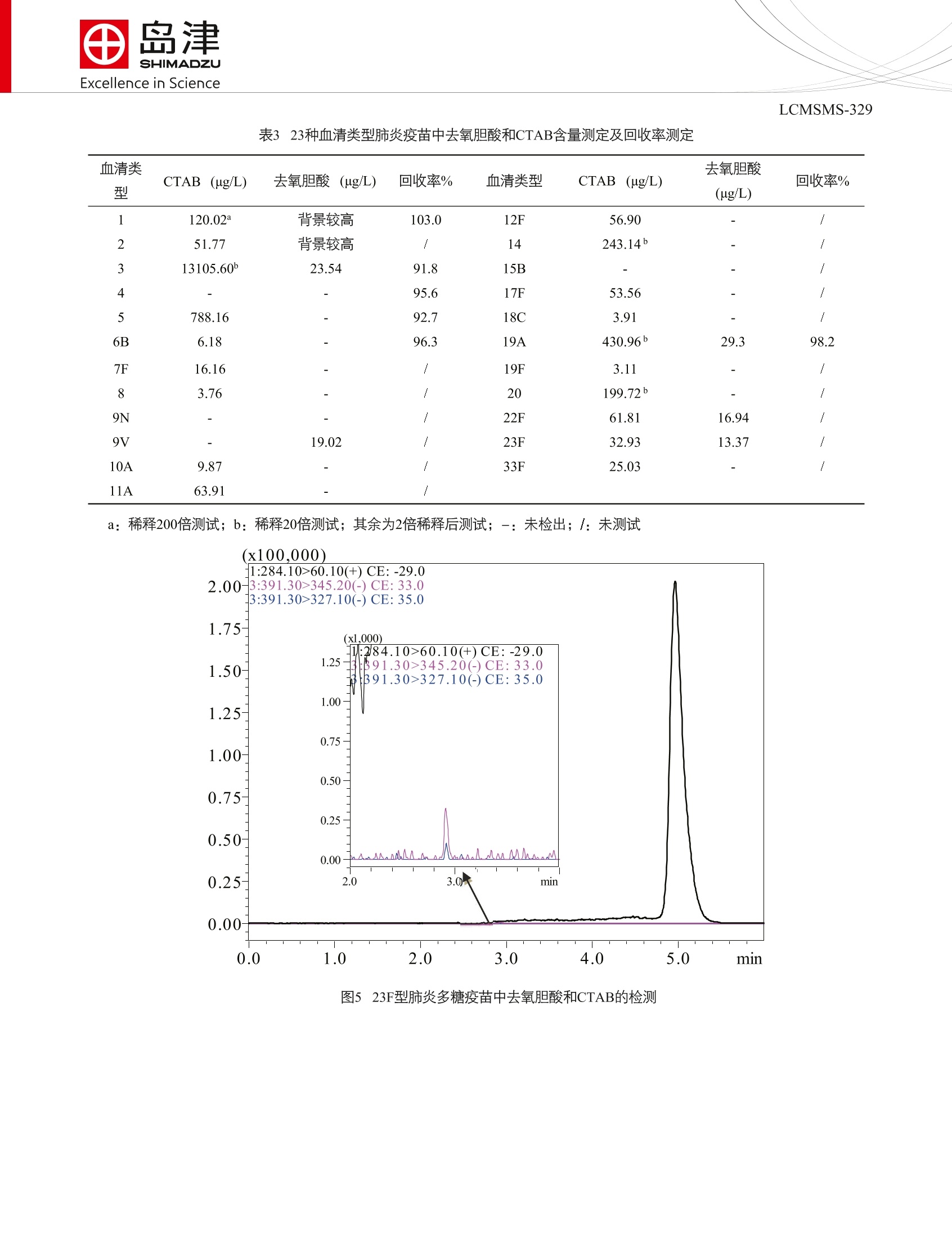
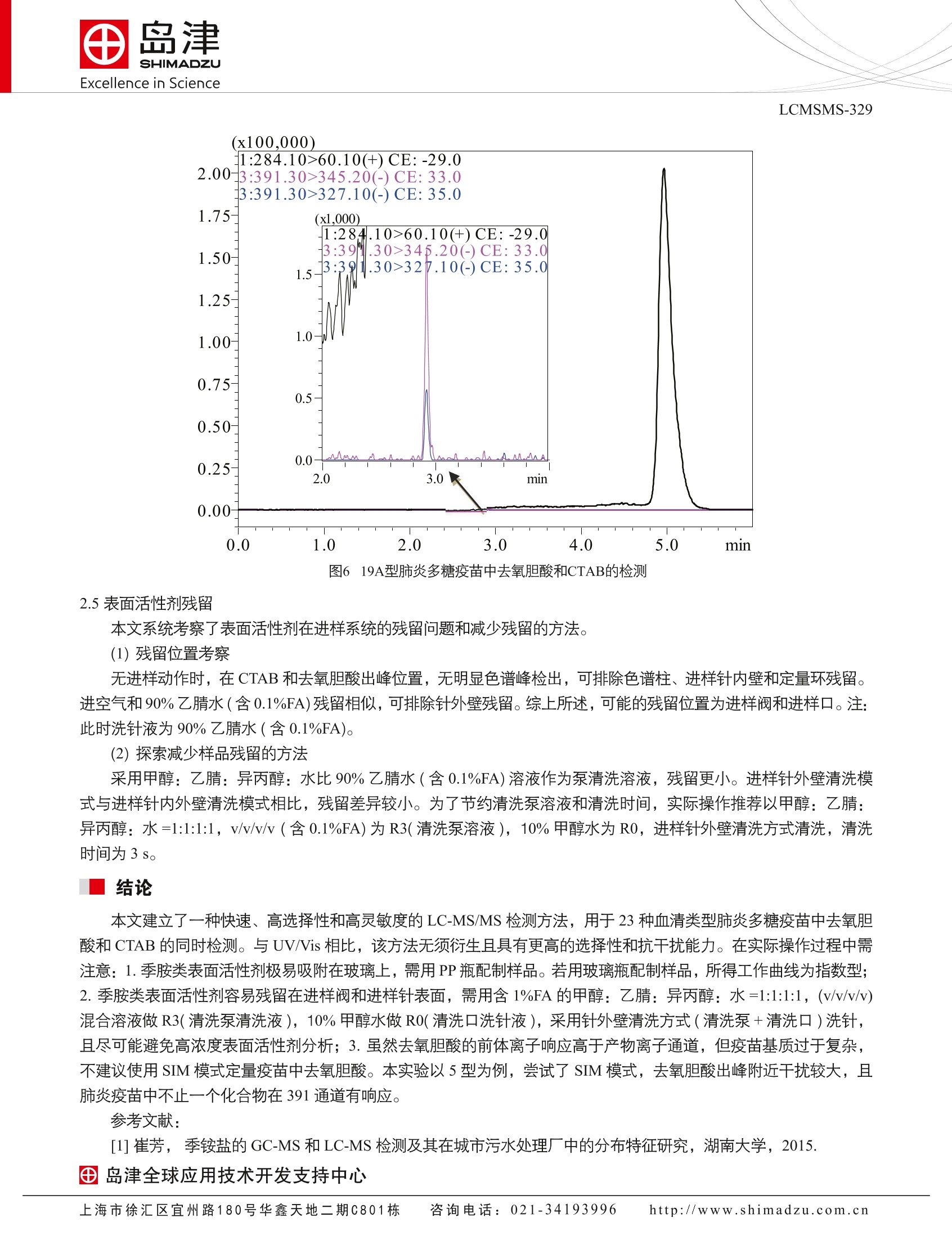
SSL-CA14-646Excellence in Science Excellence in ScienceLCMSMS-329 上海市徐汇区宜宜路180号华鑫天地二期C801栋 咨询电话:021-34193996 http://www.shimadzu.com.cn LC-MS/MS 同时定量肺炎多糖疫苗中去氧胆酸和十六烷基三甲基溴化铵 LCMSMS-329 摘要:本文用LCMS-8045 发展了一种肺炎多糖疫苗中去氧胆酸和十六烷基三甲基溴化铵(CTAB)的快速定量方法。相对于传统方法,本方法具有更好的抗基质干扰能力、更高的选择性和灵敏度。本方法具有较宽的线性范围(1.56-50ug/L)、较好的重复性(<2%)、较好的回收率(90%-103%)和较高的检测灵敏度。此外,本文还系统考察了 CTAB 在液相系统的残留和排除方法。 关键词:LCMSMS 肺炎多糖疫苗十六烷基三甲基溴化铵(CTAB)去氧胆酸 23价肺炎多糖疫苗是23种血清类型肺炎多糖疫苗的混合物,被称为疫苗史上的路标性疫苗。23种血清类型包括1、2、3、4、5、6B、7F、8、9N、9V、10A、11A、12F、14、15B、17A、18C、19A、19F、20、22F、23F 和33F。自20世纪80年代研发以后,被广泛用于2-60岁人群的免疫。在过去的40年间,23价肺炎多糖疫苗挽救和延长了大量生命,尤其是老人和艾滋病患者。据统计,55岁以下人群注射23价肺炎多糖疫苗,可获得5年甚至更长的免疫,降低85%的肺炎感染率。由于适用人群较广、效果较好、且肺炎为全球高发生率疾病,23价肺炎多糖疫苗至今仍是全球排名前十的高销量疫苗品种之一。 23价肺炎多糖疫苗从收获到最终产品,一般经历以下几个环节:1.终止液体培养(去氧胆酸杀菌);2.连续流离心,收集上清液(加入十六烷基三甲基溴化铵,CTAB);3.连续流离心,收集沉淀的复合多糖;4.复合多糖解聚(加入CaCl, 或 NaCl);5.加冷乙醇至25%,去除沉淀的核酸、杂质;6.收获离心上清液,补加冷乙醇至70%-80%,沉淀收获粗多糖;7.收获离心沉淀的粗多糖(加入醋酸钠溶液溶解);8.加2倍体积的预冷 苯酚溶液,抽提去除蛋白;9.吸取多糖-醋酸钠溶液相,重复苯酚抽提2-4次;10.于最后一次多糖-醋酸钠溶液相中加冷乙醇至70%-80%;11.离心收集沉淀,注射用水溶解;12.0.22 u.m膜除菌过滤,精制多糖原液;13.-20℃以下冷冻保存。去氧胆酸和 CTAB均为弱紫外(无紫外)吸收且具有一定毒性的化合物。未经衍生的这类化合物难以用 UV/Vis 检测和定量。欧洲药典采用衍生-UV/Vis 方法检测疫苗中去氧胆酸含量, CTAB检测方法缺乏。疫苗基质复杂, UV/Vis 检测方法受基质干扰较大,灵敏度和重复性受到极大的限制。通用型检测器可用于弱紫外化合物的直接检测,无须衍生。但该类检测器灵敏度较低且受基质干扰较大,不适合疫苗基质中微量残留物质的检测。LC-MS/MS 兼具 LC 的分离能力,又具有前体离子和产物离子双重选择性(MRM模式),可提高检测的准确性和抗基质干扰能力,适合快速检测方法的发展。 本文建立了一种LC-MS/MS 方法,采用液相分离、MRM 模式检测,实现23中血清类型肺炎多糖疫苗中去氧胆酸和 CTAB的时时、准确、快速定量,为该类疫苗的质量控制提供新思路、新方法。 1.1仪器 LC-20ADXR(高压二元泵), SIL-30ACMP(自动进样器),CTO-20AC(柱温箱), CBM-20A(系统控制器);LCMS-8045(三重四极杆质谱仪)配ESI电离源; LabSolutions Ver5.86( 色谱工作乍)。 图1 CTAB和去氧胆酸结构 1.2样品信息 对照品溶液:分别称取适量 CTAB(hexadecyltrimethyl ammonium Bromide, 购自 Sigma, CAS#: 57-09-0)和去氧胆酸 (deoxycholic acid, 购自 Sigma, CAS #:83-44-3)对照品,用50%乙腈水配制成 10 mg/L 的母液备用。取母液适量,用50%乙腈水溶液逐级容释、配制成浓度为50、25、12.5、6.25、3.13、1.56、0.78、0.39、0.185、0.093 和0.046ug/L 的对照品溶液。 重复性:浓度为1.56 ug/L样品重复进样6针。 实际样品:取样品,用50%乙腈水稀释2-200倍,进样分析。 加标回收:取100 ug/L对照品母液100uL,用0%乙腈水稀释到1mL(对照);取900 uL样品,加入100 uL50%乙腈水(样品);取900pL样品,加入100 pL 100 ug/L 对照品母液(加标样品)。回收率=((A加标样品-A样品)/A 对照)×100%。A:目标化合物峰面积。 1.3分析条件 色谱条件质谱条件色谱柱: PhenomenexKinetex C8 (2.1 x 50 mm,离子源: ESI,正和负模式2.6 um)雾化气流速:3.0L/min流动相: A-5mM 甲酸铵(pH4.0); B-乙腈干燥气流速:10L/min柱温:35℃驻留时间:30 ms梯度:0-1.0 min 40%B; 1.0-3.0 min 90%B;接口温度:300℃3.0-4.0 min 90%B;4.0-4.1 min 90%-MRM参数:见表140%B;4.1-6.0 min 40%BDL温度:220℃流速:0.3 mL/min接口电压:4.0kV 进样体积:2uL 进样清洗:泵清洗(进样前后清洗) 表1MRM参数 No. 名称 英文名称 CAS No. 前体离子 产物离子 Q1 Pre CE(V) Q3 Pre Bias(V) Bias(V) 1 CTAB hexadecyl trimethyl 57-09-0 284.3 60.1 -15 -29 -24 ammonium Bromide 2 去氧胆酸 deoxycholic acid 83-44-3 391.3 345.2 15 33 22 327.1 15 35 20 *表示定量离子 结果与讨论 2.1分析条件优化 大部分血清类型的肺炎多糖疫苗为强极性且强电荷聚合物,该类化合物在 C18固定相上以拖尾峰从死时间开始洗脱。为了快速洗脱目标化合物且减少基质干扰,在起始时间保持1 min 等度,用于强极性、强电荷物质的洗脱。去氧胆酸和CTAB 极性相差较大,为了实现快速分析,且避免过陡梯度造成的基线波动影响 CTAB 定量,使用1 min快速梯度。 以甲酸铵为流动相添加剂,去氧剂酸可获得多个碎片,其中345.2, 343.1,327.1,373.4和355.2在多个 CE值条件下均稳定出现。选择响应最强的345.2和327.1作为定量离子和参比离子。CTAB 为季铵型表面活性剂,在 scan 模式中,可观察到 m/z 为 284.3的M*峰和 m/z 为285.3的[M+H]*峰,其中M峰强度明显高于[M+H]*峰。无论以285.3还是284.3为前体离子均只能得到 m/z 为 60.1的产物离子。以上关于 CTAB 的前体离子和产物离子选择,与文献报道和化合物结构一致[1]。 2.2工作曲线和检出限 取1.2所述各浓度对照品溶溶,按照1.3所所分析条件进行测定(如图2)。用ASTM 法,以 LOD 浓度目标化合物 S/N 不小于3,测得本方法中去氧胆酸 LOD 为 1.02 ug/L(S/N:5.6)。由于 CTAB 的残留无法彻底消除,难以测定LOD 和LOQ。当 CTAB 浓度大于等于1.56 ug/L 时, 残留 CTAB 对线性曲线测定无明显影响。以待测样品大致浓度为中心,取5-6个浓度点,以浓度为横坐标,目标化合物峰面积为纵坐标,外标法制作工作曲线见图3。各组分线性回归方程及相关系数见表2。结果表明各组分在考察浓度范围内线性关系良好, R²大于0.999, 各标准点准确度在95-106%之间。 图2去氧胆酸和CTAB色谱图 图3 CTAB和去氧胆酸工作曲线 表2:各组分工作曲线及相关系数 No. 名称 线性范围(ug/L) 线性方程 R2 精准度(%) 1 CTAB 1.56-50 A=133056 C-29015 0.9999 97.4-101.9 2 去氧胆酸 6.25-99 A=250.5C-59.1 0.9997 95.4-105.6 2.3重复性 取去氧胆酸和 CTAB对照品溶液,平行进样6针,计算目标化合物的峰面积和保留时间相对标准偏差(RSD%)如表3所示。分析结果表明,去氧胆酸保留时间和峰面积和相对准偏差分别为1.24%和0.19%, CTAB 保留时间和峰面积的相对准偏差分别为0.91%和0.12%,可满足定量分析的需求。 图44浓度为1.593 ug/mL去氧胆酸和1.56 ug/LCTAB对照品重复分析图(n=6) 2.4样品测试和回收率 将本方法用于23种血清类型肺炎多糖疫苗中去氧胆酸和 CTAB 的残留测定(典型色谱图如图5和图6),所得结果如表3所示。其中,4、9N、9V和15B型疫苗无明显 CTAB 检出,其余均有不同浓度检出。3型中 CTAB 的含量高达13.1 mg/L, 需要生产企业确定该含量用于23价肺炎多糖疫苗制备以及肺炎多糖疫苗的静脉注射是否存在风险。企业宣称,以UV/Vis方法测试23种血清类型肺炎多糖疫苗,均含有较高浓度去氧胆酸,部分浓度超过20 mg/L, 但MS 检测结果显示23种血清类型肺炎多糖疫苗中,去氧胆酸含量均较低。可能的原因如下:第一,去氧胆酸在纯化过程中被去除(与 CTAB 结合、乙醇萃取去除等);第二, UV/Vis 方法存在较大干扰,测试结果准确度较低。 选择具有代表性的6种血清类型肺炎多糖疫苗(酸性、两性、中性)考察 CTAB 和去氧胆酸回收率,测试结果均在90-103%之间,表面该方法存在较好的抗干扰能力和选择性。 表323种血清类型肺炎疫苗中去氧胆酸和CTAB含量测定及回收率测定 血清类 CTAB (ug/L) 去氧胆酸 (ug/L) 回收率% 血清类型 CTAB (ug/L) 去氧胆酸 回收率% 型 (ug/L) 120.02 背景较高 103.0 12F 56.90 / 51.77 背景较高 14 243.146 / 13105.60 23.54 91.8 15B 4 95.6 17F 53.56 / 5 788.16 92.7 18C 3.91 / 6B 6.18 96.3 19A 430.966 29.3 98.2 7F 16.16 / 19F 3.11 / 8 3.76 20 199.726 9N / 22F 61.81 16.94 9V 19.02 23F 32.93 13.37 10A 9.87 33F 25.03 / 11A 63.91 / a:稀释200倍测试; b:稀释20倍测试;其余为2倍稀释后测试;-:未检出;/:未测试 图5523F型肺炎多糖疫苗中去氧胆酸和CTAB的检测 图66119A型肺炎多糖疫苗中去氧胆酸和CTAB的检测 2.5表面活性剂残留 本文系统考察了表面活性剂在进样系统的残留问题和减少残留的方法。 (1)残留位置考察 无进样动作时,在 CTAB 和去氧胆酸出峰位置,无明显色谱峰检出,可排除色谱柱、进样针内壁和定量环残留。进空气和90%乙腈水(含0.1%FA)残留相似,可排除针外壁残留。综上所述,可能的残留位置为进样阀和进样口。注:此时洗针液为90%乙腈水(含0.1%FA)。 (2)探索减少样品残留的方法 采用甲醇:乙腈:异丙醇:水比90%乙腈水(含0.1%FA)溶液作为泵清洗溶液,残留更小。进样针外壁清洗模式与进样针内外壁清洗模式相比,残留差异较小。为了节约清洗泵溶液和清洗时间,实际操作推荐以甲醇:乙腈:异丙醇:水=1:1:1:1, v/v/v/v (含 0.1%FA) 为 R3(清洗泵溶液),10%甲醇水为R0,进样针外壁清洗方式清洗,清洗时间为3s。 结论 本文建立了一种快速、高选择性和高灵敏度的 LC-MS/MS 检测方法,用于23种血清类型肺炎多糖疫苗中去氧胆酸和 CTAB 的同时检测。与 UV/Vis 相比,该方法无须衍生且具有更高的选择性和抗干扰能力。在实际操作过程中需注意:1.季胺类表面活性剂极易吸附在玻璃上,需用PP瓶配制样品。若用玻璃瓶配制样品,所得工作曲线为指数型;2.季胺类表面活性剂容易残留在进样阀和进样针表面,需用含1%FA的甲醇:乙腈:异丙醇:水=1:1:1:1,(v/v/v/v)混合溶液做R3(清洗泵清洗液),10%甲醇水做 R0(清洗口洗针液),采用针外壁清洗方式(清洗泵+清洗口)洗针,且尽可能避免高浓度表面活性剂分析;3.虽然去氧胆酸的前体离子响应高于产物离子通道,但疫苗基质过于复杂,不建议使用 SIM 模式定量疫苗中去氧胆酸。本实验以5型为例,尝试了 SIM 模式,去氧胆酸出峰附近干扰较大,且肺炎疫苗中不止一个化合物在391 通道有响应。 ( 参考文献: ) [1]崔芳,季铵盐的 GC-MS 和 LC-MS 检测及其在城市污水处理厂中的分布特征研究,湖南大学,2015. ( 岛津全球应用技术开发支持中心 ) 去氧胆酸和CTAB均为弱紫外(无紫外)吸收且具有一定毒性的化合物。未经衍生的这类化合物难以用UV/Vis检测和定量。欧洲药典采用衍生-UV/Vis方法检测疫苗中去氧胆酸含量,CTAB检测方法缺乏。疫苗基质复杂,UV/Vis检测方法受基质干扰较大,灵敏度和重复性受到极大的限制。通用型检测器可用于弱紫外化合物的直接检测,无须衍生。但该类检测器灵敏度较低且受基质干扰较大,不适合疫苗基质中微量残留物质的检测。LC-MS/MS兼具LC的分离能力,又具有前体离子和产物离子双重选择性(MRM模式),可提高检测的准确性和抗基质干扰能力,适合快速检测方法的发展。
确定


还剩4页未读,是否继续阅读?
岛津企业管理(中国)有限公司为您提供《肺炎多糖疫苗中去氧胆酸、十六烷基三甲基溴化铵检测方案(液质联用仪)》,该方案主要用于化药制剂中含量测定检测,参考标准--,《肺炎多糖疫苗中去氧胆酸、十六烷基三甲基溴化铵检测方案(液质联用仪)》用到的仪器有岛津LCMS-8045三重四极杆液质联用仪
推荐专场
相关方案
更多
该厂商其他方案
更多
















