天冬酰胺 (Asn) 脱酰胺化、天冬氨酸 (Asp) 异构化和甲硫氨酸 (Met) 氧化等修饰是重组抗体的典型降解产物。研究表明,单克隆抗体中 Asn、Asp 和 Met 残基的降解会影响蛋白质活性。因此,蛋白质候选药物(例如 mAb)中的上述修饰是关键质量属性 (CQA),需在储存和制剂条件下进行密切监测。它们通常是药物开发过程中进行的影响因素试验和强制降解研究的重点。要评估上述 CQA,需要同时进行鉴定和定量分析。
本应用简报介绍了采用一体化工作流程(包括 Agilent AssayMAP Bravo 平台、Agilent 1290 Infinity II LC、Agilent 6545XT AdvanceBio LC/Q-TOF 和 Agilent MassHunter BioConfirm 软件),通过肽谱分析方法同时鉴定和定量分析重组 mAb的化学诱导脱酰胺化和氧化修饰。
方案详情

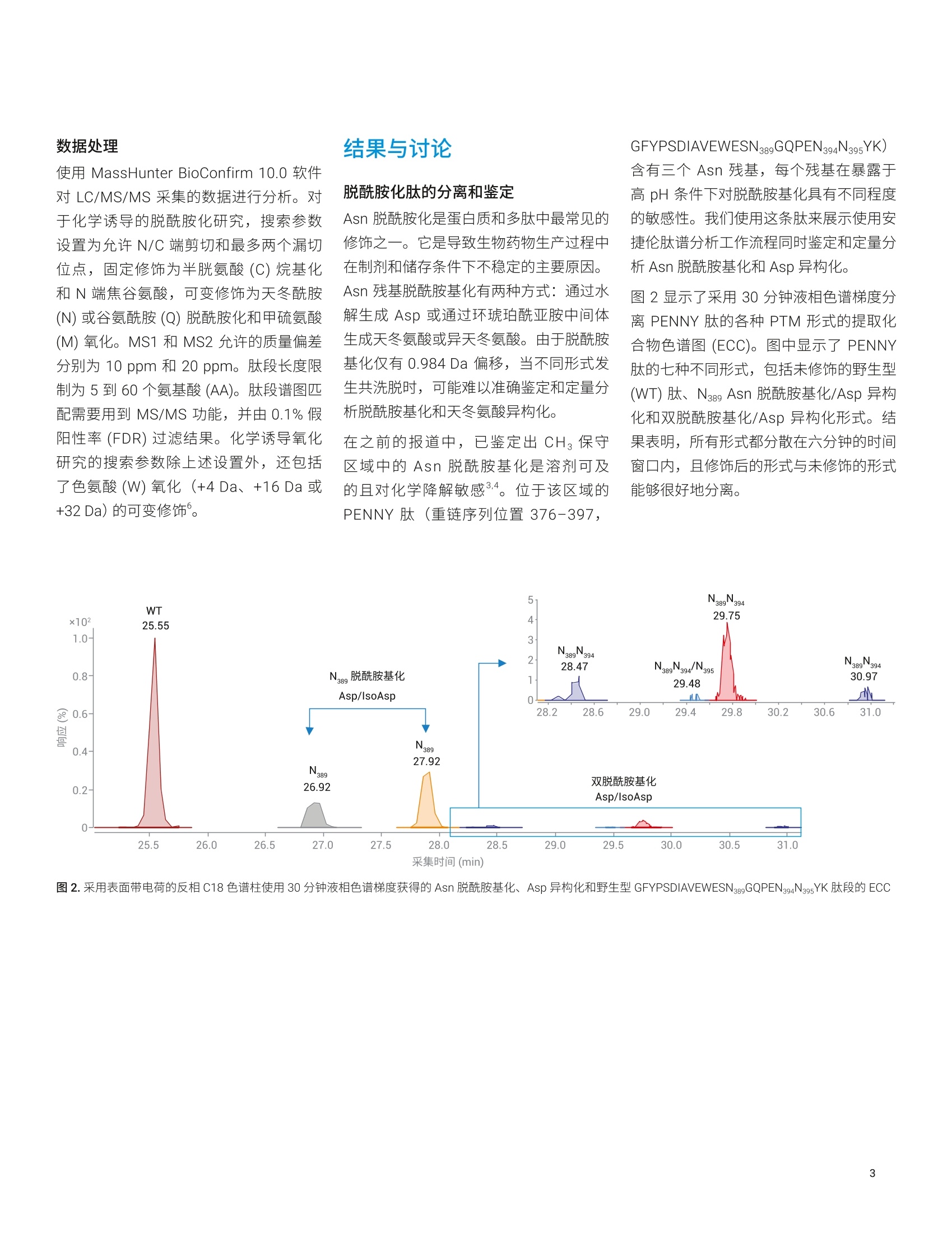
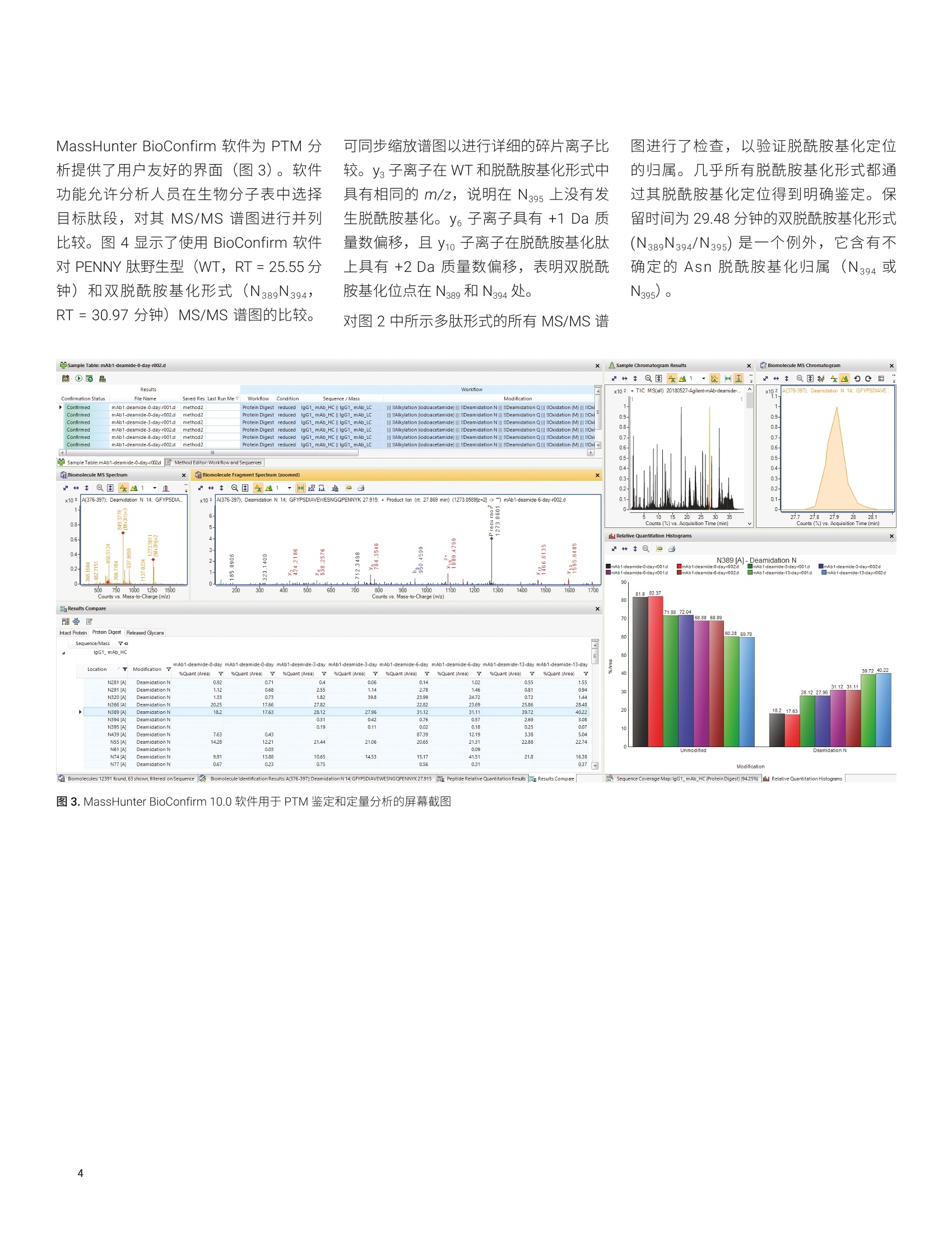
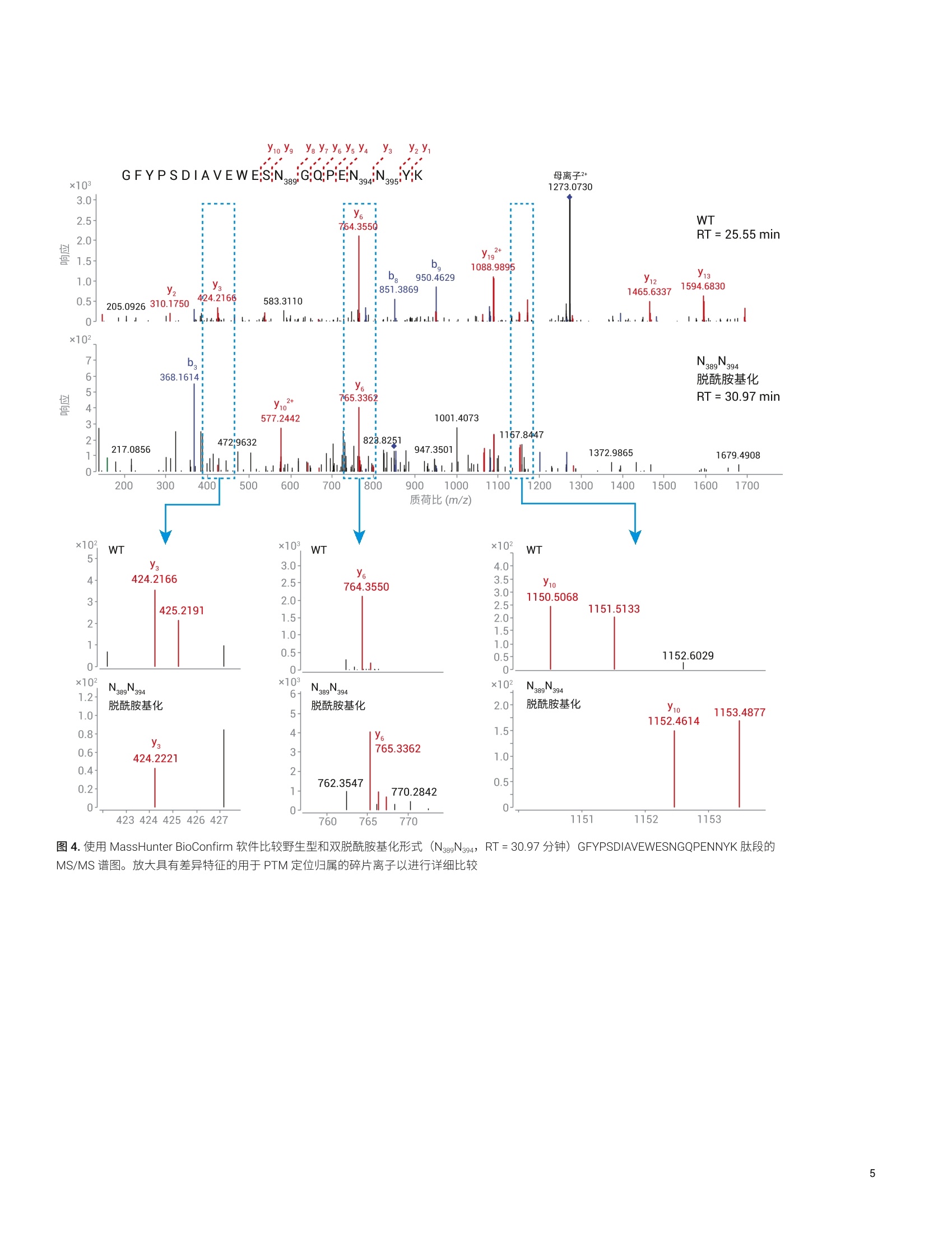
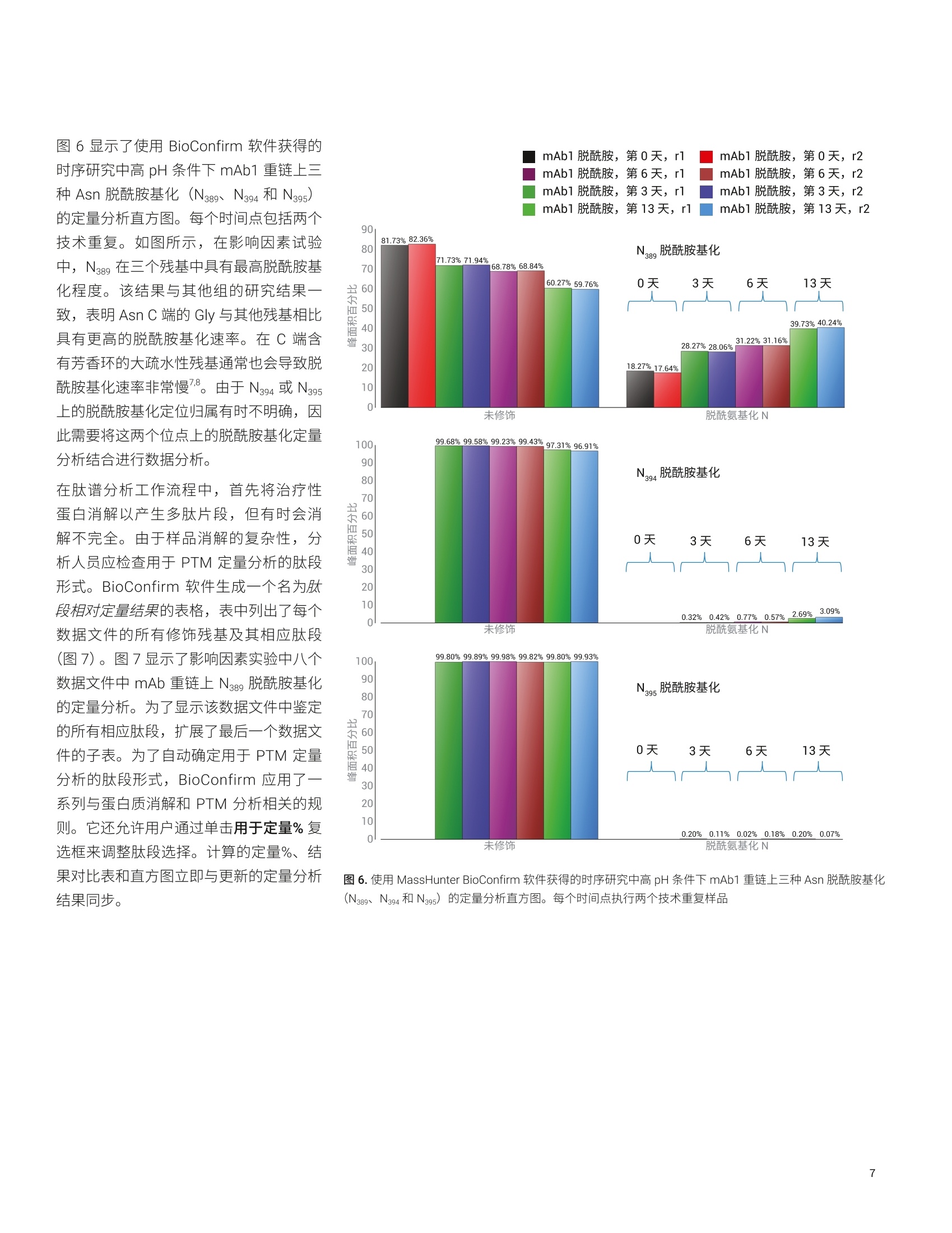
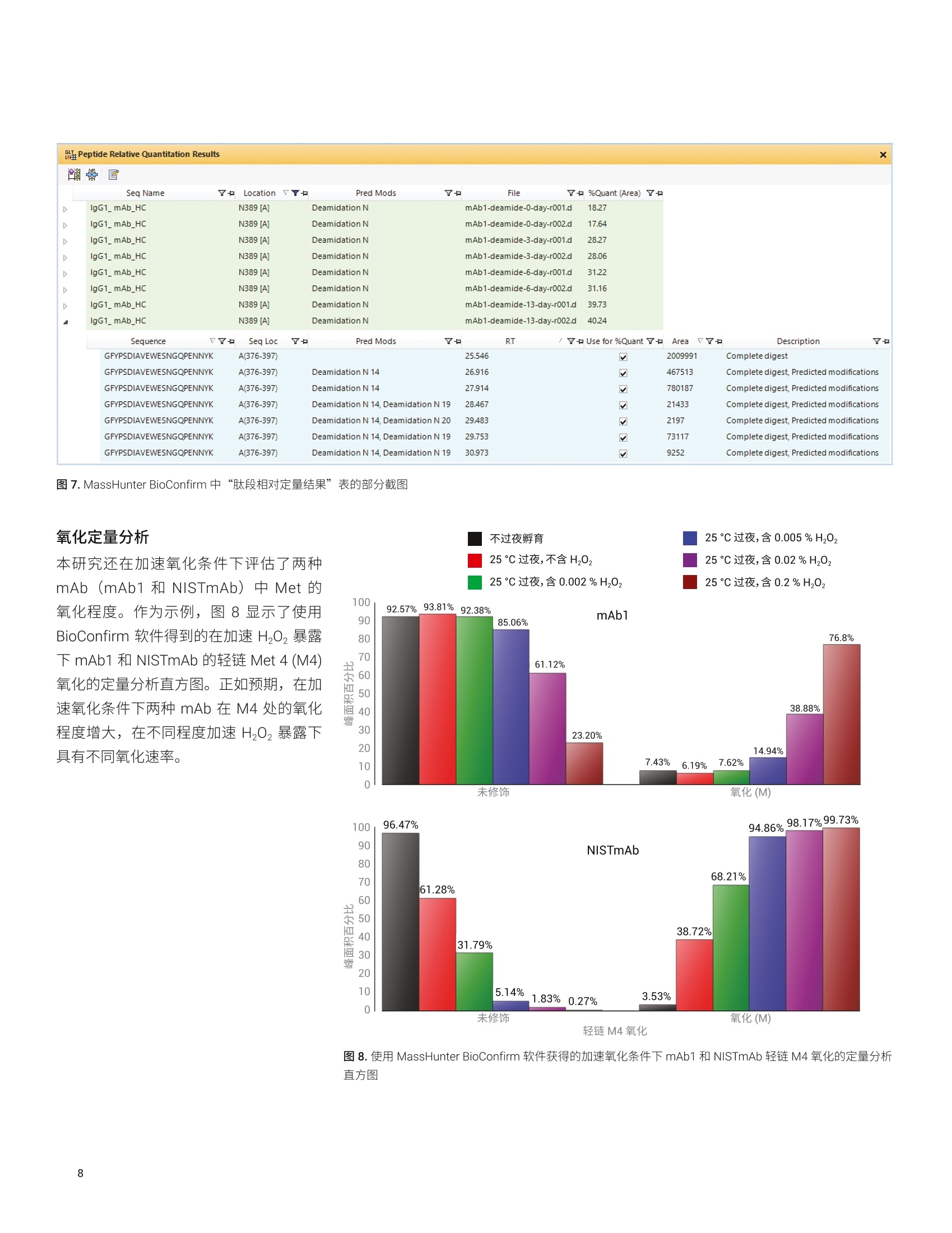
GFYPSDIAVEWESN389GQPEN394N395YK) y y2y 应用简报 Agilent生物治疗药物 Trusted Answers 单克隆抗体化学诱导脱酰胺化和氧化的定量分析 采用 Agilent 6545XT AdvanceBio LC/Q-TOF 和 AgilentMassHunter BioConfirm 软件 作者 前言 Linfeng Wu 安捷伦科技有限公司 Santa Clara, CA, USA 天冬酰胺 (Asn)脱酰胺化、天冬氨酸 (Asp) 异构化和甲硫氨酸 (Met) 氧化等修饰是重组抗体的典型降解产物。研究表明,单克隆抗体中 Asn、 Asp 和 Met 残基的降解会影响蛋白质活性1。因此,蛋白质候选药物(例如mAb) 中的上述修饰是关键质量属性(CQA),需在储存和制剂条件下进行密切监测。它们通常是药物开发过程中进行的影响因素试验和强制降解研究的重点。要评估上述 CQA,需要同时进行鉴定和定量分析。 本应用简报介绍了采用一体化工作流程(包括 Agilent AssayMAP Bravo 平台、Agilent 1290 Infinity II LC、Agilent 6545XT AdvanceBio LC/Q-TOF 和 AgilentMassHunter BioConfirm 软件),通过肽谱分析方法同时鉴定和定量分析重组 mAb的化学诱导脱酰胺化和氧化修饰(图1)。 图1.肽谱分析的一体化工作流程 材料 mAb1 样品为重组的 CHO 细胞培养的IgG1 mAb, 由第三方合作伙伴生产和纯化。NISTmAb 购自美国国家标准技术研究院(NIST)。 ( 仪器 ) ( Agilent AssayMAP Bravo 系统 (G5571AA) ) Agilent 1290 Infinity II液相色谱系统,包括: ·AAgilent 1290 Infinity lI 高速泵(G7120A) ·AAgilent 1290 Infinity IIMultisampler (G7167B), 配备样品冷却装置(选件100) ·AAgilent 1290 Infinity ⅡI柱温箱(G7116B) Agilent 6545XT AdvanceBioLC/Q-TOF (G6549A) 安捷伦双喷射流 ESI离子源(G1958-65268) 化学诱导和样品前处理 为了诱导显著水平的 Asn 脱酰胺化,将mAb1样品分别在 pH 8.7 的 Tris-HCI 缓冲液体系中暴露于较高温度(37°℃)下0、3、6和13天。为了诱导 Met 氧化,将 mAb1 和 NISTmAb 样品在含有不同浓度Hz0氧化剂(范围0%-0.2%v/v) 的Tris-HCI缓冲液中于室温下培养过夜。将所有样品冻干并储存在-80°℃,以待后续样品消解。 使用 AssayMAP Bravo 平台对所有样品进行还原、烷基化、胰蛋白酶消解和脱盐。再对消解样品进行 LC/MS 分析。 采用表面带电荷的安捷伦反相 C18色谱柱(2.1×150 mm, 2.7 pm) 进行 LC分离, 使用30分钟梯度(表1)。采用6545XTAdvanceBio LC/Q-TOF 采集原始数据(表2)。 表1.液相色谱参数 液相色谱参数 分析柱 表面带电荷的安捷伦反相 C18色谱柱 流动相A H,0,0.1%甲酸 流动相B 90%乙腈和0.1%甲酸的水溶液 柱温 60°C 流速 0.4 mL/min 梯度 0.0分钟时B为3% 30.0分钟时B为22% 32.0分钟时B为90% 35.0分钟时B为90% 37.0分钟时B为3% 停止时间 40 分钟 表2.质谱参数 参数 值 仪器 6545XTAdvanceBio LC/Q-TOF 气体温度 325°C 干燥气流速 13L/min 雾化器 35 psig 鞘气温度 275°℃ 鞘气流速 12 L/min 毛细管电压 4000V 喷嘴电压 OV 采集模式 扩展动态范围(2 GHz) 质量数范围 m/z 300-1700 采集速率 8张谱图/秒 自动 MS/MS范围 m/z 50-1700 最小MS/MS 采集速率 3张谱图/秒 分离峰宽 窄(约m/z1.3) 母离子/循环 前10 碰撞能量 对于电荷数为2的离子,为3.1*(m/z)/100+1;对于电荷数为3或大于3的离子,为3.6*(m/z)/100-4.8 MS/MS阈值 1000 响应值和 0.001% 动态排除开启 重复1次,然后排除 0.2 min 基于母离子丰度的扫描速率 是 目标值 25000响应值/质谱图 使用 MS/MS 累积时间限 是 纯度 严格性100%,截留率30% 同位素模型 肽段 母离子排序 先按电荷态,再按丰度进行排序;+2, +3,>+3 数据处理 使用 MassHunter BioConfirm 10.0 软件对 LC/MS/MS 采集的数据进行分析。对于化学诱导的脱酰胺化研究,搜索参数设置为允许N/C 端剪切和最多两个漏切位点,固定修饰为半胱氨酸(C)烷基化和N端焦谷氨酸,,I可变修饰为天冬酰胺(N)或谷氨酰胺(Q)脱酰胺化和甲硫氨酸(M)氧化。MS1 和 MS2 允许的质量偏差分别为 10 ppm和20 ppm。肽段长度限制为5到60个氨基酸 (AA)。肽段谱图匹配需要用到MS/MS功能,并由0.1%假阳性率(FDR)过滤结果。化学诱导氧化研究的搜索参数除上述设置外,还包括了色氨酸(W)氧化(+4 Da、+16 Da 或+32 Da) 的可变修饰。 脱酰胺化肽的分离和鉴定 Asn 脱酰胺化是蛋白质和多肽中最常见的修饰之一。它是导致生物药物生产过程中在制剂和储存条件下不稳定的主要原因。Asn 残基脱酰胺基化有两种方式:通过水解生成 Asp 或通过环琥珀酰亚胺中间体生成天冬氨酸或异天冬氨酸。由于脱酰胺基化仅有 0.984 Da偏移,当不同形式发生共洗脱时,可能难以准确鉴定和定量分析脱酰胺基化和天冬氨酸异构化。 在之前的报道中,已鉴定出CH。保守区域中的 Asn脱酰胺基化是溶剂可及的且对化学降解敏感3.4。位于该区域的PENNY肽(重链序列位置376-397, 含有三个 Asn 残基,每个残基在暴露于高pH条件下对脱酰胺基化具有不同程度的敏感性。我们使用这条肽来展示使用安捷伦肽谱分析工作流程同时鉴定和定量分析 Asn 脱酰胺基化和 Asp 异构化。 图2显示了采用30分钟液相色谱梯度分离 PENNY 肽的各种 PTM 形式的提仅化合物色谱图 (ECC)。图中显示了 PENNY肽的七种不同形式,包括未修饰的野生型(WT)肽、N389 Asn 脱酰胺基化/Asp 异构化和双脱酰胺基化/Asp 异构化形式。结果表明,所有形式都分散在六分钟的时间窗口内,且修饰后的形式与未修饰的形式能够很好地分离。 MassHunter BioConfirm 软件为 PTM分析提供了用户友好的界面(图3)。软件功能允许分析人员在生物分子表中选择目标肽段,对其 MS/MS 谱图进行并列比较。图4显示了使用 BioConfirm 软件对 PENNY 肽野生型 (WT, RT=25.55分钟)和和脱酰胺基化形式(N389N394)RT=30.97分钟) MS/MS 谱图的比较。 可同步缩放谱图以进行详细的碎片离子比较。ys子离子在 WT和脱胺基化形式中具有相同的 m/z, 说明在 N395上没有发生脱酰胺基化。y6子离子具有+1 Da 质量数偏移,且y1o子离子在脱酰胺基化肽上具有+2 Da 质量数偏移,表明双脱酰胺基化位点在 N389 和N394 处。 对图2中所示多肽形式的所有 MS/MS 谱 图进行了检查,以验证脱酰胺基化定位的归属。几乎所有脱酰胺基化形式都通过其脱酰胺基化定位得到明确鉴定。保留时间为29.48分钟的双脱酰胺基化形式(N389N394/N395)是一个例外,它含有不确定的 Asn 脱酰胺基化归属(N394或N395). Locatio YM Modifica %Quant (Area ea) T9 %Quant (Area] Y% %Quant (Area) %Quant (Area ea) 1%Quant (Area a)了 %Quant (Area) 丫 %Quant (Area) Y % %Quant (Area) x102: + TIC MS(all) 20180527-Agilent-mAb-deamide 0.9-0.8-0.7-0.60.5-0.4-03-0.2-0.1- 10 15 2025 0.9-0.8-0.7-0.60.50.403-0.2- 0.1- N281A 27.727.827.928 28.1 Deamidation N 0.92 0.71 0.06 0.14 0.55 1.55 N291 [A] Deamidation N 1.12 i 11 .78 146 i1 0.9 N320 [A] Deamidation N 1.33 0.73 182 23.99 24.72 0.72 1.44 N366 [A] Deamidation N 20.25 17.66 27.82 22.82 23.69 25.86 28.48 N389 A] Deamidation N 18.2 17.53 28.12 27.96 31.12 3p11.11 39.72 40.22 N394A] Deamidation N 0.31 042 0.76 0.57 2.69 3.08 N395A Deamidation N 0.1119 0.11 0.02 0.18 0.25 0.07 N439A DeamidationN 7.63 043 87.39 12.19 ,288 5.04 N55 [A] Deamidattiion 14.28 12.21 2144 21.06 20.65 21331 22.74 N61 [A] Deamidation N 0.03 0.09 N74 [A] Deamidation N 9.91 13.88 10.65 14.53 15.17 41.51 21.8 16.38 N77 AI Deamidation N 0.67 0.23 0.75 0.56 0.31 0.37 图4.使用 MassHunter BioConfirm 软件比较野生型和双脱酰胺基化形式 (N389N394, RT=30.97分钟) GFYPSDIAVEWESNGQPENNYK 肽段的MS/MS 谱图。放大具有差异特征的用于PTM 定位归属的碎片离子以进行详细比较 脱酰胺化定量分析 MassHunter BioConfirm 软件使分析人员能够定量分析一系列样品的所有修饰残基的 PTM 程度。它计算修饰肽相对于修饰和未经修饰形式总和的峰面积百分比(或峰高百分比作为一个选项)。它还将比较结果汇总于表中(图5)。通过此“结果对比”表,分析人员可了解一系列样品所有修饰残基的 PTM 定量分析结果。除“结果对比”表外, BioConfirm 还可使用直方图显示定量分析结果。要显示每个修饰残基的直方图,用户只需在“结果对比”表中单击目标残基行。 图 5. PTM定量的“结果对比”表,显示了在高pH条件下一段时间内 mAb1 重链和轻链中 Asn 脱酰胺基化的定量分析比较 图6显示了使用 BioConfirm 软件获得的 mAb1脱酰胺,第0天, r1 mAb1脱酰胺,第0天, r2 时序研究中高 pH 条件下 mAb1 重链上三种 Asn 脱酰胺基化 (N389、 N394 和N395)的定量分析直方图。每个时间点包括两个技术重复。如图所示,在影响因素试验中,N38g在三个残基中具有最高脱酰胺基化程度。该结果与其他组的研究结果一致,表明 Asn C 端的 Gly 与其他残基相比具有更高的脱酰胺基化速率。在C端含有芳香环的大疏水性残基通常也会导致脱酰胺基化速率非常慢。由于 N394或 N395上的脱酰胺基化定位归属有时不明确,因此需要将这两个位点上的脱酰胺基化定量分析结合进行数据分析。 mAb1脱酰胺,第6天, r1 mAb1脱酰胺,第6天, r2 mAb1 脱酰胺,第3天, r1 mAb1脱酰胺,第3天, r2 在肽谱分析工作流程中,首先将治疗性蛋白消解以产生多肽片段,但有时会消解不完全。由于样品消解的复杂性,分析人员应检查用于 PTM 定量分析的肽段形式。BioConfirm 软件生成一个名为肽段相对定量结果的表格,表中列出了每个数据文件的所有修饰残基及其相应肽段(图7)。图7显示了影响因素实验中八个数据文件中 mAb 重链上N389脱酰胺基化的定量分析。为了显示该数据文件中鉴定的所有相应肽段,扩展了最后一个数据文件的子表。为了自动确定用于 PTM 定量分析的肽段形式, BioConfirm 应用了一系列与蛋白质质解和 PTM 分析相关的规则。它还允许用户通过单击用于定量%复选框来调整肽段选择。计算的定量%、结果对比表和直方图立即与更新的定量分析结果同步。 图6.使用 MassHunter BioConfirm 软件获得的时序研究中高 pH条件下 mAb1 重链上三种 Asn 脱酰胺基化(N389、N3o4和N395)的定量分析直方图。每个时间点执行两个技术重复样品 IgG1_mAb_HC Sequence VY Seq Loc Pred Mods RT Y口Use for %Quant 了口 Area V了 Description 了 GFYPSDIAVEWESNGQPENNYK A(376-397) Deamidation N 25.546 2009991 Complete digest GFYPSDIAVEWESNGQPENNYK A(376-397) Deamidation N 14 26.916 467513 Complete digest, Predicted modifications GFYPSDIAVEWESNGQPENNYK A(376-397) Deamidation N 14 27.914 780187 Complete digest, Predicted modifications GFYPSDIAVEWESNGQPENNYK A(376-397) Deamidation N 14,Deamidation N 19 28.467 21433 Complete digest, Predicted modifications GFYPSDIAVEWESNGOPENNYK A(376-397) Deamidation N 14, Deamidation N 20 29.483 2197 Complete digest, Predicted modifications GFYPSDIAVEWESNGQPENNYK A(376-397) Deamidation N 14, Deamidation N 19 29.753 73117 Complete digest, Predicted modifications GFYPSDIAVEWESNGQPENNYK A(376-397) Deamidation N 14,Deamidation N 19 30.973 9252 Complete digest, Predicted modifications IgG1_mAb_HC N389 [A] Deamidation N mAb1-deamide-13-day-r002.d 40.24 图7.MassHunter BioConfirm 中“肽段相对定量结果”表的部分截图 氧化定量分析 本研究还在加速氧化条件下评估了两种mAb (mAb1和 NISTmAb)中 Met的氧化程度。作为示例,图8显示了使用BioConfirm 软件得到的在加速 H,0,暴露下 mAb1 和 NISTmAb 的轻链Met 4 (M4)氧化的定量分析直方图。正如预期,在加速氧化条件下两种mAb 在 M4 处的氧化程度增大,在不同程度加速 Hz0, 暴露下具有不同氧化速率。 图 8.使用 MassHunter BioConfirm 软件获得的加速氧化条件下mAb1 和 NISTmAb 轻链M4氧化的定量分析直方图 本文展示了一套用于同时鉴定和定量分析 mAb 的化学诱导脱酰胺基化和氧化的完整工作流程,包括使用 AssayMAPBravo 平台进行自动化样品前处理,使用 1290 Infinity ll 液相色谱仪进行液相色谱分离,使用6545XT AdvanceBioLC/Q-TOF 进行数据采集, 以及使用MassHunter BioConfirm 软件进行数据分析。MassHunter BioConfirm 10.0软件能够: 自动进行数据批处理 使用统计得分和FDR 进行肽段谱图匹配 将结果表通过链接导航链接到质谱图和色谱图 进行PTM定量分析 上述功能组合提升了蛋白类生物治疗药物开发和生产过程中肽谱分析和 PTM 定量分析工作流程的效率。 ( 参考文献 ) ( 1. Huang, L.; et al. In vivo deamidation characterization of monoclonal antibody by LC/MS/MS. A nal. Chem.2005,77(5), 1432-1439 ) 2. Vlasak, J.; et al. Identification andcharacterization of asparaginedeamidation in the light chain CDR1of a humanized IgG1 antibody.Anal.Biochem.2009,392(2),145-154 ( 3. Diepold, K.; e t a l . SimultaneousAssessment of Asp Isomerization and Asn Deamidation in Recombinant Antibodies by LC-MSfollowing Incubation at ElevatedTemperatures. PLoS One 2012,7(1):e30295 ) ( 4. Haberger, M.; et al. Assessment of chemical modifications of sites in t he CDRs of recombinant antibodies: Susceptibility vs. f unctionality ofcritical quality attributes. MAbs.2014,6(2),327-339 ) Automation of Sample Preparation for Accurate and ScalableQuantification and Characterizationof Biotherapeutic Proteins Using theAgilent AssayMAP Bravo Platform(利用 Agilent AssayMAP Bravo 平台,通过自动化样品前处理实现生物治疗蛋白质准确而可扩展的定量和表征分析),安捷伦科技公司, 出版号5991-4872EN ( 6. F olzer, E.; et a l . Selective Oxidation of Methionine and Tryptophan Residuesin a Therapeutic IgG1 Molecule. J.Pharm. S ci. 2015,104(9),2824-2831 ) ( 7. Robinson, N. E.; Robinson,A. B.; Merrifield, R. B. Mass spectrometricevaluation o f synthetic peptides a sprimary structure models for peptideand protein d eamidation. J. P ept.Res. 2001,57(6), 483-493 ) ( 8. Robinson, N. E . ; Robinson, A. B. Prediction of primary structuredeamidation r a tes of a sparaginyl andglutaminyl peptides t hrough s tericand catalytic effects. J. Pept. Res.2004,63(5),437-448 ) 查找当地的安捷伦客户中心: www.agilent.com/chem/contactus-cn 免费专线: 800-820-3278,400-820-3278(手机用户) 联系我们: LSCA-China_800@agilent.com 在线询价: www.agilent.com/chem/erfq-cn www.agilent.com 仅限研究使用。不可用于诊断目的。 本文中的信息、说明和指标如有变更,恕不另行通知。 ( C安捷伦科技(中国)有限公司,2018 ) ( 5994-0406ZHCN ) 天冬酰胺 (Asn) 脱酰胺化、天冬氨酸 (Asp) 异构化和甲硫氨酸 (Met) 氧化等修饰是重组抗体的典型降解产物。研究表明,单克隆抗体中 Asn、Asp 和 Met 残基的降解会影响蛋白质活性。因此,蛋白质候选药物(例如 mAb)中的上述修饰是关键质量属性 (CQA),需在储存和制剂条件下进行密切监测。它们通常是药物开发过程中进行的影响因素试验和强制降解研究的重点。要评估上述 CQA,需要同时进行鉴定和定量分析。本应用简报介绍了采用一体化工作流程(包括 Agilent AssayMAP Bravo 平台、Agilent 1290 Infinity II LC、Agilent 6545XT AdvanceBio LC/Q-TOF 和 Agilent MassHunter BioConfirm 软件),通过肽谱分析方法同时鉴定和定量分析重组 mAb的化学诱导脱酰胺化和氧化修饰。
确定





还剩8页未读,是否继续阅读?
安捷伦科技(中国)有限公司为您提供《重组 mAb中化学诱导脱酰胺化和氧化修饰检测方案(液质联用仪)》,该方案主要用于生物药品药物研发中含量测定检测,参考标准--,《重组 mAb中化学诱导脱酰胺化和氧化修饰检测方案(液质联用仪)》用到的仪器有Agilent 6545XT Q-TOF 液质联用系统、Agilent AssayMAP Bravo 蛋白质样品前处理平台、Agilent 1290 Infinity II 液相色谱系统、OpenLAB 软件
推荐专场
液体处理工作站(移液工作站)
更多
相关方案
更多
该厂商其他方案
更多

























