方案详情
文
本次实验基于优化的样品前处理、纳升液相系统与Orbitrap高分辨质谱,建立了迄今为止最高灵敏度的质谱HCPs检测方法,并利用内标蛋白进行准确的相对定量。由于我们没有查到NIS抗体标准品ELISA定量结果,所以未进行进一步对比质谱与ELISA的一致性。接下来将利用此方法对商品化的抗体药物进行HCPs的定性和相对定量,以及考察方法的重现性。
方案详情

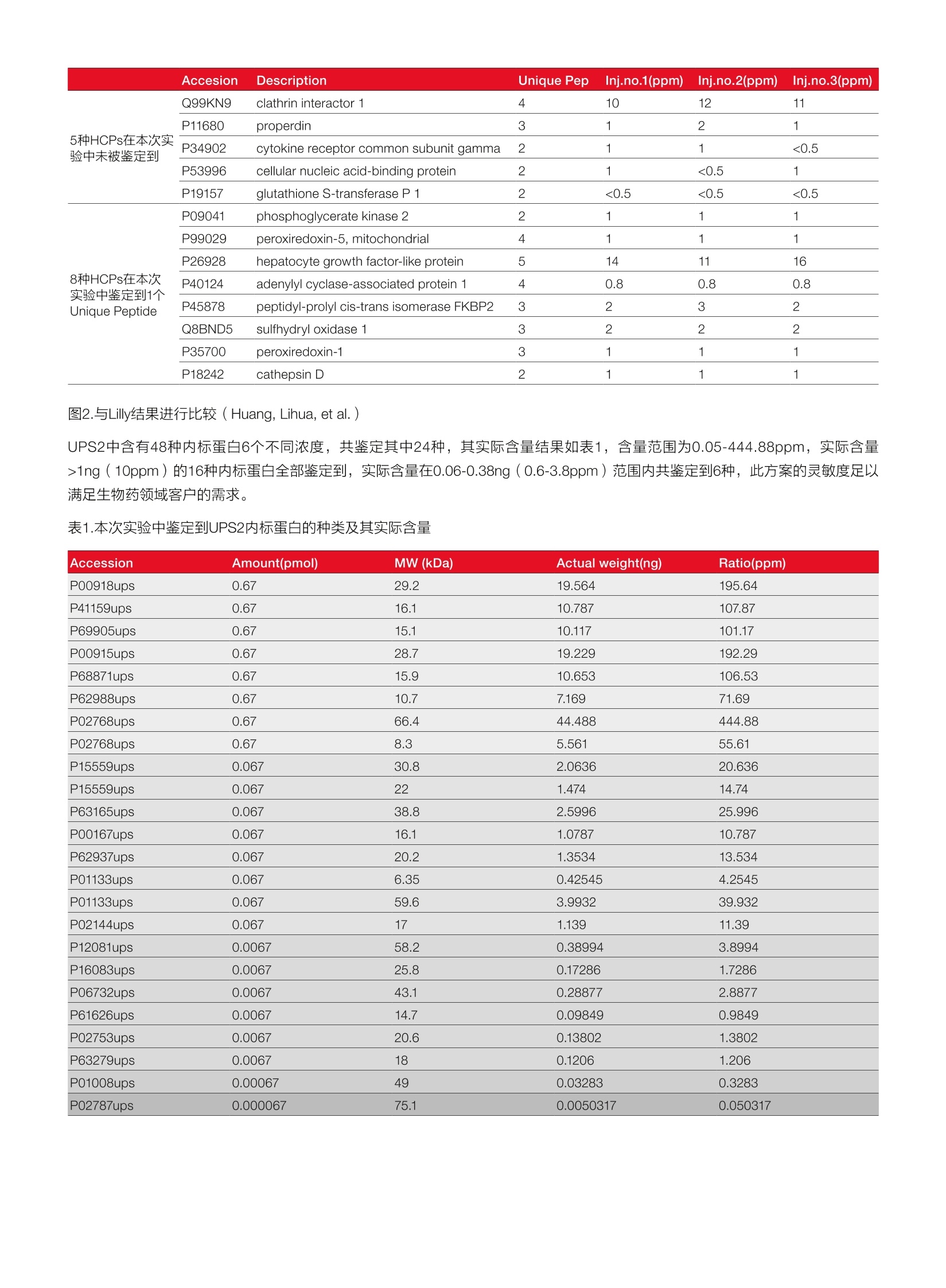
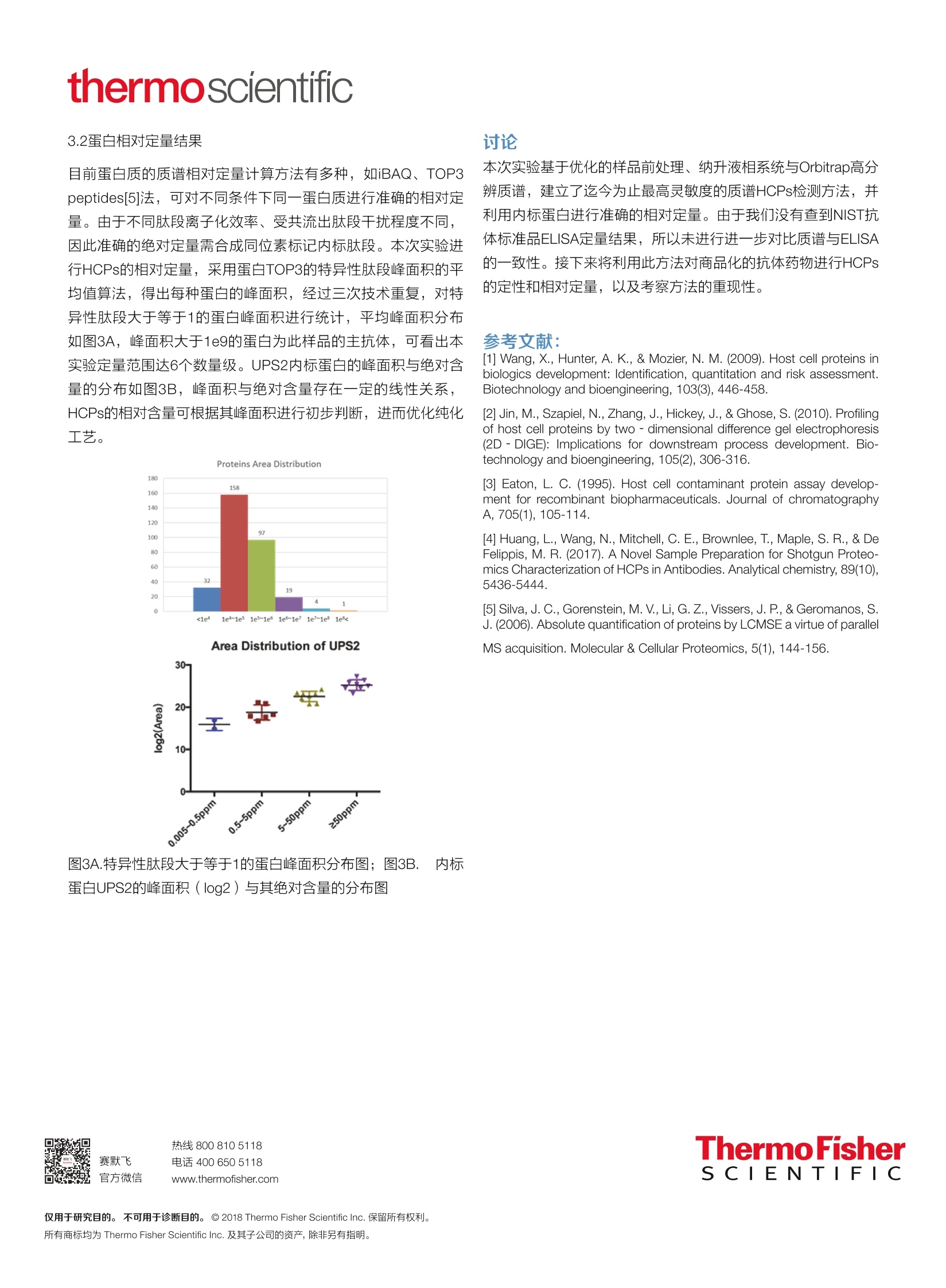
thermoscientific 梯度:见下表 热线800 8105118电话400 6505118www.thermofisher.com 基于nanoLC-MS/MS建立对重组蛋白药物中宿主细胞残留蛋白分析方法 孙佳楠1,李恺? 1赛默飞世尔科技(中国)有限公司色谱质谱部2国家蛋白质科学研究中心,北京,102206 一、前言 重组蛋白类药物是由遗传修饰的原核或真核宿主细胞培养/发酵产生,在此过程中,宿主细胞也共同产生与正常细胞功能相关的蛋白质,由于细胞凋亡/死亡/裂解,其他非必需蛋白质也可能释放到细胞培养基/发酵液中,因此残留在终产品中的其他蛋白质即为宿主细胞残留蛋白(HCPs)。HCPs的存在主要影响药物的安全性和有效性,如引起机体免疫反应,作为佐剂以增强对药物产品的免疫应答,以及具有蛋白水解活性的HCPs影响药物产品的稳定性I1][2]3],因此生物医药公司不断优化其纯化工艺,从而控制终产品中HCPs的种类和含量。ICH的Q6B指导方针指出需采用具有高灵敏度和宽动态范围的方法监测HCPs,要求其含量尽可能的低,甚至低于检测限,不同产品要求不同,一般在1-100ng/mg(1-100ppm)范围内,然而并未规定其检测的具体分析方法。目前Enzyme-Linked Immunosorbent Assay(ELISA)因其具有高灵敏度、高通量和易操作优势成为工业界的金标准,但其存在很多限制,包括不能对HCPs进行精准鉴定,低丰度HCPs的检测易受限于高丰度蛋白的干扰,定量动态范围(3个数量级)较低,抗体受限,开发周期长,无法改变已有的方法,缺少校正标准限制定量的准确性,因此需多种检测方法相结合[4]。随着高分辨质谱技术性能的不断提升,已具有高灵敏度和宽的定量动态范围,以及蛋白质组学技术的飞飞发展,可实现对未知蛋白质的高通量定性和定量。但由于HCPs含量极低,且酶切后与高含量的主成分存在共洗脱,对低含量HCPs的鉴定仍存在挑战,为进一步提升质谱检测方法的动态范围,需对样品前处理及液相方法进行优化。 本篇以NIST (National Institute of Standards and Technology)标准品Humanized IgG1 K Monoclonal Antibody ( P/N RM 8671)为例,建立基于nanoLC-MS/MS高灵敏平台的方法对HCPs进行准确定性和相对定量。 二、样品前处理、仪器、实验条件及数据分析2.1样品前处理 高通量未知蛋白质的质谱鉴定通常采用bottom-up分析流程,即蛋白质变性、还原(打开二硫键)、烷基化、酶切、LC-MS/MS分析,而对于HCPs鉴定而言,采用此流程时蛋白药物主成分同时被酶切产生高含量的肽段,降低共流出HCPs肽段的鉴定可能性,从而影响此方法的灵敏度和动态范围。2017年礼来制药公司Huang, Lihua, et al.在Analytical Chemistry杂志上发表题为“A Novel Sample Preparation for Shotgun Proteomics Cha-racterization of HCPs in Antibodies" ,以NIST抗体标准品为例,在蛋白质非变性的条件下进行酶切,抗体主成分被部分酶切,酶切后经90度高温变性,未被酶切的部分将被沉淀去除,从而提高HCPs的鉴定几率和方法的动态范围,如图1[4]。本篇应用文集在此基础上进一步优化,缩短前处理时间提高工作效率,同时为考察此套流程对1-100ppm的HCPs的鉴定和相对定量能力,加入入标蛋白UPS2(48种蛋白,6个不同浓度)进行定性和相对定量。 图1.样品前处理流程示意图(来自Huang, Lihua, et al.) 2.1.1试剂及样品信息 Trizma base (Sigma-Aldrich), 浓盐酸(Sigma-Aldrich)二硫苏糖醇(Sigma-Aldrich), SequencingGrade Modi-fied Trypsin (Promega),质谱级水(ThermoFisher), 甲酸(ThermoFisher), 乙腈 (ThermoFisher), HumanizedIgG1k Monoclonal Antibody (NIST, P/N RM 8671), UPS2内标蛋白(Sigma-Aldrich) 2.1.2前处理步骤 1.取300pg抗体标准品, 50mM Tris-HCI (pH=7.8) 将样品稀释成1pg/pL,加入2pmol内标蛋白(UPS2中浓度最高的一组蛋白质总含量为2pmol); 2. 加入1.5pg Trypsin (500ng/pL), 37℃酶切2h; 3.加入终浓度5mM DTT, 90C变性10min; 4. 14,000g 离心20min, 取上清; 5.真空浓缩仪进行样品旋干; 6.18pL 0.1%FA-H,O复溶; 7.每针进样5pL; 2.2仪器、色谱柱、数据分析软件 目前根据液相色谱的流速可分为纳升液相色谱(nanoLC, <1pL/min)、毛细管液相色谱(capillaryLC,1-10pL/min)、微流速液相色谱(microLC,10-100uL/min)、分析流速液相色谱(LC,>100pL/min),由于样品单位浓度和离子化效率依次下降,因此其灵敏度逐渐下降,本次实验采用灵敏度最高的纳升液相系统。 纳升液相色谱仪: EASY nLC 1200 高分辨质谱仪: Q Exactive Plus 色谱柱: Thermo ScientificTM AcclaimTM PepMapTM 100 C18(P/N 164941); Trap column (P/N164946),柱温45℃ 数据分析软件: Thermo Proteome Discoverer2.2 2.2.1色谱条件 流动相A:0.1%FA-H2O)流动相B:0.1%FA-80%ACN-20%H2O time A(%) B(%) 0 97 3 8 92 8 106 70 30 115 10 90 120 10 90 2.2.2质谱条件 ( 扫描方式:数据居赖型扫描方法(Data Dependent Acquisiti-on) ) ( 一级扫描参数:分辨率70K, AGC target 3e6, 扫描范围 m/z 300-1700 ) ( 二级扫描参数:分辨率35K, AGC ta r get 1e5, Top15, Fir s t Mass: 120 m/ z , 四极杆隔离窗口1.8 m/z, 碎裂能量NCE 28 ) 2.2.3软件参数设置Mus musculus,UPS2理论序 蛋白质数据库: Swiss-Prot列,NIST抗体标准品序列,污染蛋白库酶切方式: Trypsin全酶切;;最大漏切个数:2个一级质量偏差:10ppm 二级质量偏差:0.02Da可变修饰:氧化(M),蛋白N端乙酰化FDR控制: PSMFDR<1%, Peptide FDR<1%, Protein FDR<1% 三、实验结果与讨论 3.1定性结果 连续进样3针,排除污染蛋白和空白对照中存在的蛋白质,且筛选特异性肽段大于等于2的蛋白质,共鉴定HCPs有158种,具体蛋白列表见链接。Huang, Lihua,et al.文章鉴定到60种HCPs,我们的数据覆盖其中47种,其余13种鉴定到8种(特异性肽段等于1),5种未鉴定,如图2。这5种的相对含量除了一种近10ppm, 其余均近1ppm, 表明LC-MS/MS方法在不同平台之间的高度重现性和可靠性。 · 8 HCPs were found in our resultswith 1 unique peptide. ·5 HCPs weren't found in our results. Accesion Description Unique Pep Inj.no.1(ppm) Inj.no.2(ppm) Inj.no.3(ppm) Q99KN9 clathrin interactor 1 4 10 12 11 P11680 properdin 3 1 2 1 5种HCPs在本次实 验中未被鉴定到 P34902 cytokine receptor common subunit gamma 2 1 1 <0.5 P53996 cellular nucleic acid-binding protein 2 1 <0.5 1 P19157 glutathione S-transferase P 1 2 <0.5 <0.5 <0.5 P09041 phosphoglycerate kinase 2 2 1 1 1 P99029 peroxiredoxin-5, mitochondrial 4 1 1 1 P26928 hepatocyte growth factor-like protein 5 14 11 16 8种HCPs在本次 P40124 adenylyl cyclase-associated protein 1 4 0.8 0.8 0.8 实验中鉴定到1个 Unique Peptide P45878 peptidyl-prolyl cis-trans isomerase FKBP2 3 2 3 2 Q8BND5 sulfhydryl oxidase 1 3 2 2 2 P35700 peroxiredoxin-1 3 1 1 1 P18242 cathepsin D 2 1 1 1 图2.与Lilly结果进行比较(Huang, Lihua, et al.) UPS2中含有48种内标蛋白6个不同浓度,共鉴定其中24种,其实际含量结果如表1,含量范围为0.05-444.88ppm,实际含量>1ng(10ppm)的16种内标蛋白全部鉴定到,实际含量在0.06-0.38ng(0.6-3.8ppm)范围内共鉴定到6种,此方案的灵敏度足以满足生物药领域客户的需求。 表1.本次实验中鉴定到UPS2内标蛋白的种类及其实际含量 Accession Amount(pmol) MW(kDa) Actual weight(ng) Ratio(ppm) P00918ups 0.67 29.2 19.564 195.64 P41159ups 0.67 16.1 10.787 107.87 P69905ups 0.67 15.1 10.117 101.17 P00915ups 0.67 28.7 19.229 192.29 P68871ups 0.67 15.9 10.653 106.53 P62988ups 0.67 10.7 7.169 71.69 P02768ups 0.67 66.4 44.488 444.88 P02768ups 0.67 8.3 5.561 55.61 P15559ups 0.067 30.8 2.0636 20.636 P15559ups 0.067 22 1.474 14.74 P63165ups 0.067 38.8 2.5996 25.996 P00167ups 0.067 16.1 1.0787 10.787 P62937ups 0.067 20.2 1.3534 13.534 P01133ups 0.067 6.35 0.42545 4.2545 P01133ups 0.067 59.6 3.9932 39.932 P02144ups 0.067 17 1.139 11.39 P12081ups 0.0067 58.2 0.38994 3.8994 P16083ups 0.0067 25.8 0.17286 1.7286 P06732ups 0.0067 43.1 0.28877 2.8877 P61626ups 0.0067 14.7 0.09849 0.9849 P02753ups 0.0067 20.6 0.13802 1.3802 P63279ups 0.0067 18 0.1206 1.206 P01008ups 0.00067 49 0.03283 0.3283 P02787ups 0.000067 75.1 0.0050317 0.050317 3.2蛋白相对定量结果 目前蛋白质的质谱谱对定量计算方法有多种,如iBAQ、TOP3peptides[5]法,可对不同条件下同一蛋白质进行准确的相对定量。由于不同肽段离子化效率、受共流出肽段干扰程度不同,因此准确的绝对定量需合成同位素标记内标肽段。本次实验进行HCPs的相对定量,采用蛋白TOP3的特异性肽段峰面积的平均值算法,得出每种蛋白的峰面积,经过三次技术重复,对特异性肽段大于等于1的蛋白峰面积进行统计,平均峰面积分布如图3A,峰面积大于1e9的蛋白为此样品的主抗体,可看出本实验定量范围达6个数量级。UPS2内标蛋白的峰面积与绝对含量的分布如图3B,峰面积与绝对含量存在一定的线性关系,HCPs的相对含量可根据其峰面积进行初步判断,进而优化纯化工艺。 图3A.特异性肽段大于等于1的蛋白峰面积分布图;图3B.内标蛋白UPS2的峰面积(log2)与其绝对含量的分布图 讨论 本次实验基于优化的样品前处理、纳升液相系统与Orbitrap高分辨质谱,建立了迄今为止最高灵敏度的质谱HCPs检测方法,并利用内标蛋白进行准确的相对定量。由于我们没有查到NIST抗体标准品ELISA定量结果,所以未进行进一步对比质谱与ELISA的一致性。接下来将利用此方法对商品化的抗体药物进行HCPs的定性和相对定量,以及考察方法的重现性。 ( [1] Wang, X . , Hunter, A. K., & Mozier, N . M. (2 0 09). Ho s t cell pr o teins inbiologics development: Identification, quantitation and r isk assessment. B iotechnology and bioengineering,103(3),446-458. ) ( [ 2] Jin, M., Szapiel, N ., Z hang, J., H i ckey, J. , & Ghose, S. (2010). Profilingof h ost c ell proteins b y two - dimensional di f ference ge l el e ctrophoresis(2D-DIGE): I m plications f or downstream p r ocess development. Bio-technology and bioengineering, 105(2), 3 0 6-316. ) ( [ 3] Eaton, L . C . ( 1995). H ost cell c ontaminant p r otein a s say develop- m ent f o r recombinant b i opharmaceuticals. J o urnal o f c h romatographyA, 705(1), 105-114. ) ( [4] Huang, L., Wang, N., M itchell,C. E ., Brownlee, T., Maple, S. R., & De F elippis, M. R. (2017). A Novel Sample P reparation for Shotgun Proteo-mics Characterization of HCPs in A ntibodies. Analytical ch e mistry, 89(10),5436-5444. ) ( [5]Silva, J . C., Gorenstein, M. V., L i , G. Z., Vissers, J.P., & Geromanos, S.J. (2006). Absolute quantification of proteins by LCMSE a virtue of parallel ) ( MS acquisition. M o lecular & Cellular Proteomics, 5(1), 14 4 -156. ) 重组蛋白类药物是由遗传修饰的原核或真核宿主细胞培养/发酵产生,在此过程中,宿主细胞也共同产生与正常细胞功能相关的蛋白质,由于细胞凋亡/死亡/裂解,其他非必需蛋白质也可能释放到细胞培养基/发酵液中,因此残留在终产品中的其他蛋白质即为宿主细胞残留蛋(HCPs)。HCPs的存在主要影响药物的安全性和有效性,如引起机体免疫反应,作为佐剂以增强对药物产品的免疫应答,以及具有蛋白水解活性的HCPs影响药物产品的稳定性[1][2][3],因此生物医药公司不断优化其纯化工艺,从而控制终产品中HCPs的种类和含量。ICH 的Q6指导方针指出需采用具有高灵敏度和宽动态范围的方法监测HCPs,要求其含量尽可能的低,甚至低于检测限,不同产品要求不同,一般在1-100ng/mg(1-100ppm)范围内,然而并未规定其检测的具体分析方法。目前Enzyme-Linked Immunosorbent Assay (ELISA)因其具有高灵敏度、高通量和易操作优势成为工业界的金标准,但其存在很多限制,包括不能对HCPs进行精准鉴定,低丰度HCPs的检测易受限于高丰度蛋白的干扰,定量动态范围(3个数量级)较低,抗体受限,开发周期长,无法改变已有的方法,缺少校正标准限制定量的准确性,因此需多种检测方法相结合[4]。随着高分辨质谱技术性能的不断提升,已具有高灵敏度和宽的定量动态范围,以及蛋白质组学技术的飞速发展,可实现对未知蛋白质的高通量定性和定量。但由于HCPs含量极低,且酶切后与高含量的主成分存在共洗脱,对低含量HCPs的鉴定仍存在挑战,为进一步提升质谱检测方法的动态范围,需对样品前处理及液相方法进行优化。本次实验基于优化的样品前处理、纳升液相系统与Orbitrap高分辨质谱,建立了迄今为止最高灵敏度的质谱HCPs检测方法,并利用内标蛋白进行准确的相对定量。由于我们没有查到NIS抗体标准品ELISA定量结果,所以未进行进一步对比质谱与ELISA的一致性。接下来将利用此方法对商品化的抗体药物进行HCPs的定性和相对定量,以及考察方法的重现性。
确定


还剩2页未读,是否继续阅读?
赛默飞色谱与质谱为您提供《重组蛋白药物中宿主细胞残留蛋白分析检测方案(液相色谱仪)》,该方案主要用于生物药品药物研发中含量测定检测,参考标准--,《重组蛋白药物中宿主细胞残留蛋白分析检测方案(液相色谱仪)》用到的仪器有赛默飞UltiMate 3000 纳升级液相色谱、赛默飞Q Exactive Plus LCMS 系统
推荐专场
相关方案
更多
该厂商其他方案
更多

















