Agilent Captiva 增强型脂质去除产品 (EMR-Lipid) 是第二代 EMR 产品,采用便捷的 SPE 过滤柱或 96 孔板。本研究采用 96 孔板形式对人血浆和血清中的 24 种代表性滥用药进行 LC/MS/MS 定量测定。样品的前处理方法为:采用孔内蛋白质沉淀法 (PPT) 去除蛋白质,接着采用 Captiva EMR-Lipid 净化产品去除脂类。整个样品处理在 96 孔板中作为一个批处理执行,并通过离心和正压歧管验证样品的洗脱。整个批次流程简单易用,能够在两小时内完成样品板中 96 个样品的前处理。高效基质净化产品使磷脂去除率高于 99%,从而减小了基质离子抑制效应和系统污染。通过准确度和精密度的运行实现定量方法的验证,在三个 QC 浓度下均获得了优异的准确度 (100% ± 20%) 和精密度 (RSD < 20%)。血浆和血清中的定量限 (LOQ) 为0.1–0.5 ng/mL,且线性校准曲线的 R2 > 0.99。用通常的人血基质(包括含各种抗凝血剂的血清和血浆)对该方法进行了交叉验证。
方案详情

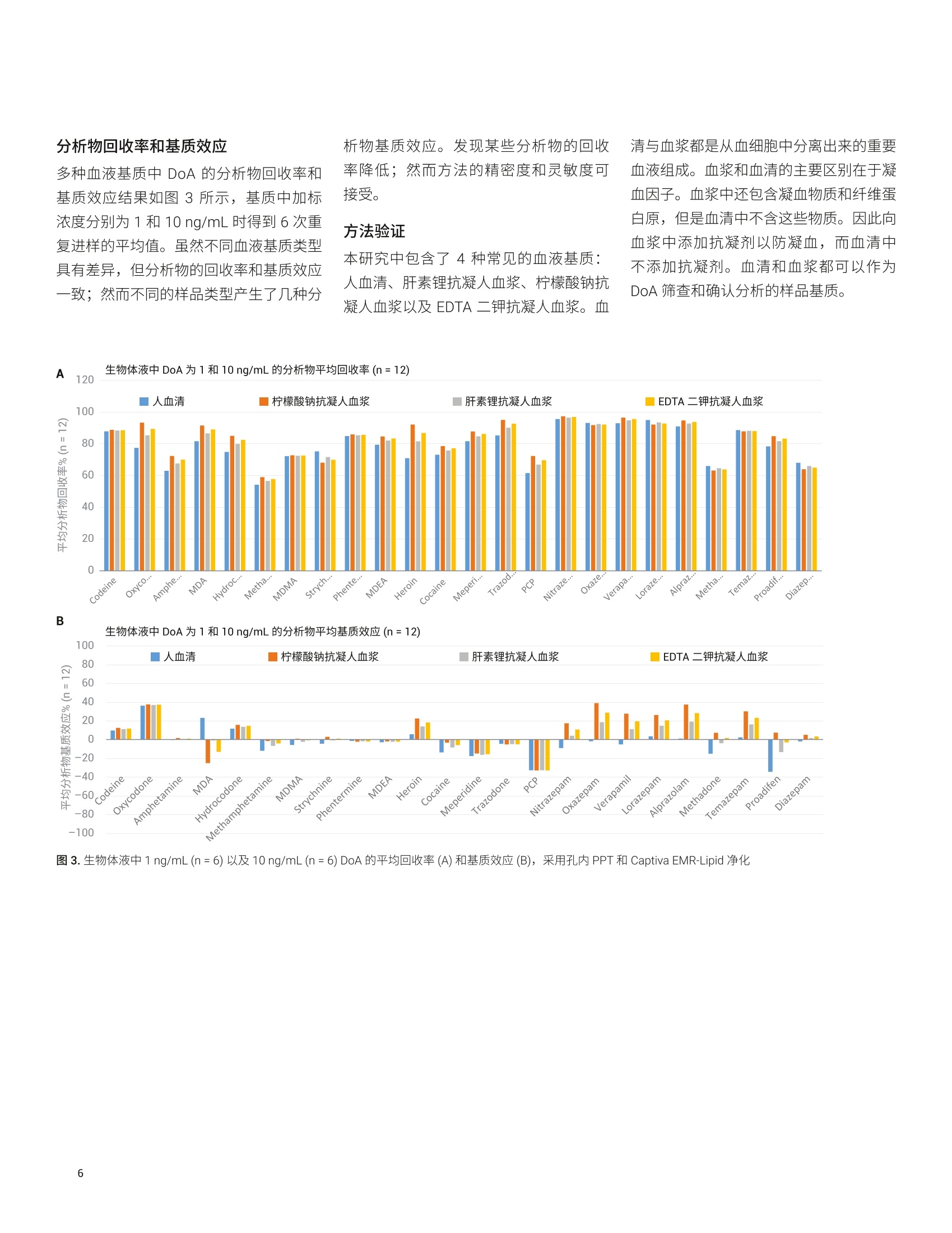
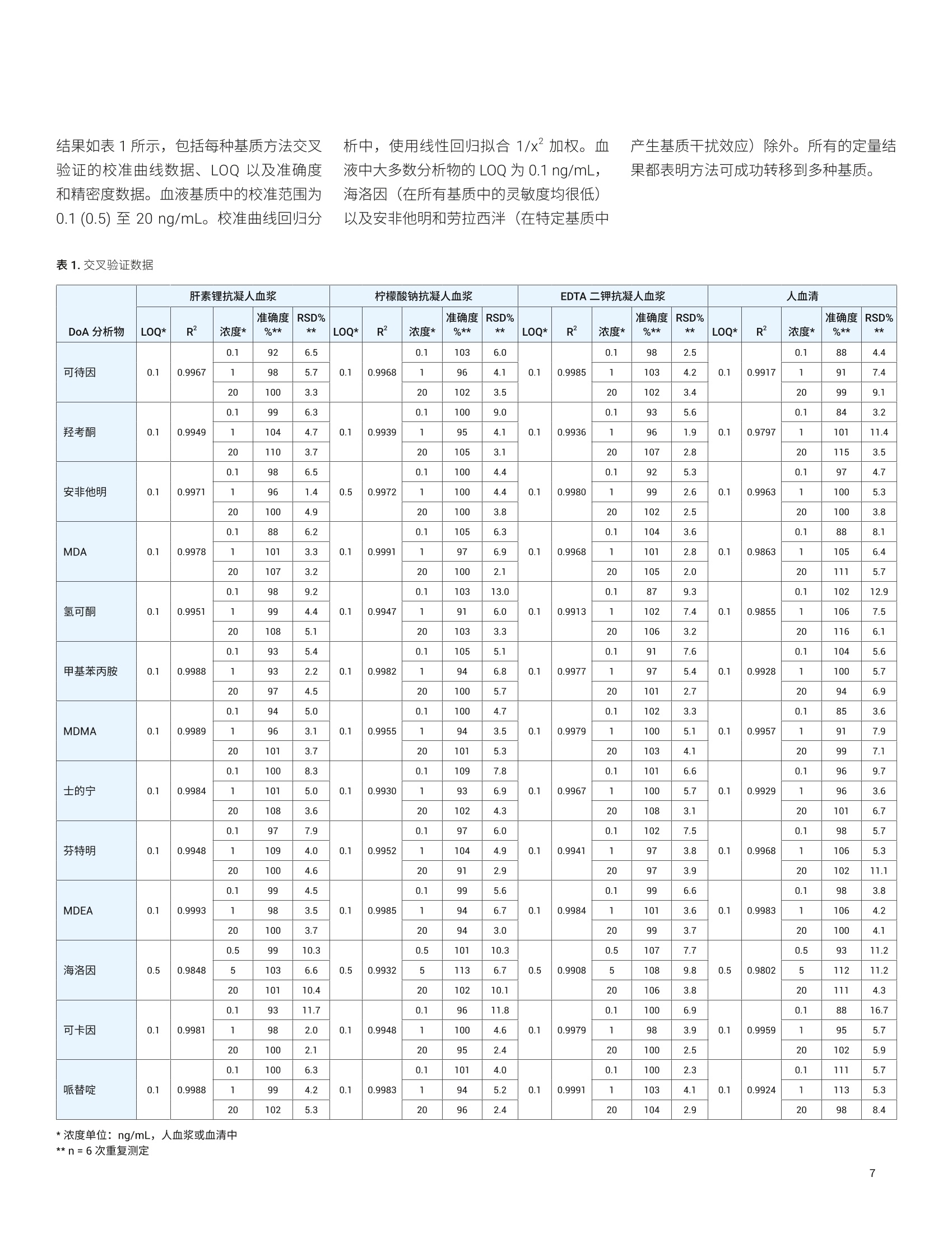
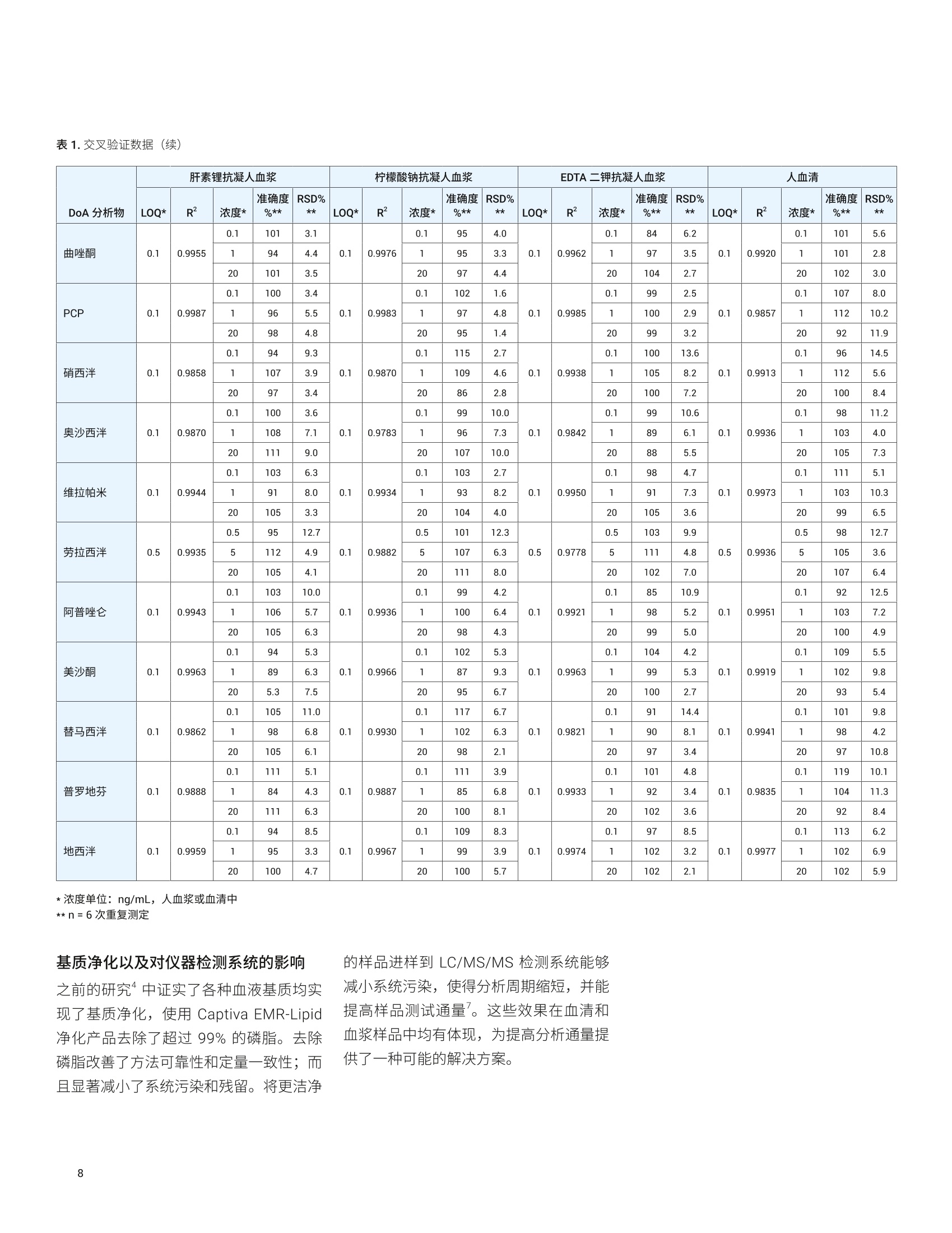
应用简报 Agilent法医学检测Trusted Answers 使用 Agilent Captiva EMR-Lipid 净化产品对人血浆和血清中的滥用药进行LC/MS/MS 定量测定 Limian Zhao 安捷伦科技公司 Agilent Captiva 增强型脂质去除产品 (EMR-Lipid) 是第二代EMR 产品,采用便捷的 SPE 过滤柱或 96 孔板。本研究采用96孔形形式对人血浆和血清中的24种代表性滥用药进行 LC/MS/MS 定量测定。样品的前处理方法为:采用孔内蛋白质沉淀法(PPT)去除蛋白质,接着接用Captiva EMR-Lipid 净化产品去除脂类。整个样品处理在96孔板中作为一个批处理执行,并通过离心和正压歧管验证样品的洗脱。整个批次流程简单易用,能够在两小时内完成样品板中96个样品的前处理。高效基质净化产品使磷脂去除率高于99%,从而减小了基质离子抑制效应和系统污染。通过准确度和精密度的运行实现定量方法的验证,在三个QC 浓度下均获得了优异的准确度(100%±20%)和精密度 (RSD<20%)。血浆和血清中的定量限(LOQ)为0.1-0.5 ng/mL,且线性校准曲线的R²>0.99。用通常的人血基质(包括含各种抗凝血剂的血清和血浆)对该方法进行了交叉验证。 前言 在法医毒理学中,对快速可靠地筛查和定量测定生物样本中的滥用药(DoA)的需求正在不断增加。主要原因是滥用药以及提交分析的样品数量日益增多。使用血液基质有以下几个优势:首先,药物一经摄入,能够在体内代谢或过滤之前立即进行检测。其次,由于生理参数的变化范围非常窄,血液相对均匀。再次,许多欧洲国家和美国一些州,在要求药驾 (DUID) 测试时指定用血液样品。因此,可靠地定量测定血液基质中的 DoA 对于常规毒理学分析非常重要。 用于系统毒理学分析的样品前处理方法包括液液萃取(LLE)、固相萃取(SPE)和固相支持液液萃取 (SLE)。然而,这些方法费力费时,并需要使用大量有毒溶剂。安捷伦增强型脂质去除产品(EMR-Lipid) 所用的吸附剂是一种新型材料,能够选择性去除样品基质中的主要脂类且不会造成分析物损失。其脂质去除机制是基于脂质与 EMR 吸附剂之间的体积排阻和疏水相互作用。第二代 Captiva EMR-Lipid 吸附剂以 SPE 过柱柱/板形式包装,只需对样品进行直通式洗脱即完成净化,留在溶液中的溶质可供分析。研究表明,使用Captiva EMR-Lipid 96 孔板进行孔内蛋白质沉淀 (PPT), 随后进行直通式净化,能够有效去除生物体液中的磷脂,并实现人血清中代表性药物的定量测定。 在之前的研究中,建立了孔内 PPT 和Captiva EMR-Lipid 板净化的方法,并针对人全血中流行的 DoA 分析进行方法验证。本研究中,将一种类似的方法应用到不同的血液基质(包括血清和血浆)中。目标分析物的化学特性和结构列于之前的应用简报中。该方法采用了一天的准确度和精密度测试以及分析物回收率和基质效应评估,就每种血液基质进行了交叉验证。 试剂与化学品 ( 所有试剂和溶剂均为 HPLC 或分析纯级。 乙腈 (ACN) 购自 Honeywell (Muskegon,MI, USA)。试剂级甲酸 (FA) 来自安捷伦(部件号 G2453-85060)。乙酸铵和氢氧化铵购自 Sig m a-Aldrich (S t . L o uis, MO,USA)。混合DoA标准储备液(1 pg/mL, 溶于甲醇(MeOH)中)来自安捷伦(部件 号5190-0470-1)。人血清、肝素锂抗凝 人血浆、柠檬酸钠抗凝人血浆以及 EDTA 二钾抗凝人血浆来自 Biolo g ical SpecialtyCorp. (Colmar, PA, USA)。 内标 (IS) 储备液(1 mg/mL, 溶于 MeOH 或 ACN中)来自 Cerilliant ( Round Rock, TX, USA)。 ) 标样和溶液 利用混合DoA 标准储备液和单独的 IS 储备液配制标样和 IS 加标溶液。在 20:80甲醇/水中配制浓度为 200 ng/mL的标样加标溶液,用于对校准标样和质量控制(QC)样品加标。用 20:80甲醇/水将单独的IS储备液稀稀至2 pg/mL,制得 IS加标溶液,并将该 IS 加标溶液直接加入样品中。 将 385.3 mg 乙酸铵溶于 1 L Milli-Q 水中,然后加入1mLFA,制得含0.1%FA的5 mmol/L乙酸铵缓冲液,作为流动相A。将1mL FA 加入1L乙腈中,制得含0.1% FA 的乙腈溶液,作为流动相B。 ( 将 400 L NHOH加入 40 mL 预混合的95:5 ACN/MeOH中,新鲜配制的 95:5 ACN/MeOH 溶哈中含1%氢氧化铵。溶剂在使用前保存于-20℃下。混合80mL乙腈和20mL水,制成80:20 乙腈/水溶液。 将7 7 .06 mg 乙酸铵溶于 200 mL M i lli-Q水 中, 制 得 5 mmol/L 乙酸铵溶液。 。以8:2 的比例混合上述缓冲液和乙腈,制成复溶溶液。 ) 仪器与材料 用于样品前处理的仪器包括: Centra CL3R离心机 (Thermo IEC,MA, USA) 多管涡旋仪 (VWR, PA, USA) Eppendorf 移液器和连续分液器SPE 干式 96 蒸发器 安捷伦PPM-96(部件号5191-4116) Agilent Captiva EMR 96孔板(部件号5190-1001) Agilent Captiva 96 孔1 mL收集板(部件号A696001000) Agilent Captiva 96 孔板盖,10/包(部件号A8961007) 仪器条件 样品在 Agilent 1290 Infinity 液相色谱系统上运行,该液相色谱系统包括Agilent 1290 Infinity 二元泵 (G4220A)、Agilent 1290 Infinity 高性能自动进样器(G4226A) 和 Agilent 1290 Infinity 柱温箱(G1316C)。该液相色谱系统与配备安捷伦喷射流 iFunnel 电喷雾离子源的 Agilent6490三重四极杆液质联用 (G6490A) 系统联用。采用 Agilent MassHunter 工作站软件进行数据采集和分析。 校准标样和QC样品前处理 使用 200 ng/mL 溶于 20:80 甲醇/水中的标样加标溶液,在相应血液基质中制得校准曲线标样。全血校准曲线的动态范围为 0.1-20 ng/mL, 包括0.1、0.5、1、5、10、15和20 ng/mL。将合适体积的标样加标溶液加入基质空白中,然后充分涡旋混合,制得这些标样。在准确度和精密度方法验证测试中,运行三个浓度的质量控制 (QC)样品,包括浓度为0.1或 液相色谱条件 色谱柱 InfinityLab Poroshell 120, EC-C8,100×2.1 mm, 2.7 pm (部件号695775-906(T))InfinityLab Poroshell 120 保护柱, EC-C18,2.1×5mm, 2.7 pm (部件号821725-911) 流速 0.5 mL/min 柱温 60°℃ 进样量 5pL 流动相 A) 5 mmol/L 醋酸铵缓冲液,含0.1%甲酸的水溶液 B)0.1%甲酸的乙腈溶液 进样针清洗 1:1:1:1 ACN/MeOH/IPA/H,0(含0.2%FA) 梯度 时间(min) %B 流速(mL/min) 0 10 0.5 0.5 10 0.53.0 50 0.5 4.0 95 0.5 6.0 100 0.5 停止时间 6 min 后运行时间 2 min 质谱条件 干燥气温度 120°C 气体流速 14L/min 雾化器 40psi 鞘气温度 400C 鞘气流速 12 L/min 毛细管电压 3000 V iFunnel 参数 高压RF: 90V(正离子),90V(负离子)低压RF: 70V(正离子),60V(负离子) 数据采集 dMRM,正离子化模式有关分析物MRM 参数请见参考文献,有关柠檬酸钠抗凝人血浆中浓度为 LOQ 的 DoA 的LC/MS/MS 色谱图,请见图1。 善混合均匀性,并确保蛋白质沉淀完全。 Captiva EMR-Lipid 板的深度过滤设计有助于样品洗脱过程,且不会堵塞。早期全血研究中的测试和验证中采用了两种样品洗脱方法,正压多孔处理装置 (PPM)和离心。本研究中仅采用 PPM 洗脱。 方法验证 通常需要在一种基质中通过为期三天的准确度和精密度运行,对方法进行完全验证,而将方法应用到不同基质时仅需要交叉验证。因此,本研究中给出全血的完全验证结果,,1可对每种额外的血液基质通过一天的准确度和精密度(A&P)运行,实施方法的交叉验证。 对校准标样和QC 样品进行合适的预加标。按照以下顺序将样品等量加入Captiva EMR-Lipid 板中:双基质空白,基质空白((加标 IS),第一组校准标样,2至3个基质空白, LLOQ(n =6),中等浓度 QC(n=6), HLOQ(n=6), 2至3个残留基质空白,双基质空白,基质空白,第二组校准标样,2至3个基质空白。 分析物回收率和基质效应 比较低浓度(血清和血浆中浓度为 1ng/mL)和高浓度(血清和血浆中浓度为10ng/mL)的预加标和后加标QC 样品之间的分析物响应(峰面积),对分析物绝对回收率进行研究。直接将预加标的QC 样品适当地加标至基质空白中,并利用开发的方法对样品进行前处理。萃取后,将后加标的 QC样品加标至基质空白 中。具体来说,后加标发生在样品的复溶阶段,是使用适当的纯标准溶液复溶干燥基质空白。比较后加标 QC样品与试剂空白制得的相应纯标样之间的分析物响应(峰面积),对基质效应进行研究。 本研究重点展示了在毒理学应用中使用Captiva EMR-Lipid 净化产品对生物基质中的滥用药进行定量测定。 方法方案一样品优先蛋白质沉淀 它表明了向粘稠全血样品中加入沉淀溶剂的加入顺序,,可获得更高的混合均匀性,从而实现了更有效的蛋白质沉淀。对于血清和某些血浆等粘度较低的生物体液来说,其生物体液混合阻力并未像全血等粘稠基质那样显著。然而,与溶剂优先PPT 相比,对生物体液进行样品优先 PPT 能够改善混合均匀性。首先添加样品还可通过使用 Captiva EMR-Lipid 板直接实现 IS原位加标,然后再添加沉淀溶剂。样品优先的添加顺序无需进行额外的样品转移,因此简化了工作流程。出色的混合均匀性无需额外的抽吸混合(之前的方法中推荐使用)即可实现完全的蛋白质沉淀4。另外,上述修改降低了样品在96孔板上的交叉污染风险,这一点对高通量测试非常重要,特别是自动化的样品前处理操作。在省略转移步骤的同时,减少了消耗品(例如收集板和移液枪头)的使用数量。根据以上几点考虑,新的样品优先 PPT可用于血清和血浆样品分析。 离心洗脱和正压洗脱均在全血的 DoA 分析中进行了测试和验证。结果显示两种洗脱技术能够获得同等的洗脱效果。本研究中,仅将正压洗脱技术用于方法的交叉验证。图2 为 Captiva EMR-Lipid 96孔板上进行样品批处理的图片。图2A和 图2B 为 Captiva EMR-Lipid 板上进行孔内 PPT 的样品均匀性和一致性。图2C和图2D 为洗脱后 Captiva EMR-Lipid 板上的干燥沉淀残留物,以及收集板上收集的一致样品洗脱液。 A 一致的孔内 PPT 高效的沉淀过滤和一致的洗脱 图2.在96孔 Captiva EMR-Lipid 板上对人血浆样品进行批处理,然后进行EMR-Lipid 直通式净化。A) 从 Captiva EMR-Lipid 板顶部看到的孔内 PPT 视图;B)从 Captiva EMR-Lipid 板侧面看到的孔内PPT视图; C) 从 EMR-Lipid 板顶部看到的孔内干燥沉淀物(洗脱后)视图;D)收集板中收集的一致样品洗脱 分析物回收率和基质效应多种血液基质中 DoA 的分析物回收率和基质效应结果如图3所示,基质中加标浓度分别为1和10 ng/mL时得到6次重复进样的平均值。虽然不同血液基质类型具有差异,但分析物的回收率和基质效应一致;然而不同的样品类型产生了几种分 A 清与血浆都是从血细胞中分离出来的重要血液组成。血浆和血清的主要区别在于凝血因子。血浆中还包含凝血物质和纤维蛋白原,但是血清中不含这些物质。因此向血浆中添加抗凝剂以防凝血,而血清中不添加抗凝剂。血清和血浆都可以作为DoA筛查和确认分析的样品基质。 结果如表1所示,包括每种基质方法交叉验证的校准曲线数据、LOQ以及准确度和精密度数据。血液基质中的校准范围为0.1(0.5)至20 ng/mL。校准曲线回归分 析中,使用线性回归拟合1/x²加权。血液中大多数分析物的LOQ 为 0.1 ng/mL,海洛因(在所有基质中的灵敏度均很低)以及安非他明和劳拉西泮(在特定基质中 产生基质干扰效应)除外。所有的定量结果都表明方法可成功转移到多种基质。 表1.交叉验证数据 基质净化以及对仪器检测系统的影响 之前的研究4中证实了各种血液基质均实现了基质净化,使用 Captiva EMR-Lipid净化产品去除了超过99%的磷脂。去除磷脂改善了方法可靠性和定量一致性;而且显著减小了系统污染和残留。将更洁净 的样品进样到 LC/MS/MS 检测系统能够减小系统污染,使得分析周期缩短,并能提高样品测试通量。这些效果在血清和血浆样品中均有体现,为提高分析通量提供了一种可能的解决方案。 在人血液基质中24种代表性 DoA 化合物的定量测定中,对一种使用孔内蛋白质沉淀和 Captiva EMR-Lipid 净化产品的羊品前处理方法进行了交叉验证。对每种血液基质进行一天的准确度和精密度评估,证实该方法能够成功转移到其他基质。采用96孔板形式开发的方案适用于高通量实验室对快速、可自动化的样品前处理方法的需求,便捷的孔内 PPT 和 CaptivaEMR-Lipid 净化产品简化了工作流程,同时仍可提供高效的样品提取和脂质净化。更干净的分析样品还可缩短清洗检测系统所耗的时间,提高样品检测通量。首先添加血浆或血清样品再添加沉淀溶剂的蛋白质沉淀方法,,可改善样品混合的均匀性,这样,易去除蛋白质并减少转移步骤。 ( 参考文献 ) ( 1. S aito, K.; et al. Analysis of D r ugsof Abuse i n Biological Specimens,J. Health Science, 2011, 5 7 (6), 472-487 ) ( 2. Moeller, M. R.; Steinmeyer, S.; K raemer, T. Determination of drugsof abuse in blood, J. Chromatog.B 1998,713,91-109 ) ( Moeller, M. R.; Kraemer, T . Drugsof Abuse M onitoring in Bloodfor Control of Driving Under theInfluence of Drugs, Therapeutic DrugMonitoring 2002, 24,210-221 ) ( 4. Zhao, L.;Lucas, D. Efficiency ofBiological Fluid Matrix RemovalUsing Agilent Captiva EMR-LipidCleanup (Agilent C aptiva EMR-Lipid 净化产品的生物体液基质去除效率),安捷伦科技公司应用简报,出版号5991-8006EN, 2017 ) ( 5. Zhao, L.; Lucas, D. 使用 Agilent EMR-Lipid 净化产品对人血清中的 药物进行LC/MS/MS定量分析,安捷伦科技公司应用简报,出版号5991-8007CHCN,2017 ) ( 6. Zhao,L.; Juck, M. QuantitativeDetermination of D rugs of Abuse inHuman Whole Blood by LC/MS/MSUsing Agilent Captiva EMR-LipidCleanup (使用 Agilent Captiva EMR-Lipid 净化产品对人全血中的滥用药进行 LC/MS/MS 定量测定), 安捷伦科技公司应用简报,出版号 5991-9251EN,2018 ) ( Zhao,L.; Juck, M. Protein Precipitation for Biological FluidSamples U s ing Agilent C aptiva EMR-Lipid 96-well Plates (使用Agilent Captiva EMR-L i pid 96 孔板对生物体液样品进行蛋白质沉淀), 安捷伦科技公司应用简报,出版号 5991-9222EN, 2018 ) 查找当地的安捷伦客户中心: www.agilent.com/chem/contactus-cn 免费专线: 800-820-3278,400-820-3278(手机用户) 联系我们: LSCA-China_800@agilent.com 在线询价: www.agilent.com/chem/erfq-cn www.agilent.com ( 本文中的信息、说明和指标如有变更,恕不另行通知。 ) ( 2018年5月8日,中国出版 ) 摘要Agilent Captiva 增强型脂质去除产品 (EMR-Lipid) 是第二代 EMR 产品,采用便捷的 SPE 过滤柱或 96 孔板。本研究采用 96 孔板形式对人血浆和血清中的 24 种代表性滥用药进行 LC/MS/MS 定量测定。样品的前处理方法为:采用孔内蛋白质沉淀法 (PPT) 去除蛋白质,接着采用 Captiva EMR-Lipid 净化产品去除脂类。整个样品处理在 96 孔板中作为一个批处理执行,并通过离心和正压歧管验证样品的洗脱。整个批次流程简单易用,能够在两小时内完成样品板中 96 个样品的前处理。高效基质净化产品使磷脂去除率高于 99%,从而减小了基质离子抑制效应和系统污染。通过准确度和精密度的运行实现定量方法的验证,在三个 QC 浓度下均获得了优异的准确度 (100% ± 20%) 和精密度 (RSD < 20%)。血浆和血清中的定量限 (LOQ) 为0.1–0.5 ng/mL,且线性校准曲线的 R2 > 0.99。用通常的人血基质(包括含各种抗凝血剂的血清和血浆)对该方法进行了交叉验证。前言在法医毒理学中,对快速可靠地筛查和定量测定生物样本中的滥用药 (DoA) 的需求正在不断增加。主要原因是滥用药以及提交分析的样品数量日益增多。使用血液基质有以下几个优势:首先,药物一经摄入,能够在体内代谢或过滤之前立即进行检测。其次,由于生理参数的变化范围非常窄,血液相对均匀。再次,许多欧洲国家和美国一些州,在要求药驾 (DUID) 测试时指定用血液样品。因此,可靠地定量测定血液基质中的 DoA 对于常规毒理学分析非常重要。用于系统毒理学分析的样品前处理方法包括液液萃取 (LLE)、固相萃取 (SPE) 和固相支持液液萃取 (SLE)。然而,这些方法费力费时,并需要使用大量有毒溶剂。安捷伦增强型脂质去除产品 (EMR-Lipid) 所用的吸附剂是一种新型材料,能够选择性去除样品基质中的主要脂类且不会造成分析物损失。其脂质去除机制是基于脂质与 EMR 吸附剂之间的体积排阻和疏水相互作用。第二代 Captiva EMR-Lipid 吸附剂以 SPE 过滤柱/板形式包装,只需对样品进行直通式洗脱即完成净化,留在溶液中的溶质可供分析。研究表明,使用 Captiva EMR-Lipid 96 孔板进行孔内蛋白质沉淀 (PPT),随后进行直通式净化,能够有效去除生物体液中的磷脂,并实现人血清中代表性药物的定量测定。在之前的研究中,建立了孔内 PPT 和 Captiva EMR-Lipid 板净化的方法,并针对人全血中流行的 DoA 分析进行方法验证。本研究中,将一种类似的方法应用到不同的血液基质(包括血清和血浆)中。目标分析物的化学特性和结构列于之前的应用简报中。该方法采用了一天的准确度和精密度测试以及分析物回收率和基质效应评估,就每种血液基质进行了交叉验证。结论在人血液基质中 24 种代表性 DoA 化合物的定量测定中,对一种使用孔内蛋白质沉淀和 Captiva EMR-Lipid 净化产品的样品前处理方法进行了交叉验证。对每种血液基质进行一天的准确度和精密度评估,证实该方法能够成功转移到其他基质。采用 96 孔板形式开发的方案适用于高通量实验室对快速、可自动化的样品前处理方法的需求,便捷的孔内 PPT 和 Captiva EMR-Lipid 净化产品简化了工作流程,同时仍可提供高效的样品提取和脂质净化。更干净的分析样品还可缩短清洗检测系统所耗的时间,提高样品检测通量。首先添加血浆或血清样品再添加沉淀溶剂的蛋白质沉淀方法,可改善样品混合的均匀性,这样,易去除蛋白质并减少转移步骤。
确定






还剩7页未读,是否继续阅读?
安捷伦科技(中国)有限公司为您提供《人血浆和血清中滥用药检测方案(液相色谱仪)》,该方案主要用于司法鉴定中滥用药检测,参考标准--,《人血浆和血清中滥用药检测方案(液相色谱仪)》用到的仪器有Agilent 1290 Infinity II 液相色谱系统、Agilent Ultivo LC/MS/MS 三重四极杆液质联用系统、Agilent 1290 Infinity II Multisampler、OpenLAB 软件
推荐专场
相关方案
更多
该厂商其他方案
更多

























