
方案详情
文
所有样品都分为两组,一组为药品,另一组为药品分别添加目标限量的元素(Cd、Pb、As、Hg)。每个样品溶液准备三份。根据样品类型的不同添加对应不同的酸,并且敞口消解时间不同,可根据试剂情况进行预消解。
方案详情

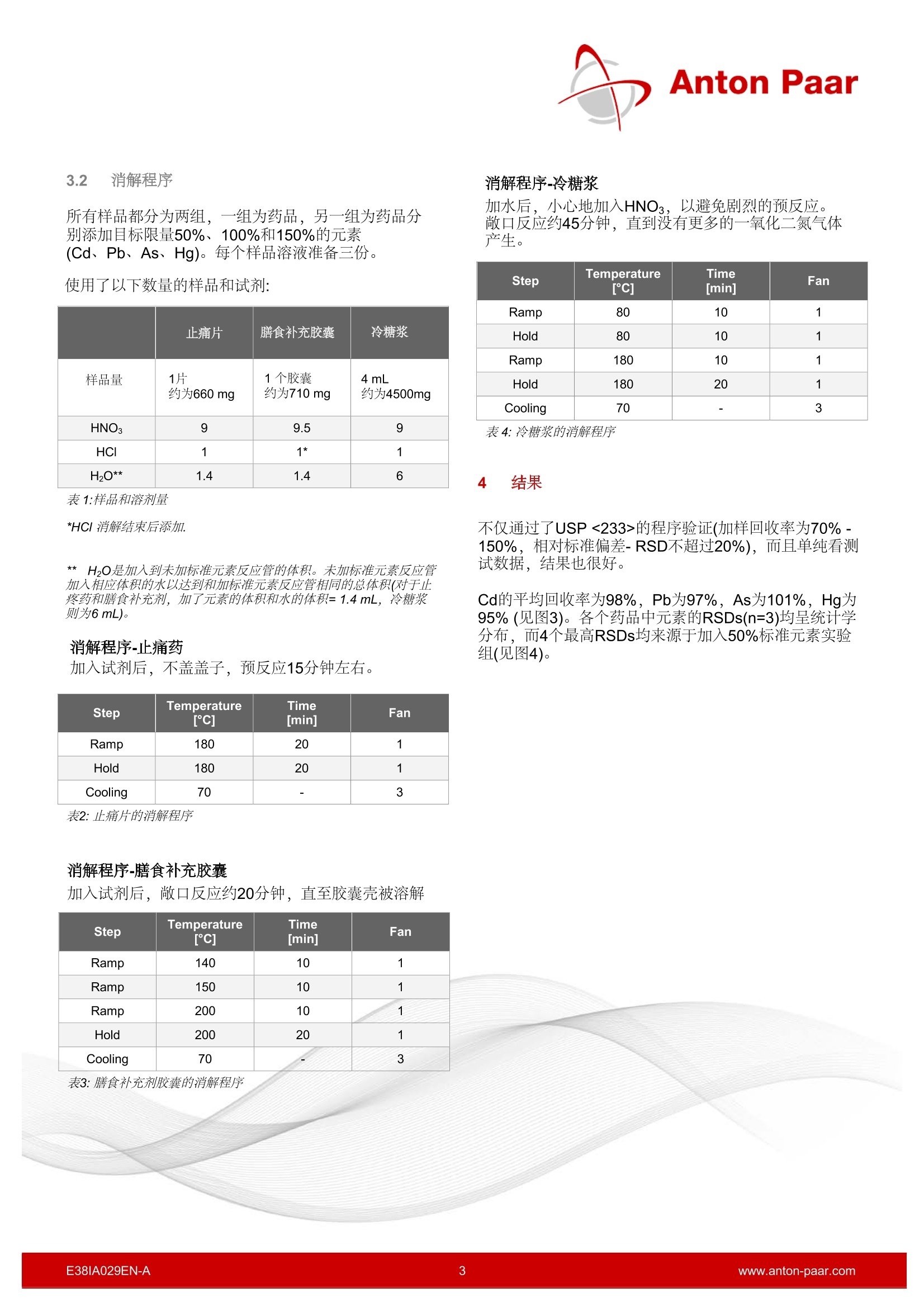
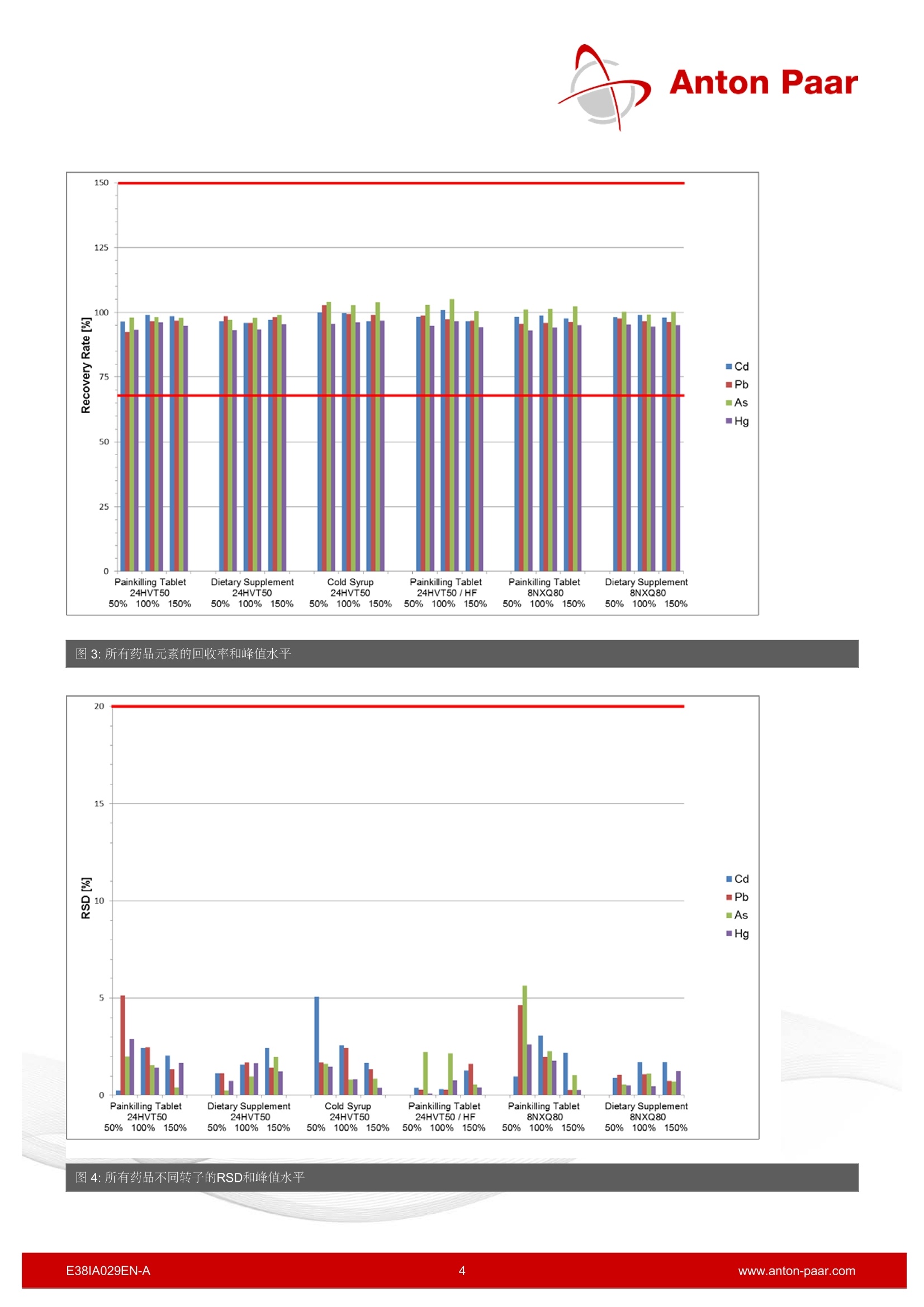
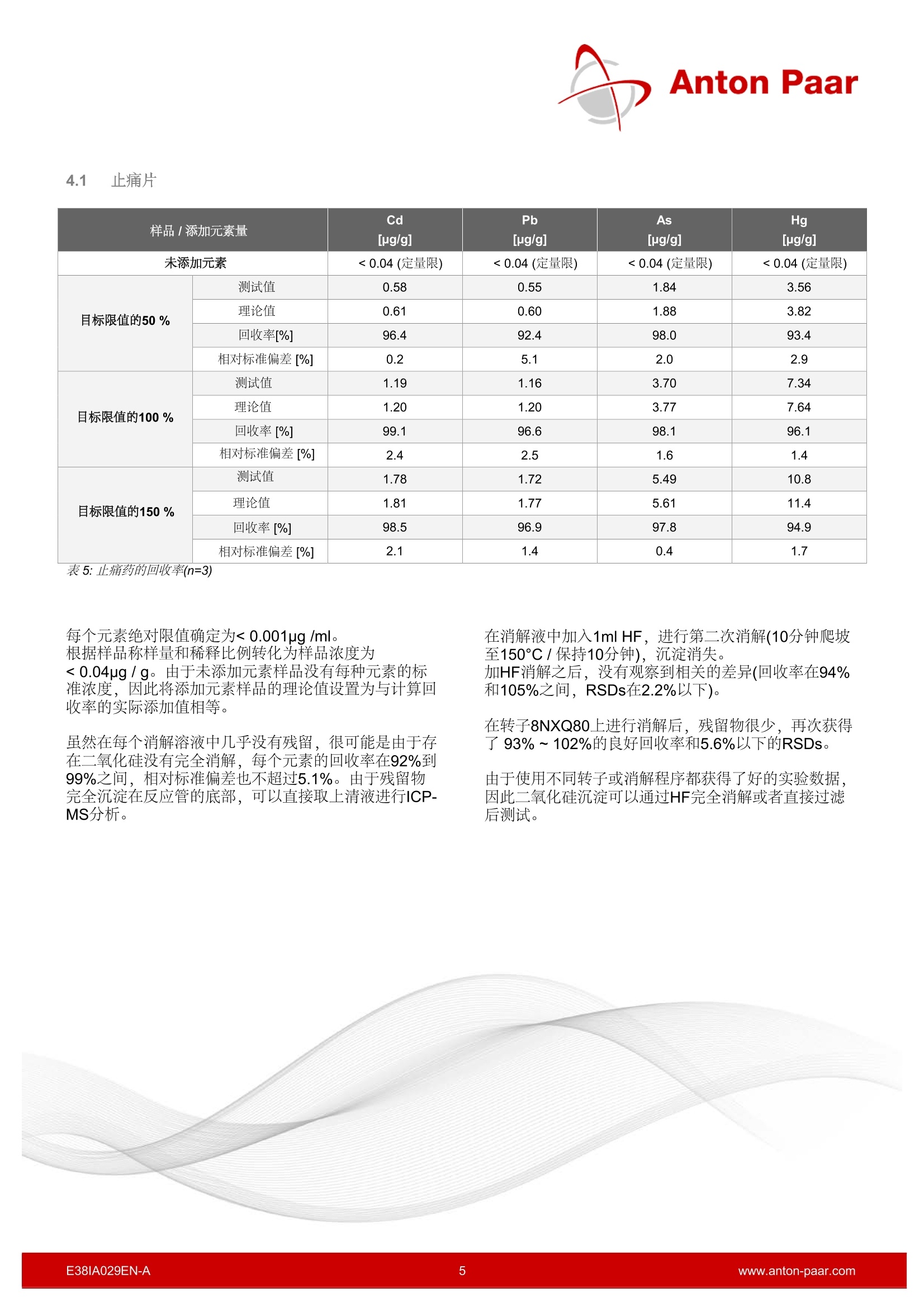
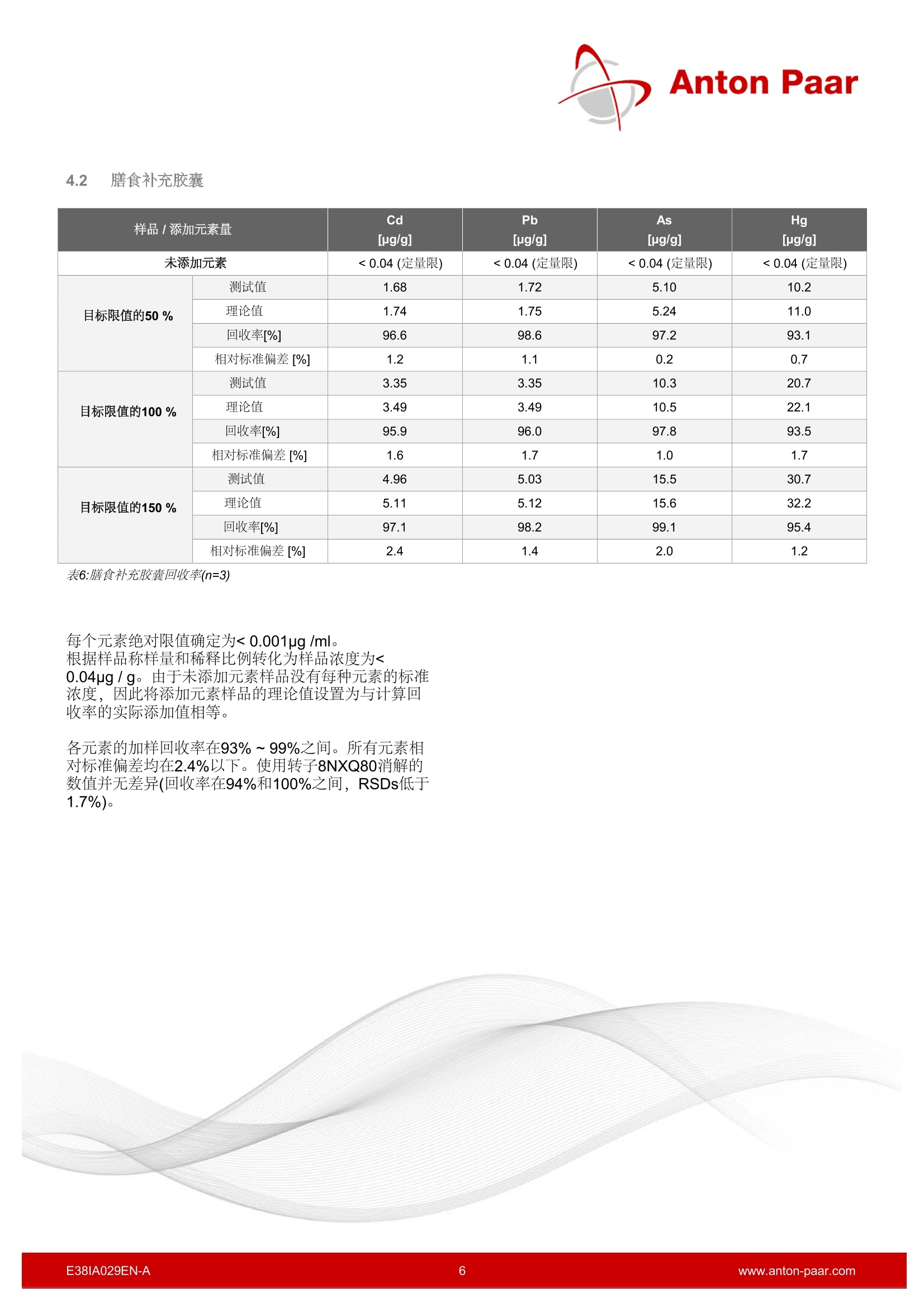
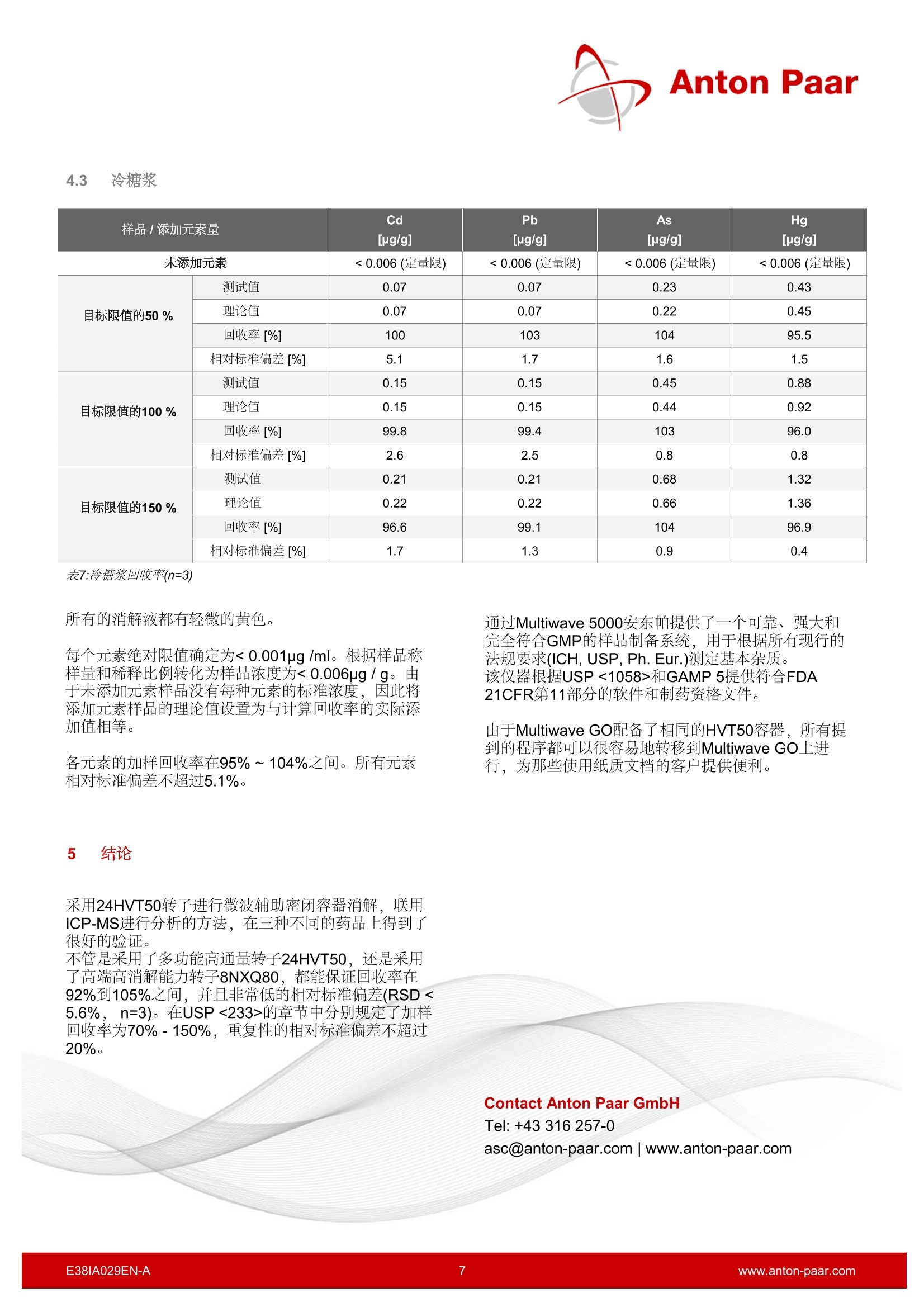
Anton Paar 根据ICH Q3D,USP <232>,,<233>,Ph. Eur. 5.20密闭消解分析元素杂质 由于重大的监管变革,自2018年1月起,所有制药产品都必须考虑元素杂质。Multiwave 5000提供丰富的样品制备选择,这些方法涵盖了各种不同的药物物方,并且完全符合GMP。 1 简介 由于元素杂质不仅对患者构成毒理风险,而且还可能影响药品的质量和功效,因此元素杂质的分析在药物的开发和质量控制中起着重要的作用。 1.1 背景介绍 到目前为止,重金属分析是根据USP <231>和Ph. Eur.2.4.8中规定的极限试验,采用硫化物沉淀法进行的。 这种已有100多年历史的方法是非特异性的,不能测定具体的定量结果。 最后,仪器行业经过一段时间的发展,在所有相关法规中,现代仪器分析已逐步取代过时的湿法化学分析。由于这些变化,使用ICP-OES或ICP-MS,以及可靠的样品制备技术,如微波辅助封闭消解,对于元素杂质的具体定量是必不可少的。 国际协调会议-ICH ICH指南Q3D step 4自2014年12月起生效,自2017年 12月起对所有产品有效。该指南根据元素杂质的毒性和它们在药物中出现的可能性,将它们分为4类:1,2A,2B和3。对于每种元素和剂型,规定了口服、非口服或吸入的 PDE(每日允许暴露)值。 特别关注的是一类无所不在的杂质,即所谓的“四大种”Cd、Pb、As和Hg, 以及2A类Co、V和Ni的金属。它们都有很强的毒性,因此具有最低的每日允许暴露值。对于这些元素,即使没有故意,也必须进行关于违反相应的每日允许暴露量可能性的风险分析。根据评估结果,必须确定合理的控制策略,管控涉及到从缺乏任何分析到定期研究,再到每批成品的常规测试。 美国药典 USP <232>元素杂质-限制和<233>元素杂质-规程于2015年12月正式生效,并取代了所有提到旧的USP<231>直到2018年1月。章节<232>中所述的限制完全符合ICH Q3D的要求。 对于膳食补充剂, USP <2232>已经于2013年8月正式发布。适用于总元素污染物分析方法USP<233>自2018年1月开始适用。 欧洲药典 欧洲药典委员会决定将ICHQ3D指南逐字翻译成欧洲药典。自2017年12月起,欧盟市场上所有现有产品都必须考虑第5.20章。 1.2 Multiwave 5000的应用 消解三种不同的配方,不同反应活性的药物: 止痛片:活性成分为乙酰水杨酸,辅料有二氧化硅不易消化 膳食补充胶囊:含有Q3脂肪酸和活性鲑鱼油 冷糖浆:三种含量高的活性成分,酒精、糖和甘油 根据USP <233>,样品中每种元素的含量需在目标限量的50%到150%之间。为了评估这些限制,我们参考了产品包装上规定的每日允许接触量和每日最大剂量。通过计算被测样品相对于理论值(未添加样品+添加值)的回收率来评估消解效果。我们特别关注是“四大中”,即镉、铅、砷和汞,因此它们的允许日暴露量最低。特别是As和Hg化合物,由于它们的挥发性,对分析有很高的要求。 2 仪器 图1: Multiwave 5000 所有的消解都是在Multiwave PRO中进行的,它是目前型号Multiwave5000的前身。使用相同的转子,容器和附件,所有方法都适用于Multiwave5000。使用24HVT50转子进行消解。为了比较不同转子消解效果,还将高端转子8NXQ80用于止疼药片和膳食补充剂胶囊的消解。 采用ICP-MS (Agilent7900) 进行定量分析。 图2: Rotor 24HVT50 3 实验 3.1 样品 止痛片 m 活性成分: 乙酰水酸 辅料: 二氧化硅,碳酸钠,巴西棕榈蜡,羟丙纤维素,硬脂酸锌 最大每日剂量: 6片(约660毫克/片) 膳食补充胶囊 活性成分: 70.4%鱼油浓缩物,含至少50%鲑鱼油、明胶、甘油、生育酚 每日最大推荐剂量: 2粒(约710毫克/胶囊) 冷糖浆 活性成分:羟苄氨嘧啶、麻黄素、氢溴酸右美沙芬、对乙酰氨基酚(扑热息痛) 辅料: 纯净水,蔗糖(27.5 g/100 mL), 乙醇96%(总含量:18vol%),甘油,聚乙二醇6000,柠檬酸钠脱水,柠檬酸一水,苯甲酸钠,安尼托尔,喹啉黄,考马斯亮蓝 每日最大剂量: 30毫升 所有样品都分为两组,一组为药品,另一组为药品分别添加目标限量50%、100%和150%的元素(Cd、Pb、As、Hg)。每个样品溶液准备三份。 使用了以下数量的样品和试剂: 止痛片 膳食补充胶囊 冷糖浆 样品量 1片约为660 mg 1个胶囊约为710 mg 4mL 约为4500mg HNO3 9 9.5 9 HCI 1 1* 1 H2O** 1.4 1.4 6 表1:样品和溶剂量 *HCI 消解结束后添加. **H20是加入到未加标准元素反应管的体积。未加标准元素反应管加入相应体积的水以达到和加标准元素反应管相同的总体积(对于止疼药和膳食补充剂,加了元素的体积和水的体积=1.4 mL,冷糖浆则为6mL)。 消解程序-止痛药 加入试剂后,不盖盖子,预反应15分钟左右。 Step Temperature [°C] Time[min] Fan Ramp 180 20 1 Hold 180 20 1 Cooling 70 3 表2:止痛片的消解程序 消解程序-膳食补充胶囊加入试剂后,敞口反应约20分钟,直至胶囊壳被溶解 Step Temperature[C] Time[min] Fan Ramp 140 10 1 Ramp 150 10 1 Ramp 200 10 1 Hold 200 20 1 Cooling 70 3 表3:膳食补充剂胶囊的消解程序 消解程序-冷糖浆 加水后,小心地加入HNO3,以避免剧烈的预反应。敞口反应约45分钟,直到没有更多的一氧化二氮气体产生。 Step Temperature [°C] Time[min] Fan Ramp 80 10 1 Hold 80 10 1 Ramp 180 10 1 Hold 180 20 1 Cooling 70 - 3 表4:冷糖浆的消解程序 4 结果 不仅通过了USP <233>的程序验证(加样回收率为70%-150%,相对标准偏差-RSD不超过20%),而且单纯看测试数据,结果也很好。 Cd的平均回收率为98%, Pb为97%,As为101%, Hg为95%(见图3)。各个药品中元素的RSDs(n=3)均呈统计学分布,而4个最高RSDs均来源于加入50%标准元素实验组(见图4)。 图3:所有药品元素的回收率和峰值水平 图4:所有药品不同转子的RSD和峰值水平 4.1 止痛片 样品/添加元素量 Cd[ug/g] Pb As Hg [ug/g] [ug/g] [ug/g] 未添加元素 <0.04(定量限) <0.04(定量限) <0.04(定量限) <0.04(定量限) 目标限值的50% 测试值 0.58 0.55 1.84 3.56 理论值 0.61 0.60 1.88 3.82 回收率[%] 96.4 92.4 98.0 93.4 相对标准偏差[%] 0.2 5.1 2.0 2.9 目标限值的100% 测试值 1.19 1.16 3.70 7.34 理论值 1.20 1.20 3.77 7.64 回收率[%] 99.1 96.6 98.1 96.1 相对标准偏差[%] 2.4 2.5 1.6 1.4 目标限值的150% 测试值 1.78 1.72 5.49 10.8 理论值 1.81 1.77 5.61 11.4 回收率[%] 98.5 96.9 97.8 94.9 相对标准偏差[%] 2.1 1.4 0.4 1.7 表5:止痛药的回收率(n=3) 每个元素绝对限值确定为< 0.001ug/ml。 根据样品称样量和稀释比例转化为样品浓度为<0.04ug/g。由于未添加元素样品没有每种元素的标准浓度,因此将添加元素样品的理论值设置为与计算回收率的实际添加值相等。 虽然在每个消解溶液中几乎没有残留,很可能是由于存在二氧化硅没有完全消解,每个元素的回收率在92%到99%之间,相对标准偏差也不超过5.1%。由于残留物完全沉淀在反应管的底部,可以直接取上清液进行ICP-MS分析。 在消解液中加入1ml HF, 进行第二次消解(10分钟爬坡至150℃/保持10分钟),沉淀消失。加HF消解之后,没有观察到相关的差异(回收率在94%和105%之间, RSDs在2.2%以下)。 在转子8NXQ80上进行消解后,残留物很少,再次获得了93%~102%的良好回收率和5.6%以下的RSDs。 由于使用不同转子或消解程序都获得了好的实验数据,因此二氧化硅沉淀可以通过HF完全消解或者直接过滤后测试。 4.2 膳食补充胶囊 样品/添加元素量 Cd[ug/g] Pb As Hg [ug/g] [ug/g] [ug/g] 未添加元素 <0.04(定量限) <0.04(定量限) <0.04(定量限) <0.04(定量限) 目标限值的50% 测试值 1.68 1.72 5.10 10.2 理论值 1.74 1.75 5.24 11.0 回收率[%] 96.6 98.6 97.2 93.1 相对标准偏差[%] 1.2 1.1 0.2 0.7 目标限值的100% 测试值 3.35 3.35 10.3 20.7 理论值 3.49 3.49 10.5 22.1 回收率[%] 95.9 96.0 97.8 93.5 相对标准偏差[%] 1.6 1.7 1.0 1.7 目标限值的150% 测试值 4.96 5.03 15.5 30.7 理论值 5.11 5.12 15.6 32.2 回收率[%] 97.1 98.2 99.1 95.4 相对标准偏差[%] 2.4 1.4 2.0 1.2 表6:膳食补充胶囊回收率(n=3) 每个元素绝对限值确定为< 0.001pg/ml。根据样品称样量和稀释比例转化为样品浓度为<0.04ug/g。由于未添加元素样品没有每种元素的标准浓度,因此将添加元素样品的理论值设置为与计算回收率的实际添加值相等。 各元素的加样回收率在93%~99%之间。所有元素相对标准偏差均在2.4%以下。使用转子8NXQ80消解的数值并无差异(回收率在94%和100%之间, RSDs低于1.7%)。 4.3 冷糖浆 样品/添加元素量 Cd [ug/g] Pb As [ug/g] Hg [ug/g] [ug/g] 未添加元素 <0.006(定量限) <0.006(定量限) <0.006(定量限) <0.006(定量限) 目标限值的50% 测试值 0.07 0.07 0.23 0.43 理论值 0.07 0.07 0.22 0.45 回收率[%] 100 103 104 95.5 相对标准偏差[%] 5.1 1.7 1.6 1.5 目标限值的100% 测试值 0.15 0.15 0.45 0.88 理论值 0.15 0.15 0.44 0.92 回收率[%] 99.8 99.4 103 96.0 相对标准偏差[%] 2.6 2.5 0.8 0.8 目标限值的150% 测试值 0.21 0.21 0.68 1.32 理论值 0.22 0.22 0.66 1.36 回收率[%] 96.6 99.1 104 96.9 相对标准偏差[%] 1.7 1.3 0.9 0.4 表7:冷糖浆回收率(n=3) 所有的消解液都有轻微的黄色。 每个元素绝对限值确定为<0.001ug/ml。根据样品称样量和稀释比例转化为样品浓度为< 0.006pg/g。由于未添加元素样品没有每种元素的标准浓度,因此将添加元素样品的理论值设置为与计算回收率的实际添加值相等。 通过Multiwave 5000安东帕提供了一个可靠、强大和完全符合GMP的样品制备系统,用于根据所有现行的法规要求(ICH, USP, Ph. Eur.)测定基本杂质。该仪器根据USP <1058>和GAMP 5提供符合FDA21CFR第11部分的软件和制药资格文件。 各元素的加样回收率在95%~104%之间。所有元素相对标准偏差不超过5.1%。 由于Multiwave GO配备了相同的HVT50容器,所有提到的程序都可以很容易地转移到Multiwave GO上进行,为那些使用纸质文档的客户提供便利。 5 结论 采用24HVT50转子进行微波辅助密闭容器消解,联用 ICP-MS进行分析的方法,在三种不同的药品上得到了 很好的验证。 不管是采用了多功能高通量转子24HVT50,还是采用了高端高消解能力转子8NXQ80,都能保证回收率在92%到105%之间,并且非常低的相对标准偏差(RSD<5.6%, n=3)。在USP<233>的章节中分别规定了加样回收率为70%-150%,重复性的相对标准偏差不超过20%。 Contact Anton Paar GmbHTel: +43 316 257-0asc@anton-paar.com|www.anton-paar.com EAN-Awww.anton-paar.com 根据USP <233>,样品中每种元素的含量需在目标限量之间。为了评估这些限制,我们参考了产品包装上规定的每日允许接触量和每日剂量。通过计算被测样品相对于理论值(未添加样品+添加值)的回收率来评估消解效果。我们特别关注是“四大中”,即镉、铅、砷和汞,因此它们的允许日暴露量低。特别是As和Hg化合物,由于它们的挥发性,对分析有很高的要求。所有样品都分为两组,一组为药品,另一组为药品分别添加目标限量的元素(Cd、Pb、As、Hg)。每个样品溶液准备三份。根据样品类型的不同添加对应不同的酸,并且敞口消解时间不同,可根据试剂情况进行预消解。
确定


还剩5页未读,是否继续阅读?
安东帕(上海)商贸有限公司为您提供《药品中重金属检测方案(微波消解仪)》,该方案主要用于化药制剂中限度检查检测,参考标准--,《药品中重金属检测方案(微波消解仪)》用到的仪器有安东帕高性能微波消解系统Multiwave 5000
推荐专场
相关方案
更多
该厂商其他方案
更多














