
方案详情
文
Multiwave 7000系列以其优越的性能,可覆盖符合GMP的各种药品的消解。
配备 PDC(加压消解腔)的 Multiwave7000 提供了消解药品样品的应用方案,可以在一次运行过程中完全消解样品直接用于后续元素分析。
300摄氏度,200bar。
配备多种反应管,耗材成本低。
可选配磁力搅拌。
方案详情

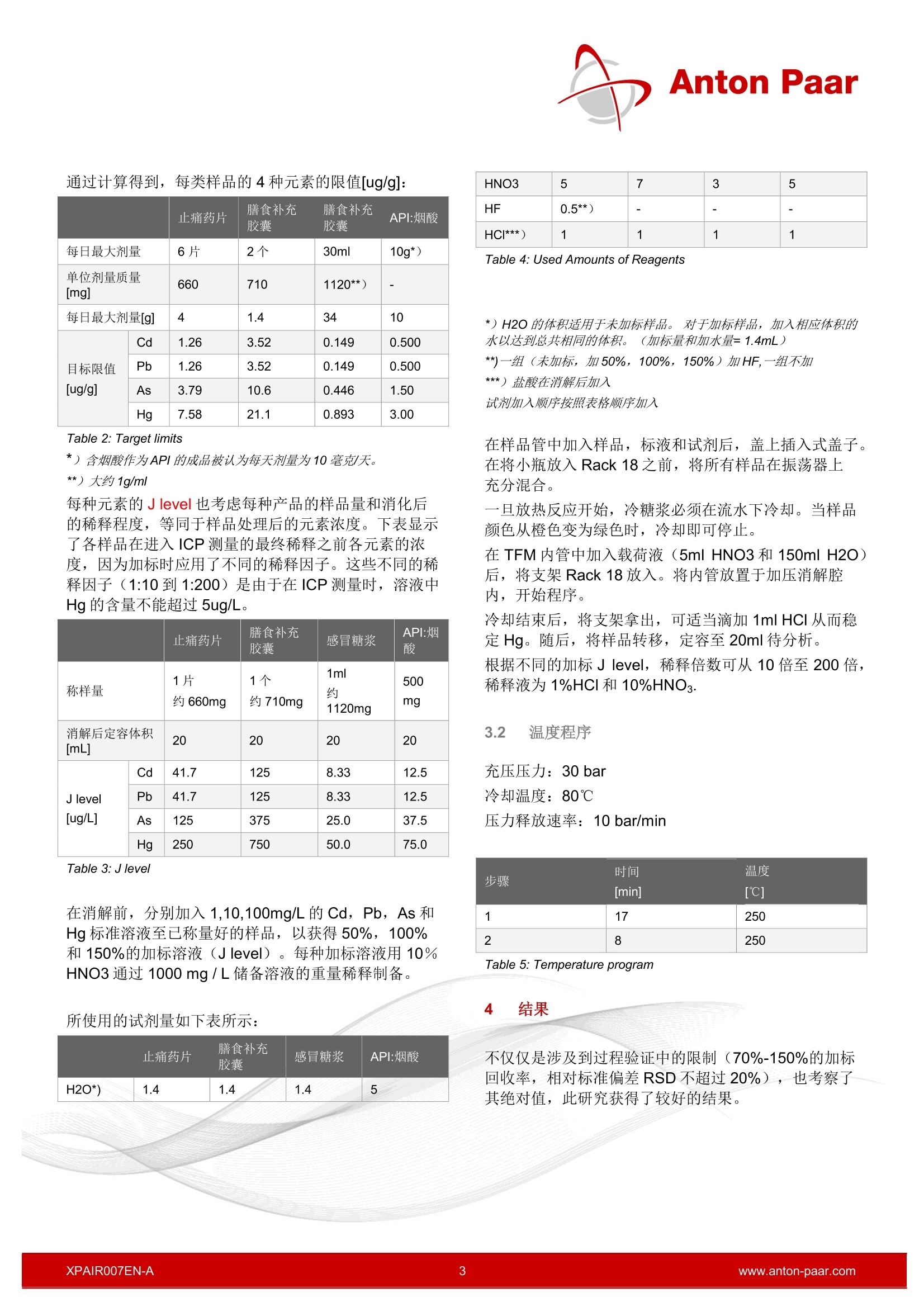
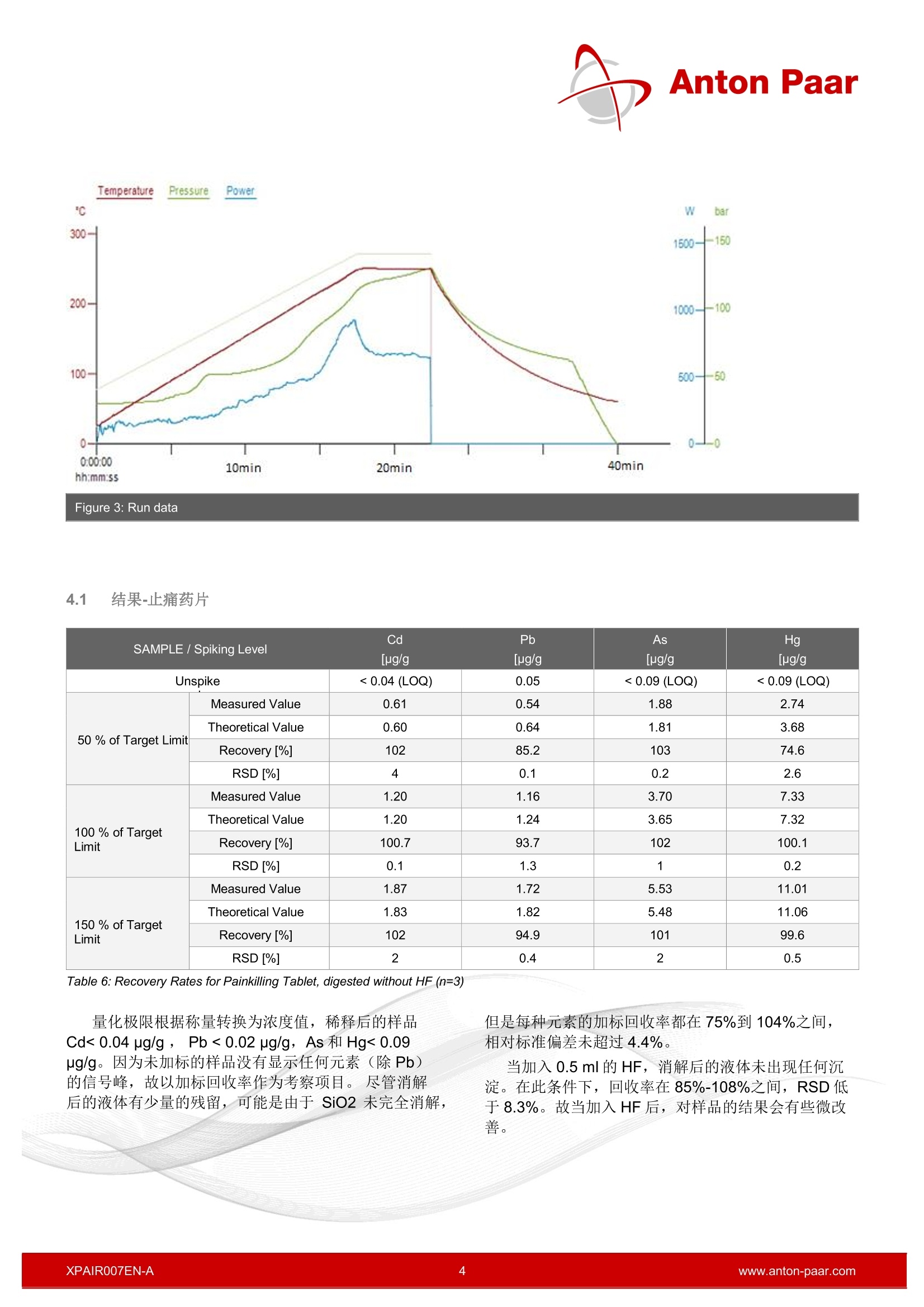
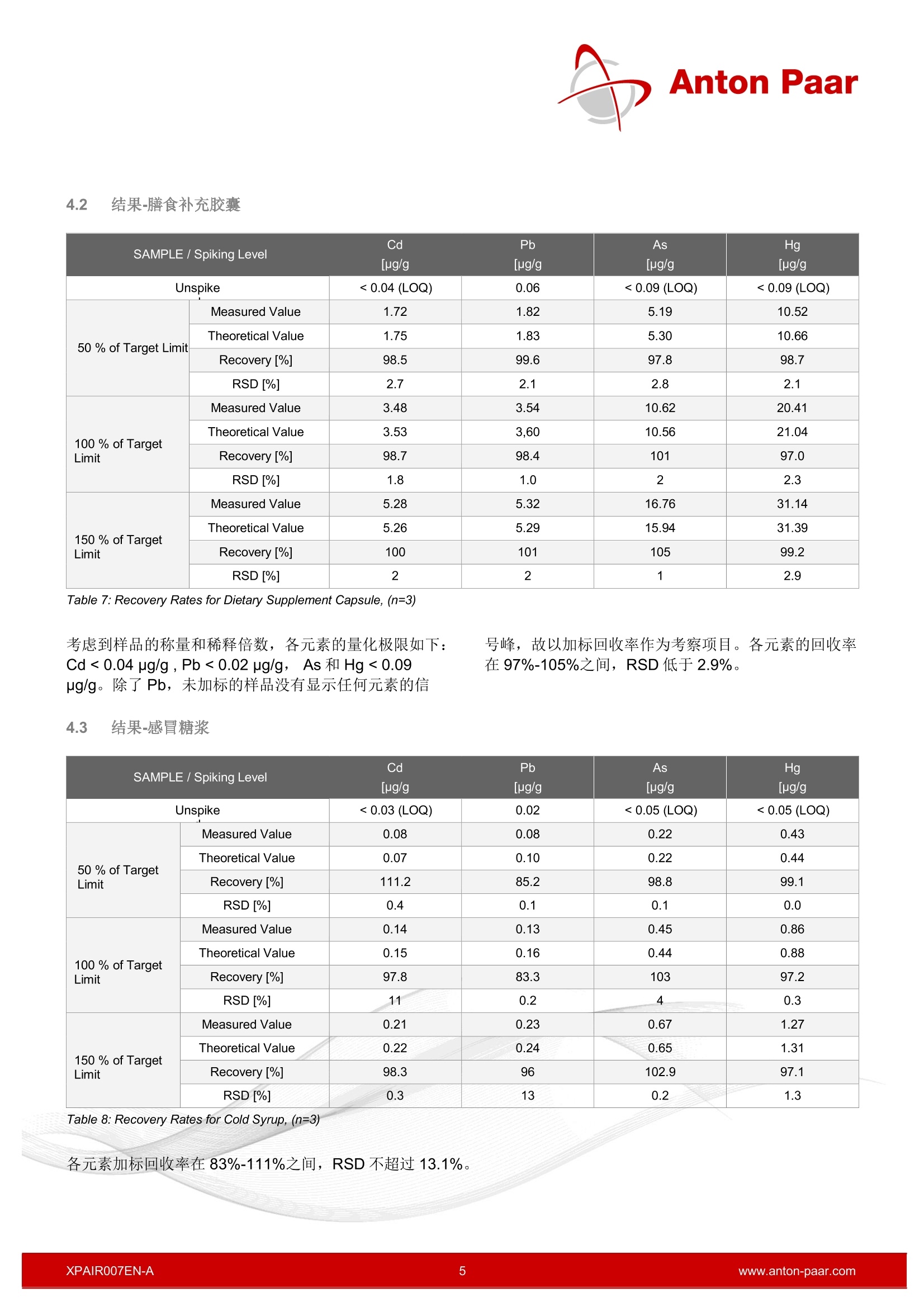
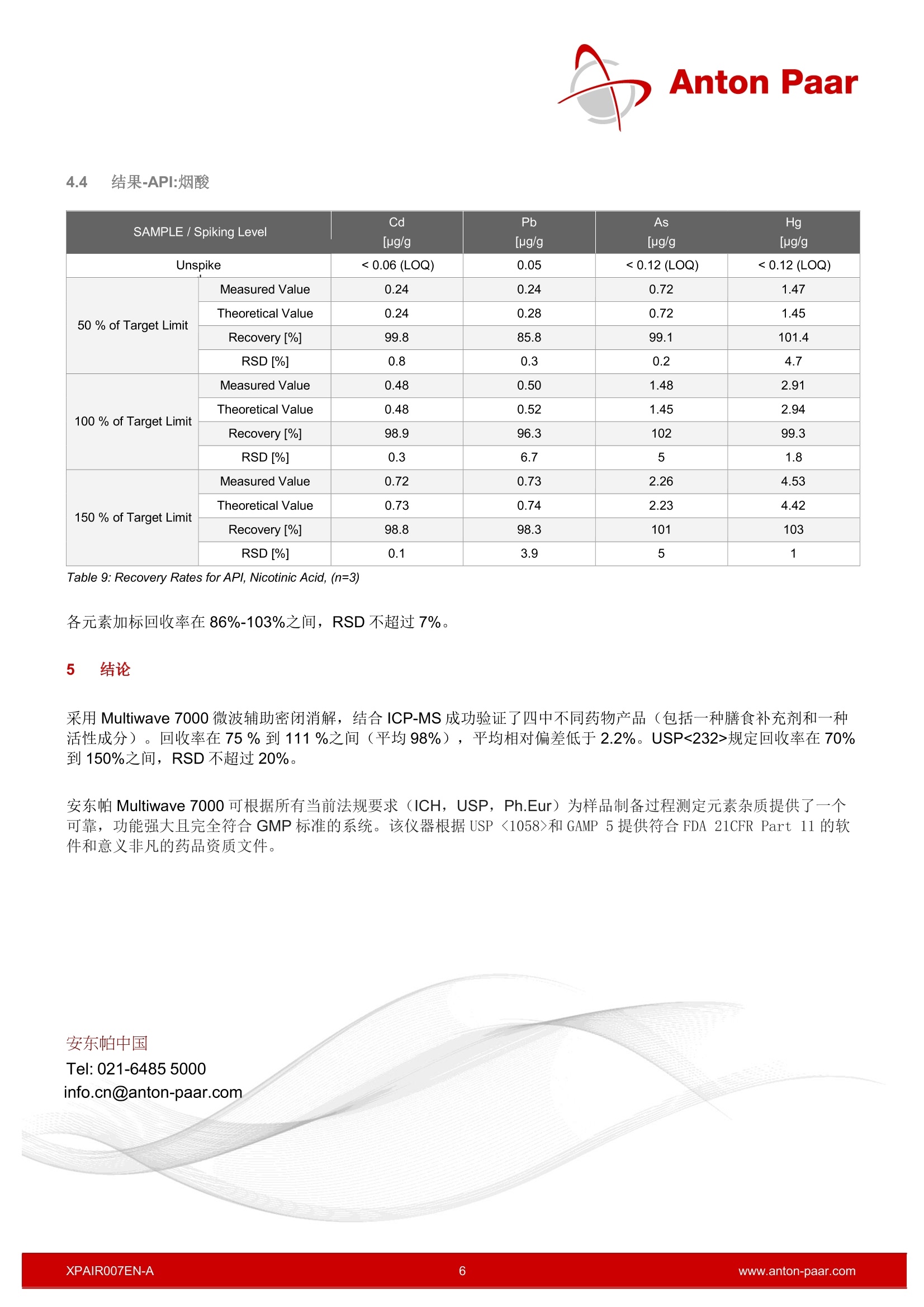
Anton Paar 超级微波在杂质元素分析中的前处理解决方案-根据法规 ICH Q3D, USP <232>,<233>, Ph. Eur. 5.20 安东帕中国 2018年1月, ICH,USP 和 Ph.Eur 等法规进行了修订,其中元素杂质的分析已作为药物产品的强制性检测项目。 Multiwave 7000 系列以其优越的性能,可覆盖符合GMP 的各种药品的消解。 1 简介 由于杂质元素不仅对病人构成中毒危险,也会影响药品的质量和药效。这些杂质元素的分析在药物的研发和质控中都扮演十分重要的角色。 1.1 法规背景 到目前为止,根据 USP<231>,Ph.Eur.2.4.8规定中的限制测试,重金属分析采用的是硫化物沉淀法。这项超过100年的旧版操作规程是不明确的,而且不允许确定具体的量化结果。终于,经过一段密集的发展期后,在相关的法律法规中,过时的湿法化学分析已逐步被现代仪器分析取代。 由于 ICP-OES 和 ICP-MS的使用,随之相关的样品前处理技术,例如微波辅助消解,目前已成为定量元素分析的主流前处理方式。 国际协调会议-ICH 自从2014年12月,ICH 指导手册中 Q3D 步骤4生效,并且市场中的所有产品都必须遵循遵循(从2018年1月开始,新的提案已提交并且已获批准)。 该指导根据元素杂质的毒性和它们在药物中产生毒性的可能性,将其分为四类-1, 2A, 2B和3,并且详细说明了元素的种类,剂型(口服,注射以及吸入)以及允许日常接触量(PDE)。口 值得注意的是,等级1中的Cd, Pb, As, Hg 和等及2种的Co, V, Ni。它们是人体致毒物,所有PDE较低。对于这些元素,即使这些金属没有人为添加,也必须进行风险分析,以防超过其PDE。根据这些评估结果,定义一个合理的控制策略,从没有任何分析到定期研究,再到最终成品的理性测试。 美国药典-USP 2015年12月, USP 232章节中元素杂质-限制和233章节元素杂质-规程正式生效,并在2018年1月,已经取代了所有对旧USP的引用。232章节中所规定的限制完全符合 ICH Q3D 的要求。 对于膳食补充剂, USP 章节<2232>自从2013年8月已正式生效。它参考了USP<233>关于全元素污染物的分析规程,也自2018年1月起开始执行。 欧洲药典-Ph.Eur. 欧洲药典委员会决定重新逐字修订 Ph. Eur. chapter5.20中的 ICH Q3D 指导方针,自2018年1月开始,欧盟市场上的所有现有产品都需考虑此问题。 1.2 Multiwave 7000 的应用 为了完美演示 Multiwave 7000 优越的消解性能,共选择4种代表性药品(包括一种膳食补充剂和一种药物活性成分-API)作为样进进行消解,这4种样品覆盖多种配方,并在消解过程中体现不同的反应行为:止痛药片:包含作为活性成分的乙酰水杨酸和难消化的作为辅料的二氧化硅。 膳食补充胶囊:包含欧米珈-3脂肪酸和鱼油 感冒糖浆:包含三重活性成分复合物和高含量的酒精,糖分和甘油 烟酸:芳香族药物活性成分,需在200℃度以上全消解。 根据 USP<233>,在样本中加入50%至150%的J等级元素标物(样品处理后的目标浓度需稀释至分析仪器的工作范围内)。为了评估这些水平,我们考虑了产品的包装单上所列的每一份的 PDE 和每日剂量的最大剂量。对于烟酸,每日最大剂量为10g/天。 通过计算被测元素的回收率(未加标和加标)来评价仪器的消解性能。由于 Cd, Pb, As, Hg的允许日常接触剂量值较低,重点考察这4种元素。由于As, Hg化合物具有挥发性,故对它们的分析要求较高。 2 仪器 Figure 1: Multiwave 7000 Figure 2: Rack 18 for Multiwave 7000 采用 Multiwave 7000微波消解仪,配备18位支架(可配18ml石英管和18mlPTFE-TFM管)来进行样品的消解。 采用 ICP-MS作为定量分析手段, Agilent 7900 和8800,配备碰撞反应池。 3 实验 3.1 样品 止痛药片 活性成分: 乙酰水杨酸 辅料: 二氧化硅,碳酸钠,巴西棕榈蜡, 羟丙甲纤维素,硬脂酸锌 膳食补充胶囊 m 配方 70.4%鱼油浓缩液(至少50%三文鱼油,,D明胶, 甘油,维生素E) 感冒糖浆 活性成分: 琥珀酸多西拉敏,麻黄碱半硫酸盐,氢溴酸右 美沙芬,对乙酰氨基酚(扑热息痛) ■ 辅料: 纯水,蔗糖(27.5 g/100 ml),96%乙醇(共18 vol%),甘油,聚乙二醇6000,无水柠檬酸钠,一水柠檬酸,苯甲酸钠,茴香脑,喹啉黄,孔雀蓝 烟酸: API 消解和加标实验 各样品加标和未加标共做3份。 下表显示了 USP<232>规定的口服剂量限制: USP 232 中的 PDE 限制 口服PDE[ug/day] Cd 5 Pb 5 As 15 Hg 30 Table 1:PDL limits, oral dosage form 通过计算得到,每类样品的4种元素的限值[ug/g]: 止痛药片 膳食补充胶囊 膳食补充胶囊 API:烟酸 每日最大剂量 6片 2个 30ml 10g*) 单位剂量质量[mg] 660 710 1120**) - 每日最大剂量[g] 4 1.4 34 10 目标限值[ug/g] Cd 1.26 3.52 0.149 0.500 Pb 1.26 3.52 0.149 0.500 As 3.79 10.6 0.446 1.50 Hg 7.58 21.1 0.893 3.00 Table 2: Target limits *)含烟酸作为 API 的成品被认为每天剂量为10毫克/天。 **) 大约1g/ml 每种元素的 J level 也考虑每种产品的样品量和消化后的稀释程度,等同于样品处理后的元素浓度。下表显示了各样品在进入 ICP 测量的最终稀释之前各元素的浓度,因为加标时应用了不同的稀释因子。这些不同的稀释因子(1:10到1:200)是由于在 ICP测量时,溶液中Hg的含量不能超过5ug/L。 止痛药片 膳食补充胶囊 感冒糖浆 API:烟 酸 称样量 1片约660mg 1个 约710mg 1ml 约 1120mg 500mg 消解后定容体积[mL] 20 20 20 20 J level[ug/L] Cd 41.7 125 8.33 12.5 Pb 41.7 125 8.33 12.5 As 125 375 25.0 37.5 Hg 250 750 50.0 75.0 Table 3: Jlevel 在消解前,分别加入1,10,100mg/L的 Cd, Pb, As和Hg标准溶液至已称量好的样品,以获得50%,100%和150%的加标溶液(Jlevel)。每种加标溶液用10%HNO3 通过 1000 mg/L储备溶液的重量稀释制备。 所使用的试剂量如下表所示: 止痛药片 膳食补充 胶囊 感冒糖浆 API:烟酸 H2O*) 1.4 1.4 1.4 5 HNO3 5 7 3 5 HF 0.5**) - - - HCI***) 1 1 1 1 Table 4: Used Amounts of Reagents *)H2O的体积适用于未加标样品。对于加标样品,加入相应体积的水以达到总共相同的体积。(加标量和加水量=1.4mL) **)一组(未加标,加50%,100%,150%)加HF,一组不加 ***)盐酸在消解后加入 试剂加入顺序按照表格顺序加入 在样品管中加入样品,标液和试剂后,盖上插入式盖子。在将小瓶放入 Rack 18 之前,将所有样品在振荡器上充分混合。 -旦放热反应开始,冷糖浆必须在流水下冷却。当样品颜色从橙色变为绿色时,冷却即可停止。 在TFM 内管中加入载荷液(5ml HNO3和150ml H2O)后,将支架 Rack 18 放入。将内管放置于加压消解腔内,开始程序。 冷却结束后,将支架拿出,可适当滴加 1ml HCI 从而稳定Hg。随后,将样品转移,定容至20ml待分析。 根据不同的加标J level,稀释倍数可从10倍至200倍,稀释液为 1%HCI 和 10%HNO3. 3.2 温度程序 充压压力:30 bar 冷却温度:80℃ 压力释放速率:10 bar/min 步骤 时间 温度 [min] [℃] 1 17 250 2 8 250 Table 5: Temperature program 4 结果 不仅仅是涉及到过程验证中的限制(70%-150%的加标回收率,相对标准偏差RSD 不超过20%),也考察了其绝对值,此研究获得了较好的结果。 Figure 3: Run data 4.1 结果-止痛药片 SAMPLE/Spiking Level Cd [pg/g Pb[ug/g As [ug/g Hg [ug/g Unspike <0.04(LOQ) 0.05 <0.09 (LOQ) <0.09 (LOQ) 50 % of Target Limit Measured Value 0.61 0.54 1.88 2.74 Theoretical Value 0.60 0.64 1.81 3.68 Recovery[%] 102 85.2 103 74.6 RSD [%] 4 0.1 0.2 2.6 100% of TargetLimit Measured Value 1.20 1.16 3.70 7.33 Theoretical Value 1.20 1.24 3.65 7.32 Recovery [%] 100.7 93.7 102 100.1 RSD [%] 0.1 1.3 1 0.2 150 % of TargetLimit Measured Value 1.87 1.72 5.53 11.01 Theoretical Value 1.83 1.82 5.48 11.06 Recovery [%] 102 94.9 101 99.6 RSD [%] 2 0.4 2 0.5 Table 6: Recovery Rates for Painkilling Tablet, digested without HF (n=3) 但是每种元素的加标回收率都在75%到104%之间,相对标准偏差未超过 4.4%。 量化极限根据称量转换为浓度值,稀释后的样品Cd<0.04 ug/g, Pb <0.02 pg/g, As 和 Hg0.09pg/g。因为未加标的样品没有显示任何元素(除Pb)的信号峰,故以加标回收率作为考察项目。尽管消解后的液体有少量的残留,可能是由于 SiO2 未完全消解, 当加入0.5 ml的HF, 消解后的液体未出现任何沉淀。在此条件下,回收率在85%-108%之间, RSD 低于8.3%。故当加入 HF后,对样品的结果会有些微改善。 4.2 结果-膳食补充胶囊 SAMPLE/Spiking Level Cd Pb As [ug/g Hg [ug/g [ug/g [ug/g Unspike <0.04 (LOQ) 0.06 <0.09 (LOQ) <0.09 (LOQ) 50 % of Target Limit- Measured Value 1.72 1.82 5.19 10.52 Theoretical Value 1.75 1.83 5.30 10.66 Recovery [%] 98.5 99.6 97.8 98.7 RSD [%] 2.7 2.1 2.8 2.1 100 % of TargetLimit Measured Value 3.48 3.54 10.62 20.41 Theoretical Value 3.53 3,60 10.56 21.04 Recovery [%] 98.7 98.4 101 97.0 RSD [%] 1.8 1.0 2 2.3 150 % of TargetLimit Measured Value 5.28 5.32 16.76 31.14 Theoretical Value 5.26 5.29 15.94 31.39 Recovery [%] 100 101 105 99.2 RSD [%] 2 2 1 2.9 Table 7: Recovery Rates for Dietary Supplement Capsule, (n=3) 考虑到样品的称量和稀释倍数,各元素的量化极限如下:Cd <0.04 pg/g, Pb <0.02 pg/g, As 和Hg<0.09pg/g。除了 Pb, 未加标的样品没有显示任何元素的信 号峰,故以加标回收率作为考察项目。各元素的回收率在97%-105%之间, RSD 低于2.9%。 4.3 结果-感冒糖浆 SAMPLE/ Spiking Level Cd Pb As[ug/g Hg [ug/g [pg/g [pg/g Unspike <0.03(LOQ) 0.02 <0.05 (LOQ) <0.05 (LOQ) 50 % of TargetLimit Measured Value 0.08 0.08 0.22 0.43 Theoretical Value 0.07 0.10 0.22 0.44 Recovery [%] 111.2 85.2 98.8 99.1 RSD [%] 0.4 0.1 0.1 0.0 100 % of TargetLimit Measured Value 0.14 0.13 0.45 0.86 Theoretical Value 0.15 0.16 0.44 0.88 Recovery [%] 97.8 83.3 103 97.2 RSD [%] 11 0.2 4 0.3 150 % of TargetLimit Measured Value 0.21 0.23 0.67 1.27 Theoretical Value 0.22 0.24 0.65 1.31 Recovery [%] 98.3 96 102.9 97.1 RSD[%] 0.3 13 0.2 1.3 Table 8: Recovery Rates for Cold Syrup, (n=3) 各元素加标回收率在 83%-111%之间, RSD 不超过 13.1%。 4.4 结果-API:烟酸 SAMPLE / Spiking Level Cd [ug/g Pb [ug/g As[ug/g Hg[ug/g Unspike <0.06 (LOQ) 0.05 <0.12 (LOQ) <0.12 (LOQ) 50 % of Target Limit Measured Value 0.24 0.24 0.72 1.47 Theoretical Value 0.24 0.28 0.72 1.45 Recovery[%] 99.8 85.8 99.1 101.4 RSD [%] 0.8 0.3 0.2 4.7 100 % of Target Limit Measured Value 0.48 0.50 1.48 2.91 Theoretical Value 0.48 0.52 1.45 2.94 Recovery [%] 98.9 96.3 102 99.3 RSD [%] 0.3 6.7 5 1.8 150 % of Target Limit Measured Value 0.72 0.73 2.26 4.53 Theoretical Value 0.73 0.74 2.23 4.42 Recovery[%] 98.8 98.3 101 103 RSD [%] 0.1 3.9 5 1 Table 9:Recovery Rates for API, Nicotinic Acid, (n=3) 各元素加标回收率在86%-103%之间, RSD 不超过7%。 5 结论 采用 Multiwave 7000 微波辅助密闭消解,结合ICP-MS 成功验证了四中不同药物产品(包括一种膳食补充剂和一种活性成分)。回收率在75%到111%之间(平均98%),平均相对偏差低于2.2%。USP<232>规定回收率在70%到150%之间, RSD 不超过 20%。 安东帕 Multiwave 7000 可根据所有当前法规要求 (ICH, USP, Ph.Eur) 为样品制备过程测定元素杂质提供了一个可靠,功能强大且完全符合 GMP标准的系统。该仪器根据 USP <1058>和 GAMP 5 提供符合FDA 21CFR Part 11 的软件和意义非凡的药品资质文件。 安东帕中国 Tel:021-6485 5000info.cn@anton-paar.com XPAIRN-Awww.anton-paar.com 由于杂质元素不仅对病人构成中毒危险,也会影响药品的质量和药效。这些杂质元素的分析在药物的研发和质控中都扮演十分重要的角色。自从2014年12月,ICH指导手册中Q3D步骤4生效,并且市场中的所有产品都必须遵循遵循(从2018年1月开始,新的提案已提交并且已获批准)。该指导根据元素杂质的毒性和它们在药物中产生毒性的可能性,将其分为四类 – 1, 2A, 2B和3,并且详细说明了元素的种类,剂型(口服,注射以及吸入)以及允许日常接触量(PDE)。值得注意的是,等级1中的Cd,Pb,As,Hg和等级2种的Co,V,Ni。它们是人体致毒物,所有PDE较低。对于这些元素,即使这些金属没有人为添加,也必须进行风险分析,以防超过其PDE。根据这些评估结果,定义一个合理的控制策略,从没有任何分析到定期研究,再到最终成品的理性测试。为了完美演示Multiwave 7000优越的消解性能,共选择4种代表性药品(包括一种膳食补充剂和一种药物活性成分-API)作为样品进行消解,这4种样品覆盖多种配方,并在消解过程中体现不同的反应行为。
确定


还剩4页未读,是否继续阅读?
安东帕(上海)商贸有限公司为您提供《药品中重金属检测方案(微波消解仪)》,该方案主要用于其他中重金属检测,参考标准--,《药品中重金属检测方案(微波消解仪)》用到的仪器有预加压型超级微波消解仪Multiwave 7X01
推荐专场
相关方案
更多
该厂商其他方案
更多














