方案详情
文
无需离子对试剂即可实现单胺神经递质与变肾上腺素的保留与基线分离
快速、同步定量尿液中的变肾上腺素和儿茶酚胺可得到线性、准确、精密的结果,线性范围为0.5-500 ng/mL
方案详情

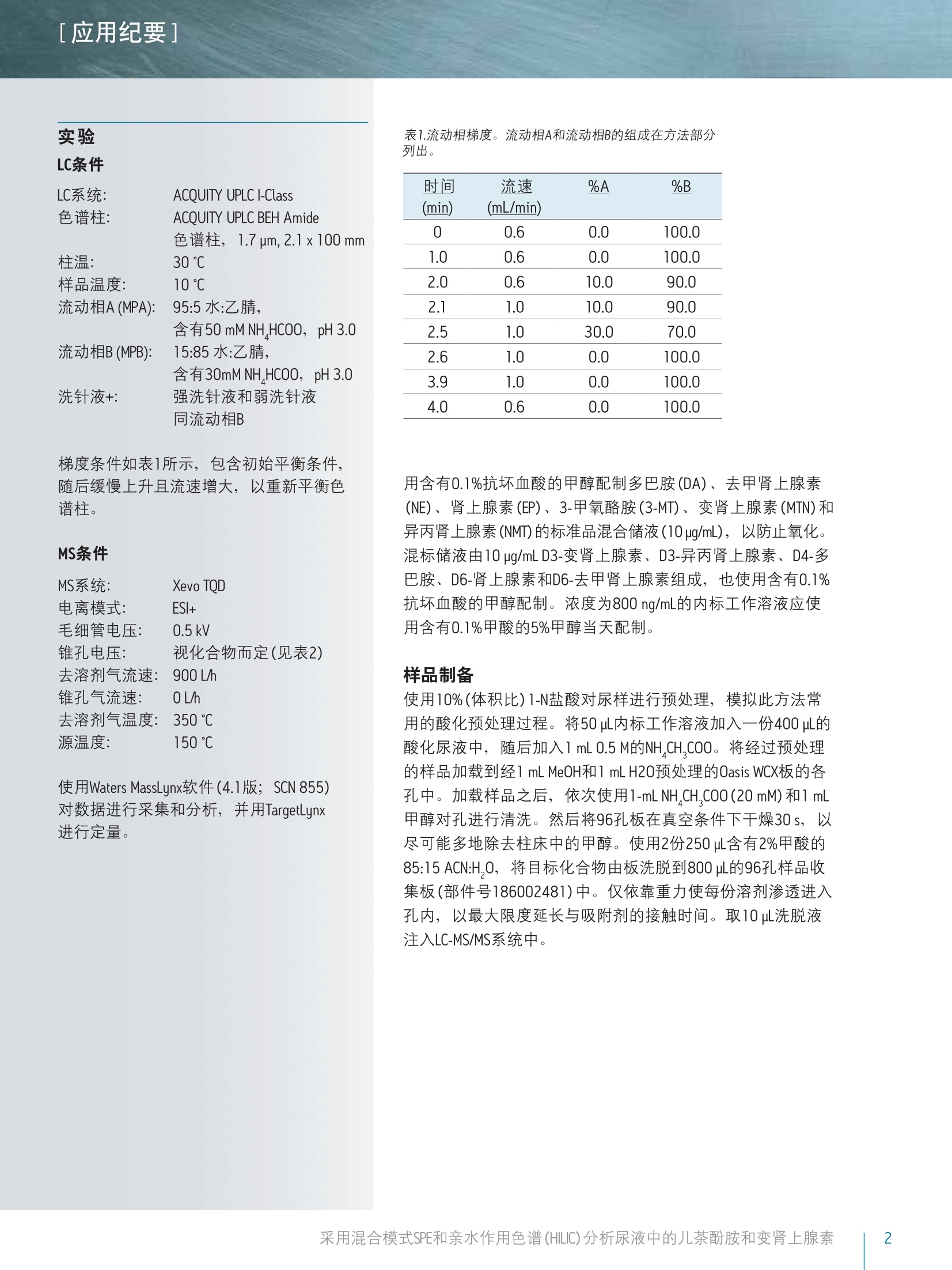
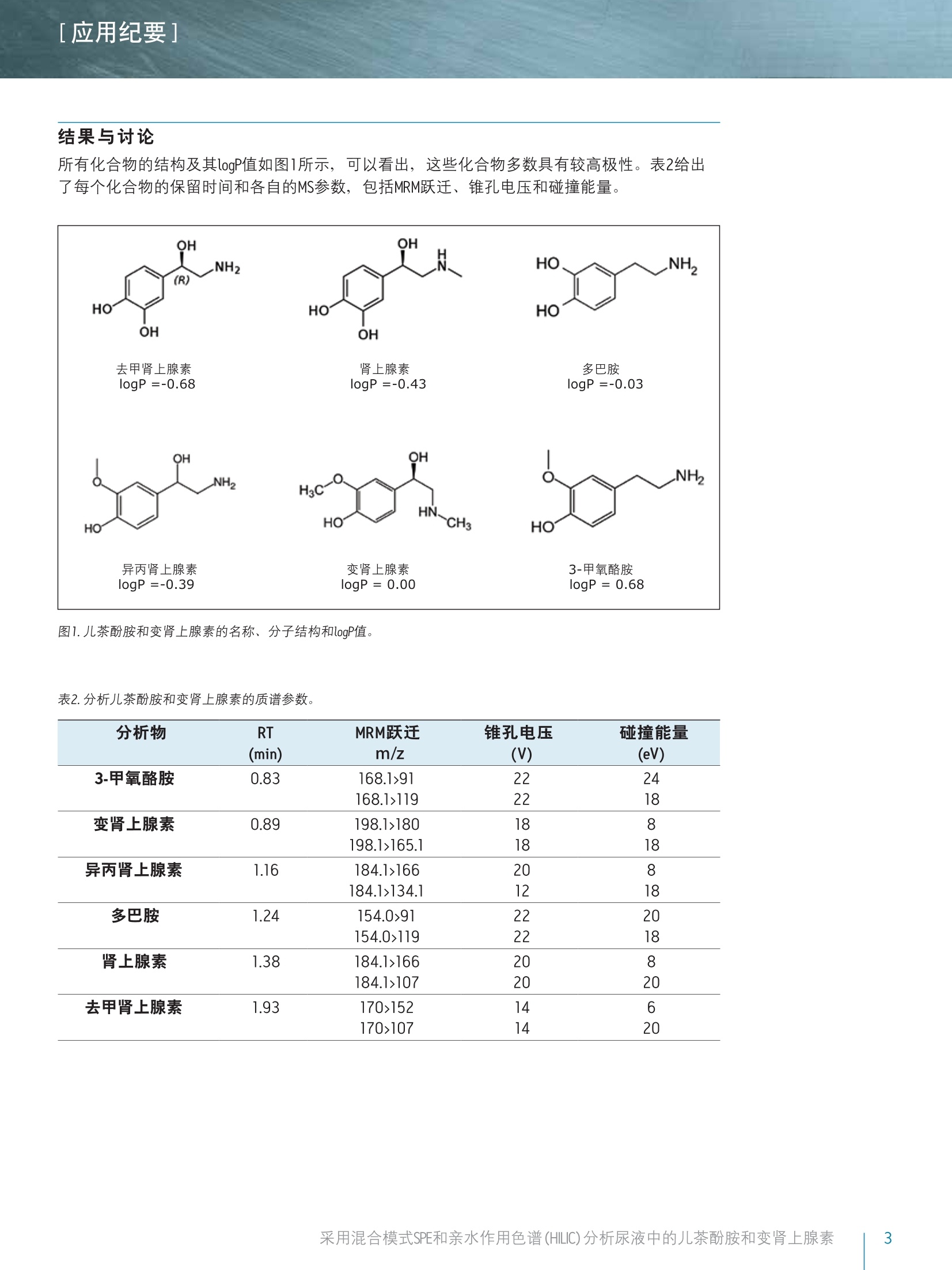
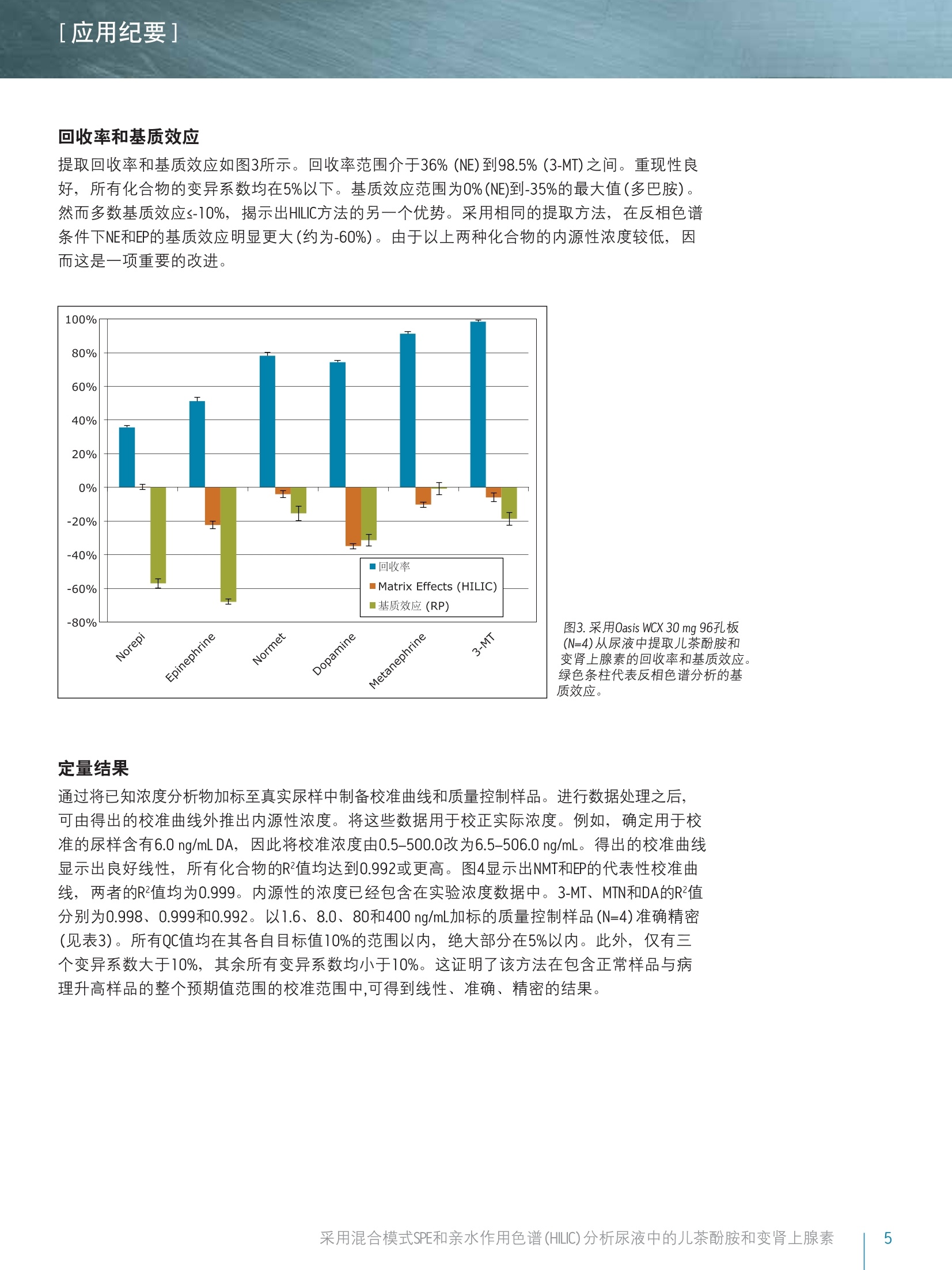
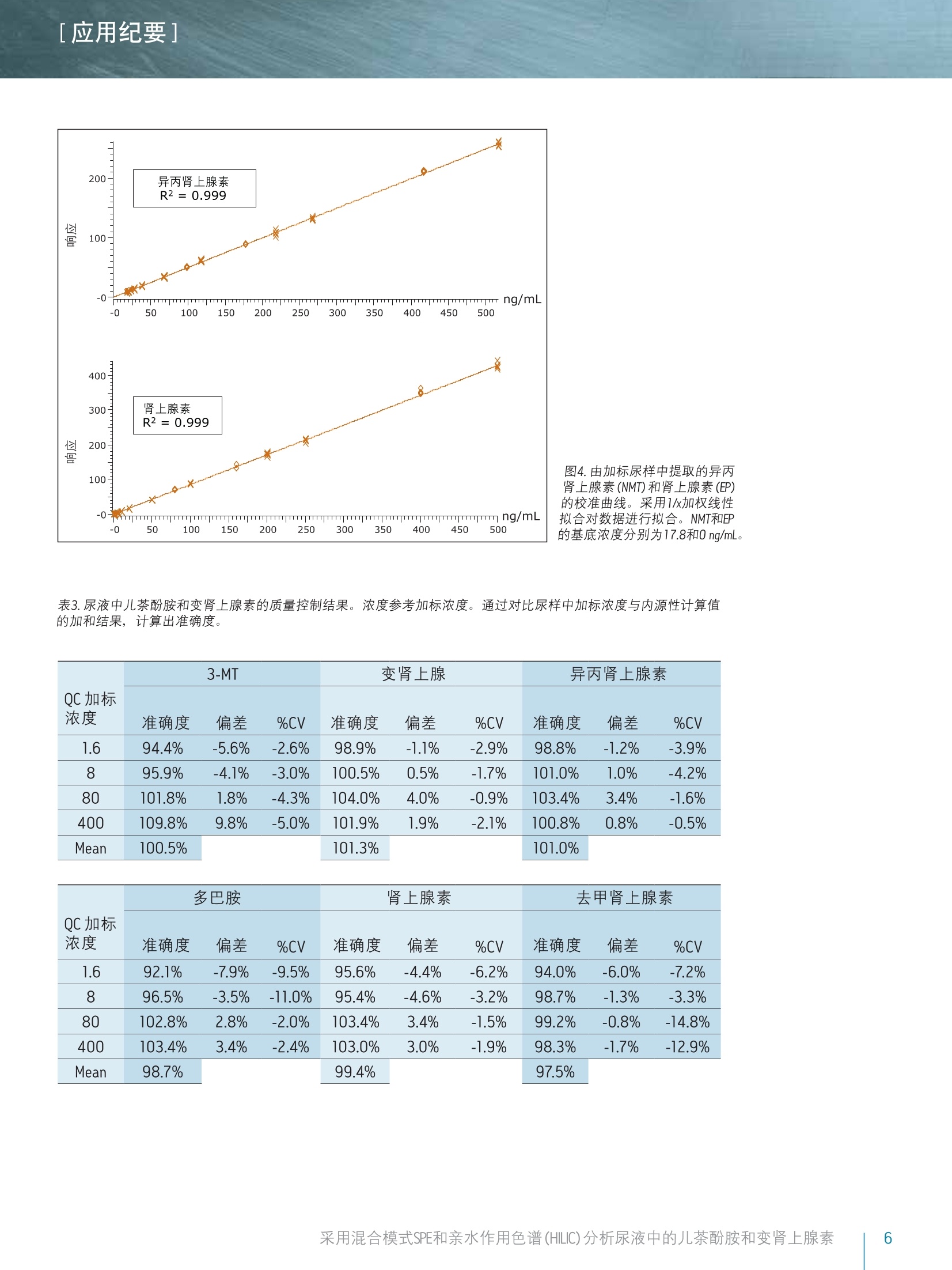
[应用纪要]THE SCIENCE OF WHAT'S POSSIBLE. [应用纪要] Waters Jonathan P. Danaceau, Erin E. Chambers 和 Kenneth J. Fountain 沃特世公司(美国马萨诸塞州米尔福德) 应用优势 ■无需离子对试剂即可实现单胺神经递质与变肾上腺素的保留与基线分离 快速、同步定量尿液中的变肾上腺素和儿茶酚胺 可得到线性、准确、精密的结果,线性范围为0.5-500 ng/mL 沃特世解决方案 Oasis@ WCX 30 mg 96孔板(部件号186002503) 96孔样品收集板,800uL圆孔(部件号186002481) ACQUITY UPLC@ BEH Amide色谱柱,1.7 um, 2.1x100 mm(部件号186004801) ACQUITY UPLC I-Class系统 Xevo TQD MassLynx@软件 关键词 儿茶酚胺,变肾上腺素, HILIC,SPE, LC-MS/MS,样品制备 简介 临床研究者通常都很关注高浓度尿液中的儿茶酚胺及其0-甲基化代谢产物(变肾上腺素)的测定。但是,这些化合物(尤其是去甲肾上腺素、肾上腺素和多巴胺)由于极性较大,利用反相LC-MS/MS对其进行分析是一项巨大挑战。因此,许多研究实验室仍采用离子对试剂与电化学检测(ECD)分析这类物质。虽然反相LC-MS/MS已得到成功应用,但由于尿液基质组分发生离子抑制、保留作用不足和异丙肾上腺素与肾上腺素未完全分离,致使挑战仍然存在。 亲水作用色谱(HILIC)已逐渐成为分析极性化合物的首选1-6。通过对之前发表的方法进行扩展6,本应用纪要介绍了尿液中单胺神经递质与儿茶酚胺的提取与分析方法。采用沃特世(Waters@) ACQUITYUPLC BEH Amide色谱柱可实现基于HILIC的色谱分离。 Waters Oasis WCX96孔板可用来提取尿液中的这些化合物。将复合模式弱阳离子交换固相萃取(SPE)板,与用于HILIC色谱和Waters Xevo TQD质谱的色谱柱结合使用,,可获得具有出色线性、准确度和精密度的快速、稳定方法,并且能最大限度减少基质效应。 梯度条件如表1所示,包含初始平衡条件,随后缓慢上升且流速增大,以重新平衡色谱柱。 MS条件 MS系统: Xevo TQD 电离模式: ESI+ 毛细管电压: 0.5kV 锥孔电压: 视化合物而定(见表2) 去溶剂气流速:900L/h 锥孔气流速: 0L/h 去溶剂气温度:350℃ 源温度: 150℃ 使用Waters MassLynx软件(4.1版; SCN 855)对数据进行采集和分析,并用TargetLynx进行定量。 表1.流动相梯度。流动相A和流动相B的组成在方法部分列出。 时间 流速 %A %B (min) (mL/min) 0 0.6 0.0 100.0 1.0 0.6 0.0 100.0 2.0 0.6 10.0 90.0 2.1 1.0 10.0 90.0 2.5 1.0 30.0 70.0 2.6 1.0 0.0 100.0 3.9 1.0 0.0 100.0 4.0 0.6 0.0 100.0 用含有0.1%抗坏血酸的甲醇配制多巴胺(DA)、去甲肾上腺素(NE)、肾上腺素(EP)、3-甲氧酪胺(3-MT)、变肾上腺素(MTN)和异丙肾上腺素(NMT)的标准品混合储液(10ug/mL),以防止氧化。混标储液由10 ug/mL D3-变肾上腺素、D3-异丙肾上腺素、D4-多巴胺、D6-肾上腺素和D6-去甲肾上腺素组成,也使用含有0.1%抗坏血酸的甲醇配制。浓度为800 ng/mL的内标工作溶液应使用含有0.1%甲酸的5%甲醇当天配制。 样品制备 使用10%(体积比)1-N盐酸对尿样进行预处理,模拟此方法常用的酸化预处理过程。将50uL内标工作溶液加入一份400uL的酸化尿液中,随后加入1 mL 0.5M的NH,CH,COO。将经过预处理的样品加载到经1 mL MeOH和1 mL H20预处理的Oasis WCX板的各孔中。加载样品之后,依次使用1-mL NH,CH,COO(20 mM)和1mL甲醇对孔进行清洗。然后将96孔板在真空条件下干燥30s,以尽可能多地除去柱床中的甲醇。使用2份250pL含有2%甲酸的85:15 ACN:H,0, 将目标化合物由板洗脱到800pL的96孔样品收集板(部件号186002481)中。仅依靠重力使每份溶剂渗透进入孔内,以最大限度延长与吸附剂的接触时间。取10pL洗脱液注入LC-MS/MS系统中。 [应用纪要] 结果与讨论 所有化合物的结构及其logP值如图1所示,可以看出,这些化合物多数具有较高极性。表2给出了每个化合物的保留时间和各自的MS参数,包括MRM跃迁、锥孔电压和碰撞能量。 图1.儿茶酚胺和变肾上腺素的名称、分子结构和logP值。 表2.分析儿茶酚胺和变肾上腺素的质谱参数。 分析物 RT MRM跃迁 锥孔电压 碰撞能量 (min) m/z (V) (eV) 3-甲氧酪胺 0.83 168.1>91 22 24 168.1>119 22 18 变肾上腺素 0.89 198.1>180 18 8 198.1>165.1 18 18 异丙肾上腺素 1.16 184.1>166 20 8 184.1>134.1 12 18 多巴胺 1.24 154.0>91 22 20 154.0>119 22 18 肾上腺素 1.38 184.1>166 20 8 184.1>107 20 20 去甲肾上腺素 1.93 170>152 14 6 170>107 14 20 [应用纪要] 图2A显示了采用ACQUITY UPLC BEH Amide色谱柱,从50 ng/mL校准标准品中得到的所有化合物的色谱图。之前的研究结果6已经表明, MPB中30 mM NH,HCOO和15%的水实现了离子强度和溶解度的完美平衡,得到的分离度和峰形如图2A所示。该分离作用的一个重要特点体现在NMT和EP之间的分离度中。这两种化合物具有相同的分子量,如果未充分分离可能会彼此干扰。在反相色谱条件下, HILIC模式中,这两种化合物之间可达到的最佳分离度为0.05 min(3 s) 和0.22 min(13.2s)的分离。HILIC模式可实现更稳定的分离,确保以上两种化合物可进行明确的定性与定量。图2B显示出未加标尿样的HILIC色谱图,表明HILIC具备校正内源性3-MT、MTN、NMT、DA、EP和NE(分别为21.6、10.6、17.8、6.0、0.0和4.1 ng/mL)的能力。未能检出EP的最大可能因素是此尿样在未进行酸化保护的情况下储存过长时间。 图2.儿茶酚胺和变肾上腺素在ACQUITY UPLC BEH Amide色谱柱(1.7um, 2.1x100 mm)上得到的色谱图。 A. 50ng/mL的代表性校准标准品。 B.显示内源性儿茶酚胺和变肾上腺素色谱图的未加标的尿样。在方法部分详细介绍了色谱条件。 [应用纪要] 回收率和基质效应 提取回收率和基质效应如图3所示。回收率范围介于36%(NE)到98.5%(3-MT)之间。重现性良好,所有化合物的变异系数均在5%以下。基质效应范围为0%(NE)到-35%的最大值(多巴胺)。然而多数基质效应s-10%,揭示出HILIC方法的另一个优势。采用相同的提取方法,在反相色谱条件下NE和EP的基质效应明显更大(约为-60%)。由于以上两种化合物的内源性浓度较低,因而这是一项重要的改进。 图3.采用Oasis WCX 30 mg 96孔板 (N=4)从尿液中提取儿茶酚胺和 变肾上腺素的回收率和基质效应。 绿色条柱代表反相色谱分析的基 质效应。 定量结果 通过将已知浓度分析物加标至真实尿样中制备校准曲线和质量控制样品。进行数据处理之后,可由得出的校准曲线外推出内源性浓度。将这些数据用于校正实际浓度。例如,确定用于校准的尿样含有6.0 ng/mL DA,因此将校准浓度由0.5-500.0改为6.5-506.0 ng/mL。得出的校准曲线显示出良好线性,所有化合物的R?值均达到0.992或更高。图4显示出NMT和EP的代表性校准曲线,两者的R²值均为0.999。内源性的浓度已经包含在实验浓度数据中。3-MT、MTN和DA的R²值分别为0.998、0.999和0.992。以1.6、8.0、80和400 ng/mL加标的质量控制样品(N=4)准确精密(见表3)。所有QC值均在其各自目标值10%的范围以内,绝大部分在5%以内。此外,仅有三个变异系数大于10%,其余所有变异系数均小于10%。这证明了该方法在包含正常样品与病理升高样品的整个预期值范围的校准范围中,可得到线性、准确、精密的结果。 图4.由加标尿样中提取的异丙 肾上腺素(NMT)和肾上腺素(EP) 的校准曲线。采用1/x加权线性 拟合对数据进行拟合。NMT和EP 的基底浓度分别为17.8和0 ng/mL。 表3.尿液中儿茶酚胺和变肾上腺素的质量控制结果。浓度参考加标浓度。通过对比尿样中加标浓度与内源性计算值的加和结果,计算出准确度。 3-MT 变肾上腺 异丙肾上腺素 QC加标 浓度 准确度 偏差 %CV 准确度 偏差 %CV 准确度 偏差 %CV 1.6 94.4% 5.6% -2.6% 98.9% -1.1% -2.9% 98.8% -1.2% -3.9% 8 95.9% -4.1% -3.0% 100.5% 0.5% -1.7% 101.0% 1.0% -4.2% 80 101.8% 1.8% -4.3% 104.0% 4.0% -0.9% 103.4% 3.4% -1.6% 400 109.8% 9.8% -5.0% 101.9% 1.9% -2.1% 100.8% 0.8% -0.5% Mean 100.5% 101.3% 101.0% 多巴胺 肾上腺素 去甲肾上腺素 QC加标 浓度 准确度 偏差 %CV 准确度 偏差 %CV 准确度 偏差 %CV 1.6 92.1% -7.9% -9.5% 95.6% -4.4% -6.2% 94.0% -6.0% -7.2% 8 96.5% -3.5% -11.0% 95.4% -4.6% 3.2% 98.7% -1.3% 3.3% 80 102.8% 2.8% -2.0% 03.4% 3.4% -1.5% 99.2% -0.8% -14.8% 400 103.4% 3.4% 2.4% 03.0% 3.0% -1.9% 98.3% -1.7% -12.9% Mean 98.7% 99.4% 97.5% 结论 本文详细描述了采用Oasis复合模式弱阳离子交换(WCX)板和ACQUITY UPLC BEH Amide色谱柱在HILIC模式下对尿液中儿茶酚胺和变肾上腺素的提取和分析过程。采用OasisWCX板进行提取,可实现所有化合物较低的基质效应和一致的回收率,并能够得到较好的精密度。与经过优化的反相分离相比, HILIC分离降低了NE和EP的基质效应,并改善了EP和NMT之间的分离度。定量结果十分出色,在0.5-500.0 ng/mL的范围内具有线性响应,并表现出出色的准确度和分析精度。 仅供研究使用。不适用于诊断。 ( 参考文献 ) ( 1. Cubbon S, AntonioC, Wilson J, T homas-Oates J. Metabolomic applications of HILIC-LC-MS. Mass Spectrom Rev. 2010 Sep-Oct;29(5):671- 8 4. ) ( . . J ian W ', Edom RW, Xu Y, Weng N. Recent advances in application of hydrophilic i nteraction c hromatography for quantitative bio a nalysis. J S ep Sci. 2010 Mar;33(6-7):681-97. ) ( 3. 1 Xu RN', Rieser MJ,El-Shourbagy T A . Bioanalytical hydrophilic interactionchromatography: re c ent challenges, solutions and applications. Bioanalysis. 2009 Apr;1(1):239-53. ) ( 4. Jian W, Xu Y, Edom RW, Weng N. Analysis of po l ar me t abolites by hydrophilic interaction chromatography-MS/MS. Bioanalysis. 201 1 Apr;3(8):899-912. ) ( 5. H emstrom P,, Irgum K. Hydrophilic interaction chromatography. J Sep Sci. 2006 Aug;29(12):1784-821. ) 6.1Danaceau JP,Chambers EE, Fountain KJ. Hydrophilic interactionchromatography (HILIC) for LC-MS/MS analysis of monoamineneurotransmitters. Bioanalysis. 2012 Apr;4(7):783-94. ( 免费售后服务热线:800( 4 00)820 2676 www.waters.com ) 采用混合模式SPE和亲水作用色谱 (HILIC)分析尿液中的儿茶酚胺和变肾上腺素
确定



还剩5页未读,是否继续阅读?
沃特世科技(上海)有限公司(Waters)为您提供《使用针对临床研究的混合模式SPE和亲水作用色谱(HILIC)对尿液中的儿茶酚胺和变肾上腺素进行快速、同步分析》,该方案主要用于尿液中--检测,参考标准--,《使用针对临床研究的混合模式SPE和亲水作用色谱(HILIC)对尿液中的儿茶酚胺和变肾上腺素进行快速、同步分析》用到的仪器有Waters ACQUITY UPLC I-Class 超高效液相色谱、Waters Xevo TQD 三重四极杆质谱
推荐专场
相关方案
更多
该厂商其他方案
更多

















