方案详情
文
无需酶水解即可分析所有代谢物,适用于由26种阿片类药物和阿片类镇痛化合物构成的综合性药物组,样品制备过程快速简单,所有分析物和代谢物具有线性响应,线性、准确度和精密度与稀释法相比都得到了提高,基质效应降低
方案详情

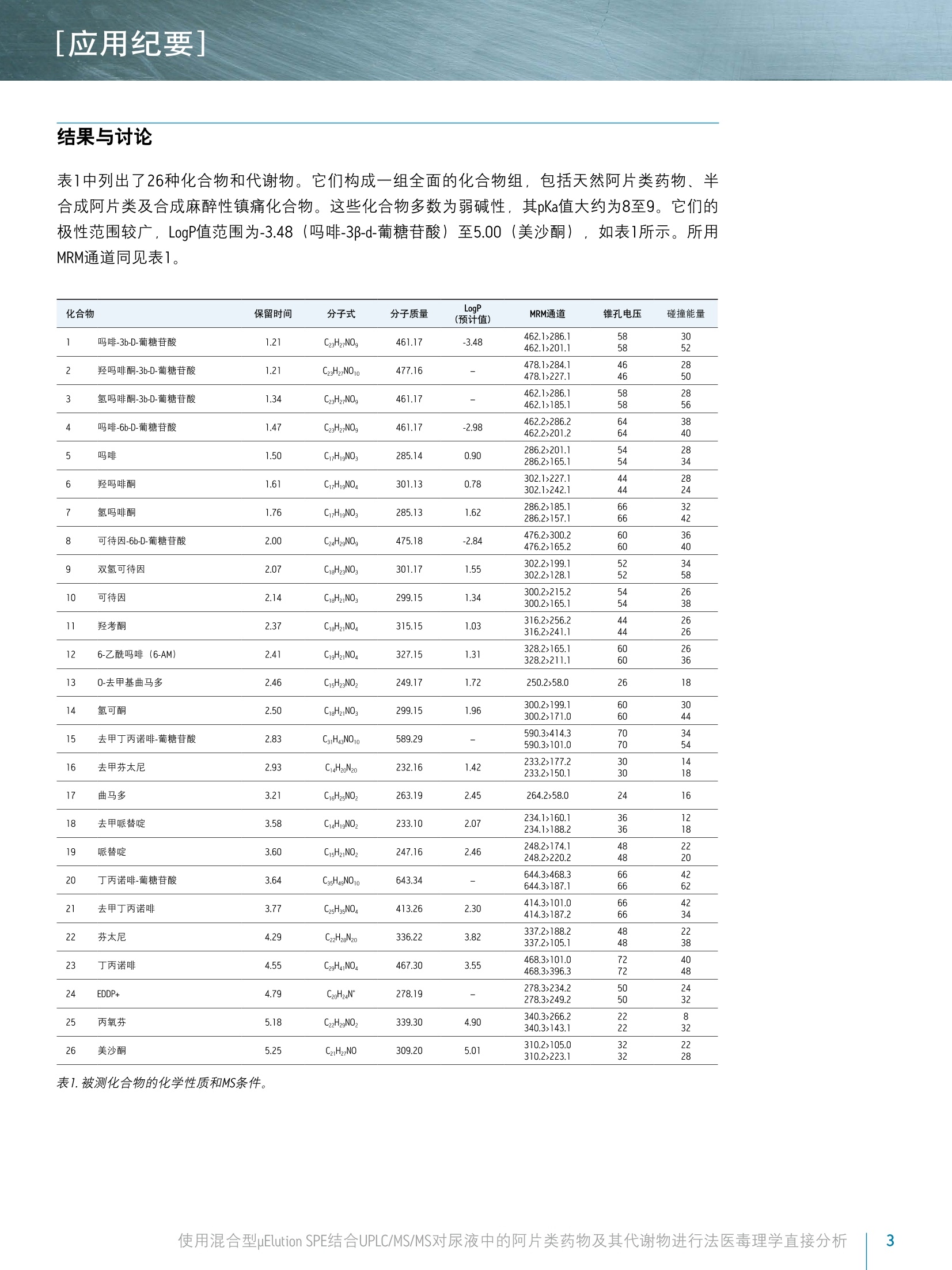
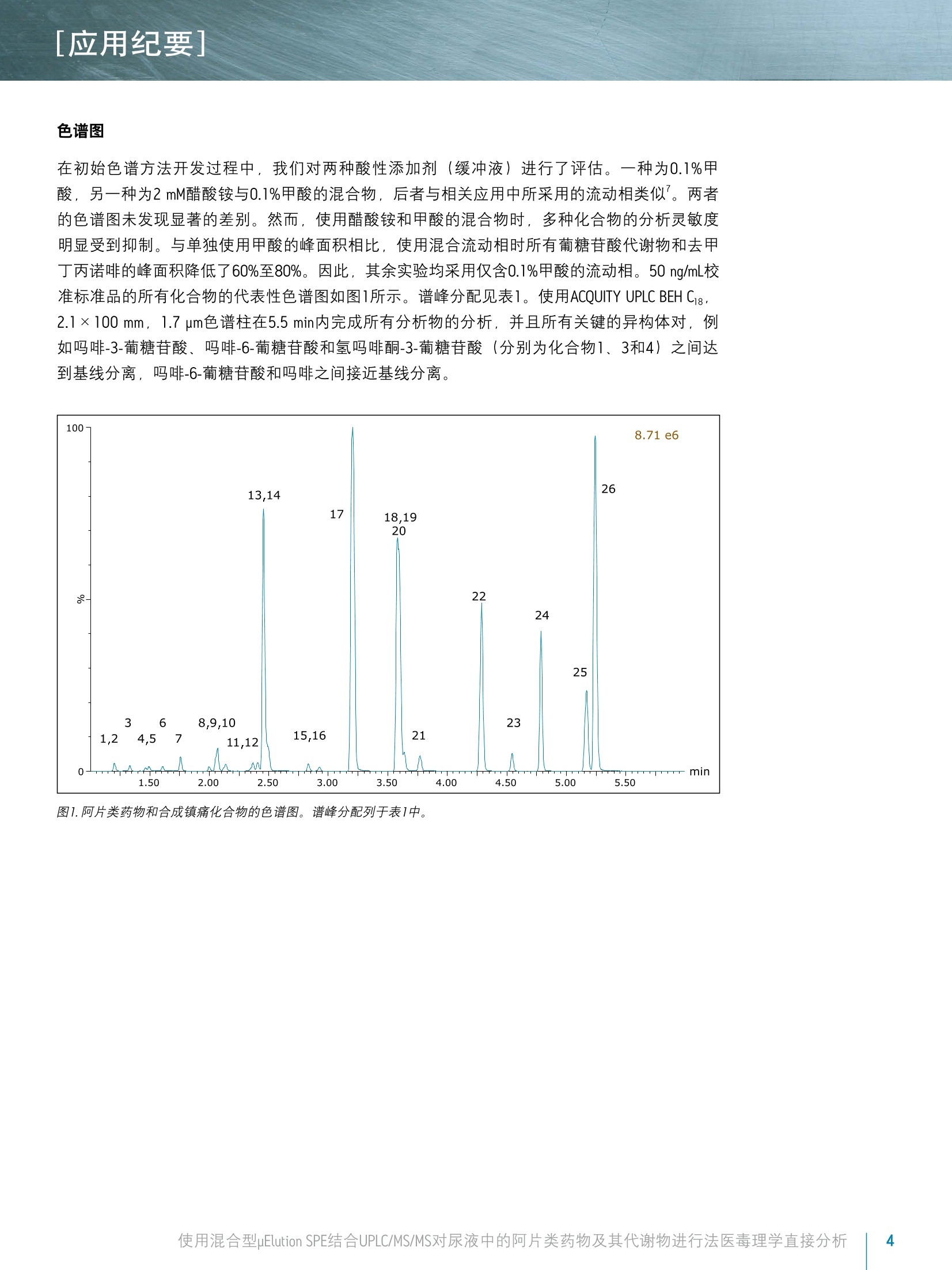
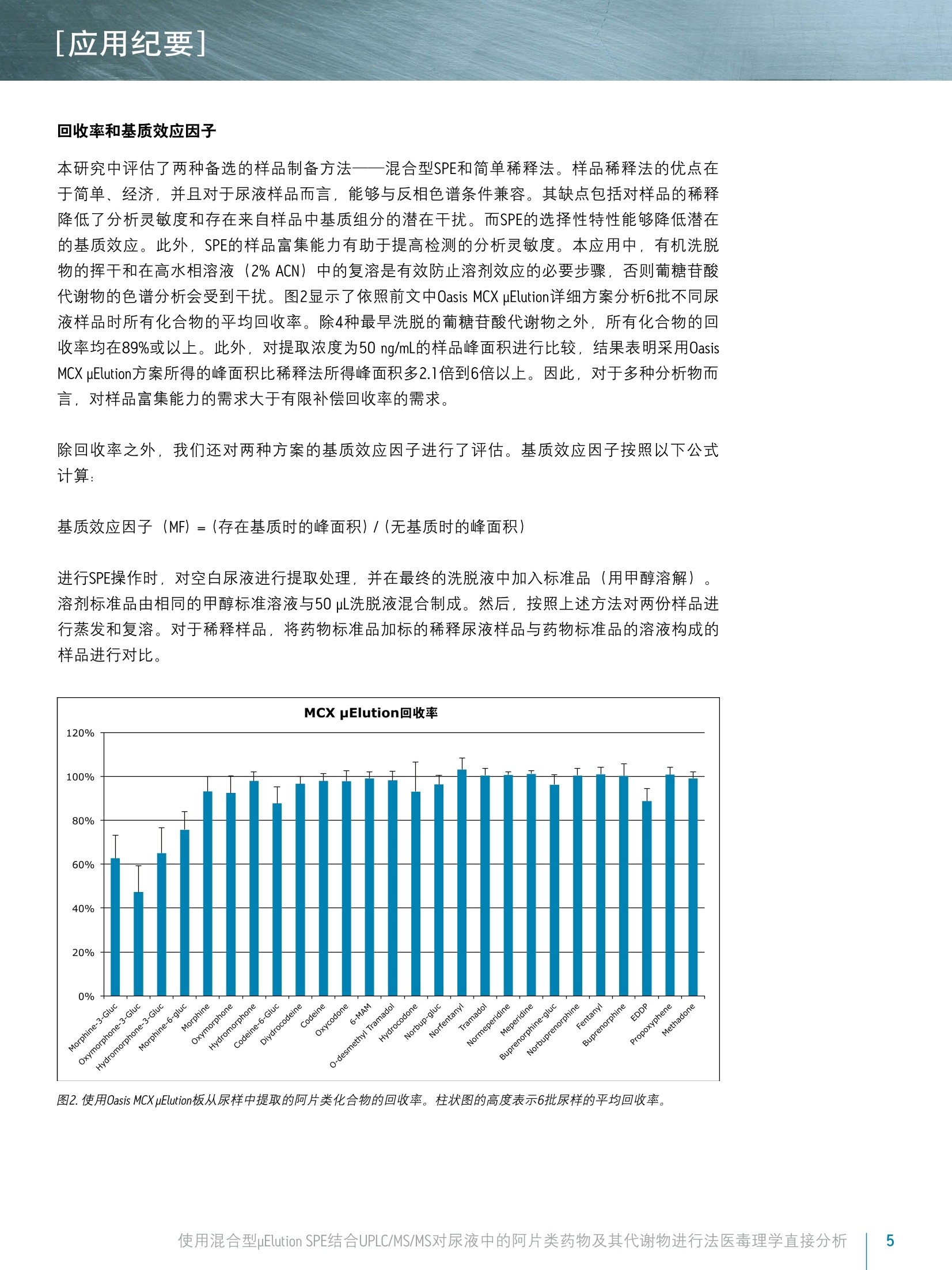
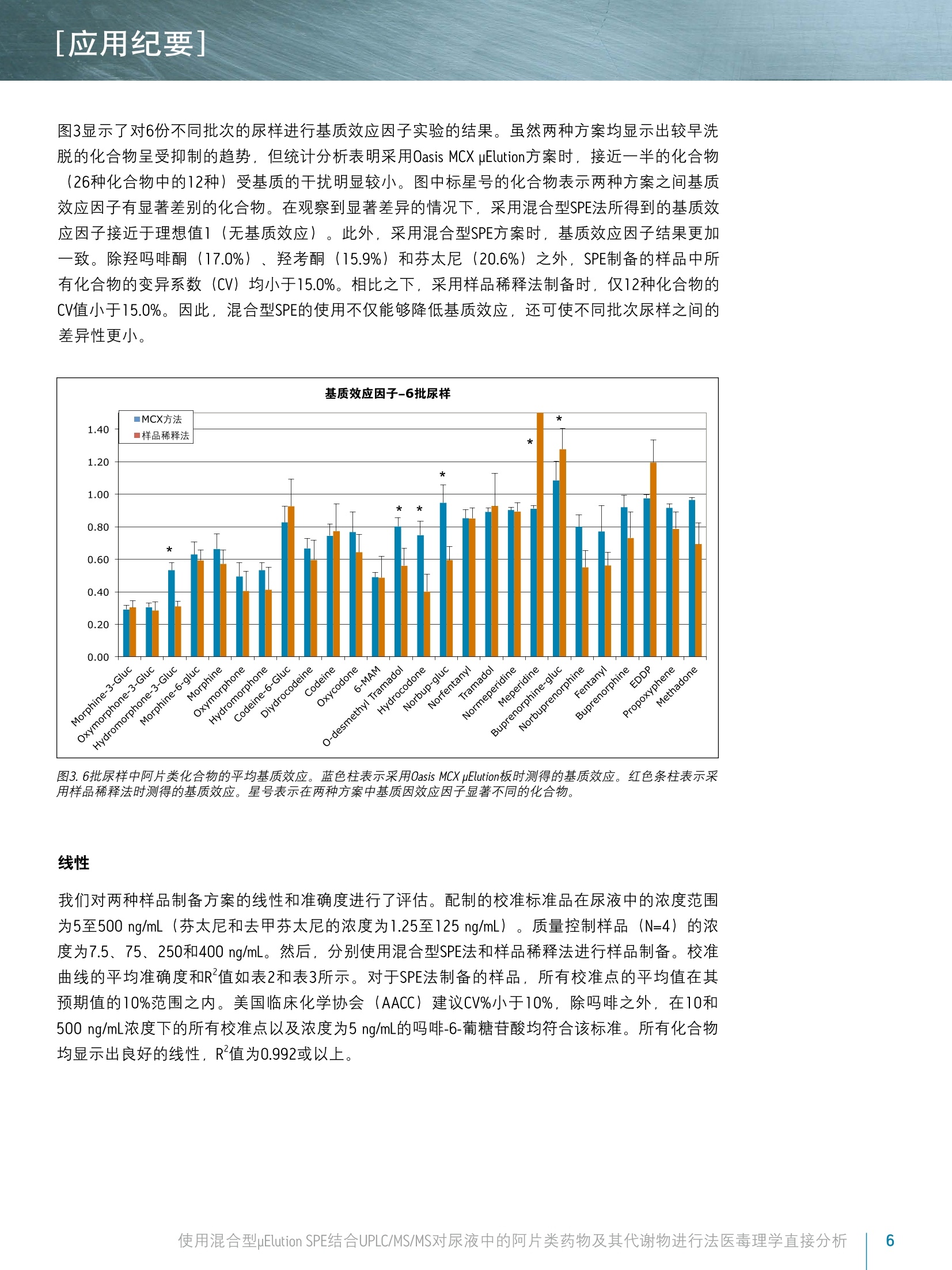
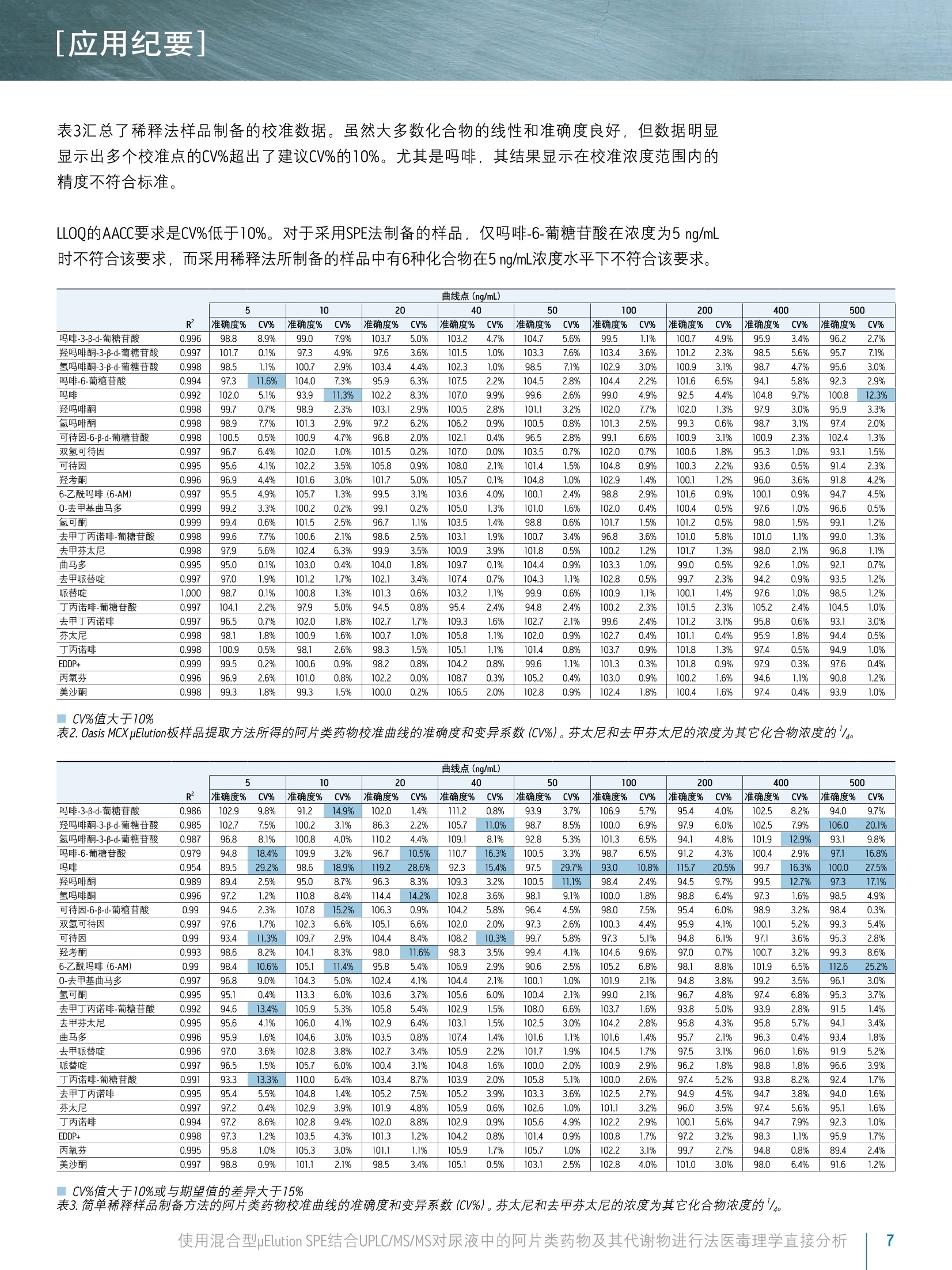
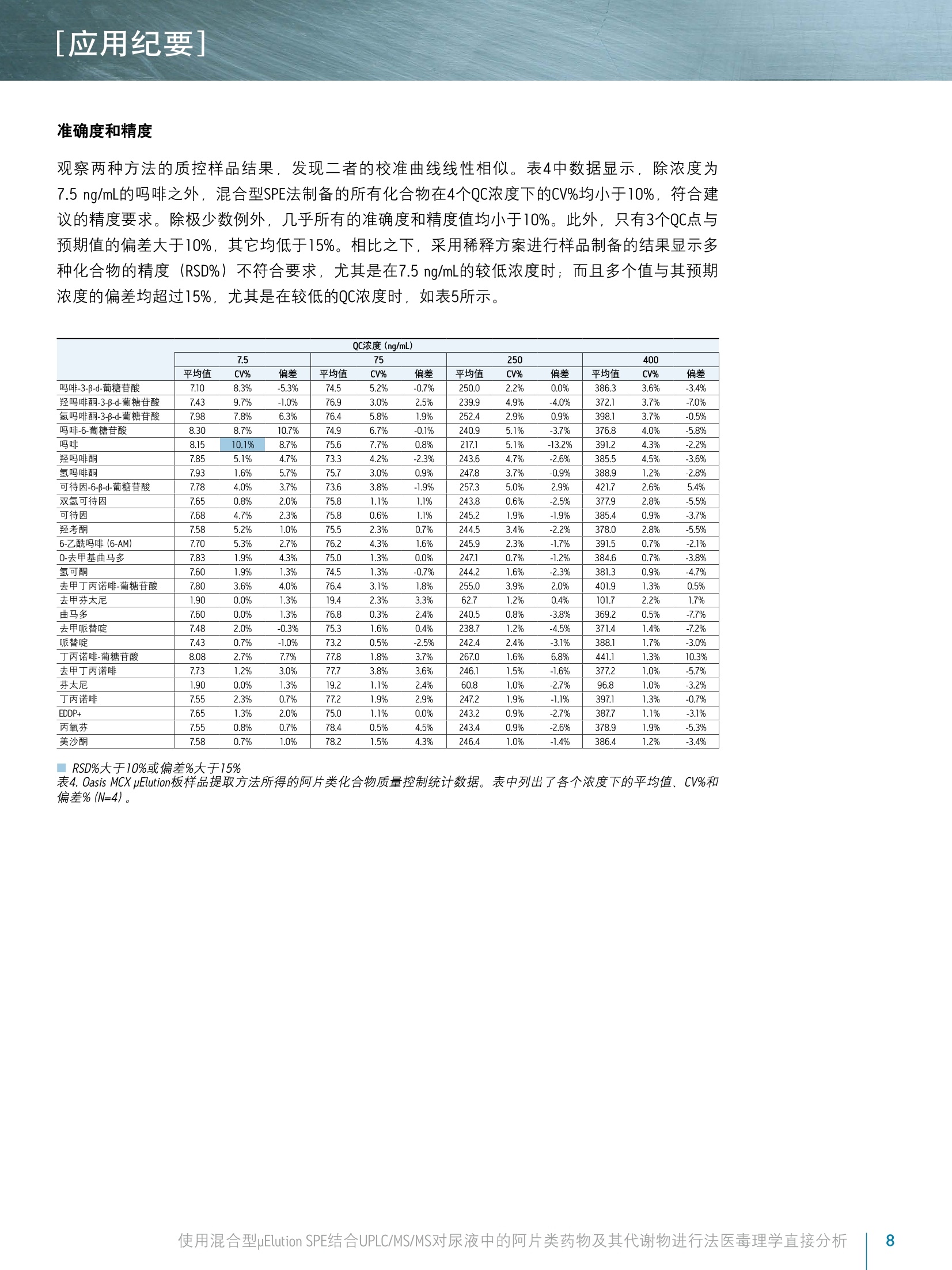
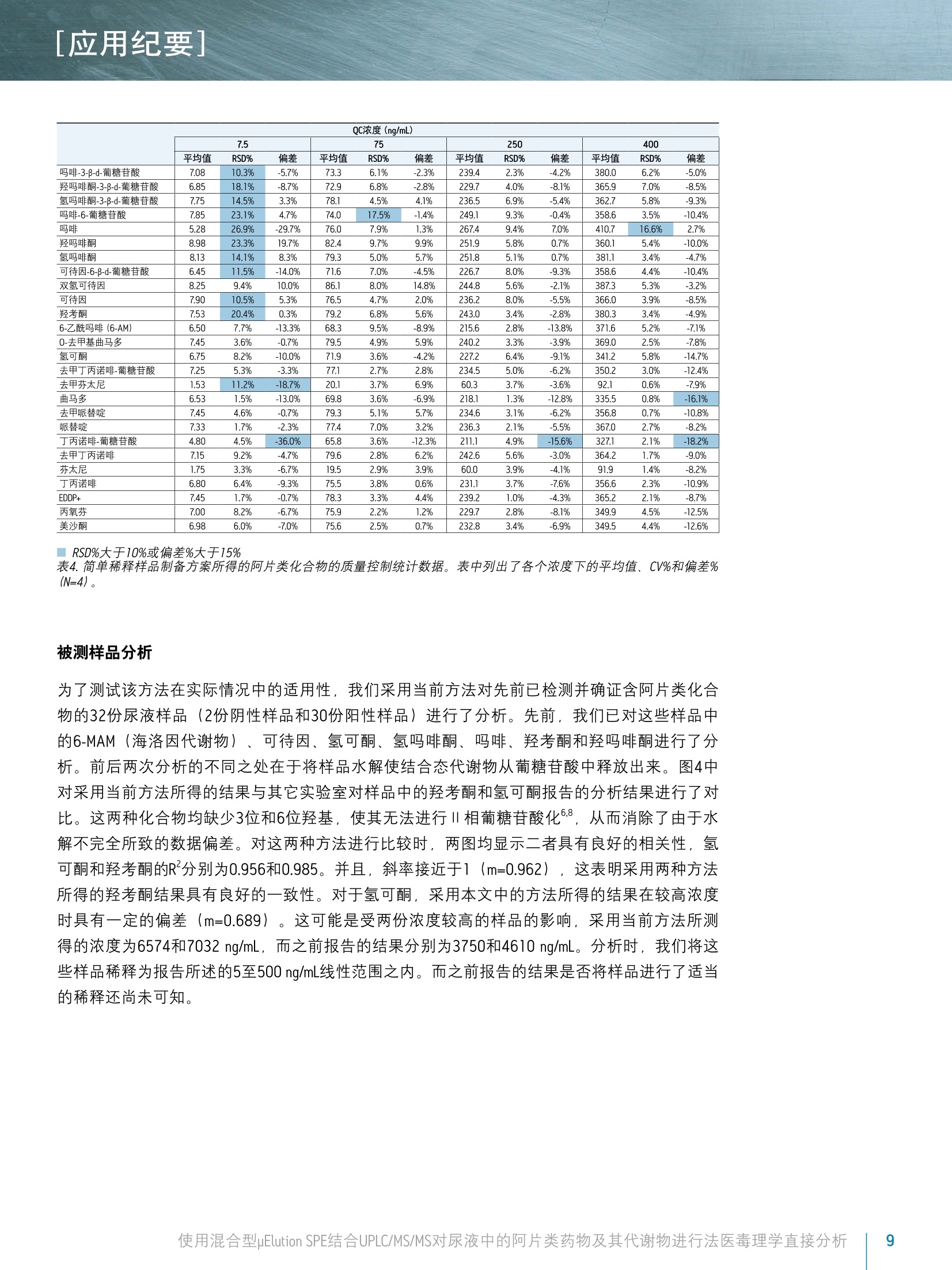
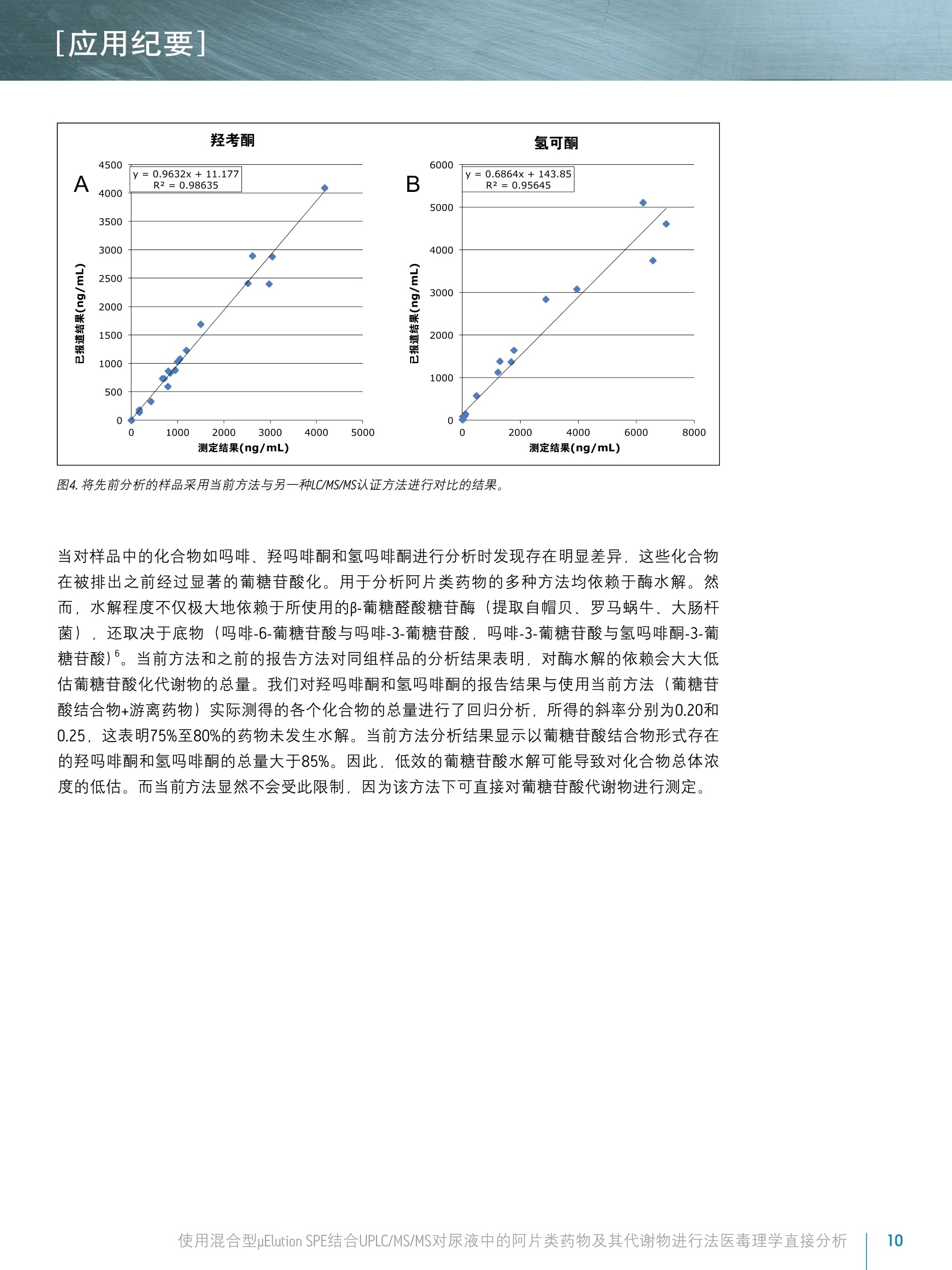
[应用纪要]THE SCIENCE OF WHAT'S POSSIBLE, [应用纪要] ■ ■ Waters Jonathan P. Danaceau. Erin E. Chambers and Kenneth J. Fountain 沃特世公司(美国马萨诸塞州米尔福德) 应用优势 无需酶水解即可分析所有代谢物 ■适用于由26种阿片类药物和阿片类镇痛化合物构成的综合性药物组 样品制备过程快速简单 ■所有分析物和代谢物具有线性响应 ■线性、准确度和精密度与稀释法相比都得到了提高 基质效应降低 沃特世解决方案 ACQUITY UPLC系统 ACQUITY UPLC BEH, 2.1×100 mm, 1.7 pm色谱柱 OasisMCX uElution板 XevoTQD质谱仪 MassLynx"软件 关键词 ( 阿片类药物,阿 片 类, UPLC, 毒理学, SPE,样品制备 ) 简介 天然和合成的阿片类药物分析一直是法医毒理学的一个重要方面。过去,通常用酸或酶使样品水解并释放出葡糖苷酸代谢物之后再进行GC/MS分析。随着LC/MS/MS技术的出现,如今可直接对葡糖苷酸代谢物进行分析25。葡糖苷酸代谢物的直接分析可消除由于水解不完全所致的假阴性风险,因为酶解效率在极大程度上取决于所使用的酶和所分析的药物底物. 与一般基质不同,尿液样品的分析可采用“稀释进样”法,即以内标混合溶液稀释样品,再直接注入LC/MS/MS系统中进行分析24。但是,这种技术的弊端是尿液样品中含有的多种基质组分可能会干扰MS信号。此外,该技术无法改变样品浓度。这可能导致某些在较高水相条件下洗脱的葡糖苷酸代谢物的定量不准确,因为在该条件下葡糖苷酸代谢物与多种阿片类药物一样会发生去溶剂化效率降低,无法生成较强的MS/MS产物碎片离子。 本应用纪要重点介绍了一种分析26种阿片类药物的方法,该方法在使用混合型SPE提取样品之后直接进行UPLC/MS/MS分析。直接分析葡糖苷酸代谢物消除了对酶解或化学水解步骤的需求。结果表明,混合型SPE与简单的 稀释进样”法相比极大地改善了线性、准确度和精密度,并减小了基质效应。此外,本实验也对之前已经确证的样品进行了分析,以便对上述方法进行进一步的评估。 实验 LC条件 LC系统: ACQUITY UPLC 色谱柱: BEH C18 2.1×100 mm, 1.7 pum 部件号186002352 柱温: 30℃ 进样体积: 10pL 流速: 0.4 mL/min流动相A: 0.1%甲酸的MilLiQ°水溶液流动相B: 0.1%甲酸的乙腈溶液梯度: 初始条件为2%的流动相B。流动相B在6.0 min内增加至47.2%,然后在0.5 min内返回至2%。重平衡系统1.5 min。整个盾环时间为8.0 min。MS条件MS系统: Xevo TQD质谱仪 电离模式: ESI*采集模式: MRM(离子通道参阅表1)毛细管电压: 1kV碰撞能量(eV): 针对具体化合物优化(参阅表1)锥孔电压(V): 针对具体化合物优化(参阅表1)数据管理: 使用MassLynx软件4.1版 采集并分析所有数据 材料 所有化合物和内标(IS) 均购自Cerilliant(德克萨斯州圆石)。除氢吗啡酮-3-葡糖苷酸、可待因-6-葡糖苷酸、去甲丁丙诺啡-葡糖苷酸、去甲芬太尼和丁丙诺啡-葡糖苷酸之外,所有化合物均有气代内标对应。对于这些化合物,具有极为相似响应的气代IS,将被选为替代物。 所有化合物的混合储液(10 ug/mL; 芬太尼和去甲芬太尼浓度为2.5 ug/mL)用甲醇配制。工作溶液需每天用使用基质(尿液)配制高浓度标准品和QC样品制备,并进行连续稀释以得到所需浓度。分析物的浓度范围为5至500 ng/mL, 只有芬太尼和去甲芬太尼的浓度配制为其它分析物浓度的25%((1.25至125 ng/mL))。所有内标混合储液(5pg/mL;芬太尼和去甲芬太尼为1.25 ug/mL)用甲醇配制。IS工作溶液每日用MilliQ水配制,浓度为50 ng/mL。 样品制备 样品制备方法包括简单稀释法或混合型SPE法。稀释法,就是将100uL尿液用含有内标的MilliQ水按照1:1进行稀释。然后将样品涡旋混合,并上样至收集板的各孔中。对于混合型SPE法,加入等量4% H,PO,和用MilliQ水配制的IS工作混合溶液(50 ng/mL),对尿液样品(空白样品、标准品、QC样品和未知样品)进行预处理。先用200pL甲醇对Oasis MCXuElution 96孔板(部件号186001830BA)各孔进行活化,然后用200uLMilliQ水进行活化。取每份制成的样品300uL加入各孔,使得载样量为100pL尿液。完成上样后,另取200pL水清洗各个孔,再用200pL甲醇清洗。然后,用含5%浓NHOH溶液 (Fisher, 20%-22%) 的50 uL 60:40 MeOH/ACN溶液洗脱所有样品,洗脱两次。洗脱结束后,在N,下将所有样品蒸干(大约5 min)),并用含0.1%甲酸和0.1%人血浆的98:2水/ACN溶液复溶。取10pL注入LC/MS/MS系统。 结果与讨论 表1中列出了26种化合物和代谢物。它们构成一组全面的化合物组,包括天然阿片类药物、半合成阿片类及合成麻醉性镇痛化合物。这些化合物多数为弱碱性,其pKa值大约为8至9。它们的极性范围较广,LogP值范围为-3.48(吗啡-3β-d-葡糖苷酸)至5.00(美沙酮),如表1所示。所用MRM通道同见表1. 化合物 保留时间 分子式 分子质量 LogP (预计值) MRM通道 锥孔电压 碰撞能量 1 吗啡-3b-D-葡糖苷酸 1.21 C23H27NO, 461.17 -3.48 462.1>286.1 462.1>201.1 58 58 30 52 2 羟吗啡酮-3b-D-葡糖苷酸 1.21 C23H27NO10 477.16 - 478.1>284.1 478.1>227.1 46 46 28 50 3 氢吗啡酮-3b-D-葡糖苷酸 1.34 C23H27NO, 461.17 - 462.1>286.1 462.1>185.1 58 58 28 56 4 吗啡-6b-D-葡糖苷酸 1.47 C23H27NO。 461.17 -2.98 462.2>286.2 462.2>201.2 64 64 38 40 5 吗啡 1.50 CHgNO 285.14 0.90 286.2>201.1 286.2>165.1 54 54 28 34 6 羟吗啡酮 1.61 C7H1gNO, 301.13 0.78 302.1>227.1 302.1>242.1 44 44 28 24 7 氢吗啡酮 1.76 C7H1gNO, 285.13 1.62 286.2>185.1 286.2>157.1 66 66 32 42 8 可待因-6b-D-葡糖苷酸 2.00 C24H2gNO, 475.18 -2.84 476.2>300.2 476.2>165.2 60 60 36 40 9 双氢可待因 2.07 CgH23NO, 301.17 1.55 302.2>199.1 302.2>128.1 52 52 34 58 10 可待因 2.14 C18H2NO: 299.15 1.34 300.2>215.2 300.2>165.1 54 54 26 38 11 羟考酮 2.37 C18H2NO 315.15 1.03 316.2>256.2 316.2>241.1 44 44 26 26 12 6-乙酰吗啡(6-AM) 2.41 C9H2NO 327.15 1.31 328.2>165.1 328.2>211.1 60 60 26 36 13 0-去甲基曲马多 2.46 C15H23NO, 249.17 1.72 250.2>58.0 26 18 14 氢可酮 2.50 C8H2NO: 299.15 1.96 300.2>199.1 300.2>171.0 60 60 30 44 15 去甲丁丙诺啡-葡糖苷酸 2.83 C31HagNO10 589.29 - 590.3>414.3 590.3>101.0 70 70 34 54 16 去甲芬太尼 2.93 CH20N20 232.16 1.42 233.2>177.2 233.2>150.1 30 30 14 18 17 曲马多 3.21 C16H25NO 263.19 2.45 264.2>58.0 24 16 18 去甲哌替啶 3.58 CIH1NOz 233.10 2.07 234.1>160.1 234.1>188.2 36 36 12 18 19 哌替啶 3.60 CsH2NO, 247.16 2.46 248.2>174.1 248.2>220.2 48 48 22 20 20 丁丙诺啡-葡糖苷酸 3.64 C35H49NO10 643.34 - 644.3>468.3 644.3>187.1 66 66 42 62 21 去甲丁丙诺啡 3.77 C25H35NO 413.26 2.30 414.3>101.0 414.3>187.2 66 66 42 34 337.2>188.2 表1.被测化合物的化学性质和MS条件。 色谱图 在初始色谱方法开发过程中,我们对两种酸性添加剂(缓冲液)进行了评估。一种为0.1%甲酸,另一种为2mM醋酸铵与0.1%甲酸的混合物,后者与相关应用中所采用的流动相类似。两者的色谱图未发现显著的差别。然而,使用醋酸铵和甲酸的混合物时,多种化合物的分析灵敏度明显受到抑制。与单独使用甲酸的峰面积相比,使用混合流动相时所有葡糖苷酸代谢物和去甲丁丙诺啡的峰面积降低了60%至80%。因此,其余实验均采用仅含0.1%甲酸的流动相。50 ng/mL校准标准品的所有化合物的代表性色谱图如图1所示。谱峰分配见表1。使用ACQUITY UPLC BEH C8,2.1×100 mm,1.7um色谱柱在5.5 min内完成所有分析物的分析,并且所有关键的异构体对,例如吗啡-3-葡糖苷酸、吗啡-6-葡糖苷酸和氢吗啡酮-3-葡糖苷酸(分别为化合物1、3和4)之间达到基线分离,吗啡-6-葡糖苷酸和吗啡之间接近基线分离。 100- 8- 图1.阿片类药物和合成镇痛化合物的色谱图。谱峰分配列于表1中。 [应用纪要] 回收率和基质效应因子 本研究中评估了两种备选的样样制备方法——混合型SPE和简单稀释法。样品稀释法的优点在于简单、经济,并且对于尿液样品而言,能够与反相色谱条件兼容。其缺点包括对样品的稀释降低了分析灵敏度和存在来自样品中基质组分的潜在干扰。而SPE的选择性特性能够降低潜在的基质效应。此外, SPE的样品富集能力有助于提高检测的分析灵敏度。本应用中,有机洗脱物的挥干和在高水相溶液(2%ACN)中的复溶是有效防止溶剂效应的必要步骤,否则葡糖苷酸代谢物的色谱分析会受到干扰。图2显示了依照前文中Oasis MCX uElution详细方案分析6批不同尿液样品时所有化合物的平均回收率。除4种最早洗脱的葡糖苷酸代谢物之外,所有化合物的回收率均在89%或以上。此外,对提取浓度为50 ng/mL的样品峰面积进行比较,结果表明采用OasisMCX uElution方案所得的峰面积比稀释法所得峰面积多2.1倍到6倍以上。因此,对于多种分析物而言,对样品富集能力的需求大于有限补偿回收率的需求。 除回收率之外,我们还对两种方案的基质效应因子进行了评估。基质效应因子按照以下公式计算: 基质效应因子(MF)=(存在基质时的峰面积)/(无基质时的峰面积) 进行SPE操作时,对空白尿液进行提取处理,并在最终的洗脱液中加入标准品((用甲醇溶解)溶剂标准品由相同的甲醇标准溶液与50uL洗脱液混合制成。然后,按照上述方法对两份样品进行蒸发和复溶。对于稀释样品,将药物标准品加标的稀释尿液样品与药物标准品的溶液构成的样品进行对比。 图2.使用Oasis MCX uElution板从尿样中提取的阿片类化合物的回收率。柱状图的高度表示6批尿样的平均回收率。 图3显示了对6份不同批次的尿样进行基质效应因子实验的结果。虽然两种方案均显示出较早洗脱的化合物呈受抑制的趋势,但统计分析表明采用Oasis MCX uElution方案时,接近一半的化合物(26种化合物中的12种)受基质的干扰明显较小。图中标星号的化合物表示两种方案之间基质效应因子有显著差别的化合物。在观察到显著差异的情况下,采用混合型SPE法所得到的基质效应因子接近于理想值1(无基质效应)。此外,采用混合型SPE方案时,基质效应因子结果更加一致。除羟吗啡酮(17.0%)、羟考酮(15.9%)和芬太太(20.6%)之外, SPE制备的样品中所有化合物的变异系数 (CV) 均小于15.0%。相比之下,采用样品稀释法制备时,仅12种化合物的CV值小于15.0%。因此,混合型SPE的使用不仅能低降低基质效应,还可使不同批次尿样之间的差异性更小。 图3.6批尿样中阿片类化合物的平均基质效应。蓝色柱表示采用Oasis MCX uElution板时测得的基质效应。红色条柱表示采用样品稀释法时测得的基质效应。星号表示在两种方案中基质因效应因子显著不同的化合物。 线性 我们对两种样品制备方案的线性和准确度进行了评估。配制的校准标准品在尿液中的浓度范围为5至500ng/mL (芬太尼和去甲芬太尼的浓度为1.25至125ng/mL)。质量控制样品(N=4)的浓度为7.5、75、250和400 ng/mL。然后,分别使用混合型SPE法和样品稀释法进行样品制备。校准曲线的平均准确度和R值如表2和表3所示。对于SPE法制备的样品,所有校准点的平均值在其预期值的10%范围之内。美国临床化学协会(AACC) 建议CV%小于10%,除吗啡之外,在10和500 ng/mL浓度下的所有校准点以及浓度为5 ng/mL的吗啡-6-葡糖苷酸均符合该标准。所有化合物均显示出良好的线性,R值为0.992或以上。 表3汇总了稀释法样品制备的校准数据。虽然大多数化合物的线性和准确度良好,但数据明显显示出多个校准点的CV%超出了建议CV%的10%。尤其是吗啡,其结果显示在校准浓度范围内的精度不符合标准。 LLOQ的AACC要求是CV%低于10%。对于采用SPE法制备的样品,仅吗啡-6-葡糖苷酸在浓度为5 ng/mL时不符合该要求,而采用稀释法所制备的样品中有6种化合物在5ng/mL浓度水平下不符合该要求。 R 曲线点(ng/mL) 5 10 20 40 50 100 200 400 500 准确度% CV% 准确度% CV% 准确度%CV% 准确度% CV% 准确度% CV% 准确度%CV% 准确度% CV% 准确度%CV% 准确度%CV% 吗啡-3-B-d-葡糖苷酸 0.996 98.8 8.9% 99.0 7.9% 103.7 5.0% 103.2 4.7% 104.7 5.6% 99.5 1.1% 100.7 4.9% 95.9 3.4% 96.2 2.7% 羟吗啡酮-3-B-d-葡糖苷酸 0.997 101.7 0.1% 97.3 4.9% 97.6 3.6% 101.5 1.0% 103.3 7.6% 103.4 3.6% 101.2 2.3% 98.5 5.6% 95.7 7.1% 氢吗啡酮-3-B-d-葡糖苷酸 0.998 98.5 1.1% 100.7 2.9% 103.4 4.4% 102.3 1.0% 98.5 7.1% 102.9 3.0% 100.9 3.1% 98.7 4.7% 95.6 3.0% 吗啡-6-葡糖苷酸 0.994 97.3 11.6% 104.0 7.3% 95.9 6.3% 107.5 2.2% 104.5 2.8% 104.4 2.2% 101.6 6.5% 94.1 5.8% 92.3 2.9% 吗啡 0.992 102.0 5.1% 93.9 11.3% 102.2 8.3% 107.0 9.9% 99.6 2.6% 99.0 4.9% 92.5 4.4% 104.8 9.7% 100.8 12.3% 羟吗啡酮 0.998 99.7 0.7% 98.9 2.3% 103.1 2.9% 100.5 2.8% 101.1 3.2% 102.0 7.7% 102.0 1.3% 97.9 3.0% 95.9 3.3% 氢吗啡酮 0.998 98.9 7.7% 101.3 2.9% 97.2 6.2% 106.2 0.9% 100.5 0.8% 101.3 2.5% 99.3 0.6% 98.7 3.1% 97.4 2.0% 可待因-6-B-d-葡糖苷酸 0.998 100.5 0.5% 100.9 4.7% 96.8 2.0% 102.1 0.4% 96.5 2.8% 99.1 6.6% 100.9 3.1% 100.9 2.3% 102.4 1.3% 双氢可待因 0.997 96.7 6.4% 102.0 1.0% 101.5 0.2% 107.0 0.0% 103.5 0.7% 102.0 0.7% 100.6 1.8% 95.3 1.0% 93.1 1.5% 可待因 0.995 95.6 4.1% 102.2 3.5% 105.8 0.9% 108.0 2.1% 101.4 1.5% 104.8 0.9% 100.3 2.2% 93.6 0.5% 91.4 2.3% 羟考酮 0.996 96.9 4.4% 101.6 3.0% 101.7 5.0% 105.7 0.1% 104.8 1.0% 102.9 1.4% 100.1 1.2% 96.0 3.6% 91.8 4.2% 6-乙酰吗啡(6-AM) 0.997 95.5 4.9% 105.7 1.3% 99.5 3.1% 103.6 4.0% 100.1 2.4% 98.8 2.9% 101.6 0.9% 100.1 0.9% 94.7 4.5% 0-去甲基曲马多 0.999 99.2 3.3% 100.2 0.2% 99.1 0.2% 105.0 1.3% 101.0 1.6% 102.0 0.4% 100.4 0.5% 97.6 1.0% 96.6 0.5% 氢可酮 0.999 99.4 0.6% 101.5 2.5% 96.7 1.1% 103.5 1.4% 98.8 0.6% 101.7 1.5% 101.2 0.5% 98.0 1.5% 99.1 1.2% 去甲丁丙诺啡-葡糖苷酸 0.998 99.6 7.7% 100.6 2.1% 98.6 2.5% 103.1 1.9% 100.7 3.4% 96.8 3.6% 101.0 5.8% 101.0 1.1% 99.0 1.3% 去甲芬太尼 0.998 97.9 5.6% 102.4 6.3% 99.9 3.5% 100.9 3.9% 101.8 0.5% 100.2 1.2% 101.7 1.3% 98.0 2.1% 96.8 1.1% 曲马多 0.995 95.0 0.1% 103.0 0.4% 104.0 1.8% 109.7 0.1% 104.4 0.9% 103.3 1.0% 99.0 0.5% 92.6 1.0% 92.1 0.7% 去甲哌替啶 0.997 97.0 1.9% 101.2 1.7% 102.1 3.4% 107.4 0.7% 104.3 1.1% 102.8 0.5% 99.7 2.3% 94.2 0.9% 93.5 1.2% 哌替啶 1.000 98.7 0.1% 100.8 1.3% 101.3 0.6% 103.2 1.1% 99.9 0.6% 100.9 1.1% 100.1 1.4% 97.6 1.0% 98.5 1.2% 丁丙诺啡-葡糖苷酸 0.997 104.1 2.2% 97.9 5.0% 94.5 0.8% 95.4 2.4% 94.8 2.4% 100.2 2.3% 101.5 2.3% 105.2 2.4% 104.5 1.0% 去甲丁丙诺啡 0.997 96.5 0.7% 102.0 1.8% 102.7 1.7% 109.3 1.6% 102.7 2.1% 99.6 2.4% 101.2 3.1% 95.8 0.6% 93.1 3.0% 芬太尼 0.998 98.1 1.8% 100.9 1.6% 100.7 1.0% 105.8 1.1% 102.0 0.9% 102.7 0.4% 101.1 0.4% 95.9 1.8% 94.4 0.5% 丁丙诺啡 0.998 100.9 0.5% 98.1 2.6% 98.3 1.5% 105.1 1.1% 101.4 0.8% 103.7 0.9% 101.8 1.3% 97.4 0.5% 94.9 1.0% EDDP+ 0.999 99.5 0.2% 100.6 0.9% 98.2 0.8% 104.2 0.8% 99.6 1.1% 101.3 0.3% 101.8 0.9% 97.9 0.3% 97.6 0.4% 丙氧芬 0.996 96.9 2.6% 101.0 0.8% 102.2 0.0% 108.7 0.3% 105.2 0.4% 103.0 0.9% 100.2 1.6% 94.6 1.1% 90.8 1.2% 美沙酮 0.998 99.3 1.8% 99.3 1.5% 100.0 0.2% 106.5 2.0% 102.8 0.9% 102.4 1.8% 100.4 1.6% 97.4 0.4% 93.9 1.0% ■CV%值大于10% 表2. Oasis MCX uElution板样品提取方法所得的阿片类药物校准曲线的准确度和变异系数(CV%)。芬太尼和去甲芬太尼的浓度为其它化合物浓度的'/4. 曲线点(ng/mL) 5 10 20 40 50 100 200 400 500 准确度%(CV% 准确度% CV% 准确度%CV% 准确度%CV% 准确度%CV% 准确度%CV% 准确度% CV% 准确度%CV% 准确度%CV% 吗啡-3-B-d-葡糖苷酸 0.986 102.9 9.8% 91.2 14.9% 102.0 1.4% 111.2 0.8% 93.9 3.7% 106.9 5.7% 95.4 4.0% 102.5 8.2% 94.0 9.7% 羟吗啡酮-3-B-d-葡糖苷酸 0.985 102.7 7.5% 100.2 3.1% 86.3 2.2% 105.7 11.0% 98.7 8.5% 100.0 6.9% 97.9 6.0% 102.5 7.9% 106.0 20.1% 氢吗啡酮-3-B-d-葡糖苷酸 0.987 96.8 8.1% 100.8 4.0% 110.2 4.4% 109.1 8.1% 92.8 5.3% 101.3 6.5% 94.1 4.8% 101.9 12.9% 93.1 9.8% 吗啡-6-葡糖苷酸 0.979 94.8 18.4% 109.9 3.2% 96.7 10.5% 110.7 16.3% 100.5 3.3% 98.7 6.5% 91.2 4.3% 100.4 2.9% 97.1 16.8% 吗啡 0.954 89.5 29.2% 98.6 18.9% 92.3 15.4% 97.5 29.7% 93.0 10.8% 115.7 20.5% 99.7 16.3% 100.0 27.5% 羟吗啡酮 0.989 89.4 2.5% 95.0 8.7% 96.3 8.3% 109.3 3.2% 100.5 11.1% 98.4 2.4% 94.5 9.7% 99.5 12.7% 97.3 17.1% 氢吗啡酮 0.996 97.2 1.2% 110.8 8.4% 114.4 14.2% 102.8 3.6% 98.1 9.1% 100.0 1.8% 98.8 6.4% 97.3 1.6% 98.5 4.9% 可待因-6-B-d-葡糖苷酸 0.99 94.6 2.3% 107.8 15.2% 106.3 0.9% 104.2 5.8% 96.4 4.5% 98.0 7.5% 95.4 6.0% 98.9 3.2% 98.4 0.3% 双氢可待因 0.997 97.6 1.7% 102.3 6.6% 105.1 6.6% 102.0 2.0% 97.3 2.6% 100.3 4.4% 95.9 4.1% 100.1 5.2% 99.3 5.4% 可待因 0.99 93.4 11.3% 109.7 2.9% 104.4 8.4% 108.2 10.3% 99.7 5.8% 97.3 5.1% 94.8 6.1% 97.1 3.6% 95.3 2.8% 羟考酮 0.993 98.6 8.2% 104.1 8.3% 98.0 11.6% 98.3 3.5% 99.4 4.1% 104.6 9.6% 97.0 0.7% 100.7 3.2% 99.3 8.6% 6-乙酰吗啡(6-AM) 0.99 98.4 10.6% 105.1 11.4% 95.8 5.4% 106.9 2.9% 90.6 2.5% 105.2 6.8% 98.1 8.8% 101.9 6.5% 112.6 25.2% O-去甲基曲马多 0.997 96.8 9.0% 104.3 5.0% 102.4 4.1% 104.4 2.1% 100.1 1.0% 101.9 2.1% 94.8 3.8% 99.2 3.5% 96.1 3.0% 氢可酮 0.995 95.1 0.4% 113.3 6.0% 103.6 3.7% 105.6 6.0% 100.4 2.1% 99.0 2.1% 96.7 4.8% 97.4 6.8% 95.3 3.7% 去甲丁丙诺啡-葡糖苷酸 0.992 94.6 13.4% 105.9 5.3% 105.8 5.4% 102.9 1.5% 108.0 6.6% 103.7 1.6% 93.8 5.0% 93.9 2.8% 91.5 1.4% 去甲芬太尼 0.995 95.6 4.1% 106.0 4.1% 102.9 6.4% 103.1 1.5% 102.5 3.0% 104.2 2.8% 95.8 4.3% 95.8 5.7% 94.1 3.4% 曲马多 0.996 95.9 1.6% 104.6 3.0% 103.5 0.8% 107.4 1.4% 101.6 1.1% 101.6 1.4% 95.7 2.1% 96.3 0.4% 93.4 1.8% 去甲哌替啶 0.996 97.0 3.6% 102.8 3.8% 102.7 3.4% 105.9 2.2% 101.7 1.9% 104.5 1.7% 97.5 3.1% 96.0 1.6% 91.9 5.2% 哌替啶 0.997 96.5 1.5% 105.7 6.0% 100.4 3.1% 104.8 1.6% 100.0 2.0% 100.9 2.9% 96.2 1.8% 98.8 1.8% 96.6 3.9% 丁丙诺啡-葡糖苷酸 0.991 93.3 13.3% 110.0 6.4% 103.4 8.7% 103.9 2.0% 105.8 5.1% 100.0 2.6% 97.4 5.2% 93.8 8.2% 92.4 1.7% 去甲丁丙诺啡 0.995 95.4 5.5% 104.8 1.4% 105.2 7.5% 105.2 3.9% 103.3 3.6% 102.5 2.7% 94.9 4.5% 94.7 3.8% 94.0 1.6% 芬太尼 0.997 97.2 0.4% 102.9 3.9% 101.9 4.8% 105.9 0.6% 102.6 1.0% 101.1 3.2% 96.0 3.5% 97.4 5.6% 95.1 1.6% 丁丙诺啡 0.994 97.2 8.6% 102.8 9.4% 102.0 8.8% 102.9 0.9% 105.6 4.9% 102.2 2.9% 100.1 5.6% 94.7 7.9% 92.3 1.0% EDDP+ 0.998 97.3 1.2% 103.5 4.3% 101.3 1.2% 104.2 0.8% 101.4 0.9% 100.8 1.7% 97.2 3.2% 98.3 1.1% 95.9 1.7% 丙氧芬 0.995 95.8 1.0% 105.3 3.0% 101.1 1.1% 105.9 1.7% 105.7 1.0% 102.2 3.1% 99.7 2.7% 94.8 0.8% 89.4 2.4% 美沙酮 0.997 98.8 0.9% 101.1 2.1% 98.5 3.4% 105.1 0.5% 103.1 2.5% 102.8 4.0% 101.0 3.0% 98.0 6.4% 91.6 1.2% CV%值大于10%或与期望值的差异大于15% 表3.简单稀释样品制备方法的阿片类药物校准曲线的准确度和变异系数(CV%)。芬太尼和去甲芬太尼的浓度为其它化合物浓度的/。 准确度和精度 观察两种方法的质控样品结果,发现二者的校准曲线线性相似。表4中数据显示,除浓度为7.5 ng/mL的吗啡之外,混合型SPE法制备的所有化合物在4个QC浓度下的CV%均小于10%,符合建议的精度要求。除极少数例外,几乎所有的准确度和精度值均小于10%。此外,只有3个QC点与预期值的偏差大于10%,其它均低于15%。相比之下,采用稀释方案进行样品制备的结果显示多种化合物的精度 (RSD%)不符合要求,尤其是在7.5 ng/mL的较低浓度时;而且多个值与其预期浓度的偏差均超过15%,尤其是在较低的QC浓度时,如表5所示。 7.5 75 250 400 平均值 CV% 偏差 平均值 CV% 偏差 平均值 CV% 偏差 平均值 CV% 偏差 吗啡-3-B-d-葡糖苷酸 7.10 8.3% -5.3% 74.5 5.2% -0.7% 250.0 2.2% 0.0% 386.3 3.6% -3.4% 羟吗啡酮-3-B-d-葡糖苷酸 7.43 9.7% -1.0% 76.9 3.0% 2.5% 239.9 4.9% -4.0% 372.1 3.7% -7.0% 氢吗啡酮-3-B-d-葡糖苷酸 7.98 7.8% 6.3% 76.4 5.8% 1.9% 252.4 2.9% 0.9% 398.1 3.7% -0.5% 吗啡-6-葡糖苷酸 8.30 8.7% 10.7% 74.9 6.7% -0.1% 240.9 5.1% -3.7% 376.8 4.0% -5.8% 吗啡 8.15 10.1% 8.7% 75.6 7.7% 0.8% 217.1 5.1% -13.2% 391.2 4.3% -2.2% 羟吗啡酮 7.85 5.1% 4.7% 73.3 4.2% -2.3% 243.6 4.7% -2.6% 385.5 4.5% -3.6% 氢吗啡酮 7.93 1.6% 5.7% 75.7 3.0% 0.9% 247.8 3.7% -0.9% 388.9 1.2% -2.8% 可待因-6-B-d-葡糖苷酸 7.78 4.0% 3.7% 73.6 3.8% -1.9% 257.3 5.0% 2.9% 421.7 2.6% 5.4% 双氢可待因 7.65 0.8% 2.0% 75.8 1.1% 1.1% 243.8 0.6% -2.5% 377.9 2.8% -5.5% 可待因 7.68 4.7% 2.3% 75.8 0.6% 1.1% 245.2 1.9% -1.9% 385.4 0.9% -3.7% 羟考酮 7.58 5.2% 1.0% 75.5 2.3% 0.7% 244.5 3.4% -2.2% 378.0 2.8% -5.5% 6-乙酰吗啡(6-AM) 7.70 5.3% 2.7% 76.2 4.3% 1.6% 245.9 2.3% -1.7% 391.5 0.7% -2.1% O-去甲基曲马多 7.83 1.9% 4.3% 75.0 1.3% 0.0% 247.1 0.7% -1.2% 384.6 0.7% -3.8% 氢可酮 7.60 1.9% 1.3% 74.5 1.3% -0.7% 244.2 1.6% -2.3% 381.3 0.9% -4.7% 去甲丁丙诺啡-葡糖苷酸 7.80 3.6% 4.0% 76.4 3.1% 1.8% 255.0 3.9% 2.0% 401.9 1.3% 0.5% 去甲芬太尼 1.90 0.0% 1.3% 19.4 2.3% 3.3% 62.7 1.2% 0.4% 101.7 2.2% 1.7% 曲马多 7.60 0.0% 1.3% 76.8 0.3% 2.4% 240.5 0.8% -3.8% 369.2 0.5% -7.7% 去甲哌替啶 7.48 2.0% -0.3% 75.3 1.6% 0.4% 238.7 1.2% -4.5% 371.4 1.4% -7.2% 哌替啶 7.43 0.7% -1.0% 73.2 0.5% -2.5% 242.4 2.4% -3.1% 388.1 1.7% -3.0% 丁丙诺啡-葡糖苷酸 8.08 2.7% 7.7% 77.8 1.8% 3.7% 267.0 1.6% 6.8% 441.1 1.3% 10.3% 去甲丁丙诺啡 7.73 1.2% 3.0% 77.7 3.8% 3.6% 246.1 1.5% -1.6% 377.2 1.0% -5.7% 芬太尼 1.90 0.0% 1.3% 19.2 1.1% 2.4% 60.8 1.0% -2.7% 96.8 1.0% -3.2% 丁丙诺啡 7.55 2.3% 0.7% 77.2 1.9% 2.9% 247.2 1.9% -1.1% 397.1 1.3% -0.7% EDDP+ 7.65 1.3% 2.0% 75.0 1.1% 0.0% 243.2 0.9% -2.7% 387.7 1.1% -3.1% 丙氧芬 7.55 0.8% 0.7% 78.4 0.5% 4.5% 243.4 0.9% -2.6% 378.9 1.9% -5.3% 美沙酮 7.58 0.7% 1.0% 78.2 1.5% 4.3% 246.4 1.0% -1.4% 386.4 1.2% -3.4% ■RSD%大于10%或偏差%大于15% 表4. Oasis MCX uElution板样品提取方法所得的阿片类化合物质量控制统计数据。表中列出了各个浓度下的平均值、CV%和偏差%(N=4)。 7.5 75 250 400 平均值 RSD% 偏差 平均值 RSD% 偏差 平均值 RSD% 偏差 平均值 RSD% 偏差 吗啡-3-B-d-葡糖苷酸 7.08 10.3% -5.7% 73.3 6.1% -2.3% 239.4 2.3% -4.2% 380.0 6.2% -5.0% 羟吗啡酮-3-B-d-葡糖苷酸 6.85 18.1% -8.7% 72.9 6.8% -2.8% 229.7 4.0% -8.1% 365.9 7.0% -8.5% 氢吗啡酮-3-B-d-葡糖苷酸 7.75 14.5% 3.3% 78.1 4.5% 4.1% 236.5 6.9% -5.4% 362.7 5.8% -9.3% 吗啡-6-葡糖苷酸 7.85 23.1% 4.7% 74.0 17.5% -1.4% 249.1 9.3% -0.4% 358.6 3.5% -10.4% 吗啡 5.28 26.9% -29.7% 76.0 7.9% 1.3% 267.4 9.4% 7.0% 410.7 16.6% 2.7% 羟吗啡酮 8.98 23.3% 19.7% 82.4 9.7% 9.9% 251.9 5.8% 0.7% 360.1 5.4% -10.0% 氢吗啡酮 8.13 14.1% 8.3% 79.3 5.0% 5.7% 251.8 5.1% 0.7% 381.1 3.4% -4.7% 可待因-6-β-d-葡糖苷酸 6.45 11.5% -14.0% 71.6 7.0% -4.5% 226.7 8.0% -9.3% 358.6 4.4% -10.4% 双氢可待因 8.25 9.4% 10.0% 86.1 8.0% 14.8% 244.8 5.6% -2.1% 387.3 5.3% -3.2% 可待因 7.90 10.5% 5.3% 76.5 4.7% 2.0% 236.2 8.0% -5.5% 366.0 3.9% -8.5% 羟考酮 7.53 20.4% 0.3% 79.2 6.8% 5.6% 243.0 3.4% -2.8% 380.3 3.4% -4.9% 6-乙酰吗啡(6-AM) 6.50 7.7% -13.3% 68.3 9.5% -8.9% 215.6 2.8% -13.8% 371.6 5.2% -7.1% O-去甲基曲马多 7.45 3.6% -0.7% 79.5 4.9% 5.9% 240.2 3.3% -3.9% 369.0 2.5% -7.8% 氢可酮 6.75 8.2% -10.0% 71.9 3.6% -4.2% 227.2 6.4% -9.1% 341.2 5.8% -14.7% 去甲丁丙诺啡-葡糖苷酸 7.25 5.3% -3.3% 77.1 2.7% 2.8% 234.5 5.0% -6.2% 350.2 3.0% -12.4% 去甲芬太尼 1.53 11.2% -18.7% 20.1 3.7% 6.9% 60.3 3.7% -3.6% 92.1 0.6% -7.9% 曲马多 6.53 1.5% -13.0% 69.8 3.6% -6.9% 218.1 1.3% -12.8% 335.5 0.8% -16.1% 去甲哌替啶 7.45 4.6% -0.7% 79.3 5.1% 5.7% 234.6 3.1% -6.2% 356.8 0.7% -10.8% 哌替啶 7.33 1.7% -2.3% 77.4 7.0% 3.2% 236.3 2.1% -5.5% 367.0 2.7% -8.2% 丁丙诺啡-葡糖苷酸 4.80 4.5% -36.0% 65.8 3.6% -12.3% 211.1 4.9% -15.6% 327.1 2.1% -18.2% 去甲丁丙诺啡 7.15 9.2% -4.7% 79.6 2.8% 6.2% 242.6 5.6% -3.0% 364.2 1.7% -9.0% 芬太尼 1.75 3.3% -6.7% 19.5 2.9% 3.9% 60.0 3.9% -4.1% 91.9 1.4% -8.2% 丁丙诺啡 6.80 6.4% -9.3% 75.5 3.8% 0.6% 231.1 3.7% -7.6% 356.6 2.3% -10.9% EDDP+ 7.45 1.7% -0.7% 78.3 3.3% 4.4% 239.2 1.0% -4.3% 365.2 2.1% -8.7% 丙氧芬 7.00 8.2% -6.7% 75.9 2.2% 1.2% 229.7 2.8% -8.1% 349.9 4.5% -12.5% 美沙酮 6.98 6.0% -7.0% 75.6 2.5% 0.7% 232.8 3.4% -6.9% 349.5 4.4% -12.6% ■RSD%大于10%或偏差%大于15% 表4.简单稀释样品制备方案所得的阿片类化合物的质量控制统计数据。表中列出了各个浓度下的平均值、CV%和偏差%(N=4)。 被测样品分析 为了测试该方法在实际情况中的适用性,我们采用当前方法对先前已检测并确证含阿片类化合物的32份尿液样品(2份阴性样品和30份阳性样品)进行了分析。先前,我们已对这些样品中的6-MAM(海洛因代谢物)、可待因、氢可酮、氢啡啡酮、吗啡、羟考酮和羟吗啡酮进行了分析。前后两次分析的不同之处在于将样品水解使结合态代谢物从葡糖苷酸中释放出来。图4中对采用当前方法所得的结果与其它实验室对样品中的羟考酮和氢可酮报告的分析结果进行了对比。这两种化合物均缺少3位和6位羟基,使其无法进行Ⅱ相葡糖苷酸化6.8,从而消除了由于水解不完全所致的数据偏差。对这两种方法进行比较时,两图均显示二者具有良好的相关性,氢可酮和羟考酮的R分别为0.956和0.985。并且,斜率接近于1(m=0.962),这表明采用两种方法所得的羟考酮结果具有良好的一致性。对于氢可酮,采用本文中的方法所得的结果在较高浓度时具有一定的偏差(m=0.689)。这可能是受两份浓度较高的样品的影响,采用当前方法所测得的浓度为6574和7032 ng/mL, 而之前报告的结果分别为3750和4610 ng/mL。分析时,我们将这些样品稀释为报告所述的5至500 ng/mL线性范围之内。而之前报告的结果是否将样品进行了适当的稀释还尚未可知。 图4.将先前分析的样品采用当前方法与另一种LC/MS/MS认证方法进行对比的结果。 当对样品中的化合物如吗啡、羟吗啡酮和氢吗啡酮进行分析时发现存在明显差异,这些化合物在被排出之前经过显著的葡糖苷酸化。用于分析阿片类药物的多种方法均依赖于酶水解。然而,水解程度不仅极大地依赖于所使用的β-葡糖醛酸糖苷酶(提取自帽贝、罗马蜗牛、大肠杆菌),还取决于底物(吗啡-6-葡糖苷酸与吗啡-3-葡糖苷酸,吗啡-3-葡糖苷酸与氢吗啡酮-3-葡糖苷酸)。当前方法和之前的报告方法对同组样品的分析结果表明,对酶水解的依赖会大大低估葡糖苷酸化代谢物的总量。我们对羟吗啡酮和氢吗啡酮的报告结果与使用当前方法(葡糖苷酸结合物+游离药物)实际测得的各个化合物的总量进行了回归分析,所得的斜率分别为0.20和0.25,这表明75%至80%的药物未发生水解。当前方法分析结果显示以葡糖苷酸结合物形式存在的羟吗啡酮和氢吗啡酮的总量大于85%。因此,低效的葡糖苷酸水解可能导致对化合物总体浓度的低估。而当前方法显然不会受此限制,因为该方法下可直接对葡糖苷酸代谢物进行测定。 本文介绍的方法展示了混合型uElution SPE结合UPLC/MS/MS在分析26种目标阿片类化合物及其代谢物中的优势。所有化合物的分析在5.5 min内完成,而且所有同量异位化合物对均达到完全分离。与简单稀释法相比, Oasis MCX uElution板的使用改善了线性并显著降低了基质效应。此外,采用混合型SPE法还显著提高了质量控制样品和校准标准品的准确度和精度。本方法下几乎所有分析物的LOQ都能达到5 ng/mL, 并且无需水解便能直接测定葡糖苷酸代谢物,因此非常适合于这类化合物的分析。 ( 参考文献 ) ( 1. Goldberger, B . A. and E.J. C o ne, Confirmatory tests fo r drugs in th e wo r kplace by gaschromatography-mass spectrometry. Journal of Chromatography A, 1994. 674(1-2): p.73-86. ) ( 2. G G i ustavsson, E . , et al., V alidation o f direct injection electrospray LC-MS/M S for confirmationof opiates i n urine drug testing. Journal of Mass Spectrometr y , 200 7 .42(7) : p.881-889. ) ( 3. M Murphy, C .M. a nd M .A. H uestis, LC-ESI-MS/MS analysis for the quantification of mor p hine, c odeine, m orp h ine-3-B-D-glucuronide,mo r phine-6-B-D-glucuronide, and codeine-6-B-D- g lucuronide inhuman urine. J ournal of Mass Spectrometry,2005.40(11): p. 1 41 2 -1416. ) ( 4. Edinboro, L.E., R.C. Backer, a nd A. Poklis, D irect A nalysis o f O p iates in Urine by LiquidChromatography-Tandem Mas s Spectrometry. Jour n al of Analytical Toxic o logy, 2005.29(7):p.704-710. ) ( 5. French, D., A . Wu, a n d K. Lynch, Hydrophilic int e raction LC- M S/MS analysis of opio i ds in u rine: significance of glucuronide metabolites. Bioanalysis,2011. 3(2 3):p.2603-2612. ) ( 6 . W ang, P., et al., Incomplete Recovery of Pre s cription Opi o ids in U r in e u s ing Enzym a ticHydrolysis o f Glucur o nide M etabolites. Journal o f Analytical T oxicology, 2006. 30(8): p.570-575. ) ( 7 . Watts,R., e t al., Simultaneous quantitative determination of opioid dependency treatmentdrugs i n human u rine using UPLC-MS/MS. Waters A p plication Note, 2 012. ) ( 8. . Smith,H.S., Opioid M etabolism. Mayo Clinic proceedings. Mayo Clinic, 2009.84(7): p.613-624. ) ( 以上信息仅用于科学研究,不能用于临床诊断。 ) THE SCIENCE OF WHAT'S POSSIBLE. 北京:010-52093866 上海:021-61562666 成都:028-65545999 免费售后服务热线:800(400) 820 2676www.waters.com 使用混合型pElution SPE结合UPLC/MS/MS对尿液中的阿片类药物及其代谢物进行法医毒理学直接分析
确定



还剩9页未读,是否继续阅读?
沃特世科技(上海)有限公司(Waters)为您提供《尿液中阿片类药物及其代谢物检测方案 》,该方案主要用于尿液中阿片类药物及其代谢物检测,参考标准--,《尿液中阿片类药物及其代谢物检测方案 》用到的仪器有ACQUITY UPLC 超高效液相色谱
推荐专场
相关方案
更多
该厂商其他方案
更多
















