方案详情
文
利用LC-MS/MS方法分析生物基质中的药物和药物化合物时,通常需要使用手动前处理方式进行样品制备。在本研究中,我们报告了一种全自动前处理系统,可直接与LC-MS/MS联用进行苯丙胺、可卡因和鸦片制剂的测定。
该方法中包含42种目标化合物和20种氘代内标物。样品前处理是通过直接与LC-MS/MS系统(Nexera X2反相LC分离和LCMS-8060,Shimadzu)连接的可编程液体处理器(CLAM-2000,Shimadzu)进行的。在正离子化模式下进行采集,每种化合物使用高达15个多反应监测(MRM)通道,每个MRM通道均有优化的碰撞能量(MRM扫描模式),从而在定量之外实现定性库检索。
已成功设计该方法为平行样品制备和分析提供支持,因此大幅提高了样品处理通量,缩短了周期时间。
方案详情

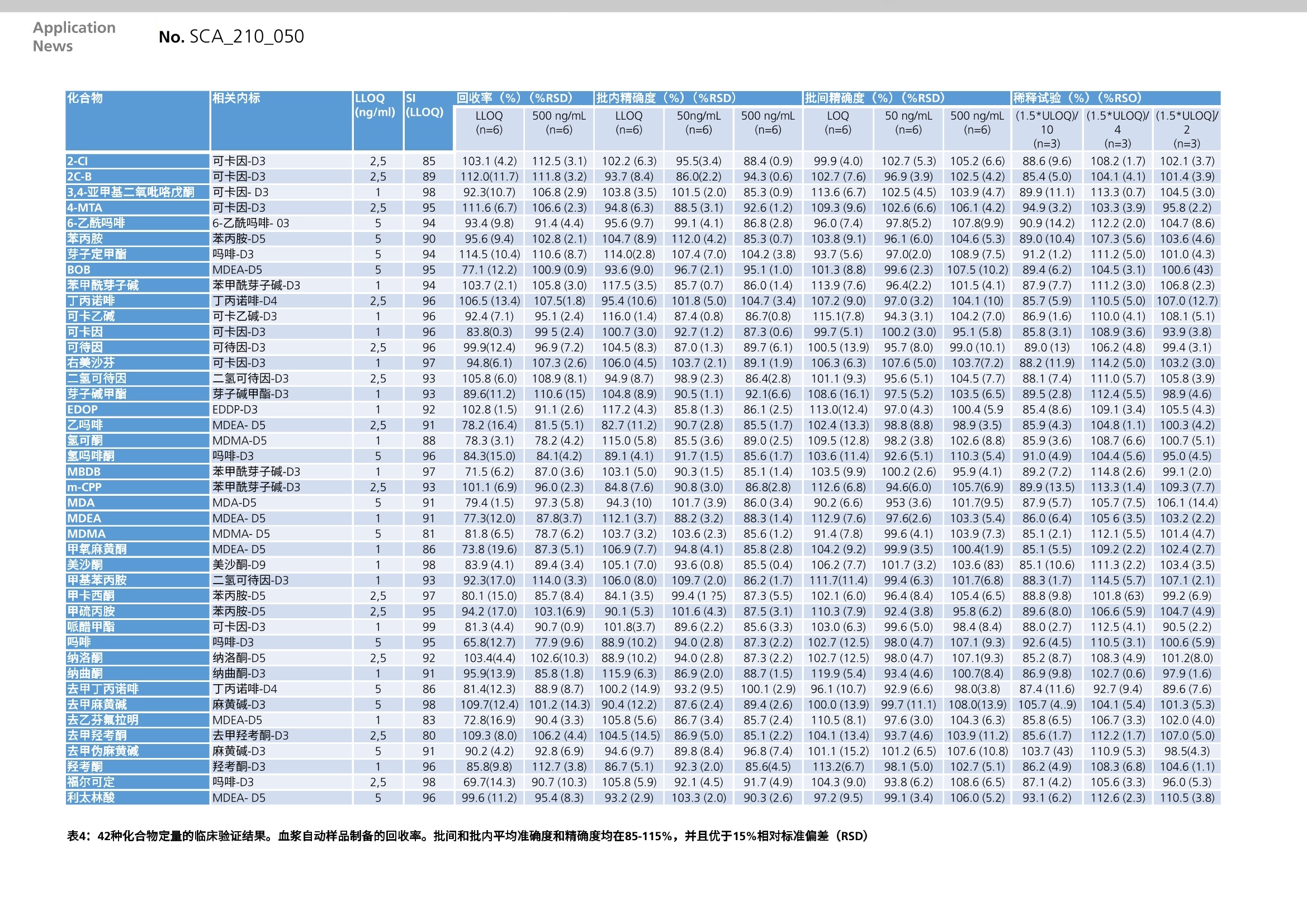
EuropeanInnovation Center Application No.SCA 210_050News 岛津SHIMADZLhttp://www.shimadzu.com.cn用户服务热线电话: 800-810-0439第一版发行日:2017年12月400-650-0439 ApplicationNews 液相色谱质谱法 全自动样品前处理系统和液相色谱串联质谱联用技术在滥用药物检测中的应用 Tiphaine Robin (), Alan Barnes 2), Sylvain Dulaurent ("), Neil Loftus 2),Sigrid Baumgarten (, Stephane Moreau (3),Pierre Marquet, Souleiman El Balkhi(), Franck Saint-Marcoux) 法国利摩日大学医院药理毒理学系 No.SCA 210_050 岛津公司,英国曼彻斯特(3)岛津欧洲有限公司,德国杜伊斯堡 利用LC-MS/MS方法分析生物基质中的药物和药物化合物时,通常需要使用手动前处理方式进行样品制备。在本研究中,我们报告了一种全自动前处理系统,可直接与LC-MS/MS联用进行苯丙胺、可卡因和鸦片制剂的测定。 该方法中包含42种目标化合物和20种氘代内标物。样品前处理是通过直接与LC-MS/MS系统( Nexera X2反相LC分离 和LCMS-8060 ,Shimadzu) 连接的可编程液体处理器(CLAM-2000, Shimadzu) 进行的。在正离子化模式下进行采集,每种化合物使用高达15个多反应监测(MRM)通道,每个MRM通道均有优化的碰撞能量(MRM扫描模式),从而在定量之外实现定性库检索。 已成功设计该方法为平行样品制备和分析提供支持,因此大幅提高了样品处理通量,缩短了周期时间。 图1:样品分析周期 鸦片制剂、苯丙胺(包括类似物)和可卡因是广泛使用的滥用药物(DOA)。许多实验室已开发出LC-MS/MS方法用于鉴定和定量这些化合物[1-51。临床和法医毒理学(怀疑药物过量、监控吸毒者、毒驾和兴奋剂检查)中的许多应用均需使用这些检测方法。 为了在不影响准确度、精确度和检测限的情况下最大程度地减少假阳性或假阴性结果,开发方法时结合了MRM检测的灵敏度和MRM扫描模式的鉴定能力。该方法可以监测每种化合物多达15个MRM通道,实现准确且精确的定量,以及库可检索化合物的鉴定。每个MRM通道均优化了离子的碰撞能量。利用每个MRM通道的离子强度构建MRM扫描谱图,从而与已记录的库MRM扫描谱进行检索匹配。 为了开发临床毒理学分析中使用的自动通用样品制备方法,将自动样品前处理系统(CLAM-2000)连接到LC-MS/MS系统 (LCMS-8060)。将样品试管放到自动系统后,无需人工干预,样品被自动输送到含过滤膜的处理管中,然后向处理管中加入试剂,混合,然后过滤。最后,将提取物进样到LC-MS/MS系统中。 从精密度、重复性、基质效应、提取率、基质间一致性、稀释试验和稳健性方面对该程序进行了全面验证。 为了检测可行性,将该方法用于病人的全血或血浆样品分析,并与已经过验证的LC-MS/MS方法 (每个目标化合物的2个MRM通道)进行比较[51. ■ 实验 样品自动输送到含过滤膜的处理管中,然后向处理管中加入试剂,混合,然后过滤。 向含PTFE过滤膜的处理管(0.45 um孔径,预先用20 uL甲醇活化平衡)准确地加入100 uL乙腈。然后加入50 uL血浆(或全血)和10uL内标溶液 (0.2 mg/L, 溶剂为乙腈),将混合物震荡120秒(1900rpm),然后施加真空压力(-60到-65kPa)1120秒将其过滤到收集管中。 最后,将3uL提取物进样到LC-MS-MS系统中。 使用1msec的驻留时间和3到10 msec的延迟时间,通过分段采集的MRM模式测定所有化合物,每个化合物有多达15个MRM通道。所有通道均通过流动注射方法获得优化的碰撞能量。使用色谱峰顶点强度提取离子强度,从而构建MRM扫描模式。 液相色谱 UHPLC Nexera LC系统 分析色谱柱 Restek Raptor Biphenyl (2.7 um 100x2.1mm) 柱温 40C 流速 0.3 mL/min 流动相A 2 mmol/L甲酸铵和0.002%甲酸 流动相B 含有2 mmol/L甲酸铵和0.002%甲酸的甲醇 梯度洗脱 时间(分钟) %B 1.0 10 2.0 40 10.5 100 13.5 100 13.51 10 17.0 结束 色谱柱调节 11-16.2min 0.5 mL/min 进样量 3 uL 表1:液相色谱采集参数 LC-MS/MS 质谱 MRM扫描模式(用于生成检索库波谱) 化合物的目标数量 42(包括20种ISTD) 延迟时间/驻留时间 1 msec./3至10 msec. 离子化模式 ESI+/- 极性切换时间 5 msec 接口温度 300°℃ 加热模块温度 400°C DL温度 250°C 雾化气 3 L/min 加热气 10 L/min 干燥气 10 L/min 利摩日大学医院的药理学-毒理学实验室致力于获得国际标准组织 (ISO) 15189标准(认证编号:8-2607)的认证。这些要求用于本方法。 开展稳健性研究来评估由标准曲线提供的可接受定量准确度。在4周内,使用新鲜制备的校准标准品来定量新鲜制备的质控准品(5和50 ng/mL)。首先使用和质控样同一天制备的校准标准品数据来处理质控样数据,然后使用最多4周内的校准标准品数据对质控样数据进行重新处理。 结果 自动化样品前处理耗时8分钟,然后DOA色谱分离耗时约9分钟(色谱柱清洗和平衡另耗时9分钟),保留时间从芽子碱甲酯的0.97分钟到美沙酮的7.9分钟。总共需要大约26分钟获得首个结果,然后平行开展提取和分离,系统每18分钟生成一个结果。表3中总结了MRM通道采集的优化结果。。-一种目标化合物获得高达15个MRM通道。 表4中总结了验证研究的结果。获得了所有探讨参数的验收标准。关于批内和批间(n=6)的精确度和准确度,CV值小于15%(苯甲酰芽子碱、可卡乙碱、EDDP和纳曲酮除外,这四种化合物的LLOQ报告值小于20%)。使用含1/x或1/x²加归回归的二次模型,所有化合物标准曲线(从LLOQ到500 ng/mL)的相关系数均高于0.99。根据每个化合物需求, LLOD和LLOQ设置为1、2.5或5ng/mL。在本报告的实验条件下无基质效应现象(n=6)。稀释试验(n=3)也报告获得了良好的结果。用最多一个月前获得的标准曲线对质控品(5和50ng/mL) 进行定量,产生的准确度变化范围在70和130%之间。5 ng/mL和50 ng/ml质控品的最大CV值分别为13.0%和14.9%。使用一个月后采集的标准曲线对质控品进行定量,也获得了较好的准确度。5 ng/ml和 50ng/ml质控品的最大CV值分别为13.4%和14.2%。 图2说明了2种同分异构体化合物的方法。 表3:采集42种化合物及其20种内标化合物所运用MRM扫描模式的MRM通道参数、保留时间和MRM通道总数。使用定量离子和参比离子(20%离子比率允许误差范围)测量定量数据。库识别还使用了其它MRM通道。 表4:42种化合物定量的临床验证结果。血浆自动样品制备的回收率。批间和批内平均准确度和精确度均在85-115%,并且优于15%相对标准偏差 (RSD) 化合物 化合物 可待因 可待因MRM扫描库RT:[3.701] (+) SI:98 氢可酮MRM扫描库RT:[4.001]](+) SI: 94 图2:运用CLAM-2000提取方法从血浆样品提取的可待因和氢可酮的MRM扫描模式MS/MS数据。通过将获得的MRM扫描数据与使用认证材料生成的参考库进行匹配,可以确定血浆样品中的同重元素化合物,例如可待因和氢可酮。 图3:提取自血浆样品的可待因和氢可酮的标准曲线数准(校准范围:1-500 ug/L)。 整个程序在实际患者中的应用 为了考察全自动样品前处理和LC-MS/MS联用方法的准确性,将运用"CLAM-LCMS-8060"方法检测的43个患者样品(血浆或全血)的定量结果与LCMS-8050系统(使用实验室中经常使用的QuEChERS盐提取方法进行手动样品前处理,该方法已验证)所定量的结果进行对比, 51."CLAM-LCMS-8060"方法通过MRM扫描模式检测,而LCMS-8050系统使用常规MRM方法检测样品。患者血液或血浆样品通过实验室的常规程序获得,例如常规药物检测、DUID (药毒驾)或紧急药物过量。 图4显示在这些化合物的定量方面具有总体一致性。 图4:回归分析:比较两种方法检测43例患者血液或血浆样品的结果,分别为使用LCMS-8060 MRM扫描模式(带库检索功能)获得的结果和常规LCMS-8050 MRM方法获得的结果。 红结论 我们报告了首个全自动LC-MS/MS分析方法用于定性和定量分析血液中DOA,其中还使用MRM扫描模式进行了库搜索。 分析程序全部或部分采用自动化技术,消除了手动样品前处理造成的人为误差,并节省了实验室的操作时间,在系统自动执行分析的同时,技术人员可执行其它手动任务。 我们开发出一种方法:将样品管放到系统上后无需人工干预。样品制备与LC-MS/MS系统同步,因此不浪费任何时间。 我们使用光谱采集方法,该方法包含被测目标物所有的特色MRM通道。在之前公布的其它方法中,使用产物离子扫描法对所有分子施加两个或三个碰撞能量。我们对每个化合物最多15个通道的碰撞能量均进行了优化。通过这种方法可以获得非常具体而丰富的质谱信息。另外,不使用阈值触发,因此在整个计划采集期间对所有MRM进行了测量。因此,即使在极低的信号强度下,也可生成MRM扫描图。相比标准2-3MRM通道方法,使用极快的延迟时间和驻留时间,测量其它MRM通道的负担不会改变灵敏度,并且经验证42个分子全部符合ISO 15189验证的要求。我们针对42 DOA的分析验证了该方法的特异性、灵敏度和稳健性。我们用患者的一组样品比较了该方法与实验室所认证方法的性能。通过校准曲线重复分析对系统稳定性和稳健性进行研究,结果表明具有良好的重现性。出于质控目的,向未知样品中添加气代内标,使用最多一个月前的校准曲线来定量未知样品,我们估计可以达到低于20%的不确定度。在急诊患者样品分析的情况下,以这样的速度将未知样品的浓度定量达到该准确度水平,意味着可能在限定的时间范围内施行急救治疗,而使用常规的样品处理和分析通常无法做到这一点。 ( m 参考文献 ) 1. Cailleux A, Le Bouil A, Auger B, BonsergentG,Turcant A. Allain P.Determination ot升opiates and cocaine and its metabolites innbiological fluids by high-performance liquidchromatography with electrospray tandemmass spectrometry. J Anal Toxicol. 1999;23:620-4. 2. Moeller MR, Steinmeyer S, Kraemerr T.Determination of drugs of abuse in blood. JChromatogr BRinmedSci Appl.1998;713:91-109. 3. Saussereau E, LacroixC, Gaulier JM, Goulle JP.On-line liquid chromatography/tandem massspectrometry simultaneous determination ofopiates, cocainics and amphetamines in driedblood spots. Chromatogr B.2012:885-886:17. 4. Anzilillotltoitti L, OdoardiS,s. Strano-RossiS.Cleaning up blood samples using a modified“QuEChERS" procedure for the determinationof drugs of abuse and benzodiazepines byUPLC-MSMS. Forensic Sci Int. 2014;243:99-106. 5..Duaurent, S., El Balkhi, S., Poncelet,L.Gaulier, J.M., Marquet, P., Saint-Marcoux, F.(2016) QuEChERS sample preparation prior toLC-MS/MS determination Cofopiates,amphetamines, and cocaine metabolites inwhole blood, Analytical and BioanalyticalChemistry, 408(5), 1467-1474. 6. Sauvage, F.L., Gaulier, J.M., Lacha tre, G.,Marquet, P (2008) Pitfalls sa nadnd PreventionStrategies; forr LiquidChromatography-Tandem Mass Spectrometry in the SelectedReaction-Monitoring Mode for Drug Analysis,Clinical Chemistry,54:9, 1519-1527 ( 岛津企业管理(中国)有限公司岛津 ( 香港)有限公司 ) ( 免责声明: ) *本资料未经许可不得擅自修改、转载、销售; ( *本资料中的所有信息 仅 供参考,不予任何保证。 ) ( 如有变动,恕不另行通知。 ) 使用手动前处理方式进行样品制备。在本研究中,我们报告了一种全自动前处理系统,可直接与LC-MS/MS联用进行苯丙胺、可卡因和鸦片制剂的测定。该方法中包含42种目标化合物和20种氘代内标物。样品前处理是通过直接与LC-MS/MS系统(Nexera X2反相LC分离和LCMS-8060,Shimadzu)连接的可编程液体处理器(CLAM-2000,Shimadzu)进行的。在正离子化模式下进行采集,每种化合物使用高达15个多反应监测(MRM)通道,每个MRM通道均有优化的碰撞能量(MRM扫描模式),从而在定量之外实现定性库检索。已成功设计该方法为平行样品制备和分析提供支持,因此大幅提高了样品处理通量,缩短了周期时间。
确定






还剩5页未读,是否继续阅读?
岛津企业管理(中国)有限公司为您提供《全血、血浆中滥用药物检测方案(液质联用仪)》,该方案主要用于全血/血清/血浆中生化检验检测,参考标准--,《全血、血浆中滥用药物检测方案(液质联用仪)》用到的仪器有岛津LCMS-8060超快速三重四极液质联用仪
推荐专场
相关方案
更多
该厂商其他方案
更多
















