方案详情
文
本文介绍了一种使用Oasis PRiME HLB μElution固相萃取(SPE)板的优化方法,评估了该方法相较于Oasis HLB SPE和蛋白质沉淀法的LysoPCs去除性能。
方案详情

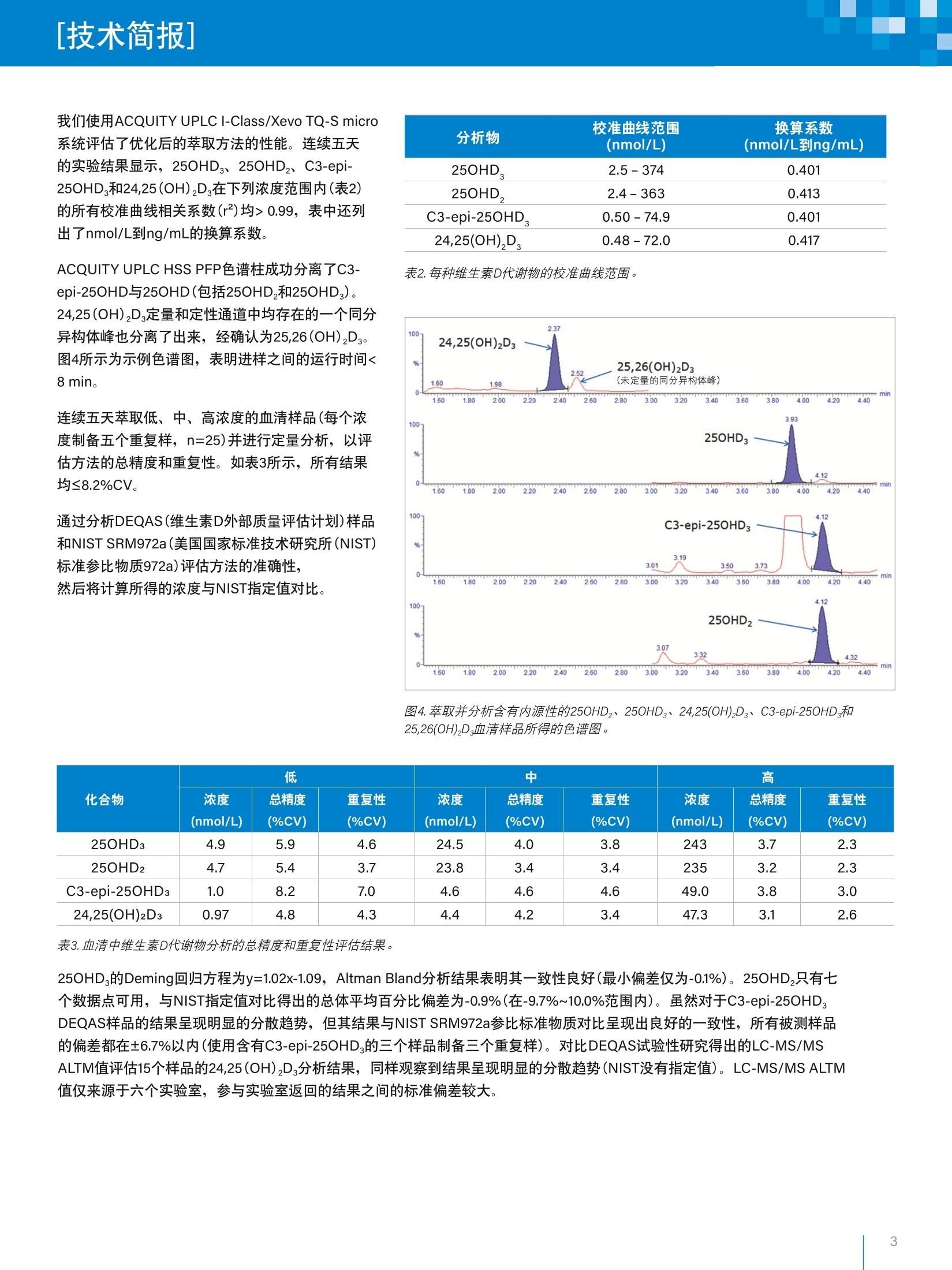
[技术简报]WatersTHE SCIENCE OF WHAT'S POSSIBLE. [技术简报] Robert Wardle和Lisa Calton 沃特世公司(英国威姆斯洛) 目的 开发一种用于分析25-羟基维生素D(250HD)、25-羟基维生素D2(25OHD,)、24,25-二羟基维生素D:(24,25(OH)2D)和C3-epi-25-羟基维生素D:(C3-epi-250HD)的LC-MS/MS方法。本方法采用Xevo°TQ-S micro质谱仪进行检测,并使用Waters°Oasis° PRiMEHLB最大限度减少磷脂干扰物和提高分析灵敏度。 背景 使用LC-MS/MS测定血清中的维生素D代谢物含量时,基质干扰物质会带来挑战。其中,疏水性与25-羟基维生素D(25OHD)相似的溶血磷脂胆碱(LysoPCs 16:0、18:1和18:0)尤为棘手,已有研究表明,在质谱分析过程中,这类物质会产生离子抑制。尽管LysoPCs的结构各不相同,但研究表明它们很难通过样品制备过程去除,也很难与维生素D代谢物实现色谱分离。 图1. Oasis PRiME HLB uElution固相萃取(SPE)板。 解决方案 本文介绍了一种使用Oasis PRiME HLB uElution固目萃取(SPE)板(图1)的优化方法,评估了该方法相较于Oasis HLB SPE和蛋白质沉淀法的LysoPCs去除性能。本研究使用Waters ACQUITY UPLCHSS PFP色谱柱分离三种样品萃取方法所得萃取物中的250HD2、25OHD3、24,25(OH)2D和C3-epi-25OHDs,并将峰面积与萃取物中目标LysoPCs(16:0、18:1和18:0,母离子为m/z 496、m/z 522和m/z 524, 子离子为m/z184)的峰面积进行了对比。使用WatersACQUITY UPLC I-Class (FTN)/Xevo TQ-S micro系统评估了优化后的萃取方法的性能。 将稳定的标记内标加入100pL校准品、QC样品和测试样品中,使用甲醇/硫酸锌(水溶液)进行蛋白质沉淀。 离心之后,将上清液转移到Oasis PRiME HLBpElution板孔内。使不同浓度的乙腈(水溶液)(0-100%)通过SPE吸附剂以洗脱分析物,使用每种浓度的洗脱溶液制备三个重复样,然后分析所得洗脱液,得到洗脱曲线。 使用配备2.1x100 mm ACQUITY UPLC HSS PFP色谱柱的ACQUITY UPLC I-Class系统,以水、甲醇、醋酸铵和甲酸为流动相,梯度分离经过稀释的洗脱液,并在Xevo TQD上采用表1所列的MRM通道和母离子扫描参数进行检测。 实验结果 将三个重复样中每种目标维生素D代谢物和LysoPCs的平均峰面积绘制成散点图,得到其洗脱曲线(图2)。 通过洗脱曲线可以看出, LysoPCs开始从OasisPRiME HLB吸附剂中洗脱出来时的有机溶剂浓度与维生素D代谢物开始洗脱出来时的有机溶剂浓度接近,这是因为它们的疏水性相似。但是,当乙腈(水溶液)的浓度>90%时, 几乎所有LysoPCs都保留在了Oasis PRiME HLB SPE吸附剂上,而维生素D代谢物成功洗脱。因此,优化方法选择以25%乙腈(水溶液)作为清洗溶液,以100%乙腈作为洗脱溶液。 我们对比了优化Oasis PRiME HLB方法、使用甲醇/硫酸锌(水溶液)的简单蛋白质沉淀萃取法,以及使用甲醇作为洗脱溶剂的优化Oasis HLB方法这三种方法得到的LysoPCs和维生素D代谢物平均峰面积。结果汇总于图3. 与使用甲醇的Oasis HLB方法和蛋白质沉淀法相比,使用乙腈的Oasis PRiME HLB方法去除了99%以上的目标LysoPCs。因此,使用该方法得到的维生素D代谢物峰面积比Oasis HLB方法增加了5倍,比蛋白质沉淀方案增加了10倍。 分析物 通道 锥孔电压 碰撞能量 (m/z) (V) (eV) 250HD,和 401.3>159.1(定量离子) 24 24 C3-epi-25OHD, 401.3>365.3(定性离子) 24 10 [H]-25OHD, 和 [H]-C3-epi-25OHD, 404.3>162.1(内标) 24 24 25OHD. 413.3>355.3(定量离子) 24 10 413.3>83.1(定性离子) 24 24 [H]-25OHD, 416.3>358.3(内标) 24 10 417.3>159.1(定量离子) 20 24 24,25(OH),D, 417.3>381.3(定性离子) 20 10 [H]-24,25(OH),D, 423.3>159.1(内标) 20 24 LysoPCs m/z 184的母离子 20 20 表1.MRM通道和母离子扫描参数 图2.使不同浓度的乙腈(0-100%)通过Oasis PRiME HLB SPE板洗脱维生素D代谢物和LysoPCs所得的洗脱曲线。 维生素D代谢物和LysoPCs-方法对比 图3.采用蛋白质沉淀法(PPT)、Oasis HLB (HLB MeOH)以及Oasis PRiME HLB (PRiME MeCN)方法制备的样品中,维生素D代谢物和LysoPCs的峰面积对比。 我们使用ACQUITY UPLCI-Class/Xevo TQ-S micro系统评估了优化后的萃取方法的性能。连续五天的实验结果显示, 25OHD3、25OHD2、C3-epi-250HD,和24,25(OH)D在下列浓度范围内(表2)的所有校准曲线相关系数(r²)均>0.99,表中还列出了nmol/L到ng/mL的换算系数。 ACQUITY UPLC HSS PFP色谱柱成功分离了C3- epi-250HD与25OHD(包括250HD,和250HD,)。24,25(OH)D定量和定性通道中均存在的一个同分异构体峰也分离了出来,经确认为25,26(OH),D。图4所示为示例色谱图,表明进样之间的运行时间< 8 min。 连续五天萃取低、中、高浓度的血清样品(每个浓度制备五个重复样, n=25)并进行定量分析,以评估方法的总精度和重复性。如表3所示,所有结果均≤8.2%CV。 通过分析DEQAS(维生素D外部质量评估计划)样品和NIST SRM972a(美国国家标准技术研究所(NIST)标准参比物质972a)评估方法的准确性, 然后将计算所得的浓度与NIST指定值对比。 分析物 校准曲线范围 换算系数 (nmol/L) (nmol/L到ng/mL) 250HD, 2.5-374 0.401 250HD. 2.4-363 0.413 C3-epi-25OHD, 0.50-74.9 0.401 24,25(OH),D, 0.48-72.0 0.417 表2.每种维生素D代谢物的校准曲线范围。 图4.萃取并分析含有内源性的250HD2、250HD,、24,25(0H)D3、C3-epi-250HD和25,26(OH),D,血清样品所得的色谱图。 化合物 低 中 高 浓度 (nmol/L) 总精度 重复性 浓度 总精度 重复性 浓度 (nmol/L) 总精度 重复性 (%CV) (%CV) (%CV) (%CV) (%CV) (%CV) (nmol/L) 25OHD3 4.9 5.9 4.6 24.5 4.0 3.8 243 3.7 2.3 250HD2 4.7 5.4 3.7 23.8 3.4 3.4 235 3.2 2.3 C3-epi-25OHD3 1.0 8.2 7.0 4.6 4.6 4.6 49.0 3.8 3.0 24,25(OH)2D3 0.97 4.8 4.3 4.4 4.2 3.4 47.3 3.1 2.6 表3.血清中维生素D代谢物分析的总精度和重复性评估结果。 250HD,的Deming回归方程为y=1.02x-1.09, Altman Bland分析结果表明其一致性良好(最小偏差仅为-0.1%)。250HD,只有七个数据点可用, 与NIST指定值对比得出的总体平均百分比偏差为-0.9%(在-9.7%~10.0%范围内)。虽然对于C3-epi-25OHD,DEQAS样品的结果呈现明显的分散趋势,但其结果与NIST SRM972a参比标准物质对比呈现出良好的一致性,所有被测样品的偏差都在±6.7%以内(使用含有C3-epi-25OHD,的三个样品制备三个重复样)。对比DEQAS试验性研究得出的LC-MS/MSALTM值评估15个样品的24,25(OH)D分析结果,同样观察到结果呈现明显的分散趋势(NIST没有指定值)。 LC-MS/MS ALTM值仅来源于六个实验室,参与实验室返回的结果之间的标准偏差较大。 分三天在经过处理的血清样品中加标低、中、高浓度的分析物并进行样品萃取(每个浓度制备10个重复样, n=30),根据分析结果评估分析灵敏度。加标浓度为1 nmol/L时的25OHD,和250HD,分析结果,以及加标浓度为0.5 nmol/L时的24,25(OH)2D和C3-epi-250HD分析结果均达到了<20%CV的精度,且信噪比S:N(ptp)>10:1。 总结 本研究为血清中25OHD3、25OHD2、C3-epi-25OHD和24,25(OH)2D3的LC-MS/MS分析成功开发出了一种临床研究方法。研究证明, Oasis PRiME HLB可去除磷脂的优势对于维生素D代谢物分析很有帮助,其具有以下优势: 使用精简的萃取工作流程去除血清样品中的磷脂 所有分析物在所有测试浓度水平均表现出优异的精度(≤8.2%CV) 将25OHD结果与DEQAS NIST指定值比较,观察到良好的一致性 有效提高了25OHD,、25OHD、C3-epi-25OHD,和24,25(OH)D的分析灵敏度提高,无需衍生化 仅供研究使用。不适用于诊断。 扫一扫,关注沃特世微信 ( 沃特斯中国有限公司 沃特世科技(上海)有限公司 ) THE SCIENCE OF WHAT'S POSSIBLE. 上海:021-61562666 Waters、The Science of What’s Possible、ACQUITY UPLC、Xevo和Oasis是沃特世公司的注册商标。其它所有商标均归各自的拥有者所有。 香港:852-29641800 免费售后服务热线:800(400)820 2676www.waters.com 本文介绍了一种使用Oasis PRiME HLB μElution固相萃取(SPE)板的优化方法,评估了该方法相较于Oasis HLB SPE和蛋白质沉淀法的LysoPCs去除性能。
确定



还剩2页未读,是否继续阅读?
沃特世科技(上海)有限公司(Waters)为您提供《血清中维生素D代谢物检测方案(固相萃取)》,该方案主要用于全血/血清/血浆中维生素D代谢物检测,参考标准--,《血清中维生素D代谢物检测方案(固相萃取)》用到的仪器有
相关方案
更多
该厂商其他方案
更多









