方案详情
文
利用nSMOL前处理试剂盒能够实现单抗药物Fab区域的选择性酶解,极大降低了酶解产物的复杂性,本方法无需经过固相萃取净化过程,采用LCMS-8060实现血浆中英利昔单抗高灵敏度分析,方法在7分钟内完成样品分析,具有分析速度快、通用性好的优势。
方案详情

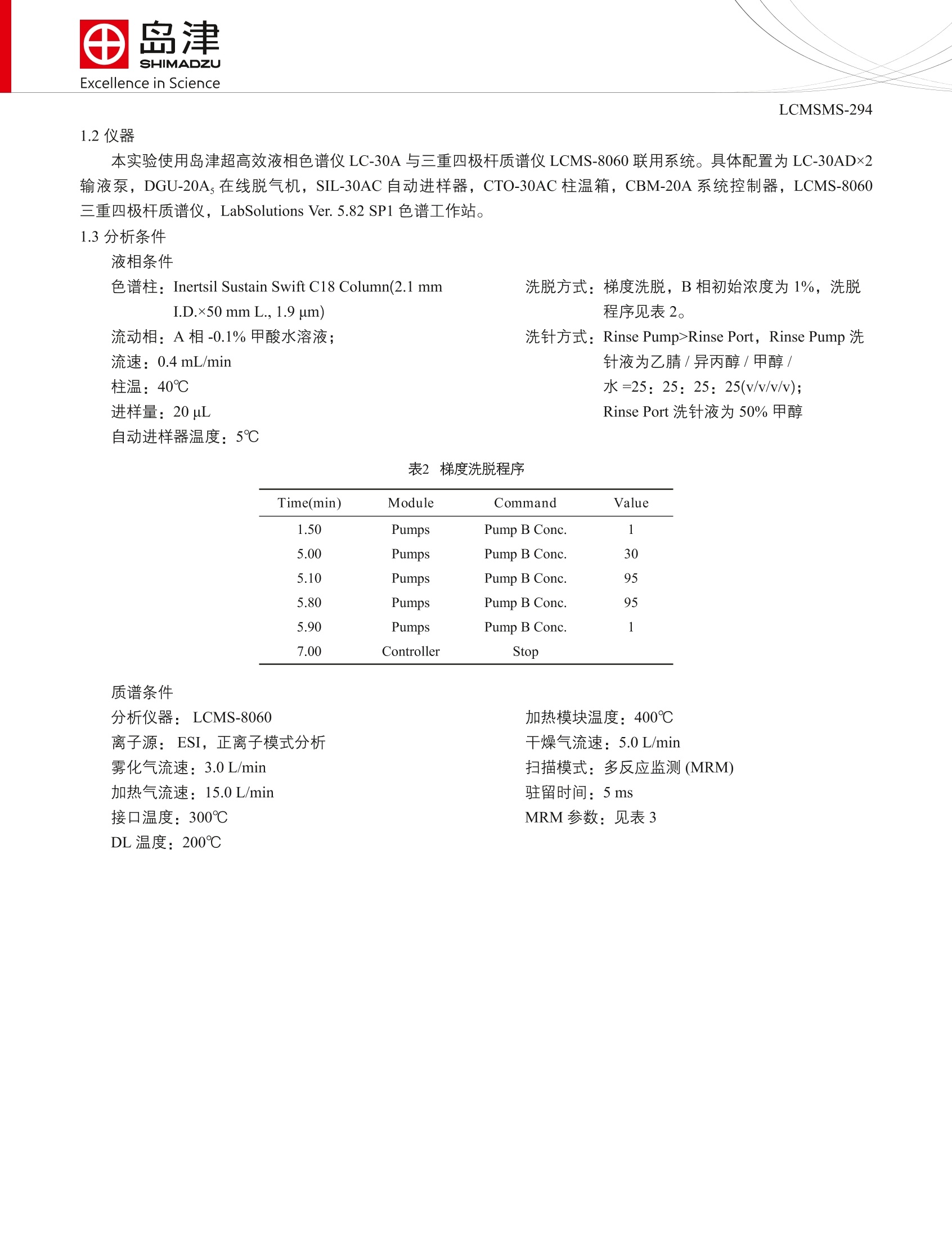
SSL-CA14-509Excellence in Science Excellence in ScienceLCMSMS-294 岛津全球应用技术开发支持中心上海市徐汇区宜州路180号华鑫天地二期C801栋 咨询电话:021-34193996http://www.shimadzu.com.cn nSMOL 技术结合UHPLC-MS/MS定量分析血浆中单抗类药物英利昔 LCMSMS-294 摘要:本文建立了一种使用 nSMOL 技术结合岛津LCMS-8060 测定复杂生物基质中单抗类药物英利昔的定量方法。 以英利昔的特征肽段 SINSATHYAESVK 作为定量肽段; STAYLQMNSLR 和 VLIYFTSSLHSGVPSR 作为定性肽段。方法特异性考察结果表明所选择的三个特征肽段均具有良好的选择性。在0.02~50 ug/mL 范围内 SINSATHYAESVK具有良好的线性关系,相关系数0.9960,方法定量限为 0.02 ug/mL,6次重复分析 RSD 为 6.40%。另外,三个浓度水平质控样品的精密度和准确度结果均满足方法验证的要求。利用 nSMOL 前处理试剂盒能够实现单抗药物 Fab 区域的选择性酶解,极大降低了酶解产物的复杂性,本方法无需经过固相萃取净化过程,即可采用LC-MS/MS 方法在7分钟内完成样品分析,具有分析速度快、通用性好的优势。 关键词: nSMOL 超高效液相色谱三重四极杆质谱血浆单抗类药物英利昔 英利昔单抗是一种人-鼠嵌合型单克隆抗体,,可以抑制肿瘤坏死因子 TNF-o和可溶性受体及膜型受体的结合,使TNF-0失去活性,临床可用于治疗 TNF-a 参与的多种疾病,目前被广泛应用于风湿、类风湿性关节炎和强直性脊柱炎等自身免疫性疾病。英利昔单抗是强生旗下抗风湿类的重磅药物,商品名为“Remicade”,,属于已上市单抗药物中销售额排名前5位的品种。近年来英利昔单抗相关生物类似药的研究如火如荼,不仅需要关注抗体药物药学性质,单抗药代\药动相关研究也具有重要意义,其中复杂生物基质中抗体药物的定量分析发挥重要作用。 在体内抗体药物定量研究中,配体结合实验 (LBA)是最为传统和广泛使用的方法。但是 LBA 方法需要针对抗体药物开发特异性抗原,方法开发周期非常漫长,方法可移植性差,不同抗体或结构类似的抗体均需要重新进行方法开发。 基于质谱法的蛋白定量因其方法开发过程简便周期 实验部分 短且方法通用性好,在抗体药物临床前及临床研究中受到越来越多的关注。在LC-MS/MS 法分析生物样品中单抗药物浓度的方法开发过程中,首先需要挑选出抗体药物的特征性肽段,通过特征肽段的浓度分析来表征整体抗体药物的含量。受生物基质复杂性的影响,样品需要经过胰酶酶解、净化等过程再进行上机分析。为简化复杂生物基质中抗体药物的定量分析工作,岛津的研发团队利用抗体药物的特殊结构对前处理过程进行了独特的设计,提出了 nSMOL 前处理试剂包,该方法能够有效富集血浆/血清中的抗体药物,实现 Fab区域的选择性酶解,提高酶解效率,同时极大降低了酶解产物的复杂性,对于复杂生物基质中抗体药物的准确定量提供了非常便利的工具。 本文基于岛津LCMS-8060液质联用系统,采用nSMOL 作为前处理方法完成英利昔单抗富集和选择性酶解,以特征肽段作为定量和定性的依据,完成血浆中英利昔单抗定量分析方法验证。 表1化合物信息 名称 英文名 CAS No. 分子式 平均分子量 英利昔单抗 Infliximab 170277-31-3 C6428H9912N1694O1987S46 144190.3 Da 1.2仪器 本实验使用岛津超高效液相色谱仪 LC-30A 与三重四极杆质谱仪 LCMS-8060 联用系统。具体配置为 LC-30ADx2输液泵, DGU-20A,在线脱气机, SIL-30AC 自动进样器, CTO-30AC柱温箱, CBM-20A 系统控制器, LCMS-8060三重四极杆质谱仪, LabSolutions Ver. 5.82 SP1 色谱工作站。 1.3分析条件 液相条件 色谱柱: Inertsil Sustain Swift C18 Column(2.1 mmI.D.x50 mm L.,1.9 um) 洗脱方式:梯度洗脱,B相初始浓度为1%,洗脱程序见表2。 流动相:A相-0.1%甲酸水溶液; 洗针方式: Rinse Pump>Rinse Port, Rinse Pump 洗 流速:0.4mL/min 针液为乙腈/异丙醇/甲醇/ 柱温:40℃ 水=25:25:25:25(v/v/v/v); 进样量:20uL Rinse Port 洗针液为50%甲醇 自动进样器温度:5℃ 表2梯度洗脱程序 Time(min) Module Command Value 1.50 Pumps Pump B Conc. 5.00 Pumps Pump B Conc. 30 5.10 Pumps Pump B Conc. 95 5.80 Pumps Pump B Conc. 95 5.90 Pumps Pump B Conc. 7.00 Controller Stop 质谱条件 分析仪器::LCMS-8060离子源:ESI, 正离子模式分析雾化气流速:3.0L/min加热气流速::15.0 L/min接口温度:300℃DL 温度:200℃ 加热模块温度:400℃ 干燥气流速:5.0L/min 扫描模式:多反应监测 (MRM) 驻留时间: 5 ms MRM参数:见表3 表3:3MRM参数 肽段选择 前体离子 产物离子 Q1 Pre CE Q3 Pre 肽段 Bias (V) )(V) Bias (V) 作用 SINSATHYAESVK 603.80**[y11] -19.0 -15.0 -22.0 469.55 546.75*[y10] -19.0 -17.0 -20.0 定量 [M+3H]3+ 503.25**[y9] -19.0 -18.0 -26.0 肽段 467.75*[y8] -19.0 -28.0 -26.0 YASESMSGIPSR 359.20*[y3] -20.0 -21.0 -25.0 642.80 616.35*[y6] -20.0 -25.0 -24.0 定性 [M+2H]2+ 834.40*[y8] -20.0 -25.0 -32.0 肽段 529.30*[y5] -20.0 -25.0 -23.0 ASQFVGSSIHWYQQR 631.30**[y10] -20.0 -18.0 -24.0 598.65 459.20**[y6] -20.0 -23.0 -20.0 定性 [M+3H]3+ 680.85**[y11] -20.0 -19.0 -26.0 肽段 780.40*[y5] -20.0 -27.0 -30.0 注:*表示定量离子 1.4样品前处理 配制英利昔单抗血浆基质标准曲线:浓度分别为0.02、0.05、0.10、0.20、0.50、1.00、2.00、5.00、20.0、50.0ug/mL,质控样品:浓度分别为0.06、4.00、40.0 ug/mL, 按照 nSMOL 试剂盒步骤进行样品前处理,获得的酶解混合物直接上机分析。 结果与讨论 2.1特征肽段确证及分析条件优化 基于之前的应用研究,利用 Skyline 软件构建 LC-MS/MS 方法,根据蛋白定量特异性原则进一步优化挑选出质谱响应较高的肽段,最终选择 SINSATHYAESVK、YASESMSGIPSR、ASQFVGSSIHWYQQR 作为特征肽段进行定量和定性分析,利用 LCMS-8060 的 MRM自动优化功能对特征肽段对应的 MRM 通道进行进一步优化,获得最佳的Q1 Bias、CE 和 Q3 Bias 表,结果见表3。血浆中英利昔单抗通过 nSMOL 试剂盒的特异性酶解,获得以上特征肽段,典型色谱图如图1所示。通过优化分离条件和质谱条件,提高目标肽段的灵敏度,最终结果表明在0.02~50 ug/mL 范围内 SINSATHYAESVK 具有良好的线性关系,标准曲线见图2a; 0.10~50 ug/mL 范围内 YASESMSGIPSR、ASQFVGSSIHWYQQR 具有良好的线性关系,标准曲线见图2b和图2c。以上实验结果证明通过 Skyline 筛选出英利昔相关特征肽段在生物基质中进一步验证满足特异性要求,其中 SINSATHYAESVK 灵敏度较高且选择性好,作为定量肽段; STAYLQMNSLR 和 VLIYFTSSLHSGVPSR 可作为定性肽段。 图1120 ug/mL血浆基质加标样品的英利单单抗典型色谱图 面积 面积 图2英利昔单抗特征肽段相关标准曲线 2.2方法选择性 考察空白血浆基质和0.02 ug/mL 英利昔血浆基质加标样品,结果如图3、4所示,空白血浆中定量肽段SINSATHYAESVK 的 MRM 通道 469.55>603.80 的干扰峰面积为0.02 ug/mL 英利昔血浆基质加标样品峰面积的13.5%,满足定量要求。 图3|30.02pg/mL英利昔血浆基质加标样品的MRM色谱图 图4 空白血浆样品的MRM色谱图 2.3线性范围和最低定量限 按照1.3所述制备浓度分别为0.02、0.05、0.10、0.20、0.50、1.00、2.00、5.00、20.0、50.0ug/mL 的标准样品,和浓度分别为0.06、4.00、40.0 ug/mL的质控样品。按照 nSMOL 试剂盒的前处理条件处理样品,采用1.4中的仪器条件进行测定,外标法定量。线性方程及相关系数见表4,其中y值代表特征肽段定量 MRM 通道色谱峰面积,x值代表血浆中英利昔浓度。方法定量限为0.02 ug/mL, 在此浓度水平,精密度和准确度均在接受标准内,6次重复测试RSD 为 6.40%, 准确度为 80.9~114.6%, S/N 平均值为156.7。 表4校准曲线参数(线性回归,权重为1/C²) 特征肽段 校准曲线 线性范围 准确度(%) 相关系数r (ug/mL) SINSATHYAESVK Y=(75575.8)X+(1976.67) 0.02~50 86.2~114.1 0.9960 YASESMSGIPSR Y=(33624.7)X+(3243.93) 0.10~50 90.1~109.0 0.9981 ASQFVGSSIHWYQQR Y=(34461.2)X+(2364.31) 0.10~50 91.7~110.0 0.9982 2.4方法精密度和准确度考察 考察三个浓度水平质控样品的精密度,结果如表5所示。各浓度水平质控样品的精密度范围为3.62~6.96%,准确度范围为86.1~114.0%。 表5方法精密度和准确度结果(n=6) 理论浓度 (ug/mL) 平均测定浓度 精密度 CV% 准确度范围% (ug/mL) 0.06 0.062 6.96 86.7~114.0 4 3.75 4.52 86.1~97.5 40 42.6 3.62 100.8~107.9 2.5 Carryover 考察 考察系统残留的影响,完成浓度最高点分析后,其后分析空白溶剂中特征肽段的峰面积,色谱图见图5,空白样品中特征肽段 SINSATHYAESVK、YASESMSGIPSR 的通道中均没有明显的目标肽段色谱峰,ASQFVGSSIHWYQQR存在一定残留,残留色谱峰面积为最低浓度 0.1 ug/mL 血浆中英利昔单抗面积的16.9%,因此分析方法所选3个目标肽段的残留量均满足样品分析要求。 结论 本文基于岛津 LCMS-8060 液质联用系统,采用 nSMOL 作为前处理方法完成单抗药物英利昔富集和选择性酶解,以特征肽段 SINSATHYAESVK 作为定量肽段; STAYLQMNSLR 和 VLIYFTSSLHSGVPSR 作为定性肽段。方法特异性考察结果表明空白血浆中定量肽段 SINSATHYAESVK 的 MRM 通道 469.55>603.80存在干扰峰面积为定量限色谱峰面积的13.5%,满足定量要求。在 0.02~50 ug/mL 范围内 SINSATHYAESVK 具有良好的线性关系,相关系数0.9960, 各浓度准确度范围86.2~114.1%。方法定量限为0.02 ug/mL, 6次重复分析 RSD 为 6.40%,准确度范围为80.9~114.6%。三个浓度水平质控样品的精密度范围为3.62~6.96%,准确度范围为 86.1~114.0%。高浓度样品分析后考察空白样品中的残留,结果表明在0.02~50 ug /mL线性范围内目标肽段残留量满足要求。本方法利用 nSMOL前处理试剂盒的优势,采用LC-MS/MS 技术实现复杂生物基质中单抗药物的准确定量分析,具有良好的通用性,可以用于英利昔单抗及其生物类似药的药代/药动学研究。 本文建立了一种使用nSMOL技术结合岛津LCMS-8060测定复杂生物基质中单抗类药物英利昔的定量方法。以英利昔的特征肽段SINSATHYAESVK作为定量肽段;STAYLQMNSLR和VLIYFTSSLHSGVPSR作为定性肽段。方法特异性考察结果表明所选择的三个特征肽段均具有良好的选择性。在0.02~50 μg/mL范围内SINSATHYAESVK具有良好的线性关系,相关系数0.9960,方法定量限为0.02 μg/mL,6次重复分析RSD为6.40%。另外,三个浓度水平质控样品的精密度和准确度结果均满足方法验证的要求。
确定




还剩4页未读,是否继续阅读?
岛津企业管理(中国)有限公司为您提供《血浆中英利昔单抗检测方案(液质联用仪)》,该方案主要用于全血/血清/血浆中生化检验检测,参考标准--,《血浆中英利昔单抗检测方案(液质联用仪)》用到的仪器有岛津LCMS-8060超快速三重四极液质联用仪
推荐专场
相关方案
更多
该厂商其他方案
更多
















