方案详情
文
Oasis MCX 96孔板提供了一种用于去除血浆样品中高浓度PEG的简便、快捷、高效的方法,从而消除早期药代动力学研究中常见的基质效应(通常是离子抑制效应)。此外,该解决方案无需进行色谱分析方法的再开发、样品的稀释、及其他费时费力的流程即可成功解决上述问题,这使得整个解决方案广泛适用于高通量分析的应用
方案详情

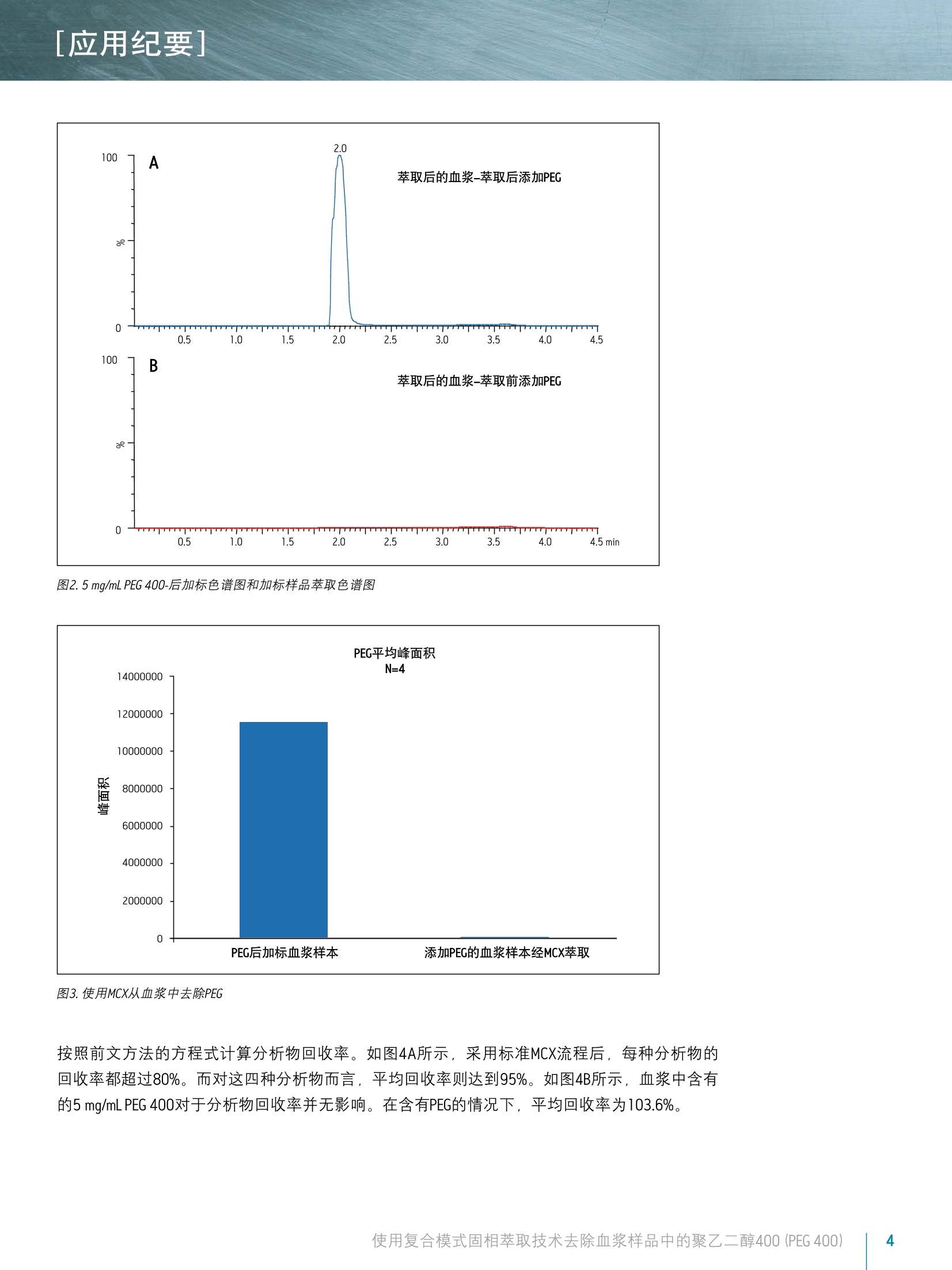
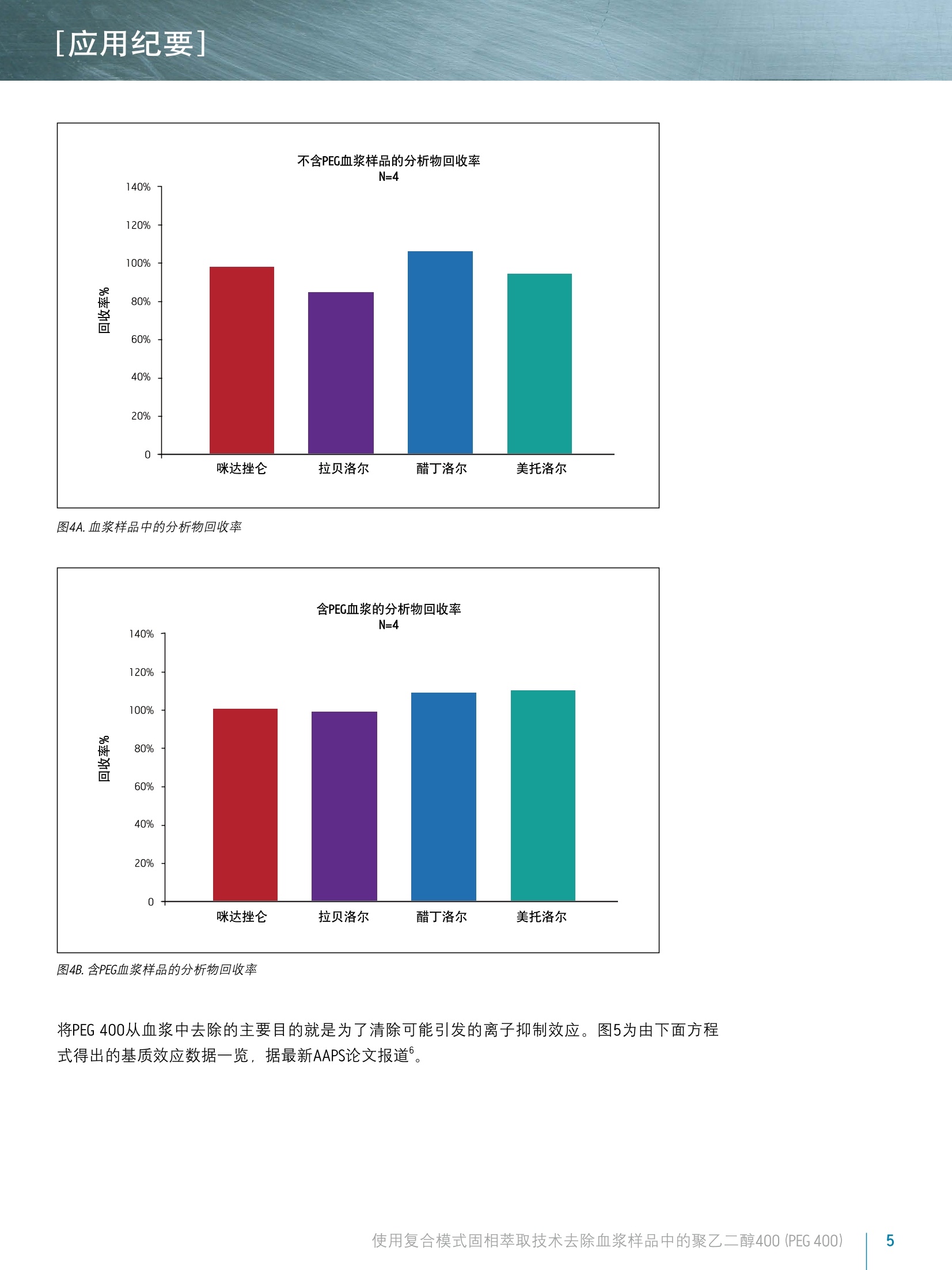
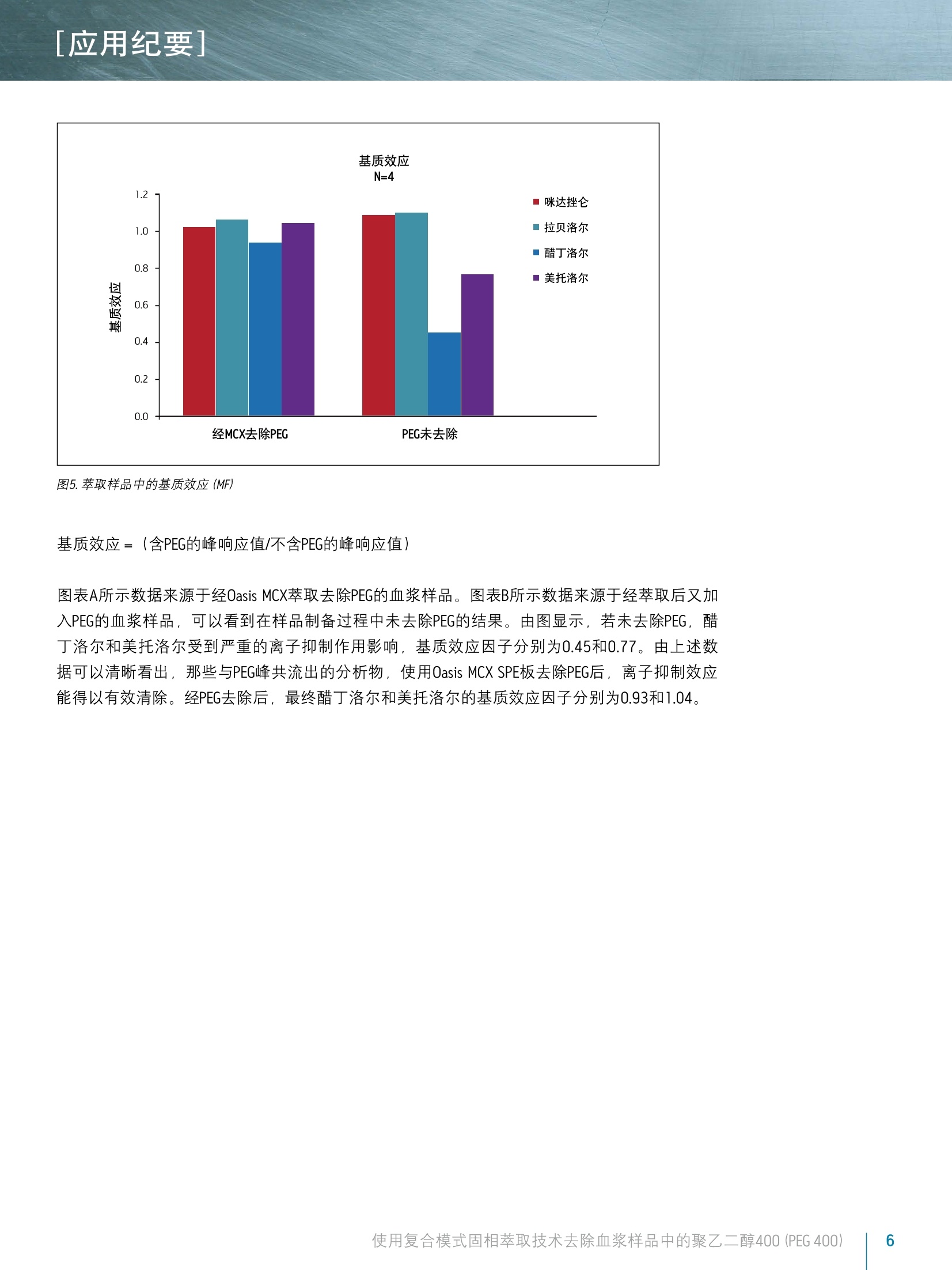
[应用纪要]THE SCIENCE OF WHAT'S POSSIBLE. [应用纪要] ■ ■ Waters 使用复合模式固相萃取技术去除血浆样品中的聚乙二醇400 (PEG 400) Jonathan P. Danaceau,Erin Chambers, and Kenneth J. Fountain 沃特世公司,美国马萨诸塞州米尔福德 应用优势 去除血浆中的PEG400 去除PEG400的离子抑制作用 ■只需快速、简单的样品前处理方法即可实现净化目的 OasisMCX96孔板ACQUITY UPLCBEHC柱 关键词 引言 PEG 400等药物赋形剂通常被加入到制剂中以促进其在介质中溶解。然而,这些化合物却可引发显著的基质效应,尤其是在LC/MS/MS分析中产生的离子抑制效应。常规药物研发流程中使用用快速LC梯度方法,容易导致此类化合物和目标分析物的共流出。由于这种共流出物已被证实是导致离子抑制效应的主要原因,因此在早期药代动力学(PK)研究中,赋形剂浓度偏高可能会带来棘手的问题。为尽量减少这一问题引发的不良影响,目前已研究出的方法包括:LC梯度调节23,分析色谱柱的选择,样品制备策略的方法开发3,样品稀释,甚至是全新制剂药的开发。即便其中部分方法已取得成效,他们也存在各自的局限性。很显然,分析员通常无法自己选择制剂药赋形剂。无论是改变梯度或流动相,还是色谱柱的选择,LC条件的优化都能够针对部分分析物解决这一问题,但它既无法应用到全部分析物,也需要更多的方法开发作为辅助支持。同时,对LC运行条件的过多优化并不利于高通量分析。有研究人员指出,若能开发出一种更优化的固相萃取 (SPE)方法,便可实现有效的净化效果。“3 针对以上问题,本应用纪要通过使用Oasis复合模式阳离子交换 (MCX)SPE方法提供了一种可以快速、便捷、高效的解决方案。碱性分析物通过强阳离子交换作用被吸附在填料中,而如PEG等非离子型的赋形剂则通过反相机理被吸附,同时能够在分析物洗脱之前被选择性去除。 沃特世解决方案 赋形剂去除, PEG去除, SPE, LC/MS, ESI,离子抑制,基质效应 实验 样品制备 标准品包含:醋丁洛尔、美托洛尔、拉贝洛尔、咪达挫伦。这些成分分别加入到空白血浆中、调整其浓度至200 ng/mL, 或是后加标到萃取后的空白血浆洗脱液中,用于回收率的计算。PEG400也是分别加入到空白血浆中调整其浓度到到5 mg/mL或者后加标到萃取后的空白血浆洗脱液中用于确定回收率。 样品按照OasisMCX的标准操作流程进行萃取。简单来说,在0.5mL兔血浆中加入0.5 mL4%HPO进行酸化。(注意:本研究中采用的是0.5mL血浆,采用更小剂量亦可)。MCX96孔板在经过1.0mL MeOH和1.0mL H,0活化平衡之后,经酸化的样品被上样到填料中.上样后,使用1.0mL2%甲酸和2×1.0 mL MeOH清洗。样品使用2×250pL含5% NHOH的MeOH溶液进行洗脱。“后加标”((FPS)样品是在空白兔血浆洗脱液中加入标准品或标准品与PEG 400的混合物。经萃取的样品则以以下方式制备:在未经萃取的血浆中加入200 ng/mL标准品、或在其基础上再加入5mg/mLPEG 400。 PEG去除的回收率依据以下算式得出: %回收率=(萃取样品峰面积/后加标样品峰面积)×100% 为进行PEG去除的相关分析,样品按照1:200的比例在流动相中进行稀释,以避免高浓度PEG400给质谱仪带来的污染。 方法条件 SPE条件 SPE板: Oasis MCX 96孔板30 pm(30 mg),部件编号:186000248 液相色谱条件 液相色谱系统: 沃特世ACQUITY UPLC系统 检测: 沃特世ACQUITY SQD 样品瓶: 2 mL 96孔收集板;部件号 WAT058958 色谱柱: ACQUITY UPLC BEH C1 1.7 pm, 2.1x50 mm, 部件号::186002350 柱温: 30℃ 样品温度: 10℃ 进样量: 10p 流速: 0.5 mL/min. 流动相A(MPA): 0.1%HCOOH水 流动相B(MPB): 0.1% HCOOH乙青 初始流动相条件为95:5 MPA:MPB。持续0.5分钟, MPB在2.5分钟之后增至90%。MPB比例随后降回5%,并持续2分钟,重新平衡色谱柱。总运行时间5.0分钟。 质谱条件 质谱系统: 沃特世ACQUITY SQD 电离模式: (+)ESI 采集范围: SIR 毛细管电压: 2.5 kV 锥孔电压: 根据化合物有所区别(针对不同分析物进行优化) 脱溶剂气体: 700 L/min 锥孔气: 0L/min 数据管理 色谱系统: MassLynx V4.1 SCN714和MS软件 结果与讨论 PEG 400及其他四种测试化合物的色谱图如图1所示。图中宽峰是PEG 400丰度较大的分子离子峰的综合TIC,包括以下分子量的PEG单峰:370、414、458、502、546、590和634。标准品(醋丁洛尔、美托洛尔、拉贝洛尔、咪达挫仑)可通过MH+离子的SIR显示,除咪达挫仑,它的MH+离子与(MH-35)*离子合并成一个峰。值得注意的是,醋丁洛尔和美托洛尔均与PEG发生共流出,因而二者更容易受到血浆样品中残留PEG产生的离子抑制的影响。图2为PEG的两个色谱图。A图显示未经过SPE处理的血浆样品中PEG含量情况。它是将PEG后加标至萃取的最终血浆洗脱液中得到的。B图则为含有5 mg/mL PEG的血浆样品经标准MCX流程萃取得到的,该图表明血浆样品中几乎全部PEG 400都得以去除。图3显示为实验所用样品组的平均PEG峰面积,如图所示,采用MCX萃取,超过99%的PEG 400得以去除。 图1.PEG400及标准品色谱图 [应用纪要] 图2.5 mg/mL PEG 400-后加标色谱图和加标样品萃取色谱图 图3.使用MCX从血浆中去除PEG 按照前文方法的方程式计算分析物回收率。如图4A所示,采用标准MCX流程后,每种分析物的回收率都超过80%。而对这四种分析物而言,平均回收率则达到95%。如图4B所示,血浆中含有的5 mg/mL PEG 400对于分析物回收率并无影响。在含有PEG的情况下,平均回收率为103.6%。 [应用纪要] 图4A.血浆样品中的分析物回收率 图4B.含PEG血浆样品的分析物回收率 将PEG 400从血浆中去除的主要目的就是为了清除可能引发的离子抑制效应。图5为由下面方程式得出的基质效应数据一览,据最新AAPS论文报道。 [应用纪要] 图5.萃取样品中的基质效应(MF) 基质效应=(含PEG的峰响应值/不含PEG的峰响应值) 图表A所示数据来源于经Oasis MCX萃取去除PEG的血浆样品。图表B所示数据来源于经萃取后又加入PEG的血浆样品,可以看到在样品制备过程中未去除PEG的结果。由图显示,若未去除PEG,醋丁洛尔和美托洛尔受到严重的离子抑制作用影响,基质效应因子分别为0.45和0.77。由上述数据可以清晰看出,那些与PEG峰共流出的分析物,使用Oasis MCX SPE板去除PEG后,离子抑制效应能得以有效清除。经PEG去除后,最终醋丁洛尔和美托洛尔的基质效应因子分别为0.93和1.04。 Oasis MCX 96孔板提供了一种用于去除血浆样品中高浓度PEG的简便、快捷、高效的方法,从而消除早期药代动力学研究中常见的基质效应(通常是离子抑制效应)/o。此外,该解决方案无需进行色谱分析方法的再开发、样品的稀释、及其他费时费力的流程即可成功解决上述问题,这使得整个解决方案广泛适用于高通量分析的应用。 ( 参考文献 ) ( 1 . T ong X , Wang J, Zheng S, Pivnichny J, G riffin P, Shen X, Donnelly M, V akerich K, Nunes C, and Fenyk-Melody J. Effect of signal interference f rom dosing e xcipients on pharmacokinetic screening of drugcandidates by liquid chromatography/mass spectrometry. Anal Chem 2002 74:6305-6313. ) ( 2.W e aver R and Ril e y R. I de n tification an d reduction of ion suppressioneffects on pharmacokinetic parameters b y polyethylene glycol 400. Rapid Comm Mass Spec2006 2 0:2559-2564. ) ( 3 . S hou W and Na i dong W. P os t -column infu s ion stude of the ‘do s ingvehicle effect’ in the liquid chromatography/tandem massspectrometric analysis of discovery p h armacokinetic samples. Rap i d Comm. Mass Spec 2003 17:589-597. ) ( 4. .T T emesi D , Law B, and Howe N . Synthesis and evaluation o f PEG414,a n ovel f ormulating a g ent that a v oids analytical problems as s ociated w ith p olydispersive v ehicles such as PEG400. J . Pharmaceutical Sciences 2003 92(12):2512-2518. ) 5. Larger P, Breda M, Fraier D, Hughes H, and James C. lon-suppressioneffects in liquid chromatography-tandem mass spectrometry due toa formulation agent, a case study in drug discovery bioanalysis. J.Pharm. Biomed. Anal. 2005 39:206-216. 6. Bansal S and DeStefano A. Key elements of bioanalytical methoddevelopment validation for small molecules. The AAPS Journal 20079(1):E109-E114. 沃特斯中国有限公司沃特世科技(上海)有限公司 北京:010-52093866 上海:021-6156 2666 广州:020-2829 6555 成戈:028-65545999 香港:852-29641800 免费售后服务热线:800(400)820 2676Wwww.waters.com 使用复合模式固相萃取技术去除血浆样品中的聚乙醇(PEG
确定




还剩5页未读,是否继续阅读?
沃特世科技(上海)有限公司(Waters)为您提供《使用复合模式固相萃取法去除血浆样品中的聚乙二醇400(PEG 400)》,该方案主要用于全血/血清/血浆中--检测,参考标准--,《使用复合模式固相萃取法去除血浆样品中的聚乙二醇400(PEG 400)》用到的仪器有二维ACQUITY UPLC系统
推荐专场
相关方案
更多
该厂商其他方案
更多
















