方案详情
文
xCELLigence RTCA 不仅可以评估针对多种血液瘤的免疫疗法的效价,还可以在生理相关效靶比下检测血液瘤细胞的破坏动力学。与传统检测方法相比,此方案的工作量更少。将血液瘤靶细胞接种并粘附在经预包被的 E-Plate 中,然后加入效应细胞,并在几天内非侵入性地检测癌细胞破坏动力学。自动连续采集数据。阻抗数据的定量和实时特征使得能够轻松比较不同免疫疗法和不同剂量之间的效价。使用这种表面粘附方法,多种效应细胞(PBMC、NK、CAR-T,以及双特异性 T 细胞 (BiTEs) 等生物分子)靶向肿瘤细胞表达的 EpCAM 蛋白,并阻断针对免疫检查点抑制剂 PD-1 的抗体(Cerignoli 等,2018)。xCELLigence 平台非常适合血液瘤的效价评估,能够为开发的免疫肿瘤疗法提供高重现性的定量评估以及简单的工作流程。
方案详情

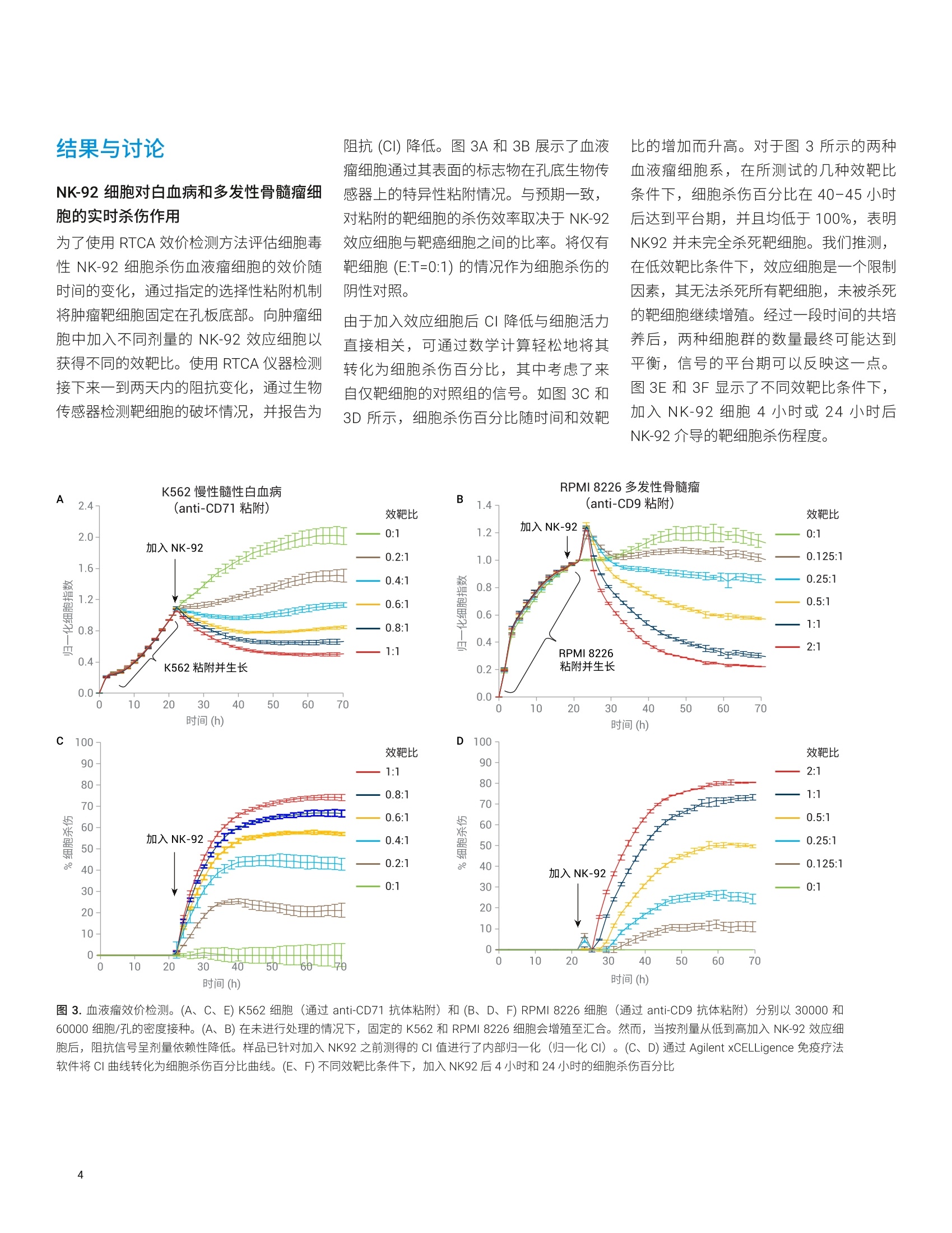
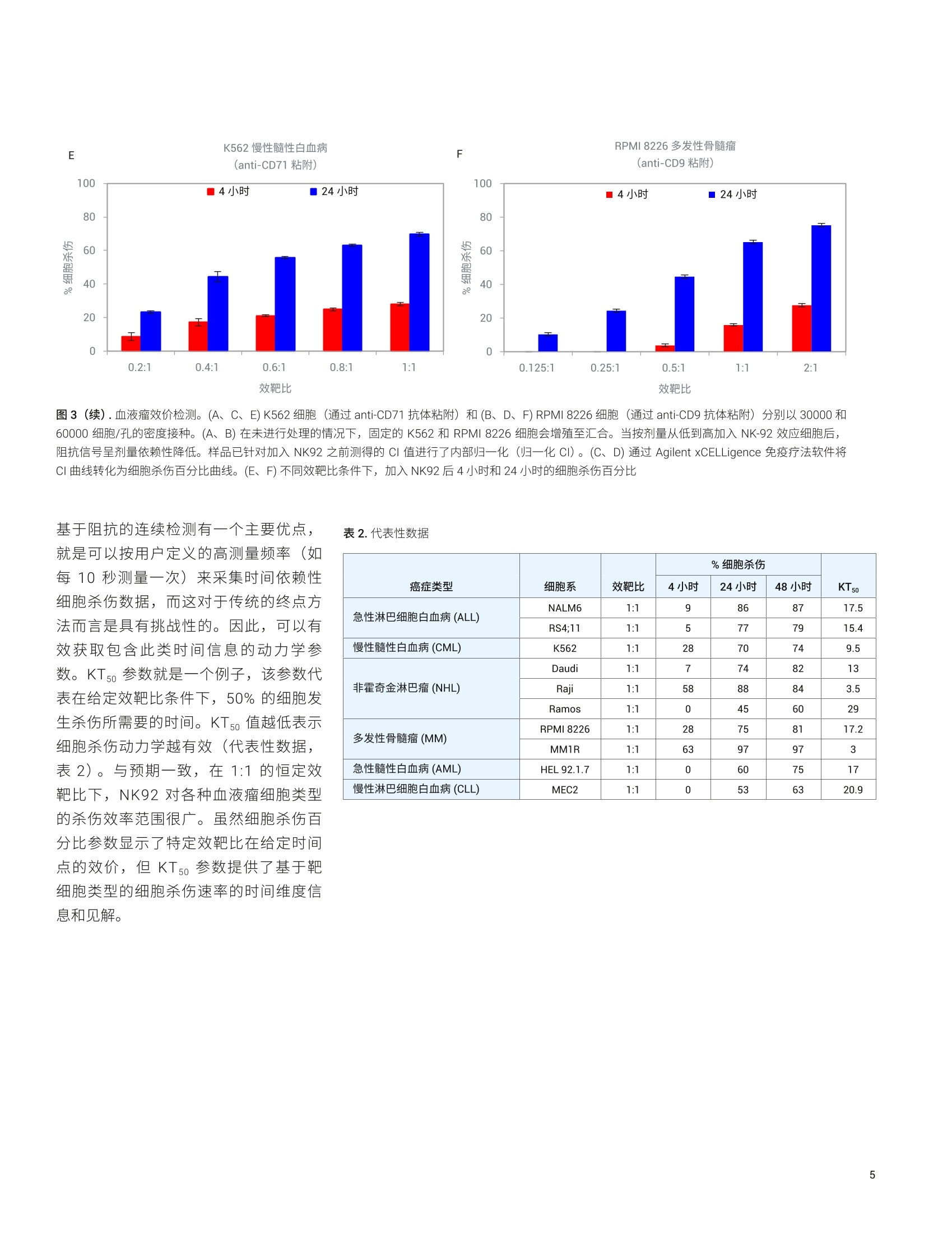
应用简报 Agilent细胞分析 Trusted Answers B细胞来源肿瘤的靶向免疫疗法功能性效价评估 Kenneth Chan 博士Yama Abassi 博士Jeff Shurong Xue 博士安捷伦科技公司 美国加利福尼亚州圣地亚哥 本应用简报介绍了使用一种粘附方法将不同来源的血液瘤细胞系固定在嵌入电子微孔板 (Agilent E-Plate) 底部的微金电极生物传感器的表面。使用这种方法成功地将多种常见的白血病细胞系(如Raji) 粘附在了 E-Plate 生物传感器上,从而产生了稳定的阻抗信号。当粘附的细胞生长汇合到一定水平后,按不同的效靶比 (E:T) 加入效应细胞,结果细胞指数 (CI)按剂量成比例下降。为了确保实验准确性,粘附试剂对靶细胞的选择性至关重要,可以排除来自效应细胞的阻抗信号。 人们对免疫效应细胞和肿瘤靶细胞之间分子相互作用的日渐了解,结合优化的基因治疗方法,共同促进了新型癌症免疫疗法的诞生,这些方法在针对实体瘤和血液瘤的测试中显示出了显著的疗效。其中最为成功的是靶向血源性肿瘤的免疫疗法。嵌合抗原受体(CAR)-T细胞疗法已成为针对复发性和难治性造血系统恶性肿瘤最具突破性的癌症免疫疗法之一。 随着近期 FDA 批准 CD19 CAR-T 用于治疗急性淋巴细胞白血病、非霍奇金淋巴瘤、弥漫性大B细胞淋巴瘤,并认定B细胞成熟抗原(BCMA) CAR-T 作为多发性骨髓瘤的突破性疗法,这项技术引起科学界极大的兴奋,并在全世界范围内引发了大量的基础研究、应用研究和临床前研究。安捷伦的目标是将 xCELLigence 实时细胞分析(RTCA)效价检测用于体外评估靶向血液瘤来源的肿瘤细胞系的免疫疗法。 E-Plate 的孔中预包被有对血液瘤细胞表达的细胞表面标志物具有特异性的粘附试剂,可以固定悬浮细胞,使其粘附到嵌有生物传感器的孔板底部(图1)。随着粘附细胞增殖,生物传感器之间的电流受阻。阻抗大小取决于细胞数量、细胞大小和粘附强度。加入免疫效应细胞(如 NK细胞、CAR-T、溶瘤病毒、检查点抑制 剂、双特异性抗体等)会导致时间依赖性和密度依赖性的靶细胞破坏,并且可以连续、灵敏地检测到相应的细胞杀伤活性。使用这项策略能够评估靶向造血系统来源的特定癌症的免疫疗法的功能性效价,通过简单的工作流程极大提高了重现性和通量。表1展示了被广泛研究的血液瘤细胞系模型,这些细胞系已经过免疫表型分析和验证,可以用于选择性粘附方法和RTCA 效价检测。 图1.使用粘附试剂预包被 Agilent E-Plate 的孔,可以使血液瘤细胞在生物传感器上粘附、增殖从而被检测 表1.广泛研究的模型血液瘤细胞系,这些细胞系已经过免疫表型分析和验证,可以用于选择性粘附方法和RTCA 效价检测 癌症类型 经验证的细胞系 选择性粘附机制 通过流式细胞术验证的靶标表达 急性淋巴细胞白血病(ALL) NALM6 CD9 CD3-, CD9+,CD19+,CD20-, CD22+,CD38+, CD138+,CD269+,HLA-DR+ RS4;11 CD9 CD3-,CD9+,CD14+,CD19+, CD20-,CD22+, CD38+,CD138+,CD269+,CD123+(low) 慢性髓性白血病(CML) K562 CD29 或 CD71 CD3-, CD14-, CD15+, CD19-,CD29+,CD33+,CD71+,CD235a+ 非霍奇金淋巴瘤 (NHL) Daudi CD40 或 CD19 CD3-,CD19+,CD20+,CD40+ Raji CD40 或 CD19 CD3-, CD19+, CD20+, CD40+ Ramos CD40 或 CD19 CD3-, CD19+,CD20+,CD40+ 多发性骨髓瘤(MM) RPMI 8226 CD9 CD3-, CD9+, CD19-,CD38+, CD138+,CD269+,HLA-DR+ MM1R CD9 和 CD71 CD3-,CD9+,CD19-,CD38+,CD71+,CD138+,CD269+,HLA-DR+ 急性髓性白血病(AML) HEL 92.1.7 CD29 CD13+, CD29+, CD33+, CD15+,CD123+ 慢性淋巴细胞白血病 (CLL) MEC2 CD40 CD3-,CD13+, CD19+, CD20+,CD40+,CD138+ 本应用简报介绍了用于评估不同血液瘤细胞系的效应细胞介导的细胞杀伤的实验设置。虽然以 NK-92 自然杀伤细胞系举例,但也可以使用其他类型的效应细胞,如 CAR-T 或外周血单核细胞 (PBMCs)。此方案可以确定靶细胞杀伤动力学以及不同效靶比下细胞毒性作用的最佳时间点。 在第一天时,将靶细胞粘附在 AgilentE-Plate VIEW 96 的孔中并进行增殖,然后连续四天检测细胞杀伤作用。 第一天:固定血液瘤细胞 a. 使用稀释的粘附试剂包被E-PlateVIEW 963个小时。清洗,加入培养基,检测背景阻抗 (CI) b. 准备血液瘤靶细胞,加入包被好的孔中 C. 将孔板在室温下静置至少30分钟,使细胞下沉 d. 将孔板放入 xCELLigence RTCA 仪器中,开始采集数据以检测靶细胞的粘附和增殖情况 第二天:加入免疫治疗效应细胞 e. 准备 NK-92效应细胞 暂停 xCELLigence 数据采集,将孔板从仪器中取出并放置在层流罩中。移除孔中的初始培养基,但要注意避免碰到粘附的细胞。使用手动多通道移液器移除培养基,不要使用真空吸液器。按不同的效靶比将效应细胞加入靶细胞中 g. 将孔板放回 xCELLigence RTCA 仪器中,开始采集数据以检测效应细胞介导的靶细胞杀伤作用。建议每30分钟采集一次数据,但确切的数据采集频率可以由用户决定 第二至五天:评估癌细胞破坏 h. 根据需要继续进行数据采集 首先将贴壁靶细胞(肿瘤细胞)接种到 Agilent E-Plate 孔中。生物传感器信号(也被称为细胞指数)随着细胞的粘附和增殖而增加,当细胞汇合率率到100%时达到平台期。 随后向悬浮液中加入非贴壁的效应细胞(免疫细胞)时,不会引起信号改变,因为这些细胞不会粘附到微金电极生物传感器上。 如果效应细胞诱导贴壁的肿瘤靶细胞死亡,则可以灵敏、精确地检测到相应的细胞杀伤活性。 使用专门为免疫肿瘤学家设计的直观图形界面, RTCA Pro 软件免疫疗法模块能够实时检测并记录细胞杀伤情况。 图 2. 使用 Agilent XCELLigence微金电极生物传感器实时检测免疫细胞介导的对固定的血液瘤细胞的杀伤作用 结果与讨论 NK-92 细胞对白血病和多发性骨髓瘤细胞的实时杀伤作用 为了使用RTCA 效价检测方法评估细胞毒性 NK-92 细胞杀伤血液瘤细胞的效价随时间的变化,通过指定的选择性粘附机制将肿瘤靶细胞固定在孔板底部。向肿瘤细胞中加入不同剂量的 NK-92 效应细胞以获得不同的效靶比。使用 RTCA 仪器检测接下来一到两天内的阻抗变化,通过生物传感器检测靶细胞的破坏情况,并报告为 阻抗(CI)降低。图3A和3B展示了血液瘤细胞通过其表面的标志物在孔底生物传感器上的特异性粘附情况。与预期一致,对粘附的靶细胞的杀伤效率取决于 NK-92效应细胞与靶癌细胞之间的比率。将仅有靶细胞 (E:T=0:1)的情况作为细胞杀伤的阴性对照。 由于加入效应细胞后 CI 降低与细胞活力直接相关,可通过数学计算轻松地将其转化为细胞杀伤百分比,其中考虑了来自仅靶细胞的对照组的信号。如图3C和3D所示,细胞杀伤百分比随时间和效靶 比的增加而升高。对于图3所示的两种血液瘤细胞系,在所测试的几种效靶比条件下,细胞杀伤百分比在40-45小时后达到平台期,并且均低于100%,表明NK92 并未完全杀死靶细胞。我们推测,在低效靶比条件下,效应细胞是一个限制因素,其无法杀死所有靶细胞,未被杀死的靶细胞继续增殖。经过一段时间的共培养后,两种细胞群的数量最终可能达到平衡,信号的平台期可以反映这一点。图 3E 和 3F 显示了不同效靶比条件下,加入NK-92细胞4小时或24小时后 NK-92介导的靶细胞杀伤程度。 图3.血液瘤效价检测。(A、C、E)K562细胞(通过 anti-CD71 抗体粘附)和(B、D、F) RPMI 8226 细胞 (通过 anti-CD9 抗体粘附)分别以30000和60000细胞/孔的密度接种。(A、B)在未进行处理的情况下,固定的 K562和 RPMI 8226 细胞会增殖至汇合。然而,当按剂量从低到高加入 NK-92 效应细胞后,阻抗信号呈剂量依赖性降低。样品已针对加入 NK92 之前测得的 CI 值进行了内部归一化(归一化CI)。(C、D) 通过 Agilent xCELLigence 免疫疗法软件将CI曲线转化为细胞杀伤百分比曲线。(E、F)不同效靶比条件下,加入NK92后4小时和24小时的细胞杀伤百分比 K562 慢性髓性白血病 RPMI 8226多发性骨髓瘤 效靶比 效靶比 图3(续).血液瘤效价检测。(A、C、E)K562细胞(通过 anti-CD71 抗体粘附)和(B、D、F)RPMI 8226细胞(通过 anti-CD9抗体粘附)分别以30000 和60000细胞/孔的密度接种。(A、B)在未进行处理的情况下,固定的 K562 和 RPMI 8226 细胞会增殖至汇合。当按剂量从低到高加入 NK-92 效应细胞后,阻抗信号呈剂量依赖性降低。样品已针对加入 NK92之前测得的CI值进行了内部归一化(归一化CI)。(C、D) 通过 Agilent XCELLigence 免疫疗法软件将CI曲线转化为细胞杀伤百分比曲线。(E、F)不同效靶比条件下,加入NK92后4小时和24小时的细胞杀伤百分比 基于阻抗的连续检测有一个主要优点,就是可以按用户定义的高测量频率(如每10秒测量一次)来采集时间依赖性细胞杀伤数据,而这对于传统的终点方法而言是具有挑战性的。因此,可以有效获取包含此类时间信息的动力学参数。KT5o参数就是一个例子,该参数代表在给定效靶比条件下,50%的细胞发生杀伤所需要的时间。KT50值越低表示细胞杀伤动力学越有效(代表性数据,表2)。与预期一致,在1:1的恒定效靶比下, NK92对各种血液瘤细胞类型的杀伤效率范围很广。虽然细胞杀伤百分比参数显示了特定效靶比在给定时间点的效价,但KT50参数提供了基于靶细胞类型的细胞杀伤速率的时间维度信息和见解。 癌症类型 细胞系 效靶比 %细胞杀伤 KT50 4小时 24小时 48小时 急性淋巴细胞白血病(ALL) NALM6 1:1 9 86 87 17.5 RS4;11 1:1 5 77 79 15.4 慢性髓性白血病(CML) K562 1:1 28 70 74 9.5 非霍奇金淋巴瘤(NHL) Daudi 1:1 7 74 82 13 Raji 1:1 58 88 84 3.5 Ramos 1:1 0 45 60 29 多发性骨髓瘤(MM) RPMI 8226 1:1 28 75 81 17.2 MM1R 1:1 63 97 97 3 急性髓性白血病(AML) HEL 92.1.7 1:1 0 60 75 17 慢性淋巴细胞白血病 (CLL) MEC2 1:1 0 53 63 20.9 结论 我们证明了 xCELLigence RTCA 不仅可以评估针对多种血液瘤的免疫疗法的效价,还可以在生理相关效靶比下检测血液瘤细胞的破坏动力学。与传统检测方法相比,此方案的工作量更少。将血液瘤靶细胞接种并粘附在经预包被的 E-Plate中,然后加入效应细胞,并在几天内非侵入性地检测癌细胞破坏动力学。自动连续采集数据。阻抗数据的定量和实时特征使得能够轻松比较不同免疫疗法和不同剂量之间的效价。 使用这种表面粘附方法,多种效应细胞(PBMC、NK、CAR-T,以及双特异性T细胞 (BiTEs) 等生物分子)靶向肿瘤细胞表达的 EpCAM 蛋白,并阻断针对免疫检查点抑制剂 PD-1 的抗体 (Cerignoli 等,2018)。xCELLigence 平台非常适合血液瘤的效价评估,能够为开发的免疫肿瘤疗法提供高重现性的定量评估以及简单的工作流程。 www.agilent.com 仅限研究使用。不可用于诊断目的。 本文中的信息、说明和指标如有变更,恕不另行通知。 c 安捷伦科技(中国)有限公司,2019 ( 2019年11月1日, 中国出版 5994-1066ZHCNAN18DE.5700231481 ) ( 1. Cerignoliet al. I n VitroImmunotherapy Potency AssaysUsing Real-T i me Cell Analysis. PLoSOne. 2018Mar 2, 13(3),e0193498 ) 2. ( Lamarche et al. Quantifying thePotency of Cancer Immunotherapies: Immune Cell-Mediated Killing Kinetics and E fficacy Analysis in Real-Time without the Use of Labels. Genetic Engineering & BiotechnologyNews (GEN). 2016,36(14),18-9 ) ( 3. S chmittnaegel et al.CommittingCytomegalovirus-Specific CD8 T Cells to Eliminate Tumor Cells by Bifunctional Major HistocompatibilityClass I Antibody Fus i on Molecules.Cancer Immunol Res. 2015 Jul, 3(7), 764-76 ) ( 4. P eper et al. An Impedance BasedCytotoxicity Assay For Real-Time and L a bel-Free Assessment of T-Cell- Mediated Killing of Adherent C ells.J. Immunol.Methods 2014 Mar, 405, 192-8 ) 5. Park et al. Evaluation of NK CellFunction by FlowcytometricMeasurement and ImpedanceBased Assay Using Real-Time CellElectronic Sensing System.Biomed. Res. Int. 2013,2013,210726 查找当地的安捷伦客户中心:www.agilent.com/chem/contactus-cn 免费专线: 800-820-3278,400-820-3278(手机用户) 联系我们: LSCA-China_800@agilent.com 在线询价: ( 6. Erskine et al. Determining OptimalCytotoxic Activit y of Human Her2neuSpecific CD8 T Cells by Comparingthe Cr51 Releaseassay to thexCELLigence System. J. V i s. E xp.2012 Aug 8, 66, e3683 ) ( 7. Fu et al. A Simple and Sensitive Method For Measuring Tumor-Specific T Cell Cytotoxicity.PLoS One. 2 010, 5 (7), e11867 ) xCELLigence RTCA 不仅可以评估针对多种血液瘤的免疫疗法的效价,还可以在生理相关效靶比下检测血液瘤细胞的破坏动力学。与传统检测方法相比,此方案的工作量更少。将血液瘤靶细胞接种并粘附在经预包被的 E-Plate 中,然后加入效应细胞,并在几天内非侵入性地检测癌细胞破坏动力学。自动连续采集数据。阻抗数据的定量和实时特征使得能够轻松比较不同免疫疗法和不同剂量之间的效价。使用这种表面粘附方法,多种效应细胞(PBMC、NK、CAR-T,以及双特异性 T 细胞 (BiTEs) 等生物分子)靶向肿瘤细胞表达的 EpCAM 蛋白,并阻断针对免疫检查点抑制剂 PD-1 的抗体(Cerignoli 等,2018)。xCELLigence 平台非常适合血液瘤的效价评估,能够为开发的免疫肿瘤疗法提供高重现性的定量评估以及简单的工作流程。
确定




还剩4页未读,是否继续阅读?
安捷伦科技(中国)有限公司为您提供《B细胞中不同来源的血液瘤细胞系检测方案(细胞定量分析)》,该方案主要用于其他中不同来源的血液瘤细胞系检测,参考标准--,《B细胞中不同来源的血液瘤细胞系检测方案(细胞定量分析)》用到的仪器有Agilent xCELLigence RTCA eSight 实时细胞分析仪、Agilent xCELLigence RTCA S16实时无标记细胞分析仪
推荐专场
相关方案
更多
该厂商其他方案
更多
















