[摘 要] 目的 建立注射用维生素C 的无菌检查方法。方法 取三批、三个厂家的维生素C ,进行无菌检
查,方法验证Ⅰ采用直接接种法;方法验证Ⅱ采用薄膜过滤法,用适量的冲洗液冲洗。结果 方法验证Ⅰ供试品
产生干扰;方法验证Ⅱ样品管无菌生长,6 株阳性对照菌生长良好,且供试品无干扰。结论 采用方法验证试验
Ⅱ进行维生素C 的无菌检查,可行。
[关键词] 无菌检查法;薄膜过滤法;方法验证
方案详情

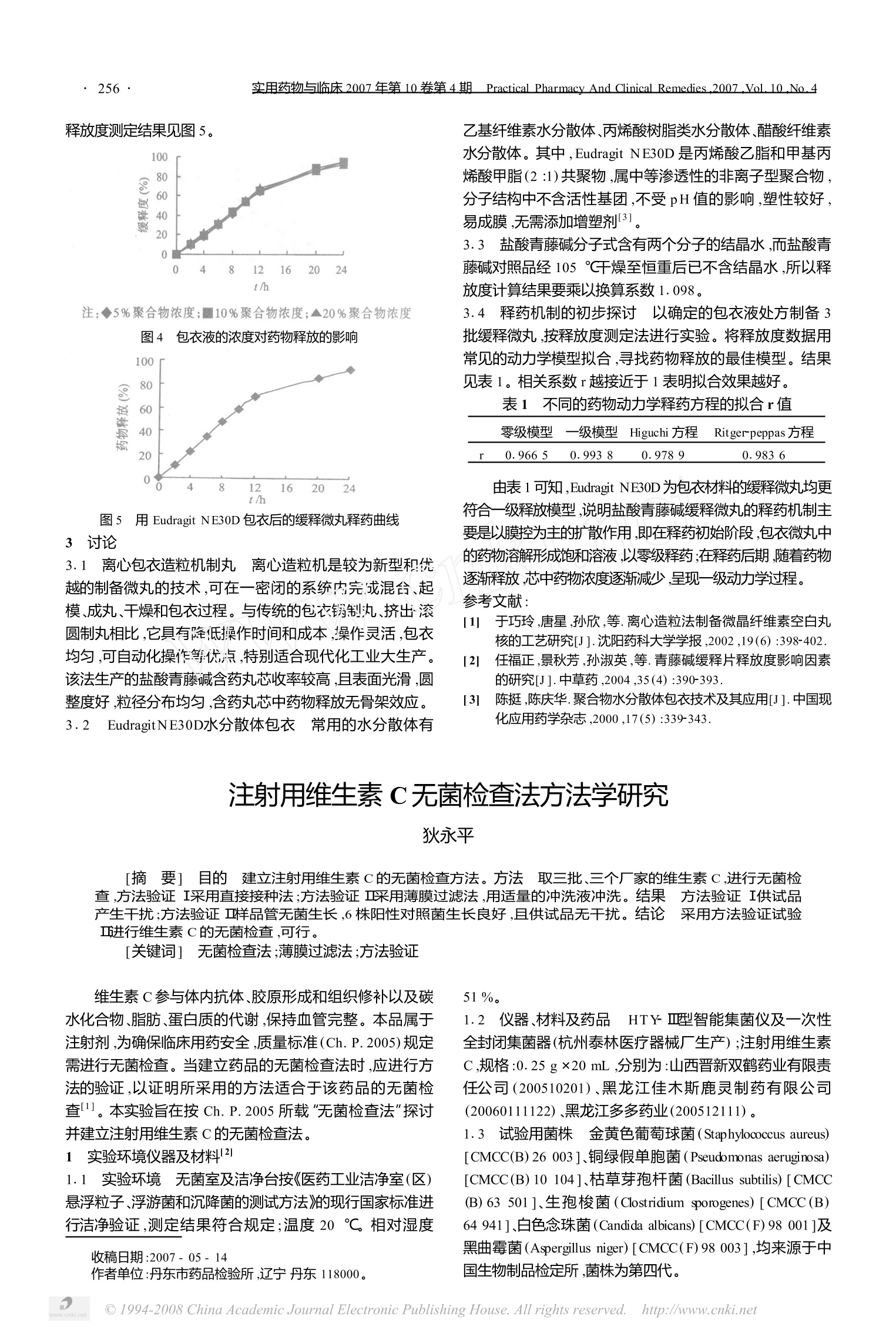
实用药物与临床2007年第10卷第4期月PracticalPharmacy And Clinical Remedies 2007 Vol.10No.4·256 释放度测定结果见图5。 注:◆5%聚合物浓度;■10%聚合物浓度;▲20%聚合物浓度 图4 包衣液的浓度对药物释放的影响 图5 用 Eudragit NE30D 包衣后的缓释微丸释药曲线 3 讨论 3.1 离心包衣造粒机制丸 离心造粒机是较为新型和优越的制备微丸的技术,可在一密闭的系统内完成混合、起模、成丸、干燥和包衣过程。与传统的包衣锅制丸、挤出滚圆制丸相比,它具有降低操作时间和成本,操作灵活,包衣均匀,可自动化操作争优点,特别适合现代化工业大生产。该法生产的盐酸青藤碱含药丸芯收率较高,且表面光滑,圆整度好,粒径分布均匀,含药丸芯中药物释放无骨架效应。 3.2 EudragitNE30D水分散体包衣 常用的水分散体有 乙基纤维素水分散体、丙烯酸树脂类水分散体、醋酸纤维素水分散体。其中,Eudragit NE30D 是丙烯酸乙脂和甲基丙烯酸甲脂(2:1)共聚物,属中等渗透性的非离子型聚合物,分子结构中不含活性基团,不受pH值的影响,塑性较好,易成膜,无需添加增塑剂31. 3.3 盐酸青藤碱分子式含有两个分子的结晶水,而盐酸青藤碱对照品经105℃干燥至恒重后已不含结晶水,所以释放度计算结果要乘以换算换数1.098。 3.4 释药机制的初步探讨 以确定的包衣液处方制备3批缓释微丸,按释放度测定法进行实验。将释放度数据用常见的动力学模型拟合,寻找药物释放的最佳模型。结果见表1。相关系数r越接近于1表明拟合效果越好。 表1 不同的药物动力学释药方程的拟合r值 零级模型 一级模型 Higuchi 方程 Ritgerpeppas 方程 0.9665 0.993 8 0.9789 0.9836 由表1可知,Eudragit NE30D 为包衣材料的缓释微丸均更符合一级释放模型,说明盐酸青藤碱缓释微丸的释药机制主要是以膜控为主的扩散作用,即在释药初始阶段,包衣微丸中的药物溶解形成饱和溶液,以零级释药;在释药后期,随着药物逐渐释放,芯中药物浓度逐渐减少,呈现一级动力学过程。 ( 参考文献: ) ( [1] 于巧玲,唐星,孙欣,等.离心造粒法制备微晶纤维素空白丸 核的工艺研究[J].沈阳药科大学学报,2002,19(6):398-402. ) ( 2 任福正,景秋芳,孙淑英,等.青藤碱缓释片释放度影响因素 的研究[J].中草药,2004,35(4):390-393. ) ( [3] 陈挺,陈庆华.聚合物水分散体包衣技术及其应用[J].中国现 化应用药学杂志,2000,17(5):339-343. ) 注射用维生素C无菌检查法方法学研究 狄永平 [摘 要1 目的 建立注射用维生素C的无菌检查方法。方法 取三批、三个厂家的维生素C,进行无菌检查,方法验证I采用直接接种法;方法验证Ⅱ采用薄膜过滤法,用适量的冲洗液冲洗。结果 方法验证I供试品产生干扰;方法验证Ⅱ样品管无菌生长,6株阳性对照菌生长良好,且供试品无干扰。结论 采用方法验证试验I进行维生素C的无菌检查,可行。 [关键词]无菌检查法;薄膜过滤法;方法验证 维生素C参与体内抗体、胶原形成和组织修补以及碳水化合物、脂肪、蛋白质的代谢,保持血管完整。本品属于注射剂,为确保临床用药安全,质量标准(Ch. P. 2005)规定需进行无菌检查。当建立药品的无菌检查法时,应进行方法的验证,以证明所采用的方法适合于该药品的无菌检查。本实验旨在按 Ch. P.2005所载“无菌检查法”探讨并建立注射用维生素C的无菌检查法。 1 实验环境仪器及材料2 1.1 实验环境 无菌室及洁净台按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法》的现行国家标准进行洁净验证,测定结果符合规定;温度20℃。相对湿度 ( 收稿日期:2007-05-14 ) ( 作者单位:丹东市药品检验所,辽宁丹东118000。 ) 51%。 ( 1.2 仪器、材料及药品 HTYⅢ型智能集菌仪及一次性全封闭集菌器(杭州泰林医疗器械厂生产);注射用维生素 C,规格:0.25gX20 mL ,分别为:山西晋新双鹤药业有限责 任公司(200510201)、黑龙江佳木斯鹿灵制药有限公司 (20060111122)黑龙江多多药业(200512111)。 ) 1.33试验用菌株 金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003]、铜绿假单胞菌(Pseudomonas aeruginosa)[CMCC(B) 10 104]、枯草芽孢杆菌(Bacillus subtilis)[ CMCC(B)63501]、生孢梭菌(Clostridium sporogenes) [ CMCC(B)64941]、白色念珠菌(Candida albicans) [CMCC(F)98 001]及黑曲霉菌(Aspergillus niger) [CMCC(F)98 003],均来源于中国生物制品检定所,菌株为第四代。 1.4 菌液制备 接种金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌的新鲜培养物至营养琼脂培养基中;接种生孢梭菌的新鲜培养物至硫乙醇酸盐流体培养基中,35℃培养20h,取上述培养物,用0.9%无菌氯化钠溶液制成小于100 cfu/mL的菌落,用营养琼脂培养基平板计数;接种白色念珠菌的新鲜培养物至改良马丁培养基中,25℃培养24h,用0.9%无菌氯化钠溶液制成小于100 cfu/mL的菌液,用改良马丁琼脂培养基平板计数;接种黑曲霉的新鲜培养物至改良马丁琼脂斜面培养基上,25℃培养5d,加4mL0.9%无菌氯化钠溶液将孢子洗脱,取洗脱液液0.9%无菌氯化钠溶液稀释至小于100 cfu/mL的菌液,用改良马丁琼脂培养基平板计数。 1.5 培养基、冲洗剂 硫乙醇酸盐流体培养基(批号:0603232)、改良马丁培养基(批号:050104)、营养琼脂培养基(批号:050905)、营养肉汤培养基(批号:059121)、改良马丁琼脂培养基(批号:061107),此5种培养基均来源于北京三药科技开发公司,配制方法均按瓶签说明配制。0.9%灭菌氯化钠(批号:041011,来源:成都五环高欣化学试剂厂)溶液、0.1%蛋白胨(批号:2004.11.15,来源北京双旋微生物培养基制品厂)水溶液。 2 试验方法选择 2.1 方法验证Ⅰ(直接接种法)) 取3支试管,分别加入培养基灭菌,其中一管接种小于100 cfu 的试验菌作为阳性对照一试验管A,取本品按规定量加入另两个管中,其中一管接种小于100 cfu 的试验菌作为试验管B,另一管不接种试验菌作为试验管C。阴性对照管:分别取硫乙醇酸盐流体培养基、改良马丁培养基加入两试管内。按规定温度将上述试管培养3~5d,各试验菌同法操作。结果:试验管AB内试验菌生长均良好,但试验管C出现网状的悬浮物,吸取悬浮物,经再培养及显微镜检,确认该悬浮物不是菌体。2.2 方法验证Ⅱ(薄膜过滤法) 取一次性全封闭集菌器(三联)一套,一管泵入培养基并接种小于100 cfu 的金黄色葡萄球菌并夹紧管口作为试验管A;另取本品10瓶按薄膜过滤法滤至另两管,用0.1%蛋白胨水溶液分3次冲洗,每 次100 mL,泵入相同培养基于一管中,接种小于100 cfu 的金黄色葡萄球菌作为试验管B;另一管不接种试验菌作为试验管C。取全封闭式集菌器两联一套,分别将硫乙醇酸盐培养基及改良马丁培养基泵入两管中,作为阴性对照管。按规定温度培养3~5d,试验管A、B内菌株生长均良好,试验管C中培养基澄明、无悬浮物。 3 结果 取30瓶的供试品按薄膜过滤法滤至一次性全封闭式集菌器(三联)中,用0.1%蛋胨水溶液分3次冲洗,每次300mL,两管加入硫乙醇酸盐培养基(其中一管接入小于100 cfu 的金黄色葡萄球菌作为阳性对照管),第3管加入改良马丁培养基,按规定温度培养14d,逐日观察,供试品澄清,阳性对照管生长良好,判断供试品符合规定。 4 讨论 4.1 方法验证显示,试验管AB两管内试验菌生长良好,说明供试品无抑菌作用。但试验管C内有网状悬浮物,经检验不是微生物,只是与微生物相类似,有可能是样品与培养基中的某些成分发生反应而析出的物质,形成结晶性网状悬浮物,干扰结果的判断,采用薄膜过滤法,用冲洗液将培养器内的维生素C冲洗干净后,不再干扰结果判断。 4.23无菌检查中有很多品种都可能有类似现象,而干扰结果的判断,故在具体工作中应细心观察,设计好验证方法,避免出现假阳性。 4.3 《中国药典》2005年版无菌检查中增加了验证方法,验证方法主要考虑的是供试品在该实验条件下有、无抑菌活性,通过适宜的实验方法消除其干扰,避免产生假阴性。而本验证方法是消除供试品的干扰,避免产生假阳性。 4.4 本验证方法既保证了所有阳性对照菌正常生长,又消除了供试品的干扰,能准确无误地检查样品染菌情况,故适合作为注射用维生素C的无菌检查法。 ( 参考文献: ) ( [1] 中国药品生物制品检定所.中国药品检验标准操作规范[M].北京:中国医药科技出版社,2005:313. ) ( [2 方玲芬.注射用奥美拉唑钠无菌检查法方法学研究[J].中国 药品标准,2006,7(1):64-66. ) 注射用脑蛋白水解物血管刺激和溶血与凝聚检查方法的建立 焉媛媛,丁晓飞 「摘 要1 目的 建立注射用脑蛋白水解物血管刺激和溶血的检查方法。方法 确定注射用脑蛋白水解物稀释液对家兔耳静脉血管的刺激作用和溶血与凝聚的检查方法。结果 注射用脑蛋白水解物稀释液对家兔血管无刺激现象,同样也无溶血与凝聚反应。结论 注射用脑蛋白水解物0.24mg/mL 可用于静脉注射给药。 「关键词] 注射用脑蛋白水解物;家兔血管刺激;溶血与凝聚 Establishment of examining methods for vascular stimulation and hemolyzationr aggregation of cerebroprotein hydrolysate forinjection YAN Yuarr yuan ,DING Xiaofei (Liaoning Institute for Drug Control,Shenyang 110023 ,China) [Abstract Objective To establish the examining methods for vascular stimulation and hemolyzation-aggrega-tion. Methods The experiments were examined by ear vascular stimulation on rabbit and hemolyzation aggregation onrabbit erythrocyte in vitro. Results It was shown that cerebroprotein hydrolysate for injection had no effect on vascular ( 收稿日期:2006-12-23 ) ◎China Academic Journal Electronic Publishing House.All rights reserved. http://www.cnki.net
确定

还剩1页未读,是否继续阅读?
浙江泰林生物技术股份有限公司为您提供《注射用维生素C中无菌检查检测方案(集菌仪)》,该方案主要用于化药制剂中微生物相关及生化特性检测,参考标准--,《注射用维生素C中无菌检查检测方案(集菌仪)》用到的仪器有集菌仪智能型HTY-601
推荐专场
相关方案
更多
该厂商其他方案
更多















