方案详情
文
[摘要] 目的:建立复方紫草油的无菌检查法。方法:采用
先3 0()()r·min 离心 20 rain,弃去上清液后的底部液体加等
量无菌聚山梨酯一8O,再转移至0.1 的聚山梨酯 8【)一氯化钠
蛋白胨缓冲液 中,然后再采用薄膜过滤法,用0.t 聚山梨
酯一80一氯化钠一蛋白胨缓冲液冲洗滤膜。结果:供试品经处理
后能通过滤膜 ,供试品FEl性对照管 24 h内实验菌生长良好
结论 :该法能消除复方紫草油的抑菌作用,使无菌检查结果
准确 可靠。
[关键词] 复方紫草油;无菌检查;离心;薄膜过滤法
方案详情

维普资讯 http://www.cqvip.com中国医院药学杂志2007年第27卷第3期 Chin Hosp Pharm J,2007 Mar, Vol 27,No. 03·407· [作者简介]孙春燕,女,硕士,主管药师,电话:027-87895875,E-mail:suncy25@126. com 不同有机溶剂中,盐酸地尔硫草的稳定性也有差别,其在极性较大的溶剂中稳定性较差,在乙醇和甲醇中稳定性较好。药物检测过程中,其在选定的配制溶剂中应是稳定的、不易发生化学变化,如果由于溶剂的选择不当导致药物发生降解、有关物质增加,将掩盖真实的实验结果。提示盐酸地尔硫草的供试品溶液和对照品溶液宜用乙醇或甲醇12-3]配制,更利于保存。 ( 参考文献: ) ( 1 王璐璐,郑稳生.盐酸地尔硫草注射液的制备及稳定性考察[J].中国医院药学杂志,2003,23(5):272-274. ) ( 中国药典.二部[S].2005:489-490. ) ( 3 The United States Pharmacopeia. Volume I [ S ]. 2000:573- 574. ) ( [收稿日期]2006-01-24 ) 复方紫草油的无菌检查法. 孙春艳,张春瑛,程樱,王敏 (湖北省药品检验所,湖北武汉430062) [摘要] 目的:建立复方紫草油的无菌检查法。方法:采用先3000 rmin离心 20 min,弃去上清液后的底部液体加等量无菌聚山梨酯-80,再转移移0.1%的聚山梨酯-80-氯化钠-蛋白胨缓冲液中,然后再采用薄膜过滤法,用0.1%聚山梨酯-80-氯化钠-蛋白胨缓冲液冲洗滤膜。结果:供试品经处理后能通过滤膜,供试品阳性对照管24h内实验菌生长良好。结论:该法能消除复方紫草油的抑菌作用,使无菌检查结果准确可靠。 [关键词] 复方紫草油;无菌检查;离心;薄膜过滤法 [中图分类号]R927.1 [文献标识码]A [文章编号]1001- 5213(2007)03-0407-02 复方紫草油是以紫草为主药,以食用植物油为基质而制得的一种制剂,为红紫色黏稠液体,主治烧伤,烫伤。该药具抗菌、消炎作用,对金葡菌、绿脓杆菌等多种细菌均有抑制作用,并能加速上皮生长,加快创面愈合。根据中国药典2005年版规定1用于皮肤烧伤的外用药物应做无菌检查。但此剂型,药典尚未有明确的检查法。而且由于复方紫草油具有抑菌作用,不能用直接接种法来检测,只能采用薄膜过滤法,但该药仅能少许通过滤膜,为此,采用离心与薄膜过滤相结合的方法进行了实验研究。 仪器与材料1 仪器 LD4-2低速离心机(北京医用离心机厂);灭菌刻度离心管,电热恒温水浴箱(上海医疗器械七厂);HTY-2000A 集菌仪,KSF220 型全封闭无菌试验过滤培养器,KSF110 型全封闭无菌试验过滤培养器(杭州高得医疗器械有限公司)。 1.2培养基 硫乙醇酸盐流体培养基(批号0601162),改良马丁培养基(批号060122),营养肉汤培养基(批号030925),营养琼脂培养基(批号060214),均由中国药品生物检定所提供;稀释液为0.1%聚山梨酯-80-氯化钠-蛋白胨缓冲液(自配)。 1.3 菌种(第三代) 金黄色葡萄球菌[CMCC(B) 26003];铜绿假单胞菌[CMCC(B)10104];枯草芽孢杆菌[CMCC(B)63501];生孢梭菌[CMCC(B)64941];白色念珠菌[CMCC(F)98001];黑曲霉[CMCC(F)98003],菌种均由中国药品生物制品检定所提供。 1.4 供试品复方紫草油(湖北省中医院,规格:100mL,批号060405) 2方法与结果 2.1 复方紫草油无菌检查方法学验证试验12-3] 2.1.1 菌液制备 取经35℃培养18~24h的金黄色葡萄球菌、铜绿假单胞菌与枯草芽孢杆菌的肉汤新鲜培养物、生孢梭菌硫乙醇酸盐液体培养物各1mL分别加入9mL0.9%无菌氯化钠溶液中,10倍系列稀释至使菌数约为50~100 cfumL-1。取经25℃培养18~24h的白色念珠菌改良马丁液体培养物1 mL,加加9 mL 0.9%无菌氯化钠溶液中,10倍稀释系列至使菌数约为50~100 cfumL-1。取经25℃培养一周的黑曲曲斜面培养物,加0.9%无菌氯化钠溶液10mL,将孢子洗脱,然后,吸出孢子悬液,用垫有脱脂棉的漏斗(已灭菌)过滤,除去菌丝,收集菌液至另一无菌试管内作为菌原液。取此菌原液0.1mL加0.9%无菌氯化钠溶液至9.9mL 中,稀释至使菌数约为50~100cfu·mL-1,上述菌液均进行菌液计数。 表1 细菌和真菌计数结果(菌数为2个平个的平均数 cfu/mL Tab 1 Bacteria and epiphyte count results (the mean of twcdiscs cfu/mL) 项目 金黄色 铜绿假 枯草芽 生胞 黑曲霉 白色 葡萄球菌 单胞菌 胞杆菌 梭菌 念珠菌 稀释级 10-5 10-5 10-5 10-6 10-5 10-5 计数(第1次) 88 3 计数(第2次) 2.1.2 供试品的处理 取供试品3瓶(供1株试验菌用),分别转移至6个50 mL无菌刻度离心管中,3000 r*min离心20 min,上去上清液,每管留底部液体约2mL,每管加入2mL已灭菌的聚山梨酯-80,振摇使混匀,然后将混合液体汇集至450 mL 的0.1%聚山梨酯-80-氯内钠-蛋白胨缓冲液中,45℃水浴中适当加热,振摇得到供试液。取 KSF110 型薄膜过滤器,先用过滤适量0.3%聚山梨酯-80-氯化钠-蛋白胨缓冲液使滤膜润湿,将上述乘热按薄膜过滤法过滤,过滤完毕后用0.3%聚山梨酯-80-氯化钠-蛋白胨缓缓液 100 mL冲洗滤器,然后在约50 mL 0.9%无菌氯化钠溶液中加入少于100 cfu一种试验菌,同法过滤,将相应的培养基加至此封闭式薄膜滤器内,作为供试品管。同法制备其他菌株所需用的供试液。 2.1.3 阳性对照 另取封闭式薄膜过滤器,不过滤供试品,同法加加等量的试验菌于 50 mL 0.9%无菌氯化钠溶液中,~过滤,作为菌液对照管,6种试验菌分别同法操作。 2.1.4 阴性对照 另取两个封闭式薄膜过滤器,每个滤器内过滤0.3%聚山梨酯-80-氯化钠-蛋白胨缓冲液100 mL,然后分别加入硫乙醇酸培养基和改良马丁培养基各100 mL,不加对照菌液。上述供试品组及对照组按规定温度培养5d,每天观察并记录结果,硫乙醇酸盐流体培养基置35℃培 2.1.5 验证试验结果 见表2. 表2 方法学验证试验结果 Tab 2 Evaluation resalt of methodology 项目 金黄色 铜绿假 枯草芽 生胞 黑曲霉 白色 葡萄球菌 单胞菌 胞杆菌 梭菌 念珠菌 培养时间/h 24 24 24 24 48 48 样品管 十 + + 十 十 + 阳性对照管 十 十 十 十 十 十 注:+表示有菌生长 表2的结果表明,与金黄色葡萄球菌、铜绿假单胞菌、枯草芽胞杆菌、生胞梭菌对照菌管比较,含样品的各管24h内生长良好;与白色念珠菌、黑曲霉对照菌管比较,样品管48h内生长良好,同时硫乙醇酸盐流体培养基和改良马丁培养基阴性对照管5d内均无菌生长,说明本品经上述处理后无抑菌作用,此无菌检查方法可行。 2.2复方紫草油无菌检查法 取复方紫草油6瓶,每瓶转移至2个50 mL 无菌刻度离心管中,3000 rmin"'离心20min,弃去上清液,每管留底部液体约2mL,每管加入2 mL已灭菌的聚山梨酯-80,振摇,得到12管混合液,将混合液分别汇集至450 mL 的0.1%聚山梨酯-80-氯化钠-蛋白胨缓冲液中,45℃水浴中适当加热,振摇。取 KSF220 型薄膜过滤器,先用过滤适量0.1%聚山梨酯-80-氯化钠-蛋白胨缓冲液使滤膜润湿,然后将上述供试液乘热按薄膜过滤法过滤,过滤完毕后用0.3%聚山梨酯+80氯化钠-蛋白胨缓冲液200mL冲洗滤器,冲洗完毕后分别加人硫乙醇酸盐和改良马丁培养基100 mL。另取复方紫草油3瓶,以金黄色葡萄球菌为阳性对照菌按方法学验证试验中的方法制备阳性对照管。阴性对照管的制备同方法学验证实验中的阴性对照。 上述供试品组及对照组按规定温度培养14d,每天观察并记录结果,硫乙醇酸盐流体培养基置35℃培养;改良马丁培养基置25℃培养。 3 讨论 根据药典中液体制剂的最小检验量的规定,供试品的装量为 10 mL时的最少检验数量为10瓶,每个样品接入每管培养基的最少检验数量是半量,因此,每管培养基最少接人的样品总量是500 mL,这么多样品根本无法通过滤膜,因此采用离心沉淀集菌法的原理来减少接入每管培养基的样品量。 离心后,底部的液体加聚山梨酯-80乳化,再转转0.1%聚山梨酯-80-氯化钠-蛋白胨缓冲液中稀释,由于底部液体中有少许沉淀,所以经45℃水浴后更易重新分散,经过上述处理后,可以大大加快样品的过滤速度。过滤后,滤器管道中及滤器壁上仍残留少许样品,所以用0.1%聚山梨酯-80-氯化钠-蛋白胨缓冲液冲洗。聚山梨酯-80的浓度不宜过高,否则会产生太多泡沫而影响过滤。 ( 参考文献: ) ( [1 ] 中国药典.二部[S].2005:9、 ) ( [2] 中国药品生物制品检定所[S].中国药品检验标准操作规范, 313-323. ) ( [3] 马绪荣,苏德模.微生物学检验手册[M].科学出版社,2000: 18-21. ) ( [收稿日期]2006-08-20 ) 药师配发的分劈药片缺乏剂量一致性 李江华,曾佳,杨煊,杨爱群,李艳 (广东药学院附属第一医院,广东广州510080) [摘要] 目的:测定由药师配发的分劈药片的剂量一致性水平。方法:将16种常被分劈的药片进行分劈,并借用美国药典 24(USP)中的剂量单位一致性测试法来评估所得半片是否有等同的剂量。结果:在所检测的16种分劈片中,有14种药片没有通过 USP 剂量单位一致性测试,且药片在分劈过程中都存在着剂量损耗。结论:药片分劈导致了较大的质量变异,为了节省开支或改善剂量而进行分劈药片的做法,有待商榷。 [关键词] 药师;分劈药片;剂量一致性 [中图分类号]R956.3 [文献标识码]A [文章编号]1001- 5213(2007)03-0408-02 药师有时会将药片分成两半或四半以调整剂量而满足临床的需要。将药片分劈成半的做法所依据的是药片能够足够准确地分劈这样一种假设。然而国外有学者研究显示,大多数的药片未能得到均匀的分劈,有些药片分劈后所得的半片剂量超出了其目标剂量的85%~105%范围1-21。为此,本试验进行了分劈药片剂量一致性研究,现将研究结果报道给各位同仁,以便引起大家的重视。 1材料和方法 1.1 材料 FA-1604S 型电子分析天平(上海天平仪器厂);从我院中心药房选择常用的16种分劈药片,见表1。 表1 分劈药片样本 Tab 1 Sampled tablet fragments 药名 生产商 批号 剂量/mg 整片药外观 倍他乐克阿斯利康 0401015 25 圆形、单面一字刻痕 博利康尼 阿斯利康 200311007 2.5 圆形、单面一字刻痕 达美康 天津施维雅一华津 030362 80 圆形、单面十字刻痕 息宁 杭州默沙东 P1019 250 椭圆形、双面一字刻痕 雅思达 法国施维雅 3L2265 4 长圆形、双面一字刻痕 美多芭 上海罗氏 SH0224 250 圆形、双面十字刻痕 维思通 西安杨森 020524757 1 长圆形、单面一字刻痕 开博通 上海施贵宝 0310031H 12.5 长圆形、双面一字刻痕 雷替斯 德国 33041 0.05 圆形、单面一字刻痕 德巴金 赛诺菲一圣德拉堡 1909 500 长圆形、双面一字刻痕 地高辛 上海信谊 030803 0.25 圆形、无刻痕 格列吡嗪 广州华南 040201 5 圆形、无刻痕 丙戊酸钠 江苏恒瑞 0302172 200 凸圆形、无刻痕糖衣片 华法林 上海九福 031102 2、5 凸圆形、无刻痕糖衣片 多塞平 上海三维 200304C03 凸圆形、无刻痕糖衣片 阿米替林常州四药 KB9659 凸圆形、无刻痕糖衣片 1.2 方法 将上述16种需要分劈的药物由同一检测人员用同一天平对其分别称重,得到每种药片的整片质量,然后将该值除以2便得到了分劈片的理论质量(TW),由同一药师用剪刀将药片对半分劈,用天平逐个称量,每种分劈药片重复次数以分劈成40个半片为准,分劈时不成两半,有碎片不能给患者使用的弃之。用 Excel 计算出分劈片的理论质量(TW)的均值和 SD及实测质量(FW)的均值和 SD。为了测评质量变异,要对3个指标进行比较。A.将分劈片实测质量(FW)的均值和SD 同其理论质量(TW)的均值和SD相比较。B.将每个单独的分劈片实测质量同该药的实测质量均值相比较。C.将每个单独的分劈片实测质量同该药的理论
确定


还剩1页未读,是否继续阅读?
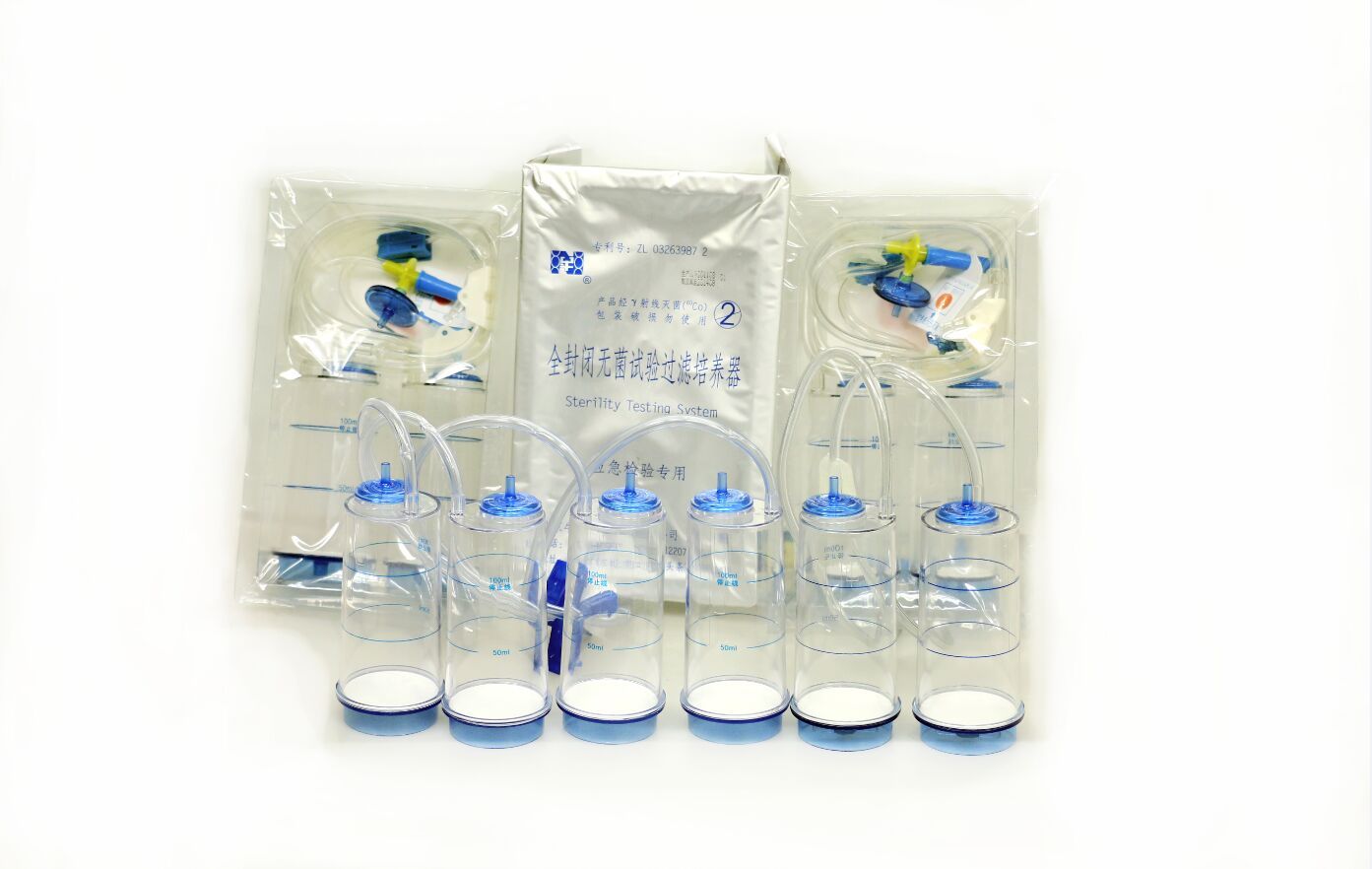
浙江泰林生物技术股份有限公司为您提供《复方紫草油中无菌检查检测方案(集菌仪)》,该方案主要用于中药制剂中微生物相关及生化特性检测,参考标准--,《复方紫草油中无菌检查检测方案(集菌仪)》用到的仪器有集菌仪智能型HTY-601
推荐专场
该厂商其他方案
更多