
方案详情
文
建立了超高压液相色谱鄄静电场轨道离子阱质谱系统对渔用投入品中可能造成风险隐患的禁限用药物的快速筛查与定量技术。以水(含1% 甲酸)鄄乙腈(1颐9, V / V)溶液进行提取,通过稀释降低基质效应,在Accucore RP鄄MS 色谱柱(100 mm 伊2. 1 mm, 2. 6 滋m)上,以水(含0. 1%甲酸)和乙腈(含0. 1% 甲酸)溶液为流动相,利用梯度洗脱、HESI 离子化,Full鄄scan ddMS2 (TopN)扫描模式进行数据采集,通过与预先建立好的药物标准品质谱、色谱数据库进行比对分析,实现了53 种禁限用药同时筛查确证与定量分析。各药物最低检出浓度均低于10 ng/ mL,在0. 01 ~1. 0 滋g/ mL 范围内,各药物的线性相关系数均大于0. 98,根据实际测定结果设定对渔药及渔用饲料中筛查药物的检出限分别为0. 5 和5. 0 mg/ L,对渔药及渔用饲料基质添加10 和100 mg/ kg 的各筛查成分,定量回收率均高于50%,相对标准偏差均小于15%。将本方法用于农业部渔用投入品质量安全隐患排查项目中,共筛查68 个样品,其中在29 个渔用兽药样品中筛查出15 种说明书中未标明成分。
方案详情

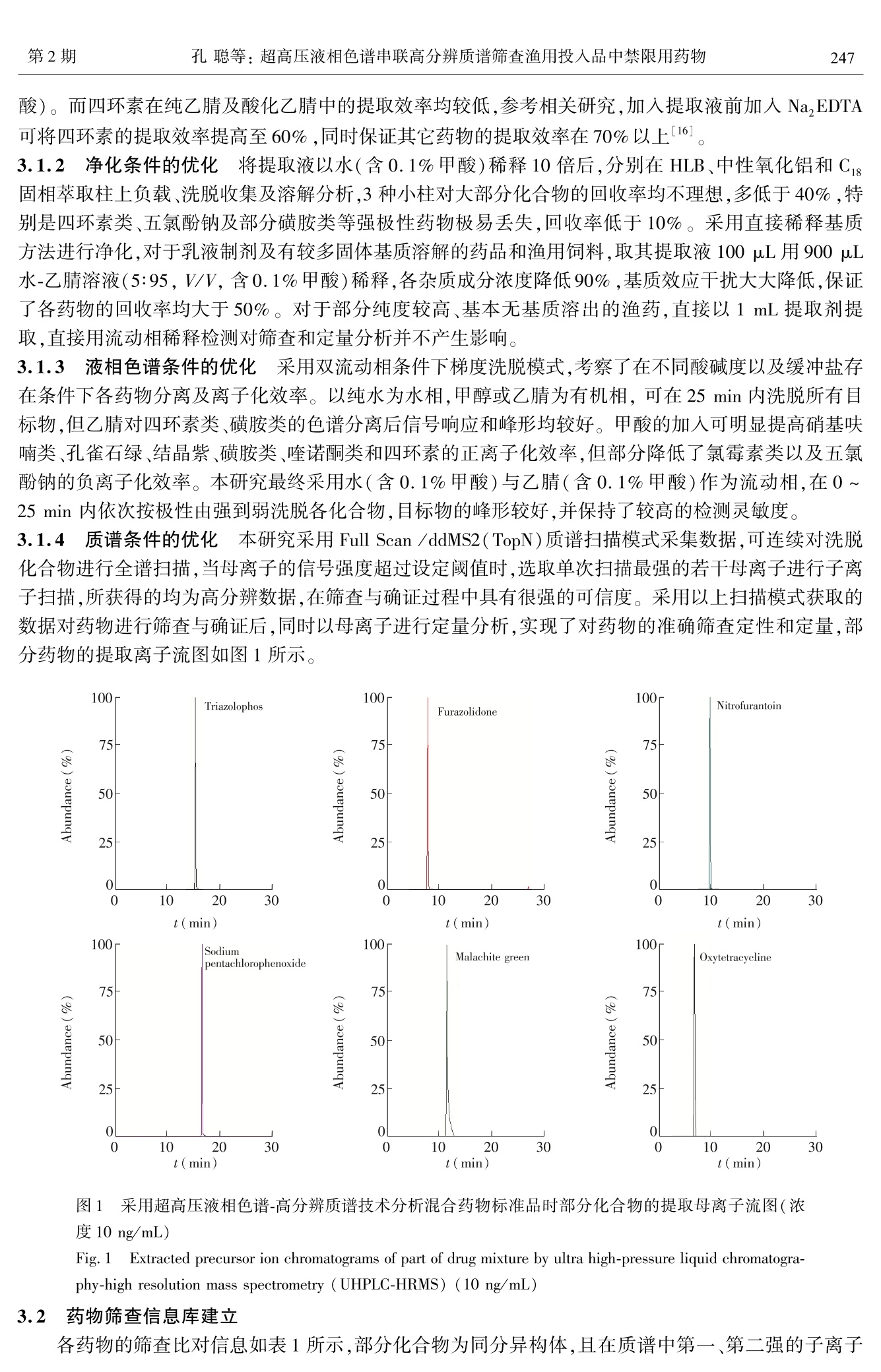
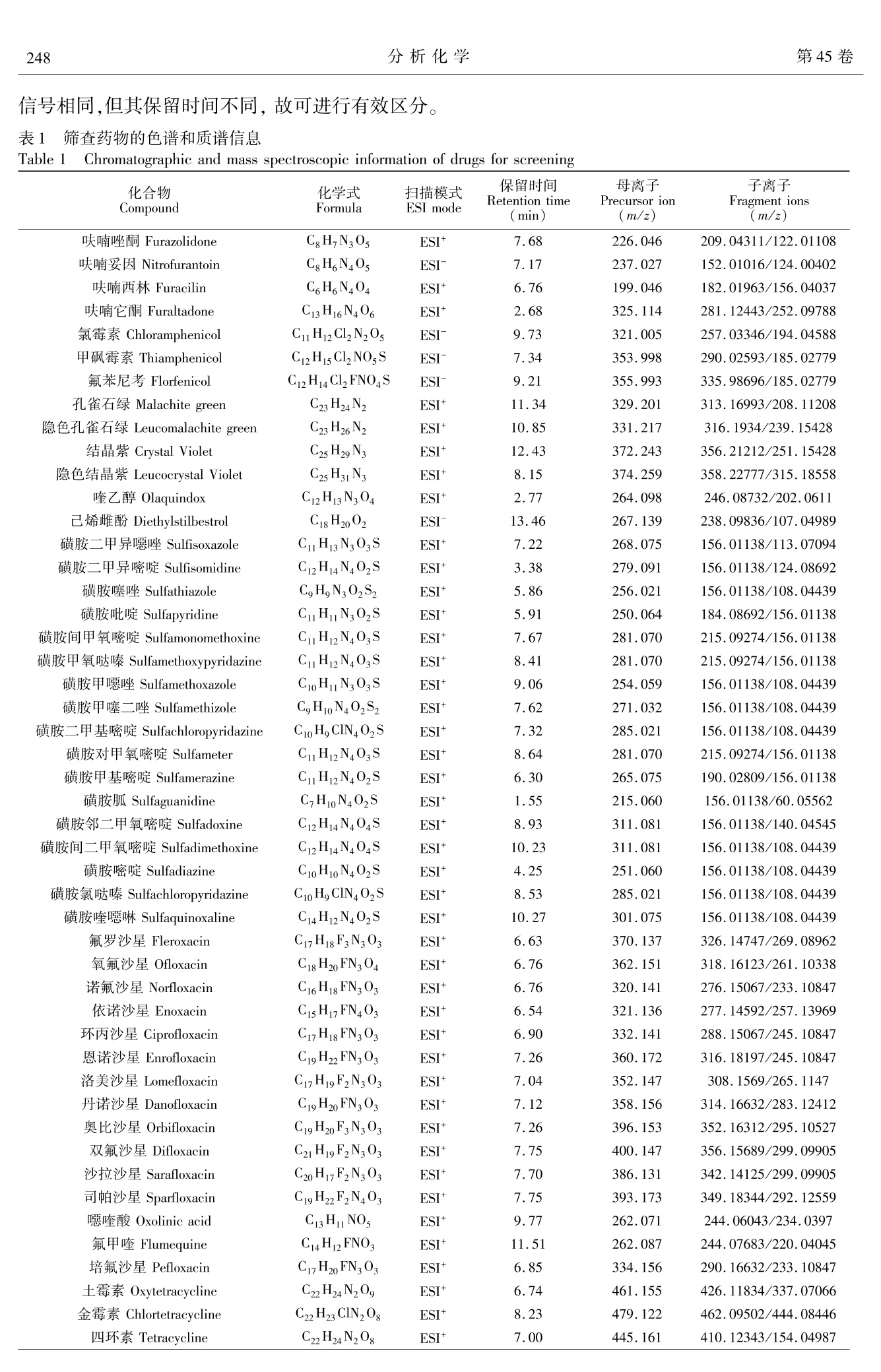
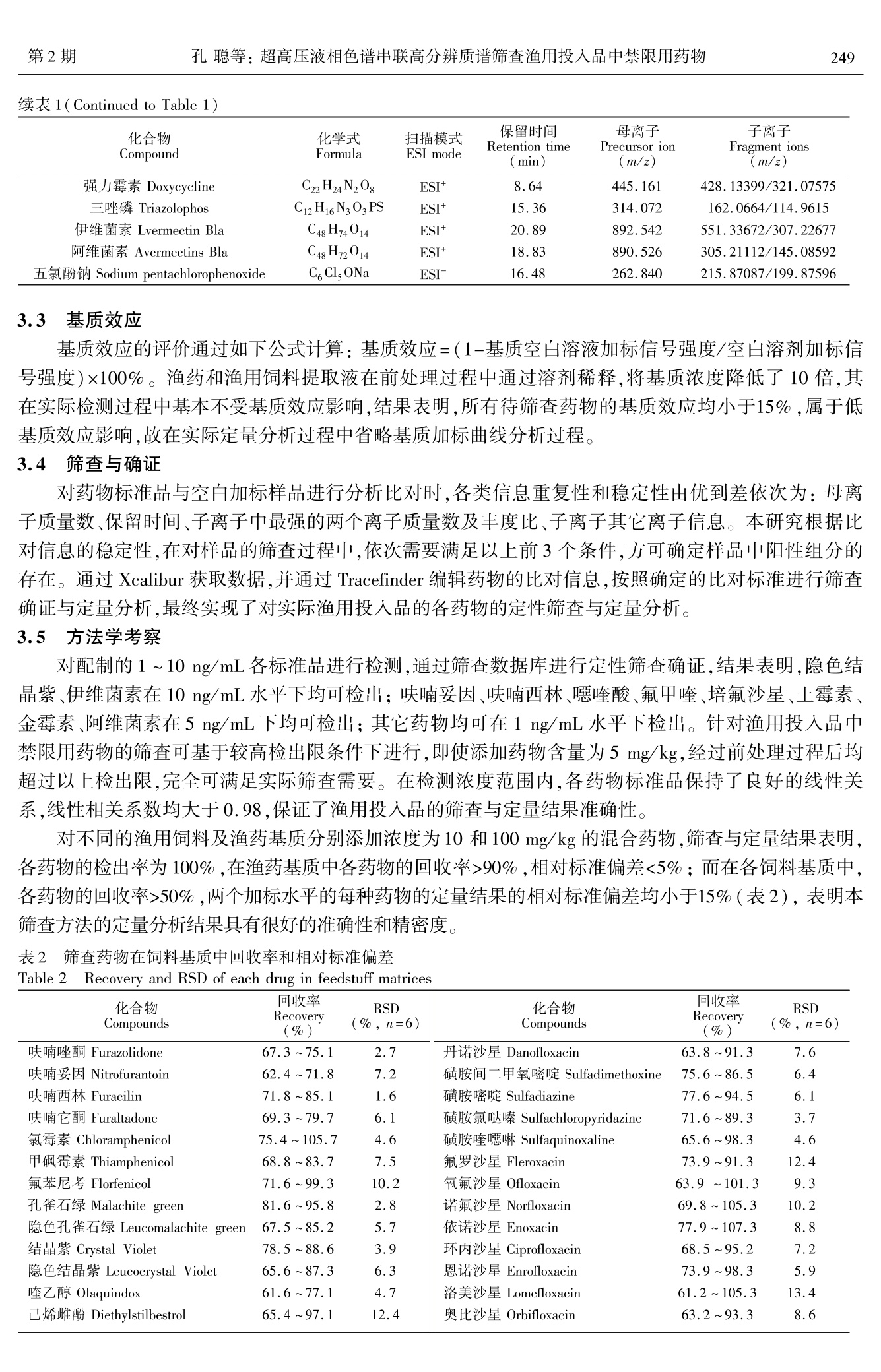
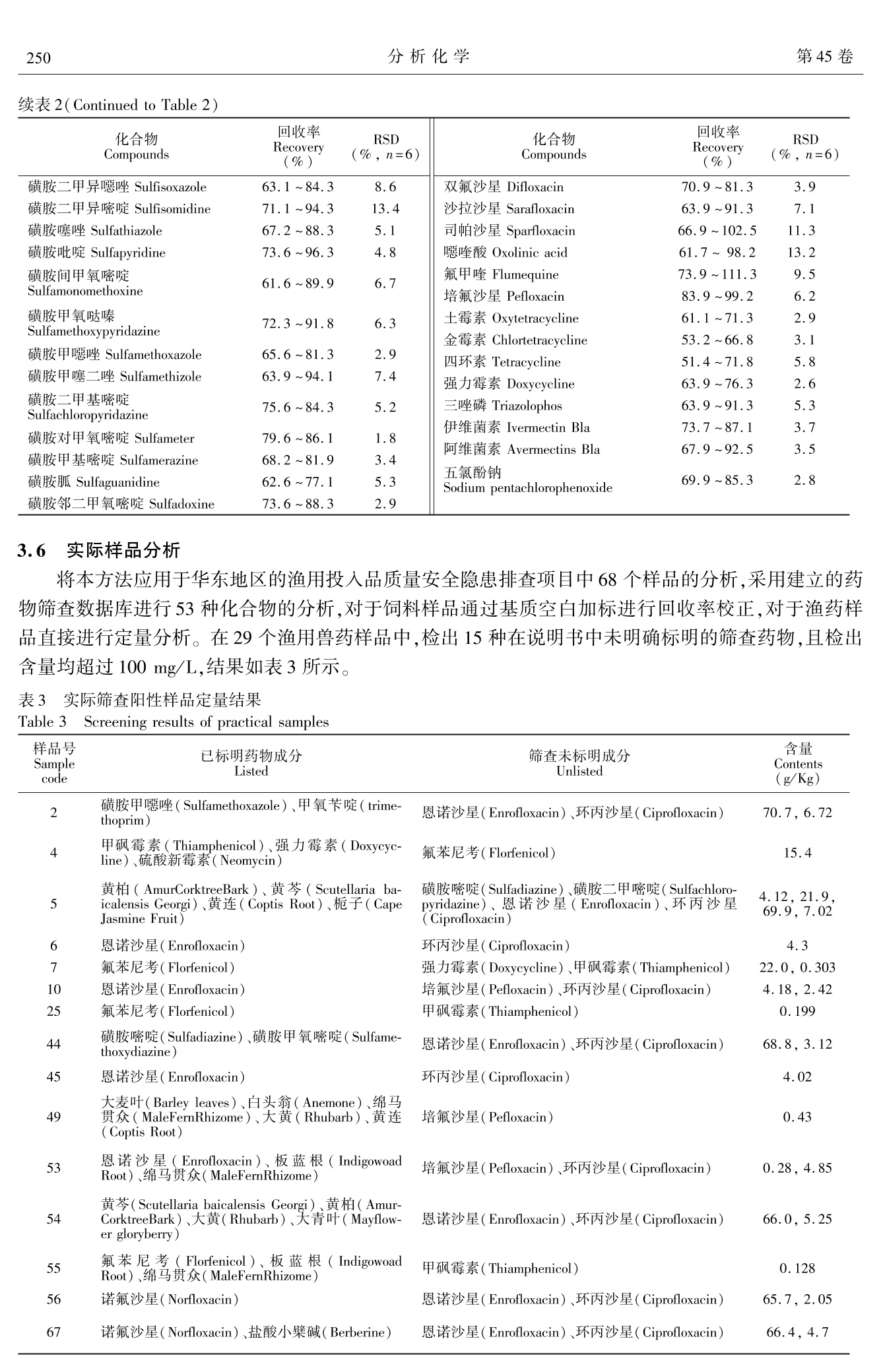
分析化学(FENXI HUAXUE) 研究报告Chinese Journal of Analytical Chemistry第45卷2017年2月第2期245~252 分析化学第45卷246 DOI:10.11895/j.issn.0253-3820.160653 超高压液相色谱串联高分辨质谱筛查渔用投入品中禁限用药物 孔聪1 周哲 汪洋 黄原飞 沈晓盛 黄冬梅 蔡友琼 于慧娟*1 (东海水产研究所水产品质量安全与加工实验室,上海200090)2(赛默飞世尔科技(中国)有限公司,上海201206) 摘 要 建立了超高压液相色谱-静电场轨道离子阱质谱系统对渔用投入品中可能造成风险隐患的禁限用药物的快速筛查与定量技术。以水(含1%甲酸)-乙腈(1:9,V/V)溶液进行提取,通过稀释降低基质效应,在Accucore RP-MS 色谱柱(100 mm×2.1 mm,2.6 um)上,以水(含0.1%甲酸)和乙腈(含0.1%甲酸)溶液为流动相,利用梯度洗脱、HESI离子化,Full-scan ddMS2 (TopN)扫描模式进行数据采集,通过与预先建立好的药物标准品质谱、色谱数据库进行比对分析,实现了53种禁限用药同时筛查确证与定量分析。各药物最低检出浓度均低于10 ng/mL,在0.01~1.0 ug/mL 范围内,各药物的线性相关系数均大于0.98,根据实际测定结果设定对渔药及渔用饲料中筛查药物的检出限分别为0.5和5.0mg/L,对渔药及渔用饲料基质添加10 和100 mg/kg 的各筛查成分,定量回收率均高于50%,相对标准偏差均小于15%。将本方法用于农业部渔用投入品质量安全隐患排查项目中,共筛查68个样品,其中在29个渔用兽药样品中筛查出15种说明书中未标明成分。 关键词 渔用投入品;筛查;高分辨质谱 1 引言 我国水产养殖产量占全世界总量70%左右,是渔用投入品(包括渔药与渔用饲料)生产与消费大国。渔用投入品中添加违禁药物将导致水体污染、水产品违禁药物残留,并通过食物链富集转移到人体中,危害人体健康2。在我国,存在渔用投入品中添加禁用或限用药物的不规范生产和使用现象,导致其在水产品中残留超标,影响我国养殖水产品质量安全,有必要对渔用投入品中禁限用药物进行检测,以确保投入品的安全使用13] 目前,渔用投入品中禁限用药物的检测主要采用液相色谱法4法液相色谱-串联质谱法151气相色谱-串联质谱法161酶联免疫吸附分析法7等。液相色谱-三重四极杆质谱联用技术具有检出限低、准确度高和重现性好等特点,在渔用投入品检测中应用最为普遍[8]。但由于渔用投入品理化性质差别较大,且三重四极杆质谱仪质量精密度较低,单次检测较多种类的化合物相互干扰较大,通常以结构类似的同族药物或单一药物来开发相应的方法91,在药物筛查中需建立多种检测方法,且对非检项目的筛查能力不足,造成检测资源浪费,通过高效的多组分同时筛查和定性技术可解生该问题110,111。 基于静电场轨道离子阱的超高分辨率质谱技术为多组分目标化合物分析提供了新的研究方向12]静电场轨道离子阱质谱系统与色谱分离技术串联,可在一次检测过程中对数百种化合物进行分析13。该质谱可进行基于母离子强度猝发的子离子扫描模式,可实现母离子全扫描模式下对目标化合物进行选择性子离子扫描,同时实现筛查与确证功能14,151。 根据历年中国农业部办公厅渔用投入品质量安全隐患排查计划,本研究针对渔用投入品中可能造成的风险隐患的各种禁限用药物成分,利用超高压液相色谱-静电场轨道离子阱质谱系统,对禁限用药物标准品在统一的参数下进行分析,建立药物色谱质谱信息库,开发禁限用药物筛查与定性确证方法,成功用于对渔用投入品的隐患排查,为我国渔用投入品安全隐患的有效监控提供了新技术。 ( 2016-09-03收稿;2016-12-05接受 ) ( 本文系上海市农业科学委员会(沪农科推字(2016)第1-4-1号)和中央级公益性科研院所基本科研业务费专项资金(中国水产科学研究院东海水产研究所)(No.2014T05)、上海市科学技术委员会扬帆人才计划项目(No.14YF1408100)资助。 ) ( * E-mail: xdyh-7@163. com ) 2 实验部分 2.1 仪器与试剂 Ultimate 3000 超高压液相色谱-Q-Exactive 静电场轨道离子阱质谱联用系统(附带 Xcalibur 及Tracefinder 操作与分析软件,美国 Thermo Fisher 公司); N-EVAP 112 氮吹浓缩仪(美国 Organomation 公司);涡旋搅拌器(德国IKA VOTEX X3); CL6R 离心机(湘仪离心机仪器有限公司);16RXII高速冷冻离心机(日本HITACHI CF公司); Milli-Q 超纯水机(美国 Millipore 公司); PL602-L电子天平(Mettler-Toledo 公司);BT 125D 精密天平( Sartorius 公司); KQ-300E 超声波提取仪(昆山市超声仪器有限公司)。Thermo Accucore RP-MS 色谱分离柱(100 mm×2.1 mm,2.6 pum, 美国 Thermo 公司)。 53种风险排查物质标准品(见表1)均购于 Dr. Ehrenstofer GmbH公司。乙腈、甲醇、乙酸乙酯、丙酮、正己烷、二氯甲烷(色谱纯,Fisher Scientific 公司);二甲基亚砜、冰醋酸、乙二胺四乙酸二钠(分析纯,国药集团化学试剂有限公司);乙酸铵(HPLC 级,Fluka 公司);甲酸( ACS 纯,美国 Sigma 公司);实验用水为超纯水。 2.2 实验方法 2.2.1 溶液配制 称取各药物标准品5 mg 左右,以甲醇溶解并定容至50 mL,不易溶解药品可先加入1 mL甲酸或二甲基亚砜溶解,继续配制成100 ug/mL 左右的单标储备液,-42℃下避光保存。 混合标准中间液:按照各药物的分类,吸取适量各单标储备液,使其质量达到25 pg,用含甲醇-水(1:1,V/V,含1%甲酸)配制成1 ug/mL 混合标准工作液,于-42℃下避光保存3个月。 2.2.2 样品提取方法 渔药:准确确取各渔药500 mg(液体药品以移液枪量取500 uL),以乙腈(含1%甲酸)25 mL 充分溶解,8000 r/min 离心 30 min,取上清液待用。 渔用饲料:将渔用饲料充分混匀均质,称取样品(5.00±0.05)g于50mL 离心管中,加入0.1 g乙二胺四乙酸二钠(Na,EDTA)以及水-乙腈溶液(1:9,V/V,含1%甲酸)提取剂25 mL,混合,常温涡旋振荡提取5 min,超声溶解 20 min, 8000 r/min 离心30 min,取上清液待用。 2.2.3 色谱分析条件 Accucore RP-MS色谱柱(100 mm ×2. 1 mm, 2.6 pm);流速:0.3mL/min;柱温:30℃;进样量:20pL;流动相A为水(含0.1%甲酸),流动相B为乙腈(含0.1%甲酸);洗脱梯度:0~3.0 min,5% B; 3.0~22.0 min,5%~100%, B;22.0~25.0 min,100%B;25.0~25.1 min,100%~5%B;25.1~30.0 min,5%B。 2.2.4 质谱分析条件 HESI 离子源,喷雾电压:3200V(+),2800V(-);鞘气:40 arb;辅气:10arb;吹扫气:1 arb;气体加热温度:350℃;离子传输管温度:325℃;质谱数据获取模式: Full-scan ddMS2(TopN)扫描模式。 2.2.5 定性筛查信息库、筛查确证、定量方法 收集整理各筛查药物分子式,以获知其分子量、分子离子峰、质荷比等信息,在优化的色谱和质谱检测条件下,获得以100 ng/mL 药物标准品的色谱保留时间与母离子和子离子信息,在 Tracefinder 中创建各药物的筛查比对信息库。对处理好的待筛查样品采用Full-scan ddMS2 (TopN)质谱采集方法上机分析,通过已建立好的各药物质谱数据信息库对待筛查样品的数据进行比对筛查、确证。以同样的方法对 10,50,100,500和1000 ng/mL 浓度的混合标准工作液进行分析,通过 Tracefinder 对定性筛查出的阳性药物选择母离子进行定量分析。 3 结果与讨论 3.1 实验条件的优化 3.1.1 提取剂的选择 渔药属于纯度较高的药品,杂质较少,采用合适的溶剂直接溶解即可获得较高的提取效率。而对于渔用饲料,考虑采用混合提取剂进行其中药物的提取。由于磺胺类、喹诺酮类在酸性条件下更容易被溶解提取,五氯酚钠在酸性条件下变为五氯酚,从而可溶于有机溶剂,其它药物(孔雀石绿、结晶紫、硝基呋喃类、喹乙醇己烯雌酚、阿维菌素类、氯霉素类等)易溶于乙腈及其酸性溶液中,而三唑磷在酸碱介质中易水解,故提取剂酸度不宜过高,因而采用水-乙腈溶液(1:9,V/V,1%甲 酸)。而四环素在纯乙腈及酸化乙腈中的提取效率均较低,参考相关研究,加入提取液前加入 Na, EDTA可将四环素的提取效率提高至60%,同时保证其它药物的提取效率在70%以上[16]。 3.1.2 净化条件的优化 将提取液以水(含0.1%甲酸)稀释10倍后,分别在 HLB、中性氧化铝和C 固相萃取柱上负载、洗脱收集及溶解分析,3种小柱对大部分化合物的回收率均不理想,多低于40%,特别是四环素类、五氯酚钠及部分磺胺类等强极性药物极易丢失,回收率低于10%。采用直接稀释基质方法进行净化,对于乳液制剂及有较多固体基质溶解的药品和渔用饲料,取其提取液 100 pL用900pL水-乙腈溶液(5:95,V/V,含0.1%甲酸)各释,各杂质成分浓度降低90%,基质效应干扰大大降低,保证了各药物的回收率均大于50%。对于部分纯度较高、基本无基质溶出的渔药,直接以1mL提取剂提取,直接用流动相稀释检测对筛查和定量分析并不产生影响。 3.1.3 液相色谱条件的优化 采用双流动相条件下梯度洗脱模式,考察了在不同酸碱度以及缓冲盐存在条件下各药物分离及离子化效率。以纯水为水相,甲醇或乙腈为有机相,可在25 min 内洗脱所有目标物,但乙腈对四环素类、磺胺类的色谱分离后信号响应和峰形均较好。甲酸的加入可明显提高硝基呋喃类、孔雀石绿、结晶紫、磺胺类、诺诺酮类和四环素的正离子化效率,但部分降低了氯霉素类以及五氯酚钠的负离子化效率。本研究最终采用水(含0.1%甲酸)与乙腈(含0.1%甲酸)作为流动相,在0~25 min 内依次按极性由强到弱洗脱各化合物,目标物的峰形较好,并保持了较高的检测灵敏度。 3.1.4 质谱条件的优化 本研究采用 Full Scan /ddMS2(TopN)质谱扫描模式采集数据,可连续对洗脱化合物进行全谱扫描,当母离子的信号强度超过设定阈值时,选取单次扫描最强的若干母离子进行子离子扫描,所获得的均为高分辨数据,在筛查与确证过程中具有很强的可信度。采用以上扫描模式获取的数据对药物进行筛查与确证后,同时以母离子进行定量分析,实现了对药物的准确筛查定性和定量,部分药物的提取离子流图如图1所示。 图1 采用超高压液相色谱-高分辨质谱技术分析混合药物标准品时部分化合物的提取母离子流图(浓度 10 ng/mL) Fig.1 Extracted precursor ion chromatograms of part of drug mixture by ultra high-pressure liquid chromatogra-phy-high resolution mass spectrometry (UHPLC-HRMS)(10 ng/mL) 3.2 药物筛查信息库建立 各药物的筛查比对信息如表1所示,部分化合物为同分异构体,且在质谱中第一、第二强的子离子 信号相同,但其保留时间不同,故可进行有效区分。 表1筛查药物的色谱和质谱信息Table 1 Chromatographic and mass spectroscopic information of drugs for screening 化合物 化学式 扫描模式 保留时间 母离子 子离子 Compound Formula ESI mode Retention time (min) Precursor ion (m/z) Fragment ions (m/z) 强力霉素 Doxycycline C22H24N20: ESI+ 8.64 445.161 428.13399/321.07575 三唑磷 Triazolophos C12H16N30,PS ESI* 15.36 314.072 162.0664/114.9615 伊维菌素 Lvermectin Bla C48H74014 ESI+ 20.89 892.542 551.33672/307.22677 阿维菌素 Avermectins Bla C48H72014 ESI+ 18.83 890.526 305.21112/145.08592 五氯酚钠 Sodium pentachlorophenoxide C6CI,ONa ESI 16.48 262.840 215.87087/199.87596 3.3 基质效应 基质效应的评价通过如下公式计算:基质效应=(1-基质空白溶液加标信号强度/空白溶剂加标信号强度)×100%。渔药和渔用饲料提取液在前处理过程中通过溶剂稀释,将基质浓度降低了10倍,其在实际检测过程中基本不受基质效应影响,结果表明,所有待筛查药物的基质效应均小于15%,属于低基质效应影响,故在实际定量分析过程中省略基质加标曲线分析过程。 3.4 筛查与确证 对药物标准品与空白加标样品进行分析比对时,各类信息重复性和稳定性由优到差依次为:母离子质量数、保留时间、子离子中最强的两个离子质量数及丰度比、子离子其它离子信息。本研究根据比对信息的稳定性,在对样品的筛查过程中,依次需要满足以上前3个条件,方可确定样品中阳性组分的存在。通过 Xcalibur 获取数据,并通过 Tracefinder 编辑药物的比对信息,按照确定的比对标准进行筛查确证与定量分析,最终实现了对实际渔用投入品的各药物的定性筛查与定定分析。 3.55方法学考察 对配制的1~10 ng/mL 各标准品进行检测,通过筛查数据库进行定性筛查确证,结果表明,隐色结晶紫、伊维菌素在10 ng/mL 水平下均可检出;呋喃妥因、呋喃西林、噁喹酸、氟甲喹、培氟沙星、土霉素、金霉素、阿维菌素在5 ng/mL 下均可检出;其它药物均可在1 ng/mL 水平下检出。针对渔用投入品中禁限用药物的筛查可基于较高检出限条件下进行,即使添加药物含量为5 mg/kg,经过前处理过程后均超过以上检出限,完全可满足实际筛查需要。在检测浓度范围内,各药物标准品保持了良好的线性关系,线性相关系数均大于0.98,保证了渔用投入品的筛查与定量结果准确性。 对不同的渔用饲料及渔药基质分别添加浓度为10和100 mg/kg的混合药物,筛查与定量结果表明,各药物的检出率为100%,在渔药基质中各药物的回收率>90%,相对标准偏差<5%;而在各饲料基质中,各药物的回收率>50%,两个加标水平的每种药物的定量结果的相对标准偏差均小于15%(表2),表明本筛查方法的定量分析结果具有很好的准确性和精密度。 表2 筛查药物在饲料基质中回收率和相对标准偏差 Table 2 Recovery and RSD of each drug in feedstuff matrices 化合物 回收率 RSD 化合物 回收率 RSD Compounds Recovery(%) (%,n=6) Compounds Recovery (%) (%,n=6) 呋喃唑酮 Furazolidone 67.3~75.1 2.7 丹诺沙星 Danofloxacin 63.8~91.3 7.6 呋喃妥因 Nitrofurantoin 62.4~71.8 7.2 磺胺间二甲氧嘧啶 Sulfadimethoxine 75.6~86.5 6.4 呋喃西林 Furacilin 71.8~85.1 1.6 磺胺嘧安 Sulfadiazine 77.6~94.5 6.1 呋喃它酮 Furaltadone 69.3~79.7 6.1 磺胺氯哒嗪 Sulfachloropyridazine 71.6~89.3 3.7 氯霉素 Chloramphenicol 75.4~105.7 4.6 磺胺喹啉 Sulfaquinoxaline 65.6~98.3 4.6 甲砜霉素 Thiamphenicol 68.8~83.7 7.5 氟罗沙星 Fleroxacin 73.9~91.3 12.4 氟苯尼考 Florfenicol 71.6~99.3 10.2 氧氟沙星 Ofloxacin 63.9~101.3 9.3 孔雀石绿Malachite green 81.6~95.8 2.8 诺氟沙星 Norfloxacin 69.8~105.3 10.2 隐色孔雀石绿 Leucomalachite green 67.5~85.2 5.7 依诺沙星 Enoxacin 77.9~107.3 8.8 结晶紫 Crystal Violet 78.5~88.6 3.9 环丙沙星 Ciprofloxacin 68.5~95.2 7.2 隐色结晶紫 Leucocrystal Violet 65.6~87.3 6.3 恩诺沙星 Enrofloxacin 73.9~98.3 5.9 喹乙醇 Olaquindox 61.6~77.1 4.7 洛美沙星 Lomefloxacin 61.2~105.3 13.4 己烯雌酚 Diethylstilbestrol 65.4~97.1 12.4 奥比沙星 Orbifloxacin 63.2~93.3 8.6 续表 2( Continued to Table 2) 化合物 Compounds 回收率 RSD 化合物 回收率 RSD Recovery(%) (%,n=6) Compounds Recovery(%) (%,n=6) 磺胺二甲异噁唑 Sulfisoxazole 63.1~84.3 8.6 双氟沙星 Difloxacin 70.9~81.3 3.9 磺胺二甲异嘧啶 Sulfisomidine 71.1~94.3 13.4 沙拉沙星 Sarafloxacin 63.9~91.3 7.1 磺胺噻唑 Sulfathiazole 67.2~88.3 5.1 司帕沙星 Sparfloxacin 66.9~102.5 11.3 磺胺吡啶 Sulfapyridine 73.6~96.3 4.8 噁喹酸 Oxolinic acid 61.7~98.2 13.2 磺胺间甲氧嘧啶 61.6~89.9 6.7 氟甲喹 Flumequine 73.9~111.3 9.5 Sulfamonomethoxine 培氟沙星 Pefloxacin 83.9~99.2 6.2 磺胺甲氧哒嗪 72.3~91.8 6.3 土霉素 Oxytetracycline 61.1~71.3 2.9 Sulfamethoxypyridazine 金霉素 Chlortetracycline 53.2~66.8 3.1 磺黄甲噁唑 Sulfamethoxazole 65.6~81.3 2.9 四环素 Tetracycline 51.4~71.8 5.8 磺黄甲噻二唑 Sulfamethizole 63.9~94.1 7.4 强力霉素 Doxycycline 63.9~76.3 2.6 磺胺二甲基嘧啶 75.6~84.3 5.2 三唑磷 Triazolophos 63.9~91.3 5.3 Sulfachloropyridazine 伊维菌素 Ivermectin Bla 73.7~87.1 3.7 磺胺对甲氧嘧啶 Sulfameter 79.6~86.1 1.8 阿维菌素 Avermectins Bla 67.9~92.5 3.5 磺胺甲基嘧啶 Sulfamerazine 68.2~81.9 3.4 磺胺胍 Sulfaguanidine 62.6~77.1 5.3 五氯酚钠Sodium pentachlorophenoxide 69.9~85.3 2.8 磺胺邻二甲氧嘧啶 Sulfadoxine 73.6~88.3 2.9 3.6:实际样品分析 将本方法应用于华东地区的渔用投入品质量安全隐患排查项目中68个样品的分析,采用建立的药物筛查数据库进行53种化合物的分析,对于饲料样品通过基质空白加标进行回收率校正,对于渔药样品直接进行定量分析。在29个渔用兽药样品中,检出15种在说明书中未明确标明的筛查药物,且检出含量均超过100 mg/L,结果如表3所示。 表3 实际筛查阳性样品定量结果 Table 3SScreening results of practical samples 样品号 已标明药物成分 筛查未标明成分 含量 Sample code Listed Unlisted Contents (g/Kg) 2 磺胺甲噁唑(Sulfamethoxazole)、甲氧苄啶(trime- thoprim) 恩诺沙星(Enrofloxacin)、环丙沙星( Ciprofloxacin) 70.7,6.72 4 甲砜霉素(Thiamphenicol)、强力霉素( Doxycyc- line)硫酸新霉素(Neomycin) 氟苯尼考(Florfenicol) 15.4 5 黄柏(AmurCorktreeBark )、黄芩(Scutellaria ba- 磺胺嘧啶(Sulfadiazine)、磺胺二甲嘧啶(Sulfachloro- 4.12,21.9, icalensis Georgi)、黄连( Coptis Root)、栀子(Cape pyridazine)、恩诺沙星(Enrofloxacin)、环丙沙星 69.9,7.02 Jasmine Fruit) (Ciprofloxacin) 6 恩诺沙星(Enrofloxacin) 环丙沙星(Ciprofloxacin) 4.3 7 氟苯尼考(Florfenicol) 强力霉素(Doxycycline)、甲砜霉素(Thiamphenicol) 22.0, 0.303 10 恩诺沙星(Enrofloxacin) 培氟沙星(Pefloxacin)、环丙沙星(Ciprofloxacin) 4.18,2.42 25 氟苯尼考(Florfenicol) 甲砜霉素(Thiamphenicol) 0.199 44 磺胺嘧啶(Sulfadiazine)、磺胺甲氧嘧啶(Sulfame- thoxydiazine) 恩诺沙星(Enrofloxacin)、环丙沙星(Ciprofloxacin) 68.8,3.12 45 恩诺沙星(Enrofloxacin) 环丙沙星(Ciprofloxacin) 4.02 49 大麦叶(Barley leaves)、白头翁(Anemone)、帛马 贯众(MaleFernRhizome)、大黄(Rhubarb)、黄连 (Coptis Root) 培氟沙星(Pefloxacin) 0.43 53 恩诺沙星( Enrofloxacin)、反蓝根(Indigowoad Root)绵马贯众(MaleFernRhizome) 培氟沙星(Pefloxacin)、环丙沙星( Ciprofloxacin) 0.28,4.85 54 黄芩(Scutellaria baicalensis Georgi)、黄柏(Amur- CorktreeBark)、大黄(Rhubarb)、大青叶(Mayflow- 恩诺沙星(Enrofloxacin)、环丙沙星(Ciprofloxacin) 66.0,5.25 er gloryberry) 55 氟苯苯考(Florfenicol)、板蓝根(Indigowoad Root)、绵马贯众(MaleFernRhizome) 甲砜霉素(Thiamphenicol) 0.128 56 诺氟沙星(Norfloxacin) 恩诺沙星(Enrofloxacin)、环丙沙星(Ciprofloxacin) 65.7,2.05 67 诺氟沙星(Norfloxacin)、盐酸小檗碱(Berberine) 恩诺沙星(Enrofloxacin)、环丙沙星(Ciprofloxacin) 66.4, 4.7 4 结论 本研究针对渔用投入品中可造成风险隐患的禁限用药物成分在投入品中高含量特点,通过简单的提取与稀释净化方法,利用超高压液相色谱串联静电场轨道离子阱质谱系统,对禁限用药物在统一的参数下进行分析,建立药物色谱质谱数据库,开发禁限用药物同时筛查、定性确证与定量方法,成功应用于渔用投入品中禁限用的药品的隐患排查。 ( References ) ( YANG Xian-Le, GUO Wei-Wei, SUN Qi. C h inese Fish. Qual. Stand.,2013,3(4):1 - 6 杨先乐,郭微微,孙琪.中国渔业质量与标准,2013,3(4): 1-6 ) ( 2 YANG X i an-Le, ZHENG Zhong-Lin. J . S h anghai Fish. Univ. , 2007, 16(4):374-380 杨先乐,郑宗林.上海 水 产大学学报,2007,16(4):374-380 ) ( 3 LI Zhao-Xin, LENG K ai-Liang, LI Jian, LI Xiao-Chua n , WANG Wei-Fen. Mar. Fish . Re s . , 2001,22(2):76-80 李兆新,冷凯良,李健,李晓川,王维芬.海洋水产研究,2001,22(2):76-80 ) ( 4 Santos L, Ramos F . Trends Food Sci. Technol. , 2016,52:16 - 30 ) ( 5 Rezk M R, Safa'a M R , Khattab FI, Marzouk H M . J . Chromatogr. B,2015,9 7 8:10 3 -110 ) ( 6 Peng X T , Jiang L, Gong Y, Hu X Z, Peng L J, Feng Y Q. Talanta, 2015, 132: 1 18-125 ) ( 7 Peng J, Kong D , Liu L, S ong S, K uang H, X u C. A n al. Me thods, 2015, 7(12):5204-5209 ) ( 8 GanJ, Lv L, Peng J, Li J, Xiong Z, Chen D, He L. Food C hem., 2016, 207:19 5 -204 ) ( 9 Lu Y, Cheng Z, Liu C, Cao X . Food Ana l . Methods,2016,9(6):1857-1866 ) ( 10 Boix C, Ibánez M, Sancho JV, Leon N, Yusá V, Hernandez F. Food Ch e m.,201 4 ,160:313-320 ) ( 11 Dasenaki M E, Thomaidis N S . Anal. Chim. Acta,2015 , 880: 1 03-121 ) ( 12 LIU Yun, D ING Tao, LIAO Xue-Qing, S HEN C h ong-Yu, J I ANG Shan, LYU Chen, GU I Qi a n-Wen, LI U Ha n , FE I Xi a o-Qing, WU Bin. Chinese J. Ana l . Chem.,2016,44(3):423-429 ) ( 刘芸,丁涛,廖雪晴,沈崇钰,姜珊,吕辰,桂茜雯,柳菡,费晓庆,吴斌.分析化学,2016,44(3):423-429 ) ( 13 Kaklamanos G, Vincent U, von Holst C . J. Chromato g r. A, 20 1 3,1293(7):60-74 ) ( 14 Rajski , del Mar Gomez-Ramos M, F e rnandez-Alba A R. J. Chromatogr. A, 2014, 1360: 119 - 127 ) ( 15 Gomez-Pérez M L, Romero-Gonzalez R, Ma r tinez V JL, Frenich A G . Ta l anta, 20 1 5, 131 : 1- 7 ) ( 16 GUO M e ng-Meng,TA N Zhi-Jun, SU N Xiao-Jie, W U Ha i -Yan, SU N Wei-Hong, XING Li-Hong, LI Zhao-Xin, ZH A I Yu- Xiu. Chinese Fish. Qual. Stand.,2013,3(1):51-58 ) ( 郭萌萌,谭志军,孙晓杰,吴海燕,孙伟红,邢丽红,李兆新,翟毓毓. 中国渔业质量与标准,2013,3(1):51-58 ) Screening of Chemical Drugs in Fishery Inputs by UltrahighPerformance Liquid Chromatography-Orbitrap HighResolution Mass spectroscopy KONG Cong',ZHOU Zhe’, WANG Yang', HUANG Yuan-Fei', SHEN Xiao-Sheng,HUANG Dong-Mei, CAI You-Qiong, YU Hui-Juan*1 (East China Sea Fisheries Research Institute, Chinese Academy of Fishery Sciences, Shanghai 200090, China)(Thermo Fisher Scientific Incorporation, Shanghai 201206, China) Abstract To screen the illegal substances in fishery inputs, we established the database including theprecursor and the daughter ions for these possible components by the quadrupole/orbit-trap mass spectrometer,and the retention time of each drug on the same chromatographic column. And then, the extracted and dilutedsamples were analyzed and the components in the real samples were identified under the same conditions.Chromatographic analysis was performed on an Accucore RP-MS column (100 mm ×2.1 mm,2.6um) using gradient elution with 0. 1% formic acid in water and 0.1% formic acid in acetonitrile as mobile phase. Eluteswere ionized through heatable electrosprayionization (HESI) in both positive and negative modesimultaneously. Data acquisition was conducted by Full-scan ddMS2 (TopN) mode, in which the full massprofile for a continuous precursor ion injection and the fragments of each high abundant precursor of targetedwere acquired with excellent time and mass resolution. Screening was carried out through comparison of theinformation of realsamples with that of standards in the database, which were processed by software(Tracefinder). The Quantification of each component was analyzed based on the precursor ion chromatographyacquired by orbit-trap mass spectroscopy, which showed a good linearity between 0. 01-1 pg/mL, withR>0.98. The method was validated by checking its minimum screening concentration (0.5 mg/L for drugsand 5 mg/L for feedstuffs) and evaluating the recovery after addition of the standard mixture in real samples(>50%, under the addition of 10 and 100 mg/kg). The results for 68 practical samples demonstrated theeffective performance of this method for screening with high-throughput, rapidness and acceptable minimumscreening concentration and accuracy, in which 15 of 29 fishery drug samples were screened out for positivecomponents that were not indicated in their labels. Keywords Fishery drug; Screen; High resolution mass spectroscopy (Received 3 September 2016; accepted 5 December 2016) 北京卓立汉光仪器有限公司荣获科技进步一等奖 近日,教育部科技发展中心正式公布了2016年度高等学校科学研究优秀成果奖(科学技术)的授奖项目结果,今年全部授奖项目为 318项,其中一等奖119 项,二等奖项目193项,青年科学奖9人。 高等学校科学研究优秀成果奖(科学技术)分设自然科学奖、技术发明奖、科技进步奖和青年科学奖。自然科学奖授予在基础研究和应用基础研究中做出重要科学发现的个人和单位;技术发明奖(其中含专利类),授予在运用科学技术知识做出产品、工艺、材料及其系统等重要技术发明的个人和单位;科技进步奖(其中含推广类和科普类)授予在应用推广先进科学技术成果、完成重要科学技术工程、计划、项目等方面做出创造性贡献,或在科学普及中做出重要贡献的个人和单位;青年科学奖授予长期从事基础性科学研究并取得了有一定影响的原创性成果的在校青年教师。高等学校科学研究优秀成果奖(科学技术)面向全国高等院校,每年评审一次。 北京卓立汉光仪器有限公司与中国农业大学、北京农业质量标准与检测技术研究中心、北京御香苑畜牧有限公司、北京绿富隆农业股份有限公司、北京科丰恒业仪器仪表有限公司等单位共同完成的《生鲜农产品品质的无损高通量实时光学检测共性关键技术》项目荣获科技进步一等奖。 同时,恭贺:由北京卓立汉光仪器有限公司和合利科技发展有限公司共同合资成立的四川双利合谱科技有限公司荣获科技进步二等奖! 奖种名称 获奖等级 项目名称/获奖人 全部完成人 全部完成单位/工作单位 科技进步奖 1 生鲜农产品品质的 彭彦昆,韩东海,李永玉,汤修 中国农业大学,北京农业质量标准与检测技 术研究中心,北京卓立汉光仪器有限公司, 无损高通量实时光 映,王冬,黄岚,江发潮,孙明, 北京御香苑畜牧有限公司,北京绿富隆农业 学检测共性关键技 陆安祥,徐杨,王伟,陈兴海, 术 李艳荣,张仲新,韩熹 股份有限公司,北京科丰恒业仪器仪表有限公司 方慧,韩忠,苑严伟,曾新安, 王松磊,刘业林,张洪,刘贵 珊,宋忠祥,赵博,李汴生,成 , 华南理工大学,浙江大学,宁夏大学,中国农 业机械化科学研究院,四川双利合谱科技有限公司,浙江睿洋科技有限公司,湖南唐人 科技进步奖 2 农产品品质波谱快 速无损检测技术与 装备研发及应用 军虎,吴剑 神肉制品有限公司 我国水产养殖产量占全世界总量70% 左右,是渔用投入品(包括渔药与渔用饲料)生产与消费大国[1] 。渔用投入品中添加违禁药物将导致水体污染、水产品违禁药物残留,并通过食物链富集转移到人体中,危害人体健康[2] 。在我国,存在渔用投入品中添加禁用或限用药物的不规范生产和使用现象,导致其在水产品中残留超标,影响我国养殖水产品质量安全,有必要对渔用投入品中禁限用药物进行检测,以确保投入品的安全使用[3] 。
确定




还剩6页未读,是否继续阅读?
赛默飞色谱与质谱为您提供《渔用投入品中禁限用药物检测方案(液相色谱仪)》,该方案主要用于渔业中兽药检测,参考标准--,《渔用投入品中禁限用药物检测方案(液相色谱仪)》用到的仪器有赛默飞 Vanquish™ UHPLC超高效液相色谱系统
推荐专场
该厂商其他方案
更多














