方案详情
文
亚甲基蓝(methylene blue, MB )是一种具有平面结构(结构式见图1)的碱性生物染色剂,在医学临床诊断及化学分析中已有较长的应用历史,可用于亚硝酸盐、磺氨类、氰化物及一氧化碳等中毒的解毒药。电分析化学中常被用作氧化还原指示剂或电子媒介体,其在水溶液中的电化学行为曾被深入地研究[ 1 - 2 ] 。在水溶液中,MB的还原态为无色中性分子,而氧化态MB +为一价阳离
子,由于分子中环平面和氮杂原子上甲基的存在而具有一定的疏水性。水溶液中MB容易形成二聚体,在电极上发生两个连续的1电子转移反应(EE mechanism) [ 1 ] ,其氧化还原电位的峰距ΔEp介于1电子转移反应( 59mV)和2电子转移反应
(2815mV)之间。以MB 为分子探针来研究其他生物大分子已有很多报道[ 3 - 9 ] ,如近年来发现MB对DNA具有插入作用[ 8 - 9 ] ,可被用于抗癌药物的
体外筛选,但对于RNA 的研究目前还没有文献报道。
方案详情

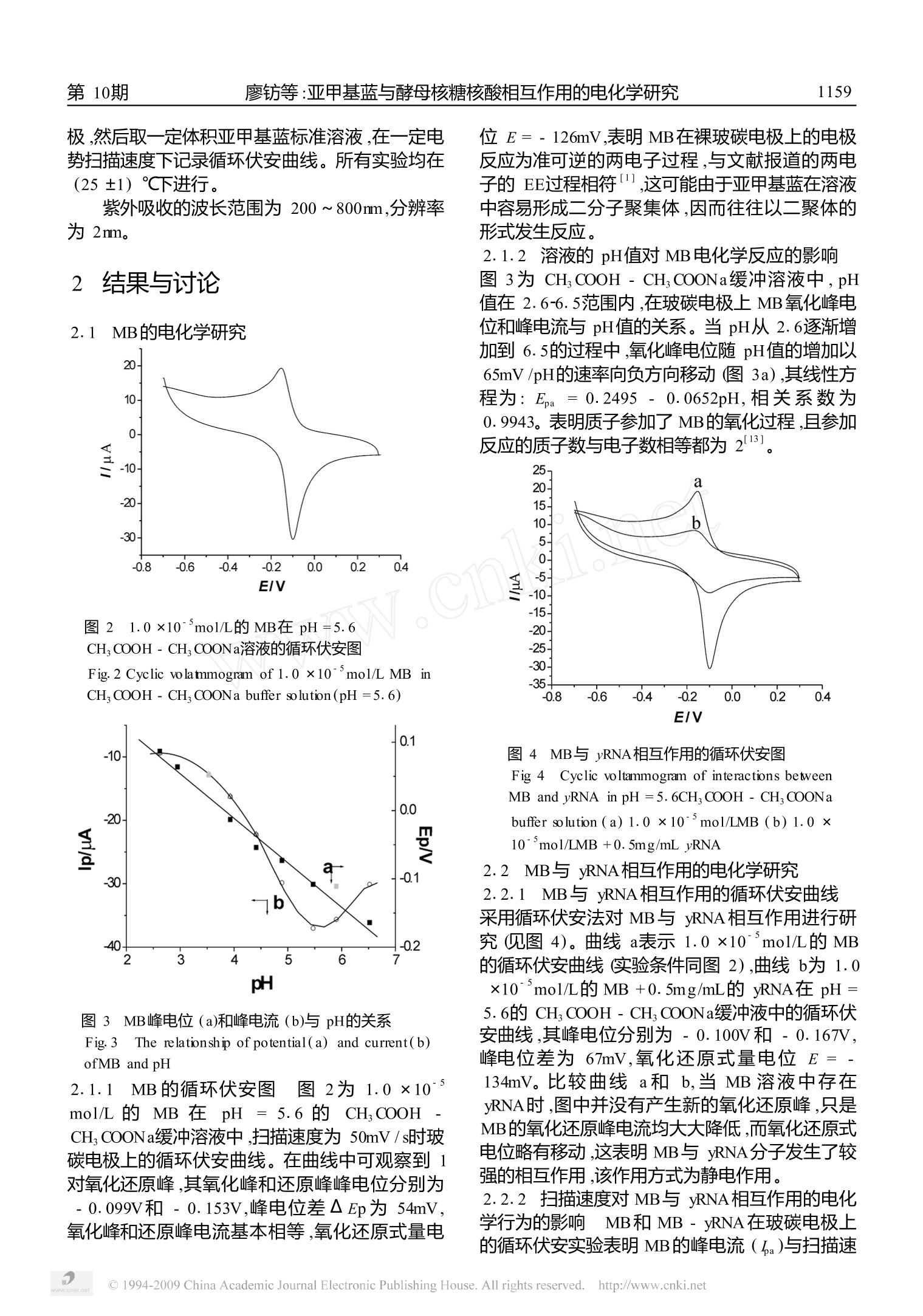
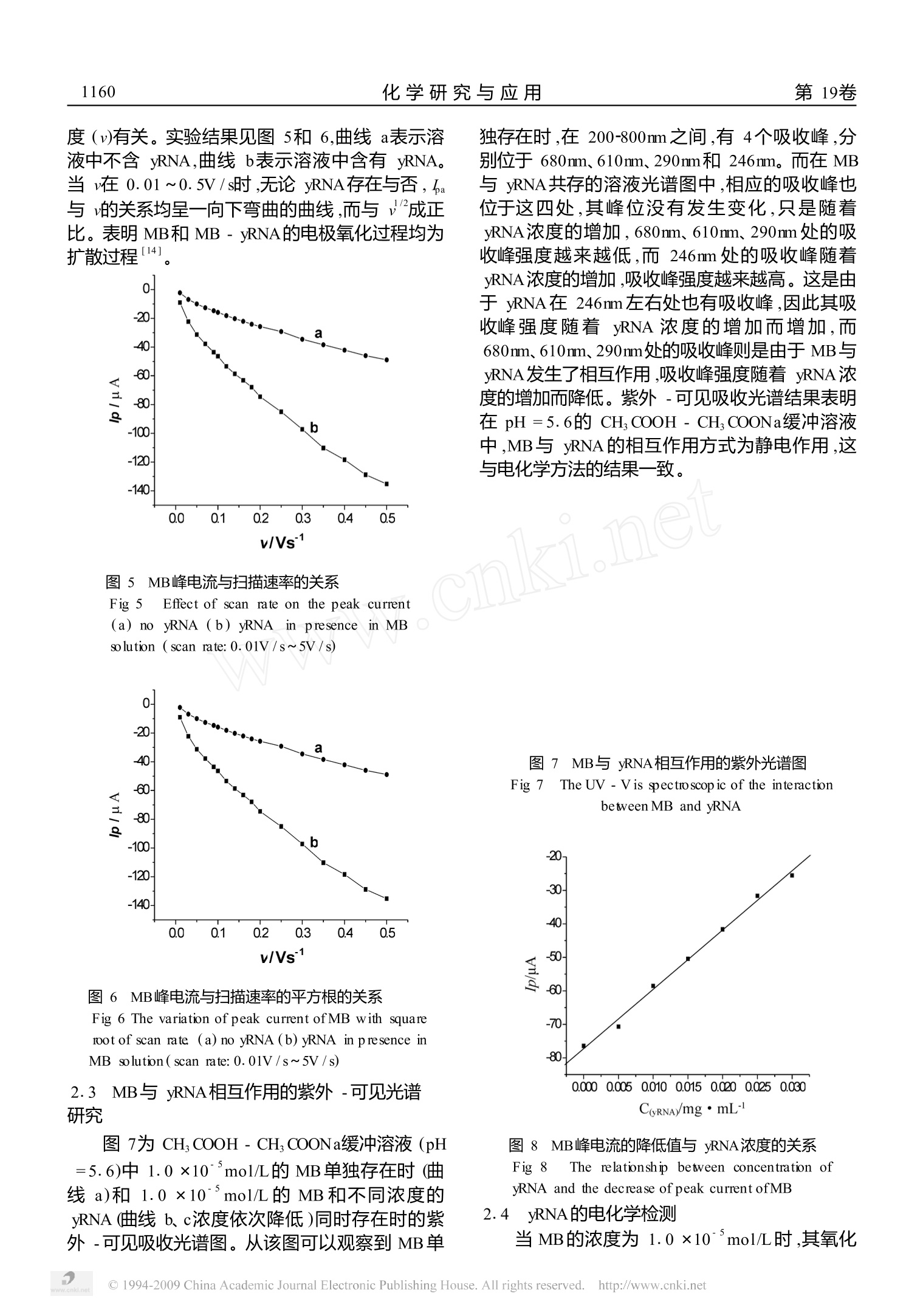
Vol. 19.No. 10Oct.,2007化学研究与应用Chem ical Research and Application第19卷第10期2007年10月 1159廖等:亚甲基蓝与酵母核糖核酸相互作用的电化学研究第10期 文章编号:1004-1656(2007)10-1158-04 亚甲基蓝与酵母核糖核酸相互作用的电化学研究 廖 纺,朱清涛,何晓英,艾 珍,蔡铎昌 (西华师范大学化学化工学院完 四川 南充 637002) 关键词:酵母核糖核酸;亚甲基蓝;循环伏安法;电化学检测 中图分类号:O657 文献标识码:A 亚甲基蓝(methylene blue, MB)是一种具有平面结构(结构式见图1)的碱性生物染色剂,在医学临床诊断及化学分析中已有较长的应用历史,可用于亚硝酸盐、黄氨类、氰化物及一氧化碳等中毒的解毒药。电分析化学中常被用作氧化还原指示剂或电子媒介体,其在水溶液中的电化学行为曾被深入地研究11-21。。在水溶液中,MB的还原态为无色中性分子,而氧化态MB 为一价阳离子,由于分子中环平面和氮杂原子上甲基的存在而具有一定的疏水性。水溶液中 MB容易形成二聚体,在电极上发生两个连续的1电子转移反应(EE mechanism),其氧化还原电位的峰距AEp介于1电子转移反应(59mV)和2电子转移反应(28.5mV)之间。以MB 为分子探针来研究其他生物大分子已有很多报道13-9],如近年来发现MB对DNA具有插入作用[8-9],可被用于抗癌药物的体外筛选,但对于 RNA的研究目前还没有文献报道。 图1 MB分子的结构式 Fig.1 The structure ofMB 核酸是所有生物的基本遗传物质,核酸与靶向小分子的相互作用是核酸研究的重要课题之一,从生物学和临床科学的角度来说研究小分子与核酸的相互作用,对于认识核酸的生物活性以 及药物作用机理有重要意义。近几年来,报道了利用某些染料如乙基紫、灿烂绿、中性红等作为标记物测定核酸10-12]。本文采用循环伏安法和紫外-可见光谱法探讨了亚甲基蓝与酵母核糖核酸(yRNA)的相互作用,建立了一种间接检测 yRNA的电化学方法。 1 实验部分 1.1 仪器与试剂 LK98BⅡ微机电化学分析系统(天津市兰力科化学电子高科技有限公司);紫外-可见分光光度计 (UV2550分光光度计日本岛津);三电极系统:玻碳电极为工作电极,饱和甘汞电极(SCE)为参比电极(以下报道的电位皆相对于此电极),铂片电极为对电极。 酵母核糖核酸(中国科学院生物化学研究所);亚甲基蓝(分析纯),其他试剂均为分析纯;实验用水均为二次蒸馏水。所有的测量溶液均是含1.0 ×10 mol/L的 MB或 1.0 x10 mol/L的MB+不同浓度的 yRNA的 CH,COOH -CH,COONa缓冲溶液。 1.2 实验方法 玻碳电极()为4mm)首先用2000目金相砂纸、0.05umA10;抛光粉抛光成镜面,然后分别在1:1的 HNO3、1:1的 NaOH和丙酮中超声清洗1m in,最后用二次蒸馏水冲洗,红外灯下烘干。 取一定体积识pHI=5.6的 CH,COOH-CH,COONa缓冲溶液通氮除氧10min,电位扫描区间在-1.0V~0.5V之间,用循环伏安法活化电 ( 收稿日期:2006-12-12;修回日期:2007-05-19 ) ( 联系人简介:何晓英(1956-),女,副教授,主要研究方向:电化学及其应用. Email: hexysctc@ yahoo. com. cn ) 极,然后取一定体积亚甲基蓝标准溶液,在一定电势扫描速度下记录循环伏安曲线。所有实验均在(25±1)℃下进行。 紫外吸收的波长范围为200~800mm,分辨率为2mm。 2 结果与讨论 2.1 MB的电化学研究 0.4 图2 1.0 ×10mol/L的 MB在 pH=5.6CH COOH- CH COONa溶液的循环伏安图 Fig.2 Cyclic volatmmogram of 1.0 ×10 mol/L MB inCH, COOH - CH, COONa buffer solution (pH=5.6) 图3 MB峰电位(a)和峰电流(b)与pH的关系 Fig.3 The relationship of potential(a) and current(b)ofMB and pH 2.1.1 MB的循环伏安图 图2为 1.0 ×10'mol/L 的NMB在 H1三=5.6的CH, COOH-CH, COONa缓冲溶液中,扫描速度为50mV/s时玻碳电极上的循环伏安曲线。在曲线中可观察到1对氧化还原峰,其氧化峰和还原峰峰电位分别为-0.099V和 -0.153V,峰电位差差Ep 为 54mV,氧化峰和还原峰电流基本相等,氧化还原式量电 位 E=-126mV,表明MB在裸玻碳电极上的电极反应为准可逆的两电子过程,与文献报道的两电子的EE过程相符,这可能由于亚甲基蓝在溶液中容易形成二分子聚集体,因而往往以二聚体的形式发生反应。 2.1.2 溶液的 pH值对MB电化学反应的影响 图3为 CH, COOH - CH,COONa缓冲溶液中,pH值在2.6-6.5范围内,在玻碳电极上MB氧化峰电位和峰电流与 pH值的关系。当 pH从 2.6逐渐增加到6.5的过程中,氧化峰电位随 pH值的增加以65mV/pH的速率向负方向移动(图3a),其线性方程为: Epaa=0.2495- 0.0652pH,相关系数为0.9943。表明质子参加了 MB的氧化过程,且参加反应的质子数与电子数相等都为2131。 0.4 图4 MB与 yRNA相互作用的循环伏安图 Fig 4 Cyclic voltammogram of interactions between MB and yRNA in pH=5.6CH,COOH- CH, COONabuffer solution(a) 1.0 ×10mol/LMB (b) 1.0 ×10 mol/LMB+0.5mg/mL yRNA 2.2 MB与 yRNA相互作用的电化学研究 2.2.1 MB与yRNA相互作用的循环伏安曲线 采用循环伏安法对 MB与 yRNA相互作用进行研究(见图4)。曲线a表示11.0 x10~mol/L的 MB的循环伏安曲线(实验条件同图2),曲线b为1.0x10mol/L的MB +0.5mg/mL的 yRNA在 pH=5.6的 CH, COOH-CH,COONa缓冲液中的循环伏安曲线,其峰电位电别为 -0.100V和 -0.167V,峰电位差为67mV,氧化还原式量电位E= -134mV。比较曲线a和b,当MB溶液中存在yRNA时,图中并没有产生新的氧化还原峰,只是MB的氧化还原峰电流均大大降低,而氧化还原式电位略有移动,这表明MB与 yRNA分子发生了较强的相互作用,该作用方式为静电作用。 2.2.2 扫描速度对MB与 yRNA相互作用的电化学行为的影响 MB和MB-yRNA在玻碳电极上的循环伏安实验表明 MB的峰电流(a)与扫描速 度(v)有关。实验结果见图5和6,曲线a表示溶液中不含 yRNA,曲线b表示溶液中含有 yRNA。当v在 0.01~0.5V/s时,无论 yRNA存在与否,h与v的关系均呈一向下弯曲的曲线,而与v'成正比。表明MB和MB-yRNA的电极氧化过程均为扩散过程14] 图5 MB峰电流与扫描速率的关系 Fig 5 Effect of scan rate on the peak current(a) no yRNA (b) yRNA in presence in MBsolution (scan rate: 0.01V/s~5V/s) 图6 MB峰电流与扫描速率的平方根的关系 Fig 6 The variation of peak current ofMB with squareroot of scan rate (a) no yRNA (b) yRNA in presence inMB solution ( scan rate:0.01V/s~5V/s) 2.3 MB与 yRNA相互作用的紫外-可见光谱研究 图7为 CH, COOH - CH, COONa缓冲溶液 (pH=5.6)中 1.0×10mol/L的MB单独存在时(曲线 a)和1.0 ×10mol/L的 MB和不同浓度的yRNA(曲线 b、c浓度依次降低)同时存在时的紫外-可见吸收光谱图。从该图可以观察到MB单 独存在时,在200-800mm之间,有4个吸收峰,分别位于 680mm、610nm、290mm和246mm。而在MB与 yRNA共存的液液光谱图中,相应的吸收峰也位于这四处,其峰位没有发生变化,只是随着yRNA浓度的增加,680mm、610nm、290mm处的吸收峰强度越来越低,而246mm处的吸收峰随着yRNA浓度的增加,吸收峰强度越来越高。这是由于 yRNA在 246mm左右处也有吸收峰,因此其吸收峰强度随着yRNA 浓度的增加而增加,而680nm、610mm、290mm处的吸收峰则是由于 MB与yRNA发生了相互作用,吸收峰强度随着yRNA浓度的增加而降低。紫外-可见吸收光谱结果表明在 pH=5.6的 CH, COOH -CH, COONa缓冲溶液中,MB与 yRNA的相互作用方式为静电作用,这与电化学方法的结果一致。 图7 MB与 yRNA相互作用的紫外光谱图 Fig 7 The UV-V is spectro scop ic of the interactionbetweenMB and yRNA 图8 MB 峰电流的降低值与 yRNA浓度的关系 Fig8 The relationship between concentration ofyRNA and the decrease of peak current ofMB 2.4 yRNA的电化学检测 当MB的浓度为1.0 ×10mol/L时,其氧化 峰电流的减小值△与所加入 yRNA的浓度在5.0×10 mg/mL-3.0 ×10 mg/mL范围内呈线性关系,如图8所示,线性回归方程为△为a(uA)=-77.24+1.770 X10 c(mg/mL),线性相关系数为0.9976。 综上所述,亚甲基蓝能够在裸玻碳电极上实现其直接电化学反应,且在裸玻碳电极上具有强的吸附性。电化学和紫外-可见吸收光谱方法的研究都表明,在 pH= 5.6的 CH,COOHH- ( 参考文献: ) ( [1] Zutic V, S v etlicic V , L o vric M , et al. El e ctron tr a nsfer kinetics of an a dsorbed r e dox coup led by double pot e ntial- step c chronocoulometry: methylene b l ue/leucomethyleneblue[ J ]. J . E lectroanal C hem. I nt erfacial E l ectrochen, 1984. 1 77:253-268. ) ( [2]冶保献,张娟,李风菊,等.聚亚甲蓝修饰碳纤维微电极的性质及对多巴胺的电催化测定[J].天津师大学 报(自然科学版),2000,20(4): 10-1 4 . ) ( [3]易平贵,刘俊峰,商志才,等.荧光光谱法研究亚甲基蓝与蛋白质的结合反应[J].光谱学与光谱分析, 2001,21(6):826-828 ) ( [4]赵发琼,曾百肇,庞代文.几种表面活性剂与 DNA的 相目作用[J].化学学报,2006,61(1):22-28. ) ( [5]沈鸿强,尹屹梅,张洪斌.甲基纤维素(MC)疏水作用的 电化学研究[J].化学学报,2005,63(17):16 2 1-1625 ) ( [6]向海艳,陈小明,李松青,等.亚甲基蓝共振光谱散射法测定脱氧核糖核酸[J].分析化学.2000,28(11): 1398-1401. ) ( [7]张旭志,焦奎,徐桂云,等.亚甲基蓝与脱氧腺苷三磷 酸相互作用的电化学研究[J].青岛科技大学学报, 2005,26(5): 3 77-3 8 1. ) ( 8 1 ] P Pinar Kara. , Kagan Keman,Dilsat Ozkan. et a l. ) CH,COONa缓冲溶液中 MB和 MB-yRNA的电极氧化过程的控制步骤为扩散控制过程,且溶液中yRNA的存在不影响MB的电化学行为,MB与yRNA相互作用的方式主要为静电作用,根据这个作用可间接对 yRNA进行定量分析测定,从而建立一种间接检测 yRNA的电分析方法。该试剂以及反应体系均较稳定,方法简单,灵敏度高,结果令人满意。 ( Electrochem ical genosensor for the d etection o f interactionbetween methylene b lue a nd D NA [J ] . E lec trochem is t ry Comm unications, 4(2002) 7 0 53709 ) ( [9] Z hao Guang- Chao , Z hu Jun- J i e, Z h ang Jing-Jie. e t a1. Voltammetric s t udies of t h e i n teraction o f methylene blue with DNA by means ofβ- c yclodextrin[J]. J. Anal..Chin. Acta, 1999, 394: 3 37-344. ) ( [10]李天剑,沈熙熙.基基紫-脱氧核糖核酸共振发光体系的研究及其分析应用[J].高等学校化学学报, 1998, 19(10) : 1570-1 5 73. ) ( [11]苏界殊,陈小明,龙云飞.灿烂绿共振光散射法检测脱氧核糖核酸 [J].分析化学, 2004. 31 (12): 1 534. ) ( [12]NU Shu-yan, ZHANG Shu - sheng, SHI Xin, et al E lectrochemical s tudy o n t h e interacti0n between neutral r e d and DNA[J]. Chen. R e s. Chinese U. 2005, 21(1):2 4 -27. ) ( [ 1 3]B a rd . A . J., John W iley & Sons. E lectrochem ical M ethods[M]. 1980:521~522. ) ( [14]Laviron E J . General ex p ression fo r the linear potentialsweep voltammogram in th e ca s e di f fusionless electrochem icalsystems[J] J .E le c troanal. Che n . Inter f acial Eletrochen . 1979 . 101 : 19~28 ) Electrochem ical study on the interaction betweenm ethylene blue and yea st RNA Liao Fang, Zhu Qing-tao, He Xiao-ying, Ai Zhen,CaiDuo - chang (College of Chem ical Engineering, China West Nommal University, Nanchong, SiChuan, 637002) Abstract: The interaction between methylene blue (MB) and yeast RNA (yRNA) was studied by the cyclic voltammetry. Theinteraction was also testified by the UV- visual absop tion spectrum. The result indicated that the interaction ofMB and yRNA waselectrostatic action in the CH,COOH - CH,COONa buffer solution (pH=5.6). And with the increase of the concentration ofyRNA, the absoiption peak intensity was weaker and weaker. An indirect electroanalytical method for detem ining yRNA wasdeveloped. The m inished peak currents ofMB were proportional to the concentration of yRNA in the range of 5. 0 ×10 mg/mL-3.0X10 mg/mL, and the linear regression coefficient was 0. 9976. Key words:methylene blue; yeast RNA; cyclic voltammetry; electroanalytical chem istry ( (责任编辑 张文华) ) @ China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
确定


还剩2页未读,是否继续阅读?
天津市兰力科化学电子高技术有限公司为您提供《亚甲基蓝与酵母核糖核酸中电化学研究检测方案(电化学工作站)》,该方案主要用于其他中电化学研究检测,参考标准--,《亚甲基蓝与酵母核糖核酸中电化学研究检测方案(电化学工作站)》用到的仪器有天津兰力科电化学工作站LK98BII
推荐专场
相关方案
更多
















