方案详情
文
研究了多壁碳纳米管/纳米二氧化钛- 聚苯胺载铂(CNT/nanoTiO2 - PAn - Pt)复合电极对葡萄糖的电催化氧化作用。以015 mol/L KOH水溶液为底液,采用微分脉冲法在- 015 - 012V电位区间扫描,在- 0133V( vs, SCE)附近产生的氧化电流峰灵敏度高且峰型好,故以此峰为定量峰。葡萄糖浓度在1125 ×10 - 2 ~ 110×10 - 5 mol/L与峰电流呈良好的线性关系,线性相关系数为0199881, 检出限为510 ×10 - 6mol/L。加入0106m mol/L的抗坏血酸或013m mol/L的尿酸(模拟人血成份)均不干扰葡萄糖的测定。该电极对模拟血液中葡萄糖的测定,结果令人满意。
方案详情

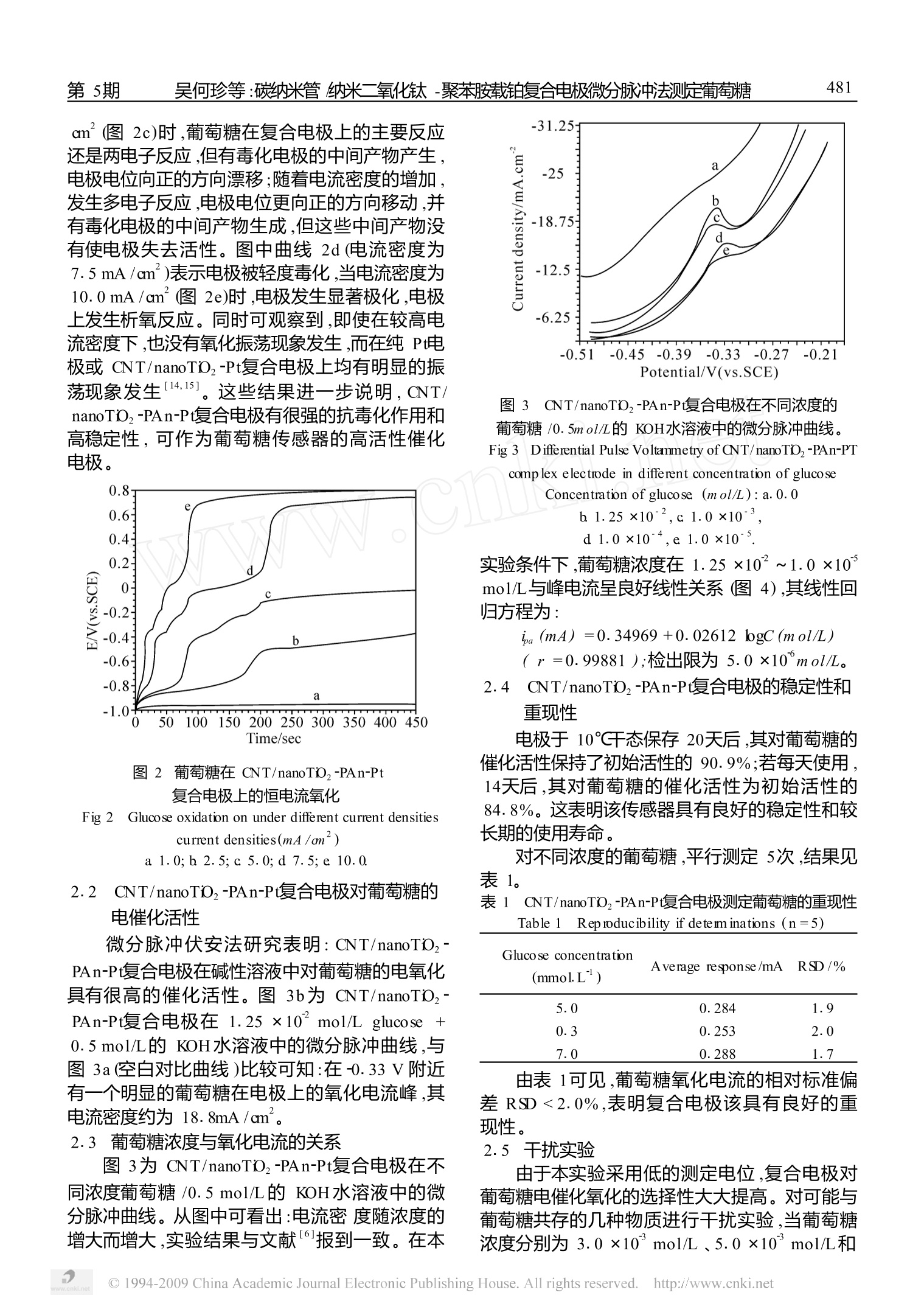
第19卷第5期2007年5月化学研究与应用Chem ical Research and ApplicationVo119,No5May,2007 480化学研究与应用第19卷 碳纳米管/纳米二氧化钛-聚苯胺载铂复合电极微分脉冲法测定葡萄糖 吴何珍,褚道葆",陈忠平23..尹晓娟“ (1.安庆职业技术学院,安徽 安庆 246003: 2.安徽师范大学化学与材料科学学院,安徽 芜湖 241000:3.安徽科技学院理学院,安徽 凤阳 233100) 摘要:研究了多壁碳纳米管/纳米二氧化钛-聚苯胺载铂(CNT/nanoTiO,- PAn- Pt)复合电极对葡萄割的电催化氧化作用。以 0.5 mol/L KOH水溶液为底液,采用微分脉冲法在-0.5-0.2V电位区间扫描,在 -0.33V(vs,SCE)附近产生的氧化电流峰灵敏度高且峰型好,故以此峰为定量峰。葡萄糖浓度在1.25×102~1.0x10mol/L与峰电流呈良好的线性关系,线性相关系数为 0.99881,检出限为5.0 ×10mol/L。加入 0.06m mol/L的抗坏血酸或 0.3m mol/L的尿酸(模拟人血成份)均不干扰葡萄糖的测定。该电极对模拟血液中莆萄糖的测定,结果令人满意。 关键词:碳纳米管/纳米 TO,-PAn膜载 Pt复合电极;葡萄糖;电催化氧化;微分脉冲法 中图分类号:0646 文献标识码:A 目前测试葡萄糖糖浓度的方法主要有三种:显色法、酶电极法和荧光法。Yoshino等人的荧光法采用嵌二萘作为荧光剂修饰葡萄糖氧化酶,测量范围为1~17m mol/L。比色法具有非特异性,容易受到干扰21,难以保证重复性和检测的精确度。王荣等人在制备PB膜的基础上采用明胶包埋法将葡萄糖氧化酶固定在PB/Pt电极表面,研制得到电流型酶电极传感器。用酶电极测葡萄糖,都是在有氧存在下,葡萄糖氧化酶将葡萄糖氧化成葡萄糖酸,同时产生由电化学方法测定的过氧化氢,这是一种间接的、一次性的测定方法,且酶比较昂贵,而且储存期限短,耐高温性能差,不适合工业化生产,因此大众化使用受到限制。使用二茂铁及其衍生物等作为电子传递体的葡萄糖传感器,虽克服了溶解氧的影响,但作为葡萄糖传感器介体的二茂铁易流失,且存在二茂铁对尿酸、坏血酸均有催化作用的缺点,因此造成样品测定误差很大。也有文献报道以铂电极和金电极来催化氧化葡萄糖,虽克服了葡萄糖酶电极的缺点,但其催化活性和稳定性不理想,更因其价格昂贵而使应用受到限制。 碳纳米管和纳米 TiO,是优良的催化剂载体, 同时也具有催化活性’。本文采用电氧化聚合和扫描电沉积方法制备碳纳米管/纳米TTO2-PAr膜载 Pt(CNT/nanoTD2-PAn-Pt)复合电极,初步探讨葡萄糖在 CNT/nanoTD2-PAn-Pt复合电极上的直接电氧化,用电化学循环伏安法、微分脉冲法和计时电位法研究了复合电极电催化氧化葡萄糖的催化活性和灵敏性。葡萄糖在催化电极上的电化学氧化电流正比于葡萄糖的浓度,利用这一特性可研制葡萄糖传感器,方便地检测糖尿病患者血液中葡萄糖的含量。实验研究表明:(CNT/nanoTD2-PAn-Pt)复合电极作为葡萄糖传感器,具有检测范围较宽、催化活性高、抗干扰性能好、易于保存、检测方便等优点。 1 实验部分 1.11仪器与试剂 CHI660A电化学工作站(上海辰华仪器公司);LK2005微机电化学分析系统(中国科学院研究生院应用化学研究所);78HM-I型恒温磁力搅拌器(江苏省金坛市医疗仪器厂);KQ-100型超声波清洗器(昆山市超声仪器公司)WS70-1型 ( 收稿日期:2006-08-17;修回日期:2007-03-29 ) ( 基金项目:国家自然科学基金(20476001)项目资助;安徽省自然科学基金(00045317)项目资助 ) ( 联系人简介:吴何珍(1967-),女,讲师,主要从事电化学方面的研究。Email: zhenhezi67@126. com ) 红外线快速干燥器;XMT-数显温控仪;TL-02型链条天平(上海第二天平仪器厂)。 实验所用试剂葡萄糖、氧化钾、乙醇、H PtCl等均为分析纯,单体苯胺为化学纯,使用前经提纯、除氧,溶液配置用二次蒸馏水配制。碳纳米管为多壁碳纳米管(厦门大学化学系),Ti金属用ITA型纯钛(纯度为99.5%)。 1.2 CNT/nano TiO-PAn-Pt复合电极的制备 1.2.1 CNT/nano TO,膜电极的制备 前驱体Ti(OEt)4的电合成见文献17~9],按文献〔10,11]的方法直接水解Ti(OEt)4乙醇溶液制成 TO纳米溶胶,加入经超声分散过的碳纳米管乙醇溶液,再经超声分散10min得到碳纳米管-TD纳米溶胶。采用提拉法将纳米溶胶涂覆在清洁过的Ti表面,自然干燥后红外灯下加热干燥30 min,马弗炉中恒温723K煅烧30min,冷却后取出。上述提拉、干燥、煅烧等过程重复操作4~5次,即制成CNT/nano TO 膜电极。 1.2.21(CNT/nano TO,PAn膜电极的制备 以CNT/nanoTD,膜电极为基体电极,于含苯胺(0.2mol/L)的 H SO4(0.5 mol/L)溶液中,通氮除氧,在溶液静止的条件下,用三电极体系、循环伏安法在-0.1~0.9V电位下,以100mV/s的扫描速度进行电化学聚合,联机电脑自动记录聚合过程的循环伏安曲线。制备完毕,取出电极依次用1mol/L H, SO 和二次蒸馏水清洗,以除去未聚合和低聚合度的苯胺。CNT/nano TiO,-PAn复合膜性质的电化学测量在 1 mol/L HSO4溶液中进行12] 1.2.3 CNT/nano TO, -PAn- Pt复合电极的制备将上述制得的 CNT/nanoTiO2-PAn莫电极,在5mmol/L H PtCl 酒稀硫酸溶液中用循环伏安法进行电斗积Pt,在-0.2~0.6V电位条件下扫描90圈,再在 0.0~0.6V电位条件下扫描30圈,使Pt微粒分散在 CNT/nano TO2-PAn膜基体上,制得 CNT/nano TiO-PAn-Pt复合电极(电极面积0.2 cm X0.08 cm =0.016cm²)。 1.3 实验方法 循环伏安法和微分脉冲法研究采用三电极体系:采用 CNT/nano TiOz- PAn-Pt复合电极(0.016cm)为工作电极,铂黑电极为辅助电极,饱和甘汞电极(SCE)为参比电极。 以 0.5 mol/L KOH水溶液为电解液,在容量瓶中配制不同浓度的葡萄糖溶液,摇匀,转移至电解池中,搅拌富集2min,静置10s后记录其微分脉冲伏安(DPV)曲线。测试结束后,将电极置于1mol/L H, SO4溶液中,在-0.2~1.3V电位下清洗1m in,以更新电极表面。 测试在室温下完成,通过 CHI660A 电化学工作站得到的测试结果由联机计算机进行数据处理。表观电流密度按实测电流除以表观电极面积得到。 2 结果与讨论 2.1 CNT/nano TO,-PAn-Pt复合电极的表征 图1为复合电极在1mol/L的 H SO4溶液中循环伏安曲线。从图中可以看出,CNT/nano TO2-PAn-Pt复合电极具有 CNT/nano TiO,-Pt复合电极和 Pt电极的电化学行行为[为13、14],0.0V(vs. SCE) 附近出现氢的吸脱附电流,回扫期间的峰电流为Pt微粒表面吸附氧化物种的还原峰,峰电流密度为70.25 mA /cm,反映了修饰在聚苯胺表面的Pt微粒具有很高的催化活性;经反复扫描(15次),其循环伏安曲线变化很小(图1a与图1b),这说明CNT/nanoTO,-PAn-Pt复合电极的稳定性很好。 图1 CNT/nanoTO,-PAn-Pt复合电极循环伏安曲线。V: 100mV/S Fig 1 Cyclic votammograms CNT/nanoTO,-PAn-Pt electrodea第一次扫描 The first time; b第15次扫描 The fifteen times 图2为葡萄糖在 CNT/nanoTiOz-PAn-Pt复合电极上恒电流氧化时的典型电位响应图(电解液为0.1mol/L Glucose +0.5 mol/L KOH)。从图中可以看出,在较小的电流密度下(1.0mA/cm ),葡萄糖氧化能保持在较低的电位下进行(图2a),经长时间反应(800 s)电极几乎不被极化,这时葡萄糖主要是进行两电子反应,生成葡萄糖酸盐,当电流密度为2.5 mA/cm (图 2b)、5.0mA/ cm(图2c)时,葡萄糖在复合电极上的主要反应还是两电子反应,但有毒化电极的中间产物产生,电极电位向正的方向漂移;随着电流密度的增加,发生多电子反应,电极电位更向正的方向移动,并有毒化电极的中间产物生成,但这些中间产物没有使电极失去活性。图中曲线2d(电流密度为7.5 mA/cm)表示电极被轻度毒化,当电流密度为10.0mA /cm (图2e)时,电极发生显著极化,电极上发生析氧反应。同时可观察到,即使在较高电流密度下,也没有氧化振荡现象发生,而在纯 Pt电极或CNT/nanoTiO,-Pt复合电极上均有明显的振荡现象发生[14,15]。这些结果进一步说明,CNT/nanoTi,-PAn-Pt复合电极有很强的抗毒化作用和高稳定性,可作为葡萄糖传感器的高活性催化电极。 图2 葡萄糖在CNT/nanoTO,-PAn-Pt复合电极上的恒电流氧化 Fig 22Glucose oxidation on under different current densitiescurrent densities(mA/m²) a 1.0;b 2.5;c 5.0; d 7.5; e 10.0. 2.2 CNT/nanoTO,-PAn-Pt复合电极对葡萄糖的电催化活性 微分脉冲伏安法研究表明:CNT/nanoTiO,-PAn-Pt复合电极在碱性溶液中对葡萄糖的电氧化具有很高的催化活性。图3b为 CNT/nanoTiD"PAn-Pt复合电极在1.25 ×10mol/L glucose +0.5mol/L的 KOH水溶液中的微分脉冲曲线,与图3a(空白对比曲线)比较可知:在-0.33Ⅴ附近有一个明显的葡萄糖在电极上的氧化电流峰,其电流密度约为18.8mA/cm。 2.3 葡萄糖浓度与氧化电流的关系 图3为 CNT/nanoTO,-PAn-Pt复合电极在不同浓度葡萄糖/0.5 mol/L的 KOH水溶液中的微分脉冲曲线。从图中可看出:电流密度随浓度的增大而增大,实验结果与文献报到一致。在本 图3 CNT/nanoTD,-PAn-Pt复合电极在不同浓度的 葡萄糖/0.5mol/L的 KOH水溶液中的微分脉冲曲线。 Fig3 Differential Pulse Voltammetry ofCNT/nanoTD,-PAn-PTcomplex electrode in different concentration of glucose Concentration of gluco se (mol/L): a.0.0 b 1.25 x10-2, c 1.0 ×10-3, 实验条件下,葡萄糖浓度在 1.25 ×10~1.0×10°mol/L与峰电流呈良好线性关系(图4),其线性回归方程为: a(mA)=0.34969 +0.02612 bogC(mol/L) (r=0.99881 );检出限为5.0 X10°mol/L。 2.4 CNT/nanoTi,-PAn-Pt复合电极的稳定性和重现性 电极于10℃干态保存20天后,其对葡萄糖的催化活性保持了初始活性的90.9%:若每天使用,14天后,其对葡萄糖的催化活性为初始活性的84.8%。这表明该传感器具有良好的稳定性和较长期的使用寿命 对不同浓度的葡萄糖,平行测定5次,结果见表11 表1 CNT/nanoTD,-PAn-Pt复合电极测定葡萄糖的重现性 Table 1 Reproducibility if detemm inations(n=5) 5.0 0.284 1.9 0.3 0.253 2.0 7.0 0.288 1.7 由表1可见,葡萄糖氧化电流的相对标准偏差 RSD<2.0%,表明复合电极该具有良好的重现性。 2.5 干扰实验 由于本实验采用低的测定电位,复合电极对葡萄糖电催化氧化的选择性大大提高。对可能与葡萄糖共存的几种物质进行干扰实验,当葡萄糖浓度分别为3.0 ×10°mol/L 、5.0 ×10 mol/L和 5.0 ×10 mol/L时,100倍的 Na*、K*、Ca*、Mg?+、Zn*、cu*和无机阴离子CI、POcoHCO,以及其加入(0.06mmol/L的抗血血酸或0.3mmol/L的尿酸(模拟人血成份)均不干扰葡萄糖的测定。 2.6 样品的测定与回收实验 用模拟样品进行测定。称取一定量的葡萄糖,在容量瓶中配置不同浓度的葡萄糖溶液,按实验方法进行回收率实验,实验结果见表2。 ( 参考文献: ) ( [ 1 ]YO SH RO T, S O ICH RO Y . F l uorescence measurement of glucose by pyrene modified oxidase[J]. J oumal ofM olec- ular Catalysis B: Enzym atic,2002, 1 7(3-5):203-206. ) ( [2]何立千.血糖测定方法的进展[J]中华医学检验杂 志,1982,5(1):49-52. ) ( [3]王荣,郭晓明,吴霞琴,等.基于普鲁士蓝(PB)膜修饰铂电极的葡萄糖传感器的研究[J].化学研究与应用, 2001, 1 3(4):380-382. ) ( [4]Christian B, Christoph e D , JacquesM, e t al. New i n- sights into the enzymatic catalysis of the ox i dation of g lu- cose by native and r ecombinant glucose oxidase m ediated by electrochem icslly generated one-electron redox cosub- strates[J] . J Am Chen S oc, 1993,115:2-10. ) ( [5]顾家山,褚道葆,周幸福,等.纳米 TO,膜修饰电极异 相电催化还原马原酸[J].化学学报,2003, 6 1 : 1405-1407. ) ( [6] Zhang X, Chan K Y , Tseung A C C[J ] J . E lectroanal Chem , 1995,386: 2 41-246. ) ( [7]褚道葆,周幸福,林昌健.电化学合成金属醇盐的研究 [J].高等学校化学学报,2000,21,133 -135. ) 表2试样的测定结果 Table 2 Detemm ination results of sample No. Added Found Recovery RSD (10°mol/L) (10mol/L) (%) (%n=6) 1.00 0.95 95.0 2.3 2 2.00 1.93 96.5 1.7 3 4.00 3.89 97.3 1.1 4 6.00 5.98 99.7 2.0 5 8.00 7.93 99.1 1.5 ( [8]周幸福,褚道葆,林昌健.钛醇盐电化学合成的研究 [J].化学学报,2000,111327-1331. ) ( [9 ]Zhou X F , Chu D B,L in C J. A n o dic disso lution of spongy titanium i n e thanol s o lution f o r p r eparation of na n o-sized T io,powder[J1 . Electroch i m Acta , 2002, 47:2769-2771. ) ( [10]褚道葆,沈广霞,周幸福,等.高活性Ti基纳米 TO, 膜催化电极的制备[J].电化学,2001,7:249-254. ) ( [11]褚道葆,沈广霞,周幸福,等.Ti表面修饰纳米 TO,膜电极的电催化活性[J].高等学校化学学报,2002, 23:678-681. ) ( [12]侯丽波,贾梦秋,胡刚.聚苯胺薄膜电极的制备及性 能研究[J].北京化工大学学报,2004,31(4):65-69. ) ( [13]吴何珍,褚道葆,陈忠平,等.CNT/nanoTD,-Pt修饰 电极对葡萄糖的直接电氧化[J].安庆师范学院学报 (自然科学版),2006,12(2):89-91. ) ( [14]魏小兰,沈培康.碱性介质中葡萄糖在铂电极上的阳 极氧化[J].化学物理学报,2003,10:395-340. ) ( [15]褚道葆,李晓华,冯德香,等.葡萄糖在碳纳米管/纳 米 TiO,膜载 Pt复合电极上的电催化氧化[J].化学 学报,2004,62:2403-2406. ) Carbon nanotubes/nanocrystlline TD,-PAn film loaded Pt com plex electrodedeterm ines glucose by differen tial pulse str ipping voltamm etry wU He-zhen2, cHU DaoBao, CHEN Zhongping,YN Xiao-juan (1. Anqing Vocational Techno logy College, Anqing 246003, China; 2. College of Chem istry and M aterials Science,AnhuiNomal University, W uhu 241000, China 3. Anhui Science Technology College, Fengyang 233100,China) Abstract: Electrocatalytic oxidation of glucose on carbon nanotubes/nanocrystllineTioz-PAn fim loaded Pt (CNT/nanoTiDO,-PAn-Pt) complex electrode was investigated by cyclic voltammetry and chronopotentiometry. Under the op timum conditions (0.5 mol/LKOH solution), scan potention is -0.5~-0.2V by differential pulse stripp ing voltammetry. One peak is produced sensitively andwell-defined at near -0.33V (vs. SCE). This is taken for the quantitative detem ination peak. The linear range of glucose is 1.25x10²~ 1.0 ×10°mol/L (r=0.899). The detection limit is 1.0 10°mol/L. 0.06 m mol/L ascorbic acid or 0. 3m mol/L uricacid (simulate the blood composition ofman) etc, did not interfere with the detemmination. The results revealed that the modified e-lectrode could be used to the detemm ination of glucose in imitative samp les with good results. Key words: nanocrystllineie1TTio,-PAn-Pt laded complex electrode; glucose; electrocatalyticic oxidation;differentialpulsestripp ing voltammetry ( (责任编辑 刘科伟) ) ◎China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
确定



还剩2页未读,是否继续阅读?
天津市兰力科化学电子高技术有限公司为您提供《葡萄糖中碳纳米管/ 纳米二氧化钛- 聚苯胺载铂复合电极微分脉冲分析检测方案(电化学工作站)》,该方案主要用于其他中碳纳米管/ 纳米二氧化钛- 聚苯胺载铂复合电极微分脉冲分析检测,参考标准--,《葡萄糖中碳纳米管/ 纳米二氧化钛- 聚苯胺载铂复合电极微分脉冲分析检测方案(电化学工作站)》用到的仪器有LK2005电化学工作站
推荐专场
相关方案
更多
该厂商其他方案
更多
















