方案详情
文
使用仪器:DIONEX ICS2500离子色谱仪
摘要:建立了化妆品和保健品中Cr3+ 、Cr6+的柱后衍生- 离子色谱检测法。样品中的铬经柱前络合为2,6-嘧啶二羧酸铬, 柱后衍生为1,5二苯碳酰二肼铬, 于520 nm波长检测。优化了衍生反应条件, 提高了检测灵敏度, Cr3+和Cr6+方法检出限(LODs, 3σ)分别为0112、01011 mg/kg。样品加标回收率为89%~108% ,
重复性好。共存离子Fe2+ 、Fe3+ 、Pb2+ 、Cu2+ 、Al3+ 、Zn + 、Hg2+等, 以及常见有机物均不干扰测定。
方案详情

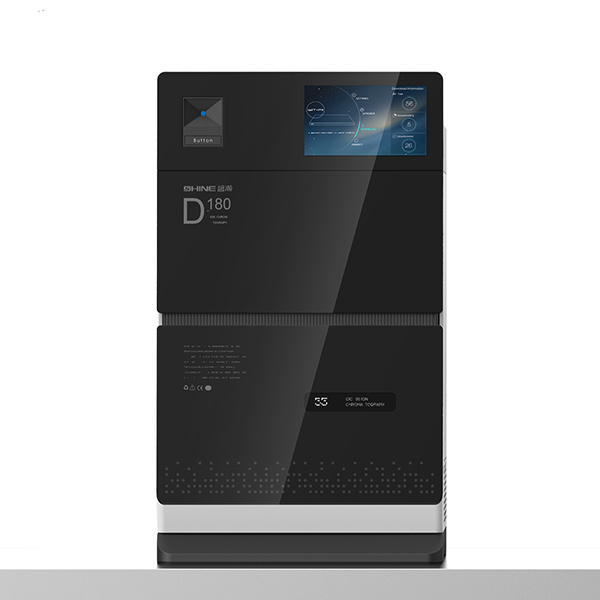
第27卷第5期2008年5月分析测试学报FENXICESHI XUEBAO (Joumal of Instrumental Analysis)Vol. 27 No.5546~548 745钟志雄等:化妆品及保健品中 Cr*和 Cr的柱后衍生-离子色谱法测定第5期 化妆品及保健品中Cr+和 Cr的柱后衍生-离子色谱法测定 钟志雄,朱炳辉,吴西梅 (广东省疾病预防控制中心,广东广州 510300) 摘要:建立了化妆品和保健品中Cr+、cr*的柱后衍生-离子色谱检测法。样品中的铬经柱前络合为2,6-嘧啶二羧酸铬,柱后衍生为1,5二苯碳酰二肼铬,于520 nm波长检测。优化了衍生反应条件,提高了检测灵敏度, Cr*和 Cr*方法检出限(LODs, 3J)分别为 0.12、0.011 mg/kg.样品加标回收率为89%~108%,重复性好。共存离子 Fe+、Fe、Pb、Cu*、Af*、Zn*、Hg*等,以及常见有机物均不干扰测定。 关键词:柱后衍生;离子色谱法;化妆品;保健品; Cr+; cr 中图分类号:O657.75; P578.8 文献标识码:A 文章编号:1004-4957(2008)05-0546-04 Determ ination ofCrand Crin Cosmetics and HygienicalFood by bon Chromatography with Post-column Derivatization ZHONG Zhi-xiong, ZHU B ing-hui, WU Ximei (Center for D isea se Control and Prevention of Guangdong Province, Guangzhou 510300, China) Abstract: A method was developed for the detem ination ofCrand Cr in cosmetics and hygienicalfood by ion chromatography using post-column derivatization with spectrophotometric detection TThesamp le was pretreated respectively with acetic acid to extract the Cr and sodium hydroxide to extractthe Cr*followed by comp lexing with pyridine dicarboxylic acid (PDCA) to fom Cr*- PDCA andCr*-PDCA, respectively Using diphenylcarbohydrazide(PDC) as the post-column derivative rea-gent, the absorbances of Cr-PDC and the Cr+-PDC fommed were detected at 520 nm, respec-tivelyyUnder op tim ized derivative conditions,the detection lim its(3) for Cr and Cr+were 0. 12and 0.011 mg/kg, respectively The relative standard deviatations(RSD) for Crand Cr were 1.1%and 1.3%(n=8), respectively, and the average recoveries were in the range of 89%-108%.The de-teminations were not interfered by the coexistent cations, namely Fe+, Fe+, Pb*, Cu+, Alt,Zn*, Hg and the organic matter Key wo rd s: ppoosstt--ccoo lluumn derivitization:ion chromatography;cosmeticshygienical food; Cr*; co+ 铬是人体必需的微量元素,环境中铬主要以三价和六价形式存在,三价铬广泛分布于人体的各组织器官,维持人体糖和脂肪的正常代谢,其有机化合物如吡啶甲酸铬,常用于降糖的保健品中。六价铬则表现出明显的毒性,对皮肤粘膜有刺激和腐蚀性,已证实有致癌作用。食品和化妆品中铬形态分析尚没有标准检验方法,开展检测方法研究非常必要。 铬分析常采用分光光度法,为提高灵敏度,可选择高灵敏的显色剂21、富集浓缩和阴离子交换树脂微柱浓缩样品[4],以及萃取光度法等[5]。原子吸收光度法用于铬形态分析,样品需经萃取、浓集、洗脱处理,再测定 Cr*、cr+[6]。化学发光法、电感耦合等离子体光谱、质谱测定铬的灵敏度较高17-91,但联用设备不普及。毛细管电泳检测 Cr*等重金属离子, Fe*干扰 Cr*测定110]。液相色谱法测定铬形态,多采用固相萃取富集,以提高灵敏度。保健食品、化妆品组成复杂,难以准确分析其有害元素形态含量,通常只测定总量,但不能真实反映危害水平。离子色谱法可用于于形态分 ( 收稿日期:2007-06-28;修回日期:2007-07-17 ) ( 基金项目:广东省卫生厅医学科学技术研究基金资助项目(A2006079) ) ( 第一作者:钟志雄(1965-),男,广东龙川人,副主任技师, Tel: 020 - 84 4 51366-8155, E- m ail:l: zzxiong608@yahoo. com. cn ) 析12-13],在化妆品检测中的应用尚未见报道,本文探讨离子色谱-光度法检测 Cr*和 Cr*,为保健食品及化妆品监管提供检测方法。 1实验部分 1.1仪器与试剂 Dionex ICS-2500型离子色谱仪,AD25紫外可见检测器, PC-10柱后反应装置,AS50自动进样器,色谱柱 bnPac CS5 (4 mm i.d. ×250mm)、CG5(4 mm i.d. ×50 mm)。 1 016 mg/L Cr*、1 017 mg/L Cr*为国家标准物质,2,6嘧啶二羧酸(PDCA)、1,5二苯碳酰二肼(PDC)、磷酸氢二钠、碘化钾、乙酸铵、氢氧化钠、硫酸、甲醇、盐酸、十二烷基三甲基氯化铵为优级纯或分析纯。标准溶液用淋洗液配制,实验用水为 18.0MQ 去离子水。 淋洗液:0.668 g PDCA、3.85 g乙酸铵、0.72g磷酸氢二钠、1.67g碘化钾和0.30 g氢氧化钠溶于 100mL水,得到混合储备液,用时稀释10倍,调节溶液 pH6.8。 衍生试剂:0.5g十二烷基三甲基氯化铵溶于 100 mL热水,冷却加法约 500mL、硫酸 20mL,另称取 0.5 g PDC, 溶于 150mL甲醇,两液混合加水定容到1000 mL,过滤后使用,冰箱储存稳定7 d. 1.22色谱条件 淋洗液流速 1.0mL /m in, 衍生剂流速 0.5mL /m in, 反应温度40℃, 检测波长520mm,进样量75uL,以保留时间定性,峰面积定量。 1.3样品预处理 准确称取1g样品于 25 mL比色管中,其中一组加入1.0 mol/L乙酸约 15 mL, 用于 Cr*的则定,另一组加入0.5 mol/L氧氧化钠勺 15mL用于 Cr*测定。两管水浴加热至沸腾20 min, 充分溶解,高速振荡5min, 超声浸提 10 min, 用 3.0 mol/L氢氧化钠、1.5 mol/L 盐酸调节样品溶液的 pH为6.5~7.0,加入2mL淋洗液储备液,水浴加热煮沸2min, 冷却,加水定容至刻度。取上清液,14000 r/m in离心分离 10 min, 过 0.45um滤膜,备用。 2 结果与讨论 2.1衍生剂浓度、反应温度与检测波长的确定 二苯碳酰二肼 (PDC)是测定铬常用的显色剂,但灵敏度不高。本研究优化了反应条件,以提高灵敏度。分别固定 PDC、甲醇、十二烷基三甲基氯化铵和硫酸中的3种试剂含量,改变其中1种试剂的浓度,测定标准溶液中 Cr *和 cr*的峰面积。实验结果表明, PDC从 0.3 g/L增加到0.8g/L时,Cr*的峰面积增大, cr*的峰面积则减小;甲醇体积分数从5%增加到 20%时, Cr*的峰面积稍微增大,cr*的峰面积增加较多;十二烷基三甲基氯化铵从 0.2 g/L增加到 4 g/L时, Cr*和 Cr*的峰面积先增加后减小;硫酸体积分数从1.5%增加到3.0%时, Cr*和 Cr*的峰面积变化不明显。综合考虑,选择0.5g/L PDC、15%甲醇、2.0%硫酸、0.5 g/L十二烷基三甲基氯化铵混合液作衍生剂。 反应温度对显色反应有明显的影响,在室温、40℃、60℃80℃时,分别测定标准溶液中 Cr*和Cr*的峰面积。实验结果表明,温度增加,Cr*峰面积略有减小, cr*峰峰面积明显增加,反应温度为40℃较合适。 Cr(Ⅲ) - PDCA和 Cr(VI) -PDCA在255、325、365mm有紫外吸收,但吸收弱[5。Cr(Ⅲ)-PDC和 Cr(VI)- PDC在 520、540 nm等有较强的可见吸收,因此,选取520 nm为检测波长。 2.221样品预处理方法的选择 铬形态分析样品前处理方法有多种,可采用PIS聚合物吸附、阴离子微柱浓缩法13-4],中性氧化铝小柱吸附样品的 Cr*和 Cr*, 然后用酸、碱分别洗脱,回收率好。Cathum等采用嘧啶二酸铵萃取环境样品中的 Cr*、 cio和 Cr0。综合文献报道,碱性条件有利于 Cr*的提取,但 cr*会生成 Cr(OH),沉淀,采用酸提取 Cr*更合适。本实验分别测定 0.5mol/L碳酸氢钠、氢氧化钠,1.0mol/L硫酸、乙酸、盐酸溶液等浸提样品中 Cr*和 Cr*的效率。结果表明,碳酸氢钠、盐酸、硫酸提取效率极低,0.5 mol/L氢氧化钠溶液浸提 Cr*和1.0 mol/L乙酸提取 Cr *的效率较高(见表1)。故本 文选先 0.5 mol/L氢氧化钠和1.0mol/L乙酸分别作为 Cr*、Cr*的提取液。 表1浸提液对化妆品和保健品中 Cr+、cr*回收率的影响 (n=3) Table 1 Effect of extractive reagent on the recoveries of Cr a and Cr in co smetics and hygienical food(n =3) Extractive Original Added Found Recovery Sample reagent Cation wo/(mg kg) w/(mg kg) wp/(mg kg) R/% Color focus palette 0. 5 mol/L NaOH Cr+ <0.12 30.48 7.28±0.61 24 cr+ 0.81 4.07 5.22±0.22 108 1 mol/L CH,COOH cr+ <0.12 30.48 26.97±1.54 89 Crt 0.75 6.10 3.5 ±0.31 45 Foundation cream 0. 5 mol/L NaOH <0.12 30.48 5.35±0.14 17 Cr+ 0.59 4.07 4.83 ±0.57 104 1 mol/L CH,COOH Cr+ <0.12 30.48 27.87±1.68 91 Cr+ 0.75 6.10 3.33±0.25 42 Anti-diabetic cap sule 0.5 mol/L NaOH Cr+ <0.12 30.48 6.1±0.78 20 Cr+ <0.011 6.10 5.62±0.22 91 1 mol/L CH, COOH Cr+ 10.36 30.48 38.58±3.23 93 c6+ <0.011 6.10 3.92±0.57 64 2.3干扰实验 考察了常见共存离子对铬测定的影响,实验发现, 10.0mg/L的 Fe*、Fe+、Pb、Cu+、Ai*、zn*、Hg*, 15.0 mg/L的苯甲酸、山梨酸、糖精钠、柠檬酸、酒石酸,均不影响测定。 2.4线性方程、线性关系与检出限 在实验选定的最佳条件下,分别测定 Cr*和 cr*的混合标准溶液,求得线性方程和相关系数。配制 0.05 mg/L Cr*和 0.02 mg/L Cr*的混合标准溶液,连续进样11次,得到浓度平均值和标准差,计算方法的检出限 (LODs, 30)见表 2。 表2线性方程、线性关系与检出限 Table 2LI inear regression equations, correlation coefficients and detection lim its (3) Cation Correlation Average concentration LODs Linear regression equations coefficient r (n=11)p/(mg. L) p/(ug. L-) w/(mg kg) cr+ A=-3.10×10-6+5.59×10-5c 0.999 4 0.068±1.559×10 4. 7 0.12 Cr+ 4=-1.07×10-4+7.27×10-3c 0.999 6 0.0158±1.391×10“ 0.42 0.011 2.57方法的精密度与加标回收率 配制 0.245 mg/L Cr*和 0.100 mg/L Cr*的混合标准溶液连续进样8次,峰面积平均值和相对对准偏差分别为1.045×10±1.195×10、RSD为1.1%, 1.086×10±1.367×10、RSD为1.3%。 准确称取1g胭脂粉样品3份,其中2份分别加入 Cr(Ⅲ)和Cr(VI)标准溶夜,按照"1.3”处理羊品,测定。Cr*平均回收率为 89%~93%,Cr*平均回收率为 91%~108%(见表1),色谱图见图 1A、1B。 图1标准溶液(A)及胭脂粉(B)的离子色谱图 Fig.1 bn chromatogram of standard mixture(A) and powder blush refill(B) A: 1.Cr+(8.13 mg/L), 2. Cr+ (0.816 mg/L); B: 2. Cr+ (0.025mg/L) (下转第552页) ( 参考文献: ) ( 1T 陈青川,于文莲,王静.高效液相色谱法同时测定多种食品添加剂 [J].色谱,2001,19(2):105-108. ) ( [2] 陈金东,李蔚.高效液相色谱法同时测定食品中的阿斯巴甜、阿力甜[J].中国卫生检验杂志,2006, 1 16(9):1069-1070. ) ( [3] 中华人民共和国卫生部. GB2760食品添加剂使用卫生标准[S].北京:中国标准出版社,1997:28-29. ) ( 陈少波,潘超华.食品中甜蜜素的紫外分光光度法测定[J].分析测试学报,2000,19(3): 82-83. ) ( 贾玉珠,骆和东,林健. . I HPLC法同时测定饮料中5种添加剂的研究[J].中国卫生检验杂志,2005, 15(4): 448-449. ) ( 6 郭又珍,王志宏.同时测定碳酸饮料中苯甲酸钠、山梨酸钾和安赛蜜的高效液效色谱法[J].分析测试学报, 2001,20(4): 6 7-68. ) ( [71 郭莹莹,朱岩,叶明立.淋洗液发生器离子色谱抑制电导法测定甜味剂[J]浙江大学学报,2004,31(4): 435-437. ) ( [8] ZHU Yan, GUO Yingying, Y YEM ingli, e t al Separation a nd s i multaneous detemm ination of four artificial sweeteners in food and beverages by ion chromatography[J]. J Chromatogr A, 20 0 5,108 5 : 143-146. ) ( 19 BOYCEMC Simul t aneous detemm ination of antioxidants, preservatives and sweeteners pemm itted as ad d itives in f o od bym ixed m icellar electrokine t ic chromatography [J ]. J Chromatogr. A, 1999,847:369 - 375. ) ( 1101 CA THER N E O T, CR A IGE TRENERRYV. Micellar el e ctrokinetic capillary chrom a tographic deteim ination of a rtificial sweeteners in l ow-Joule s oft drinks and other foods[J l . . . J Chromatog r A,1995,694: 5 07-514. ) (上接第548页) ( 参考文献: ) ( T1 FLORAS De Thr es hold mechanism s and s i te specificity in c hrom ium (VI) car c inogenesis[J ]. Car c inogenesis, 200 0 ,21 (4):533-541. ) ( T2 FANG Guozhen, LUO J ikuen n S p ectrophotometric detem ination of chrom ium (Ⅲ, VI ) by use of chrom ium (Ⅲ, VI) chrom A z url S - cetylpyridinium b rom ide-hydroxylam ine hydrochloride-zinc (Ⅱ) system [ J ]. Talanta. ,1 1992, 3 9(12): 1579-1582. ) ( [31 SCND A Y M , PANDEY A K, REDDY A V, et al Selecti ve preconcentration and d ete m m ination of chromium (VI) u - sing a flat sheet polymer inclusion sorbent potential a pplication for Cr(VI) d e tem ination in real samples [J]. A n a lChem, 2 002, 74(16):4204-4212. ) ( 14 SAMANTA G, BO R NG CB, DASGU P TA P K Continuo u s automated measurement of hexavalent chrom ium in airb o me particu la t e matter[J]. Anal Chem , 2001, 73(9): :2 2034-2040. ) ( 5 THORBUM D, DANGOLLE CD F. Sp e ctrophotometric detem ination of chrom ium (VI) by e x traction of the dichromateanion into propylene carbonate [J]. Anal Chim Acta, 1 997, 356: 14 5 -152. ) ( 16 SAHA YAM A C Speciation ofCr(Ⅲ) and Cr( V I) in potab l e waters by using activated neutral alum ina as collector andET-AAS for detemm ination[J] . Anal B ioanal Chem,2002, 372(7/8):840-842. ) ( [71 XU Yi, BESSO TH F G , EIKEJC T, e t al O n- l ine monitoring of ch rom ium (Ⅲ) using a fastm icromachined m ixer/reac-tor and chem ilum inescence detection[ J ]. Analyst, 20 0 0,125:677-685. ) ( [8] FRANCESCO C, ANDREA R. De t em ination of ca d m ium, lead , iron , nic k el and chrom ium in se l ected food matrices by plasma spectrometric techniques[ J ] . M icrochem ical Jouma l , 2002, 79(1/2) :9 1-96 . ) ( [9] WU Ying, H U B in, P ENG Tong, et al In-situ separatio n of chrom ium (Ⅲ) and chrom ium (VI) a nd s e quential ETV - ICP-A E S de t emm ination u sing acetylacetone and PTFE as chemical m odifiers[J]. I Fresenius J Anal Chem, 2001, 370(7):904-910. ) ( [10 ] 王柏松,李华,丁富新,等.毛细管电泳柱上络合分离、间接紫外检测重金属离子[J].分析测试学报,2006, 25(5):25-29. ) ( 「111 CATHUM S, B R OWN C E, WON G Wei Detem ination ofCrt, Cro and CrO, ’ in environmentalmatrixes by high- perfomance liquid chromatography with diodearray detection[J] . Anal B ioanal Chem, 2002,373(1/2):103-110 . ) ( 1121 TOMASD H, ROH R ER J S, JACKSON PE, et al Detemm i n a tion of hexavalent chrom ium at the level of the Cal i foria Public Health Goal by ion chromatography[J ] . JChromatogr . A, 2002, 956(1 / 2):255-259 . ) ( [13]周光明,刘珍,杨光明,等.低压离子色谱分离-化学发光学线检测过渡金属离子[J].色谱,2005,23(3): 265-268. ) ◎China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
确定



还剩2页未读,是否继续阅读?
赛默飞色谱与质谱为您提供《化妆品及保健品中Cr3+和Cr6+检测方案(离子色谱仪)》,该方案主要用于美容/修饰类化妆品中Cr3+和Cr6+检测,参考标准--,《化妆品及保健品中Cr3+和Cr6+检测方案(离子色谱仪)》用到的仪器有赛默飞ICS5000多功能离子色谱、赛默飞戴安ICS-1600离子色谱系统
推荐专场
相关方案
更多
该厂商其他方案
更多