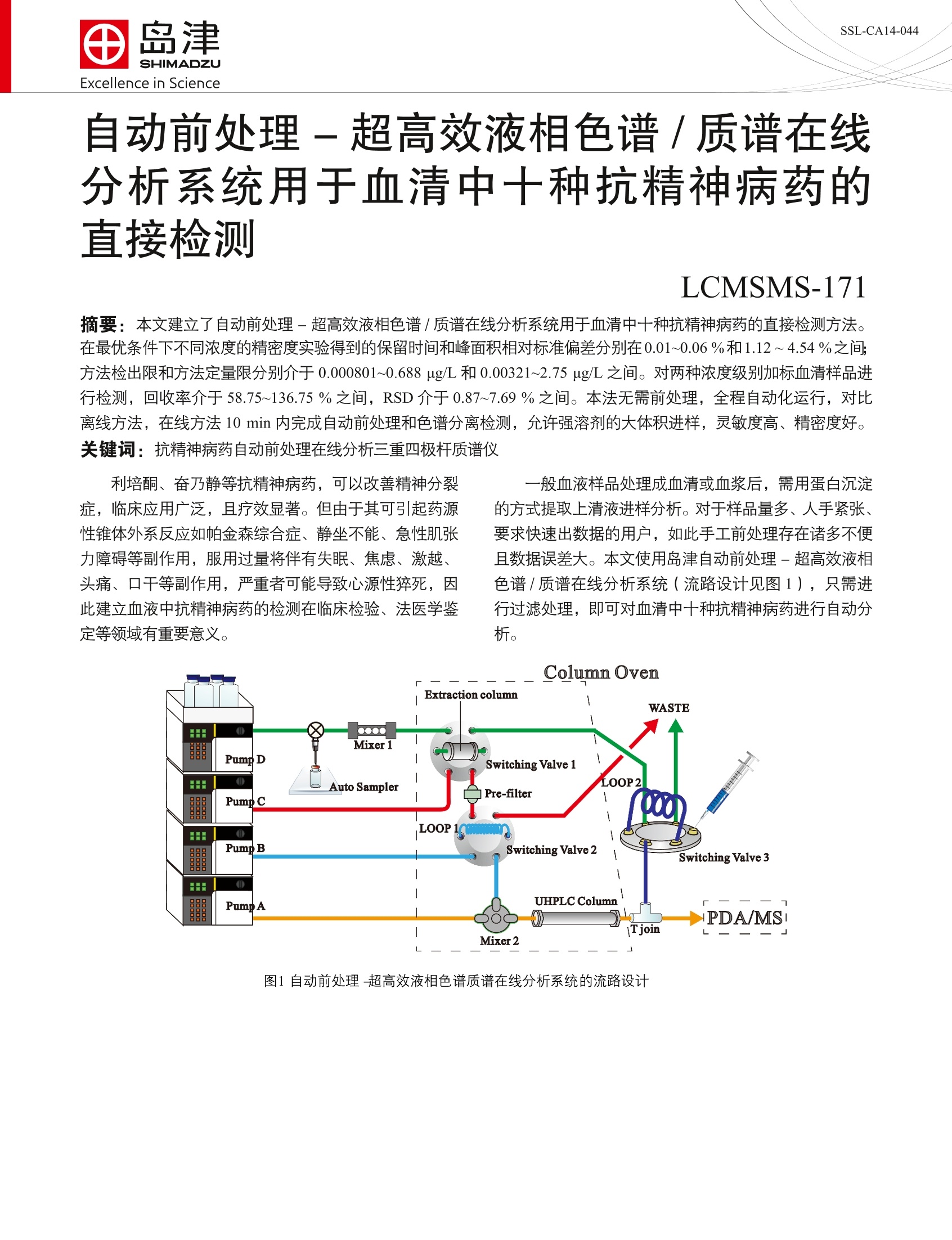
一般血液样品处理成血清或血浆后,需用蛋白沉淀等方式提取上清液进样分析。对于样品量多、人手紧张、要求快速出数据的用户,如此手工前处理存在诸多不便且数据误差大。岛津自动前处理-超高效液相色谱/质谱在线分析系统,只需进行过滤处理,即可直接对血清中十种抗精神病药进行自动分析。该方法无需前处理,全程自动化运行,对比离线方法,在线方法10 min内完成自动前处理和色谱分离检测,允许强溶剂的大体积进样,灵敏度高、精密度好。
方案详情

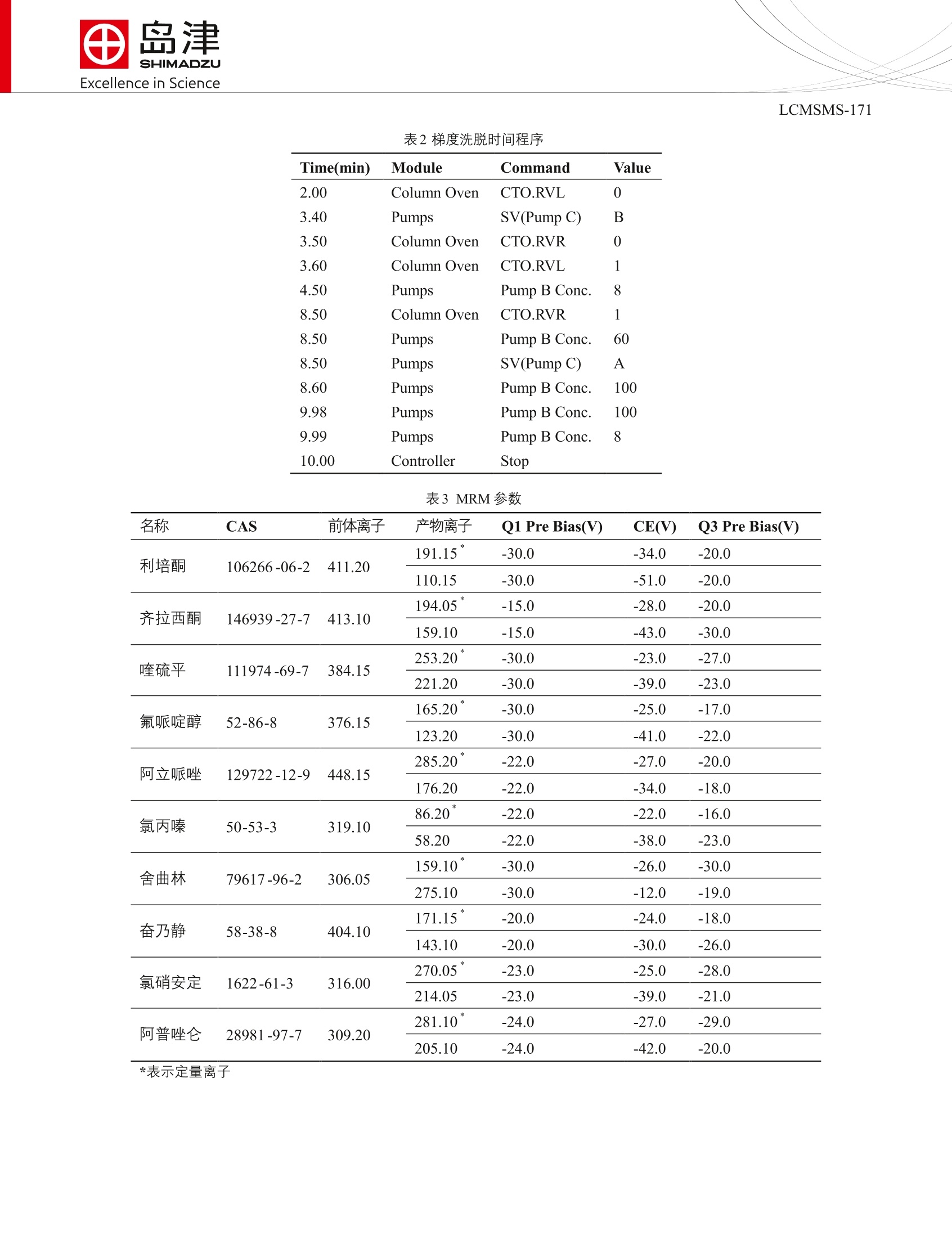
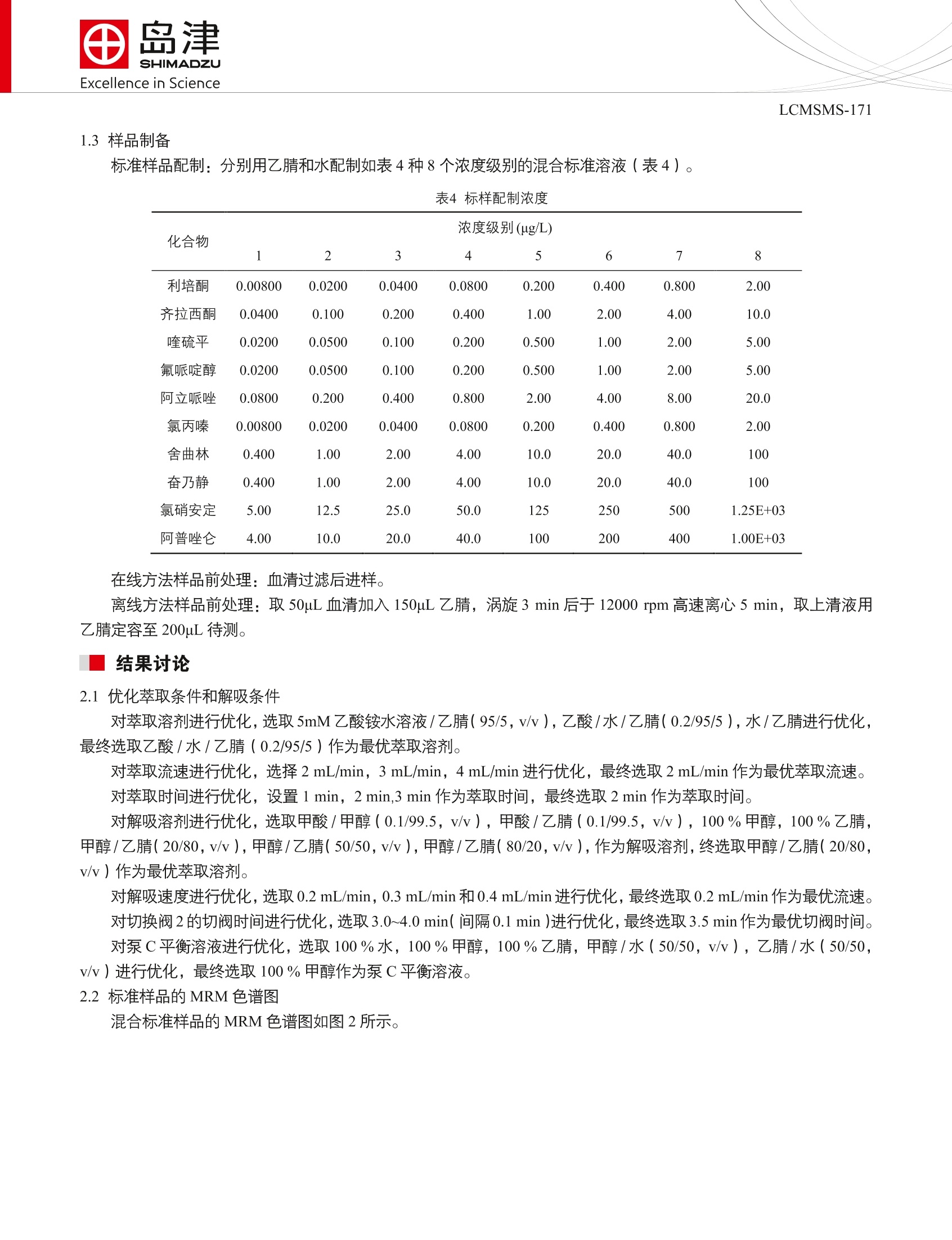
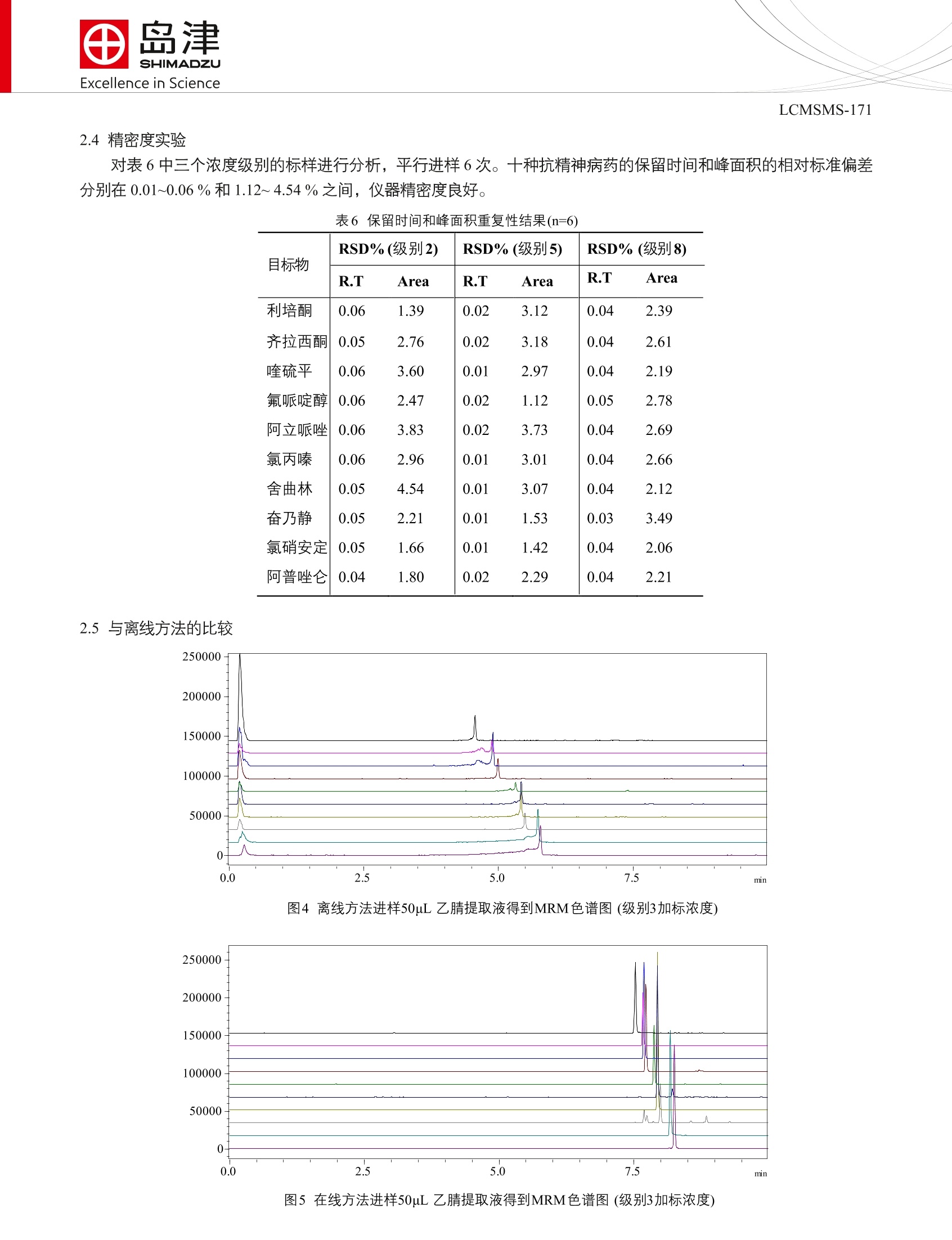
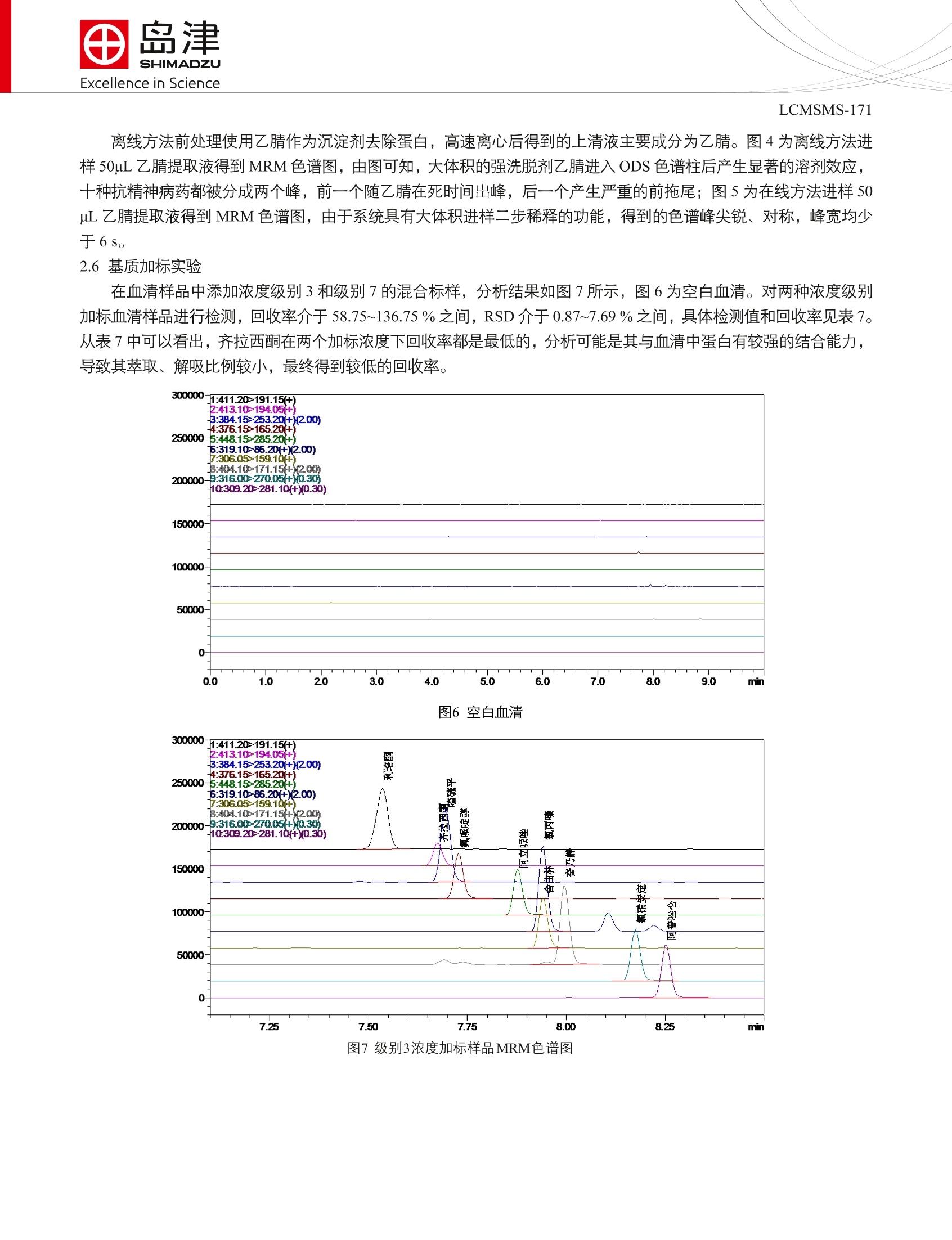
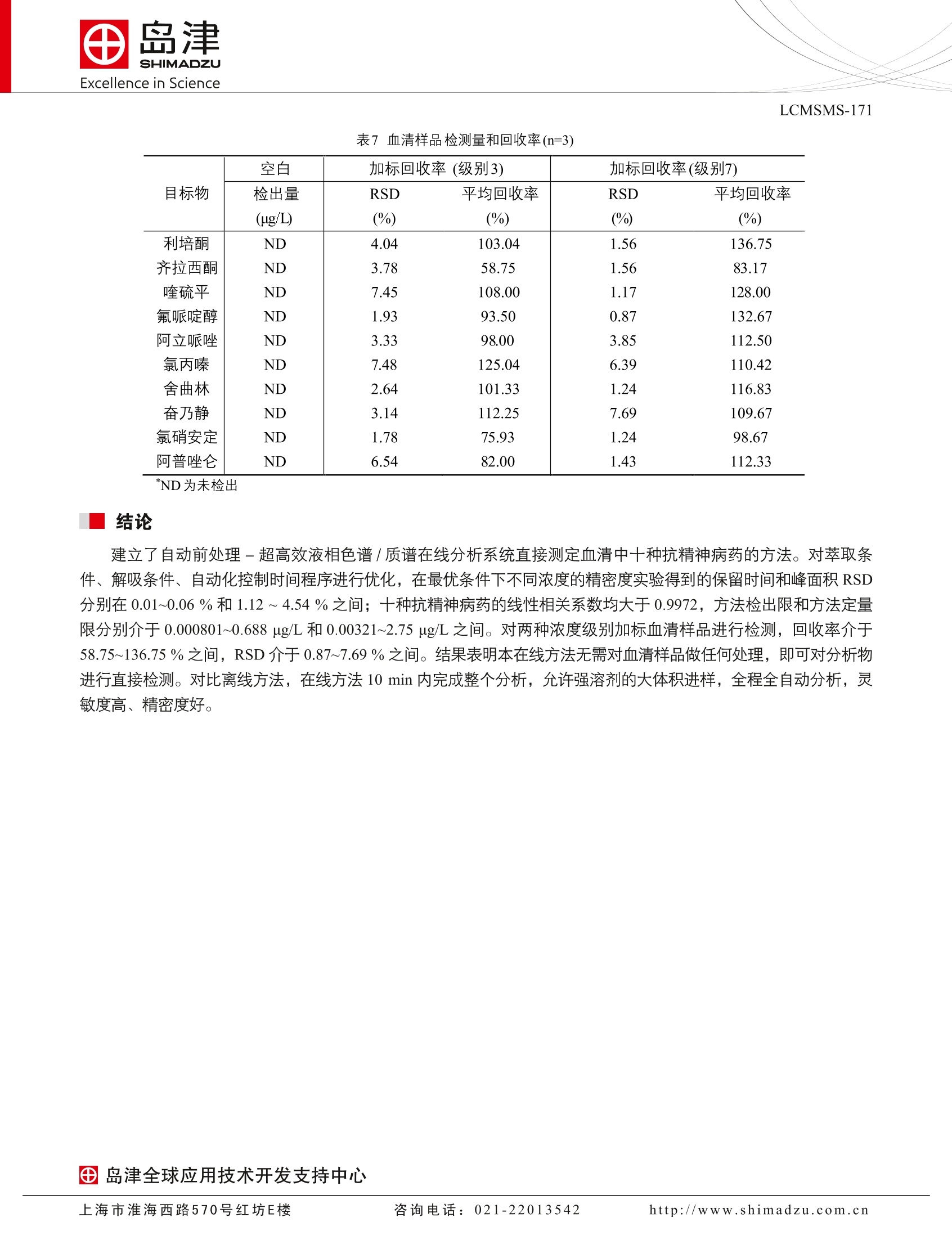
SSL-CA14-044 Excellence in ScienceLCMSMS-171 田岛津全球应用技术开发支持中心咨询电话:021-22013542上海市淮海西路570号红坊E楼http://www.shimadzu.com.cn 自动前处理-超高效液相色谱/质谱在线分析系统用于血清中十种抗精神病药的直接检测 LCMSMS-171 摘要:本文建立了自动前处理-超高效液相色谱/质谱在线分析系统用于血清中十种抗精神病药的直接检测方法。在最优条件下不同浓度的精密度实验得到的保留时间和峰面积相对标准偏差分别在0.01~0.06%和1.12~4.54%之间;方法检出限和方法定量限分别介于 0.000801~0.688 ug/L 和0.00321~2.75 ug/L 之间。对两种浓度级别加标血清样品进行检测,回收率介于58.75~136.75%之间, RSD 介于 0.87~7.69%之间。本法无需前处理,全程自动化运行,对比离线方法,在线方法10 min 内完成自动前处理和色谱分离检测,允许强溶剂的大体积进样,灵敏度高、精密度好。 关键词:抗精神病药自动前处理在线分析三重四极杆质谱仪 利培酮、奋乃静等抗精神病药,可以改善精神分裂症,临床应用广泛,且疗效显著。但由于其可引起药源性锥体外系反应如帕金森综合症、静坐不能、急性肌张力障碍等副作用,服用过量将伴有失眠、焦虑、激越、头痛、口干等副作用,严重者可能导致心源性猝死,因此建立血液中抗精神病药的检测在临床检验、法医学鉴定等领域有重要意义。 一般血液样品处理成血清或血浆后,需用蛋白沉淀的方式提取上清液进样分析。对于样品量多、人手紧张、要求快速出数据的用户,如此手工前处理存在诸多不便且数据误差大。本文使用岛津自动前处理-超高效液相色谱/质谱在线分析系统(流路设计见图1),只需进行过滤处理,即可对血清中十种抗精神病药进行自动分析。 图1自动前处理-超高效液相色谱质谱在线分析系统的流路设计 实验部分 1.1仪器配置 表1仪器配置 硬件 配置 控制器 CBM-20A 泵C&D LC-20AD 泵D溶剂切换阀 FCV-11AL,初始状态为 A:泵D1(上样液) , 泵C1(解吸液)送 液;B状态为泵D2(平衡液),泵C1送液 泵A&B LC-30AD 自动进样器 SIL-30AC 柱温箱 CTO-20AC,内置切换阀1和切换阀2 切换阀1 FCV-20AH2,初始状态=1:2-3口、6-1-4-5口分别联通 切换阀2 FCV-32AH, 初始状态=1:2-3口、6-1-4-5口分别联通 脱气机 DGU-20A52 切换阀3 无 混合器1 LC2010 柱前混合器, SN 228-37112-91 混合器2 LC-30A 混合器 MiRC 20uL 过滤器 0.5 um 虑孔,零死体积在线过滤器SN 290-46042-06 定量环1 500 pL 不锈定定量环 定量环2 无 PDA SPD-M20A MS LCMS-8040 工作站 LabSolutions Ver. 5.60 1.2分析条件 流速:0.5mL/min 萃取、解吸条件 萃取柱: Shim-pack MAYI-C8(G) 10 Lx4.6 萃取溶液:甲酸/水/乙腈(0.2/95/5, v/v) 流速:2mL/min 柱温:40℃ 进样体积:50pL 萃取时间:2 min 解吸溶液:乙腈/甲醇(80/20, v/v) 解吸流速:0.2mL/min 平衡溶剂:甲醇 平衡流速:2mL/min 切阀时间、清洗程序:将时间程序表2 液相色谱条件 色谱柱: Shim-pack XR-ODS ⅢI, 2.0 mmx50 mm L,1.6 um粒径 流动相:A相-0.1%甲酸+5 mM乙酸铵水溶容; B相-乙腈 柱温:40℃ 洗脱方式:梯度洗脱,B相初始浓度为8%,时间程序见表2。 质谱条件 分析仪器::LCMS-8040 离子源: ESI,正离子扫描 离子源接口电压:4.5kV 雾化气:氮气3.0L/min 干燥气:氮气15 L/min 碰撞气:氩气 脱溶剂管温度:250℃ 加热模块温度:400℃ 扫描模式:多反应监测(MRM) 驻留时间:12ms 延迟时间:3ms 喷针位置:+3mm MRM参数:见表3 Time(min) Module Command Value 2.00 Column Oven CTO.RVL 0 3.40 Pumps SV(Pump C) B 3.50 Column Oven CTO.RVR 0 3.60 Column Oven CTO.RVL 1 4.50 Pumps Pump B Conc. 8 8.50 Column Oven CTO.RVR 1 8.50 Pumps Pump B Conc. 60 8.50 Pumps SV(Pump C) A 8.60 Pumps Pump B Conc. 100 9.98 Pumps Pump B Conc. 100 9.99 Pumps Pump B Conc. 8 10.00 Controller Stop 表3MRM参数 名称 CAS 前体离子 产物离子 Q1 Pre Bias(V) CE(V) Q3 Pre Bias(V) 利培酮 411.20 191.15 -30.0 -34.0 -20.0 106266-06-2 110.15 -30.0 -51.0 -20.0 194.05 -15.0 -28.0 -20.0 齐拉西酮 146939-27-7 413.10 159.10 -15.0 -43.0 -30.0 喹硫平 111974-69-7 384.15 253.20 -30.0 -23.0 -27.0 221.20 -30.0 -39.0 -23.0 氟哌啶醇 52-86-8 376.15 165.20 -30.0 -25.0 -17.0 123.20 -30.0 -41.0 -22.0 阿立哌唑 129722-12-9 448.15 285.20 -22.0 -27.0 -20.0 176.20 -22.0 -34.0 -18.0 氯丙嗪 50-53-3 319.10 86.20 -22.0 -22.0 -16.0 58.20 -22.0 -38.0 -23.0 舍曲林 79617-96-2 306.05 159.10) -30.0 -26.0 -30.0 275.10 -30.0 -12.0 -19.0 奋乃静 58-38-8 404.10 171.15 -20.0 -24.0 -18.0 143.10 -20.0 -30.0 -26.0 氯硝安定 1622-61-3 316.00 270.05 -23.0 -25.0 -28.0 214.05 -23.0 -39.0 -21.0 阿普唑仑 28981-97-7 309.20 281.10 -24.0 -27.0 -29.0 205.10 -24.0 -42.0 -20.0 *表示定量离子 1.3样品制备 标准样品配制:分别用乙腈和水配制如表4种8个浓度级别的混合标准溶液(表4)。 表4标样配制浓度 化合物 浓度级别(ug/L) 1 2 3 4 5 6 7 8 利培酮 0.00800 0.0200 0.0400 0.0800 0.200 0.400 0.800 2.00 齐拉西酮 0.0400 0.100 0.200 0.400 1.00 2.00 4.00 10.0 喹硫平 0.0200 0.0500 0.100 0.200 0.500 1.00 2.00 5.00 氟哌啶醇 0.0200 0.0500 0.100 0.200 0.500 1.00 2.00 5.00 阿立哌唑 0.0800 0.200 0.400 0.800 2.00 4.00 8.00 20.0 氯丙嗪 0.00800 0.0200 0.0400 0.0800 0.200 0.400 0.800 2.00 舍曲林 0.400 1.00 2.00 4.00 10.0 20.0 40.0 100 奋乃静 0.400 1.00 2.00 4.00 10.0 20.0 40.0 100 氯硝安定 5.00 12.5 25.0 50.0 125 250 500 1.25E+03 阿普唑仑 4.00 10.0 20.0 40.0 100 200 400 1.00E+03 在线方法样品前处理:血清过滤后进样。 离线方法样品前处理:取 50pL 血清加入150pL乙腈, 涡旋3 min 后于 12000 rpm 高速离心5 min, 取上清液用乙腈定容至 200pL 待测。 结果讨论 2.1优化萃取条件和解吸条件 对萃取溶剂进行优化,选取5mM乙酸铵水溶液/乙腈(95/5, v/v),乙酸/水/乙腈(0.2/95/5),水/乙腈进行优化,最终选取乙酸/水/乙腈(0.2/95/5)作为最优萃取溶剂。 对萃取流速进行优化,选择2 mL/min, 3 mL/min, 4 mL/min 进行优化,最终选取2 mL/min 作为最优萃取流速。 对萃取时间进行优化,设置1 min, 2 min,3 min 作为萃取时间,最终选取 2 min 作为萃取时间。 对解吸溶剂进行优化,选取甲酸/甲醇(0.1/99.5, v/v),甲酸/乙腈(0.1/99.5, v/v),100%甲醇,100%乙腈,甲醇/乙腈(20/80, v/v),甲醇/乙腈(50/50, v/v),甲醇/乙腈(80/20, v/v), 作为解吸溶剂,终选取甲醇/乙腈(20/80,v/v) 作为最优萃取溶剂。 对解吸速度进行优化,选取0.2 mL/min, 0.3 mL/min 和 0.4 mL/min 进行优化,最终选取0.2 mL/min 作为最优流速。 对切换阀2的切阀时间进行优化,选取3.0~4.0 min( 间隔0.1 min )进行优化,最终选取3.5 min作为最优切阀时间。 对泵C平衡溶液进行优化,选取100%水,100%甲醇,100%乙腈,甲醇/水(50/50,v/v),乙腈/水(50/50,v/v)进行优化,最终选取100%甲醇作为泵C平衡溶液。 2.2标准样品的MRM色谱图 混合标准样品的 MRM色谱图如图2所示。 图2十种生长素标准样品的 MRM色谱图(浓度级别1:0.00800~5.00 ug/L) 2.37标准曲线和检出限 按1.2中的分析条件进行测定,外标法制作校准曲线,如图3所示线性良好。线性方程、相关系数、线线范围、检出限和定量限见表5:十种抗精神病药的线性相关系数均大于0.9972,检出限介于0.000801~0.688 ug/L,定量限介于 0.00321~2.75 ug/L 之间。 图3利培酮、喹硫平和氯丙嗪的标准工作曲线 表510种物质的校准曲线参数 名称 校准曲线 相关系数 线性范围 检出限 定量限 (ug/L) (ug/L) 利培酮 Y=(1.82282e+007)X+(2499.88) 0.9999 0.00800~2.00 0.000801 0.00321 齐拉西酮 Y=(1.70074e+006)X+(4452.61 0.9988 0.0400~4.00 0.00891 0.0356 喹硫平 Y=(3.09441e+006)X+(5194.65 0.9992 0.0500~0.500 0.00572 0.0229 氟哌啶醇 Y=(4.31181e+006)X+(9916.14) 0.9972 0.0200~2.00 0.00412 0.0165 阿立哌唑 Y=(553682)X+(6811.70) 0.9984 0.0800~20.0 0.0254 0.102 氯丙嗪 Y=(7.32360e+006)X+(4106.56 0.9993 0.00800~2.00 0.00185 0.00740 舍曲林 Y=(218658)X+(5283.00) 0.9986 0.400~100 0.142 0.569 奋乃静 Y=(88445.5)X+(2474.88) 0.9984 1.00~100 0.0722 0.289 氯硝安定 Y=(101919)X+(6994.22) 0.9994 5.00~125E+03 0.688 2.75 阿普唑仑 Y=(92225.7)X+(21083.5) 0.9982 4.00~100E+03 0.573 2.29 级别2浓度标样重复进样7次,计算浓度标准偏差SD,计算方法检出限MDL=3.14×S;**方法定量限MQL=4XMDL. 2.4精密度实验 对表6中三个浓度级别的标样进行分析,平行进样6次。十种抗精神病药的保留时间和峰面积的相对标准偏差分别在0.01~0.06%和1.12~4.54%之间,仪器精密度良好。 表6保留时间和峰面积重复性结果(n=6) 目标物 RSD%(级别2) RSD%(级别5) RSD% (级别8) R.T Area R.T Area R.T Area 利培酮 0.06 1.39 0.02 3.12 0.04 2.39 齐拉西酮 0.05 2.76 0.02 3.18 0.04 2.61 喹硫平 0.06 3.60 0.01 2.97 0.04 2.19 氟哌啶醇 0.06 2.47 0.02 1.12 0.05 2.78 阿立哌唑 0.06 3.83 0.02 3.73 0.04 2.69 氯丙嗪 0.06 2.96 0.01 3.01 0.04 2.66 舍曲林 0.05 4.54 0.01 3.07 0.04 2.12 奋乃静 0.05 2.21 0.01 1.53 0.03 3.49 氯硝安定 0.05 1.66 0.01 1.42 0.04 2.06 阿普唑仑 0.04 1.80 0.02 2.29 0.04 2.21 2.5与离线方法的比较 图4离线方法进样50uL乙腈提取液得到MRM色谱图(级别3加标浓度) 图5在线方法进样50pL乙腈提取液得到MRM色谱图(级别3加标浓度) 离线方法前处理使用乙腈作为沉淀剂去除蛋白,高速离心后得到的上清液主要成分为乙腈。图4为离线方法进样50uL乙腈提取液得到 MRM 色谱图,由图可知,大体积的强洗脱剂乙腈进入 ODS 色谱柱后产生显著的溶剂效应,十种抗精神病药都被分成两个峰,前一个随乙腈在死时间出峰,后一个产生严重的前拖尾;图5为在线方法进样 50uL乙腈提取液得到 MRM 色谱图,由于系统具有大体积进样二步稀释的功能,得到的色谱峰尖锐、对称,峰宽均少于6s。 2.6 基质加标实验 在血清样品中添加浓度级别3和级别7的混合标样,分析结果如图7所示,图6为空白血清。对两种浓度级别加标血清样品进行检测,回收率介于 58.75~136.75%之间, RSD 介于0.87~7.69%之间,具体检测值和回收率见表7。从表7中可以看出,齐拉西酮在两个加标浓度下回收率都是最低的,分析可能是其与血清中蛋白有较强的结合能力,导致其萃取、解吸比例较小,最终得到较低的回收率。 图6空白血清 图7级别3浓度加标样品MRM色谱图 表7血清样品检测量和回收率(n=3) 空白 加标回收率(级别3) 加标回收率(级别7) 目标物 检出量 RSD 平均回收率 RSD 平均回收率 (ug/L) (%) (%) (%) (%) 利培酮 ND 4.04 103.04 1.56 136.75 齐拉西酮 ND 3.78 58.75 1.56 83.17 喹硫平 ND 7.45 108.00 1.17 128.00 氟哌啶醇 ND 1.93 93.50 0.87 132.67 阿立哌唑 ND 3.33 98.00 3.85 112.50 氯丙嗪 ND 7.48 125.04 6.39 110.42 舍曲林 ND 2.64 101.33 1.24 116.83 奋乃静 ND 3.14 112.25 7.69 109.67 氯硝安定 ND 1.78 75.93 1.24 98.67 阿普唑仑 ND 6.54 82.00 1.43 112.33 *ND 为未检出 结论 建立了自动前处理-超高效液相色谱/质谱在线分析系统直接测定血清中十种抗精神病药的方法。对萃取条件、解吸条件、自动化控制时间程序进行优化,在最优条件下不同不度的精密度实验得到的保留时间和峰面积 RSD分别在 0.01~0.06%和1.12~4.54%之间;十种抗精神病药的线性相关系数均大于0.9972,方法检出限和方法定量限分别介于0.000801~0.688 ug/L 和 0.00321~2.75 ug/L 之间。对两种浓度级别加标血清样品进行检测,回收率介于58.75~136.75%之间, RSD 介于 0.87~7.69%之间。结果表明本在线方法无需对血清样品做任何处理,即可对分析物进行直接检测。对比离线方法,在线方法10 min 内完成整个分析,允许强溶剂的大体积进样,全程全自动分析,灵敏度高、精密度好。 岛津建立了自动前处理-超高效液相色谱/质谱在线分析系统直接测定血清中十种抗精神病药的方法。对萃取条件、解吸条件、自动化控制时间程序进行优化,在最优条件下不同浓度的精密度实验得到的保留时间和峰面积RSD分别在0.01~0.06%和1.12 ~4.54%之间;十种抗精神病药的线性相关系数均大于0.9972,方法检出限和方法定量限分别介于0.000801~0.688 μg/L和0.00321~2.75 μg/L之间。对两种浓度级别加标血清样品进行检测,回收率介于58.75~136.75%之间,RSD介于0.87~7.69%之间。本在线方法无需对血清样品做任何处理,即可对分析物进行直接检测。对比离线方法,在线方法10 min内完成整个分析,允许强溶剂的大体积进样,全程全自动分析,灵敏度高、精密度好。
确定


还剩6页未读,是否继续阅读?
岛津企业管理(中国)有限公司为您提供《血清中十种抗精神病药检测方案(液质联用仪)》,该方案主要用于全血/血清/血浆中十种抗精神病药检测,参考标准--,《血清中十种抗精神病药检测方案(液质联用仪)》用到的仪器有岛津三重四极杆液相色谱质谱联用仪LCMS-8040
推荐专场
相关方案
更多
该厂商其他方案
更多















