
药物杂质是活性药物成分 (API) 或药品制剂中不希望存在的化学成分。原料药中的杂质可能源于合成过程或原料、中间体、试剂、溶剂、催化剂以及反应副产物等其他来源。在药品开发过程中,杂质可能:
• 由于原料药固有的不稳定性而形成
• 由于与加入的辅料不相容而产生,或
• 与包装材料和容器密封系统 (CCS) 相互作用而产生
原料药中各种杂质的含量决定了最终成品药物的安全性。因此,杂质的鉴定、定量、定性和控制已成为药物开发过程的关键组成部分。
很多监管机构都在关注杂质的控制:
• 国际协调会议 (ICH)
• 美国食品药品监督管理局 (USFDA)
• 欧洲药品管理局 (EMA)
• 加拿大药品与健康管理局
• 日本药物和医疗器械管理局 (PMDA)
• 澳大利亚卫生和老龄治疗商品管理局
此外,很多官方药典(如英国药典 (BP)、美国药典 (USP)、日本药典 (JP)、欧洲药典 (EP) 和中华人民共和国药典 (ChP))也越来越多地加入了对 API 和药品制剂中杂质限量水平的规定。这些法规以暴露限值为依据,因此必须对施用时最终剂型中的污染物浓度进行控制。在实践中,这意味着药物制造商必须进行风险评估,考虑到制造后(如包装、运输和 CCS)的污染源以及来自原料和生产过程的污染。
方案详情

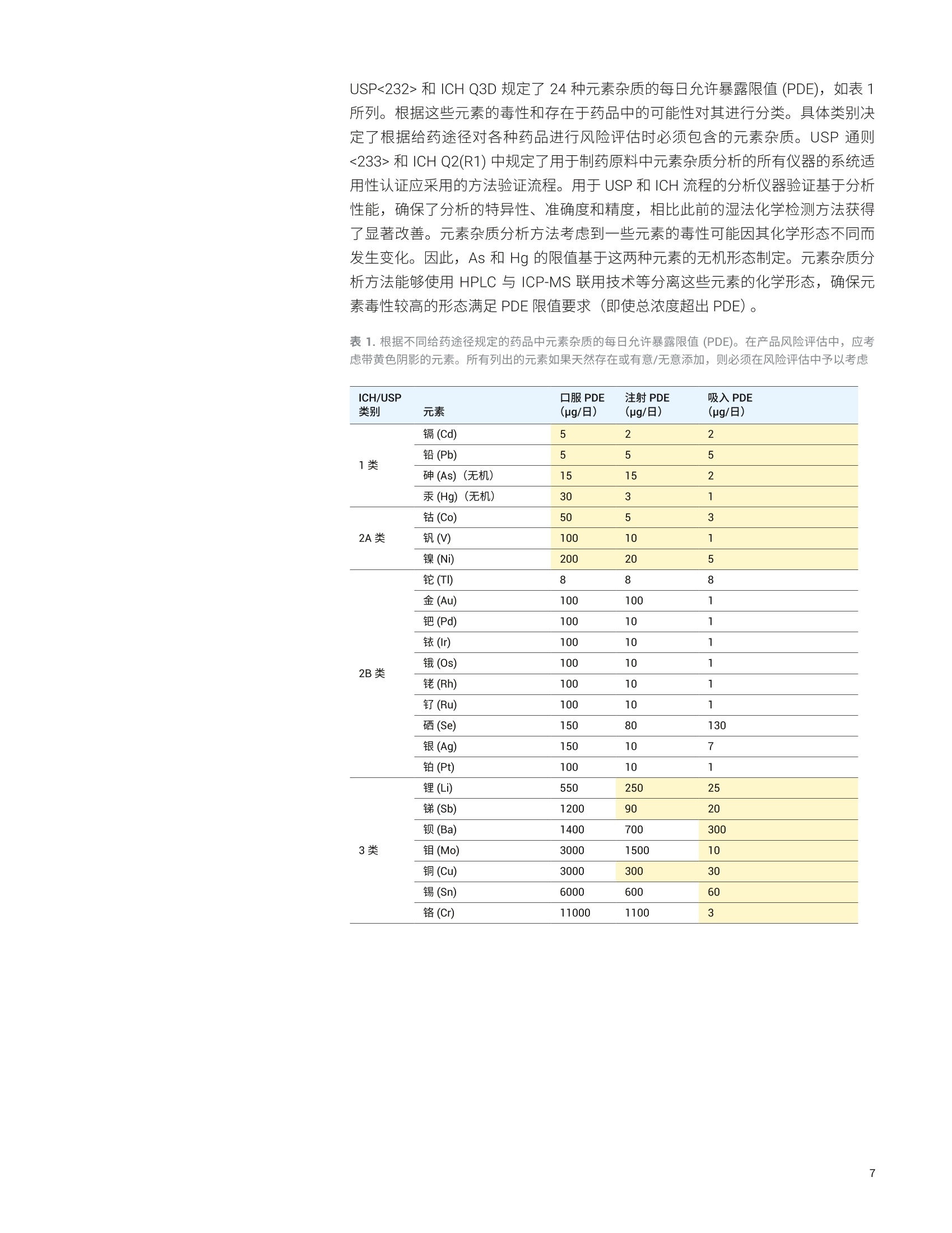
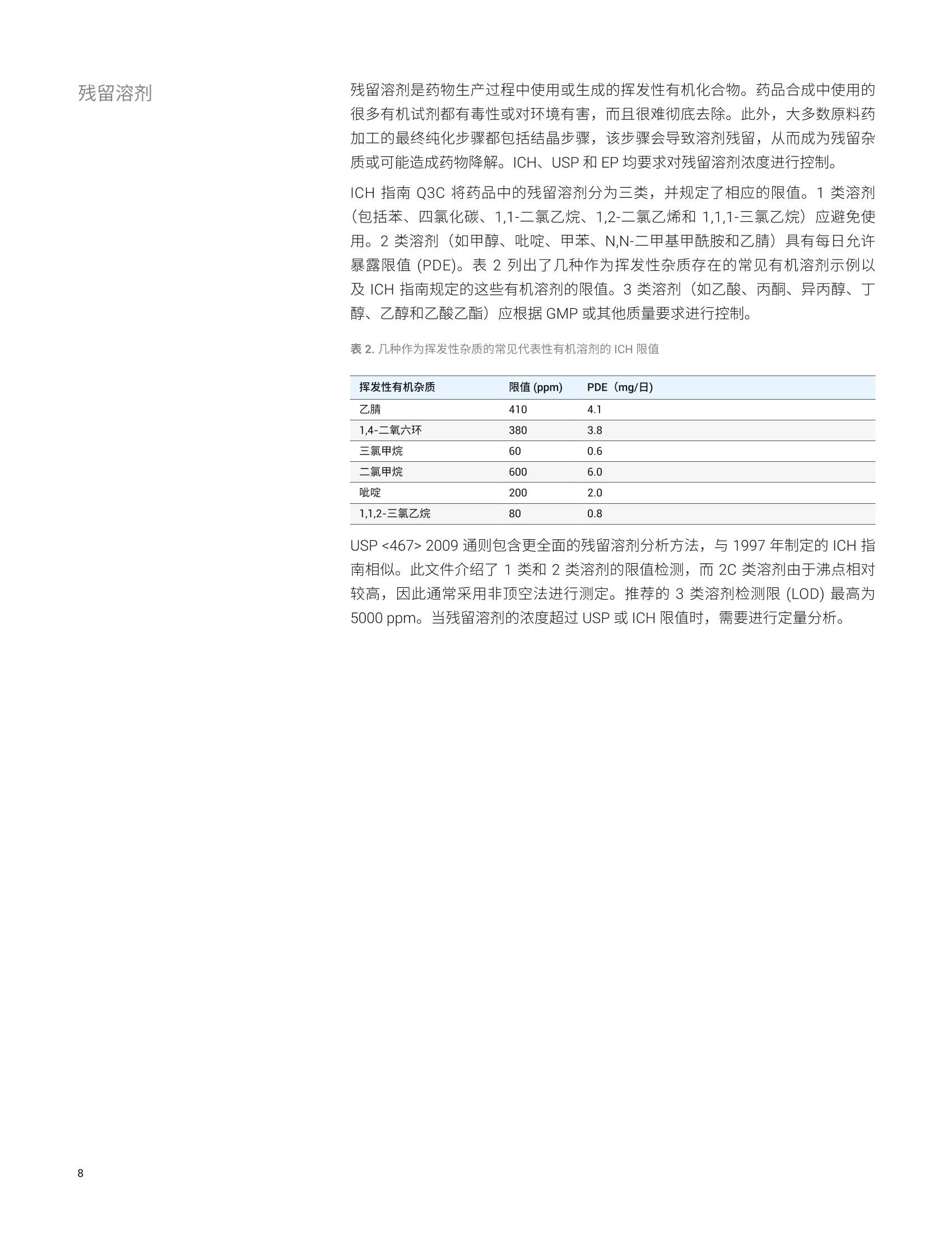
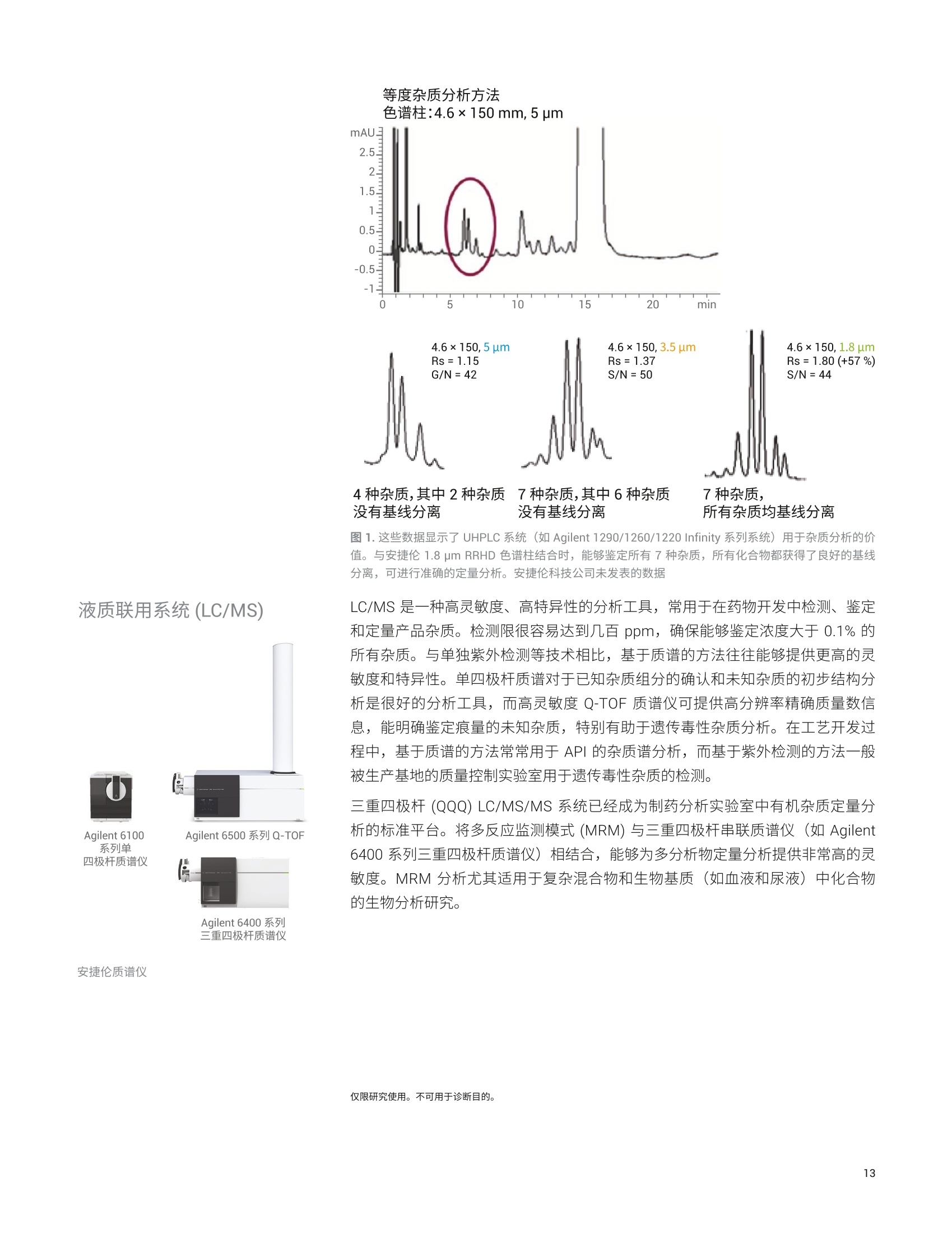
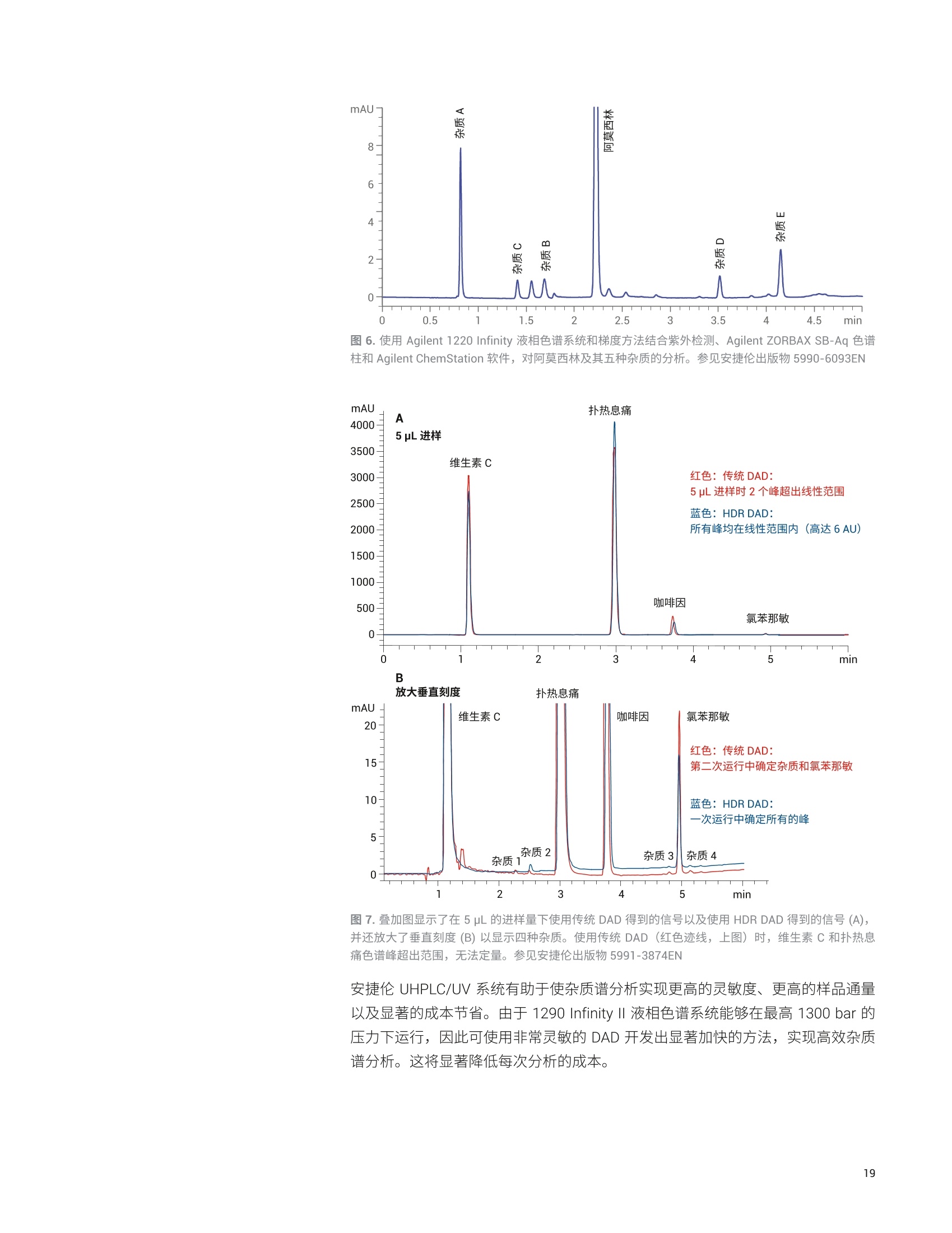
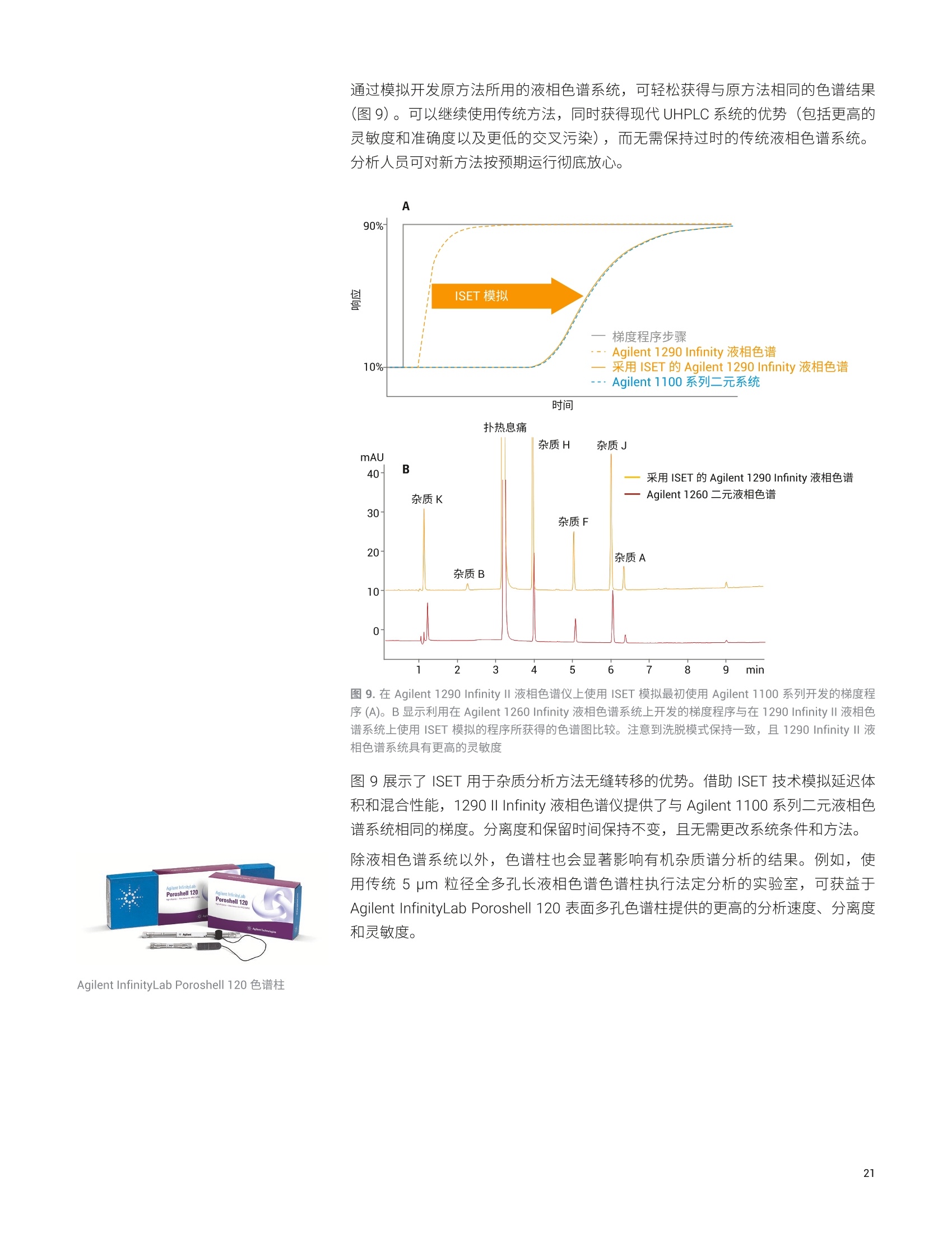
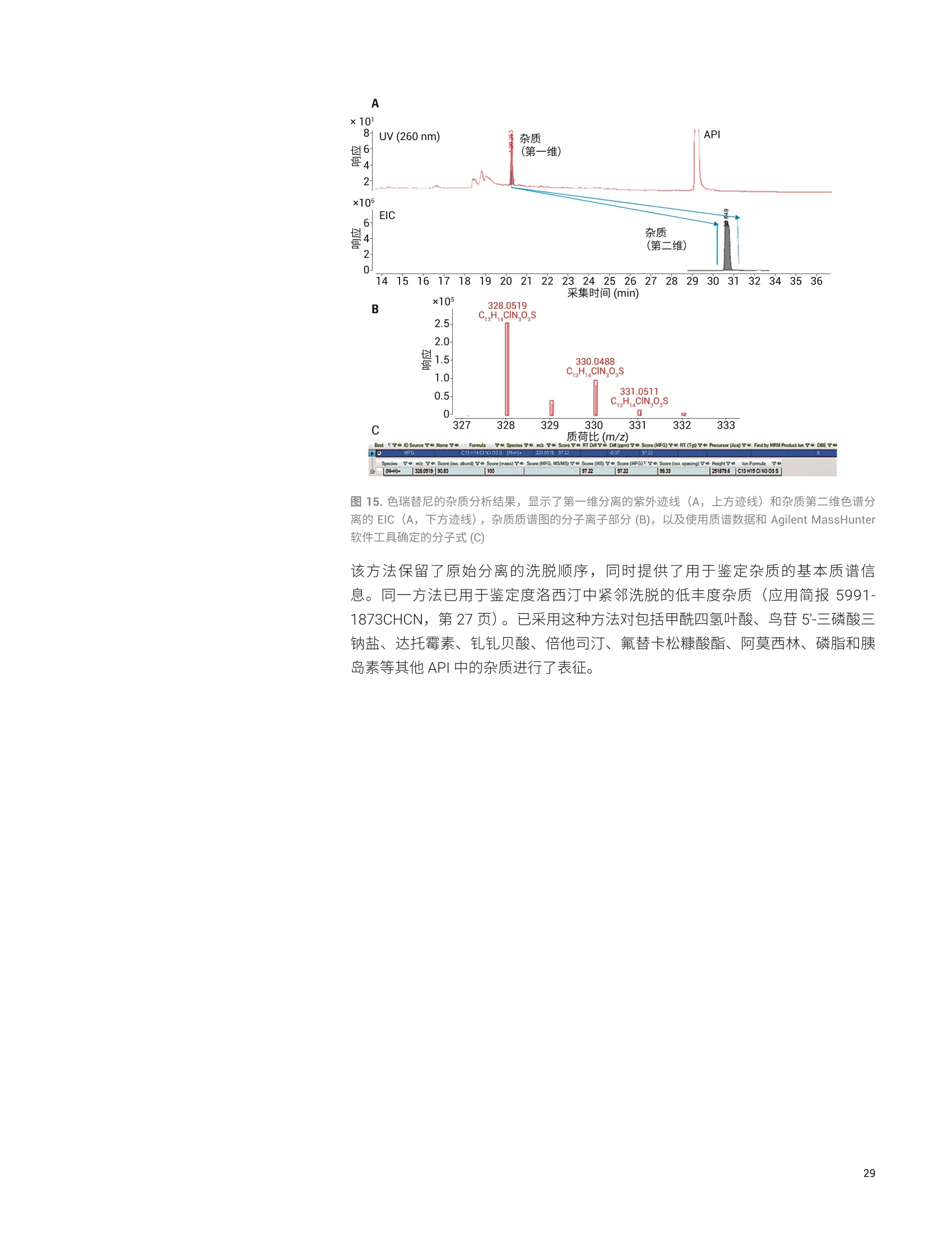
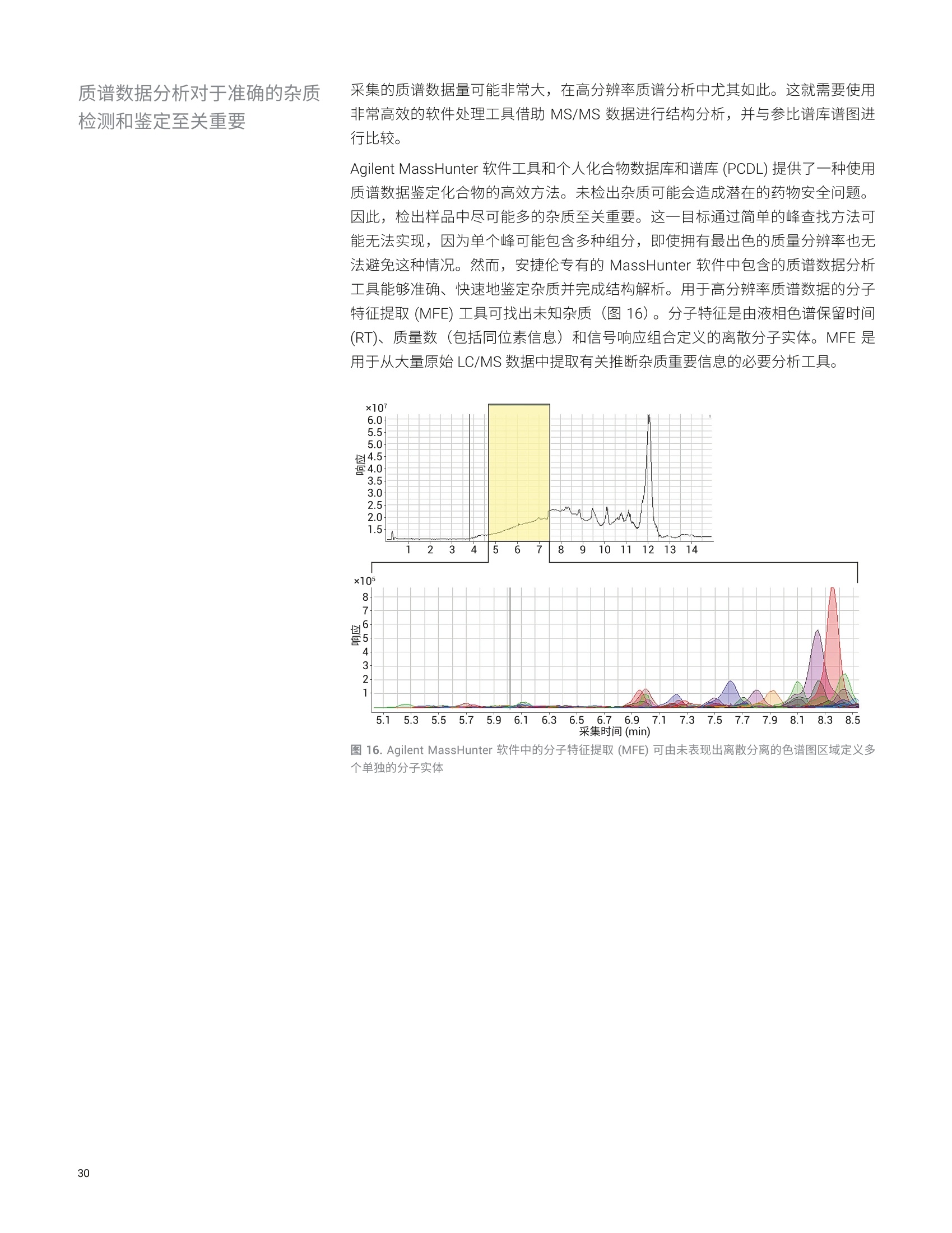
目录 残留溶剂 Trusted Answers 基础导论 1.:药物杂质分析一概述和法规现状 5 1.1药物杂质的三个主要类别 6 有机杂质 6 无机(元素)杂质 6 残留溶剂 8 1.2药品杂质控制的代表性出版物和指南 9 2..用于药物开发中杂质谱分析的分析技术 11 概述 11 2.1制备型液相色谱 (LC) 12 液相色谱和紫外检测 (LC/UV) 12 液质联用系统 (LC/MS) 13 2.2气相色谱 (GC) 14 2.3毛细管电电(CE) 14 2.4电感耦合等离子体发射光谱 (ICP-OES) 和电感耦合 等离子体质谱(ICP-MS) 15 ICP-OES 15 ICP-MS 15 ICP-MS/MS 16 2.5超临界流体色谱 (SFC) 16 2.6傅立叶变换红外光谱仪(FTIR) 17 3..针对三类主要杂质的一系列安捷伦应用解决方案概述 BB 3.1有机杂质分析 18 用于药物中有机杂质的严格分析的LC/MS系统 24 使用单四极杆 LC/MS仪进行经济有效的高性能杂质分析 24 使用安捷伦液相色谱/三重四极杆质谱联用仪对 API 中的 杂质进行灵敏、可靠的分析 25 使用安捷伦 LC/TOF 和 LC/Q-TOF仪器提高痕量杂质鉴定的分析效率 27 使用 2D-LC/MS优化方法转移以实现质谱兼容性 28 质谱数据分析对于准确的杂质检测和鉴定至关重要 30 安捷伦有机杂质谱分析资源 33 3.2无机杂质分析 34 安捷伦元素杂质分析出版物 36 3.3残留溶剂分析 36 安捷伦残留溶剂分析出版物 38 4.2色谱柱与备件 40 4.3软件与信息学产品 40 4.4实验室法规认证和法规认证咨询 40 药物杂质是活性药物成分(API)或药品制剂中不希望存在的化学成分。原料药中的杂质可能源于合成过程或原料、中间体、试剂、溶剂、催化剂以及反应副产物等其他来源。在药品开发过程中,杂质可能: 由于原料药固有的不稳定性而形成 ,由于与加入的辅料不相容而产生,或,与包装材料和容器密封系统 (CCS) 相互作用而产生 原料药中各种杂质的含量决定了最终成品药物的安全性。因此,杂质的鉴定、定量、定性和控制已成为药物开发过程的关键组成部分。 很多监管机构都在关注杂质的控制: ·国际协调会议(ICH) 美国食品药品监督管理局(USFDA) 区欧洲药品管理局(EMA) ,加拿大药品与健康管理局 日本药物和医疗器械管理局(PMDA) 澳大利亚卫生和老龄治疗商品管理局 此外,很多官方药典(如英国药典(BP)、美国药典 (USP)、日本药典(JP)、欧洲药典(EP)和中华人民共和国药典 (ChP))也越来越多地加入了对 API和药品制剂中杂质限量水平的规定。这些法规以暴露限值为依据,因此必须对施用时最终剂型中的污染物浓度进行控制。在实践中,这意味着药物制造商必须进行风险评估,考虑到制造后(如包装、运输和 CCS) 的污染源以及来自原料和生产过程的污染。 药物杂质的三个主要类别 ICH 指南将原料药相关杂质分为三个大类:有机杂质、无机杂质和溶剂残留。 有机杂质可能来源于 API或药品制剂的生产过程,也可能来源于原料药的储存过程。它们可能是已知、未知、挥发或不挥发的化合物,其来源包括原料、中间体、意外副产物和降解产物。它们也可能来自于对映体间的消旋或污染。所有这些情况下产生的杂质都有可能导致不良的生物活性或毒性。 最近,遗传毒性药物杂质引起了监管机构和制药企业的广泛关注。一般来说,遗传毒性杂质包括可能直接破坏 DNA 的 DNA 活性物质。潜在遗传毒性杂质包括痕量工艺杂质或降解物,这些杂质产生于药物生产和储存过程中。根据 FDA 和EMA指南的规定,潜在遗传毒性杂质的控制浓度远低于一般杂质。药物中遗传毒性杂质的建议接受阈值可以参见 USFDA 和 EMA 发布的指南文件(参见本章最后提供的代表性重要出版物列表)。有关遗传毒性杂质的 ICH M7 指南正在制定中,暂定名称为“M7评估和控制药品中的 DNA 活性(致突变性)杂质以防范潜在的致癌风险”。 元素杂质是药物制剂中存在的不需要的元素。它们可能来源于活性药物成分、原料、合成添加剂、辅料、催化剂、生产过程以及制造过程中使用的设备。监管机构要求药物制造商执行风险评估,确保对最终药品中的此类杂质进行监测和控制。伟造商还必须评估来自包装、容器密封系统和给药系统的潜在污染源,且必须使用可萃取物与可浸出物(E&L)评估对这些污染物进行鉴定和定量。必须对所有药品中四种毒性最高的元素杂质浓度进行测定,即As、Cd、Hg 和Pb。生产过程中可能加入另外一些元素;必须对成品药中的这些杂质进行监测。除原料以外,其他潜在的无机杂质来源包括配体、催化剂等生产过程试剂(如铂族元素(PGE))、来源于其他生产阶段的金属((如工艺用水和不锈钢反应容器)、活性炭以及过滤材料中的元素。 用于检测元素杂质的美国药典 (USP) 流程(通则 USP<232>) 已经与人用药品注册技术国际协调会议(ICH) 指南 Q3D 协调。新流程取代了现有的比色和湿化学检测方法(如USP 重金属限值检测 (USP<231>)) 和EP中的重金属章节2.4.8,这两种现有的检测方法已被公认在范围、准确度、灵敏度和特异性方面无法满足要求。USP 还引入了仅适用于膳食补充剂的相关元素杂质检测方法<2232>。 USP<232>和 ICH Q3D 规定了24种元素杂质的每日允许暴露限值(PDE), 如表1所列。根据这些元素的毒性和存在于药品中的可能性对其进行分类。具体类别决定了根据给药途径对各种药品进行风险评估时必须包含的元素杂质。USP 通则<233>和 ICH Q2(R1)中规定了用于制药原料中元素杂质分析的所有仪器的系统适用性认证应采用的方法验证流程。用于 USP 和 ICH流程的分析仪器验证基于分析性能,确保了分析的特异性、准确度和精度,相比此前的湿法化学检测方法获得了显著改善。元素杂质分析方法考虑到一些元素的毒性可能因其化学形态不同而发生变化。因此, As 和 Hg 的限值基于这两种元素的无机形态制定。元素杂杂分析方法能够使用 HPLC 与 ICP-MS联用技术等分离这些元素的化学形态,确保元素毒性较高的形态满足 PDE限值值求(即使总浓度超出 PDE)。 表1.根据不同给药途径规定的药品中元素杂质的每日允许暴露限值 (PDE)。在产品风险评估中,应考虑带黄色阴影的元素。所有列出的元素如果天然存在或有意/无意添加,则必须在风险评估中予以考虑 ICH/USP 口服PDE 注射 PDE 吸入 PDE 类别 元素 (pg/日) (pg/日) (pg/日) 镉(Cd) 5 2 2 1类 铅(Pb) 5 5 5 砷(As)(无机) 15 15 2 汞(Hg)(无机) 30 3 1 2A类 钴(Co) 50 5 3 钒(V) 100 10 1 镍(Ni) 200 20 5 铊(TI) 8 8 8 金 (Au) 100 100 1 钯 (Pd) 100 10 1 铱 (Ir) 100 10 1 2B类 (Os) 100 10 1 铑(Rh) 100 10 1 钉 (Ru) 100 10 1 硒 (Se) 150 80 130 银(Ag) 150 10 7 铂 (Pt) 100 10 1 锂(Li) 550 250 25 锑 (Sb) 1200 90 20 3类 (Ba) 1400 700 300 钼(Mo) 3000 1500 10 铜(Cu) 3000 300 30 锡 (Sn) 6000 600 60 铬(Cr) 11000 1100 3 残留溶剂是药物生产过程中使用或生成的挥发性有机化合物。药品合成中使用的很多有机试剂都有毒性或对环境有害,而且很难彻底去除。此外,大多数原料药加工的最终纯化步骤都包括结晶步骤,该步骤会导致溶剂残留,从而成为残留杂质或可能造成药物降解。ICH、USP和EP均要求对残留溶剂浓度进行控制。 ICH 指南 Q3C将药品中的残留溶剂分为三类,并规定了相应的限值。,1类溶剂(包括苯、四氯化碳、1.1,1-二氯乙烷、1,2-二氯乙烯和1,1,1-三氯乙烷)应避免使用。2类溶剂(如甲醇、吡啶、、甲苯、N,N-二甲基甲酰胺和乙腈)具有每日允许暴露限值(PDE)。表2列出了几种作为挥发性杂质存在的常见有机溶剂示例以及 ICH 指南规定的这些有机溶剂的限值。3类溶剂(如乙酸、丙酮、异丙醇、丁醇、乙醇和乙酸乙酯)应根据 GMP 或其他质量要求进行控制。 表2.几种作为挥发性杂质的常见代表性有机溶剂的 ICH 限值 挥发性有机杂质 限值(ppm) PDE (mg/日) 乙腈 410 4.1 1,4-二氧六环 380 3.8 三氯甲烷 60 0.6 二氯甲烷 600 6.0 吡啶 200 2.0 1,1,2-三氯乙烷 80 0.8 USP <467> 2009 通则包含更全面的残留溶剂分析方法,与1997年制定的ICH指南相似。此文件介绍了1类和2类溶剂的限值检测,而2C类溶剂由于沸点相对较高,因此通常采用非顶空法进行测定。推荐的3类溶剂检测限(LOD) 最高为5000 ppm。当残留溶剂的浓度超过 USP 或 ICH限值时,需要进行定量分析。 药品杂质控制的代表性出版物和指南 注:本文件所涉及杂质的法规限值仅作为示例提供,可能不包含需要的完整信息。有关完整现行法规信息和最新动态,请参见各监管机构的网站。 国际协调会议(ICH)三方协调指南Q8(R2):药物开发,2009年8月 注:此列表仅列出了部分近期发布的重要法规文件。有关完整现行法规信息和最新动态,请参见各监管机构的网站。 杂质谱是对原料药中存在的已鉴定和未鉴定杂质的描述(来源:行业指南Q3A,新原料药中的杂质)。杂质谱分析通常从杂质检测开始,然后是分离和表征。对于所有上述三类杂质,关键是在工艺开发过程中建立一种可靠的方法,要求该方法最终可以得到验证并能够转移到 QA/QC。针对受监管的极低浓度杂质(如遗传毒性杂质)开发可靠的分析方法,是这个过程的一大挑战。 为了更好地检测、鉴定、定量和表征原料药和药品中存在的杂质,制药科学家需要借助具有高灵敏度和高特异性的稳定分析工具。杂质分析的主要分析手段包括光谱、色谱、质谱以及它们的各种组合(即联用技术)。可以根据杂质的特性和分析所需的信息水平选择合适的技术。药物开发中各种复杂的分析问题往往需要采用多种分析技术才能解决。LC/UV、LC/MS、GC/MS、CE/MS 和 LC/UV等分析技术可提供正交检测和互补的信息,有助于高效解决这些难题。因此,这些技术在药物杂质谱分析(从未知杂质的鉴定到最终结构解析)中起到重要作用。 表3总结了一些杂质分析技术。有关杂质谱分析的主要单一技术和联用技术的详细介绍,请参见后续章节。 表3.杂质分析技术 杂质类型 技术 有机杂质 FTIR、制备型 LC、LC/UV、LC/MS (SQ、Q-TOF和QQQ)、CE和 SFC 无机/元素杂质 ICP-OES 和 ICP-MS 有关缩写的定义,请参见后续章节。 制备型液相色谱(LC) Agilent 1260 Infinity Ⅱ制备型 LC/MSD 系统 液相色谱和紫外检测 (LC/UV) Agilent InfinityLab 系列液相色谱仪和色谱柱 原料药中的杂质浓度一般较低,因此必须将杂质分离后才能进行详细分析。这是制药实验室面临的一项重大挑战。制备型液相色谱有助于(通常从APl结晶后剩余的溶液等富含杂质的分析物中)分离出足够量的杂质,以使用FTIR、NMR、LC/MS 或 GC/MS等技术进行结构分析。 药物质量控制 (QC)实验室中的很多杂质分析方法将高效液相色谱 (HPLC) 与紫外检测联用 (HPLC/UV 法)。紫外检测可根据最大吸光度来鉴定药物中的杂质或降解物。此项技术具有高选择性(可通过单一分析流程对样品中的多个不同组分进行定量测定),是目前用于杂质谱分析最重要、最通用的分析方法,尤其适用于存在标准品的常规分析。固定相系统可在若干种操作模式(如离子对、增强疏水作用)和变化的 pH条件下操作,能够根据各种样品的独特性质对它们进行同时分析。高分离度 LC/UV分析对于杂质检测非常有用,它能准确鉴定所有杂质。 针对分析型液相色谱的 Agilent InfinityLab 解决方案包括高效 HPLC 和 UHPLC 系统,这些系统采用最新技术,同时保持与传统液相色谱仪完全兼容。 Agilent 1220Infinityll液相色谱仪能够以超值的价格提供高质量结果。 Agilent 1260 Infinity l液相色谱仪是一种灵活的仪器选择,有助于提高操作效率,其中1260 Infinity ⅡlPrime 液相色谱仪具有极高的操作便捷性。 Agilent 1290 Infinity lI液相色谱仪是新一代液相色谱仪的顶尖代表,具有超高性能,可提供出色的结果。1260 Infinity ⅡPrime 液相色谱仪是 1260 Infinity II液相色谱产品组合中功能最强大、最便捷的液相色谱仪,压力范围高达800 bar, 流速高达5 mL/min。这款色谱仪配备了成熟的1290 Infinity lI 液相色谱技术,为您的日常工作提供最佳的易用性和最丰富的功能。 液质联用系统 (LC/MS) Agilent 6100系列单四极杆质谱仪 Agilent 6400 系列三重四极杆质谱仪 等度杂质分析方法色谱柱:4.6×150mm, 5 um 4种杂质,其中2种杂质 7种杂质,其中6种杂质没有基线分离 没有基线分离 图1.这些数据显示了 UHPLC 系统(如 Agilent 1290/1260/1220 Infinity 系列系统)用于杂质分析的价值。与安捷伦1.8 um RRHD 色谱柱结合时,能够鉴定所有7种杂质,所有化合物都获得了良好的基线分离,可进行准确的定量分析。安捷伦科技公司未发表的数据 LC/MS是一种高灵敏度、高特异性的分析工具,常用于在药物开发中检测、鉴定和定量产品杂质。检测限很容易达到几百 ppm, 确保能够鉴定浓度大于 0.1%的所有杂质。与单独紫外检测等技术相比,基于质谱的方法往往能够提供更高的灵敏度和特异性。单四极杆质谱对于已知杂质组分的确认和未知杂质的初步结构分析是很好的分析工具,而高灵敏度 Q-TOF质谱仪可提供高分辨率精确质量数信息,能明确鉴定痕量的未知杂质,特别有助于遗传毒性杂质分析。在工艺开发过程中,基于质谱的方法常常用于 API的杂质谱分析,而基于紫外检测的方法一般被生产基地的质量控制实验室用于遗传毒性杂质的检测。 三重四极杆 (QQQ) LC/MS/MS 系统已经成为制药分析实验室中有机杂质定量分析的标准平台。将多反应监测模式 (MRM)与三重四极重串联质谱仪(如 Agilent6400系列三重四极杆质谱仪)相结合,能够为多分析物定量分析提供非常高的灵敏度。 MRM 分析尤其适用于复杂混合物和生物基质(如血液和尿液)中化合物的生物分析研究。 2.2气相色谱 (GC) Agilent 7890A 与 Agilent 5975C GC/MS系统相结合并配备 Agilent 7697A 顶空进样器 Agilent Intuvo 9000 气相色谱仪 Agilent Intuvo 气相色谱柱 2.3毛细管电泳(CE) 配备火焰离子检测器 (FID)的气相色谱仪是挥发性有机杂质(如残留溶剂)分析的标准选择。由于严格遵守 ICH Q3C 指南要求,气相色谱顶空方法为全世界的质量控制实验室广泛用于残留溶剂分析。通过静态顶空进行样品前处理和进样,有利于选择性地将挥发性溶剂引入色谱,而不会受到基本上不挥发的原料药或药品的污染。因此, FID 检测器能够很好地对残留溶剂进行鉴定和定量分析。气质联用系统 (GC/MS) 可用于确认和鉴定目的,突出了气相色谱技术的灵活性。 2.4 电感耦合等离子体发射光谱(ICP-OES) 和电感耦合等离子体质谱 (ICP-MS) |CP-OES Agilent 5110ICP-OES ICP-MS 图2.采用高浓度缓冲液和 25 um 鼓泡池毛细管对肝素和相关杂质进行毛细管电泳分析。参见安捷伦伦版物5990-3517CHCN USP和ICH协调的元素杂质分析方法 (ICHQ3D/Q2(R1) 和 USP<232>/<233>) 要求使用适当的特异性定量分析流程测定元素杂质的浓度。 USP<233>要求使用仪器方法,参考方法使用的是 ICP-MS 或 ICP-OES。对于这两种方法,可通过三种方式完成样品分析: 直接分析(非溶剂化) 样品前处理后溶于水性或有机溶剂中进行分析,或 使用密闭微波消解系统进行酸消解后分析 ICP-OES 能够使药品中受监管的大多数元素检测限达到 ppb 级,能够轻易满足样品直接分析或低倍稀释情况下的检测限要求。它还具有扩展的动态范围、稳定的等离子体,以及一步测定主要、微量和痕量元素的分析能力。因此, ICP-OES 可以满足众多用户的需求,包括寻求对散装原料和口服剂型药品中的元素杂质进行直接分析的低成本解决方案的用户。 ICP-MS是一种高灵敏度、高特异性的分析技术,能够对 ICH Q3D 和USP<232>中提出限值规定的所有24种元素进行可靠的痕量分析。ICP-MS的低检测限(通常为 ng/L (ppt))确保准确测定注射和吸入药物以及口服给药的原料药或药品中限值极低的所有受监管元素。即使在样品前处理过程中使用高倍样品稀释(例如可用的样品量非常少时),需要测定的所有分析物也能够在等于或低于规定浓度下轻松得到测定。 ICP-MS 还能与色谱分离技术(通常是HPLC)相结合,对元素的不同形态进行分离(或形态分析)。 Agilent 7800 和 7900 四极杆 ICP-MS 仪器能够有效地控制干扰物质,耐受变化的高浓度样品基质(包含有机溶剂),并具有宽动态范围,能够在一次运运中准确测量主要元素和痕量元素。安捷伦 ICP-MS 系统包含预设方法和设置向导、系统优化功能以及标准操作规程,有助于快速实施和验证常规药物分析。 Agilent 8900 ICP-MS/MS 2.5超临界流体色谱(SFC) Agilent 1260 Infinity II SFC 系统 虽然ICP-MS 和 ICP-OES 非常适合药品和组分中元素杂质的常规分析,但一些方法开发应用可获益于三重四极杆 ICP-MS (ICP-MS/MS) 的灵活性和高性能。与四极杆 ICP-MS相比,安捷伦 ICP-MS/MS 仪器提供了更出色的检测限,尤其适用于难以测定的元素 ((如S、P和Si),并在痕量元素((特别是复杂样品基质中)分析中具有优异的准确度。 SFC 使用超临界 CO,作为流动相,是一种可用于杂质检测的色谱分离技术,因为它具有与 HPLC 相当的灵敏度,而有机溶剂用量更低(图3)。 SFC 的另一个优势是手性化合物的分析,并有助于极低浓度杂质水平的对映体过量测定(图4)。 图3.主成分(A)咖啡因和(B)雌三醇中低浓度杂质 (0.05% w/w)的等度分离;0.01%浓度杂质的信噪比(S/N)远大于2-3(通常为LOD)。参见安捷伦出版物5990-6413EN 图4. SFC 对杂质浓度低于 0.05%的对映体过量的测定。浓度为5000 ppm 的 R-1,1'-联-2-萘酚(A)和S-1,1'-联-2-萘酚(B)的色谱图。参见安捷伦出版物5990-5969EN 傅立叶变换红外光谱仪 (FTIR) FTIR 能够为每种化合物提供独特的指纹图谱,因此对杂质或降解物的结构鉴定和确认非常有帮助。尤其在有机化合物分析中, FTIR 光谱可反映出分子结构和存在的官能团。反过来,官能团分析有助于在分析中鉴定化合物的结构并测定其浓度。通过比较纯标准物质的 FTIR 谱库光谱与杂质或降解物光谱,可以找到结构变化的关联性。 Agilent Cary 630 FTIR 集高精度和合规性于一身,是制药实验室中定性和定量分析的最佳 FTIR系统。完善的系列附件使630 FTIR 能用用于液体和固体样品的分析。使用专利 Dialpath 进行液体进样有助于轻松确定合适的光程和最佳测量条件,便于进样,并可降低出错的风险。利用 Cary 630 FTIR 能够快速简便地测量污染物,如甘油中的乙二醇和甘二醇。 MicroLab Pharma 软件能够简化满足21 CFR 11 法规要求的过程,当杂质浓度超标时,方法驱动的软件将会提醒用户(图5)。 Agilent Cary 630 FTIR Agilent DialPath 附件 图 5. Agilent MicroLab 软件显示了甘油中乙二醇杂质的浓度分析结果。红色条带表明杂质浓度超标。参见安捷伦出版物 5990-7880EN 3.1 有机杂质分析 利用 Agilent 1200 Infinity 系列液相色谱系统实现高选择性、灵敏和精确的杂质分析 这部分列举了安捷伦应对以下分析挑战开发的一系列应用示例:痕量有机杂质的定性和定量量析,元素杂质的测定,以及根据 USP 流程对残留溶剂进行分析。 3.1有机杂质分析 利用 Agilent 1200 Infinity 系列 HPLC/UV 系统实现高精度、线性、灵敏和快速的杂质分析 ,使用安捷伦LC/Q-TOF 系统提高痕量杂质鉴定效率 使用安捷伦 LC/MS/MS仪器定量分析API中的遗传毒性杂质 .根据 USP <467>流程,使用安捷伦气相色谱仪加快残留溶剂分析的速度并提高其灵敏度 Agilent 1200 Infinity 系列 LC/UV 检测系统是药物质量控制实验室进行杂质分析的理想解决方案,帮助您实现杂质分析法规标准所要求的精确、线性、灵敏而快速的分析。图7为使用 Agilent 1290 Infinity ll 高动态范围 (HDR)二极管阵列检测器(DAD) 解决方案对固定剂量复方药及其杂质的分析结果。该方法能够在单次液相色谱分析中同时检测并定量分析主要药物成分以及微量成分和杂质。该分析在7分钟内完成,并将 LOD 改善至 0.1 ng 左右。相比之下,使用传统 DAD 得到的 LOD约为1ng。还实现了优异的峰面积精度,药物成分(维生素C、扑热息痛、咖啡因和氯胺)的 RSD 小于0.1%,且四种杂质的 RSD 介于 1%和3%之间。相比之下,使用传统 DAD 得到的药物成分的 RSD 小于 2%, 杂质的 RSD 为5%-15%。 图6.使用 Agilent 1220 Infinity 液相色谱系统和梯度方法结合紫外检测、Agilent ZORBAX SB-Aq 色谱柱和 Agilent ChemStation 软件,对阿莫西林及其五种杂质的分析。参见安捷伦出版物5990-6093EN 图7.叠加图显示了在5 pL 的进样量下使用传统 DAD 得到的信号以及使用 HDR DAD 得到的信号(A),并还放大了垂直刻度(B)以显示四种杂质。使用传统 DAD (红色迹线,上图)时,维生素C和扑热息痛色谱峰超出范围,无法定量。参见安捷伦出版物5991-3874EN 安捷伦 UHPLC/UV系统有助于使杂质谱分析实现更高的灵敏度、更高的样品通量以及显著的成本节省。由于 1290 Infinity ll 液相色谱系统能够在最高1300 bar的压力下运行,因此可使用非常灵敏的 DAD 开发出显著加快的方法,实现高效杂质谱分析。这将显著降低每次分析的成本。 1290 Infinity II HDR-DAD 杂质分析仪解决方案是安捷伦专门用于实现良好表征药物杂质分析的系统,能够同时进行检测和定量分析。相比传统的紫外检测,其动态范围拓宽了30倍,灵敏度提高了30倍, 具有与 UHPLC 相当的分析速度和分离度。 用于 UHPLC 和 HPLC 的 Agilent 1290 Infinity lI 方法开发工具非常适合用于测试实验色谱条件,如确定固定相和流动相的最佳组合。它使得固定相和流动相的评估成为一项简单而能够自动完成的工作,特别适合分析时间较短的情况。 除优异的分析能力以外,1290 InfinityⅡl液相色谱仪还可优化任意色谱分析的性能。当需要在不同液相色谱系统之间进行方法转移时,安捷伦智能系统模拟技术(ISET) 能够快速模拟其他(U)HPLC 系统的性能,包括其他制造商的仪器系统。 分析人员不再受限于色谱柱尺寸、颗粒类型、流动相或固定相、流速或压力。采用 ISET 的1290 Infinity l液相色谱系统(图8)能够在采用不同设计的 HPLC 和UHPLC 系统之间无缝切换,所有这一切只需轻点鼠标即可完成。 图8.安捷伦 ISET 系统可有效地将方法从各种系统转移到最终的 QC 环境。参见安捷伦出版物5991-4605CHCN 通过模拟开发原方法所用的液相色谱系统,可轻松获得与原方法相同的色谱结果(图9)。可以继续使用传统方法,同时获得现代 UHPLC 系统的优势(包括更高的灵敏度和准确度以及更低的交叉污染),而无需保持过时的传统液相色谱系统。分析人员可对新方法按预期运行彻底放心。 图9.在 Agilent 1290 Infinity lI液相色谱仪上使用 ISET 模拟最初使用 Agilent 1100 系列开发的梯度程序 (A)。B 显示利用在 Agilent 1260 Infinity 液相色谱系统上开发的梯度程序与在1290 Infinity ll液相色谱系统上使用 ISET 模拟的程序所获得的色谱图比较。注意到洗脱模式保持一致,且1290 Infinity ll液相色谱系统具有更高的灵敏度 图9展示了 ISET 用于杂质分析方法无缝转移的优势。借助 ISET 技术模拟延迟体积和混合性能,1290 ⅡI Infinity 液相色谱仪提供了与 Agilent 1100 系列二元液相色谱系统相同的梯度。分离度和保留时间保持不变,且无需更改系统条件和方法。 除液相色谱系统以外,色谱柱也会显著影响有机杂质谱分析的结果。例如,使用传统 5 um 粒径全多孔长液相色谱色谱柱执行法定分析的实验室,-可获益于Agilent InfinityLab Poroshell 120 表面多孔色谱柱提供的更高的分析速度、分离度和灵敏度。 Agilent InfinityLab Poroshell 120 色谱柱 由于USP和EP 指南均支持等度方法并可灵活减小色谱柱长度和粒径,因此将方法转移到更短的2.7 pm InfinityLab Poroshell 120 色谱柱上,能够在保持色谱分离性能的同时节省大量时间。结果表明,相比传统 5 um 色谱柱,使用 AgilentInfinityLab Poroshell 120 色谱柱能够获得更高的通量和分析效率(图10)。 图 10.使用 Agilent ZORBAX Eclipse Plus (5 pm) 和 Agilent InfinityLab Poroshell 120 EC-C18(2.7 pm)色谱柱快速分析头孢吡肟及其相关杂质。参见安捷伦出版物5990-7492CHCN 软件也能帮助完成杂质谱分析所需的许多关键工作。例如, Agilent OpenLABECM 能够引导化学家完成整个工作流程并将所有数据存储在满足法规标准的安全的中心数据库中。 Agilent OpenLAB 色谱数据软件 (CDS) 提供内置的峰纯度评估功能(图11),能够生成最终杂质谱分析报告。通过对紫外光谱的上升段、顶点和下降段进行比较,可以鉴定出含量低于0.5%的杂质。这一功能可以作为也应当作为一种日常分析手段,以获得可靠的高质量数据。分析软件中的自定义计算功能有助于在完整分析中计算杂质总浓度,并可根据杂质毒性类别和用户可定义义限值提供通过/失败通知。 图11. Agilent ChemStation 峰纯度评估软件可根据谱图差异鉴定出含量低于0.5%的杂质。参见安捷伦出版物5988-8647EN 用于药物中有机杂质的严格分析的 LC/MS 系统 在选择方法时,将液相色谱的分离能力与定量质谱的选择性、分析灵敏度和准确度相结合,能够满足实验室的有机杂质分析需求。选择用于特定杂质分析应用的液质联用系统必须满足一些关键标准。 一般来讲,必须能够检出含量为0.05%或更高(相对于API)的杂质,且需要鉴定出含量为0.1%的杂质。必须能够了解0.15%浓度杂质的药理学和毒理学特性。为满足这些要求,利用液相色谱分离杂质必须高效并与质谱分析兼容,提供所需的特异性和分析灵敏度。最后一步要求进行有效的数据分析,以鉴定杂质并实现准确定量。 安捷伦提供了完善的分析解决方案,成功解决了从高分离度色谱分离到中心切割二维液相色谱、无需复杂方法转移以实现质谱兼容性以及高效的质谱数据分析等挑战。 使用单四极杆 LC/MS仪进行经济有效的高性能杂质分析 在杂质分析中,安捷伦 MSD 系列单四极杆液质联用系统以简便易用、紧凑的高性能套装提供了卓越的质谱数据质量。这种业界最通用的单四极杆液质联用系统对实验室现有的液相色谱检测器形成补充,并能够与 Agilent ChemStation 液相色谱控制软件完全兼容,不同配置可满足各种预算要求。 6100系列单四极杆液质联用系统提供了与二极管阵列分析互补的信息,有助于杂质检测和鉴定(图12)。例如, LC/MSD 充分利用了更快速的 UHPLC 色谱分析所具有的高通量。 Agilent InfinityLab LC/MSD 图12.利用 LC/MS 分析加标 1 ppm 潜在遗传性性杂质 (PGI) 的维生素C所得到的色谱图。PGI 经衍生化后进行分析。参见 G.Vanhoenacker, et al. J. Chromatogr. A 2009, 1216,3563-3570. 即使UHPLC峰宽仅为1秒,超快速离子极性切换仍可同时提供正离子和负离子谱图,在一次进样中获得最丰富的信息。进样周期不到10ms,每小时能够分析更多的样品,从而进一步提高了分析效率。还可以将质谱数据转换为MassHunter 数据格式,用于进一步定性和定量分析。 使用安捷伦液相色谱/三重四极杆质谱联用仪对 API 中的杂质进行灵敏、可靠的分析 具有安捷伦喷射流技术的 Agilent 6470 三重四极杆 LC/MS系统 在API 和植物性药物中痕量遗传毒性杂质的定量分析等应用中, Agilent 6400 系列三重四极杆液质联用系统可提供行业领先的灵敏度、高效率和价值。最大的离子化效率和全质量范围的离子传输效率,确保各种类型的样品均获得较低的 LOD和定量限(LOQ),灵敏度可达飞克级。 创新的碰撞池设计消除了交叉污染,并支持快速多反应监测(MRM), 离子驻留时间可短至1ms, 从而实现更高的分析效率。创新的动态MRM (dMRM)支持在单一时间范围内自动分析最多4000 个 MRM。 Agilent MassHunter Optimizer可自动优化用于各种化合物的质谱参数((如碰撞电压和碰撞能量),进一步提高效率。 图13展示了将1290 Infinity 液相色谱仪与 Agilent 6400 系列三重四极杆液质联用系统联用,根据 MRM 对九种痕量(相对于API,浓度远低于1 ppm)芳胺和氨基吡啶类潜在遗传毒性杂质 (PGI) 的定量分析结果。使用 MS/MS 得到的这九种 PGI的检测限均远低于 20 ppb (相对于 API),请参见安捷伦出版物 5990-5732EN。对每一种 PGI 均采集特定的定量离子和定性离子,确保存在相关杂质情况下的选择性。使用 Agilent ZORBAX Eclipse Plus C18 RRHD 色谱柱(2.1×150 mm,1.8 pm), 所有九种PGI在9分钟内得到完全分离。使用柱长50 mm 的 ZORBAXEclipse Plus C18 RRHD 色谱柱,分析时间可进一步缩短至3分钟。通过与 PGI标准溶液比较计算得到的回收率表明,准确度高达 70%-130%,这是药物痕量分析流程的典型范围(如限值检测)。 AmAU洗必泰,加标1 ppm PGIDAD 260 nmA0M.L2 3 4 5 6 7 min B响应(%) 响应P11GI5, 166.1>130.0(80.4%) PGI5, 166.1>130.020000PGI4, 163.1>120.0(98.3%) PGI4, 163.1>120.0111000- 0. x10-2PGI6, 150.1>108.0 (3.8%,与API共流出) PG16, 150.1>108.011000www/×10-PGI3, 136.1>121.0(101.7%) PGI3, 136.1>121.011 20000- ×10-PGI7, 129.1>93.0(79.1%) PGI7, 129.1>93.011 5000- *10 PGI8, 128.1>93.0(存在于API中,>20 ppm) PGI8, 128.1>93.011 10000x10-2PGI2, 126.1>111.0(96.0%) PGI2, 126.1>111.011100.0 ×10-PGI9, 122.1>105.1(98.5%) PGI9, 122.1>105.1115000 ×102PGI1,119.1>92.0(89.6%) PGI1, 119.1>92.0112502 3 4 5 6 7 0.8 1.0 1.2 1.41.6 1.8 2.02.2 2.4采集时间(min) 采集时间(min) 图13.在加标 PGI的洗必泰样品分析中得到的 DAD 结果和定量 MRM 离子对结果。对采用柱长分别为 150 mm (A) 和 50 mm (B) 的 Agilent ZORBAX Eclipse Plus C18 RRHD (内径2.1mm, 填料粒径1.8pm)得到的结果进行了比较。相应的离子对和计算回收率也显示在图中。参见安捷伦出版物5990-5732EN 使用安捷伦 LC/TOF 和LC/Q-TOF 仪器提高痕量杂质鉴定的分析效率 为通过精确质量数确认合成药物化合物并鉴定其杂质, Agilent 6200 系列精确质量数飞行时间 (TOF) 液用联用系统以紧凑的台式仪器提供了最高的速度和性能。亚 ppm级质量准确度大大提高了结果的可信度并减少了假阳性结果。高达20000的质量分辨能力可以区分目标化合物与干扰物质。谱图内动态范围高达5个数量级,能够同时检测和定量高浓度及低浓度化合物。低皮克级柱上灵敏度有利于检测和定量浓度极低的杂质。 当需要进行结构分析以鉴别未知 API 杂质时, Agilent 6500 系列 Q-TOF 液质联用系统可提供无可比拟的质量准确度、质量分辨率、灵敏度、动态范围和分析速度的组合,确保实现准确的鉴定与定量。该四极杆系统提供了碰撞诱导解离 (CID),可生成用于鉴定样品成分结构的碎片(MS/MS)。 6500 Q-TOF 的亚 ppm 级质量准确度能够显著降低不确定性,改善未知物的数据库检索分值及分子式生成,同时大大减少假阳性结果。高达45000 的高分辨能力大大增强了复杂样品中所有目标组分结果的可靠性,优异的 MS/MS 灵敏度有助于鉴别飞克级组分峰。 Agilent 6500 系列Q-TOF系统 凭借其无可比拟的长期可靠性、高分辨率和质量准确度,6500 Q-TOF 系统是用于药物杂质结构分析的理想仪器。使用该 Q-TOF 系统、配置用于标准中心切割的Agilent 1200 系列 Infinity 液相色谱仪以及 Agilent MassHunter 软件工具,鉴定出度洛西汀中紧紧洗脱出的杂质为该药物的甲基衍生物(图14)。该2D-LC/MS 方法将在后续章节中进行更详细的讨论。 图14.API度洛西汀 (298.1257) 及其杂质 (312.1416) 的质谱图,该杂质被确定为度洛西汀的甲基衍生物。参见安捷伦出版物5991-1873CHCN 使用2D-LC/MS 优化方法转移以实现质谱兼容性 为获得良好的色谱分离效果, HPLC 方法通常需要使用大量的缓冲盐,如磷酸盐、EDTA、TFA、硫酸钠、三乙醇胺和离子对试剂,这些试剂与质谱不兼容。将它们替换成与质谱兼容的试剂可能导致一系列问题,其中包括杂质保留时间和峰洗脱顺序的改变。这种方法更改使杂质分离和鉴定更加复杂。为应对这一挑战,安捷伦提供了独特的创新解决方案。 安捷伦开发出基于阀切换的二维液相色谱方法,该方法在第二维中将原液相色谱分离中与质谱不兼容的流动相改为与质谱兼容的流动相。每个色谱峰的保留行为保持不变,因为原色谱条件并未改变。将第一维中分离的各种目标组分转移至第二维色谱柱中进行后续的质谱分析。该方法使用户能够将质谱分析应用于流动相与质谱不兼容的液相色谱方法,而无需修改初始液相色谱方法。使用这种技术与安捷伦杂质鉴定数据处理工作流程相结合,可快速高效地完成杂质鉴定。 事实证明,配备用于标准中心切割二维液相色谱的1290 Infinity lI 液相色谱仪适用于含无机盐(磷酸盐)的流动相体系以及含有机离子对改性剂(如十二烷基硫酸钠和四丁基氢氧化铵)的体系。此外,用户可根据实验的具体需要扩展该方法的应用范围,例如替换分析方法中的流动相并减小基质抑制效应。最后,安捷伦液相色谱系统的模块化设计有助于根据色谱分离的性能要求灵活配置系统。只需添加或移除模块即可将传统安捷伦液质联用系统升级为二维液相色谱/质谱联用系统配置,从而充分利用现有仪器。配备用于标准中心切割二维液相色谱的1290Infinity 液相色谱仪已用于多种 API 的杂质分析。图15显示了其中一种API(色瑞替尼)的分析结果。原色谱分离条件使用含四丁基氢氧化铵缓冲液的流动相A,该流动相与电喷雾质谱分析不兼容。在使用这些条件和 DAD 检测器将 API与杂质分离后(图15A,上方迹线),将杂质峰中心切割,并送至使用水和甲醇梯度的第二根 C18色谱柱。将该色谱柱的流出物引入 Agilent 6540 Q-TOF 质谱仪进行分析。图15A 显示了该组分的提取离子流(EIC)迹线,图15B显示了其质谱图。使用MassHunter 软件对这些数据进行分析,分子式生成器(第29页)将杂质的分子式确定为 C13H15CIN0,S (图15C)。 图15.色瑞替尼的杂质分析结果,显示了第一维分离的紫外迹线(A,上方迹线)和杂质第二维色谱分离的 EIC (A,下方迹线),杂质质谱图的分子离子部分(B),以及使用质谱数据和 Agilent MassHunter软件工具确定的分子式 (C) 该方法保留了原始分离的洗脱顺序,同时提供了用于鉴定杂质的基本质谱信息。同一方法已用于鉴定度洛西汀中紧邻洗脱的低丰度杂质(应用简报5991-1873CHCN, 第27页)。已采用这种方法对包括甲酰四氢叶酸、鸟苷5'-三磷酸三钠盐、达托霉素、钆钆贝酸、倍他司汀、氟替卡松糠酸酯、阿莫西林、磷脂和胰岛素等其他 API中的杂质进行了表征。 质谱数据分析对于准确的杂质检测和鉴定至关重要 采集的质谱数据量可能非常大,在高分辨率质谱分析中尤其如此。这就需要使用非常高效的软件处理工具借助 MS/MS 数据进行结构分析,并与参比谱库谱图进行比较。 Agilent MassHunter 软件工具和个人化合物数据库和谱库 (PCDL)提供了一种使用质谱数据鉴定化合物的高效方法。未检出杂质可能会造成潜在的药物安全问题。因此,检出样品中尽可能多的杂质至关重要。这一目标通过简单的峰查找方法可能无法实现,因为单个峰可能包含多种组分,即使拥有最出色的质量分辨率也无法避免这种情况。然而,安捷伦专有的 MassHunter 软件中包含的质谱数据分析工具能够准确、快速地鉴定杂质并完成结构解析。用于高分辨率质谱数据的分子特征提取 (MFE) 工具可找出未知杂质(图16)。分子特征是由液相色谱保留时间(RT)、质量数(包括同位素信息)和信号响应组合定义的离散分子实体。 MFE 是用于从大量原始 LC/MS数据中提取有关推断杂质重要信息的必要分析工具。 图16. Agilent MassHunter 软件中的分子特征提取(MFE) 可由未表现出离散分离的色谱图区域定义多个单独的分子实体 对于已知杂质,分子式查找(FBF)和分子式生成器 (MFG) 是用于杂质表征最直接有效的 MassHunter 工具。这些软件工具可使用已知杂质的特性从原始质谱数据中直接搜索并提取分子实体。软件根据分子式、质谱图以及同位素丰度和间隔匹配的组合提供准确的结果(图17)。 图17.使用 FBF 和 MFG Agilent MassHunter 软件工具鉴定 API 中的已知杂质。确定杂质峰的质谱 EIC 并由 ESI扫描生成同位素谱图。然后将它们与已知杂质的同位素谱图进行比较,从而确认这种杂质的存在 安捷伦个人化合物数据库和谱库 (PCDL)对于高效的杂质分析至关重要。用户可轻松将化合物信息导入 PCDL中,创建高度定制的项目数据库。PCDL 可包括化合物名称、结构、分子式、精确质量数、CAS 和 IUPAC 标识符。它还可用于执行组合的保留时间和精确质量数匹配,以进一步提高化合物鉴鉴的可信度。 此外, MS/MS 谱库搜索与 PCDL 提供了一种高特异性化合物鉴定方法。可以保存不同碰撞能量下获得的参比化合物的高分辨率质谱图,与杂质分析中获得的碎片离子谱图进行比较。对数据库中化合物的 MS/MS 谱图进行相似度搜索有助于结构确认,这对于工艺杂质和降解杂质的分析均非常有用。 软电离技术,特别是电喷雾电离(ESI), 可生成准分子离子。这些质谱图可能缺少有结构意义的诊断碎片。为获得此类信息,可使用 CID 和 MS/MS 技术。然而,由于碰撞气体的选择或碰撞能量的调节,因此采用不同仪器分析同一化合物可能生成不同的 MS/MS 谱图,所以,几种市售的标准质谱库中包含在各种条件下采集的谱图。 可创建针对特定项目的 ESI-MS/MS PCDL, 来弥补这一不足。然后,,1可采用MassHunter 分子结构关联 (MSC) 软件,根据 MS/MS 碎片离子的精确质量数和元素组成来确认未知杂质的结构(图18)。MSC 还支持数据库搜索功能(如ChemSpider),有助于通过各种方式(包括相似度搜索)鉴定未知杂质。 图18.Agilent MassHunter 软件中 MSC 结构分析工具的应用 为了对相同 API 或杂质进行重复数据分析,可以将 MassHunter 数据分析工作流程(从分子特征提取过程到结构分析和设置)自动化,以便在采集数据时尽快开始。结果得到简化的分析流程,分析效率得到显著改善 安捷伦有机杂质谱分析资源 出版号 标题 5991-3874EN 使用 Agilent 1200 Infinity 系列宽动态范围二极管阵列检测器解决方案对固定剂量 复方药进行单次运行分析和杂质检测 5991-5743EN 使用 Agilent 1290 Infinity II HDR-DAD 杂质分析仪解决方案对固定剂量复方药进行 杂质检测 5991-4605CHCN Agilent 1290 Infinity lI 液相色谱仪:快速高效,自由随心 5990-7492CHCN 使用 Agilent Poroshell 120 EC-C18色谱柱快速分析头孢吡肟及其相关杂质 5990-9715EN 通过智能系统模拟技术 (ISET)实现 Agilent 1290 Infinity 液相色谱仪的方法开发以 及随后向 Agilent 1100 系列液相色谱仪的转移:镇痛药混合物分析 5989-7925EN AstraZeneca 成功案例:通过LC/MS直接分析加快确定候选药物中的潜在基因毒素 5990-4460CHCN 利用 Agilent 1200 RRLC 和 Agilent 6410B三重四极杆液质联用仪对阿替洛尔中存 在的基因毒性“杂质D”进行定量分析 使用 Agilent 1290 Infinity 液相色谱系统和 Agilent 6460A 三重四极杆质谱系统通过 5990-5732EN UHPLC 和 UHPLC-MS/MS分析活性药物成分中潜在的遗传毒性芳香胺和氨基吡啶 杂质 5991-3175CHCN 使用二维液相色谱中心切割实现阿莫西林杂质分析中质谱兼容流动相的替换 5991-1873CHCN 使用Agilent 6540 Q-TOF LC/MS 系统通过中心切割 2D-LC/MS 法进行药物杂质鉴定 5991-5643EN 多中心切割二维液相色谱在杂质分析方法开发中的应用: Agilent 1290 Infinity 二维 液相色谱解决方案 5991-1375CHCN 安捷伦Q-TOF LC/MS 和先进的 MassHunter 数据处理软件结合使用进行药物杂质 的鉴定和分析 5991-5564CHCN 安捷伦 2D-LC/MS 中心切割技术在药物杂质鉴定中的应用 5991-2796CHCN 纯度和杂质分析制药行业应用文集 5991-0090CHCN 药物杂质分析解决方案 5991-1876CHCN 药物开发中纯化、纯度分析和杂质分析解决方案选择指南 5990-9380CHCN 用于医药研发过程的纯化、纯度分析和杂质分析解决方案 5989-8529EN 药物中杂质的检测与鉴定:使用 Agilent MassHunter 软件对 Q-TOF 数据进行计算 机辅助提取、谱分析和分析以测定杂质 5991-1876CHCN 药品中的遗传毒性杂质:法规和分析基础导论 3.2 无机杂质分析 根据 ICH 和 USP 方法,使用安捷伦 ICP-OES 和 ICP-MS仪器 测定药物成分中的元素杂质 药物样品的前处理和分析方法在 ICH Q3D 以及 USP 通则章节<232>和<233>中有所描述。为取代之前过时的“重金属限值检测”(USP<231>),这些最新更新的流程使得制药实验室有机会获益于简化的方法和现代仪器。新方法要求实验室使用准确的定量分析方法(如 ICP-OES 或 ICP-MS) 测定有关元素杂质的 USP<233>和 ICH/Q3D 文件中的所有目标元素。 ICP 技术提供了快速多元素分析、良好的基质耐受性、宽线性动态范围和高样品通量的完美组合。 Agilent 5110 ICP-OES 拥有稳定的等离子体系统,能够分析最具挑战性的样品,如未稀释的有机溶剂和浓盐溶液。检测限满艮散装原料和口服药品的法规要求。5110 ICP-OES 提供了一种经济有效的解决方案,适用于对前处理或消解过程中无需较高稀释倍数的样品进行快速、准确的分析(见图19)。 图 19. Agilent 5110 ICP-OES 稳定的垂直等离子体系统确保复杂样品获得稳定的分析结果,如图中所示加标浓度为 250 ppb 的25% NaCl溶液。安捷伦科技公司未发表的结果 Agilent 7800 和7900四极杆 ICP-MS 系统可测定各种制药原料中所有低浓度的监管元素。该系统适用于测定注射给药和吸入给药的药品(规定限值低得多)以及口服剂型中元素杂质的实验室(参见安捷伦出版物5991-8333EN 和5991-7674CHCN)。内置 USP/ICH元素杂质预设方法提供了简便的方法开发和常规操作,对于所有分析物和样品采用同一组一致的氦(He)池模式条件。根据USP<233>的要求,在 He模式下的得的二级(定性)同位素可对分析物结构提供明确鉴定和验证。 低检测限 (LOD) 对于重要的潜在毒性痕量元素((特别是定义为1类杂质的As、Cd、Hg和Pb)尤其重要,根据ICH Q3D 和 USP<232>的规定,必须对所有药品中的这些元素进行测量。图20显示了这些元素以及 Pd 和 Pt 的校准曲线。Pd和Pt代表了铂族元素(PGE),按照 ICH Q3D 和 USP<232>的要求,如果 PGE 作为催化剂加入时,必须对其进行监测。需要注意,所有元素均在同一模式(He 池气体))下进行测量,显示出方法设置的简便性,这是安捷伦四极杆 ICP-MS 系统所具有的一项极为重要的特性。 As浓度(ppb) 浓度(ppb)208 Pb [He] ISTD: 209 Bi [He] 105 Pd [He] ISTD: 159 Tb [He] 195 Pt [He] ISTD: 209 Bi [He]×10-1R=0.9999 ×10-1R=0.9999 ×10-1R=0.9999.3.2. 5.0.5.1Pb Pd Pt01 0 .5.0 10.0 .5.0 10.0 5.0 10.0 浓度(ppb) 浓度(ppb) 浓度(ppb) 图 20. Agilent 7800 ICP-MS 在 He 模式下得到的 As、Cd、Hg、 Pb、Pd 和 Pt校准曲线,表明LOD小于等于1 ng/L, 包括 Hg、Pd 和 Pt在内(需要在 HCI中保持稳定)的所有元素均获得了良好的灵敏度和线性。参见安捷伦出版物5991-8335EN 7800 和7900 ICP-MS 系统的系统性能验证数据表明,它们可轻松满足方法要求的准确度、稳定性和加标回收率,检测限比当前受控痕量元素的浓度要低几个数量级。这将确保7800和7900四极杆 ICP-MS 系统能够满足 ICH/USP 方法中规定的所有制药原料的法规要求,即使未来控制限值降低,也能够满足要求。 7800和7900四极杆ICP-MS 系统还提供了全质谱图筛查能力,能够耐受所有常用的有机溶剂,并且在需要确认符合 ICH Q3D 和 USP<232>中规定的这些元素无机形态限值要求的情况下,可连接色谱系统以对不同形态的 As和Hg实现集成式分离和分析。 3.3 残留溶剂分析 根据 USP <467>流程,使用安捷伦气相色谱仪加快残留溶剂分析的速度并提高其灵敏度 出版号 标题 5991-8140CHCN 用于工作流程法规认证的安捷伦资源一测定制药原料中的元素杂质 5991-8335EN 按照 USP <232>/<233>和 ICH Q3D/Q2(R1)验证 Agilent 7800 ICP-MS 的性能: 药物中的元素杂质分析 5991-7674CHCN 使用 USP/ICH 方法和 ICP-MS 测定药物成分中的元素杂质 5991-8337EN 阿司匹林中的元素杂质;使用5110 ICP-OES 验证 USP <233>和 ICH Q3D 5991-8149CHCN USP <232>/<233>和 ICH Q3D元素杂质分析:安捷伦ICP/MS解决方案 5991-8150CHCN USP <232>/<233>和 ICH Q3D元素杂质分析:安捷伦ICP-OES 解决方案 5991-2002CHCN 支持21 CFR Part 11 和附录11的法规要求: Agilent ICP-MS MassHunter 软件的 SDA模块 5991-8143CHCN 支持21 CFR Part 11 和附录 11的法规要求: Agilent ICP Expert 软件的 SDA模块 5991-2593CHCN 利用 Agilent ICP-MS MassHunter 和 OpenLAB 服务器符合法规认证指南的要求 5991-1925CHCN 利用 Agilent ICP-MS MassHunter 和 OpenLAB 企业内容管理器(ECM)符合法规认 证指南的要求 质量保证实验室日常采用美国药典 (USP) 方法<467>进行残留溶剂分析。Agilent7697A 顶空进样器与 Agilent Intuvo 气相色谱仪或 7890 气相色谱仪联用,为水溶液中USP<467>1类和2类残留溶剂浓度限值的分析提供了一种非常高效的解决方案。 USP<467>规定了用于1类和2类残留溶剂的三种流程: 流程A:鉴定和限值检测 流程B:确证试验(如果溶剂超出限值) 流程C:定量检测 流程A使用 G43 固定相 Agilent 624 色谱柱 (VF-624ms 或 DB-624)!),而流程B使用 G16固定定 (HP-INNOWax)色谱柱。,一般来讲,在其中一种固定相中共流出的分析物在另一种固定相中不会共流出。 图18和19 证明, Agilent 7697A 顶空进样器能够为残留溶剂分析提供出色的重现性。对于1类、2A类和2B类溶剂,重现性通常优于2.5%的相对标准偏差(RSD)。 惰性样品流路、稳定性设定值优于±0.1℃的热区以及使用绝对压力进样的EPC控制样品瓶进样,均有助于实现优异的系统性能。在所有配置中,基本上不存在交叉污染。用户可编程的流速和时间、针头/定量环吹扫以及放空管线吹扫,可有效地用于在运行之间清洗系统。根据 USP 或 ICH指南要求,实验室应执行系统适用性研究并验证其提出的方法。 对于新药开发和质量控制, FID 检测器和质谱检测器 (MSD) 的双通道配置是溶剂残留分析,尤其是未知物鉴定或确认分析的有效工具。该系统特别适合用于开发无需遵守 USP<467>指南的通用方法。鉴于目前药物生产过程中使用的溶剂超过60种, MSD分析还有助于避免误判。当出现未知峰或溶剂时,该系统是确认和定量分析的最佳解决方案。 FID2 B. BackSi DEC14BRLF2010-12-14D S1LSIG10000012.D) 2 B. Back Signal(NOV15B\14.D) lorm. C 5 7 8 4- 1.己烷 2.硝基甲烷 3.氯仿 4.1,2-二甲氧基乙烷 5.三氯乙烷 6.吡啶 2- 7.2-己酮 8.四氢萘 6 3 4 2 小 2 10 12 图 21. USP<467>限值浓度的1类(A)、2A类(B)和2B类(C)溶剂。参见安捷伦出版物5990-7625CHCN 安捷伦残留溶剂分析出版物 L2JT Abundance 400000300000-200000100000- Time-> TIC A 3.00 10.00 12.00 Abundan 120000100000-8000060000--40000-20000 9.00 图22.利用 FID-MSD 得到的限值浓度下2A溶剂的分析结果。参见安捷伦出版物5990-7625CHCN 出版号 标题 5990-7625CHCN 使用 Agilent 7697A 顶空进样器以更高的重现性进行 USP <467>残留溶剂分析 5989-8085EN 根据USP <467>同时采用双毛细管主 顶空气相色谱和火焰离子化检测器进行确认和定量分析 5989-9726CHCN 静态顶空 GC-FID/MS用于药品中残留溶剂分析的一种通用方法 5990-5094CHCN 使用 Agilent 7890A GC 和低热容(LTM)系统快速分析 USP <467>残留溶剂 5989-6079CHCN 改善分析残留溶剂的保留时间和峰面积重现性,提高灵敏度 5991-4418EN 简化 USP <467>残留溶剂检测宣传单页 4.附录 4.1 安捷伦以其广泛的仪器、液相色谱柱和气相色谱柱选择以及软件和信息学解决方案,成为了杂质分析领域的行业领导者。 安捷伦药物杂质分析解决方案 色谱柱与备件 安捷伦提供完善的气相色谱柱和液相色谱柱以及色谱、质谱和光谱备件,且所有产品均符合 ISO 9001标准,确保了最高的仪器性能和结果重现性。 安捷伦以其 InfinityLab 产品成为液相色谱领域的行业领导者。 Agilent InfinityLab是一套经过优化的液相色谱仪、色谱柱和备件产品组合,可通过无缝协同工作实现分析效率和性能最大化,适合各种应用领域。 InfinityLab Poroshell 120色谱柱可实现高效分离,并获得优异的峰形和分离度。包括三种粒径(1.9 um、2.7 um和4 pm) 的各种固定相可供实验室开发设置选择,具有良好的可扩展性,可为药物的整个生命周期提供支持。安捷伦还提供最广泛的气相色谱柱产品组合,包括创新的超高惰性气相色谱柱。 安捷伦广泛的备件系列产品包括样品瓶、进样针、气体管理系统、流量计、泄漏检测器、接头、工具和标准品,所有产品都经过我们的仪器设计团队设计或选择,按照我们严格的标准进行生产,并通过了各种苛刻条件下的测试。 4.3 软件与信息学产品 安捷伦行业领先的软件和信息学产品组合不断扩充,涵盖了更广泛的分析工作站、数据和实验室管理解决方案及应用,'可满足生命科学和化学行业日益增长的需求。安捷伦整合的软件解决方案能帮助您处理科学数据整个生命周期的问题,包括实验设计、数据采集、知识管理和开放系统架构下的数据分析。AgilentOpenLAB 软件套装包括多种色谱数据系统和内容管理解决方案,可满足任何实验室的需求。 4.4实验室法规认证和法规认证咨询 数据完整性在各个行业的实验室中均受到越来越多的关注。这一关注延伸到实验室审计中如何对仪器性能进行评估、记录和保护。 Agilent ACE 是安捷伦工程师用于测试和记录实验室仪器的软件,适用于任何制造商的仪器。它能够提供符合2017 版 USP<1058>关于制药实验室要求的分析仪器认证(AIQ)服务,以及旨在帮助实验室遵守 ISO 17025 认证要求的功能验证(FV)服务。安捷伦还提供了定制验证服务,如计算机系统验证、审计和评估、自定义程序编写等。安捷伦迄今为止拥有数十万项认证记录,因此您可以信赖安捷伦以确保数据完整性的方式为您提供安全的认证服务。 www.agilent.com/lifesciences/pharma 查找当地的安捷伦客户中心: www.agilent.com/chem/contactus-cn 免费专线: 800-820-3278, 400-820-3278(手机用户) 联系我们: LSCA-China_800@agilent.com 在线询价: www.agilent.com/chem/erfq-cn ( 仅限研究使用。不可用于诊断目的。 ) ( 本文中的信息、说明和指标如有变更, 恕 不另行通知。 ) ( ◎安捷伦科技(中国)有限公司,2018 ) ( 2018年4月20日,中国出版 5991-0090ZHCN ) Agilent 药物杂质是活性药物成分 (API) 或药品制剂中不希望存在的化学成分。原料药中的杂质可能源于合成过程或原料、中间体、试剂、溶剂、催化剂以及反应副产物等其他来源。在药品开发过程中,杂质可能:• 由于原料药固有的不稳定性而形成• 由于与加入的辅料不相容而产生,或• 与包装材料和容器密封系统 (CCS) 相互作用而产生原料药中各种杂质的含量决定了最终成品药物的安全性。因此,杂质的鉴定、定量、定性和控制已成为药物开发过程的关键组成部分。很多监管机构都在关注杂质的控制:• 国际协调会议 (ICH)• 美国食品药品监督管理局 (USFDA)• 欧洲药品管理局 (EMA)• 加拿大药品与健康管理局• 日本药物和医疗器械管理局 (PMDA)• 澳大利亚卫生和老龄治疗商品管理局此外,很多官方药典(如英国药典 (BP)、美国药典 (USP)、日本药典 (JP)、欧洲药典 (EP) 和中华人民共和国药典 (ChP))也越来越多地加入了对 API 和药品制剂中杂质限量水平的规定。这些法规以暴露限值为依据,因此必须对施用时最终剂型中的污染物浓度进行控制。在实践中,这意味着药物制造商必须进行风险评估,考虑到制造后(如包装、运输和 CCS)的污染源以及来自原料和生产过程的污染。
确定






















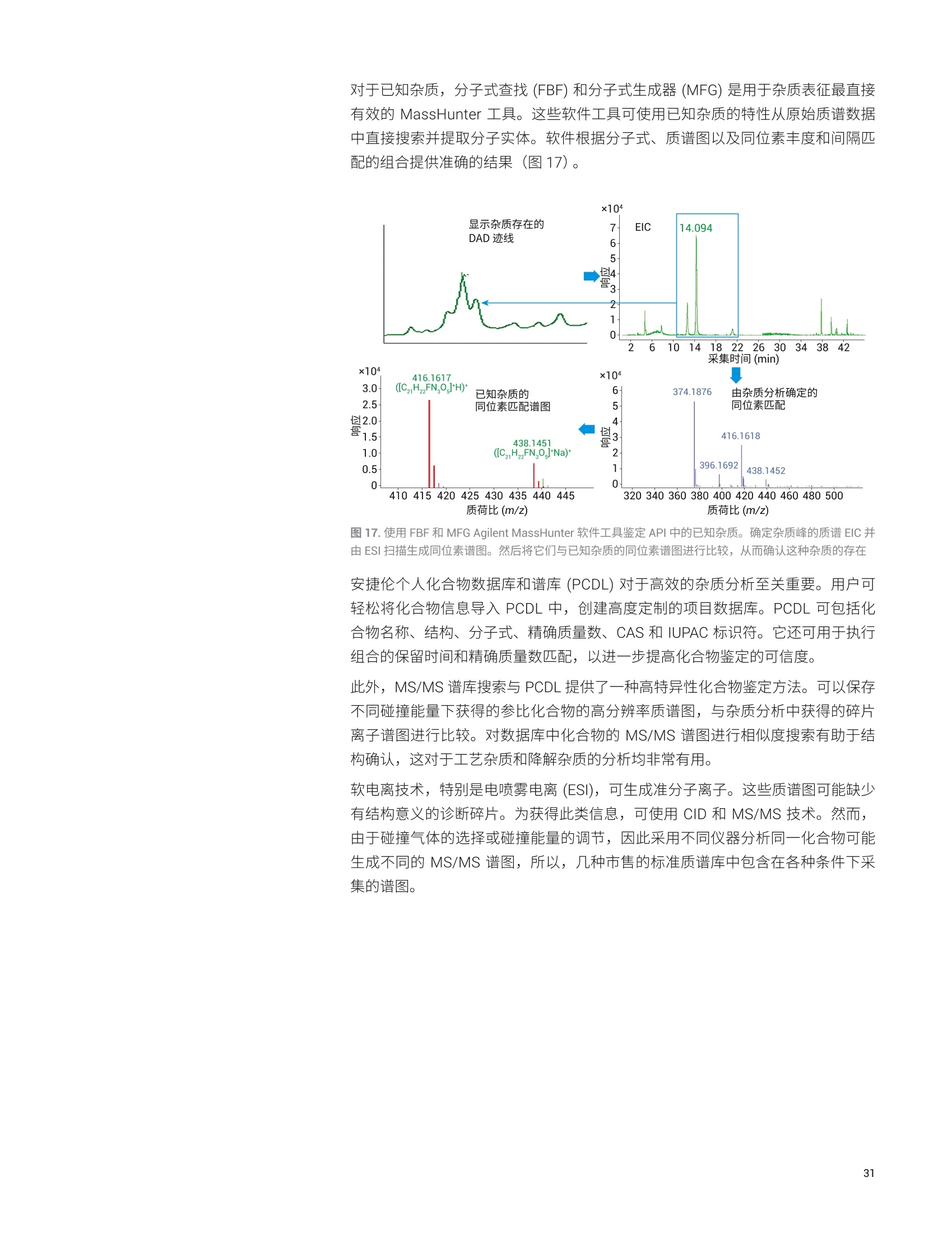



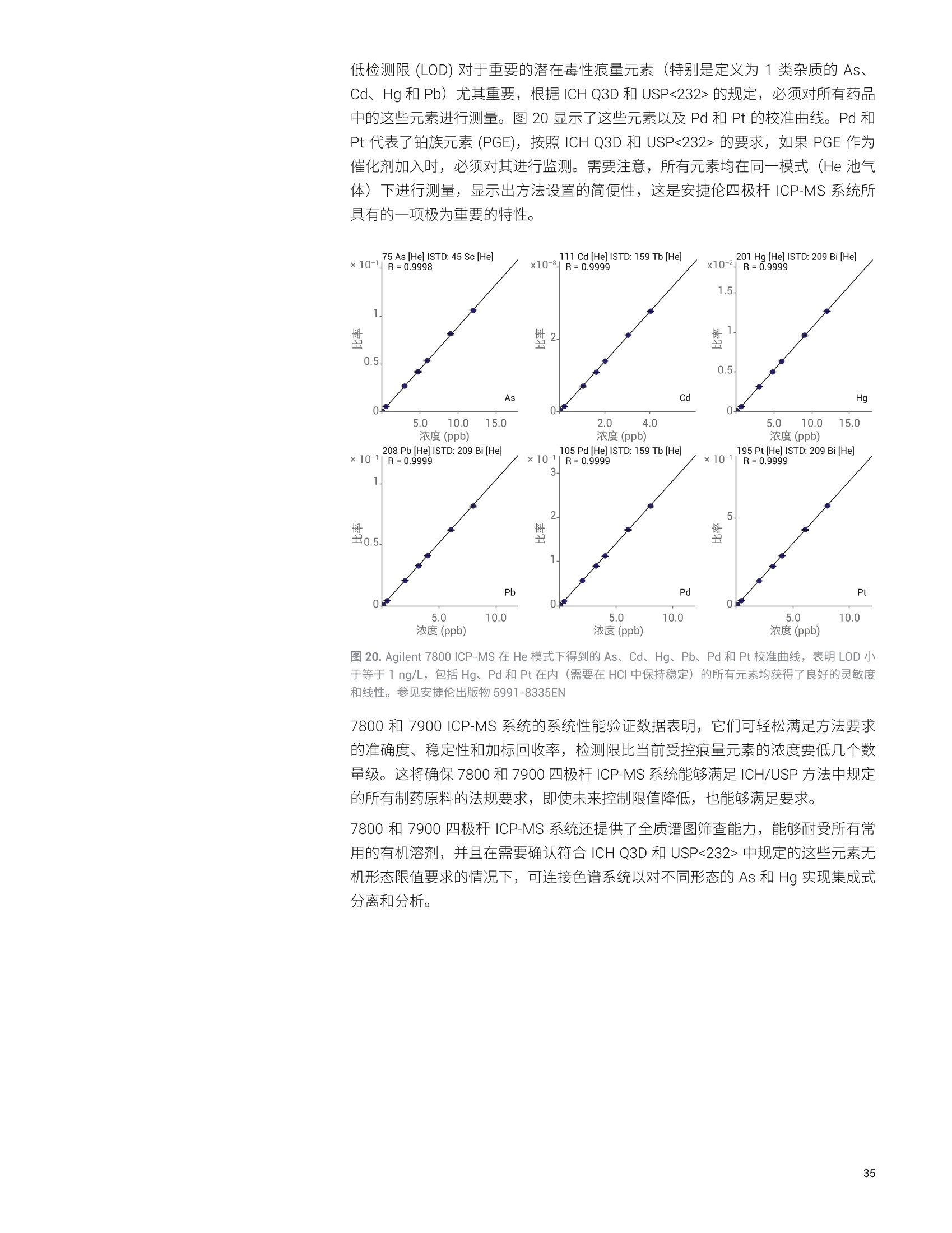







还剩40页未读,是否继续阅读?
安捷伦科技(中国)有限公司为您提供《药物中杂质检测方案(制备液相色谱)》,该方案主要用于化药制剂中杂质检测,参考标准--,《药物中杂质检测方案(制备液相色谱)》用到的仪器有Agilent 1290 Infinity II 制备型液相色谱、Agilent 1260 Infinity II SFC 系统、Agilent 6470 三重四极杆液质联用系统、Agilent CE/MS 系统
推荐专场
相关方案
更多
该厂商其他方案
更多

























