方案详情
文
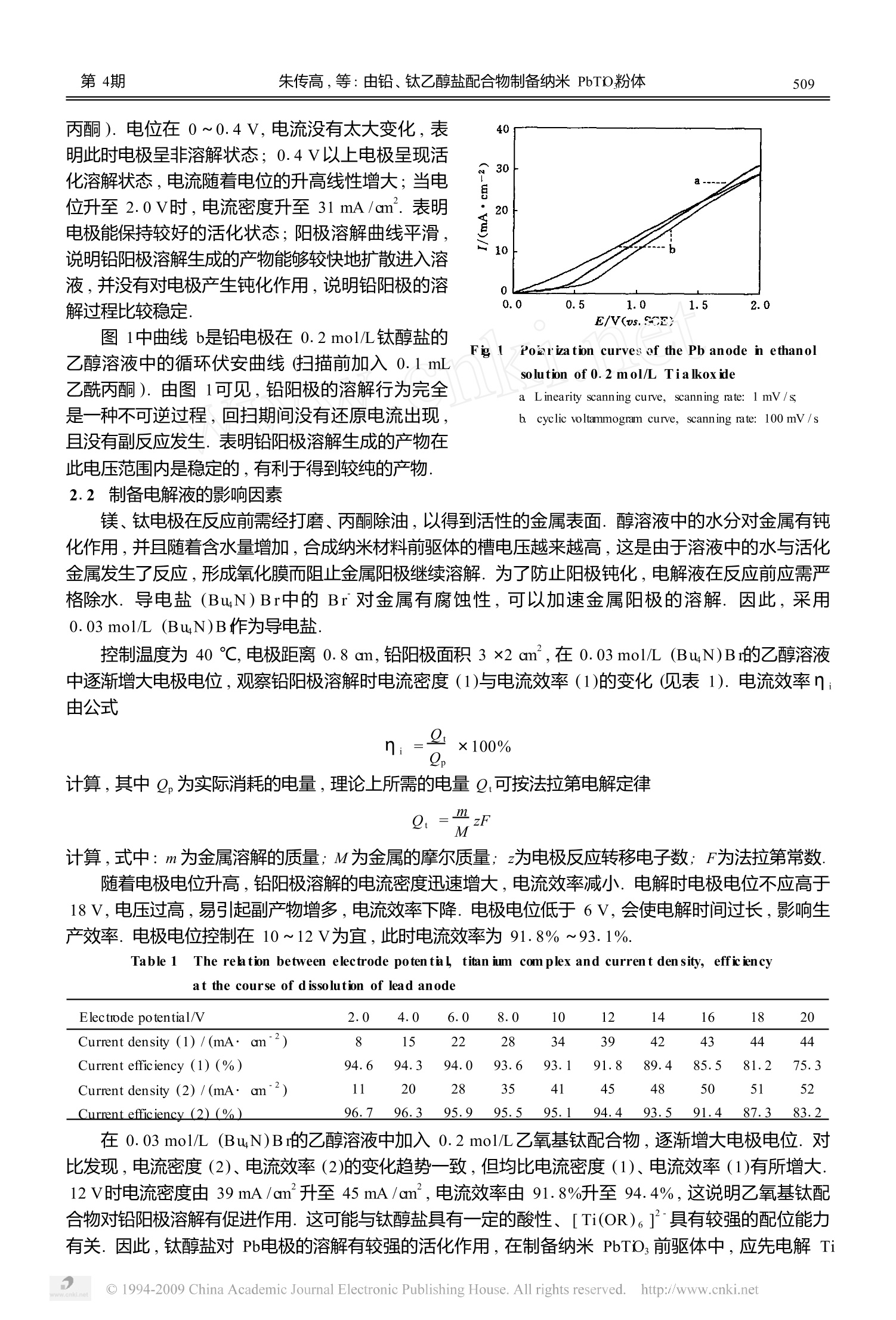
在0. 03 mol/L (Bu4N)Br的乙醇溶液中, 电解钛片4 h, 然后电解铅片2 h, 每隔30 min加入0. 1 mL乙酰丙酮, 制得铅、钛金属醇盐. 采用红外、拉曼光谱测试结果表明, 纳米PbTiO3前驱体结构中含有acac2(乙酰丙酮基) , 可以有效克服团聚现象. 经差热2热重分析、X射线衍射、电子透射显微镜测试表明, 凝胶经乙醇洗涤、真空干燥24 h后粒径为10 nm;700 ℃煅烧2 h制得纳米PbTiO3 粉体, 粒径在10~15 nm.
方案详情

Vol 43 No 4July 2005第43卷 第4期2005年7月吉林大学学报.(理学版)JOURNAL OF JLNUNVERSITY (SCIENCE ED ITDN) 第43卷吉林大学学报 (理学版)508 由铅、钛乙醇盐配合物制备纳米 PbTD粉体 朱传高.,褚道葆:2 (1.淮南师范学院化学系,安徽省淮南232001;2安徽师范大学有机化学研究所,安徽省芜湖241000) 摘要:在0.03 mol/L (BuN)Br的乙醇溶液中,电解钛片4h,然后电解铅片2h,每隔 30min加入0.1mL酰酰丙酮,制得铅、钛金属醇盐.采用红外、拉曼光谱测试结果表明,纳米PbTD:前驱体结构中含有acac-(乙酰丙酮基),可以有效克服团聚现象..经差热热重分析、X射线衍射、电子透射显微镜测试表明,凝胶经乙醇洗涤、真空干燥24h后粒径为10 mm;700℃煅烧2h制得纳米 PbTiO;粉体,粒径在10~15 nm. 关键词:电化学;铅、钛乙醇盐配合物;溶胶凝胶;纳米 PbTO丫 中图分类号:O646 文献标识码:A 文章编号:1671-5489(2005)04-0507-06 Prepara tion of Nanocrystallne PbTD Powder by Leadand Titan ium Ethox ide Complexes ZHU Chuan-gao, CHU Dao-bao D eparm ent of Chem istry, Huainan Nom al College, Huainan 232001, Anhui Province, China;Institute ofO rganic Chen istry, Anhui Nom alUniversity, Wuhu 241000, Anhui Province, China) Abstract The precursor PbTi(OCH, CH,)6-y (acac), of nanocrystalline PbTis was prepared by the electro-chem ical disso lution of titanium for4 h at 50℃ and then of lead for2 h at 40℃ in an ethanol solution of0. 03 mol/L (BuN)BrR and Raman spectroscopy were used to investigate the structure of the precursorThe results show that the precursor contained acac group, which could prevent the precursor from gatheringTG-DT, XRD, and TEM were used to investigate the structure of nano-sized PbTO.The xerogel of 10 nmwas obtained by drying in vacuum for24h PbTDs with a narrow size distribution of 10~15 nm was preparedby heating it at 700℃ for2 h Keywords: electro-chem ical;lead and titanium ethoxide complexes; sol-gel; nanocrystalline PbTiOs PbTiO,在发光、铁电、压电等领域有重要的应用价值,制备PbTiD,粉体的有效方法是溶胶凝胶法1~5].主要采用 Pb(CH,COO),·3H,O、钛酸丁酯为原材料.由于 Pb(CH;COO),·3H,O溶解度极小,实验中使用乙二醇乙醚作为溶剂,同时添加硼酸三丁酯等有机物作稳定剂.此法价格较高,对环境污染较严重. Clem以及 Wang等人采用醋酸铅溶液与四氯化钛水解制得胶体,在形成凝胶时内部缺少足够的有机体,在煅烧过程中容易团聚,因而得到的粉体粒径较大. 有机电合成反应具有产率启、副产物少、反应过程中无毒无害或低毒低害等优点,是一种“绿色"过程,它可以通过调节电压控制反应速度,容易控制反应的开始、中断和停止,具有连续操作等特点.溶胶凝胶(Sol-gel)工艺就是将含有金属氧化物或氢氧化物的溶胶转变为凝胶,再将凝胶干燥后 ( 收稿日期:2004-09-27. ) ( 作者简介:朱传高(1969~),男,汉族,硕士,讲师,从事纳米材料合成及电化学研究, Email: zhucg88@126. com. ) ( 基金项目:安徽省高等学校青年教师科研基金(批准号:2004jq185)和安徽省淮南市科技局计划项目基金(批准号:2004B16). ) 进行煅烧,然后制得氧化物超微细粉的方法.由于溶胶凝胶法是以金属醇盐为起始原料,所以也称为醇盐水解法.现普遍认为,金属醇盐水解法是制备纳米粉体的有效方法,此法能够在较低合成温度下得到具有良好均一性、高纯度的产品.但传统方法1合成金属醇盐过程复杂、后处理困难,且使用的原料价格昂贵,在实际应用中受到限制.电化学技术在制备金属醇盐时最大优点是简便,使用纯金属电极为原料比化学方法使用的原料易于购买和处理.因此,电化学法合成金属醇盐以其显著的优点受到人们的青睐.我们采用钛片、铅片为“牺牲阳极,在乙醇和乙酰丙酮混合溶液中依次按一定电量进行电解,制得纳米 PbTiO,前驱体 PbTi(OCH, CH)-y(acac)然后将电解液直接水解,在700℃煅烧2h制备纳米 PbTO,粉体.由于胶体内部含有稳定性较高的乙酰丙酮基团,煅烧时放出一定量的二氧化碳,可以克服粉体团聚,同时也解决了 Pb(CH,COO)2·3H,O的溶解性.我们在实验中发现,钛醇盐对铅电极的溶解有促进作用,提高了电流效率.煅烧后所得纳米粉体产物粒径小、分布均匀,同时原料成本低、生产设备简单,适宜进行工业化生产. 1 实验部分 1.1 仪器与试剂 无水乙醇、氨水、乙酰丙酮均为AR级;石英亚沸蒸馏水自制;导电盐 BuNBr(AR)重结晶后备用;金属铅片(AR)、钛片(AR)分别经丙酮除油活化、无水乙醇清洗处理后作为“牺牲阳极待用.电解电源采用 HYL-A型直流电源(延吉市永恒电化学仪器厂产品).电解槽为自行设计的两电极无隔膜玻璃电解槽.电化学测定在 LK98B Ⅱ型微机电化学分析仪(天津兰力科化学电子高技术公司)上进行.采用日本岛津 DT-40热重分析仪和扫描差热分析析测试 TGDTA,升温速率为10℃/min,氩气保护.PbTiO,微晶的物相结构测定采用 Shimadzu公司的XRD-6000型X射线衍射仪(Cu靶,靴=0.15406nm). 利用 Hitachi H-600透射电子显微镜(TEM)观察样品微结构. 1.2 实验过程 电化学研究采用三电极系统,Pb电极(0.01cm)为工作电极,213型Pt电极(0.2×0.6 cm)为辅助电极,饱和甘汞电极(SCE为参比电极), 0.03 mol/L (BuN)Br和 0.2mol/L钛醇盐的乙醇溶液为电解液.线性扫描(扫描速度为1mV/s)与循环伏安扫描(扫描速度为100mV/s)在室温下进行,测试结果由计算机自动记录. 配制 0.03 mo1/L (BuN)Br的乙醇溶液,清洗处理后的铅片和钛片经准确称重,分别作为阴、阳两极,移入干燥的无隔膜电解槽中(电极距离为0.8cm、电极面积为2×3cm).控制电流0.2A电解钛片4h,交换电极电解铅片2h;电解过程中每隔30min加入 0. 1 cm乙酰丙酮.即可制得纳米PbTDO,前驱体铅、钛金属醇盐配合物.E电解反应机理阳极为: Ti→Tf*+4e. 阴极为: 总反应为: 向所得溶液中加入 0.5 cm蒸蒸馏水,同时用稀氨水调节 pH~8.5,控制温度40℃,溶液在18h后成为凝胶.凝胶经真空干燥24h后,于程序控温炉中(厦门宇光电子技术有限公司产品)在700℃煅烧2h,得到纳米PbTO,粉体. 2 结果与讨论 2.1 电化学分析 图1曲线a是铅电极在0.2mol/L钛醇盐的乙醇溶液中的线性扫描曲线(扫描前加入0.1cm乙酰 丙酮)..电位在0~0.4V,电流没有太大变化,表明此时电极呈非溶解状态;0.4V以上电极呈现活化溶解状态,电流随着电位的升高线性增大;当电位升至2.0V时,电流密度升至 31mA/cm.表明电极能保持较好的活化状态;阳极溶解曲线平滑,说明铅阳极溶解生成的产物能够较快地扩散进入溶液,并没有对电极产生钝化作用,说明铅阳极的溶解过程比较稳定. 图1中曲线b是铅电极在 0.2mol/L钛醇盐的乙醇溶液中的循环伏安曲线(扫描前加入0.1mL乙酰丙酮).由图1可见,铅阳极的溶解行为完全是一种不可逆过程,回扫期间没有还原电流出现,且没有副反应发生.表明铅阳极溶解生成的产物在此电压范围内是稳定的,有利于得到较纯的产物. Fig12APoarization curves of the Pb anode in ethanolsolution of 0.2 mol/L Tia lkoxide a Linearity scanning curve, scanning rate: 1 mV/s b.)ccyclic voltammogram curve, scanning rate: 100 mV/s 2.2 制备电解液的影响因素 镁、钛电极在反应前需经打磨、丙酮除油,以得到活性的金属表面.醇溶液中的水分对金属有钝化作用,并且随着含水量增加,合成纳米材料前驱体的槽电压越来越高,这是由于溶液中的水与活化金属发生了反应,形成氧化膜而阻止金属阳极继续溶解.为了防止阳极钝化,电解液在反应前应需严格除水.导电盐(BuN)Br中的Br对金属有腐蚀性,可以加速金属阳极的溶解.因此,采用0. 03 mo1/L (BuN)B作为导电盐. 控制温度为40℃,电极距离0.8cm,铅阳极面积 3X2cm,在0.03 mol/L (BuN)Br的乙醇溶液中逐渐增大电极电位,观察铅阳极溶解时电流密度(1)与电流效率(1)的变化(见表11).电流效率?;由公式 计算,其中0为实际消耗的电量,理论上所需的电量O.可按法拉第电解定律 计算,式中:m为金属溶解的质量;M为金属的摩尔质量;z为电极反应转移电子数;F为法拉第常数.随着电极电位升高,铅阳极溶解的电流密度迅速增大,电流效率减小.电解时电极电位不应高于18V,电压过高,易引起副产物增多,电流效率下降.电极电位低于6V,会使电解时间过长,影响生产效率.电极电位控制在10~12V为宜,此时电流效率为91.8%~93.1%. Table1 The relation between electrode potental titan ium complex and current density, effic iencyat the course of d issolution of lead anode Electrode potential/V 2.0 4.0 6.0 8.0 10 12 14 16 18 20 Current density (1) /(mA ·cm ) 8 15 22 28 34 39 42 43 44 44 Current efficiency (1)(%) 94.6 94.3 94.0 93.6 93.1 91.8 89.4 85.5 81.2 75.3 Current density (2)/(mA·cm) 11 20 28 35 41 45 48 50 51 52 Current efficiency (2)(%) 96.7 96.3 95.9 95.5 95.1 94.4 93.5 91.4 87.3 83.2 在 0.03 mol/L (BuN)Br的乙醇溶液中加入0.2 mol/L乙氧基钛配合物,逐渐增大电极电位.对比发现,电流密度(2)、电流效率(2)的变化趋势一致,但均比电流密度(1)、电流效率(1)有所增大.12V时电流密度由39mA/cm升至 45mA/cm,电流效率由91.8%升至94.4%,这说明乙氧基钛配合物对铅阳极溶解有促进作用.这可能与钛醇盐具有一定的酸性、[Ti(OR)具有较强的配位能力有关.因此,钛醇盐对 Pb电极的溶解有较强的活化作用,在制备纳米 PbTiO,前驱体中,应先电解 Ti 片,后电解 Pb片. 2.3 电解液的制备与结构表征 控制电解温度50℃、电流 0.2A,电解钛片约90min后,电解液出现淡黄色混虫,这是因生成的钛醇盐在乙醇中部分水解的所致,为不影响电解反应的进行,对其可用微量注射器加入0.1mL乙酰丙酮.由于乙酰丙酮的配位作用,既提高了钛醇盐在乙醇中的溶解度,又可以抑制醇盐水解,电解液恢复澄清.方法是每电解30min, 加入乙酰丙酮0.1cm.电解钛片过程中,电解液经历了无色-淡黄色-深棕色的颜色变化.乙酰丙酮在阴极上发生如下反应: 之后,控制温度40℃,在钛醇盐溶液中电解铅片,反应约30min后,铅片表面有一层黑色物质出现,这可能是金属阳极中不溶性碳与相应金属部分发生点蚀引起的.此时金属呈现多孔状,比表面积增大,溶解速率加快,少量金属来不及电解便从铅片表面脱落.随着电解的进行,溶液颜色逐渐变浅,最终成灰白色.由于生成的铅、钛醇盐在乙醇中的溶解度较小,并且很容易水解,沉积于电极表面,阻止电解反应的顺利进行.因此,为了加快电解过程中醇盐的扩散,提高乙酰丙酮与金属离子的配位能力,电解过程中应不断搅拌电解液. 图2是前驱体 PbTi(OCH, CH)6-y(acac),的红外光谱图.在1559cm 和1422cm处有配位的乙酰丙酮基的两个特征吸收收,即C一O键的谱峰和C和C键的谱峰.在1090cm 附近出现 CO键伸缩振动的吸收峰;在652~573 cm 有金属与氧原子间配位键的振动吸收峰.与文献[12]对照,表明前驱体中含有乙酰丙酮基团.图3是前驱体PbTi(OCH, CH, )6-y (acac),的拉曼光谱图.在1500 cm 附近出现配位的乙酰丙酮基C=0键和C=C键的特征吸收峰,其为一宽峰;在1180 cm 出现C—O键伸缩振动的吸收峰;在676 cm,551cm有铅、钛金属与氧原子间配位键的振动吸收峰.与红外光谱图一致,粉体中含有乙酰丙酮基团可以有效克服煅烧过程中的硬团聚现象,得到结构疏松分散的粉体. Fig.2 FTIR spectra of the precursorPbTi(OCH,CH,)s-,(acac), Fig.3 Raman spectrum of the precursorPbTi(OCH,CH,)6-,(acac), 2.4 干凝胶的制备与煅烧 实验结果表明,先电解钛片4h,再电解铅片2h所得到的前驱体浓度约为0.20mo1/L,适宜直接进行水解.水解温度控制在40℃, pH值为 8.5,此时产率超过90%. 当用乙醇洗涤胶体时,乙醇在替换吸附水以降低硬团聚的同时,还能替换胶体颗粒内部的水合分子.因此,采用醇洗的办法可以明显降低粉体的团聚程度. 经三次醇洗后的胶体真空干燥(60℃)24h, 得到干凝胶[PbTi(OCH,CH)6-x-p(OH). (acac),]为疏松、均匀的粉体,图4为其电子透射形貌图.粉体颗粒尺寸分布均匀,粒径在10 mm左右.这是由于凝胶颗粒表面上的自由水分子很少,难以和相邻颗粒表面形成氢键,颗粒间相互接近而形成化学键的可能性几乎没有,引入乙酰丙酮基也增加了产物位阻及稳定性,从而防止了硬团聚.而经水洗的胶体干燥后,呈结块状. 干燥后的凝胶经煅烧可除去吸附的有机基团以促进产物晶体的形成.煅烧温度及时间对粉体的颗粒大小和团聚程度均有一定影响.[14]利用差热热重分析可以了解在不断升温过程中干凝胶粉的变化情况.图5为干凝胶的差热分析、热重分析曲线.从图5可以看出,热分解过程可以分为两个阶段.第一阶段分解温度在 68.6~286℃,呈现吸热反应,其中失重率为25.6%,这是由于剩余水分、乙醇的挥发以及乙醇基团的分解所致.在374~683℃出现一个很强的放热峰,失重率为7.91%,这主要归因于干凝胶中乙酰丙酮基和部分炭化产物燃烧引起的放热反应的影响.在640℃之后失重率极小,却出现了很强的放热现象,这主要是由于纳米 PbTiO晶晶体结构的逐渐形成,所以煅烧的适宜温度约为640℃.化学反应方程式为: PbTi(OCH, CH,)6-x-y(OH). (acac),→ PbTio; +(12-2x+3y)COz + (15-2x+y)H,0. Fig. 4 TEM micrograph of the xerogel PbTi(OCH,CH,)6-r-(OH)(acac), Fig.5 TG-DTA curves for the xerogela. Curve for DTA; b. curve for TG. 2.5 纳米粉体的结构与形貌表征 图6是钛、铅复合醇盐水解后的粉体在700℃下煅烧2h后的 XRD谱图.从图6可以看出,产物在20为21.38°,22.76°,31.44°,32.41°,39.17°,46.51°,55.34和57.24处均出现清晰的特征吸收峰,分别归属于钙钛矿型 PbTiO,的(001),(100),(101),(110),(111),(200),(112)和(211)处晶面峰.其中22.76°,31.44和32.41处为主峰,与标准卡片(JCPD S06-0452)吻合,与文献[6,7]报道的结果一致. 图7是干凝胶在700℃下煅烧2h后所得粉体样品的颗粒形貌图.从图7可以看到,粉体的颗粒尺寸比较均匀,粒径在10~15 nm之间.这是由于干凝胶中含有乙酰丙酮基团和乙醇基团,在煅烧过程中产生CO,等气体,形成许多空隙,从而抑制了粉体团聚,使制得的 PbTO粉体粒径较小且分布较均匀.当温度超过700℃时,PbTiO;粉体会出现一定程度的团聚现象.结合差热热重分析结果,煅烧温度控制在640~700℃为宜. Fig. 6 X-ray diffraction patterns of nanometerPbTiO, calcined at 700 ℃ Fig.7 TEM image of nanometer powder PbTiO,calcined at 700℃ 综上,电化学方法制备的纳米 PbTD;前驱体含有乙酰丙酮基团,在水解、干燥、煅烧过程中起到抑制团聚的作用.水解后在60℃真空干燥24h,得到疏松、均匀的干凝胶粉体,粒径在 10mm左右.干凝胶煅烧温度控制在700℃时,得到的 PbTiO,粉体粒径分散均匀,平均粒径在10~15 mm,无团聚 发生.该方法操作步骤简单. ( 参 考 文 献 ) ( [1] LuC J, K uang A X , H uang G Y. X -ray P h otoelectron S p ectro scopy Study on Co m position and Structure of Sol-gelDerived PbTiD, Thin Fims [J]. J Appl Phys, 1996, 80(1):202—207. ) ( [2] JaberB, R e miens D, Thierry B. Su bs trate Temperature and Target Composition Effects on PbT i o, Thi n Fims Produ c ed in Situby Sputter i ng [ J]. J Appl P hys,1 9 96,79(2 ) :1182—1185 ) ( [3] Yamashita A, T atsumi T Growth Model fo r PbTo, Thi n Fim s Grow n by Su r fa c e-reaction Enh a nced Metalorganic Chem ical Vapor Depositio n [J ]. Appl Phys Lett, 19 9 5,67(9) : 1208—1211. ) ( [4] Fujisawa H, Okaniwa M, Nonomura H , e t al Ferielectricity of th e 1 . 7 nm-high a nd 38 n m wide Se l f-assembled PbTD, Island [ J ]. Joumal of the European Ceram ic Society, 2004, 2 4(6):16 4 1—1645. ) ( [5] Politova ED, A b dulova A S, K al e va OM, et al Proces s ing, Dielec t ric and Piezoe l ectric Prope r ties of the PbTi o , -based Ceramics [J] .F erroelectric s , 2003,293(1) : 247—252 ) ( [6] Clem P G , P a yne D A, Warren W L. Ob s er v ation of Two Charge States of Ruthenium in PbTi , S i ngle C r ystals [J ]. J Appl Phys , 199 5 ,77( 1 1) : 5865—5868. ) ( 「71 WANG Yu-guo, ZHA N G Pei-lin, QU B a o-d o ng, et al Orien t ed PbTD, Fims from Metalor g anic Precursors [J]. J ApplPhys, 1992 , 71(12) : 6121—6124 ) ( [8] WEIYi-jun, CHEN Shi-k u n, CHU D a o-bao, et al E l ectrochem ical Preparation and Characterization of Comp lex Fim ofNanocrystalline TiO /polyaniline [J]. Joumal of Jili n Universi t y (Science Editi on ), 2003, 4 1(4) : 521—525. (魏亦军,陈士昆,褚道葆,等.纳米 TO,/聚苯复复合膜电极的电化学制备及其表征[J].吉林大学学报(理学版), 2003,41(4):521—525.) ) ( [9] ZHU Chuan-gao, WEI Yi-jun, ZHU Qi-yong, et alElectro-synthesis ofL i and A1 A lkoxides, and I ts Sol-gel Course[J]. New Technology & New Process , 2004 , 10: 6 7—69 (朱传高,魏亦军,朱其永,等.锂、铝醇盐的电合成及 其凝胶工艺[J].新技术新工艺,2004,10:67—69) ) ( [10] Caulton K G , Hubert-PfalzgrafL G Synthesis, Structural Principles, and React i vity of Heterometallic A lkoxides [J]. Chem Rev, 1990, 90(6):969—995. ) ( [11] ZHU C huan-gao, ZHOU X i ng-fu, C HU D a o-bao Electrolytic Preparatio n of Nano-grade LiTi04 P owder [ J ]. . Fine Chem icals,2003,20(4):244—246. (朱传高,周幸福,褚道葆.电解法制备纳米LiTi04粉体 J1.精细化工, 2003,20(4):244—246.) ) ( [12] Errington R H, R idland J , Clegg W. BDi k etonate Deri v atives of Titanium A lkoxides: X-ray Crystal Str u ctures andSolution Dynamics of the B inuclear Comp lexes [Ti(OR), (di k )]?[J]. Polyhedron, 1998,5 ( 6):659 — 665. ) ( [13] Selvaraj U , B rooks K, Parasadaro A V, et al S ol-gel Fabrication of Pb (Zr 5 2 Ti4 8 )O Thin Fim sU sing Lead Acetylac- etonate as the Lea d Sourc e [J ] . Am Ceram Soc , 1997, 76(6):1441—1447. ) ( [14] ZHA I Xue-liang, ZHANG Su-fang Effect o f Hydrothemal Parameter s on Grain Siz e an d Momholgy of PbTiO,Nano-crystalline [J]. Joumal of the Chinese Ceram ic Society, 200 4 , 32(2):196—199. (翟学良,张素芳.水热条件对PbTO纳米晶粒径和形貌的影响 [ J]. 硅酸盐学报,20 0 4,32(2):1 9 6—199. ) ) ( [15] SONG Xiu-qin, C HEN Ru-fen, JA Mi-ying Synthesis ofL i Si by S ol-gelMethod [J]. Appl Chen, 2000 , 17(3): 304—306. (宋秀芹,陈汝芬,贾密英.溶胶凝胶法合成 LiSio [J]. 应用化学,2000,17(3):30 4 —306.) ) ( (责任编辑:李桂英) ) ◎China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
确定





还剩4页未读,是否继续阅读?
天津市兰力科化学电子高技术有限公司为您提供《纳米PbTiO3 粉体中由铅、钛乙醇盐配合物制备过程检测方案(电化学工作站)》,该方案主要用于其他中由铅、钛乙醇盐配合物制备过程检测,参考标准--,《纳米PbTiO3 粉体中由铅、钛乙醇盐配合物制备过程检测方案(电化学工作站)》用到的仪器有天津兰力科电化学工作站LK98BII
推荐专场
相关方案
更多
该厂商其他方案
更多
















