钛酸镁是一种优良的微波介质材料9":8;& 以钛酸镁为主晶相制作的谐振器’ 滤波器在通信产业中获得广泛的应用9!<%;" 目前$制备这类粉体的方法有固相
反应法’气相淀积法’溶液法等" 如何减少这些方法获得的=5>?@8中的=5>?*@%
含量$成为常规工艺要研究的难题之一"现普遍认为$ 金属醇
方案详情

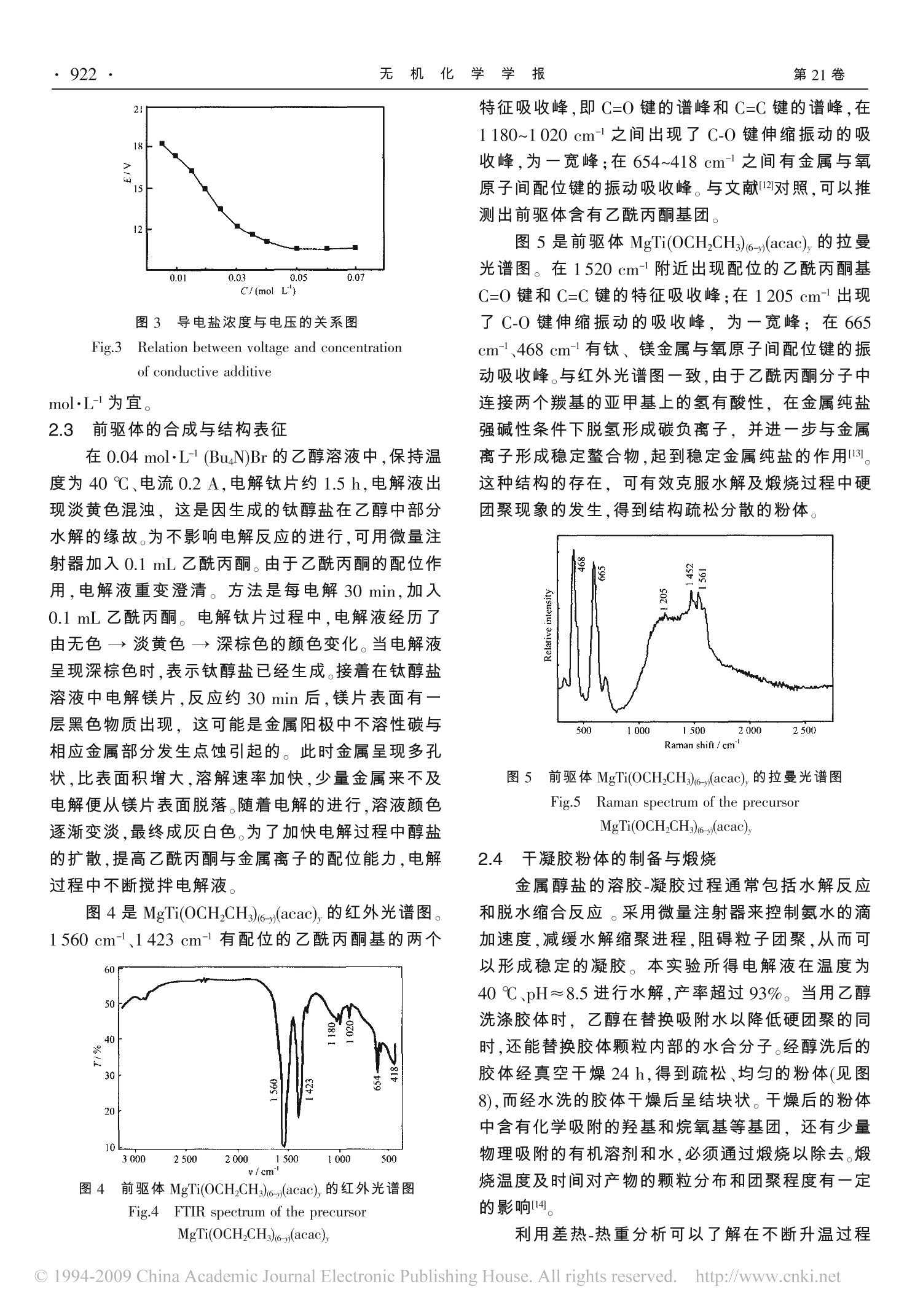
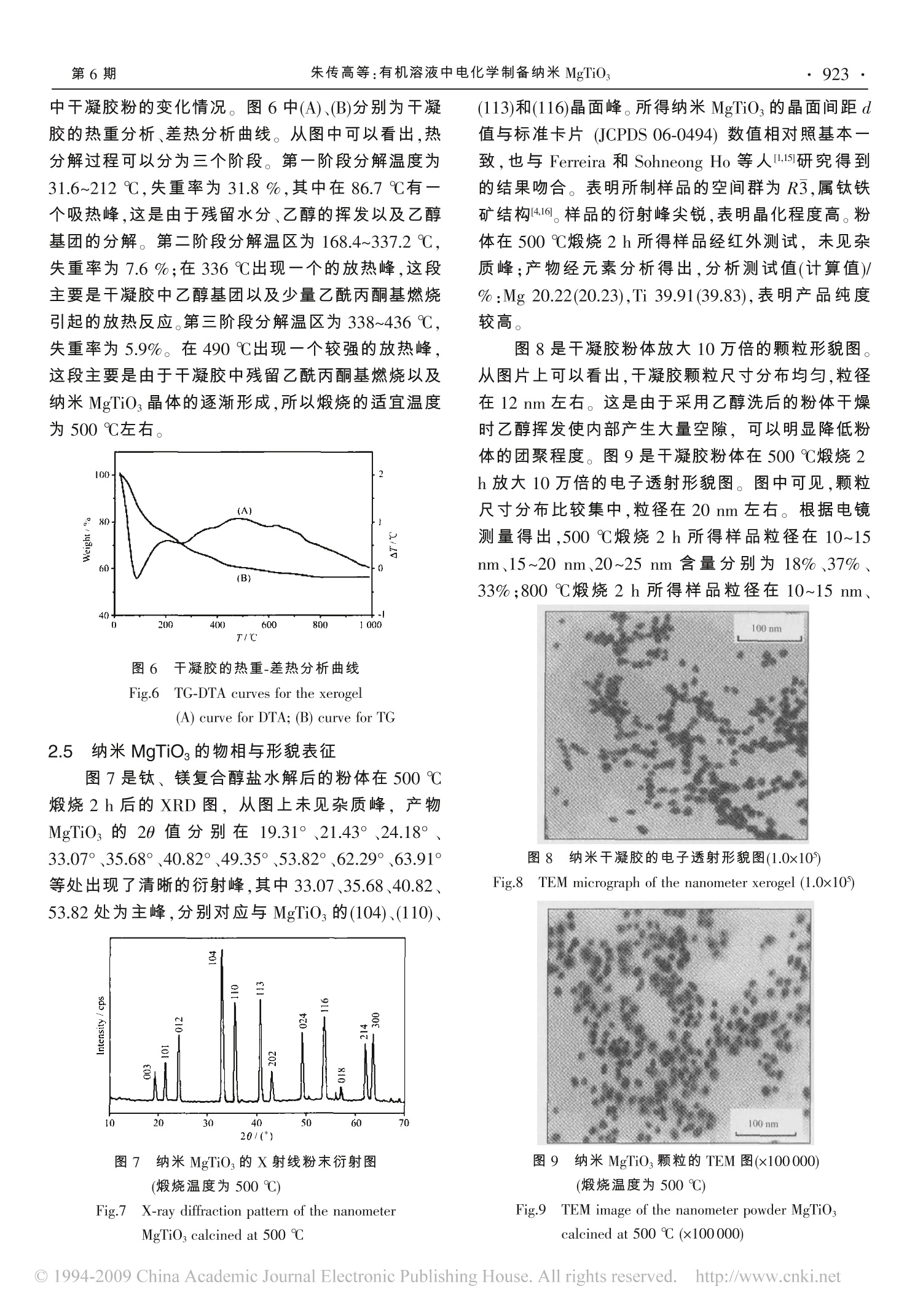
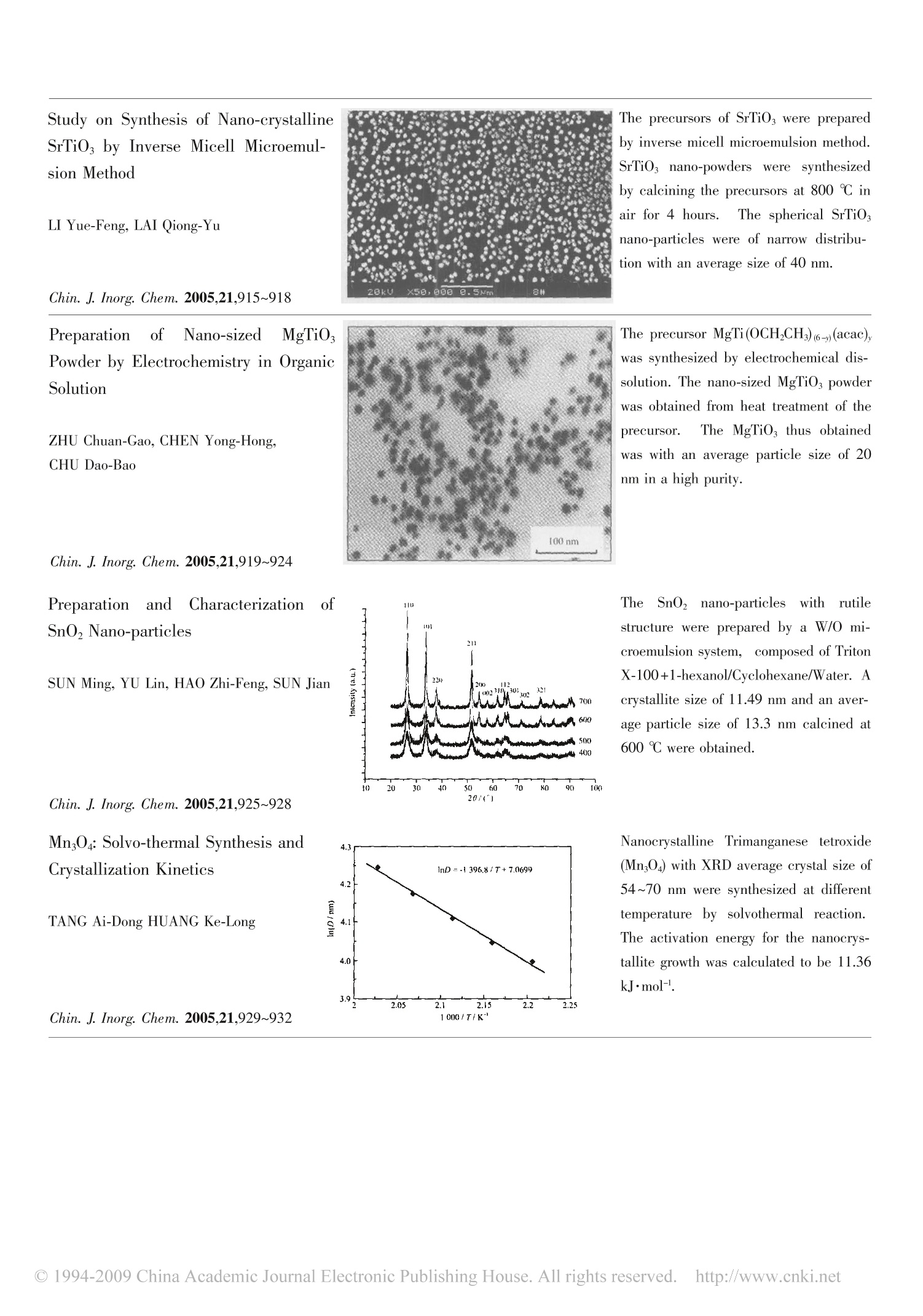
Vol.21 No.6Jun.,2005无 机 化 学 学 报CHINESE JOURNAL OF INORGANIC CHEMISTRY第6期2005年6月 无 机 化 学 学 报·920·第21卷 研究简报 CGe 有机溶液中电化学制备纳米 MgTiOg 朱传高*1 陈永红1 褚道葆² (淮南师范学院化学系,淮南 232001)(安徽师范大学有机化学研究所,芜湖 241000) 关键词:电化学;电合成;溶胶-凝胶;纳米 MgTiO 中图分类号:0646;0614.2;0612.4 文献标识码:A 文章编号:1001-4861(2005)06-0919-06 Preparation of Nano-sized MgTiO,Powder by Electrochemistry in Organic Solution ZHU Chuan-Gao*,1CHEN Yong-HongCHU Dao-Bao² (Department of Chemistry, Huainan Normal College, Huainan 232001) (Institute of Organic Chemistry, Anhui Normal University, Wuhu 241000) Abstract: In a cell without separating the cathode and anode spaces, the precursor MgTi(OCH,CH)(6-)(acac), ofthe mixed oxide MgTiOs was directly synthesized by electrochemical dissolution of titanium for 4 hours and thenof magnesium for 1 hour 40 minutes at the current of 0.2 A in ethanol and acetyl-acetone solution..The nano-MgTiOs powder was prepared by a direct sol-gel process of the electrolyte solution under pH≈8.5 followed bywashing, drying in vacuum for 24 h, and calcination at 500 ℃ for 2 h. IR and Raman spectroscopy, XRD, andTEM were used to investigate the structure of nano-MgTiOs and its precursor. The result suggested that it wasmore appropriate to control the temperature between 35~40 ℃ and the concentration of conductive additive(BuN)Br at 0.04 mol·L-. The xerogel with an average particle size of 12 nm and the nano-MgTiOs of 20 nm wasthus obtained in a high purity. 钛酸镁是一种优良的微波介质材料1-3。以钛酸镁为主晶相制作的谐振器、滤波器在通信产业中获得广泛的应用[45]。目前,制备这类粉体的方法有固相反应法、气相淀积法、溶液法等。如何减少这些方法获得的 MgTiOs中的 MgTizOs 含量,成为常规工艺要研究的难题之一。 现普遍认为,金属醇盐水解法是制备纳米粉体的有效方法,能够在较低合成温度下得到具有良好均一性、高纯度的产品16.7。这是由于醇盐水解得到的 胶体内部含有较多的有机体,煅烧时放出一定量的二氧化碳,可有效地克服粉体的团聚。但传统方法合成金属醇盐过程复杂、后处理困难,且使用的原料价格昂贵,在实际应用中受到了限制。因此,对其合成方法的研究具有重要的意义。电化学方法可以通过控制电极电位或电流强度来较好地控制产物的化学计量比,合成条件也比较简单89。 本文采用钛片、镁片为“牺牲”阳极,在乙醇和乙酰丙酮混合溶液中依次按一定电量进行电解,制得 ( 收稿日期:2004-11-08 。 收修改稿日期:2005-01-05。 ) ( 安徽省高校青年教师科研资助计划(No.2004jq185)资助,安徽省淮南市科技局计划项目(No.2004B16)资助。 ) ( *通讯联系人。E-mail:zhucg88@126.com ) ( 第一作者:朱传高,男,36岁,安徽滁州人,讲师,硕士;研究方向:纳米材料合成及电化学研究。 ) 纳米 MgTiOs前驱体MgTi(OCH,CH)(6-)(acac),[acac 为乙酰丙酮基],再用 Sol-gel法制备纳米MgTiOs。产物中未发现 MgTiz0s杂质,纳米MgTiOs平均粒径在20nm 左右。不仅克服了产物纯度不高、产率低等缺点,而且具有成本低、适宜工业化生产等优点。 实验部分 1.1 仪器与试剂 无水乙醇、氨水、乙酰丙酮,均为分析纯;石英亚沸蒸馏水,实验室自制;导电盐(BuN)Br(A.R.)经过重结晶备用;镁条(A.R.)、钛片(A.R.)分别经丙酮除油活化、无水乙醇清洗处理后作为“牺牲”阳极待用。电解电源采用 HYL-A 型直流电源(延吉市永恒电化学仪器厂)。电解槽采用自行设计的两电极无隔膜玻璃电解槽。电化学测定在LK98BⅡ型微机电化学分析系统(天津兰力科化学电子高技术公司)上进行。 1.2 实验过程 电化学研究:采用三电极系统,Mg电极(0.01cm²)为工作电极,213型Pt电极(0.2×0.6cm²)为辅助电极,饱和甘汞电极(SCE)为参比电极,0.04 mol.L(BuN)Br的乙醇溶液以及钛醇盐溶液为电解质,扫描前均加入 0.1 mL 乙酰丙酮。电化学测试在室温下进行,测试结果由计算机自动记录。 纳米 MgTiOs制备:处理后的镁条和钛片经准确称重,分别作为阴、阳两极,移入干燥的无隔膜电解槽中,0.04 mol·L-(BuzN)Br 的乙醇溶液作为电解液。在磁力搅拌、氩气保护的条件下,控制电流为0.2 A电解钛片4.0h,然后再交换电极电解镁片1.67h,电解过程中每隔30 min 加入 0.1 mL乙酰丙酮。电解反应原理如下: 得到具有弹性的胶体。向所得溶液中加入1.0mL 的亚沸蒸馏水,同时滴加稀氨水控制pH~8.5,溶液12h后凝胶。将此胶状物用无水乙醇清洗,以1500 rpm 转速离心分离2次,放置陈化 24h。将凝胶在60℃下真空干燥24 h,把干凝胶放入马弗炉中在500℃下煅烧2h,得到纳米MgTiO3粉体。 红外光谱测试在 Nicolet 公司的AVATAR360 型傅立叶变换红外光谱仪上进行(KBr压片,直径为13 mm,用量约2.0 mg),收集范围400~4000 cm-,分辨率为4cm-,收集10次。在惰性气氛下前驱体密封在毛细玻璃管中测定其拉曼光谱,采用 Labram I型共聚焦显微拉曼系统(Dilor,France),激发线波长为632.8 nm 的 He-Ne 激光器。TG-DTA采用日本岛津DT-40热分析仪测试,升温速率为10℃·min-。MgTiOs微晶的物相采用 Shimadzu 公司的 XRD-6000型X-射线衍射仪(Cu Ko 靶,入=0.15406 nm, 35kV-25mA), 扫描范围10°~70°,以扫速 4°·min-测试。TEM 测试在 Hitachi H-600 透射电子显微镜上进行。 2 结果与讨论 2.1 电化学分析 图1(I)是镁电极在 0.04 mol·L-(BuN)Br 的乙醇溶液中的极化曲线(扫描速度为1mV·s-l)。从图中可以看出,电压在0.4V以上,电极表面钝化膜被击穿,随着电位的升高,电流迅速增大;当电位升至2.0Ⅴ时,电流密度升至31.5 mA·cm。表明镁电极活化溶解状态良好;镁阳极溶解生成的产物能够较快地扩散进入溶液,并没有对电极产生钝化作用,说明镁阳极的溶解过程是比较稳定的。 图1(Ⅱ)是在上述溶液中加入0.2 mol·L-乙氧基钛时的极化曲线(扫描速度为1mV·s-)。在没有外加电压时,电流密度为1.7 mA·cm2,表明此时电极呈溶解状态,即镁条在一定程度上被活化溶解,这既与镁条的活泼性有关,也与导电盐(BuN)Br 中 Br对金属的腐蚀性0以及钛醇盐具有一定酸性有关。随着 图1 镁阳极在0.04 mol·L-(BuN)Br的乙醇溶液中的极化曲线(扫描速度为1 mV·s-) Fig.1 Polarization curve of the Mg anode in ethanolsolution of 0.04 mol·L-(Bu N)Br(scanning rate: 1 mV·s-)C(Ti alkoxide) / (mol·L-): (I):0; (I):0.2 电位的升高,电流迅速增大,与曲线(I)变化趋势相同;但电位相同时,电流强度均有不同程度增大;当电位升至2.0Ⅴ时,电流密度升至37.5 mA·cm。表明钛醇盐能促进镁阳极的迅速溶解,提高电流效率。 2.2制备纳米 MgTiOs前驱体的影响因素 2.2.1 电极活化与电解次序 镁、钛电极在反应前需先用丙酮除油,或采用高 电位溶解击穿氧化膜的方法活化,以便得到新鲜的金属表面,这是电化学合成纳米材料前驱体的关键因素。另外,醇溶液中的微量水份对金属表面有钝化作用,生成一层金属氧化物的保护膜,阻止金属阳极的溶解,故电解液在反应前应严格除水。电解过程中电极电位、钛醇盐浓度对镁电极溶解的电流效率有较大的影响(见表1)。 Table 1 Effect on of anode voltage and titanium complex on the current efficiency (n;)for magnesium dissolution (T=40℃) Anode voltage/V 1.0 2.0 4.0 8.0 10.0 12.0 14.0 16.0 18.0 7% 97.4 97.0 96.5 95.6 95.1 93.6 92.0 89.2 86.1 2/% 98.1 97.8 97.2 96.6 96.0 94.7 93.1 90.2 86.9 n3/% 98.7 98.4 98.0 97.3 96.9 96.1 94.8 91.5 87.6 74/% 98.4 98.1 97.6 96.8 96.3 95.0 93.5 900.0 86.7 温度为40℃在0.04 mol·L- (BuN)Br 的乙醇溶液中电解镁片时,随着电极电位的升高,电流效率下降(见电流效率n);但电流强度大,电解时间短,生产效率高。因此,选择电极电位为10V比较合适,此时电流效率为95.1%。当加入一定量钛醇盐时电流效率会有所增大(见电流效率2、73、74),这可能与钛醇盐具有一定的酸性有关,也与[Ti(OR)。P具有较强的配位能力有关,同时镁醇盐的溶解度比钛醇盐要小。因此,在制备纳米 MgTiO前驱体时,宜先电解钛片,然后电解镁片。通过表1可以发现,当钛醇盐浓度超过 0.2 mol·L-,电流效率不再增大,甚至出现下降趋势。这是由于溶液浓度增大,阻碍了镁醇盐的扩散,形成农差极化而降低电流效率。同时,钛醇盐浓度增大,水解性增强,易在电极表面形成沉积而阻碍电解。因此,钛醇盐浓度控制在0.2 mol·L-较为适宜。 以恒电流方式电解反应,根据时间得出实际消耗的电量Q;称出阳极溶解的质量,可按法拉第电解定律计算理论上所需的电量Q,并由此计算出电流效率ni: 式中m:金属溶解的质量;M:金属的摩尔质量;z:电极反应转移电子数;F:法拉第常数。 2.2.2导电盐浓度与电解温度 图2是镁电极在0.04 mol·L-1(BuN)Br 的乙醇溶液中温度与电流强度关系图。由图看出,控制槽电压为15V,温度为10℃时电流强度为 0.14A;随着 温度的升高,电流随之增大,温度与电流呈线性关系。而在30~40℃之间电流增加趋缓;在40℃以上,电流出现一平台,甚至有下降的趋势,这是由于温度的升高加速了镁醇盐的水解而形成了部分溶胶阻止电解的缘故。升高温度可以提高导电盐的导电能力,提高电解过程的电流效率。所以反应的最佳温度宜控制在35~40℃,此时镁阳极溶解的电流效率为94.7%。 图2 电解温度与电流强度的关系 Fig.2 Relation between temperature for electrolysisand current intensity 图3是镁电极溶解时导电盐浓度与电压的关系图。保持温度为40℃、电流0.2A不变,在导电盐浓度为0.005~0.10 mol·L-1范围内逐渐增大其浓度,观察电压的变化。结果表明,在浓度为0.005~0.04mol·L-1,电压随导电盐浓度的增大呈线性降低;浓度为0.03 mol·L-时,电压下降至12V。当浓度超过0.04 mol·L-时,电压下降的速度明显减小以至不再降低。因此,实际电解时有机胺导电盐浓度以0.04 图3 导电盐浓度与电压的关系图 Fig.3 Relation between voltage and concentrationof conductive additive mol·L-为宜。 2.3 前驱体的合成与结构表征 在0.04 mol·L-(BuaN)Br的乙醇溶液中,保持温度为40℃、电流0.2A,电解钛片约1.5h,电解液出现淡黄色混浊,这是因生成的钛醇盐在乙醇中部分水解的缘故。为不影响电解反应的进行,可用微量注射器加入0.1 mL乙酰丙酮。由于乙酰丙酮的配位作用,电解液重变澄清。方法是每电解30 min,加入0.1 mL 乙酰丙酮。电解钛片过程中,电解液经历了由无色→淡黄色→深棕色的颜色变化。当电解液呈现深棕色时,表示钛醇盐已经生成。接着在钛醇盐溶液中电解镁片,反应约 30 min 后,镁片表面有一层黑色物质出现,这可能是金属阳极中不溶性碳与相应金属部分发生点蚀引起的。此时金属呈现多孔状,比表面积增大,溶解速率加快,少量金属来不及电解便从镁片表面脱落。随着电解的进行,溶液颜色逐渐变淡,最终成灰白色。为了加快电解过程中醇盐的扩散,提高乙酰丙酮与金属离子的配位能力,电解过程中不断搅拌电解液。 图4是MgTi(OCHCH3)(6-)(acac),的红外光谱图。1560 cm-、1423 cm-有配位的乙酰丙酮基的两个 图4 前驱体MgTi(OCH,CH3)(6-)(acac), 的红外光谱图 Fig.4 FTIR spectrum of the precursorMgTi(OCH,CH3)(6-)(acac), 特征吸收峰,即 C=O 键的谱峰和 C=C键的谱峰,在1180~1020 cm-之间出现了 C-O 键伸缩振动的吸收峰,为一宽峰;在654~418 cm-之间有金属与氧原子间配位键的振动吸收峰。与文献对照,可以推测出前驱体含有乙酰丙酮基团。 图5是前驱体MgTi(OCH,CH)(6-))(acac), 的拉曼光谱图。在1520 cm-附近出现配位的乙酰丙酮基C=O 键和 C=C 键的特征吸收峰;在1205cm-出现了 C-O 键伸缩振动的吸收峰,为一宽峰;在665cm-、468 cm-有钛、镁金属与氧原子间配位键的振动吸收峰。与红外光谱图一致,由于乙酰丙酮分子中连接两个羰基的亚甲基上的氢有酸性,在金属纯盐强碱性条件下脱氢形成碳负离子,并进一步与金属离子形成稳定螯合物,起到稳定金属纯盐的作用3。这种结构的存在,可有效克服水解及煅烧过程中硬团聚现象的发生,得到结构疏松分散的粉体。 图5 前驱体 MgTi(OCH,CH)6-y)(acac),的拉曼光谱图 Fig.5 Raman spectrum of the precursorMgTi(OCH,CH36-)(acac), 2.4干凝胶粉体的制备与煅烧 金属醇盐的溶胶-凝胶过程通常包括水解反应和脱水缩合反应。采用微量注射器来控制氨水的滴加速度,减缓水解缩聚进程,阻碍粒子团聚,从而可以形成稳定的凝胶。本实验所得电解液在温度为40℃、pH≈8.5进行水解,产率超过93%。当用乙醇洗涤胶体时,乙醇在替换吸附水以降低硬团聚的同时,还能替换胶体颗粒内部的水合分子。经醇洗后的胶体经真空干燥 24 h,得到疏松、均匀的粉体(见图8),而经水洗的胶体干燥后呈结块状。干燥后的粉体中含有化学吸附的羟基和烷氧基等基团,还有少量物理吸附的有机溶剂和水,必须通过煅烧以除去。煅烧温度及时间对产物的颗粒分布和团聚程度有一定的影响4。 利用差热-热重分析可以了解在不断升温过程 中干凝胶粉的变化情况。图6中(A)、(B)分别为干凝胶的热重分析、差热分析曲线。从图中可以看出,热分解过程可以分为三个阶段。第一阶段分解温度为31.6~212℃,失重率为31.8%,其中在86.7℃有一个吸热峰,这是由于残留水分、乙醇的挥发以及乙醇基团的分解。第二阶段分解温区为168.4~337.2℃,失重率为7.6%;在336℃出现一个的放热峰,这段主要是干凝胶中乙醇基团以及少量乙酰丙酮基燃烧引起的放热热应。第三阶段分解温区为338~436℃,失重率为5.9%。在490℃出现一个较强的放热峰,这段主要是由于干凝胶中残留乙酰丙酮基燃烧以及纳米 MgTiO晶体的逐渐形成,所以煅烧的适宜温度为500℃左右。 图6 干凝胶的热重-差热分析曲线 Fig.6 TG-DTA curves for the xerogel(A) curve for DTA; (B) curve for TG 2.5 纳米 MgTiOs的物相与形貌表征 图7是钛、镁复合醇盐水解后的粉体在500℃煅烧2h后的XRD图,从图上未见杂质峰,产物MgTiO,的 20 值分别在19.31°21.43°24.18°、33.07°35.68°40.82°49.35°53.82°、62.29°63.91°等处出现了清晰的衍射峰,其中33.07、35.68、40.82、53.82处为主峰,分别对应与 MgTiOs 的(104)、(110)、 图7 纳米 MgTios的X射线粉末衍射图(煅烧温度为500℃) Fig.7 X-ray diffraction pattern of the nanometerMgTiOs calcined at 500 C (113)和(116)晶面峰。所得纳米 MgTiOs的晶面间距d值与标准卡片 (JCPDS 06-0494) 数值相对照基本一致,也与 Ferreira 和 Sohneong Ho 等人I.15]研究得到的结果吻合。表明所制样品的空间群为R3,属钛铁矿结构[4.161。样品的衍射峰尖锐,表明晶化程度高。粉体在500℃煅烧2h所得样品经红外测试,未见杂质峰;产物经元素分析得出,分析测试值(计算值)/%:Mg 20.22(20.23),Ti 39.91(39.83),表明产品纯度较高。 图8是干凝胶粉体放大10万倍的颗粒形貌图。从图片上可以看出,干凝胶颗粒尺寸分布均匀,粒径在12 nm 左右。这是由于采用乙醇洗后的粉体干燥时乙醇挥发使内部产生大量空隙,可以明显降低粉体的团聚程度。图9是干凝胶粉体在500℃煅烧2h放大10万倍的电子透射形貌图。图中可见,颗粒尺寸分布比较集中,粒径在20 nm 左右。根据电镜测量得出,500℃煅烧2h所得样品粒径在10~15nm、15~20 nm、20~25 nm含量分别为18%、37%、33%;800℃煅烧2h所得样品粒径在10~15 nm、 图8 纳米干凝胶的电子透射形貌图(1.0×10) Fig.8TEM micrograph of the nanometer xerogel (1.0x10) 图9 纳米MgTiO,颗粒的 TEM 图(x100000)(煅烧温度为500℃) Fig.9 TEM image ofthe nanometer powder MgTiO,calcined at 500℃(×100000) 15~20 nm、20~25nm、25~30 nm 含量分别为9%、14%、31%、36%。表明500℃煅烧后颗粒粒径分布较集中,粒子没有明显的团聚现象,这是由于干凝胶中含有一定量有机体,在煅烧过程中有机体分解产生许多空隙,抑制了粉体团聚的形成,从而使所得的MgTiOs粉体粒径较小;800℃煅烧2h所得样品粒径有所增大。因此,干凝胶的适宜煅烧温度为500℃左右。 3 结 论 本文探索了一种电化学合成前驱体,直接水解制备纳米 MgTiOs粉体的方法,初步考察了制备过程的影响因素。结果表明,保持有机胺导电盐浓度为0.04 mol·L-1,控制阳极电流强度0.2A,先电解钛片4h,再电解镁片1.67 h,即可得到适宜水解的前驱体 MgTi(OCH,CH)(6-)(acac),,胶体内部含有稳定性较高的乙酰丙酮基团,煅烧时放出一定量的二氧化碳,可以克服粉体团聚。粉体煅烧的温度控制在500℃较为适宜,电化学溶解金属阳极直接水解法制备的纳米 MgTiOs,平均粒径在20 nm。该方法操作步骤简单,容易控制产物的配比,同时具有产物纯度高、原材料成本等特点。 ( 参考文献: ) ( [1] F erreira V M . Journal ofMaterials Science, 1993,28(11):5894~ 5900 ) ( [2] Ferreir a V M. J . Am. Ceram. Soc., 1996,79(6):1697~1698 ) ( [3] Ferrelra V M. Materials Research Bulletin, 1994,29(10):1017~ 1023 ) ( [4] Mitchell J N, Yu N, Sickafus K E , e t al. Philosophical Maga-zine A,1998,78(3):713~725 ) ( [ 5 ] Alberta E F , G uo R, Bhalla A S . F er r oelectrics, 2002,268: 169~174 ) ( [6] XU Bing-She(许并社). General Material Science(材料科学概论). Be i jing: Beijing In d ustry Un i versity Pr e ss, 2002.164. ) ( [7] CHU Dao-Bao(褚道葆), ZHOU X ing-Fu(周幸福), LIN Chang- Jian(林昌健). Gaodeng Xuexiao H u axue X u ebao(Chem. J . Chin. U niv.), 2000,1:133~135 ) ( [8] ZHU Chuan-Gao(朱传高), WEI Y i-Jun(魏亦军), ZHU Qi- Y ong(朱其永), et al. Xinjishu X ingongyi(New T echnology & New Process), 2004,10:67~69 ) ( [9] ZHU Chuan-Gao(朱传高), ZHOU Xing-Fu(周幸福), CHUDao-Bao(褚道葆). Ji n gxi Huagong(Fine C h emicals), 2003,20 (4):244~246 ) ( [10JLI Di(李 荻 ). Electrochem Principle(电化学原理). Bei j ing:Beijing Aerospace Un i versity Press, 1998.416 ) ( [ 1 1]CHEN Ti-Xian(陈体衔). El e ctrochemical on E xperiment(实验电化学). Xiamen: Xiamen Univ e rsity Press, 1992.3 ) ( [12]R. John Errington, John Ridland, W illiam Clegg. Polyhedron., 1998.5~6:659~665 ) ( [13]HiranoSI, Y o go T, K i kuta K, et a l. Am. Ceram. Soc., 1 992,75(10):2785~2790 ) ( [14]ZHA I Xue-Liang(翟学良), ZHANG S u-Fang(张素芳). Guisuanyan X u ebao(Journal ofthe Chinese Ceramic So c iety). 2004,32(2):196~199 ) ( [15]Sohneong Ho. Jpn. J. Appl. Phys., 1994,33(9):5466~5470 ) ( [ 1 6]Wakino K, N i shikawa Y, Tamura H. J. Ce r am. Trans., 19 9 0,89(2):39~43 ) Study on Synthesis of Nano-crystallineSrTiO, by Inverse Micell Microemul-sion Method LI Yue-Feng, LAI Qiong-Yu The precursors of SrTiOs were preparedby inverse micell microemulsion method.SrTiOs nano-powders were synthesizedby calcining the precursors at 800 ℃ inair for 4 hours. The spherical SrTiO:nano-particles were of narrow distribu-tion with an average size of 40 nm. Chin. J. Inorg. Chem. 2005,21,915~91820kU X58.008 8.5Mm 8# PreparationofNano-sizedMgTiOsPowder by Electrochemistry in OrganicSolution ZHU Chuan-Gao, CHEN Yong-Hong,CHU Dao-Bao The precursor MgTi(OCHCH3)(6-))(acac),was synthesized by electrochemical dis-solution. The nano-sized MgTiOs powderwas obtained from heat treatment of theprecursor. The MgTiO, thus obtainecwas with an average particle size of 20nm in a high purity. Chin. J. Inorg. Chem. 2005,21,919~924 The SnO,2nano-particlesSWwithrutilestructure were prepared by a W/O mi-croemulsion system,composed of TritonX-100+1-hexanol/Cyclohexane/Water. Acrystallite size of 11.49 nm and an aver-age particle size of 13.3 nm calcined at600℃ were obtained. Nanocrystalline Trimanganese tetroxide(Mn;04) with XRD average crystal size of54~70 nm were synthesized at differenttemperature by solvothermal reaction.The activation energy for the nanocrys-tallite growth was calculated to be 11.36kJ·mol-. ◎ China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
确定




还剩5页未读,是否继续阅读?
天津市兰力科化学电子高技术有限公司为您提供《纳米钛酸镁中有机溶液电化学制备检测方案(电化学工作站)》,该方案主要用于其他中有机溶液电化学制备检测,参考标准--,《纳米钛酸镁中有机溶液电化学制备检测方案(电化学工作站)》用到的仪器有天津兰力科电化学工作站LK98BII
推荐专场
相关方案
更多
该厂商其他方案
更多
















