方案详情
文
高效液相色谱法(High Performance Liquid Chromatography \ HPLC)又称“高压液相色谱”、“高速液相色谱”、“高分离度液相色谱”、“近代柱色谱”等。高效液相色谱是色谱法的一个重要分支,以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,在柱内各成分被分离后,进入检测器进行检测,从而实现对试样的分析。该方法已成为化学、医学、工业、农学、商检和法检等学科领域中重要的分离分析技术应用。
方案详情

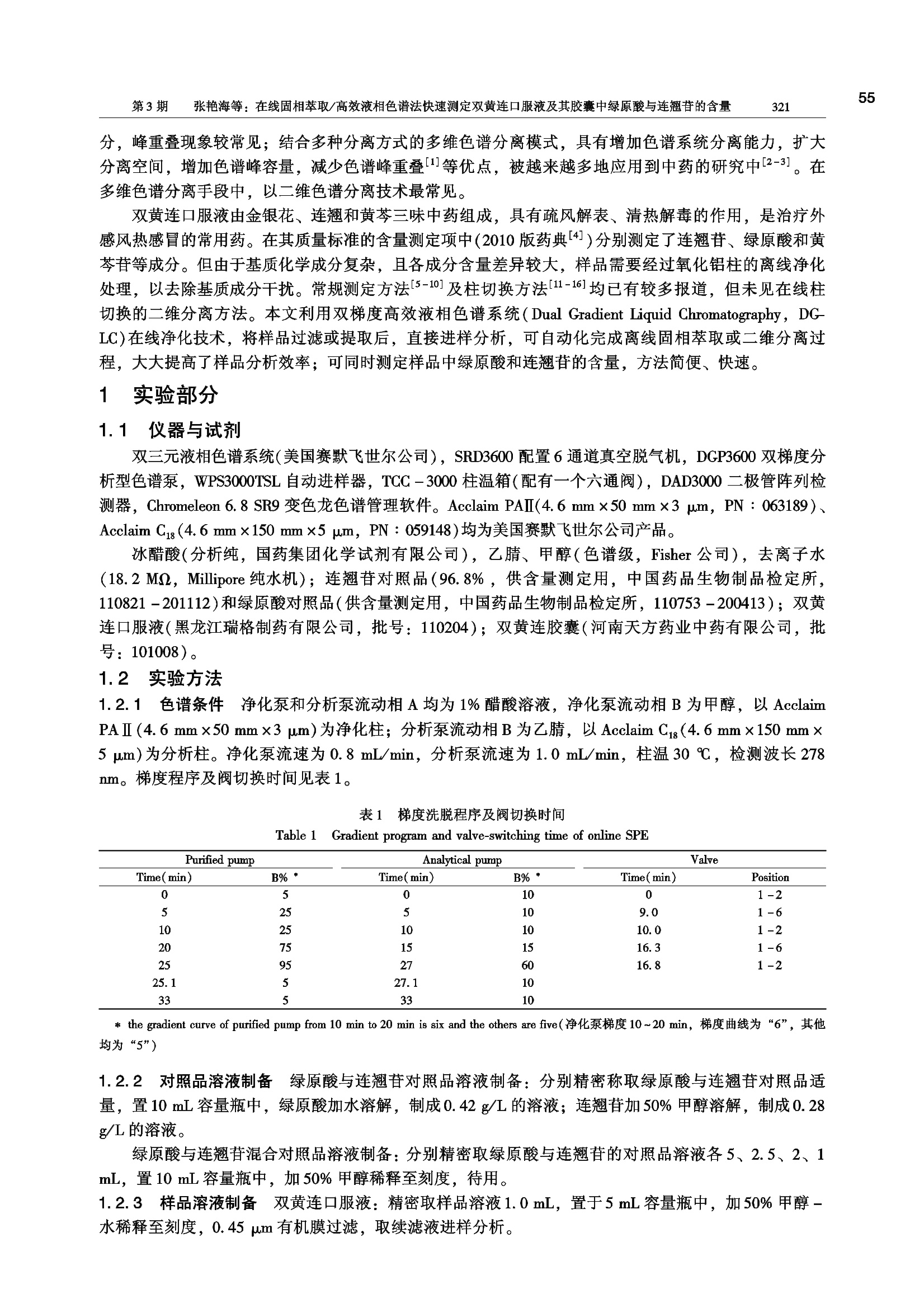
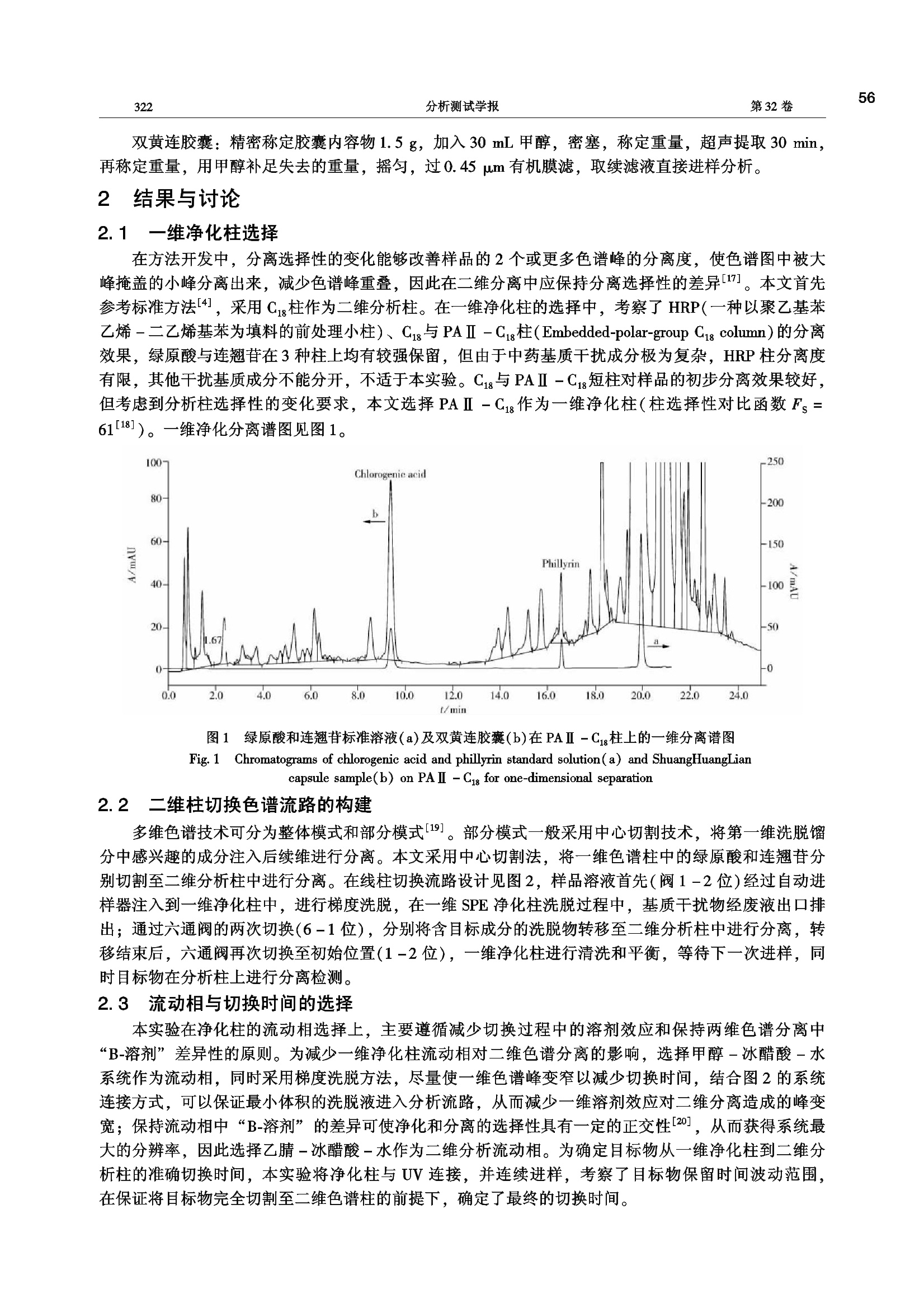
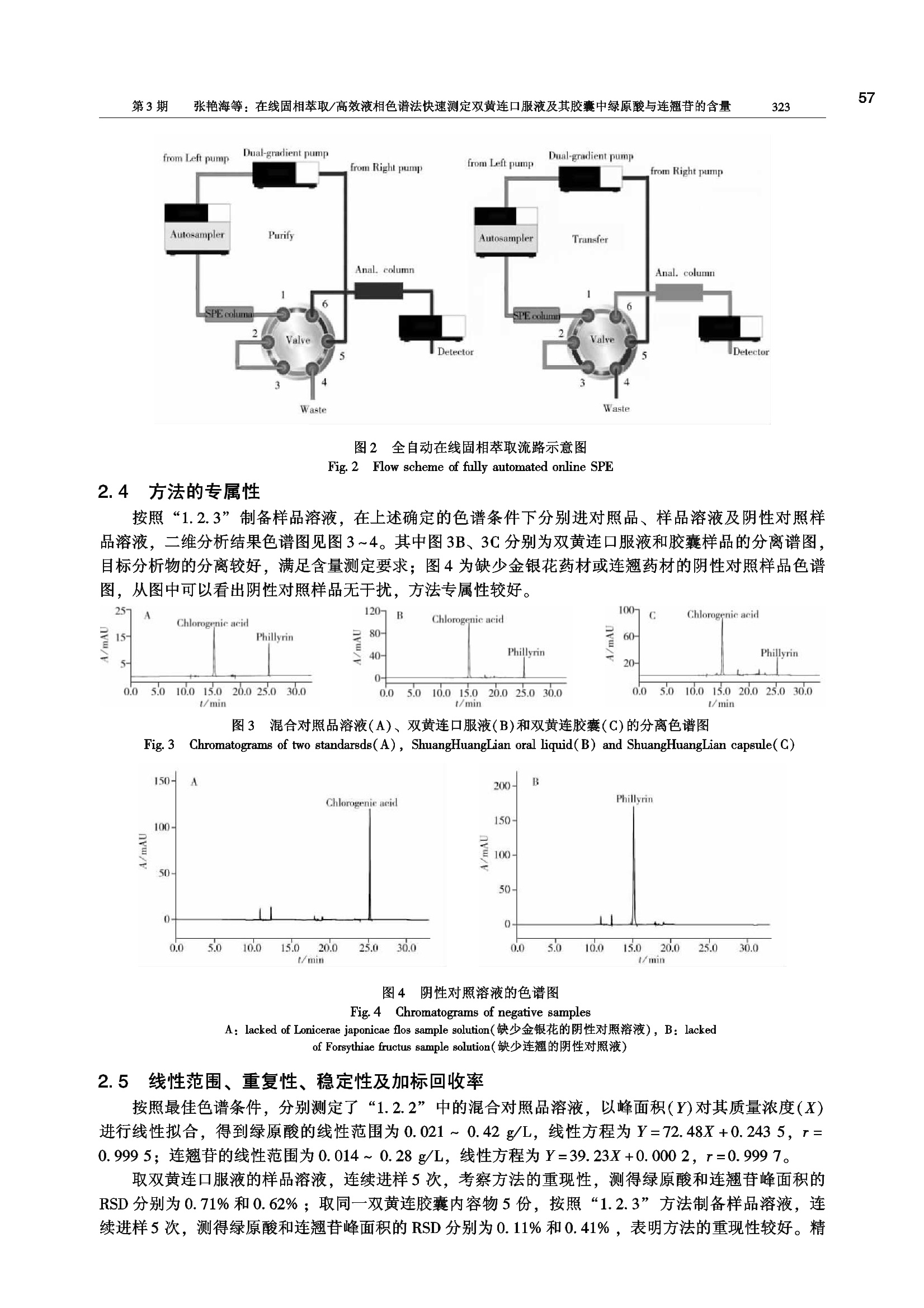
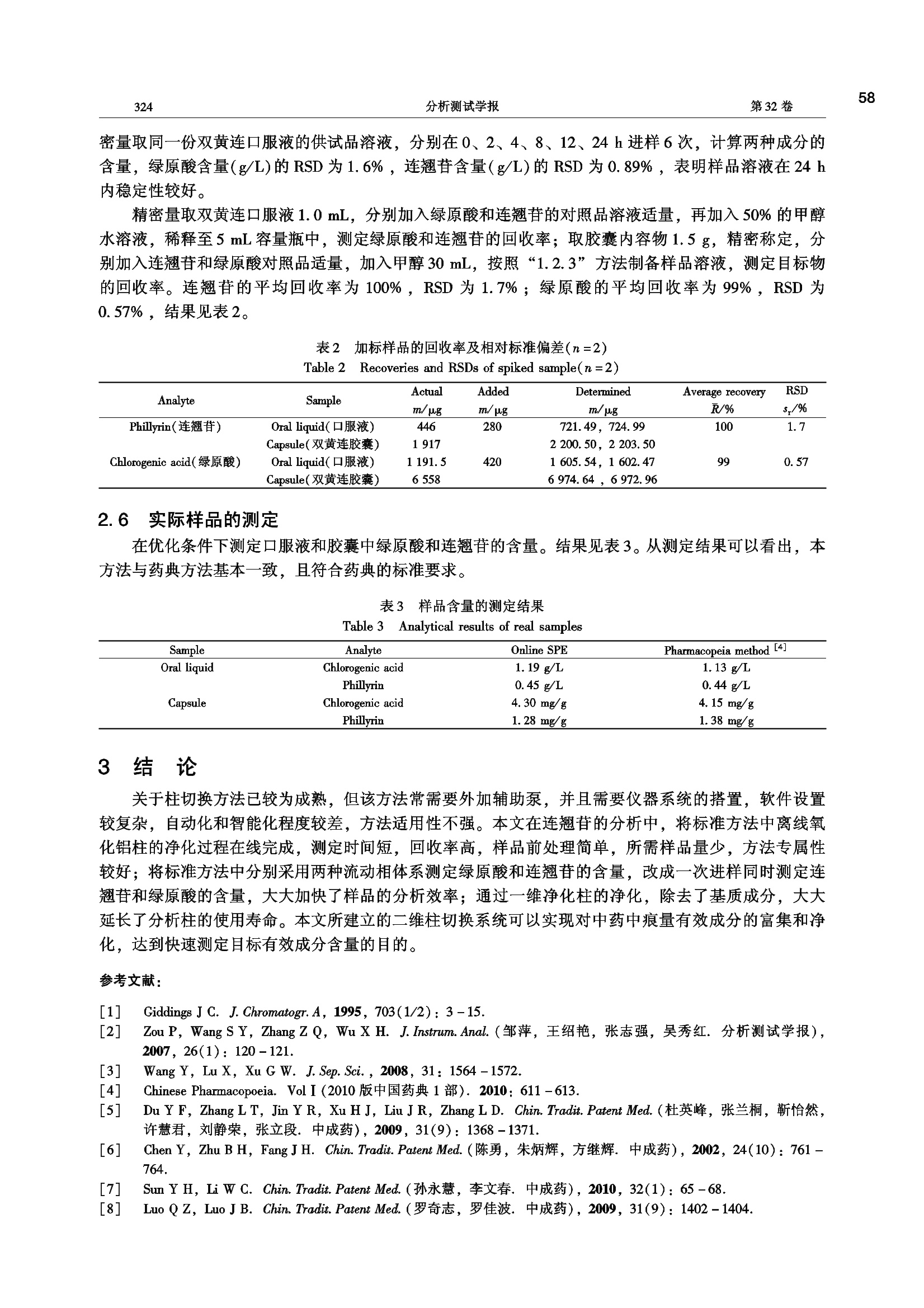
第32卷第3期2013年3月分析测试学报FENXI CESHI XUEBAO( Journa of Instrumental Analysis)Vol.32 No. 3320~32554 55第3期张艳海等:在线固相萃取/高效液相色谱法快速测定双黄连口服液及其胶囊中绿原酸与连翘的含量321 !形究简报 在线固相萃取/高效液相色谱法快速测定双黄连口服液及其胶囊中绿原酸与连翘苷的含量 张艳海1*,张大伟2,孟兆青3.4,叶明立' (1.戴安分析仪器有限公司,上海 201203;2.黑龙江省农垦总局总医院,黑龙江 哈尔滨 150088:3. 江苏康缘药业股份有限公司,江苏 连云港2222001;4.中国药科大学,江苏 南京 210009) 摘 要:建立了在线样品前处理/HPLC 测定双黄连口服液中连翘和绿原酸含量的方法。右泵为在线纯化泵, 采用 Acclaim Polar Advantage Ⅱ Cj(4.6 mm×50 mm×3 u.m)为在线一维净化柱,以甲醇-1%醋酸-水为流动相;左泵为分析泵,采用 Acclaim C (4.6 mm×150 mm×5p.m)为二维分析柱,以乙腈-1%醋酸-水为流动相,柱温30℃, 流速1.0mL/min; UV 检测波长为278 nm。绿原酸和连翘苷的相关系数分别为0.9995、0.9997,口服液中连翘苷与绿原酸的平均回收率分别为100%和99%。方法快速、简便,专属性、重现性好,测定结果与药典方法基本一致。 关键词:在线固相萃取;高效液相色谱法;双黄连口服液;绿原酸;连翘苷 中图分类号:0657.72; R282 文献标识码:A 文章编号:1004-4957(2013)03-0320-06 doi: 10.3969/j.issn. 1004-4957.2013.03.009 Simultaneous Determination of Chlorogenic Acid and Phillyrin in ShuangHuangLianOral Liquid and Capsule by HPLC with Online Solid Phase Extraction ZHANG Yan-hai*, ZHANG Da-wei, MENG Zhao-qing34, YE Ming-li' (1. Dionex Analytical Instrument Co., Ltd., Shanghai Laboratory, Shanghai 201203, China; 2. Heilongjiang AgriculturalReclamation General Hospital, Harbinn150088, China; 3. Jiangsu Kanion Pharmaceutical Co., Ltd.,Lianyungang222001, China; 4. China Pharmaceutical University, Nanjingg210009, China) Abstract: An online SPE coupled with HPLC method was developed for the determination of chloro-genic acid and phillyrin in ShuangHuangLian oral liquid and capsule. Acclaim Polar Advantage Ⅱ Cjg(4.6 mm×50 mm×3 u.m) was used as online one dimensional column with a mobile phase consistingof methanol-1% acetic acid - water by gradient elution with a right pump at a flow rate of 0.8 mL/min. The left pump was used to analyze the elute in SPE using Acclaim C18(4.6 mm×150 mm×5um) as its two-dimensional analytical column by gradient elution with acetonitrile -1% acetic acid-water as mobile phase at a flow rate of 1.0 mL/min. The UV detector was set at 278 nm. Good line-ar relationships were observed between peak areas and concentrations in the ranges of 0.021 -0.42 g/L for chlorogenic acid and 0.014-0.28 g/L for phillyrin, with correlation coefficients of 0. 999 5 and0.999 7, respectively. The average recoveries of phillyrin and chlorogenic acid in ShuangHuangLianoral liquid were 100% and 99%, respectively. This method was simple and fast, and had good spe-ciality and repeatability. Key words: online solid-phase extraction; HPLC; ShuangHuangLian oral liquid; chlorogenicacid; phillyrin 高效液相色谱技术已成为中药复杂体系研究中强有力的技术支撑,在中药质量控制方面占据着重要的地位。当前,新型色谱固定相和填料技术的不断发展为中药各类成分的分析提供了多种选择。然而很多中药复方,其复杂性超出了单一色谱分离系统的分离能力,且中药含有很多理化性质相似的成 ( 收稿日期:2012-06-28;修回日期:2012-08-19 ) ( *通讯作者:张艳海 , 硕士,研究方向:色谱分析, Tel: 021-58957001, E-mail: zhangyanh a i2012@ gmail.com ) 分,峰重叠现象较常见;结合多种分离方式的多维色谱分离模式,具有增加色谱系统分离能力,扩大分离空间,增加色谱峰容量,减少色谱峰重叠等优点,被越来越多地应用到中药的研究中[2-3]。在多维色谱分离手段中,以二维色谱分离技术最常见。 双黄连口服液由金银花、连翘和黄芩三味中药组成,具有疏风解表、清热解毒的作用,是治疗外感风热感冒的常用药。在其质量标准的含量测定项中(2010版药典4])分别测定了连翘苷、绿原酸和黄芩苷等成分。但由于基质化学成分复杂,且各成分含量差异较大,样品需要经过氧化铝柱的离线净化处理,以去除基质成分干扰。常规测定方法[5-10]及柱切换方法[11-16]均已有较多报道,但未见在线柱切换的二维分离方法。本文利用双梯度高效液相色谱系统(Dual Gradient Licuid Chromatography, DG-LC)在线净化技术,将样品过滤或提取后,直接进样分析,可自动化完成离线固相萃取或二二分离过程,大大提高了样品分析效率;可同时测定样品中绿原酸和连翘苷的含量,方法简便、快速。 实验部分 1.1 仪器与试剂 双三元液相色谱系统(美国赛默飞世尔公司), SRD3600 配置6通道真空脱气机, DGP3600双梯度分析型色谱泵, WPS3000TSL 自动进样器, TCC -3000 柱温箱(配有一个六通阀), DAD3000 二极管阵列检测器, Chromeleon 6. 8 SR9 变色龙色谱管理软件。Acclaim PAI(4.6 mm×50 mm×3 p.m, PN :063189)、Acclaim Cg (4.6 mmx150 mm x5 um, PN: 059148)均为美国赛默飞世尔公司产品。 冰醋酸(分析纯,国药集团团学试剂有限公司),乙腈、甲醇(色谱级,Fisher 公司),去离子水(18.2 MQ, Millipore纯水机);连翘苷对照品(96.8%,供含量测定用,中国药品生物制品检定所,110821-201112)和绿原酸对照品(供含量测定用,中国药品生物制品检定所,110753-200413);双黄连口服液(黑龙江瑞格制药有限公司,批号:110204);双黄连胶囊(河南天方药业中药有限公司,批号:101008)。 1.2 实验方法 1.2. 1 色谱条件 净化泵和分析泵流动相A均为1%醋酸溶液,净化泵流动相B为甲醇,以AcclaimPAⅡ(4.6 mm×50 mm×3 p.m)为净化柱;分析泵流动相B为乙腈,以 Acclaim C18(4.6 mm×150 mm×5 um)为分析柱。净化泵流速为0.8 mL/min,分析泵流速为1.0 mL/min, 柱温30℃,检测波长278nm。梯度程序及阀切换时间见表1。 表1 梯度洗脱程序及阀切换时间 Table 1 Gradient program and valve-switching time of online SPE Purified pump Analytical pump Valve Time(min) B%* Time(min) B%* Time(min) Position 0 5 0 10 0 1-2 5 25 5 10 9.0 1-6 10 25 10 10 10.0 1-2 20 75 15 15 16.3 1-6 25 95 27 60 16.8 1-2 25.1 5 27.1 10 33 5 33 10 * the gradient curve of purified pump from 10 min to 20 min is six and the others are five(净化泵梯度10~20 min,梯度曲线为“6”,其他均为“5”) 1.2.2对照品溶液制备 绿原酸与连翘苷对照品溶液制备:分别精密称取绿原酸与连翘苷对照品适量,置10 mL容量瓶中,绿原酸加水溶解,制成0.42 g/L的溶液;连翘苷加50%甲醇溶解,制成0.28g/L 的溶液。 绿原酸与连翘苷混合对照品溶液制备:分别精密取绿原酸与连翘苷的对照品溶液各5、2.5、2、1mL, 置10 mL容量瓶中,加50%甲醇稀释至刻度,待用。 1.2.3 样品溶液制备 双黄连口服液:精密取样品溶液1.0mL, 置于5mL容量瓶中,加50%甲醇-水稀释至刻度,0.45 um有机膜过滤,取续滤液进样分析。 双黄连胶囊:精密称定胶囊内容物1.5 g, 加入30 mL甲醇,密塞,称定重量,超声提取30 min,再称定重量,用甲醇补足失去的重量,摇匀,过0.45 p.m有机膜滤,取续滤液直接进样分析。 2 结果与讨论 2.1 一维净化柱选择 在方法开发中,分离选择性的变化能够改善样品的2个或更多色谱峰的分离度,使色谱图中被大峰掩盖的小峰分离出来,减少色谱峰重叠,因此在二维分离中应保持分离选择性的差异1171。本文首先参考标准方法4,采用Cg柱作为二维分析柱。在一维净化柱的选择中,考察了 HRP(一种以聚乙基苯乙烯-二乙烯基苯为填料的前处理小柱)、Cig与PAⅡ-Cg柱(Embedded-polar-group Cig column)的分离效果,绿原酸与连翘苷在3种柱上均有较强保留,但由于中药基质干扰成分极为复杂, HRP柱分离度有限,其他干扰基质成分不能分开,不适于本实验。C与PAⅡ-C短柱对样品的初步分离效果较好,但考虑到分析柱选择性的变化要求,本文选择PAⅡ-C18作为一维净化柱(柱选择性对比函数Fs=6118])。一维净化分离谱图见图1。 图1 绿原酸和连翘翘标标溶液(a)及双黄连车囊(b)在PAⅡ-C柱上的一维分离谱图 Fig. 11Chromatograms of chlorogenic acid and phillyrin standard solution(a) and ShuangHuangLiancapsule sample(b) on PA Ⅱ -Cig for one-dimensional separation 2.2 二维柱切换色谱流路的构建 多维色谱技术可分为整体模式和部分模式[191。部分模式一般采用中心切割技术,将第 -维洗脱馏分中感兴趣的成分注入后续维进行分离。本文采用中心切割法,将一维色谱柱中的绿原酸和连翘苷分别切割至二维分析柱中进行分离。在线柱切换流路设计见图2,样品溶液首先(阀1-2位)经过自动进样器注入到一维净化柱中,进行梯度洗脱,在一维 SPE 净化柱洗脱过程中,基质干扰物经废液出口排出;通过六通阀的两次切换(6-1位),分别将含目标成分的洗脱物转移至二维分析柱中进行分离,转移结束后,六通阀再次切换至初始位置(1-2位),一维净化柱进行清洗和平衡,等待下一次进样, 同时目标物在分析柱上进行分离检测。 2. 3 流动相与切换时间的选择 本实验在净化柱的流动相选择上,主要遵循减少切换过程中的溶剂效应和保持两维色谱分离中“B-溶剂”差异性的原则。为减少一维净化柱流动相对二维色谱分离的影响,选择甲醇-冰醋酸-水系统作为流动相,同时采用梯度洗脱方法,尽量使一维色谱峰变窄以减少切换时间,结合图2的系统连接方式,可以保证最小体积的洗脱液进入分析流路,从而减少一维溶剂效应对二维分离造成的峰变宽;保持流动相中“B-溶剂”的差异可使净化和分离的选择性具有一定的正交性120J,从而获得系统最大的分辨率,因此选择乙腈-冰醋酸-水作为二维分析流动相。为确定目标物从一维净化柱到二维分析柱的准确切换时间,本实验将净化柱与 UV连接,并连续进样,考察了目标物保留时间波动范围,在保证将目标物完全切割至二维色谱柱的前提下,确定了最终的切换时间。 图2 全自动在线固相萃取流路示意图 Fig.2 Flow scheme of fully automated online SPE 2.4 方法的专属性 按照“1.2.3”制备样品溶液,在上述确定的色谱条件下分别进对照品、样品溶液及阴性对照样品溶液,二维分析结果色谱普见图3~4。其中图3B、3C分别为双黄连口服液和胶囊样品的分离谱图,目标分析物的分离较好,满足含量测定要求;图4为缺少金银花药材或连翘药材的阴性对照样品色谱图,从图中可以看出阴性对照样品无干扰,方法专属性较好。 图3 混合对照品溶液(A)、双黄连口服液(B)和双黄连胶囊(C)的分离色谱图 Fig.3 Chromatograms of two standarsds(A), ShuangHuangLian oral liquid(B) and ShuangHuangLian capsule(C) 图4 阴性对照溶液的色谱图 Fig. 4 Chromatograms of negative samples A: lacked of Lonicerae japonicae flos sample solution(缺少金银花的阴性对照溶液), B: lackedof Forsythiae fructus sample solution(缺少连翘的阴性对照液) 2.5 线性范围、重复性、稳定性及加标回收率 按照最佳色谱条件,分别测定了“1.2.2”中的混合对照品溶液,以峰面积(Y)对其质量浓度(X)进行线性拟合,得到绿原酸的线性范围为0.021~0.42 g/L,线性方程为Y=72.48X+0.243 5,r=0.9995;连翘苷的线性范围为0.014~ 0.28 g/L, 线性方程为Y=39.23X+0.0002, r=0.9997。 取双黄连口服液的样品溶液,连续进样5次,考察方法的重现性,测得绿原酸和连翘苷峰面积的RSD 分别为0.71%和0.62%;取同一双黄连胶囊内容物5份,按照“1.2.3”方法制备样品溶液,连续进样5次,测得绿原酸和连翘苷峰面积的 RSD 分别为0.11%和0.41%,表明方法的重现性较好。精 密量取同一份双黄连口服液的供试品溶液,分别在0、2、4、8、12、24h进样6次,计算两种成分的含量,绿原酸含量(g/L)的 RSD 为1.6%,连翘苷含量(g/L)的 RSD 为 0.89%,表明样品溶液在24h内稳定性较好。 精密量取双黄连口服液1.0mL,分别加入绿原酸和连翘苷的对照品溶液适量,再加入50%的甲醇水溶液,稀释至5 mL容量瓶中,测定绿原酸和连翘苷的回收率;取胶囊内容物1.5g,精密称定,分别加入连翘苷和绿原酸对照品适量,加入甲醇30mL,按照“1.2.3”方法制备样品溶液,测定目标物的回收率。连翘苷的平均回收率为100%, RSD为1.7%;绿原酸的平均回收率为99%, RSD 为0.57%,结果见表2。 表2 加标样品的回收率及相对标准偏差(n=2) Table 2 Recoveries and RSDs of spiked sample(n=2) Analyte Sample Actual Added Determined Average recovery RSD m/pg m/ug m/ug R/% s./% Phillyrin(连翘苷) Oral liquid(口服液) 446 280 721.49,724.99 100 1.7 Capsule(双黄连胶囊) 1917 2200.50, 2 203.50 Chlorogenic acid(绿原酸) Oral liquid(口服液) Capsule(双黄连胶囊) 1 191.5 6 558 420 1605.54, 1 602.47 6974.64,6972.96 99 0.57 2.6实际样品的测定 在优化条件下测定口服液和胶囊中绿原酸和连翘苷的含量。结果见表3。从测定结果可以看出,本方法与药典方法基本一致,且符合药典的标准要求。 表3桂样品含量的测定结果 Table 3 Analytical results of real samples Sample Analyte Online SPE Pharmacopeia method 14] Oral liquid Chlorogenic acid 1. 19 g/L 1. 13 g/L Phillyrin 0.45 g/L 0.44 g/L Capsule Chlorogenic acid 4.30 mg/g 4. 15 mg/g Phillyrin 1.28 mg g 1.38 mg/g 3 结 论 关于柱切换方法已较为成熟,但该方法常需要外加辅助泵,并且需要仪器系统的搭置,软件设置较复杂,自动化和智能化程度较差,方法适用性不强。本文在连翘苷的分析中,将标准方法中离线氧化铝柱的净化过程在线完成,测定时间短,回收率高,样品前处理简单,所需样品量少,方法专属性较好;将标准方法中分别采用两种流动相体系测定绿原酸和连翘苷的含量,改成一次进样同时测定连翘苷和绿原酸的含量,大大加快了样品的分析效率;通过一维净化柱的净化,除去了基质成分,大大延长了分析柱的使用寿命。本文所建立的二维柱切换系统可以实现对中药中痕量有效成分的富集和净化,达到快速测定目标有效成分含量的目的。 ( 参考文献: ) ( Giddings J C . J . Chromatogr.A, 1995,703(1/2):3 - 15. ) ( Zou P , Wang S Y, ZhangZ Q, Wu X H. J. Instrum. Anal.(邹萍,王绍艳,张志强,吴秀红.分析测试学报), 2007,26(1):120-121. ) 3WangY, Lu X, Xu G W. J. Sep. Sci., 2008, 31: 1564-1572.45 ( Chinese Pharmacopoeia. Vol I (2010版中国药典1部).2010:611-613. ) ( Du Y F, Zhang LT, Jin YR, Xu HJ, L iuJR, Zhang L D. C hin. Tradit. Patent Med.(杜英 峰 ,张兰桐,靳怡然, 许慧君,刘静荣,张立段. 中成药),2009,31(9):1368-1371. ) ( [6] Chen Y, Zhu B H , Fang J H. Chin. Tradit. Patent Med.(陈勇,朱辉,方继辉. 中 成药),2002,24(10):761- 764. ) ( Sun Y H, Li WC. Chin. Tradit. Patent Med.(孙永慧,李文春. . 中成药),2010,32(1):65-68. ) ( Luo QZ, L uo J B. Chin. Tradit. Patent Med.(罗奇志,罗佳波.中成药),2009,31(9):1402-1404. ) ( 第3期 张艳海等:在线固相萃取/高效液相色谱法快速测定双黄连口服液及其胶囊中绿原酸与连翘苷的含量 ) ( [9] Zhou W, Di L Q, Bi X L, Zhao X L. China Journal of TCM and Pharmacy(周伟,狄留庆, 毕 肖林,赵晓莉.中华 中医药杂志),2011,26(9):2111-2113. ) ( 10 Wang X H, An R, Zou Y, Zhang Y, Wang Z H, Hong X K. Acta Pharm. Sin. (王新宏 , 安睿,邹云,张艺,王 智 华,洪筱坤.药学学报),2001,36(12):917-920. ) ( [11] Zhao K X, Ge B K, Chen X Y, Xu H. Chin. J. Anal. Chem.(赵孔祥,葛宝坤,陈旭艳, 许 泓.分析化学),2011, 39(9):1341-1346. ) ( [12] Lu Q, Shao Q , Qu H B , Cheng Y Y. China J. Chin. Mater. Med. ( 陆倩,邵青,瞿海斌,程翼宇.中国中药杂志), 2008, 3 3(23):2776-2780. ) ( 13 Zhao XF, Zhu Z M, Liu A F, Wang Z, Zheng X H. Chin. Tradit. Patent Me d .(赵新锋,祝忠民,刘爱芳,汪珍,郑晓晖.中成药),2004,26(6):490-492. ) ( 14 ] Huang W H, Y a ng J, Zhao J, Wang C Z, Y u an C S, LiS P. J. Pharm. Biomed. Anal.,2 0 10,(5 3 ):906- 9 10. ) ( 15 ] Xie R, Wen J , Wei H, Fan G R, Zhang D B. J . Pharm. Biomed. Ana l ., 2010 , (52): 114-121. ) ( 16 Peng L H, Lu H M , Guo F Q, Cai P P, Liang Y Z. J. Instrum. Anal. (彭丽华,卢红梅, 郭 方遒,蔡品品,梁逸曾.分析测试学报),2012,31(1):109-112. ) ( [17] Dolan J W, Snyder L R . J. Chromatogr. A , 200 9 , 1216:3467-3472. ) ( 18 Snyder L R, Dolan J W, Carr P W. J . Chromatogr. A , 2004 , 1060: 7 7-11 6 . ) ( 19 Wang Z C, Zhang Q H, Zhao Z Y, Zhang W B, LiT. Chin. J. Anal. Chem. (王智聪,张庆合,赵中一,张维冰, 李彤.分析化学),2005,5:722. ) ( 20 Pellet t J , Lukulay P, Mao Y, Bowen W, Reed R , M a M, Munger R C , D ol a n J W, Wris l ey L, Medw i d K, Toltl N P, Chan C C , S kibic M, Biswas K, Wells K A, S n yder L R. J. Chromatogr. A, 2006, ( 1101):122-135. ) 欢迎订阅 欢迎投稿 欢迎刊登广告《分析测试学报》 国内刊号: CN 44-1318/TH国际标准刊号: ISSN 1004-4957国际刊名化代码 CODEN: FCEXES邮发代号:46-104国外代号: BM 6013广告经营许可证:440000100186 《分析测试学报》是由中国广州分析测试中心、中国分析测试协会共同主办的全国性学术刊物,中文核心期刊。刊登质谱学、光谱学、色谱学、波谱学、电化学、电子显微学等方面的分析测试新理论、新方法、新技术的研究成果,介绍新仪器装置及在生物、医药、化学化工、商检、食品检验等方面实用性强的实验技术。适合科研院所、高等院校、检测机构、医药、卫生以及厂矿企业分析测试工作和管理人员阅读。 经过多年的发展,本刊已成为国内知名的化学类核心期刊。2011年,影响因子在全国化学类刊物排名中位列第5名,被引频次每年递增约30%,稿源丰富,基金论文比超过70%。近几年,本刊刊发的论文被 CA(美国化学文摘)收录率达94%,2006年引文频次在 CA 千种表中国部分中列第38名,并被国际上其它知名的数据库如日本科技文献速报、俄罗斯文摘、英国分析文摘(AA)、《质谱公报》等收录。在《中文核心期刊要目总览》2011年版的化学类期刊列第9位;入选2012年度“中国国际影响力优秀学术期刊”;进入由全国8000种期刊遴选出的500种科技期刊组成的“中国科技期刊精品数据库”;中国学术期刊综合评价数据库(CAJCED)统计刊源;中国科技论文统计源期刊(中国科技核心期刊);《中国科学引文数据库》来源期刊;中国期刊全文数据库(CJFD)收录期刊;《中国核心期刊(遴选)数据库》收录;《中国学术期刊(光盘版)》全文收录期刊;《中国期刊网》全文收录期刊;《中国学术期刊文摘(中、英文版)》收录为源期刊等。 本刊为月刊,国内外公开发行。大16开,单价:12.00元/册, 全年144元。请在全国各地邮局订阅。未在邮局订到者可直接向本编辑部补订。补订办法:请从邮局汇款至广州市先烈中路100号《分析测试学报》编辑部,邮编:510070,写明订户单位、详细地址、收刊人姓名、邮编及补订份数(全年或某期),电话:(020)87684776 或 37656606, http: //www. fxcsxb. com(可在线投稿), E-mail: fxcsxb@china. com。 此外高效液相色谱还有色谱柱可反复使用、样品不被破坏、易回收等优点,但也有缺点,与气相色谱相比各有所长,相互补充。高效液相色谱的缺点是有“柱外效应”。在从进样到检测器之间,除了柱子以外的任何死空间(进样器、柱接头、连接管和检测池等)中,如果流动相的流型有变化,被分离物质的任何扩散和滞留都会显著地导致色谱峰的加宽,柱效率降低。高效液相色谱检测器的灵敏度不及气相色谱。
确定


还剩4页未读,是否继续阅读?
赛默飞色谱与质谱为您提供《双黄连口服液及其胶囊中绿原酸与连翘苷的含量检测方案(液相色谱仪)》,该方案主要用于中药制剂中含量测定检测,参考标准--,《双黄连口服液及其胶囊中绿原酸与连翘苷的含量检测方案(液相色谱仪)》用到的仪器有赛默飞 Vanquish™ UHPLC超高效液相色谱系统、赛默飞UltiMate3000制备液相色谱
推荐专场
相关方案
更多
该厂商其他方案
更多

















