目的建立测定生物制品保护剂中蔗糖和乳糖含量的高效液相色谱(HPLC)法。方法样品用磺基水杨酸沉淀、离心除去蛋白质,上清液采用氨基柱分离,示差折光检测器进行监测,依外标法建立校正曲线,并对建立的方法进行验证。采用建立的方法测定4种疫苗成品中蔗糖和乳糖的含量。结果蔗糖和乳糖的标准曲线的相关系数r2均达0.999 9以上。该方法能将两种糖完全分离;测定两种糖的特异性较好;该法检测4个浓度的蔗糖和乳糖的平均回收率分别为97.9%和100.5%,变异系数分别为1.28%和0.48%;最低检测限及定量限分别为0.01 mg/ml和0.1 mg/ml;采用该法测定的4种疫苗成品中蔗糖和乳糖的变异系数分别为2.59%和1.44%。结论已建立了测定生物制品保护剂中蔗糖和乳糖含量的HPLC法,该方法定量准确,重复性好,可作为生物制品保护剂中蔗糖和乳糖含量的常规检测方法。
方案详情

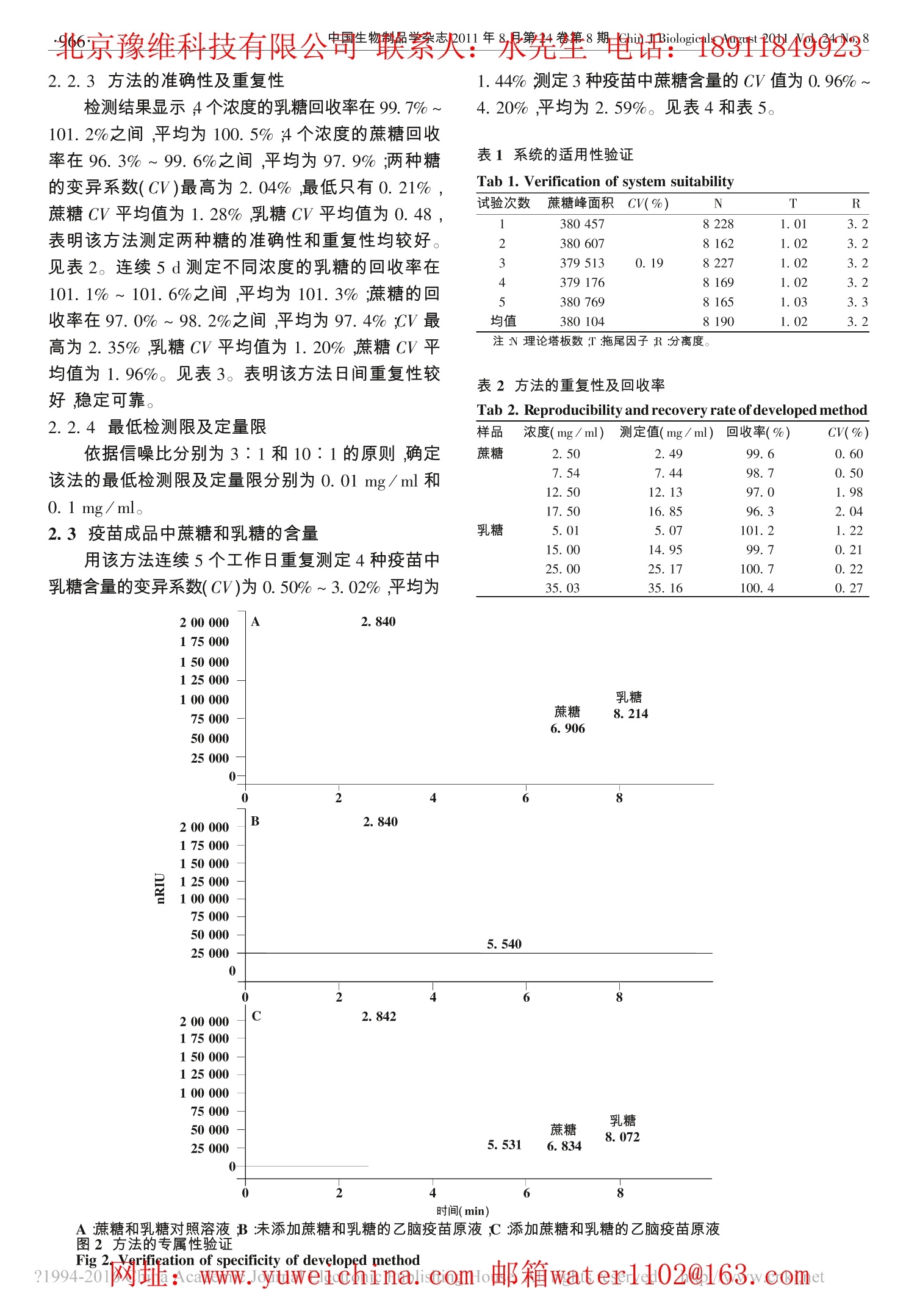
DOI: 10.13200/j.cjb.2011.08.97.luolh.009京豫维科技有限公司生物志P2011年第上8期Tialo189118499238【实验技术】 北京豫维科维有限公司联系est20水.20水先生电话:18911849923 高效液相色谱法测定生物制品保护剂中蔗糖和乳糖的含量 雒丽红 高雪军 魏然 朱莉萍 程瑞霞 郑学刚 【摘要】 目的 建立测定生物制品保护剂中蔗糖和乳糖含量的高效液相色谱(HPLC)法。方法样品用磺基水杨酸沉淀、离心除去蛋白质,上清液采用氨基柱分离,示差折光检测器进行监测,依外标法建立校正曲线,并对建立的方法进行验证。采用建立的方法测定4种疫苗成品中蔗糖和乳糖的含量。结果 蔗糖和乳糖的标准曲线的相关系数r均达0.9999以上。该方法能将两种糖完全分离;测定两种糖的特异性较好;该法检测4个浓度的蔗糖和乳糖的平均回收率分别为97.9%和100.5%,变异系数分别为1.28%和0.48%;最低检测限及定量限分别为 0.01 mg/ml 和0.1 mg/ml;采用该法测定的4种疫苗成品中蔗糖和乳糖的变异系数分别为2.59%和1.44%。结论已建立了测定生物制品保护剂中蔗糖和乳糖含量的 HPLC 法,该方法定量准确,重复性好,可作为生物制品保护剂中蔗糖和乳糖含量的常规检测方法。 【关键词】 色谱法,高压液相;生物制品;保护剂;蔗糖;乳糖;外标法 【中国图书分类号】0657.7 R392-33【文献标识码】A 【文章编号】1004-5503 (2011) 08-0964-04 Determination of Sucrose and Lactose Contents in Stabilizers of Biologics byHPLC LUO Li-hong, GAO Xue-jun, WEI Ran, ZHU Li-ping, CHENG Rui-xia, ZHENG Xue-gang (Lanzhou InstituteofBiological Products, Lanzhou 730046, China 【Abstract】 ObjectiveTo develop a HPLC method for determination of sucrose and lactose contents in stabilizers of biologics.Methods Test samples were precipitated with sulfosalicylic acid and centrifuged to remove the protein, and the supernatant wasseparated by amino column chromatography and monitored by refractive index detector (RID) , based on which a correction curve wasplotted by external standard method, and the developed method was verified. The sucrose and lactose contents in the final products offour kinds of vaccines were determined by the developed method. Results Both the correlation coefficients r of standard curves ofsucrose and lactose were more than 0. 999 9. Sucrose and lactose were separated completely by the developed method. The methodshowed high specificity for determination of sucrose and lactose. The mean recovery rates of sucrose and lactose, each at four con-centrations, were 97. 9% and 100. 5%, while the variation coefficients were 1. 28% and 0.48%, respectively. The minimum andquantitative detection limits of the developed method were 0. 01 and 0. 1 mg /ml respectively. The variation coefficients of detectionresults of sucrose and lactose contents in final products of four kinds of vaccines by the developed method were 2. 59% and 1. 44%respectively. ConclusionA HPLC method for determination of sucrose and lactose contents in stabilizers of biologics was devel- oped, which was accurate and showed high reproducibility, and might be used as a routine determination method. 【Key words】 Chromatography, high performance liquid; Biologics; Stabilizer; Sucrose; Lactose; External standard method 生物制品中常用的保护剂有羟基化合物、糖、氨基酸和聚合物等,其中,糖的保护作用随着其浓度的升高而增强,当达到某一浓度时,保护作用达最大值,此后,浓度再增大,保护作用也不再显著增强。同时,糖还具有赋形剂和抗氧化剂的作用,其含量直接与疫苗滴度及稳定性相关〔2]。因此,糖含量的监测在生物制品的质量控制中具有重要意义。本实验对兰州生物制品研究所生产的4种生物制品,应用磺基水杨酸沉淀离心去除蛋白质,再采用氨基柱分离,示差折光检测器测定,能够很好地分离蔗糖和乳糖并准确定量,现报道如下。 ( 基金项目:国家科技支撑计划 (2008BAI54B05-04). ) ( 作者单位:兰州生物制品研究所质量检定室(兰州730046). ) ( 通讯作者:丽红,E-m a il:lz_luo l ihong@163.com ) 。材料与方法 1.1疫苗 乙型脑炎减毒活疫苗原液(批号:H-20091105)、乙型脑炎减毒活疫苗(批号:J20091004 J20091204)、麻疹减毒活疫苗(批号:M201005054、M201005055)、冻干人用狂犬病疫苗(批号:R20090901、R20091101)及口服轮状病毒活疫苗(批号:0201005066 0201005067均由本所提供。 1.2主要试剂及仪器 磺基水杨酸(批号:T20100112) 购自国药集团化学试剂公司;乙腈(批号:I508130943) 购自 MERCK公司;蔗糖(批号:097k8619) 和乳糖(批号:BCBB0783)购白Sisma公司;液相色谱仪、自动进样器、示差折 光检测器及工作软件均为美国Agilent 公司1200系列产品;色谱柱(型号:Kromasil KR100-5NH2,规格:25 mmx 4.6 mm) 购自瑞典 Eka Chemicals 公司。 1.3蔗糖和乳糖对照品溶液的配制 准确称取干燥恒重〔3]的蔗糖和乳糖对照品,分别配制成浓度为 40、80 mg/ml的储备液,再分别稀释至1、5、10、15、20 mg/ml 和1、10、20、30、40 mg/ml,即为对照品溶液。 1.4供试品的处理 成品疫苗每批各取3支,每支加水1ml 溶解后,3支合并摇匀,取1ml加1.5%磺基水杨酸1 ml,混匀,室温至少放置2 h,3 000 r/ min 离心10 min,取上清,经0.45 um膜过滤,备用。 1.5 HPLC方法的建立 色谱条件:流动相为乙腈:水(v/v)=75:25;流速:1.2ml/min;上样量:10 pl;柱温:30℃。以流动相平衡系统至基线平稳后,将对照品和供试品上样,收集色谱图,绘制标准曲线。 1.6方法的验证 1.6.1适用性验证:按1.5项色谱条件平衡系统,分别取浓度为20 mg/ml的蔗糖和乳糖对照品溶液各1ml混匀,经0.45 p.m 膜过滤,待基线平稳后连续上样5次,收集色谱图,以蔗糖峰为主,记录其峰面积,计算重复性和理论塔板数以及拖尾因子,并记录蔗糖与乳糖的分离度4]。 1.6.2专属性验证:先上样确定蔗糖和乳糖的保留时间,再分别测定添加和未添加蔗糖和乳糖的乙脑疫苗原液中糖的保留时间,验证色谱峰的专属性。 1.6.33准确性及重复性验证:在乙型脑炎减毒活疫苗原液中分别加入蔗糖和乳糖,使其浓度分别为2.50、7.54、12.50、17.50 mg/ml 和5.01、15.00、25.00、35.03 mg/ml,分别取2 ml加入1.5%磺基水杨酸2ml,室温放置 2 h,3 000 r/ min 离心10 min,取上清,经0.45 pum 膜过滤后,连续上样测定,计算回收率和变异系数。将上述不同浓度的蔗糖和乳糖分别加入乙型脑炎减毒活疫苗原液中,按上述方法连续测定5d,计算回收率及变异系数。 1.6.4最低检测限和定量限的测定:在乙型脑炎减毒活疫苗原液中加入不同浓度的蔗糖和乳糖(1、0.1、0.01、0.001、0.0001mg/ml),并对其进行测定,确定最低检测限和定量限。 1.7疫苗成品中蔗糖和乳糖含量的测定 按照1.4项处理供试品,在连续5个工作日分别重复测定麻疹减毒活疫苗、乙型脑炎减毒活疫苗、冻干人用狂犬病疫苗和口服轮状病毒活疫苗中的乳 糖含量及乙型脑炎减毒活疫苗、冻干人用狂犬病疫苗和口服轮状病毒活疫苗中的蔗糖含量。 2. 结果 2.1标准曲线 蔗糖和乳糖的标准曲线见图1,二者的r分别为0.999 96和0.99999,表明该法线性较好。 图1蔗糖(A)和乳糖(B)的标准曲线 Fig 1. Standard curves for sucrose (A) and lactose (B) 2.22方法的验证 2.2.1系统的适用性 检测结果显示,5次峰面积测定值的变异系数为0.19%,表明系统稳定性极佳;理论塔板数(N)均高于5000,符合通常所要求的不低于5000的规定;拖尾因子(T)在0.95~1.05的范围之内;分离度(R)大于1.5,表明该方法能够将两种糖完全分离。见表1。 2.2.2方法的专属性 检测结果显示,浓度为 10mg/ml 的蔗糖和20mg/ml的乳糖混合溶液直接进样后,蔗糖和乳糖的保留时间(tn)分别为6.906和8.214;而不含蔗糖和乳糖的乙型脑炎减毒活疫苗原液加入1.5%磺基水杨酸沉淀蛋白后,在上述保留时间前后没有吸收峰;在乙脑疫苗原液中加入蔗糖和乳糖后再进行测定,在 te分别为6.834和8.072处出现吸收峰,与蔗糖乳糖直接测定的 t& 相差少于±0.2,表明该法测定两种糖的特异性较好。见图2。 2.2.3方法的准确性及重复性 检测结果显示,4个浓度的乳糖回收率在99.7%~101.2%之间,平均为100.5%;4个浓度的蔗糖回收率在96.3%~99.6%之间,平均为97.9%;两种糖的变异系数(CV) 最高为2.04%,最低只有0.21%,蔗糖 CV 平均值为1.28%,乳糖 CV 平均值为0.48,表明该方法测定两种糖的准确性和重复性均较好。见表2。连续5d测定不同浓度的乳糖的回收率在101.1%~101.6%之间,平均为101.3%;蔗糖的回收率在97.0%~98.2%之间,平均为 97.4%;CV 最高为2.35%,乳糖 CV 平均值为1.20%,蔗糖 CV平均值为1.96%。见表3。表明该方法日间重复性较好,稳定可靠。 2.2.4最低检测限及定量限 依据信噪比分别为3:1和10:1的原则,确定该法的最低检测限及定量限分别为0.01 mg/ml 和0. 1 mg/ml。 2.3疫苗成品中蔗糖和乳糖的含量 用该方法连续5个工作日重复测定4种疫苗中乳糖含量的变异系数 (CV) 为0.50%~3.02%,平均为 1.44%;测定3种疫苗中蔗糖含量的 CV 值为0.96%~4.20%,平均为2.59%。见表4和表5. 表1¥系统的适用性验证 Tab 1. Verification of system suitability 试验次数 蔗糖峰面积CV(%) N T R 1 380457 8228 1.01 3.2 2 380607 8162 1.02 3.2 3 379 513 0.19 8227 1.02 3.2 4 379176 8169 1.02 3.2 5 380769 8165 1.03 3.3 均值 380104 8190 1.02 3.2 注:N:理论塔板数;T:拖尾因子;R:分离度。 表2方法的重复性及回收率 Tab 2. Reproducibility and recovery rate of developed method 样品 浓度(mg/ml) 测定值(mg/ml) 回收率(%) CV (%) 蔗糖 2.50 2.49 99.6 0.60 7.54 7.44 98.7 0.50 12.50 12.13 97.0 1.98 17.50 16.85 96.3 2.04 乳糖 5.01 5.07 101.2 1.22 15.00 14.95 99.7 0.21 25.00 25.17 100.7 0.22 35.03 35.16 100.4 0.27 A:蔗糖和乳糖对照溶液;B:未添加蔗糖和乳糖的乙脑疫苗原液;C:添加蔗糖和乳糖的乙脑疫苗原液 图2方法的专属性验证 Fig 2erification of specificity of developed method ?1994-201:caWww.JouweichinanlailsciocmoImoio邮箱water1102@163wcomet 表3方法的日间重复性及回收率 Tab 3. Reproducibility on various days and recovery rate of developed method 样品 浓度(mg/ml) 第1天 第2天 第3天 第4天 第5天 回收率(%) CV (%) 蔗糖 2.50 2.51 2.37 2.42 2.48 2.49 97.2 2.35 7.54 7.42 7.26 7.43 7.29 7.23 97.2 1.27 12.50 12.24 12.10 12.48 12.00 11.80 97.0 2.11 17.50 17.43 17.38 17.50 17.03 16.63 98.2 2.11 乳糖 5.01 5.07 5.20 5.10 5.02 5.04 101.6 1.39 15.00 14.96 15.37 14.98 15.27 15.50 101.5 1.57 25.00 25.15 25.42 25.16 25.20 25.47 101.1 0.60 35.03 35.30 35.43 35.19 35.05 36.15 101.1 1.21 Tab 4. Lactose contents in final products of four kinds ofvaccines 疫苗 第1天第2天第3天第4天第5天 S CV(%) M201005054 53.34 54.97 55.03 56.16 54.82 1.01 1.83 M201005055 56.68 56.44 56.39 56.96 56.99 0.280.50 J20091004 48.26 49.30 49.20 45.80 48.96 1.463.02 J20091204 49.14 49.69 4 48.91 48.86 49.39 0.350.70 R20090901 45.54 45.3244.52 45.26 44.81 0.410.92 R20091101 44.14 44.0042.74 43.98 44.38 0.64 1.46 0201005066 12.59 11.84 11.83 12.07 12.16 0.922.54 0201005067 10.60 10.66 10.72 10.75 10.68 0.170.53 表53种成品疫苗中的蔗糖含量 Tab 5. Sucrose contents in final products of three kinds ofvaccines 疫苗 第1天 第2天第3天第4天第5天 CV(%) J20091004 19.13 19.38 20.11 19.71 18.96 0.46 2.37 J20091204 20.54 18.93 19.23 19.38 20.00 0.65 3.30 R20090901 21.96 22.2221.17 22.41 23.75 0.94 4.20 R20091101 22.28 23.12 22.49 22.88 24.34 0.81 3.50 0201005066 21.84 21.44 21.49 21.14 21.33 0.77 1.20 0201005067 19.39 19.45 19.55 19.08 19.23 0.56 10.96 3. 讨论 目前,国内外对糖类的测定方法报道较多,但多集中于食品及农副产品[5-7],而对生物制品保护剂中糖类测定的报道相对较少,随着生物制剂生产与质量控制的不断发展与完善,对保护剂中糖类含量的监测也将成为必然。本实验旨在建立一种生物制剂中通用的糖类保护剂含量的测定方法,实验结果显示,在对乙脑疫苗原液和4种疫苗成品的测定中,两种糖类能够与样品中的杂质峰和溶剂峰完全分离,后者未对目标物的测定产生影响。对4种生物制剂的测定中,以5 pl 进样量进行试验,标准曲线的相关系数(r)也能达到0.999 9,表明该方法对试验条件的改具有一定的耐受性。 HPLC 法由于操作步骤简便,易于掌握,从而降低了人为因素造成的系统误差;也无需考虑化学反应的条件控制等因素,大大降低了环境因素导致的系统误差;另外,免除了传统化学方法中用的一些有毒物质,如苦味酸(即2,4,6-三硝基苯酚,俗称黄色炸药)、苯酚、浓硫酸等对人体的危害〔8-9],加强了实验人员的安全性保障。 综上所述,HPLC法测定保护剂中两种糖类含量,具有无需配制多种试剂、样品处理简便、检测速度快、不易受环境因素干扰等特点,且该方法重复性好、定量准确、稳定可靠,适用于生物制品保护剂中乳糖和蔗糖的常规定量检测。 ( 参考文献 ) ( [1]赵铠,章以浩,李河民.医学生物制品学[M].2版.北京:人民卫 生出版社,2007:450-451. ) ( [2]王玉琳,曾鸣,王玲,等.病毒活疫苗冻干保护剂筛选研究 [J] 微生物学免疫学进展,1996,24 (1):22-27. ) ( [3]中国国家标准化管理委员会.食品中果糖、葡萄糖、蔗糖、麦芽 糖、乳糖的测定[S].GB/T 22221-2008. ) ( [4]国家药典委员会.中华人民共和国药典(三部) [S]. 北京:中国医药科技出版社,2010:附录16-18. ) ( [5]罗进,夏敏,叶能胜,等. HPLC-ELSD 同时测定食品中5种糖含 量 [ J ].食品科学,2010,31(8 ) :226-229. ) ( [6]邢亚东.高效液相色谱技术在食品卫生领域的应用[].现代医 药卫生,2005,21(5):550-551. ) ( [7] . J Joung HK, Won JC. Si m ultaneous qu a ntitative d e termination o f mono-, d i -, t r i-, t etra-, and p enta-saccharides in yogurt products by a simple H PLC sy s tem wi t h a r e f ractive i n dex d e tector []. Bu l lKorean Chem Soc, 2001, 22(1): 1 23-126. ) ( [8]樊宏,陈强.乳制品中乳糖直接比色测定方法探讨[J].中国卫 生检验杂志,2006,16 (3):2 9 6-297. ) ( [9] Grandy AS , E r ich M S , Po r ter GA . Suitability o f the anthorne-sul-furic acid reagent for det e rmining water soluble carbohydrates insoil water extract s [J]. So i l Biolo g y Biochem, 2000, 32 (5) : 725-727. ) ( 收稿 日期:2010-12-26) ) ?址:caWww.ivuweichinalicomio邮箱waterlcomet 目的建立测定生物制品保护剂中蔗糖和乳糖含量的高效液相色谱(HPLC)法。方法样品用磺基水杨酸沉淀、离心除去蛋白质,上清液采用氨基柱分离,示差折光检测器进行监测,依外标法建立校正曲线,并对建立的方法进行验证。采用建立的方法测定4种疫苗成品中蔗糖和乳糖的含量。结果蔗糖和乳糖的标准曲线的相关系数r2均达0.999 9以上。该方法能将两种糖完全分离;测定两种糖的特异性较好;该法检测4个浓度的蔗糖和乳糖的平均回收率分别为97.9%和100.5%,变异系数分别为1.28%和0.48%;最低检测限及定量限分别为0.01 mg/ml和0.1 mg/ml;采用该法测定的4种疫苗成品中蔗糖和乳糖的变异系数分别为2.59%和1.44%。结论已建立了测定生物制品保护剂中蔗糖和乳糖含量的HPLC法,该方法定量准确,重复性好,可作为生物制品保护剂中蔗糖和乳糖含量的常规检测方法。
确定


还剩2页未读,是否继续阅读?
北京豫维科技有限公司为您提供《生物制品保护剂中蔗糖和乳糖的含量检测方案(液相色谱柱)》,该方案主要用于其他中蔗糖和乳糖的含量检测,参考标准--,《生物制品保护剂中蔗糖和乳糖的含量检测方案(液相色谱柱)》用到的仪器有SilcoCan 空气采样罐(硅烷化苏玛罐)27409
推荐专场
相关方案
更多
















