
方案详情
文
本文通过瑞士万通离子色谱建立用离子色谱法同时分离测定三种麻黄碱类药物的方法.该方法的线性相关系数分别为0. 9996 ,0. 9999 ,0. 9999. 去甲麻黄碱的检出限为0. 04μgPml. 麻黄碱及伪麻黄碱的检出限均为0. 08μgPml.
方案详情

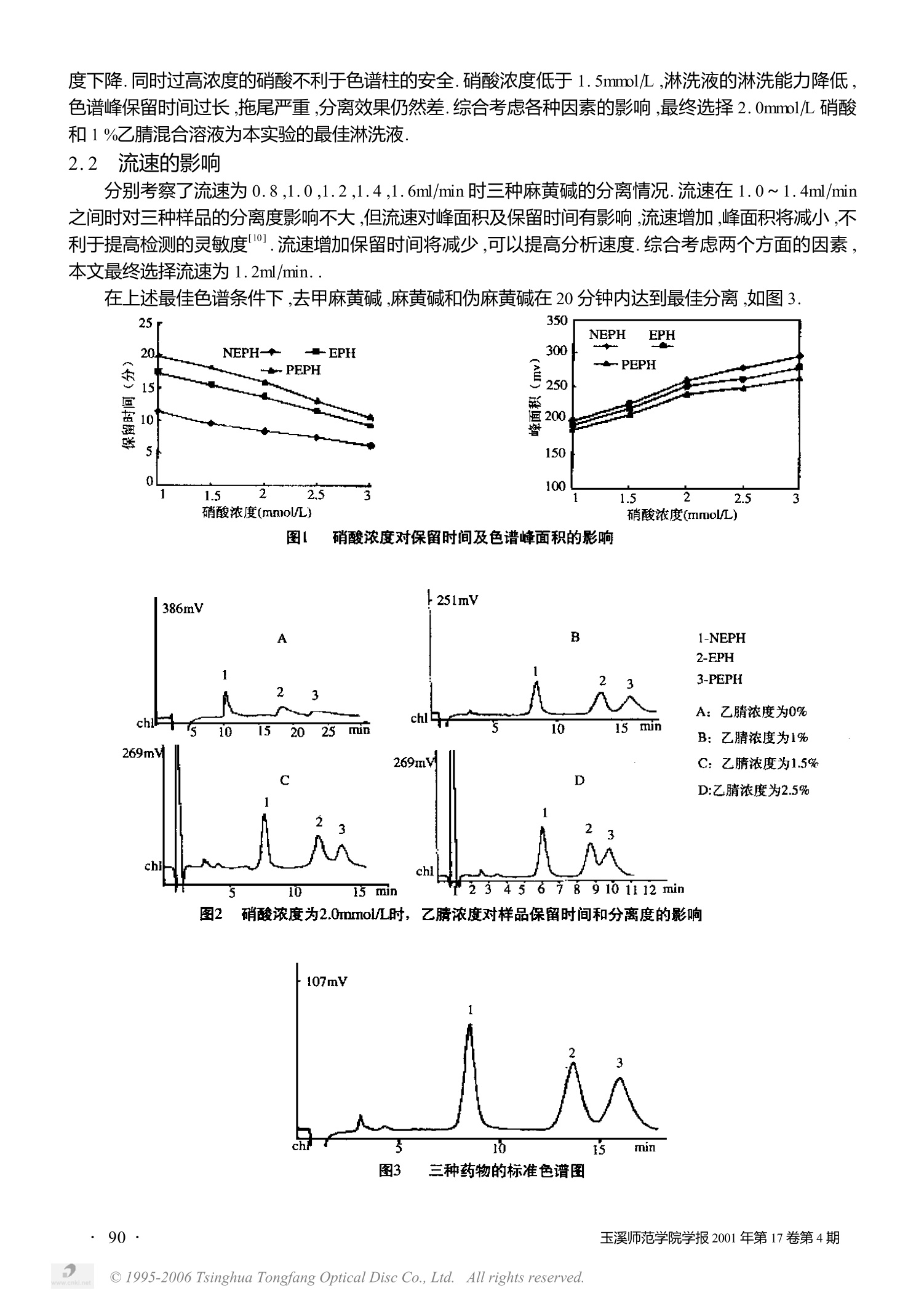
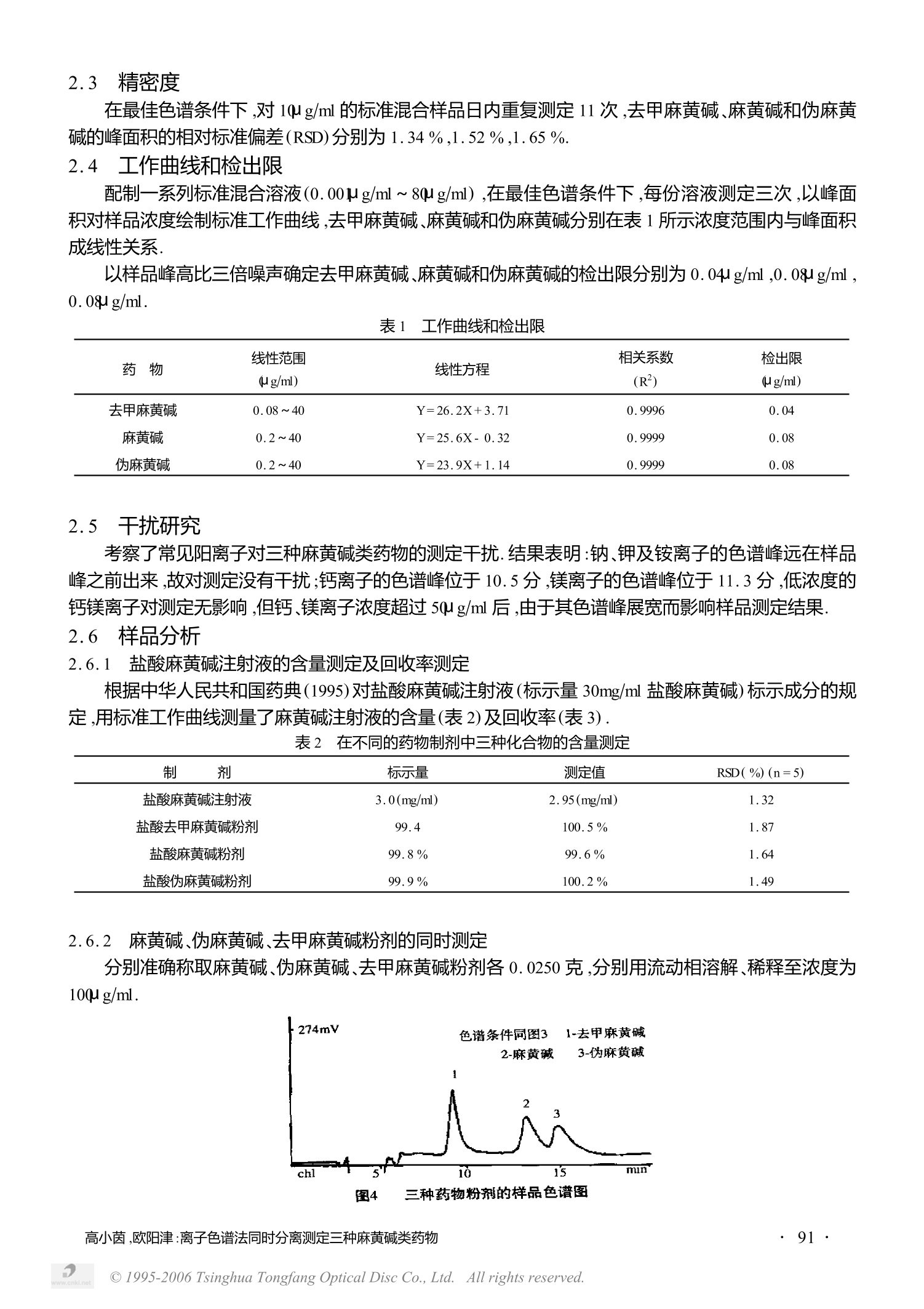
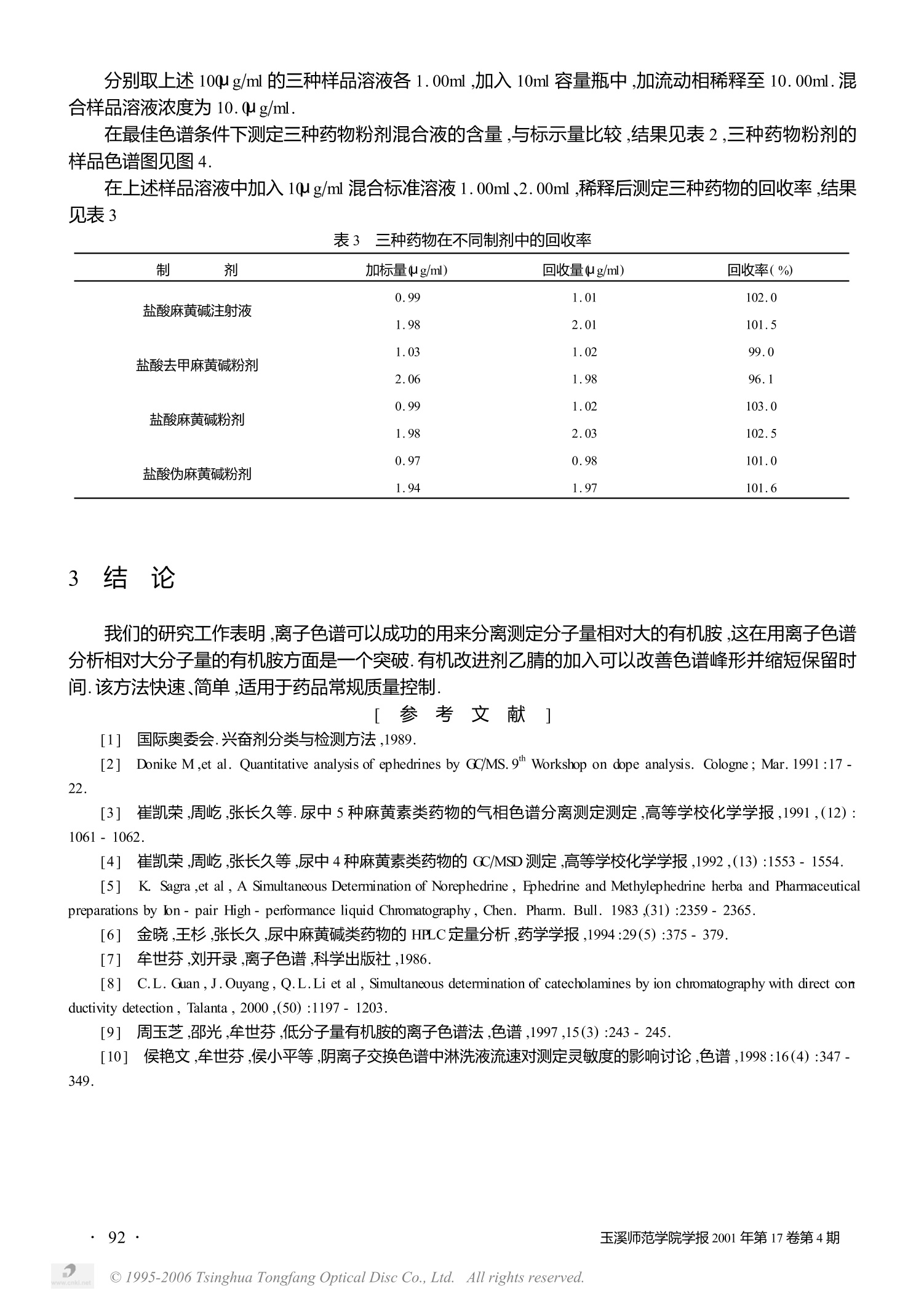
离子色谱法同时分离测定三种麻黄碱类药物 高小茵 欧阳津 (1.玉溪师范学院化学与环境科学系,云南玉溪653100;2.北京师范大学化学系,北京100875) [关键词]离子色谱法;麻黄碱;伪麻黄碱;苯丙醇胺 [摘 要]用离子色谱法同时分离测定三种麻黄碱类药物.在 Metrohm cation 1-2阳离子交换上,用2.0mmol/L HNO和1%乙腈混合溶液作为流动相,在20分钟内同时分离测定了麻黄碱、伪麻黄碱和去甲麻黄碱三种药物.去甲麻黄碱在0.08ug/ml- 40ug/ml 浓度范围内与色谱峰面积成正比:麻黄碱、伪麻黄碱在0.2ug/ml- 40ug/ml 浓度范围内与峰面积成线性关系,线性相关系数分别为0.9996 ,0.9999 ,0.9999.去甲麻黄碱的检出限为0.04ug/ml.麻黄碱及伪麻黄碱的检出限均为0.08ug/ml. [中图分类号]0658 [文献标识码]A [文章编号]1009-9506(2001)04-0088-05 Simultaneous Determination of Three Ephedrines by ChromatographyGAO Xiaoyin OUYANGJin" ( Chemistry Dept. of Yuxi Teachers’ College ,653100 Yuxi, Yunnan;Chemistry Dept. Of Beijing Normal University, 100859 Beijing) Key Words: ion chromatography; ephedrine; pseudoephedrine; phenylpropylamine alcohol Abstract : The medicine containing three ephedrines can be simultaneously separated and determined with the ion chromatography. Byusing a mixture of 2.0 nmol/L HNO3 and 1 % acetonitrile as mobile phase on the exchange of Metrosep cation 1-2, we can simultaneouslyseparate and determine the three medicines containing phedrine, pseudoephedrine & norephedrine in 20 minutes. When the concentrationrange is between 0.08ug/ml- 40ug/ml, norephedrine is directly proportional to the chromatographic peak area. When the concentration rangeis0.2ug/ml-40pg/ml, ephedrine &pseudoephedrine are linear to the chromatographic peak area with its respective phase relation numbersas 0.9996, and 0.9999. The detection limit for norephedrine is 0.04ug/ml, and that for ephedrine &pseudoephedrine is 0.08pg/ml. 前 言 麻黄碱类药物,去甲麻黄碱(NEPH)、麻黄碱(EPH)和伪麻黄碱(PEPH)具有相似的结构,其中麻黄碱和伪麻黄碱属于同分异构体,是中药麻黄的主要有效成分.麻黄碱类药物在临床上广泛用于治疗伤风、哮喘和过敏等症.许多含麻黄的中成药、中西复方制剂中都含有麻麻碱类药物. 麻黄碱类药物有较强的中枢兴奋奋用,在体育比赛中作为兴奋剂使用.国际奥委会在1989年将麻黄碱、伪麻黄碱、去甲麻黄碱、去甲伪麻黄碱、甲基麻黄碱列入禁用药物.鉴于麻黄碱类药物在临床上广泛应用,国际田联又对其作了限量规定.因此,建立一个既能同时分离又能准确定量麻黄碱类药物的测定方法,对药物质量控制及兴奋剂检测都是十分必要的. 目前用于麻黄碱类检测的方法较多,最常用的方法有 GC/MC法,即将其先进行选择性衍生化后,GC/MS分离测定,但由于同一药物会产生多于一种的衍生化产物,使方法的重现性现佳.崔凯荣等314小进行了尿中四种麻黄碱类药物不经衍生化的直接 GC/MSD方法测定,但所需时间较长,线性范围较窄.Sagra等用高效离子对色谱法分离测定了麻黄碱类药物,但所使用的流动相过于复杂.金晓等用高效液相色谱法以甲基苯丙醇胺为内标,在C18柱上测定了尿中的6种麻黄碱类药物的含量,但该方法需进行梯度洗脱,流动相及操作过于复杂,线性范围过小. ( [收稿日期12001-03-08 ) ( [作者简介]高小茵(1966-),女,云南玉溪人,讲师,硕士,从事化学教学工作。 ) 本工作使用一根瑞士万通产的 Metrosep cation 1-2阳离子交换柱来分离上述三种麻黄碱化合物,用硝酸与乙腈的混合溶液作为流动相,使这三种药物离子化,发生离子交换反应而被分离检测.该方法简单、快速;克服了其它方法流动相复杂,操作繁琐的缺点,适合于麻黄碱类药物制剂的常规控制分析. 实验部分 1.1 仪器与试剂 仪器:瑞士万通离子色谱仪(Switzerland Metrohm LTD),包括733 IC分离中心、709IC泵、732电导检测器和一台记录色谱图和数据处理的个人电脑及软件. 试剂:盐酸苯丙醇胺、盐酸麻黄碱、盐酸伪麻黄碱:对照品,购自中国药品与生物制品检验所.盐酸麻黄碱注射液:北京市永康制药厂.盐酸麻黄碱、盐酸伪麻黄碱、盐酸去甲麻黄碱粉剂:内蒙古赤峰制药厂.其它试剂均为分析纯,水为去离子水.流动相及被测溶液都经过0.45um的微膜过滤. 1.2 色谱条件 分离柱:Metrosep cation 1- 2(6.1010.0000);流动相:2.0mmol/L硝酸与1%乙腈的混合溶液;流速:1.2ml/min;进样量:20pl 2 结果与讨论 2.1 流动相的选择 去甲麻黄碱,麻黄碱和伪麻黄碱属于有机胺类,在文献中,用于分析有机胺的淋洗液通常为低浓度的无机酸如硝酸、盐酸.考虑到相同浓度的盐酸比硝酸具有更大的背景电导值,过高的背景电导将降低电导检测器的灵敏度.为了提高检测灵敏度,故本文一开始就选用硝酸作淋洗液.参照文献,首先在0-3.0mmol/L范围内变换硝酸浓度,硝酸浓度较低时,在20分钟内三个样品不出峰,当硝酸浓度达到2.0mmol/L时,三个样品在25分钟内出峰,但麻黄碱和伪麻黄碱的峰形较宽且拖尾严重,对定量分析不利.为了节省时间并改善峰形,根据文献报导,加入了适量的乙腈作为有机改进剂,结果发现,三个样品的保留时间大大减少且峰形也得到了较好的改善.不加乙腈时的色谱图见图2(A) 为了找到最佳的淋洗液组成条件,分别考察了乙腈浓度及硝酸浓度对三个样品的分离度及保留时间的影响. 2.1.1 乙腈浓度的影响 分别固定硝酸浓度为3.0mmol/L,2.5mmol/L ,2.0mmol/L,考察了乙腈浓度对分离度及保留时间的影响,结果发现,在硝酸浓度一定的条件下: (a)在乙腈浓度为0%~1%的范围内,乙腈浓度对样品的保留时间有较大的影响,乙腈浓度增大则三个样品的保留时间都减少,且麻黄碱及伪麻黄碱的保留时间减少的较多.乙腈浓度过小则色谱峰形较宽,拖尾严重,保留时间过长. (b)乙腈浓度超过1%后后,乙腈浓度对三种化合物保留时间的影响减弱;同时随着乙腈浓度增加麻黄碱和伪麻黄碱的分离度越来越差. :(c)乙腈浓度对去甲麻黄碱的保留时间有影响,但影响不太大.当乙腈浓度为1%时,上述三个浓度的硝酸对样品的分离度都达到最佳化. 2.1.2 硝酸浓度的影响 保持乙腈浓度为1%,在1.0mmol/L~3.0mmol/L范围内改变淋洗液中的硝酸浓度,结果发现随着硝酸浓度的增大,样品色谱峰的保留时间缩短(图2),硝酸浓度增加,色谱峰面积也增大(图3).硝酸浓度在1.5~2.0mmol/L范围内,样品的分离度最佳.硝酸浓度超过2.0mmol/L后,麻黄碱与伪麻黄碱的分离 高小茵,欧阳津:离子色谱法同时分离测定三种麻黄碱类药物 度下降.同时过高浓度的硝酸不利于色谱柱的安全.硝酸浓度低于 1.5mmol/L,淋洗液的淋洗能力降低,色谱峰保留时间过长,拖尾严重,分离效果仍然差.综合考虑各种因素的影响,最终选择2.0mml/L硝酸和1%乙腈混合溶液为本实验的最佳淋洗液. 2.2 流速的影响 分别考察了流速为0.8,1.0,1.2,1.4,1.6ml/min 时三种麻黄碱的分离情况.流速在1.0~1.4ml/min之间时对三种样品的分离度影响不大,但流速对峰面积及保留时间有影响,流速增加,峰面积将减小,不利于提高检测的灵敏度0.流速增加保留时间将减少,可以提高分析速度.综合考虑两个方面的因素,本文最终选择流速为1.2ml/min.. 在上述最佳色谱条件下,去甲麻麻碱,麻黄碱和伪麻黄碱在20分钟内达到最佳分离,如图3. 图l 硝酸浓度对保留时间及色谱峰面积的影响 图2 硝酸浓度为2.0mmol/L时,乙腈浓度对样品保留时间和分离度的影响 图3 三种药物的标准色谱图 2.3 精密度 在最佳色谱条件下,对10ug/ml的标准混合样品日内重复测定11次,去甲麻黄碱_麻黄碱和伪麻黄碱的峰面积的相对标准偏差(RSD)分别为1.34%,1.52%,1.65% 2.4 工作曲线和检出限 配制一系列标准混合溶液(0.001ug/ml~80ug/ml),在最佳色谱条件下,每份溶液测定三次,以峰面积对样品浓度绘制标准工作曲线,去甲麻黄碱、麻黄碱和伪麻黄碱分别在表1所示浓度范围内与峰面积成线性关系. 以样品峰高比三倍噪声确定去甲麻黄碱、麻黄碱和伪麻黄碱的检出限分别为 0.04ug/ml,0.08ug/ml,0.08ug/ml. 表1 工作曲线和检出限 药 物 线性范围 线性方程 相关系数 检出限 (ug/ml) (R²) (ug/ml) 去甲麻黄碱 0.08~40 Y=26.2X+3.71 0.9996 0.04 麻黄碱 0.2~40 Y=25.6X-0.32 0.9999 0.08 伪麻黄碱 0.2~40 Y=23.9X+1.14 0.9999 0.08 2.5 干扰研究 考察了常见阳离子对三种麻黄碱类药物的测定干扰.结果表明:钠、钾及铵离子的色谱峰远在样品峰之前出来,故对测定没有干扰;钙离子的色谱峰位于10.5分,镁离子的色谱峰位于11.3分,低浓度的钙镁离子对测定无影响,但钙、镁离子浓度超过50ug/ml后,由于其色谱峰展宽而影响样品测定结果. 2.6 样品分析 2.6.1 盐酸麻黄碱注射液的含量测定及回收率测定 根据中华人民共和国药典(1995)对盐骏麻黄碱注射液(标示量30mg/ml盐酸麻黄碱)标示成分的规定,用标准工作曲线测量了麻黄碱注射液的含量(表2)及回收率(表3). 表2 在不同的药物制剂中三种化合物的含量测定 制 剂 标示量 测定值 RSD(%)(n=5) 盐酸麻黄碱注射液 3.0(mg/ml) 2.95(mg/ml) 1.32 盐酸去甲麻黄碱粉剂 99.4 100.5% 1.87 盐酸麻黄碱粉剂 99.8% 99.6% 1.64 盐酸伪麻黄碱粉剂 99.9% 100.2% 1.49 2.6.2 麻黄碱、伪麻黄碱、去甲麻黄碱粉剂的同时测定 分别准确称取麻黄碱、伪麻黄碱、去甲麻麻碱粉剂各0.0250克,分别用流动相溶解、稀释至浓度为100ug/ml. 4 三种药物粉剂的样品色谱图 高小茵,欧阳津:离子色谱法同时分离测定三种麻黄碱类药物 分别取上述 100ug/ml 的三种样品溶液各1.00ml,加入10ml容量瓶中,加流动相稀释至10.00ml.混合样品溶液浓度为 10.0ug/ml. 在最佳色谱条件下测定三种药物粉剂混合液的含量,与标示量比较,结果见表2,三种药物粉剂的样品色谱图见图4. 在上述样品溶液中加入10ug/ml混合标准溶液1.00ml2.00ml,稀释后测定三种药物的回收率,结果见表3 表3 三种药物在不同制剂中的回收率 制 剂 加标量(ug/ml) 回收量(ug/ml) 回收率(%) 盐酸麻黄碱注射液 0.99 1.01 102.0 1.98 2.01 101.5 盐酸去甲麻黄碱粉剂 1.03 1.02 99.0 2.06 1.98 96.1 盐酸麻黄碱粉剂 0.99 1.02 103.0 1.98 2.03 102.5 盐酸伪麻黄碱粉剂 0.97 0.98 101.0 1.94 1.97 101.6 3 结 论 我们的研究工作表明,离子色谱可以成功的用来分离测定分子量相对大的有机机,这在用离子色谱分析相对大分子量的有机胺方面是一个突破.有机改进剂乙腈的加入可以改善色谱峰形并缩短保留时间.该方法快速、简单,适用于药品常规质量控制. ( 参 考 文 献 1 ) ( 国际奥委会.兴奋剂分类与检测方法,1989. ) ( D onike M,et a l . Quantitative analysi s of ephedrines b y GC/MS.9" Workshop on dope a nalysis. Cologne ; Mar.1991:17- 22. ) ( [3] 崔凯荣,周屹,张长久等.尿中5种麻麻素类药物的气相色谱分离测定测定,高等学校化学学报,1991,(12) 1061- 1 062. ) ( 崔凯荣,周屹,张长久等,尿中4种麻黄素类药物的 GC/MSD测定,高等学校化学学报,1992,(13):1553-1554. ) ( K . S agra ,et al , A S imultaneous Determination of Norephedrine , Ephedrine and M ethylephedrine herba and P h armaceutical preparations by Ion- pair High- performance liqui d Chromatography, Chen. Pharm. B ull. 1 983 ,(31) : 2359-23 6 5. ) ( 金晓,王杉,张长久,尿中麻黄碱类药物的 HPLC定量分析,药学学报,1994:29(5):375-379. ) ( 弃世芬,刘开录,离子色谱,科学出版社,1986. ) ( C .L . Guan,J. Ouyang, Q.L.Li e t al, Simultaneous determination of catecholamines by ion chromatography with direct c o n ductivity detection , Talanta , 2000 ,(5 0 ) : 1197- 1 2 03. ) ( [9] 周玉芝,邵光,牟世芬,低分子量有机胺的离子色谱法,色谱,1997,15(3):243-245. ) ( [101 :侯艳文,牟世芬,侯小平等,阴离子交换色谱中淋洗液流速对测定灵敏度的影响讨论,色谱,1998:16(4):347- 349. ) ·溪师范学院学报第第期Tsinghua Tongfang Optical Disc Co.,Ltd.All rights reserved.
确定


还剩3页未读,是否继续阅读?
扬州华明仪器设备有限公司为您提供《化学药中特殊物质和基团检测方案 》,该方案主要用于中药制剂中含量测定检测,参考标准--,《化学药中特殊物质和基团检测方案 》用到的仪器有
相关方案
更多







