方案详情
文
治疗性单克隆抗体 (mAb) 是生物制药行业中发展最快的蛋白质类药物。由于蛋白质药物的异质性,必须对此类生物分子进行全面的分析表征。使用液相色谱和电喷雾质谱 (LC/MS) 进行的肽谱分析是基本的蛋白质药物表征技术。蛋白质药物的深入表征不仅能确认一级结构序列,还可以对脱酰氨基化、氧化和糖基化等翻译后修饰 (PTM) 进行鉴定和定量分析。本应用简报介绍了 mAb 肽谱分析的一体化工作流程,涵盖了从自动化样品前处理 到数据分析等过程,流程中涉及到 Agilent AssayMAP Bravo 液体处理自动化系统、Agilent 1290 Infinity II 液相色谱系统、Agilent 6545XT AdvanceBio Q-TOF 和 Agilent MassHunter BioConfirm B.09 软件。Agilent 6545XT AdvanceBio LC/Q-TOF 提供的全新数据采集方法(迭代 MS/MS)可用于深入的肽谱分析,以提高序列覆盖率并改进 PTM 分析。
方案详情

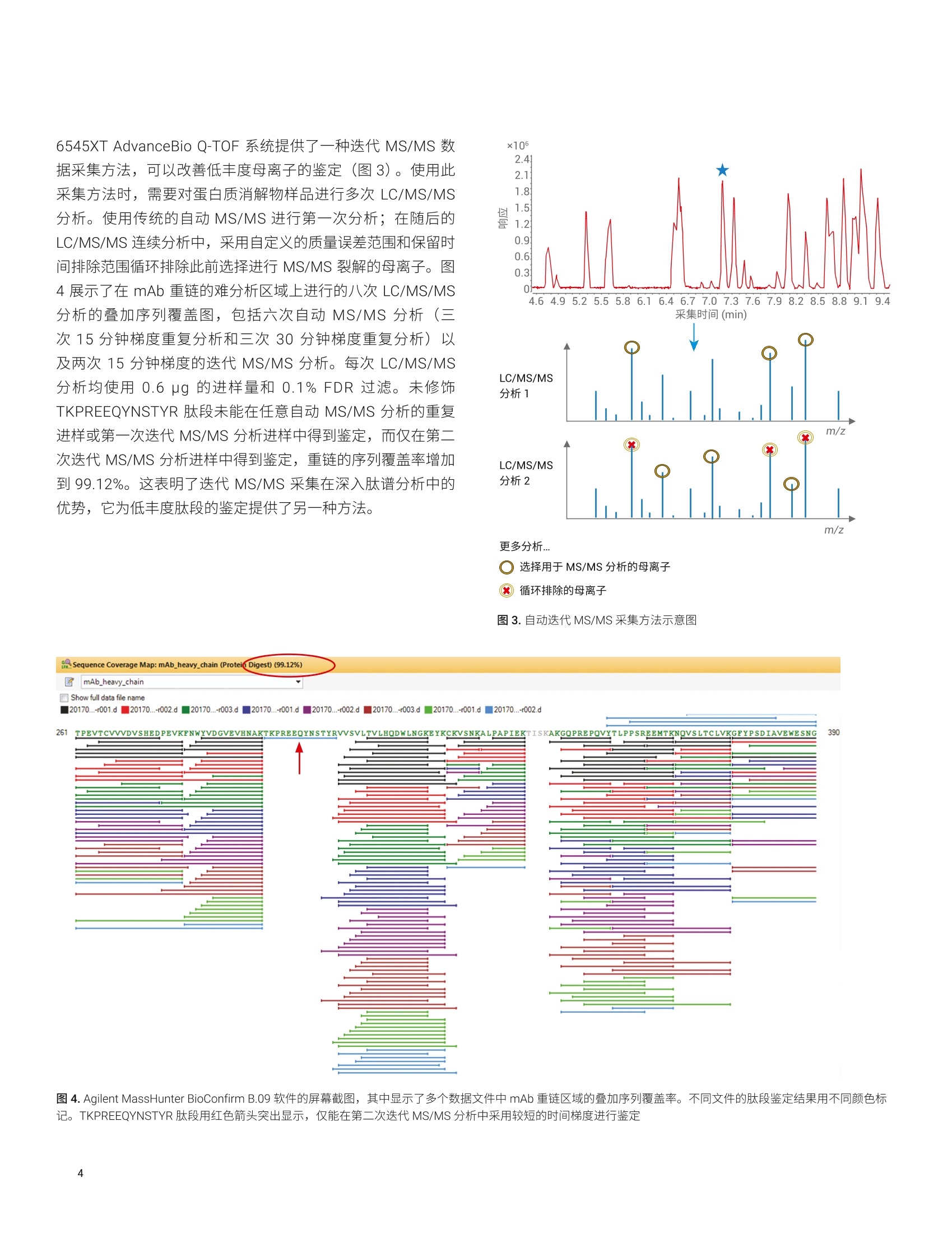
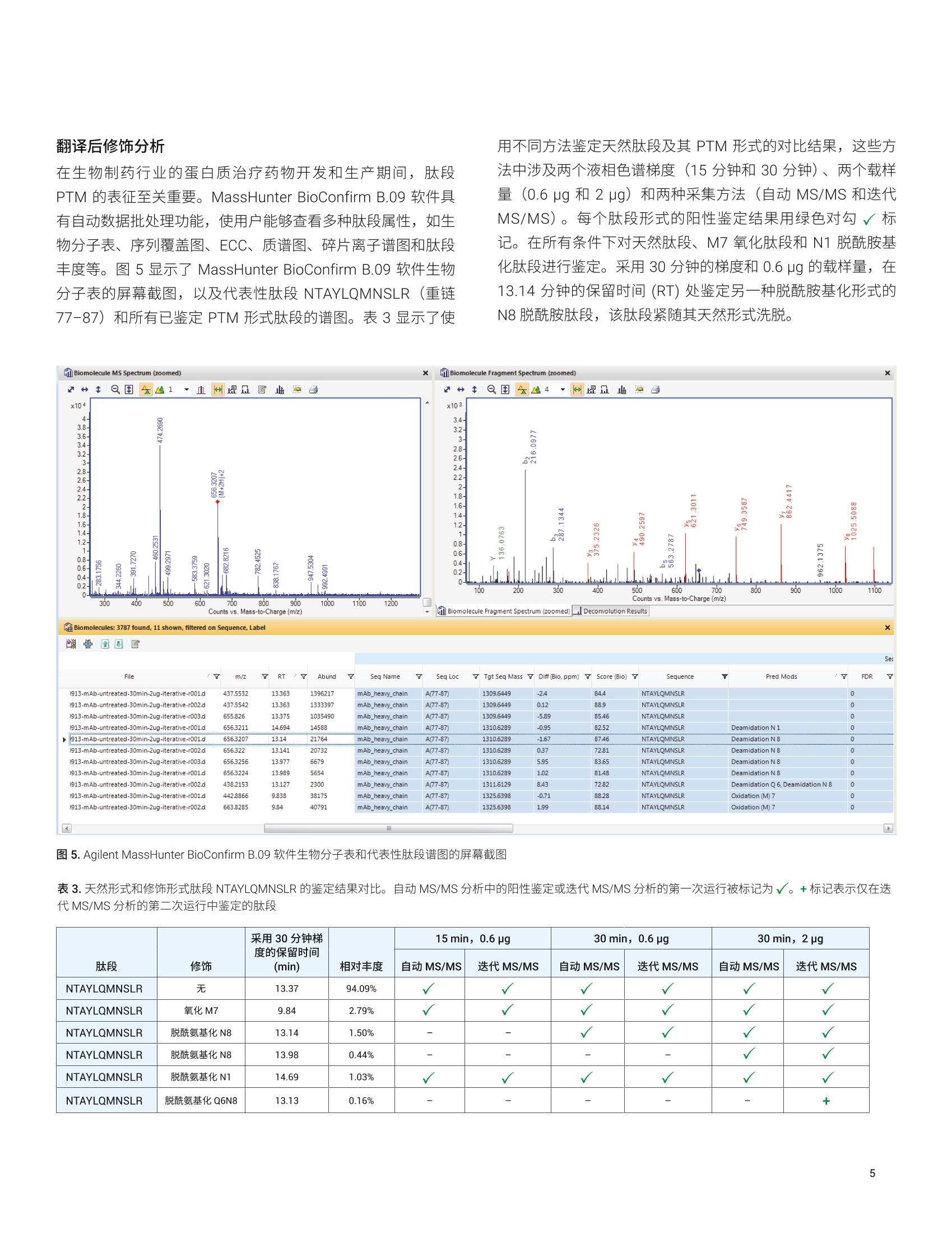
Linfeng Wu 和 David L. Wong 安捷伦科技有限公司 采用 Agilent 6545XT AdvanceBioLC/Q-TOF 的迭代MS/MS采集方法进行深入的肽谱分析 前言 治疗性单克隆抗体(mAb) 是生物制药行业中发展最快的蛋白质类药物。由于蛋白质药物的异质性,必须对此类生物分子进行全面的分析表征。使用液相色谱和电喷雾质谱(LC/MS) 进行的肽谱分析是基本的蛋白质药物表征技术。蛋白质药物的深入表征不仅能确认一级结构序列,还可以对脱酰氨基化、氧化和糖基化等翻译后修饰(PTM) 进行鉴定和定量分析。 本应用简报介绍了 mAb 肽谱分析的一体化工作流程,涵盖了从自动化样品前处理到数据分析等过程,流程中涉及到 Agilent AssayMAP Bravo 液体处理自动化系统Agilent 1290 Infinity ll液相色谱系统、Agilent 6545XT AdvanceBio Q-TOF 和Agilent MassHunter BioConfirm B.09 软件。 Agilent 6545XT AdvanceBio LC/Q-TOF提供的全新数据采集方法(迭代 MS/MS) 可用于深入的肽谱分析,以提高序列覆盖率并改进 PTM 分析。 材料 CHO 培养的人 IgG1 mAb 由安捷伦研发实验室进行表达和纯化。将单克隆抗体还原、烷基化并用胰蛋白酶消解,然后使用Agilent AssayMAP Bravo 液体处理自动化系统对其进行脱盐处理。如文中所述,每次使用0.6 pg或 2 pg 的载样量对酶解样品进行LC/MS/MS分析。 仪器 样品前处理工作站 Agilent AssayMAP Bravo 系统 液相色谱系统 Agilent 1290 Infinity 液相色谱系统,包括: Agilent 1290 Infinity ll 高速泵 G7120A Agilent 1290 Infinity II Multisampler G7167B Agilent 1290 Infinity ⅡI柱温箱 G7116B 色谱柱 Agilent AdvanceBio 肽谱分析色谱柱(2.1×150mm, 2.7 um) 质谱系统 使用配备安捷伦双喷射流电喷雾离子源的 Agilent 6545XTAdvanceBio LC/Q-TOF系统。 LC/MS分析 如文中所述,采用15分钟或30分钟的梯度, 在 AgilentAdvanceBio 肽谱分析色谱柱(2.1×150mm, 2.7 pm) 上进行液相色谱分离。如文中所述,使用传统的自动 MS/MS 方法或迭代 MS/MS 方法采集数据。表1和表2列出了 LC/MS 参数。 数据处理 使用 Agilent MassHunter BioConfirm B.09.00 软件处理从LC/MS/MS分析中采集的数据。将搜索参数设置为允许半胰蛋白酶肽段和最多两个未裂解肽段的胰蛋白酶消解,包括半胱氨酸 (C)烷基化、天冬酰胺(N)或谷氨酰胺 (Q)脱酰氨基化、蛋氨酸(M)氧化和N 端焦谷氨酸(E)等可变修饰。允许的质量容差:MS1和MS2 分别为 10 ppm 和30 ppm。将肽段长度限制为5到60个氨基酸 (AA)。肽段谱图匹配需要用到MS/MS功能, 并由0.1%假阳性率 (FDR) 过滤结果。 表1.液相色谱参数 Agilent 1290 Infinity I液相色谱系统 分析柱 Agilent AdvanceBio 肽谱分析柱, 2.1×150 mm, 2.7 pm (部件号653750-902) 柱温 60°℃ 自动进样器温度 4°C 溶剂A 0.1%甲酸的水溶液 溶剂B 0.1%甲酸的90%乙腈溶液 梯度 15分钟梯度 0-15分钟, 3%-40%B 15-18分钟, 40%-90%B18-20分钟, 90%B 20-22分钟,90%-3%B 30分钟梯度 0-30分钟,3%-40%B30-33分钟,40%-90%B 33-35分钟, 90%B 35-37分钟,90%-3%B 流速 0.4mL/min 表2. MS 参数 Agilent 6545XT AdvanceBio LC/Q-TOF 干燥气温度 325°C 干燥气流速 13 L/min 雾化器 35 psig 鞘气温度 275°C 鞘气流速 12 L/min 毛细管电压 4000V 喷嘴电压 0V 碎裂电压 175V 锥孔电压 65 参比质量 121.050873,922.009798 采集模式 扩展动态范围(2 GHz) 质量数范围 110-1700 m/z 采集速率 8质谱图/秒 自动MS/MS 范围 50-1700 m/z 最小MS/MS 采集速率 3质谱图/秒 分离峰宽 窄(约1.3m/z) 母离子/循环 前10 碰撞能量 对于电荷数为2的离子,为3.1*(m/z)/100+1; 对于电荷数为3或大于3的离子,为 3.6*(m/z)/100-4.8 MS/MS阈值 3000响应值和0.001% 动态排除 重复一次,然后排除0.1 或 0.2 min 基于母离子丰度的 扫描速率 是 目标物 25000 响应值/质谱图 使用MS/MS累积时间限 是 纯度 严格性100%,截留率30% 同位素模型 肽段 母离子排序 先按电荷态,再按丰度进行排序;+2,+3,>+3 采用迭代 MS/MS 采集方法的肽谱分析 蛋白质药品的肽谱分析通常需要可重现的样品前处理、深入的肽段鉴定以及批处理数据文件的全面数据分析。我们采用包括AssayMAP Bravo 液体处理自动化系统、6545XT AdvanceBioLC/Q-TOF 系统和 MassHunter BioConfirm B.09 软件在内的一体化肽谱分析工作流程,对 CHO 培养的人 IgG1 mAb 进行肽谱分析实验(图1)。使用 AssayMAP Bravo 平台自动进行样品前处理已在其他应用简报中得到了大量报道13。因此,本应用简报主要介绍数据采集和处理。 图2示出了在15分钟梯度下胰蛋白酶消解 mAb 所得肽段的提取化合物色谱图(ECC)。使用 0.6 pg 的进样量和0.1%FDR过滤器,获得的重链和轻链的序列覆盖率分别为 96.24%和98.63%。轻链的未覆盖序列为短链肽段 EAK (测序位置148-150)。使用1% FDR 过滤器可鉴定出未裂解肽段TASVVCLLNNFYPREAK (测序位置134-150),得到的总覆盖率可达到100%。重链的分析难点在于短序列 TISK (测序位置340-343)和具有一个N-糖基化位点 TKPREEQYNSTYR(测序位置294-306)的肽段。糖肽的糖链会优先裂解,这导致肽段骨架裂解状态不理想,所得到的鉴定分数远低于未修饰肽段的分数,而未修饰肽段在样品中的浓度却非常低。 图 2. 采用 Agilent AdvanceBio肽谱分析色谱柱分离的胰蛋白酶消解 mAb 的肽段 ECC。重链和轻链肽段分别被标记为A和B 6545XT AdvanceBio Q-TOF 系统提供了一种失代 MS/MS 数据采集方法,可以改善低丰度母离子的鉴定(图3)。使用此采集方法时,需要对蛋白质消解物样品进行多次 LC/MS/MS分析。使用传统的自动 MS/MS 进行第一次分析;在随后的LC/MS/MS 连续分析中,采用自定义的质量误差范围和保留时间排除范围循环排除此前选择进行 MS/MS 裂解的母离子。图4展示了在 mAb 重链的难分析区域上进行的八次 LC/MS/MS分析的叠加序列覆盖图,包括六次自动 MS/MS分析(三次15分钟梯度重复分析和三次30分钟梯度重复分析)以及两次15分钟梯度的迭代 MS/MS 分析。每次 LC/MS/MS分析均使用 0.6 pg 的进样量和 0.1% FDR 过滤。未修饰TKPREEQYNSTYR 肽段未能在任意自动 MS/MS分析的重复进样或第一次迭代 MS/MS 分析进样中得到鉴定,而仅在第二次迭代MS/MS 分析进样中得到鉴定,重链的序列覆盖率增加到99.12%。这表明了迭代 MS/MS 采集在深入肽谱分析中的优势,它为低丰度肽段的鉴定提供了另一种方法。 循环排除的母离子 图3.自动迭代MS/MS采集方法示意图 图 4. Agilent MassHunter BioConfirm B.09 软件的屏幕截图,其中显示了多个数据文件中 mAb 重链区域的叠加序列覆盖率。不同文件的肽段鉴定结果用不同颜色标记。TKPREEQYNSTYR 肽段用红色箭头突出显示,仅能在第二次迭代 MS/MS分析中采用较短的时间梯度进行鉴定 翻译后修饰分析 在生物制药行业的蛋白质治疗药物开发和生产期间,肽段PTM 的表征至关重要。MassHunter BioConfirm B.09 软件具有自动数据批处理功能,使用户能够查看多种肽段属性,如生物分子表、序列覆盖图、ECC、质谱图、碎片离子谱图和肽段丰度等。图5显示了 MassHunter BioConfirm B.09 软件生物分子表的屏幕截图,以及代表性肽段 NTAYLQMNSLR(重链77-87)和所有已鉴定 PTM 形式肽段的谱图。表3显示了使 用不同方法鉴定天然肽段及其 PTM 形式的对比结果,这些方法中涉及两个液相色谱梯度(15分钟和30分钟)、两个载样量(0.6 pg和2 pg) 和两种采集方法(自动 MS/MS 和迭代MS/MS)。每个肽段形式的阳性鉴定结果用绿色对勾√标记。在所有条件下对天然肽段、M7氧化肽段和N1脱酰胺基化肽段进行鉴定。采用30分钟的梯度和 0.6 pg 的载样量,在13.14分钟的保留时间 (RT)处鉴定另一种脱酰胺基化形式的N8脱酰胺肽段,该肽段紧随其天然形式洗脱。 图5.Agilent MassHunter BioConfirm B.09 软件生物分子表和代表性肽段谱图的屏幕截图 表3.天然形式和修饰形式肽段 NTAYLQMNSLR 的鉴定结果对比。自动 MS/MS分析中的阳性鉴定或迭代 MS/MS 分析的第一次运行被标记为√。+标记表示仅在迭代MS/MS 分析的第二次运行中鉴定的肽段 肽段 修饰 采用30分钟梯 度的保留时间(min) 相对丰度 15 min, 0.6 pg 30 min, 0.6 pg 30 min,2pg 自动 MS/MS 迭代 MS/MS 自动 MS/MS 迭代MS/MS 自动 MS/MS 迭代 MS/MS NTAYLOMNSLR 无 13.37 94.09% NTAYLQMNSLR 氧化 M7 9.84 2.79% NTAYLQMNSLR 脱酰氨基化N8 13.14 1.50% - NTAYLQMNSLR 脱酰氨基化 N8 13.98 0.44% 一 一 NTAYLQMNSLR 脱酰氨基化N1 14.69 1.03% NTAYLQMNSLR 脱酰氨基化Q6N8 13.13 0.16% - + 通过将载样量进一步增加至2 pg, N8脱酰胺基化形式的肽段还可在不同的 RT (13.98分钟)处得到鉴定,这表明可能存在天冬氨酸异构化。在迭代 MS/MS、30 分钟梯度和2 pg载样量的组合条件下,可在第二次迭代 MS/MS 进样(而不是自动MS/MS分析重复进样)中鉴定出双脱酰胺基化形式的 Q6N8脱洗胺肽段,将其标记为+。该Q6N8 脱酰胺肽段与 N8脱酰胺肽段共洗脱。图6显示了肽段 NTAYLQMNSLR 的天然形式和所有 PTM 形式的 MS/MS 谱图对比结果。用蓝框突出显示的碎片离子是代表性离子,使天然形式和各种 PTM 形式的肽段能够彼此清晰地区分开来,证明可实现高质量的肽段鉴定。 4.5- A 4.0- NTAYLQMNSL'R b. 3.5- b2b3 b5 216.09754 y 3.0- 748.3746 2.5 b, 450.1969 2.0- 287.1358 1024.5211 y4 489.2760 620.3186 1.5- 861.4595 图6.肽段 NTAYLQMNSLR 的翻译后修饰分析。天然形式(A)、M7氧化形式(B)、N8脱酰胺基化形式 (RT=13.14min)(C);接下页:N8脱酰胺基化形式 (RT=13.98 min) (D)、N1脱酰胺基化形式(E)和Q6N8脱酰胺基化形式 (F)的MS/MS 谱图。肽段序列中的修饰氨基酸以红色突出显示。每种类型的代表性碎片离子用蓝框突出显示,以便区分 ×103 D NTAYLQMNSLR 2.0 b2b3b465 0.1- 0-JJilm ....... 11 150 200 250 300 350 400 450 500 550 600 650 700 质荷比(m/z) 图6.承上页:肽段 NTAYLQMNSLR 的翻译后修饰分析。N8脱酰胺基化形式 (RT=13.98min) (D)、N1脱酰胺基化形式(E)和Q6N8脱酰胺基化形式(F)的 MS/MS谱图。肽段序列中的修饰氨基酸以红色突出显示。每种类型的代表性碎片离子用蓝框突出显示,以便区分 MS 数据的定量分析结果显示了肽段 NTAYLQMNSLR 每种类型的相对数量。图7显示了在30分钟梯度的液相色谱分离条件下,肽段的天然形式和所有修饰形式的叠加ECC 及其相对丰度。约94.09%的肽段为天然形式,另外: M7氧化形式占2.79% 两种N8脱酰胺基化形式分别占1.5%和0.44% N1脱酰胺基化形式占1.03% Q6N8脱酰胺基化形式占0.16% 总体而言,采用迭代 MS/MS 采集方法进行两次进样即可鉴定所有天然形式和 PTM 形式的肽段,其中共洗脱脱酰胺肽段的含量可低至0.16%。这些结果表明,采用了迭代 MS/MS 方法进行深入肽谱分析的一体化工作流程具有强大的功能。 图7.天然形式和修饰形式肽段 NTAYLQMNSLR 的叠加 ECC和相对定量分析结果 结论 这一完整的工作流程使用 Agilent AssayMAP Bravo 酶解系统进行自动样品前处理, 将 Agilent 1290 Infinity lI液相色谱与Agilent 6545XT AdvanceBio Q-TOF 联用进行 LC/MS/MS分析,并使用 Agilent MassHunter BioConfirm B.09 软件进行数据分析,证明该工作流程可实现高序列覆盖率的肽谱分析和低丰度 PTM 检测。采用 6545XT AdvanceBio LC/Q-TOF 系统提供的迭代 MS/MS 采集方法,可大幅提高复杂蛋白质消解样品中低丰度肽段的鉴定效率。MassHunter BioConfirm B.09软件能够自动进行数据批处理,使用统计得分和 FDR 通过肽段谱图匹配来过滤MS/MS谱图质量,叠加多个数据文件的序列覆盖率,并将结果表通过链接导航链接到选定肽段的质谱图和色谱图。将 6545XT AdvanceBio LC/Q-TOF 系统和 MassHunterBioConfirm B.09 软件的功能相结合,可提升蛋白质生物治疗药物开发和生产过程中深入肽谱分析的工作流程效率。 www.agilent.com 仅限研究使用。不可用于诊断目的。 本文中的信息、说明和指标如有变更,恕不另行通知。 ( 1 . 自动化液质联用样品前处理:通过 Agilent AssayMAP Bravo 平台实现高通量溶液内酶解和多肽纯化,安捷伦科技公司,出 版 号5991-2957CHCN ) ( 2. 用于单克隆抗体肽谱分析的一体化工作流程,安捷伦科技 公司,出版号5991-7811CHCN ) ( 3. 利用 Agilent AssayMAP Bravo 平台,通过自动化样品前处理实现生物治疗蛋白质准确而可扩展的定量和表征分 析,安捷伦科技公司,出版号5991-4872CHCN ) ( 4. Yang, H.; Zubarev, R. A. Mass spectrometric analysis ofasparagine deamidation and aspartate isomerization inpolypeptides. Electrophoresis 2010,31(1 1 ),1764-1772 ) 查找当地的安捷伦客户中心: www.agilent.com/chem/contactus-cn 免费专线: 800-820-3278,400-820-3278(手机用户) 联系我们: LSCA-China_800@agilent.com 在线询价: www.agilent.com/chem/erfq-cn 前言治疗性单克隆抗体 (mAb) 是生物制药行业中发展最快的蛋白质类药物。由于蛋白质药物的异质性,必须对此类生物分子进行全面的分析表征。使用液相色谱和电喷雾质谱 (LC/MS) 进行的肽谱分析是基本的蛋白质药物表征技术。蛋白质药物的深入表征不仅能确认一级结构序列,还可以对脱酰氨基化、氧化和糖基化等翻译后修饰(PTM) 进行鉴定和定量分析。本应用简报介绍了 mAb 肽谱分析的一体化工作流程,涵盖了从自动化样品前处理到数据分析等过程,流程中涉及到 Agilent AssayMAP Bravo 液体处理自动化系统、Agilent 1290 Infinity II 液相色谱系统、Agilent 6545XT AdvanceBio Q-TOF 和 Agilent MassHunter BioConfirm B.09 软件。Agilent 6545XT AdvanceBio LC/Q-TOF 提供的全新数据采集方法(迭代 MS/MS)可用于深入的肽谱分析,以提高序列覆盖率并改进 PTM 分析。结论这一完整的工作流程使用 Agilent AssayMAP Bravo 酶解系统进行自动样品前处理,将 Agilent 1290 Infinity II 液相色谱与 Agilent 6545XT AdvanceBio Q-TOF 联用进行LC/MS/MS 分析,并使用 Agilent MassHunter BioConfirm B.09 软件进行数据分析,证明该工作流程可实现高序列覆盖率的肽谱分析和低丰度 PTM 检测。采用 6545XT AdvanceBio LC/Q-TOF 系统提供的迭代 MS/MS 采集方法,可大幅提高复杂蛋白质消解样品中低丰度肽段的鉴定效率。MassHunter BioConfirm B.09 软件能够自动进行数据批处理,使用统计得分和 FDR 通过肽段谱图匹配来过滤 MS/MS 谱图质量,叠加多个数据文件的序列覆盖率,并将结果表通过链接导航链接到选定肽段的质谱图和色谱图。将 6545XT AdvanceBio LC/Q-TOF 系统和 MassHunterBioConfirm B.09 软件的功能相结合,可提升蛋白质生物治疗药物开发和生产过程中深入肽谱分析的工作流程效率。
确定






还剩6页未读,是否继续阅读?
安捷伦科技(中国)有限公司为您提供《单克隆抗体(mAb)中肽谱分析检测方案(液质联用仪)》,该方案主要用于预防类生物药品中其他检测,参考标准--,《单克隆抗体(mAb)中肽谱分析检测方案(液质联用仪)》用到的仪器有Agilent 6545XT Q-TOF 液质联用系统、Agilent AssayMAP Bravo 蛋白质样品前处理平台、Agilent 1290 Infinity II 液相色谱系统
推荐专场
相关方案
更多
该厂商其他方案
更多
























