方案详情
文
本文参照ICH、《中国药典》及国家食品药品监督管理局药品评审中心(CDE)的指导原则,
针对人工牛黄在生产工艺过程中使用的二氯甲烷,开发了能测定这种残留溶剂的顶空气相色谱分析方法,并进行了方法学验证。
方案详情

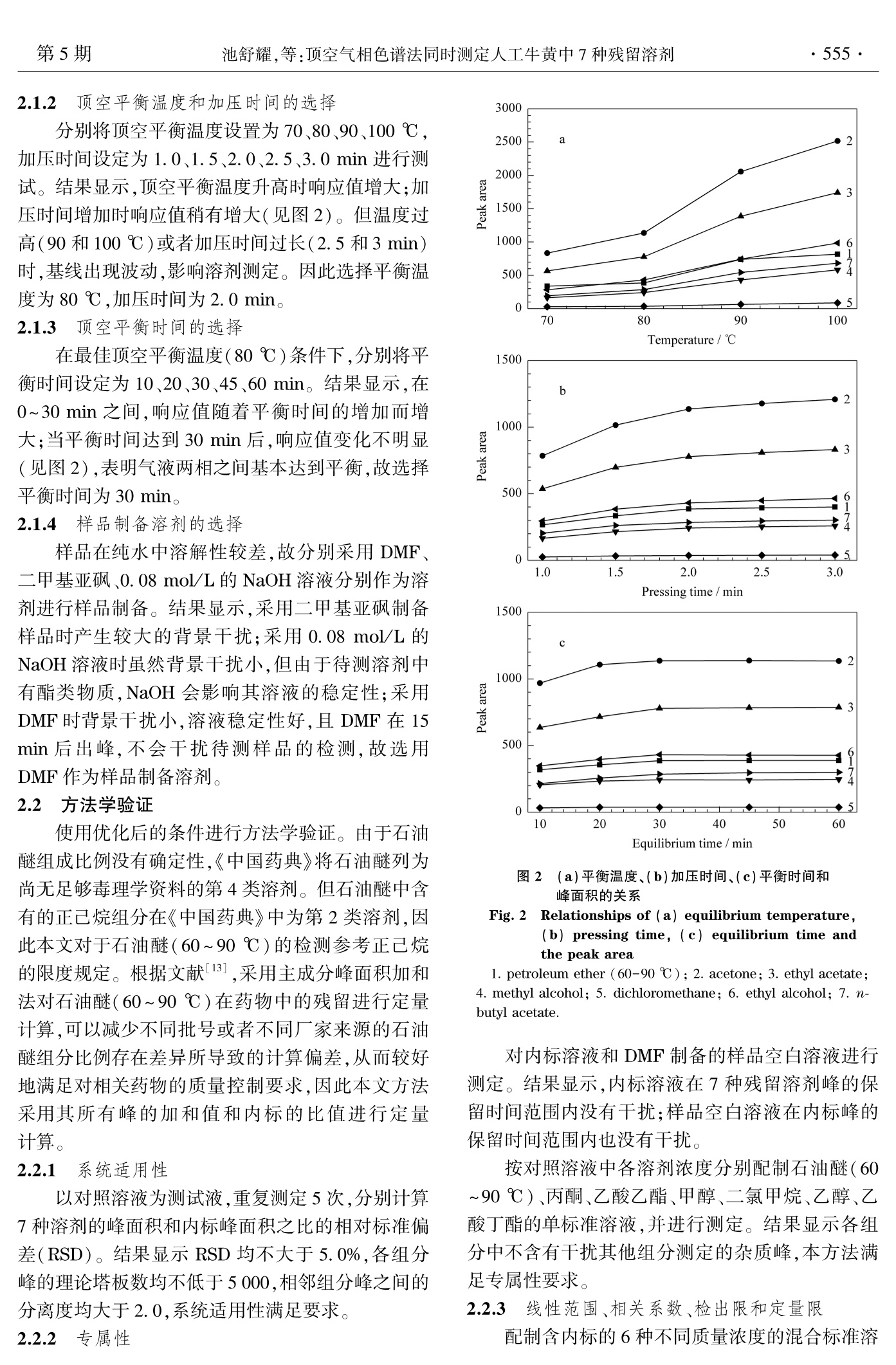
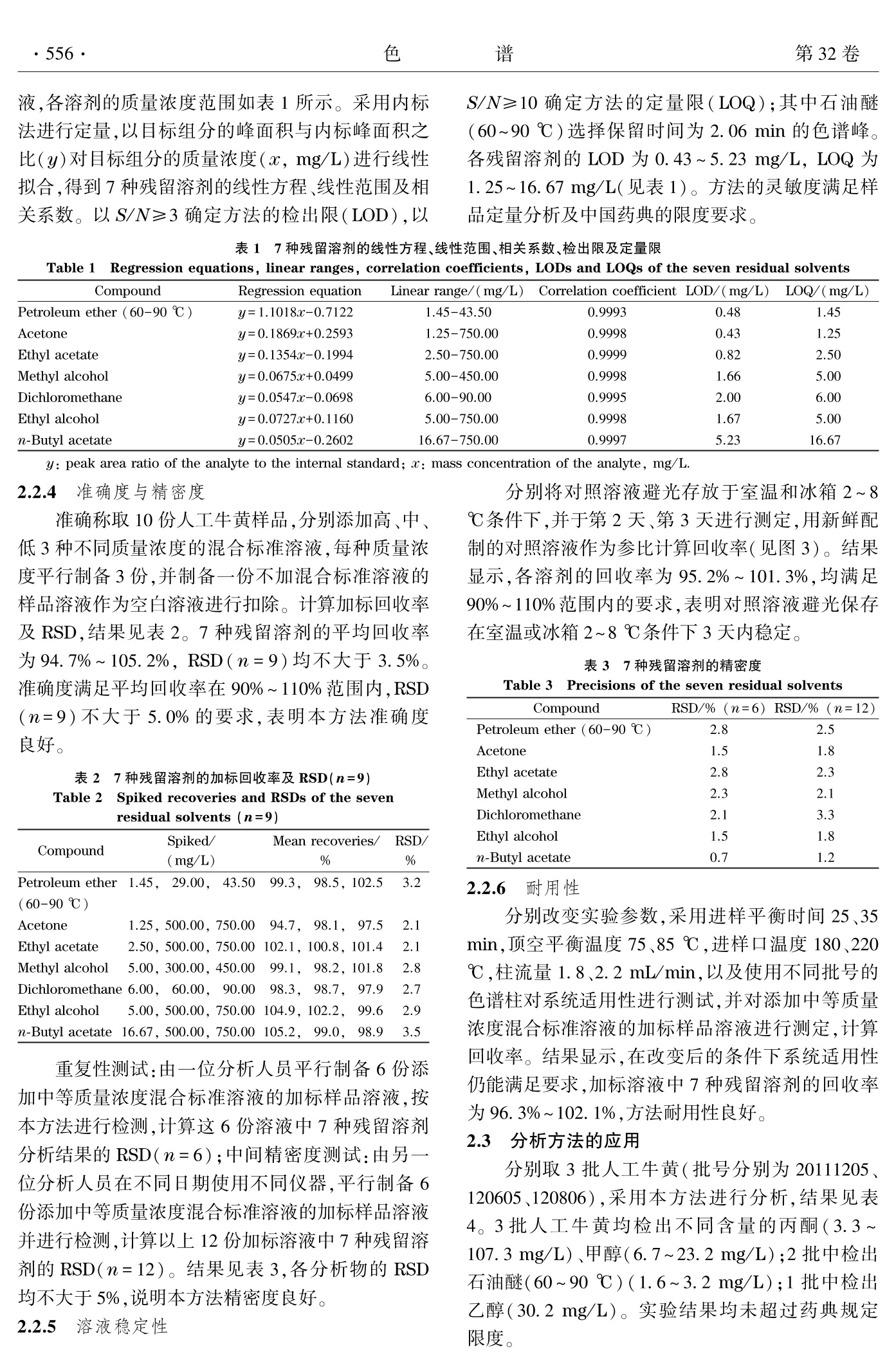
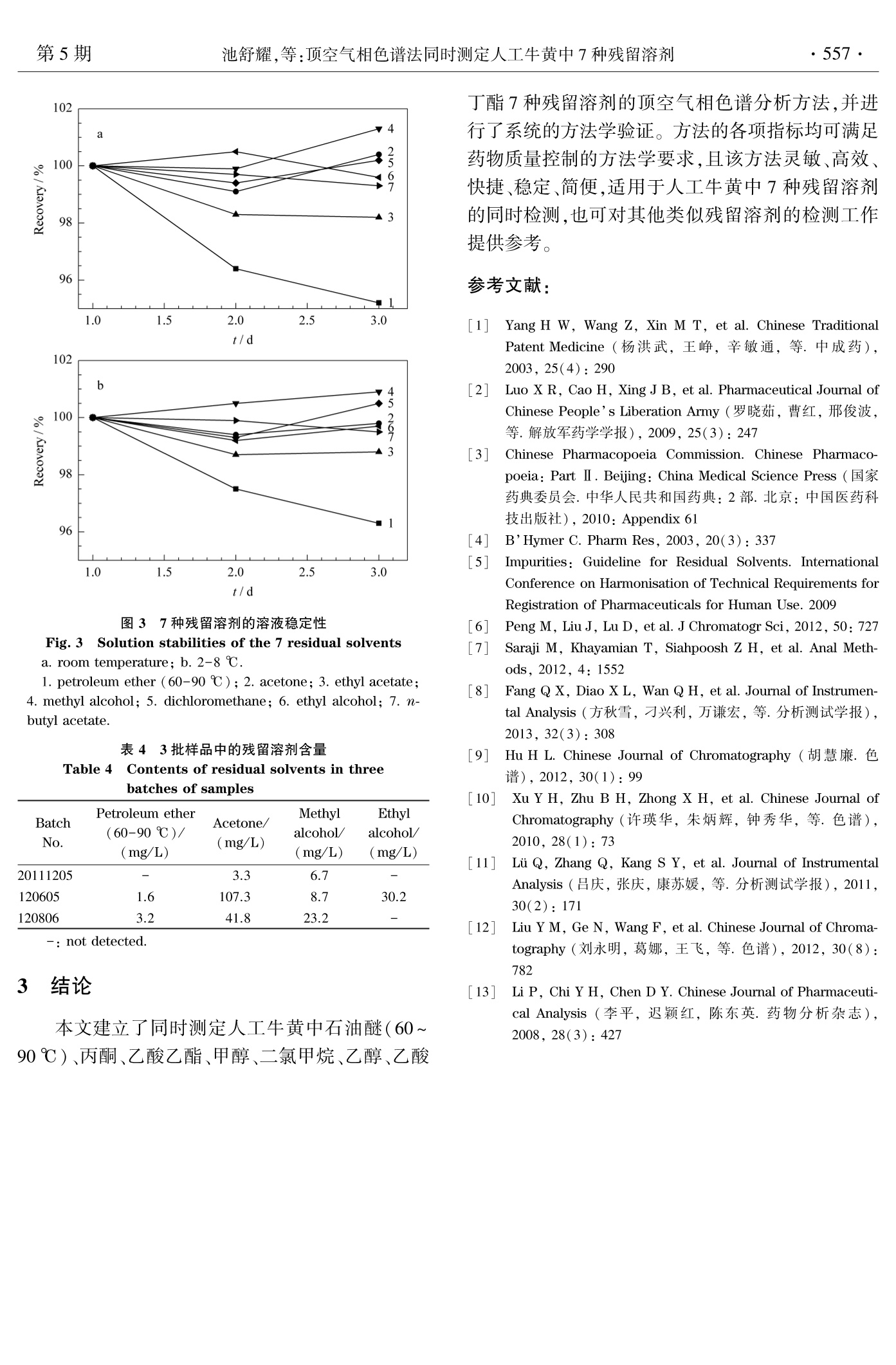
色 谱Chinese Journal of Chromatography2014年5月May 2014Vol.32 No.5553~557 色 谱第32卷·554· 顶空气相色谱法同时测定人工牛黄中7种残留溶剂 池舒耀1,2*,伍迪科',孙晋红',叶汝汉',王晓燕1(1.广州法尔麦兰药物技术有限公司,广东广州510070;2.中国广州分析测试中心,广东广州510070) 摘要:建立了同时测定人工牛黄中石油醚(60~90℃)、丙酮、乙酸乙酯、甲醇、二氯甲烷、乙醇、乙酸丁酯7种残留溶剂的顶空气相色谱分析方法。以Agilent DB-WAX 毛细管色谱柱为分离柱,氢火焰离子化检测器检测,内标法定量,并考察了顶空平衡温度、加压时间、平衡时间等对残留溶剂测定的影响。在优化的条件下,7种残留溶剂在选择的浓度范围内线性关系良好,相关系数(r)均不小于0.999 3;在高、中、低3个加标水平下,平均回收率为94.7%~105.2%,相对标准偏差(RSD)均不大于3.5%。方法的检出限(LOD)为0.43~5.23 mg/L,定量限(LOQ)为1.25~16.67 mg/L。该方法操作简单、准确灵敏、高效快捷,适用于人工牛黄中7种残留溶剂的同时检测。 关键词:内标法;顶空气相色谱法;残留溶剂;人工牛黄 中图分类号:O658 文献标识码:A 文章编号:1000-8713(2014)05-0553-05 Simultaneous determination of seven residual solvents inbovis calculus artifactus by headspace gas chromatography CHI Shuyao1,2*, WU Dike,SUN Jinhong, YE Ruhan', WANG Xiaoyan' (1. Guangzhou PharmaLab Co. Ltd., Guangzhou 510070, China; 2. China National Analysis Centre (Guangzhou), Guangzhou 510070, China) Abstract: A headspace gas chromatography (HS-GC) method was developed for the simulta-neous determination of seven residual solvents (petroleum ether (60-90℃), acetone, ethylacetate, methanol, methylene chloride, ethanol and butyl acetate) in bovis calculus artifactus.The DB-WAX capillary column and flame ionization detector (FID) were used for the separa-tion and detection of the residual solvents, and the internal standard method was used for thequantification. The chromatographic conditions, such as equilibrium temperature and equilibri-um time, were optimized. Under the optimized conditions, all of the seven residual solventsshowed good linear relationships with good correlation coefficients (not less than 0.999 3) inthe prescribed concentration range. At three spiked levels, the recoveries for the seven residualsolvents were 94.7%-105.2% with the relative standard deviations (RSDs) less than 3.5%. Thelimits of detection (LODs) of the method were 0.43-5.23 mg/L, and the limits of quantifica-tion (LOQs) were 1.25-16.67 mg/L. The method is simple, rapid, sensitive and accurate, andis suitable for the simultaneous determination of the seven residual solvents in bovis calculusartifactus. Key words: internal standard method; headspace gas chromatography (HS-GC); residual sol-vent; bovis calculus artifactus 人工牛黄主要是由牛胆粉、胆酸、猪去氧胆酸、牛磺酸、红素、胆固醇、微量元素等有效成分加工而成,具有清热、解毒、祛痰、定惊之功效。天然牛黄价格昂贵,国内大部分厂家在生产含有牛黄的 中药制剂中采用人工牛黄代替天然牛黄人药,所以控制人工牛黄的质量尤为重要[2] 药品中的残留溶剂是指在原料药或辅料的生产中以及在制剂制备过程中使用的、在工艺过程中未 ( *通讯联系人.Tel:(020)87686318,E-mail:shu335@ 126.com. ) ( 基金项目:广东省科技计划项目(2012B040307002). ) ( 收稿日期:2014-01-07 ) 能完全去除的有机溶剂13]。这些有机溶剂的使用对药物的产率、晶型以及溶解度等产生重要影响,在药物合成反应中必不可少,但药物中残留过量的溶剂会对人体造成潜在的危害4J。人类用药注册技术要求国际协调会议(ICH)将残留溶剂分为3个类别,并规定了明确的限度[5]。因此,为保障用药安全,控制残留溶剂十分重要。 气相色谱法检测残留溶剂,常用的有直接进样气相色谱法16静静态和动态顶空气相色谱法7等,其中静态顶空气相色谱法优点明显,文献_8-12J报道较多,但尚未见对人工牛黄中残留溶剂进行测定的相关文献。本文参照 ICH、《中国药典》及国家食品药品监督管理局药品评审中心(CDE)的指导原则,针对人工牛黄在生产工艺过程中使用的石油醚(60~90℃)、丙酮、乙酸乙酯、甲醇、二氯甲烷、乙醇、乙酸丁酯,开发了能同时测定这7种残留溶剂的顶空气相色谱分析方法,并进行了方法学验证。 1实验部分 1.1 仪器与试剂 Agilent 7890A 气相色谱仪(美国 Agilent 公司,配 FID 检测器);自动顶空进样器(成都科林分析技术有限公司);天平:DENVER T-2002(分度值0.01g)和 DENVER TB-215D(分度值0.01 mg)(德国Sartorius 公司)。 标准物质:丙酮(中国计量科学研究院),乙酸乙酯、二氯甲烷(美国J.T. Baker公司),甲醇、乙酸丁酯(美国 Sigma-Aldrich 公司),乙醇(美国Aladdin公司),石油醚(60~90℃,瑞典 Oceanpak公司);内标:正丙醇(中国药品生物制品检定所);以上试剂纯度均大于98%。供试品:人工牛黄(市场随机购买);试剂:N,N-二甲基甲酰胺(DMF)(分析纯,广州化学试剂厂)。 1.2 气相色谱和顶空条件 色谱条件:Agilent DB-WAX 毛细管色谱柱(30m×0.32 mmx0.50 um);载气为氮气(纯度≥99.999 2%),载气流速 2 mL/min,分流比1:1,顶空进样;进样口温度200℃;起始柱温40℃,保持15min,以 10℃/min 程序升温至120℃,保持 10min. 顶空条件:平衡温度80℃,平衡时间30 min,转移线温度110℃,针温度100℃,加压时间2 min,进样时间3s,放空时间20 s. 1.3 实验方法 1.3.1 内标溶液的配制 精密量取正丙醇适量,用DMF 稀释成质量浓度为 500 mg/L 的内标溶液。 1.3.2 对照溶液的配制 精密量取石油醚(60~90℃)、丙酮、乙酸乙酯、甲醇、二氯甲烷、乙醇、乙酸丁酯适量,置于同一容量瓶中,用内标溶液稀释成含石油醚(60~90℃)29mg/L,甲醇 300 mg/L,二氯甲烷 60 mg/L,其余分析物均为 500 mg/L 的对照溶液。 1.3.3 供试品溶液的配制 取人工牛黄约 0.2 g,精密称定,置于顶空瓶中,精密量取内标溶液2.0 mL 到瓶中,压盖,摇匀。 2结果与讨论 2.1 色谱条件的优化 2.1.1 色谱柱的选择 实验考察了中国科学院兰州化学物理研究所色谱中心的非极性色谱柱 AT. SE-54(30m×0.32 mm×1.00um)和 Agilent公司的极性色谱柱DB-WAX(30 mx0.32 mmx0.50 um)对7种有机溶剂分离的效果。实验发现非极性色谱柱对各溶剂分离效果较差,且乙酸丁酯在溶剂 DMF 后出峰;而使用极性色谱柱则能有效分离各溶剂,如图1所示。故选择使用 Agilent DB-WAX 极性色谱柱。 图1 7种残留溶剂标准混合溶液的色谱图 Fig.1 Chromatograms for the mixed standard solution of the seven residual solventsColumns: a. AT. SE-54; b. Agilent DB-WAX. Peaks: 1. petroleum ether (60-90℃);2. acetone; 3. ethylacetate;4. methyl alcohol;5. dichloromethane; 6. ethyl alco-hol; 7. n-propanol (internal standard); 8. n-butyl acetate. 2.1.2 顶空平衡温度和加压时间的选择 分别将顶空平衡平度设置为70、80、90、100℃,加压时间设定为1.0、1.52.0、2.53.0 min 进行测试。结果显示,顶空平衡温度升高时响应值增大;加压时间增加时响应值稍有增大(见图2)。但温度过高(90和100℃)或者加压时间过长(2.5和3min)时,基线出现波动,影响溶剂测定。因此选择平衡温度为80℃,加压时间为 2.0 min。 2.1.3 顶空平衡时间的选择 在最佳顶空平衡温度(80℃)条件下,分别将平衡时间设定为10、20、30、45、60 min。结果显示,在0~30 min 之间,响应值随着平衡时间的增加而增大;当平衡时间达到30 min 后,响应值变化不明显(见图2),表明气液两相之间基本达到平衡,故选择平衡时间为 30 min。 2.1.4 样品制备溶剂的选择 样品在纯水中溶解性较差,故分别采用 DMF、二甲基亚砜、0.08 mol/L的 NaOH溶液分别作为溶剂进行样品制备。结果显示,采用二甲基亚砜制备样品时产生较大的背景干扰;采用0.08 mol/L 的NaOH溶液时虽然背景干扰小,但由于待测溶剂中有酯类物质, NaOH 会影响其溶液的稳定性;采用DMF时背景干扰小,溶液稳定性好,且DMF 在15min 后出峰,不会干扰待测样品的检测,故选用DMF 作为样品制备溶剂。 2.2 方法学验证 使用优化后的条件进行方法学验证。由于石油醚组成比例没有确定性,《中国药典》将石油醚列为尚无足够毒理学资料的第4类溶剂。但石油醚中含有的正己烷组分在《中国药典》中为第2类溶剂,因此本文对于石油醚(60~90℃)的检测参考正己烷的限度规定。根据文献13],采用主成分峰面积加和法对石油醚(60~90℃)在药物中的残留进行定量计算,可以减少不同批号或者不同厂家来源的石油醚组分比例存在差异所导致的计算偏差,从而较好地满足对相关药物的质量控制要求,因此本文方法采用其所有峰的加和值和内标的比值进行定量计算。 2.2.1 系统适用性 以对照溶液为测试液,重复测定5次,分别计算7种溶剂的峰面积和内标峰面积之比的相对标准偏差(RSD)。结果显示 RSD 均不大于 5.0%,各组分峰的理论塔板数均不低于5000,相邻组分峰之间的分离度均大于2.0,系统适用性满足要求。 2.2.2 专属性 Equilibrium time / min 图2 (a)平衡温度、(b)加压时间、(c)平衡时间和峰面积的关系 Fig. 2 Relationships of (a) equilibrium temperature,(b) pressing time, (c) equilibrium time andthe peak area 1. petroleum ether (60-90℃); 2. acetone; 3. ethyl acetate;4. methyl alcohol; 5. dichloromethane; 6. ethyl alcohol; 7. n-butyl acetate. 对内标溶液和 DMF 制备的样品空白溶液进行测定。结果显示,内标溶液在7种残留溶剂峰的保留时间范围内没有干扰;样品空白溶液在内标峰的保留时间范围内也没有干扰, 按对照溶液中各溶剂浓度分别配制石油醚(60~90℃)、丙酮、乙酸乙酯、甲醇、二氯甲烷、乙醇、乙酸丁酯的单标准溶液,并进行测定。结果显示各组分中不含有干扰其他组分测定的杂质峰,本方法满足专属性要求。 2.2.3 线性范围、相关系数、检出限和定量限 配制含内标的6种不同质量浓度的混合标准溶 液,各溶剂的质量浓度范围如表1所示。采用内标法进行定量,以目标组分的峰面积与内标峰面积之比(y)对目标组分的质量浓度(c,mg/L)进行线性拟合,得到7种残留溶剂的线性方程、线性范围及相关系数。以 S/N≥3确定方法的检出限(LOD),以 S/N≥10确定方法的定量限(LOQ);其中石油醚(60~90℃)选择保留时间为2.06 min 的色谱峰。各残留溶剂的 LOD 为0.43~5.23 mg/L, LOQ 为1.25~16.67 mg/L(见表1)。方法的灵敏度满足样品定量分析及中国药典的限度要求。 表17种残留溶剂的线性方程、线性范围、相关系数、检出限及定量限 Table 1Regression equations, linear ranges, correlation coefficients, LODs and LOQs of the seven residual solvents Compound Regression equation Linear range/(mg/L) Correlation coefficient LOD/(mg/L) LOQ/(mg/L) Petroleum ether (60-90℃) y=1.1018x-0.7122 1.45-43.50 0.9993 0.48 1.45 Acetone y=0.1869xc+0.2593 1.25-750.00 0.9998 0.43 1.25 Ethyl acetate y=0.1354x-0.1994 2.50-750.00 0.9999 0.82 2.50 Methyl alcohol y=0.0675x+0.0499 5.00-450.00 0.9998 1.66 5.00 Dichloromethane y=0.0547xc-0.0698 6.00-90.00 0.9995 2.00 6.00 Ethyl alcohol y=0.0727xc+0.1160 5.00-750.00 0.9998 1.67 5.00 n-Butyl acetate y=0.0505sc-0.2602 16.67-750.00 0.9997 5.23 16.67 2.2.4 准确度与精密度 准确称取10份人工牛黄样品,分别添加高、中、低3种不同质量浓度的混合标准溶液,每种质量浓度平行制备3份,并制备一份不加混合标准溶液的样品溶液作为空白溶液进行扣除。计算加标回收率及 RSD,结果见表2。7种残留溶剂的平均回收率为94.7%~105.2%, RSD(n=9)均不大于3.5%。准确度满足平均回收率在 90%~110% 范围内,RSD(n=9)不大于5.0%的要求,表明本方法准确度良好。 表2 7种残留溶剂的加标回收率及 RSD(n=9) Table 2 Spiked recoveries and RSDs of the sevenresidual solvents (n=9) Compound Spiked/ Mean recoveries/ RSD/ (mg/L) % % Petroleum ether 1 1.45,229.00.43.50 99.3,98.5,102.5 3.2 (60-90℃) Acetone 1.25,500.00,750.00 94.7,98.1,97.5 Ethyl acetate 2.50,500.00,750.00 102.1,100.8,101.4 Methyl alcohol 5.00,300.00,450.00 99.1.,98.2,101.8 2.8 Dichloromethane 6.00, 60.00,90.00 98.3.,998.7.97.9 2.7 Ethylalcohol 5.00,500.00,750.00 104.9,102.2. 99.6 2.9 n-Butyl acetate 16.67,500.00,750.00 105.2, 99.0,998.9 3.5 重复性测试:由一位分析人员平行制备6份添加中等质量浓度混合标准溶液的加标样品溶液,按本方法进行检测,计算这6份溶液中7种残留溶剂分析结果的 RSD(n=6);中间精密度测试:由另一位分析人员在不同日期使用不同仪器,平行制备6份添加中等质量浓度混合标准溶液的加标样品溶液并进行检测,计算以上12份加标溶液中7种残留溶剂的 RSD(n=12)。结果见表3,各分析物的 RSD均不大于5%,说明本方法精密度良好。 2.2.5 溶液稳定性 分别将对照溶液避光存放于室温和冰箱2~8℃条件下,并于第2天、第3天进行测定,用新鲜配制的对照溶液作为参比计算回收率(见图3)。结果显示,各溶剂的回收率为95.2%~101.3%,均满足90%~110%范围内的要求,表明对照溶液避光保存在室温或冰箱2~8℃条件下3天内稳定。 表3 7种残留溶剂的精密度 Table 3 Precisions of the seven residual solvents Compound RSD/%(n=6) RSD/%(n=12) Petroleum ether (60-90℃) 2.8 2.5 Acetone 1.8 Ethyl acetate 2.3 Methyl alcohol Dichloromethane Ethyl alcohol n-Butyl acetate 0.7 2.2.6 耐用性 分别改变实验参数,采用进样平衡时间 25、35min , 顶空平衡温度75、85℃,进样口温度180、220℃,柱流量1.8、2.2 mL/min,以及使用不同批号的色谱柱对系统适用性进行测试,并对添加中等质量浓度混合标准溶液的加标样品溶液进行测定,计算回收率。结果显示,在改变后的条件下系统适用性仍能满足要求,加标溶液中7种残留溶剂的回收率为96.3%~102.1%,方法耐用性良好。 2.3 分析方法的应用 分别取3批人工牛黄(批号分别为20111205、120605、120806),采用本方法进行分析,结果见表4。3批人工牛黄均检出不同含量的丙酮(3.3~107.3mg/L)、甲醇(6.7~23.2 mg/L);2批中检出石油醚(60~90℃)(1.6~3.2 mg/L);1批中检出乙醇(30.2mg/L)。实验结果均未超过药典规定限度。 图3 7 种残留溶剂的溶液稳定性 Fig. 3 Solution stabilities of the 7 residual solvents a. room temperature;b. 2-8℃. 1. petroleum ether (60-90℃); 2. acetone; 3. ethyl acetate;4. methyl alcohol; 5. dichloromethane; 6. ethyl alcohol; 7. n-butyl acetate. 表4 3批样品中的残留溶剂含量 Table 4 Contents of residual solvents in threebatches of samples Batch Petroleum ether Acetone/ Methyl Ethyl (60-90℃)/ alcohol/ alcohol/ No. (mg/L) (mg/L) (mg/L) (mg/L) 20111205 3.3 120605 107.3 30.2 120806 41.8 23.2 -: not detected. 3 结论 本文建立了同时测定人工牛黄中石油醚(60~90℃)、丙酮、乙酸乙酯、甲醇、二氯甲烷、乙醇、乙酸 丁酯7种残留溶剂的顶空气相色谱分析方法,并进行了系统的方法学验证。方法的各项指标均可满足药物质量控制的方法学要求,且该方法灵敏、高效、快捷、稳定、简便,适用于人工牛黄中7种残留溶剂的同时检测,也可对其他类似残留溶剂的检测工作提供参考。 ( 参考文献: ) ( [ 1] Yang H W, Wang Z, Xi n M T, et al. Chinese Traditional Patent Medicine( 杨 洪武, 王 峥,辛敏通,等.中成药), 2003,25(4):290 ) ( [ 2 1 Luo X R, Cao H, Xing J B, et al. Pharmaceutical J o urnal of Chinese People's Liberation Army(罗 晓 茹,曹红,邢俊波, 等.解放军药学学报),2009,25(3):247 ) ( [ 3 ] Chinese Pharmacopoeia Commission. Chinese Pharmaco- poeia: Part Ⅱ. Beijing : China Medica l Scienc e Press (国家 药典委员会.中华人民共和国药典:2部.北京:中国医药科 技出版社),201 0 : Appendix 61 ) ( B’Hymer C. P harm Res, 2 003, 20(3):337 ) ( 1 4 1 Impurities: Guideline f or R esidual S olvents. I nternationalConference on Harmonisation of Technical Requirements fo r Registration of Pharmaceuticals for Human Use. 2009 ) ( P eng M, L i u J , Lu D , et a l .J Chromatogr Sci, 20 1 2, 50: 727 ) ( 1 6 . Saraji M , Khayamian T, Siahpoosh Z H, et al. A n al Meth- ods, 2012, 4: 1 552 ) ( [ 8 ] Fang Q X, Diao X L, Wan Q H, et al. Journal o f Instrumen- tal Analysis ( 方秋雪,刁兴利,万谦宏,等.分析测试学报), 2013,32(3):308 ) ( [ 9 ] Hu H L. Chinese Journal of Chromatography(胡慧廉 . 色 谱),2012,3 0 (1 ) : 99 ) ( [1 0] Xu Y H, Z hu B H, Zhong X H, et al. Ch i nese Jo u rnal of Chromatography (许瑛华,朱炳辉,钟秀华,等.色谱), 2010,28(1):73 ) ( [ 11] Lu Q , Z hang Q , Kang S Y , et al . Journal o f I n strumental Analysis (吕庆,张庆,康苏媛 , 等.分析测试学报),2011, 30(2):171 ) ( | 12 Liu Y M, G e N , Wang F, e t al. Chinese Journal of Chroma- tography(刘永明,葛娜,王飞,等.色 谱 ),2012,30(8): 782 ) ( [ 13] Li P, Chi Y H, C hen D Y. Chinese Journal of P h armaceuti- cal Analysis(李平,迟颖红,陈东英.药物分析杂志), 2008,28(3):427 )
确定


还剩3页未读,是否继续阅读?
成都科林分析技术有限公司为您提供《人工牛黄中二氯甲烷检测方案(顶空进样器)》,该方案主要用于原料药中限度检查检测,参考标准--,《人工牛黄中二氯甲烷检测方案(顶空进样器)》用到的仪器有AutoHS®自动顶空进样器
推荐专场
相关方案
更多
该厂商其他方案
更多
















