以克拉霉素为模型药物,通过液中干燥法制备克拉霉素-乙基纤维素微球,并用海藻酸钠进行包裹,最后壳聚糖包衣以增强微囊的生物粘附性能,制备出以乙基纤维素为核心材料,海藻酸钠、壳聚糖为包衣材料的克拉霉素-乙基纤维素-海藻酸钠-壳聚糖微囊。考察了影响微囊体外释药的因素及其在大鼠胃粘膜上的粘附性能。结果表明,克拉霉素-乙基纤维素-海藻酸钠-壳聚糖微囊不仅具有显著的缓释效果,且在大鼠胃粘膜上具有良好的粘附性能。
方案详情

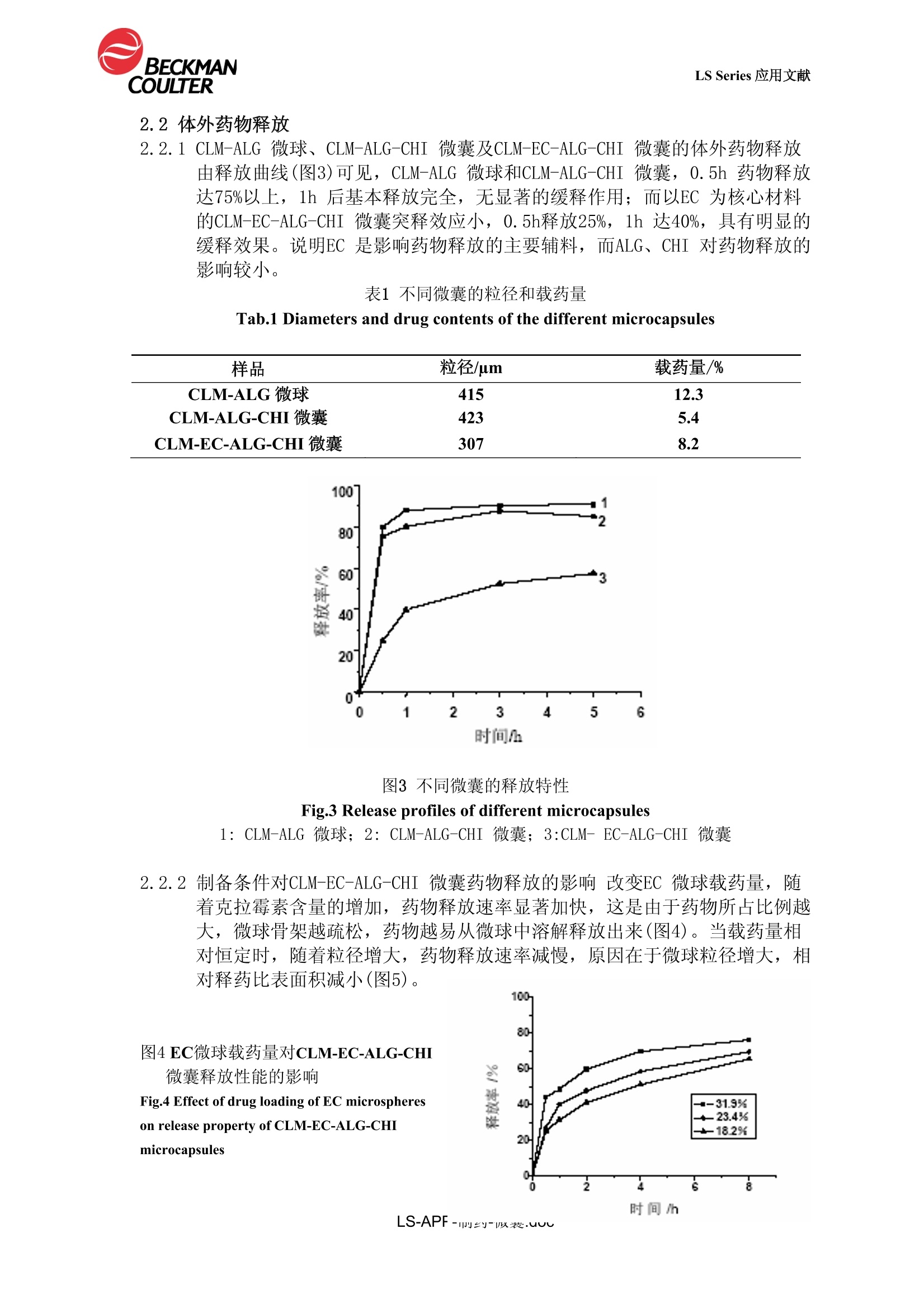
LS Series 应用文献化学通报2005年第68卷w106http://www.hxtb.org LS Series 应用文献 刘朝武1,2郑建华1,2包德才1,2赵燕军1,2王为1马小军1* (1 中国科学院大连化学物理研究所大连1160232中国科学院研究生院北京100039) 摘 要以克拉霉素为模型药物,通过液中干燥法制备克拉霉素-乙基纤维素微球,并用海藻酸钠进行包裹,最后壳聚糖包衣以增强微囊的生物粘附性能,制备出以乙基纤维素为核心材料,海藻酸钠、壳聚糖为包衣材料的克拉霉素-乙基纤维素-海藻酸钠-壳聚糖微囊。考察了影响微囊体外释药的因素及其在大鼠胃粘膜上的粘附性能。结果表明,克拉霉素-乙基纤维素-海藻酸钠-壳聚糖微囊不仅具有显著的缓释效果,且在大鼠胃粘膜上具有良好的粘附性能。 关键词微囊克拉霉素生物粘附乙基纤维素壳聚糖 Preparation and Characteristics of Bioadhesive Sustained-releaseMicrocapsules of Clarithromycin Liu Chaowu1,2, Zheng Jianhua1,2, Bao Decai1,2, Zhao Yanjun1,2Wang Wei1, Ma Xiaojun1* (1 Dalian Institute of Chemical Physics, Chinese Academy of Sciences Dalian 1160232 Graduate School of Chinese Academy of Sciences Beijing 100039) Abstract Clarithromycin-loading microcapsules which consist of ethylcellulose (EC)microcores were prepared by drying-in-liquid method and two layers coating withalginate and chitosan for the enhancement of bioadhesive property. The bioadhesion wasevaluated via counting the microcapsules retaining on the surface of gastric mucosa. Invitro drug release was also studied. The factors influencing the drug release includedparticle size of EC microspheres, drug loading of EC microspheres were discussed,respectively. The results showed that the microcapsules had obvious bioadhesiveproperty and sustained-release characteristic in pH5 acetate buffer medium. Key words Microcapsule, Clarithromycin, Bioadhesive, Ethylcellulose, Chitosan ( 刘朝武男,26岁,硕士生,现从事医用高分子与药物控释的研究。*联系人, E-mail: maxj@dicp. ac. cn 国家自然科学基金(20176056)、中国科学院知识创新工程领域前沿项目(K2002A2)资助 2005-01-25收稿,2005-05-13接受 ) 幽门螺旋杆菌(Helicobacter pylori, HP)寄生在胃粘膜特定区域,经若干年可在易感个体中引起慢性活动性胃炎、胃及十二指肠溃疡,甚至诱发恶性淋巴瘤[1]。HP 在我国普通人群中的感染率为30%~60%[2]。目前临床上的治疗方案主要采用三联疗法,即阿莫西林、克拉霉素两种抗生素和抑酸剂奥美拉唑, HP 杀伤率虽然达90%左右,但不能完全根除,导致病人治愈后易复发[3,4],主要原因是药物在胃中滞留时间太短,在粘膜层不能达到有效的杀菌浓度所致[5,6]。因此提高药物在胃内的滞留时间对完全根除HP有重要意义。目前已有文献报道了阿莫西林生物粘附微球,对蒙古沙土鼠体内的HP根除率达100%[7],而克拉霉素 (Clarithromycin, CLM)生物粘附微囊尚未见文献报道。 壳聚糖(chitosan, CHI)与胃肠道表面粘蛋白的相互作用,可延长其在胃肠道的滞留时间。上世纪末, Gaserod 等[8]报道了壳聚糖微囊在猪的胃粘膜上具有显著的生物粘附作用,为壳聚糖在生物粘附型口服定位释药制剂中的应用奠定了基础。 本文选用乙基纤维素(ethylcellulose,EC)为核心材料,壳聚糖为粘附材料,将克拉霉素制成生物粘附微囊,考察了影响其体外缓释效果的因素及粘附性能。 15实验部分 1.1材料和仪器 克拉霉素(浙江华义医药有限公司,批号040405);壳聚糖分子量6kD(自制);海藻酸钠(青岛市水产产业总公司);乙基纤维素(中国医药集团上海化学试剂公司);聚乙烯醇(中国医药集团上海化学试剂公司); Span80(中国医药集团上海化学试剂公司);其它化学试剂均为分析纯。 大功率微胶囊制备仪[9](自制); EUROSTAR digital 型数控搅拌器(德国IKA公司);LS-100Q型激光粒度仪(美国Beckman-Coulter 公司); CK40 型显微镜(日本Olympus公司); UV-2550IPC型紫外可见分光光度仪(日本岛津公司)。 1.2载药海藻酸钠-壳聚糖微囊的制备 1.2.1载药海藻酸钠(Alginate, ALG)微球(CLM-ALG 微球)的制备将一定量的克拉霉素与1.5%(W/V)的海藻酸钠溶液混合均匀,利用微胶囊制备仪,将该混悬液滴入1%(W/V)CaC12 溶液中进行凝胶化反应,形成CLM-ALG微球。 1.2.2载药海藻酸钠-壳聚糖微囊(CLM-ALG-CHI微囊)的制备配置0.5%(W/V)的壳聚糖溶液,加入1.2.1制备的CLM-ALG微球适量,反应成膜5 min 后过滤即得。 1.3载药乙基纤维素-海藻酸钠-壳聚糖微囊的制备 1.3.1载药乙基纤维素微球(CLM-EC微球)的制备将溶有一定量克拉霉素和乙基纤维素的二氯甲烷溶液滴入200mL 含1%(W/V) PVA的水溶液中,在室温下400r/min 搅拌,使温度逐渐升高至40℃搅拌4h,过滤,微球用去离子水洗涤3次,室温干燥即得。 1.3.2载药乙基纤维素-海藻酸钠微囊(CLM-EC-ALG 微囊)的制备取不同比例的乙基纤维素微球加入10mL 1.5%(W/V)的海藻酸钠溶液(含0.2g CaC03粉末)中,搅拌使其均匀分散后加入含2%(W/V)Span 80 的液体石蜡溶液中, 200r/min 搅拌15min,加入混有0.8mL 冰醋酸的5mL 液体石蜡,继续搅拌5min 过滤,依次用正己烷、去离子水洗涤3次。 1.3.载3药乙基纤维素-海藻酸钠-壳聚糖微囊(CLM-EC-ALG-CHI微囊)的制备配置0.5%(W/V)的壳聚糖溶液,加入制备的CLM-EC-ALG 微囊适量,成膜反应5min 后过滤即得。 1.4载药微囊载药量的确定 精密称取微囊适量(约相当克拉霉素10mg)于乳钵中研碎后放入100mL 容量瓶中,加入40mL甲醇,超声0.5h 后,加pH5 的醋酸缓冲液稀释至刻度,取10mL 用0.8Hm 滤膜过滤,取滤液4mL置于10mL容量瓶中,加硫酸溶液(75→100)4mL,混匀显色,冷却30min 后加醋酸缓冲液至刻度,摇匀,于482nm 波长处测定吸光度,由预先测定的标准曲线(Y=0.01793X-0.02800, r2=0.996)得药物含量,计算出微囊载药量。 1.5载药微球(囊)中CLM 体外释放的测定[10] 称取-一-定量微囊,置于一定体积的pH 为5的醋酸缓冲溶液中(37℃),以100r/min 的转速振荡,定时移取5mL 溶液(同时补充等温度等体积的释放介质),取4mL 置于10mL 容量瓶中,加硫酸溶液(75→100)4mL,混匀显色,冷却30min 后加醋酸缓冲液至刻度,摇匀,于482nm 波长处测定吸光度,由的标准曲线计算累积释放百分率。 1.6微胶囊体外粘附的测定[11] 将禁食供水饲养24h后的大鼠随机分为3组,处死后取胃,平铺于载物台上。分别取CLM-EC微球、CLM-EC-ALG 微胶囊及CLM-EC-ALG-CHI微胶囊各100粒,均匀撒在胃粘膜表面,置于于和氯化钠溶液的密闭容器中,保湿20min 后取出,使载物台呈45°斜角放置。用pH5醋酸缓冲液以流速22mL/min 冲洗5min,记录淋洗后分别保留在胃粘膜组织上的微囊个数,获取滞留率。 2结果与讨论 2.1微胶囊的形态 由液中干燥法制备的CLM-EC 微球为白色球体,外形圆整,大小较均匀,无粘连(图1);粒度仪测得平均粒径为205.4um,标准偏差为1.330。 CLM-EC-ALG-CHI 微囊内含1~3个CLM-EC微球,球形度较好(图2),制备的CLM-EC-ALG-CHI 微囊最高载药量可达16.9%。 图1 CLM-EC 微球显微镜照片(40×) 图2 CLM-EC-ALG-CHI微囊显微镜照片(40×) 2.2体外药物释放 2.2.1 CLM-ALG 微球、CLM-ALG-CHI 微囊及CLM-EC-ALG-CHI 微囊的体外药物释放由释放曲线(图3)可见, CLM-ALG 微球和CLM-ALG-CHI 微囊,0.5h 药物释放达75%以上, 1h 后基本释放完全,无显著的缓释作用;而以EC 为核心材料的CLM-EC-ALG-CHI 微囊突释效应小,0.5h释放25%,1h 达40%,具有明显的缓释效果。说明EC是影响药物释放的主要辅料,而ALG、CHI对药物释放的影响较小。 表1不同微囊的粒径和载药量 Tab.1 Diameters and drug contents of the different microcapsules 样品 粒径/pm 载药量/% CLM-ALG微球 415 12.3 CLM-ALG-CHI 微囊 423 5.4 CLM-EC-ALG-CHI 微囊 307 8.2 6 图3不同微囊的释放特性 Fig.3 Release profiles of different microcapsules 1: CLM-ALG 微球;2: CLM-ALG-CHI微囊;3:CLM- EC-ALG-CHI 微囊 2.2.2制备条件对CLM-EC-ALG-CHI 微囊药物释放的影响改变EC 微球载药量,随着克拉霉素含量的增加,药物释放速率显著加快,这是由于药物所占比例越大,微球骨架越疏松,药物越易从微球中溶解释放出来(图4)。当载药量相对恒定时,随着粒径增大,药物释放速率减慢,原因在于微球粒径增大,相对释药比表面积减小(图5)。 图4EC微球载药量对CLM-EC-ALG-CHI微囊释放性能的影响 ( Fig.4 Effect of drug loading of EC microsphereson release property of CLM-EC-ALG-CHImicrocapsules ) 时间/h 100- 图5 EC 微球粒径对CLM-EC-ALG-CHI微囊释放性能的影响 Fig.5 Effect of particle diameter of ECmicrospheres on release property of CLM-EC-ALG-CHI microcapsules 2.3微胶囊粘附性能 不同微球(囊)在离体大鼠胃粘膜上的体外粘附实验表明, CLM-EC 微球在胃粘膜滞留率为37%,经ALG包衣后的CLM-EC-ALG 微囊在胃粘膜滞留率提高至62%。CLM-EC-ALG 微囊与CHI 成膜后形成的CLM-EC-ALG-CHI 微囊在胃粘膜滞留率可达89%(表2)。 表2不同微囊在离体大鼠胃粘膜上的滞留率 Tab.2 The retaining of different microcapsules on the gastric mucosa in vitro (n=3) 类型 EC 微求 EC-ALG 微囊 EC-ALG-CHI 微囊 滞留率/% 37±5 62±7 89±4 3结论 CLM-EC-ALG-CHI 微囊对药物具有显著的缓释效果,药物释放持续时间可达8h以上;随EC 微球载药量的增加,释药速率加快;随EC微球粒径的增大,释药速率减慢。同时CLM-EC-ALG-CHI微囊在大鼠胃粘膜上具有良好的粘附性能,其滞留率达89%,比EC 微球高52%。 ( 参考文献 ) ( [1]黄静琳,陆锦芳.药学学报,2002, ,3 37(3):226~228. ) 潘国宗.中国消化杂志,2002,20(3):194~198.CCK Lin, P I Hsu, .K H Lai. J. Clin. Gastroenterol, 2002,,334(5): 547~551. ( [4] E Kawabami, S K Ogata, A C P ortorreal. A rq. Gastroenterol, 2001, 38(3):203 ~ 206. ) [5]M P Cooreman, lP Krausgrill, K J Hengels, Antimicrob. Agents. (Chemother, 1993,37:1506~1509. [66]JJ C Atherton, A Cockayne, M Balsitis et al. Gut,,11995, 36: 670~674. [7]N Nagahara,YY Akiyama, M Nakao et al. Antimicrob Agents Chemother, 1998,,442(10):2492~2494. ( [8]O Gaserod, ,J I G J olliffe, F C Hampson et al. Int. J. Pharm., 1998, 175(2):237 ~ 246. ) [9]任吉伦,马小军,何洋.中国专利, ZL 00 253 538.6[P],2000. ( [10]国家药典委员会编.中华人民共和国药典(二部).2000:271~271. ) ( [11] Y Akiyama, N Nagahara, T Kashihara et al. Pharm. Res., 1 995, 12(3): 397~405. ) http://www.hxtb.org 化学通报第 wS-APP-制药-微囊.doc LS-APP-制药-微囊.doc
确定





还剩4页未读,是否继续阅读?
贝克曼库尔特国际贸易(上海)有限公司为您提供《克拉霉素生物粘附缓释微囊中制备及性能检测方案(激光粒度仪)》,该方案主要用于化药制剂中理化性质检测,参考标准--,《克拉霉素生物粘附缓释微囊中制备及性能检测方案(激光粒度仪)》用到的仪器有
相关方案
更多









