
方案详情
文
"文章介绍采用AA600对鸡蛋中六价铬进行了分析,结果:测试液中Cr(Ⅵ)浓度在0.001~0.010mg/L 内呈良好线性关系,线性回归系数为0.9997。鸡蛋样品中Cr(Ⅵ)不同加入量的平均回收率在75%~96%;相对标准偏差在3.5%~11.5%;最低定量限为0.3μg/L。"
方案详情

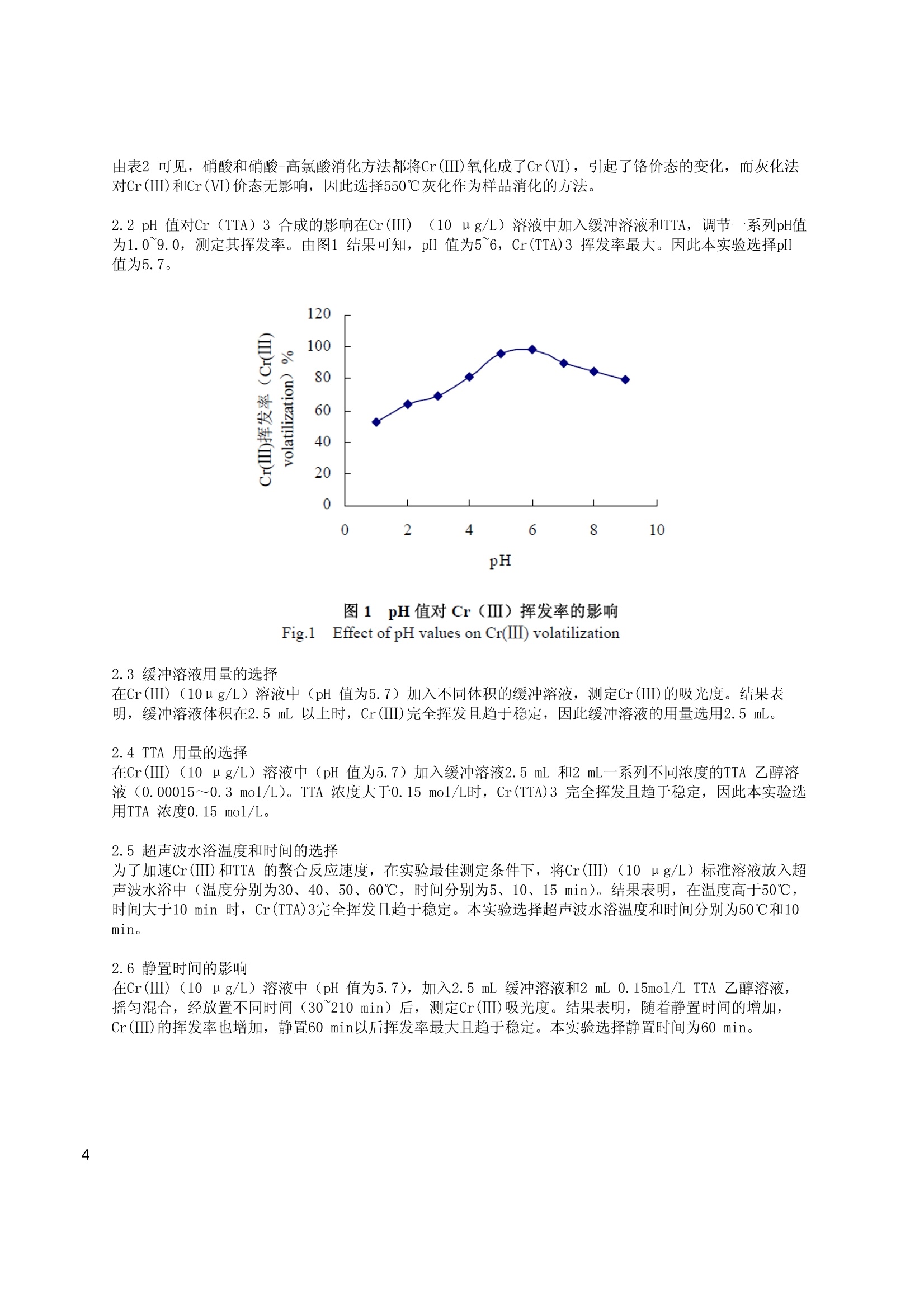
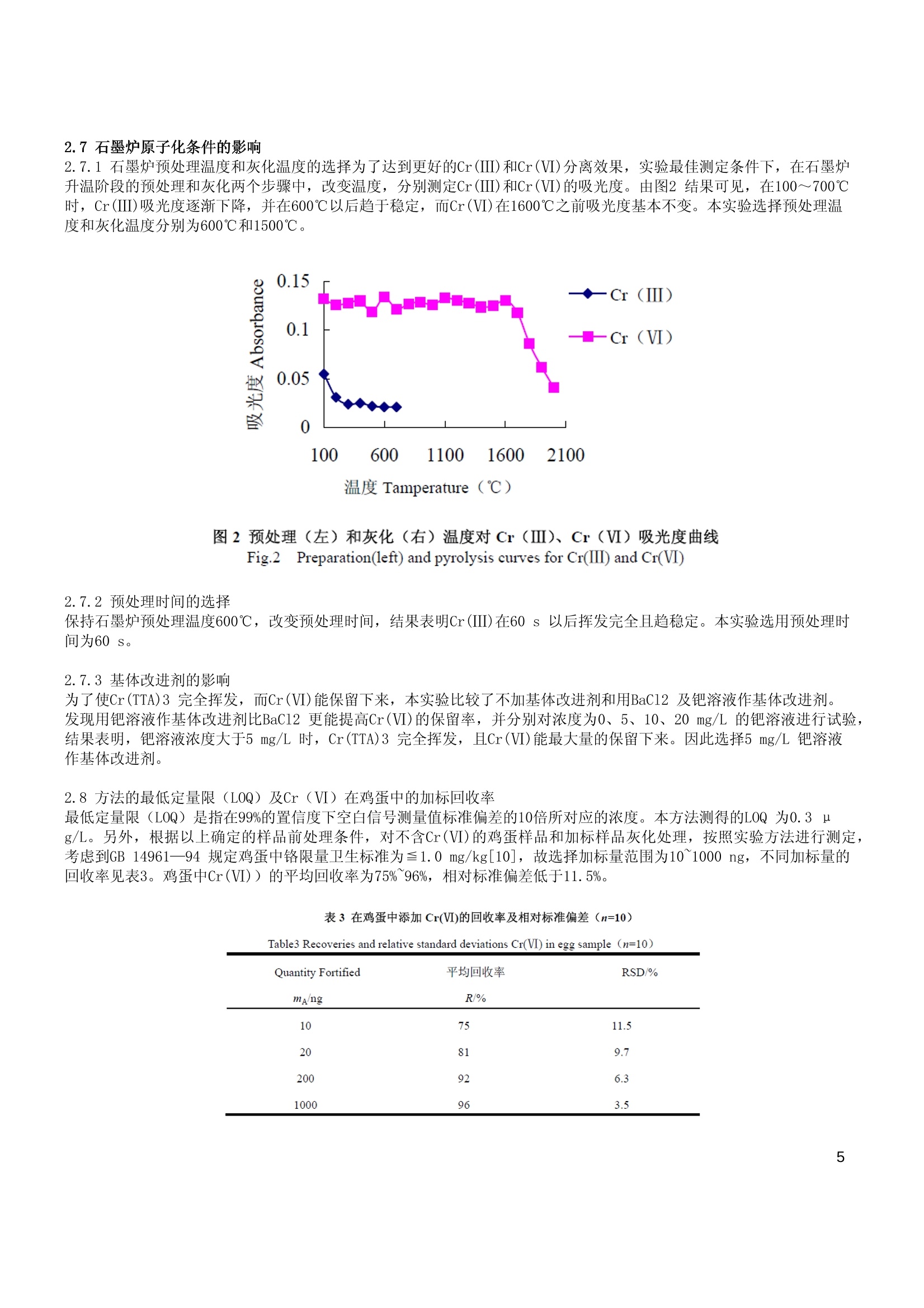
Cr (TTA)3挥发-石墨炉原子吸收光谱法直接测定鸡蛋中六价铬 摘要 基于 Cr(III)与噻吩甲酰三氟丙酮(TTA)生成的络合物在石墨炉中的挥发性,建立了一种前处理简单、灵敏度高的测定鸡蛋中六价铬的分析方法。研究了鸡蛋样品的消化方式、Cr(ⅢI)与 TTA 络合的反应酸度、各种试剂的加入量、超声波水浴的温度和时间、静置时间等条件,并对石墨炉挥发 Cr(III)的原子化条件进行了探讨。测试液中 Cr(ⅥI)浓度在 0.001~0.010mg/L 内呈良好线性关系,线性回归系数为0.9997。鸡蛋样品中 Cr(V)不同加入量的平均回收率在75%~96%;相对标准偏差在 3.5%~11.5%;最低定量限为0.3ng/L。 食品中的微量元素与人体健康密切相关。研究表明,三价铬的生物学功能主要是作为胰岛素的强化剂,可激活胰岛素,参与机体糖、脂肪、蛋白质的代谢,能增强胆固醇的分解和排泄,防止动脉硬化,促进氨基酸的转运和蛋白质的合成,促进人体的生长发育。而六价铬通过毒理学研究已被证明是致癌物,因此只有分 别测定出食品中的三价铬和六价铬,才能对其营养与安全做出正确的评价。 目前国内外测定六价铬的分析方法主要有:原子吸收法(AAS)[1-2]、吸光光度法[3]、高效液相色谱法(HPLC)[4]、电感耦合等离子体原子发射光谱法(ICP-AES)[5]、电感耦合等离子体质谱法(ICP-MS)[6]和流动注射与质谱谱用(FI-MS)[7]等。这些方法多数都是在试样前处理阶段分离三价铬和六价铬,分离操作繁琐,,且易引起样品丢失或污染。 R. Moshier[8]对乙化丙酮化合物(ACAC)、三氟乙酰丙酮(TFA)和六氟乙酰丙酮(HFA)的挥发性进行了详细报道,而 Y. An[9]提出了利用 Cr(TFA)3 在石墨炉内挥发分离三价铬而直接测定六价铬的方法。另外,由于富铬蛋中三价铬含量较高,对铬卫生学评价有实际意义,而且鸡蛋基质较复杂,在各类食品中具有代表 性。本实验选择富铬蛋为测试样品,建立了一种鸡蛋中六价价形态分析的的方法。 1实验部分 1.1主要仪器 AA600 石墨炉原子吸收分光光度计附AS-800 自动进样器 (美国PerkinElmer公司); Mp220 酸度计(瑞士Mettler 公司);300型超声波水浴器(美国Ney 公司)。 1.2工作条件 灯电流25 mA, 波长357.9 nm, 光谱通带宽度0.7 nm, 进样体积20uL,氩气流量300 mL/min, 原子化时停气,测定峰面积。石墨炉参数见表1。 表1石墨炉参数(Cr(ⅥI)的测定) Table 1 Graphite furnace program for Cr(VI) determination Step Temperation/℃ Ramp time/s Hold time/s Dry 110 1 20 Preparation 600 15 60 Pyrolysis 1500 10 20 Atomization 2400 0 5 Clean 2600 1 3 1.3试剂 Cr(ⅢI)标准溶液:1 mg/mL Cr(Ⅲ)标准溶液(国家标准物质中心);; 1 mg/mLCr(Ⅵ)标准溶液:称取0.093 gK2Cr207(99.8%,分析纯,天津市天大化工实验厂),以去离子水溶解并定容至25mL 容量瓶中;噻吩甲酰三氟丙酮(TTA,进口分装)0.15 mol/L 乙醇溶液;硝酸钯溶液:称取300 mg钯(99.999%)用1mL 优级纯硝酸溶解,然后用去离子水稀释至100 mL;缓冲溶液:0.1 mol/L 乙酸钠和0.1 mol/L乙酸混合,调pH值至5.7。 1.4测定步骤 1.4.1样品的灰化 用玻璃棒打碎鲜蛋蛋壳,蛋黄、蛋清一并倒入均浆机,快速打成匀浆。准确称取1.0g(精确至0.0001 g)样品于埚中,加2mL 优级纯盐酸,浸泡1h以上,将甘埚于电热板上,小心蒸干,炭化至不冒烟为止,转至马马炉,550℃恒温2 h,取出冷却加数滴浓HCl,再灰化至白灰状,取出放冷。 1.4.2 Cr(TTA)3 螯合物的合成 将灰化好的样品用去离子水溶解于10 mL容量瓶中,加入缓冲溶液2.5 mL, 调pH值至5.7,再加入0.15 mol/LTTA 乙醇溶液2 mL,定容至10mL,超声波水浴(50℃)10 min 后,取出静置1 h。 1.4.3工作曲线的绘制 在一系列10mL容量瓶中加入一定量的Cr(ⅥI)标准溶液、2 mL 0.15 mol/L TTA乙醇溶液、5 mL 缓冲溶液,用去离子水定容,配成浓度为0.001、0.002、0.004、0.008、0.010 mg/L 的标准系列,按表1的石墨炉升温程序来测定吸光度,绘制工作曲线。 1.4.4样品测定 将处理好的样品在1.2节条件下按表1中石墨炉升温程序来测定样品中Cr(ⅥI)的吸光度,由工作曲线求出浓度,换算成鸡蛋中Cr(Ⅵ)的含量。 2结果与讨论 2.1消化方式的选择 分别以硝酸、硝酸-高氯酸(1:4)、550℃灰化等消化方式来处理定量的Cr(ⅢI)、Cr(Ⅵ)混合标准溶液和样品加Cr(III)、Cr(Ⅵ)混合标准溶液,按1.4步骤来测定,并根据工作曲线计算浓度,结果见表2。 表2 几种样品消化方式对测定结果的影响 Table 2 Effect of sample digestion on detection result 标准溶液 消解方式 测定值p (ugL) Cr(III) (5 pg/L)+ HNO: 9.8 HNO3-HCLO4 9.7 Cr(VI) (5 pg/L) 550℃ Pyrolysis 5.2 样品+Cr(Ⅲ) (5 ug /L)+Cr(VI) HNO: 11.9 HNO3-HCLO4 12.3 (5 pg/L) 550℃Pyrolysis 7.4 由表2可见,硝酸和硝酸-高氯酸消化方法都将Cr(ⅢI)氧化成了Cr(ⅥI),引起了铬价态的变化,而灰化法对Cr(ⅢI)和Cr(Ⅵ)价态无影响,因此选择550℃灰化作为样品消化的方法。 2.2 pH 值对Cr (TTA)3合成的影响在Cr(Ⅲ) (10 ng/L) 溶液中加入缓冲溶液和TTA,调节一系列pH值为1.0~9.0,测定其挥发率。由图1结果可知, pH 值为5~6, Cr(TTA)3挥发率最大。因此本实验选择pH值为5.7。 图111pH 值对Cr (Ⅲ)挥发率的影响 Fig.1Effect of pH values on Cr(ⅢII) volatilization 2.3缓冲溶液用量的选择 在Cr(Ⅲ)(10ug/L) 溶液中(pH 值为5.7)加入不同体积的缓冲溶液,测定Cr(ⅢI)的吸光度。结果表明,缓冲溶液体积在2.5 mL 以上时, Cr(ⅢI)完全挥发且趋于稳定,因此缓冲溶液的用量选用2.5 mL。 2.4 TTA 用量的选择 在Cr(Ⅲ)(10 ug/L)溶液中(pH值为5.7)加入缓冲溶液2.5mL 和2mL一系列不同浓度的TTA 乙醇溶液(0.00015~0.3 mol/L)。 TTA 浓度大于0.15 mol/L时, Cr(TTA)3 完全挥发且趋于稳定,因此本实验选用TTA 浓度0.15 mol/L。 2.5超声波水浴温度和时间的选择 为了加速Cr(ⅢII)和TTA 的螯合反应速度,在实验最佳测定条件下,将Cr(ⅢI)(10ug/L)标准溶液放入超声波水浴中(温度分别为30、40、50、60℃,时间分别为5、10、15 min)。结果表明,在温度高于50℃,时间大于10 min 时,Cr(TTA)3完全挥发且趋于稳定。本实验选择超声波水浴温度和时间分别为50℃和10min。 2.6静置时间的影响 在Cr(Ⅲ) (10 ug/L)溶液中(pH 值为5.7),加入2.5 mL 缓冲溶液和2 mL 0.15mol/L TTA 乙醇溶液,摇匀混合,经放置不同时间(30~210 min) 后, 测定Cr(I)吸光度。结果表明,随着静置时间的增加,Cr(III)的挥发率也增加,静置60 min以后挥发率最大且趋于稳定。本实验选择静置时清为60 min。 2.7石墨户原子化条件的影响 2.7.1石墨炉预处理温度和灰化温度的选择为了达到更好的Cr(II)和Cr(Ⅵ)分离效果,实验最佳测定条件下,在石墨炉升温阶段的预处理和灰化两个步骤中,改变温度,分别测定Cr(ⅢI)和Cr(Ⅵ)的吸光度。由图2结果可见,在100~700℃时, Cr(ⅢII)吸光度逐渐下降,并在600℃以后趋于稳定,而Cr(Ⅵ)在1600℃之前吸光度基本不变。本实验选择预处理温度和灰化温度分别为600℃和1500℃。 图2预处理(左)和灰化(右)温度对 Cr (Ⅲ)、Cr(Ⅵ)吸光度曲线 Fig.2 FPreparation(left) and pyrolysis curves for Cr(Ⅲl) and Cr(VI) 2.7.2预处理时间的选择 保持石墨炉预处理温度600℃,改变预处理时间,结果表明Cr(Ⅲ)在60 s 以后挥发完全且趋稳定。本实验选用预处理时间为60 s。 2.7.3基体改进剂的影响 为了使Cr(TTA)3完全挥发,而Cr(Ⅵ)能保留下来,本实验比较了不加基体改进剂和用BaCl2及钯溶液作基体改进改。发现用钯溶液作基体改进剂比BaCl2 更能提高Cr(Ⅵ)的保留率,并分别对浓度为0、5、10、20 mg/L 的钯溶液进行试验,结果表明,钯溶液浓度大于5 mg/L 时, Cr(TTA)3完全挥发,且Cr(Ⅵ)能最大量的保留下来。因此选择5 mg/L 钯溶液作基体改进剂。 2.8方法的最低定量限(LOQ)及Cr(Ⅵ)在鸡蛋中的加标回收率 最低定量限(LOQ)是指在99%的置信度下空白信号测量值标准偏差的10倍所对应的浓度。本方法测得的LOQ为0.3 pg/L。另外,根据以上确定的样品前处理条件,对不含Cr(Ⅵ)的鸡蛋样品和加标样品灰化处理,按照实验方法进行测定,考虑到GB 14961—94 规定鸡蛋中铬限量卫生标准为≤1.0 mg/kg[10],故选择加标量范围为10~1000 ng, 不同加标量的回收率见表3。鸡蛋中Cr(Ⅵ))的平均回收率为75%~96%,相对标准偏差低于11.5%。 表3 在鸡蛋中添加Cr(Ⅵ)的回收率及相对标准偏差(n=10) Table3 Recoveries and relative standard deviations Cr(VI) in egg sample (n=10) Quantity Fortified 平均回收率 RSD/% ma/ng R/% 10 75 11.5 20 81 9.7 200 92 6.3 1000 96 3.5 ( 3参考文献 ) ( [1 ] Sahayam A C . Sperciation of Cr(ⅢII) and Cr(ⅥI)in Potable W a ters by using Activated Neutral Alumina as Collector a nd E T-AAS f or D etermination [ J ]. A nal B ioanal Chem, 2 0 02, 372:840-842. ) ( [2 ] 袁建,杨晓蓉,浮东宝,等 . 食品中品(Ⅲ)与铬(Ⅵ)分析方法的探讨[J].中国粮油学报,1999,14(4):59-62. ) ( [3 ] 谢华林. 二 苯碳碳二肼吸光光度法测定水中铬(Ⅵ)[J].理化检验:化学分册, 2 003,39(6):362-364. ) ( [4] J.F. Jen, G. L. O u -Yang , C.S . Chen, et al . Simultaneous Determination of Chromium (Ⅲ) and Chromium (VI) with R eversed-phase I o n-pair H i gh-Performance Liquid Ch r omatography[J].Analyst, 1993, , 118:1281-1284. ) ( [5] 范哲锋.活性氧化铝微柱分离富集-电感耦合等离子体原子发射光谱法在线测定水中铬(Ⅲ)和铬(Ⅵ) [J].分析化 学,2 0 03, 3 1(9):1 0 73-1075. ) ( [6] Balarama Krishna M V, Chandrasekaran K, Sarva V Rao, et al. Speciation of Cr (Ⅲ) a nd Cr( Ⅵ ) inWaters using Immobilized Moss and D etermination b y I CP- M S a nd F AAS [J]. Tanata, 2005,65:135-1 4 3. ) ( [7] Zoorob G, TomLinson M, l, W ang J S , et a l. Evaluation o f t h e D i rect I n jection Ne b ulizer in the Co u pling of High Performance Liquid Chromatography t o Inductively C oupled P lasma Mass Spectrometry [J]. J Anal At Spectrom,1995.10: 8 53-858. ) ( [8] Moshier R, S ievers R . Gas Chromatography of Metal Chelates [M]. New York: Pergamon Pr e ss,1965. ) ( [9] An Y, Willie S N, Sturgeon R E. I n S itu C oncentration o f Volatil e Chromium I β -diketonate f or t he Determination of GFAAS[J]. F resenius J A nal C hem, 1992,344: 6 4-65. ) ( [10] GB 14961—94,食品中铬限量卫生标准,中华人民共和国国家标准[S] ) PerkinElmer, Inc. 大中华区总部 地址:上海张江高科园区李冰路67弄4号邮编:201203 电话: (021) 38769510 传真: (021)38791316 www.perkinelmer.com.cn ( .要获取全球办事处的完整列表,请访问 http://w ww.perkinelmer.com.cn/AboutUs/ContactUs/ContactUs ) ( C2 009 PerkinElm e r , Inc. 保 留所有权利。Pe rkinElmer 徽 标 和外观设计是P e r ki n Elm e r的注册商 标 。文中提 及的其它非Perk i n Elmer 及其 子公 司所 有的其它商标 均 为其 各 自所 有 者 的财 产。 ) ( P e rkin E l mer 保 留 随 时更改此文档的权 利 , 恕 不另行 通 知。对于编辑、图 片 或排版错误概不 承担任何 责任。 ) PerkinElmerFor the Better "文章介绍采用AA600对鸡蛋中六价铬进行了分析,结果:测试液中Cr(Ⅵ)浓度在0.001~0.010mg/L 内呈良好线性关系,线性回归系数为0.9997。鸡蛋样品中Cr(Ⅵ)不同加入量的平均回收率在75%~96%;相对标准偏差在3.5%~11.5%;最低定量限为0.3μg/L。"
确定



还剩4页未读,是否继续阅读?
珀金埃尔默企业管理(上海)有限公司为您提供《鸡蛋中6价铬检测方案(原子吸收光谱)》,该方案主要用于蛋制品中重金属检测,参考标准--,《鸡蛋中6价铬检测方案(原子吸收光谱)》用到的仪器有原子吸收光谱仪PerkinElmer PinAAcle 900
推荐专场
该厂商其他方案
更多














