
辅料是生物制剂中的重要组成部分,其组成和含量影响蛋白类药物的稳定性和安全性,并在一定程度上影响着药物的治疗效果。例如,糖和麦芽糖的含量影响蛋白药物的蓬松程度和复溶效果。吐温(吐温 20 或 80)的含量影响蛋白药物的溶解性和稳定性。蛋白药物中吐温(吐温 20 或 80)浓度过低无法实现助溶的作用,浓度过高将引起溶血等副作用。PEG 是常见的蛋白药物修饰剂,残留的 PEG 影响蛋白药物的安全性。盐酸胍是蛋白增溶剂,残留的胍离子影响蛋白的安全性和有效性。辅料含量的高低对蛋白药物的有效性和安全性有明显的影响,但中国药典和药用辅料手册均未提供蛋白药物中辅料的含量测定方法。因此,急需建立蛋白药物中药用辅料的含量测定方法。
方案详情

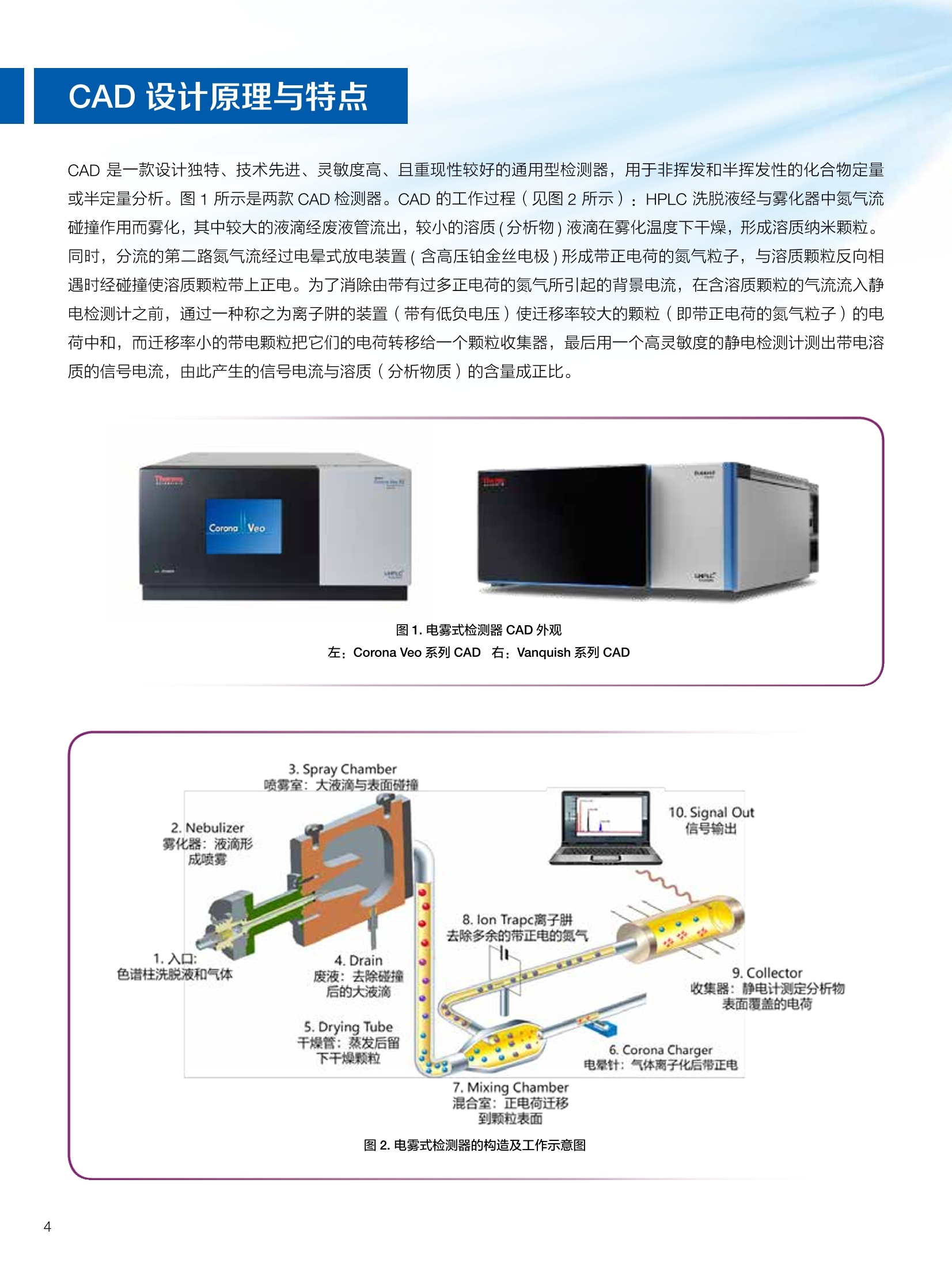
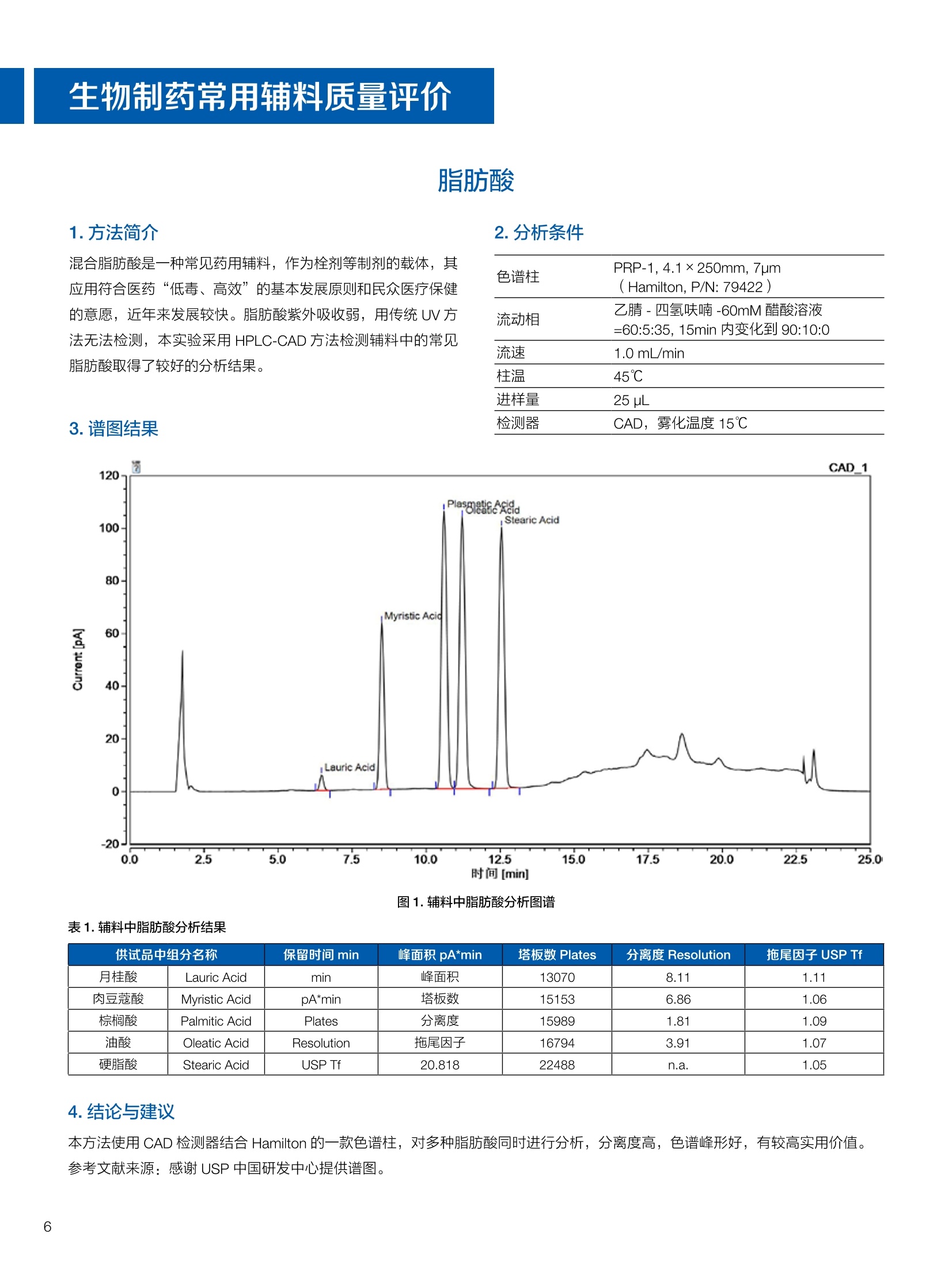
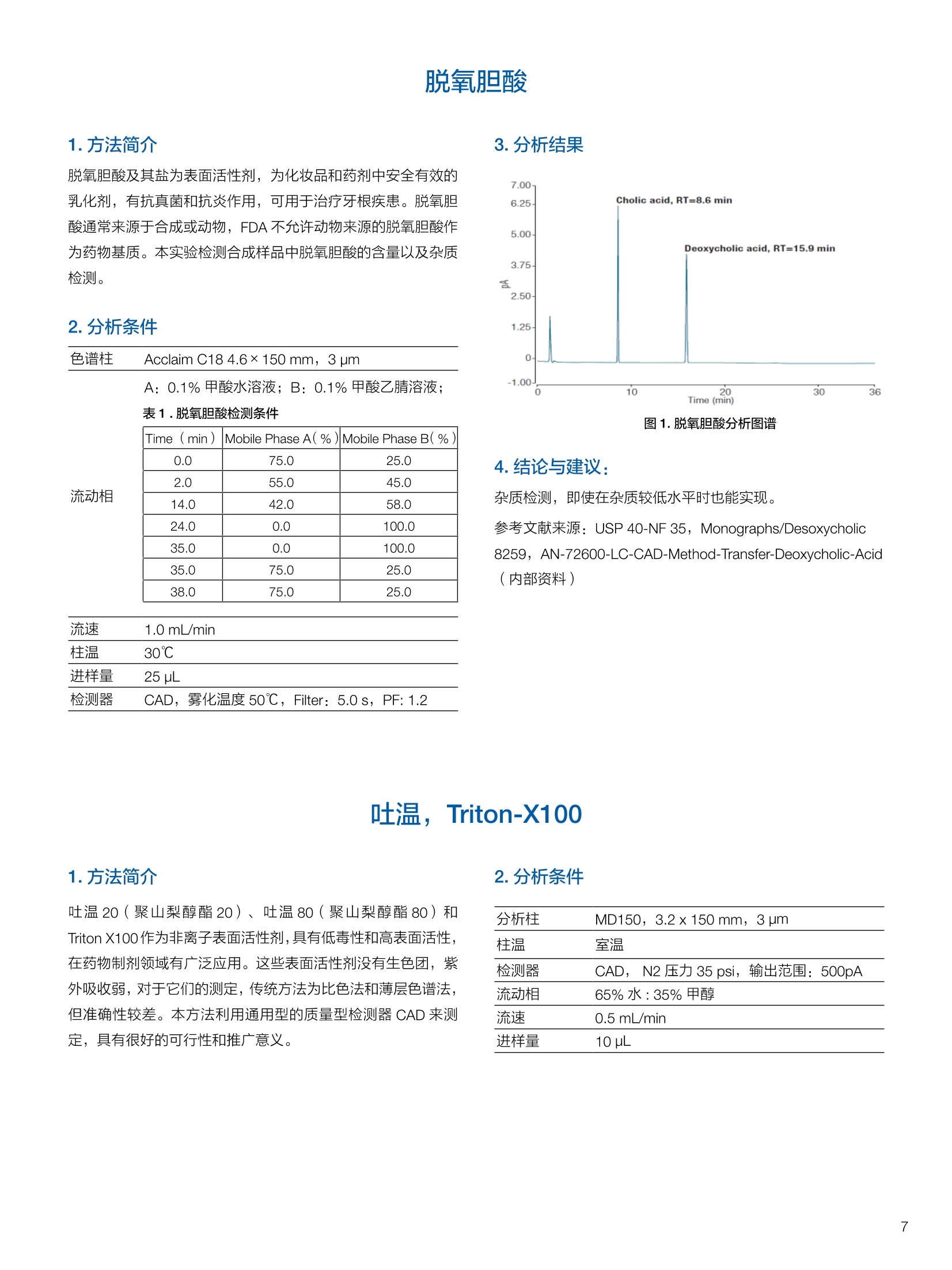
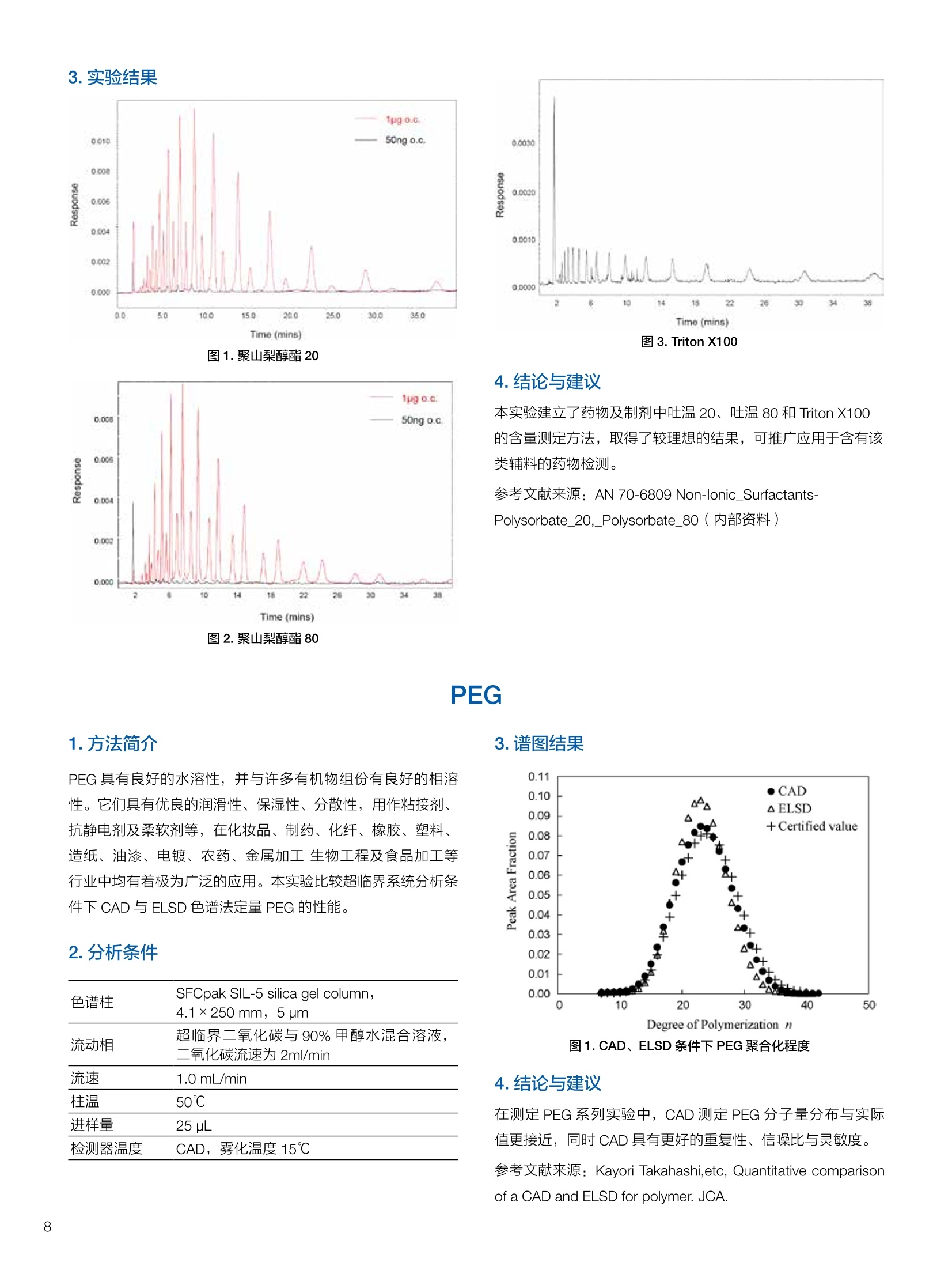
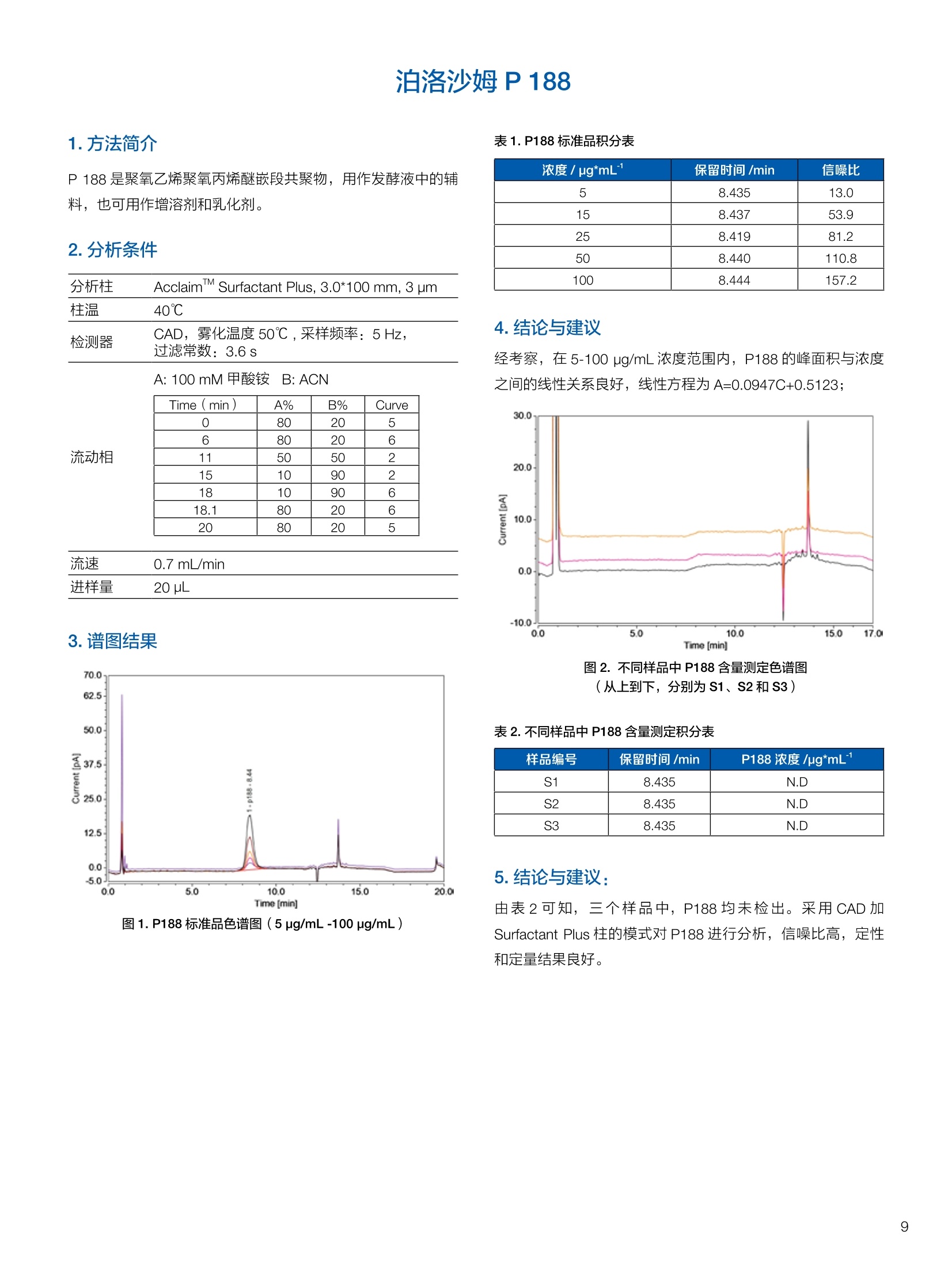
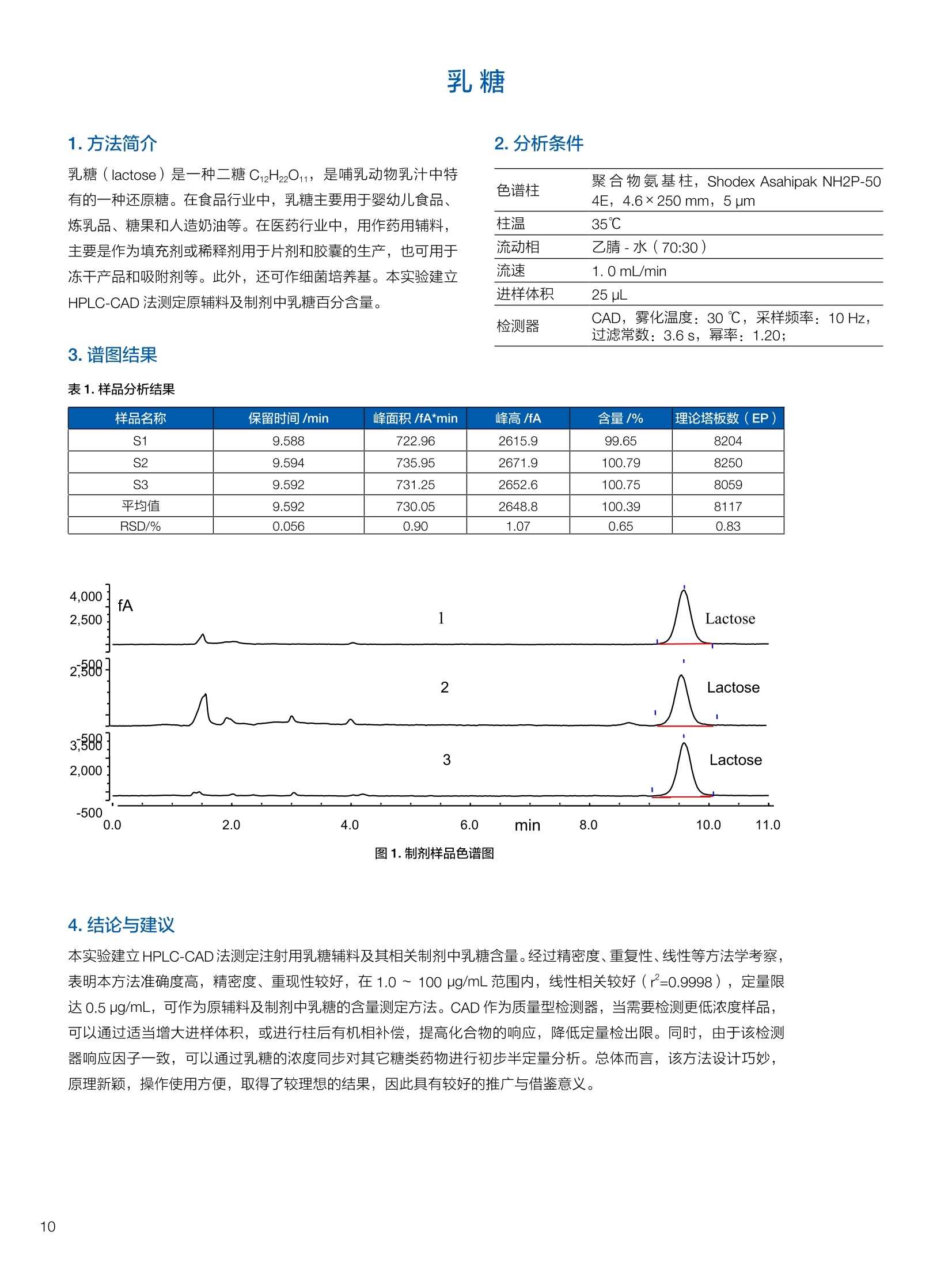
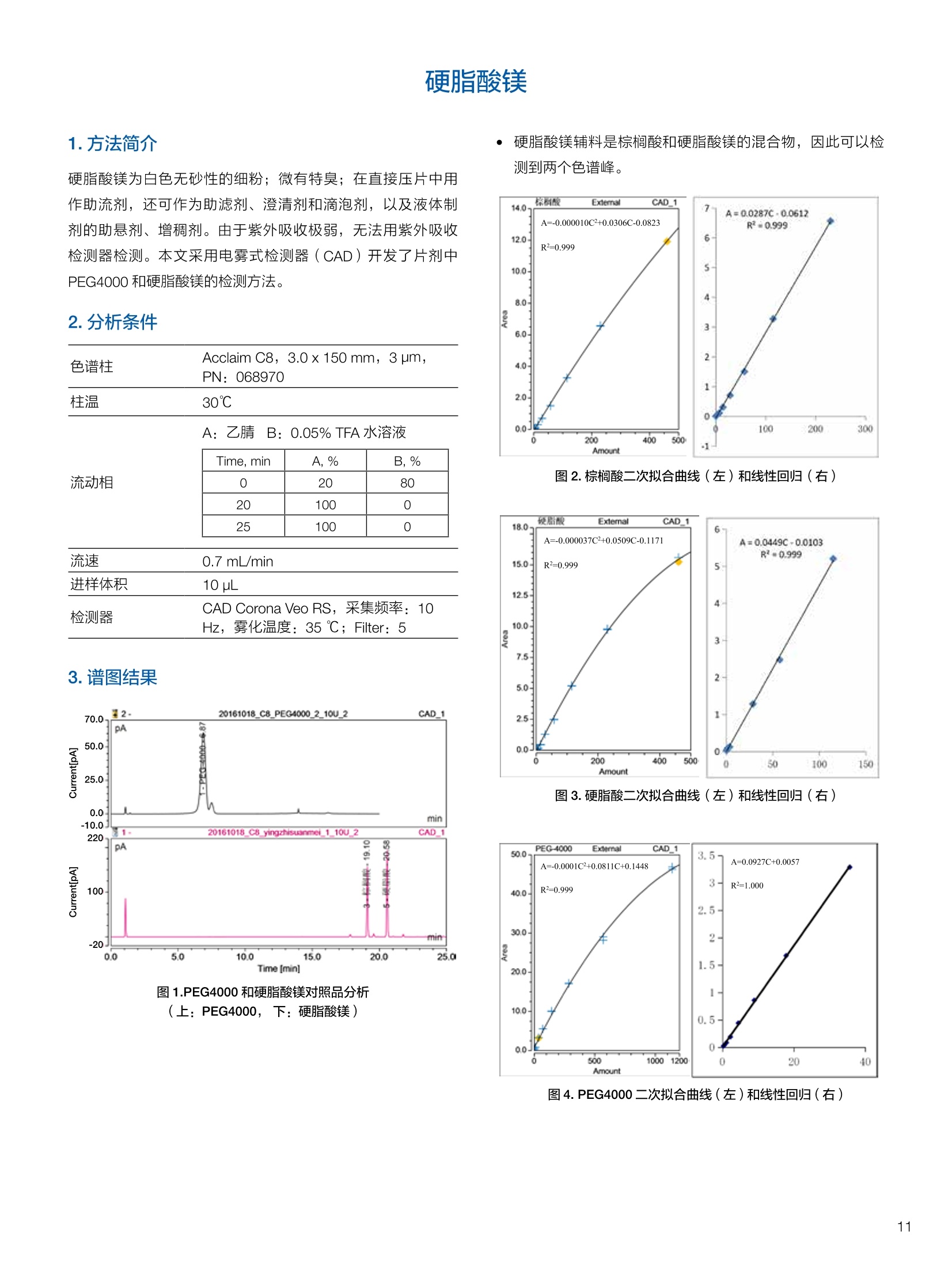
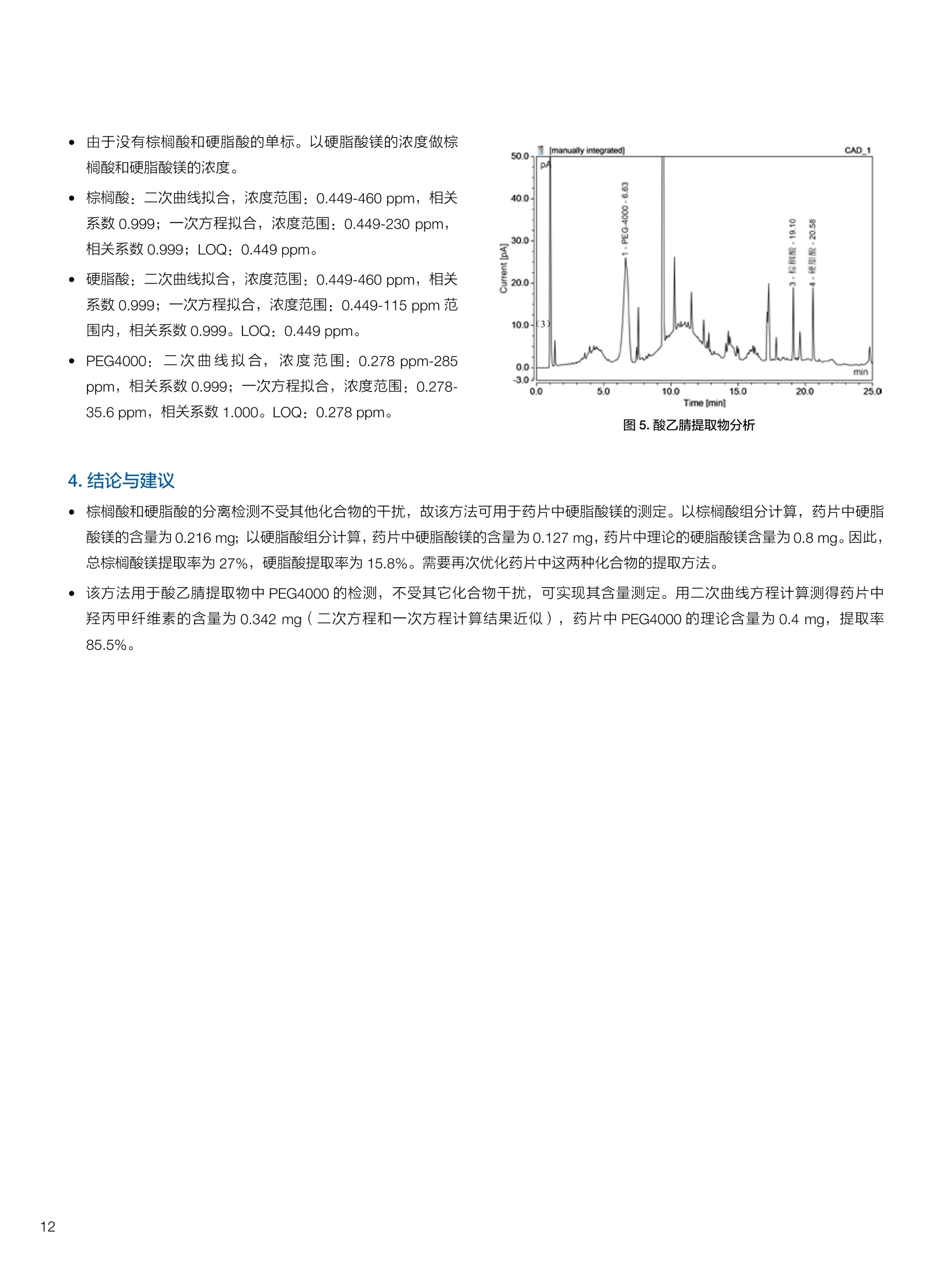
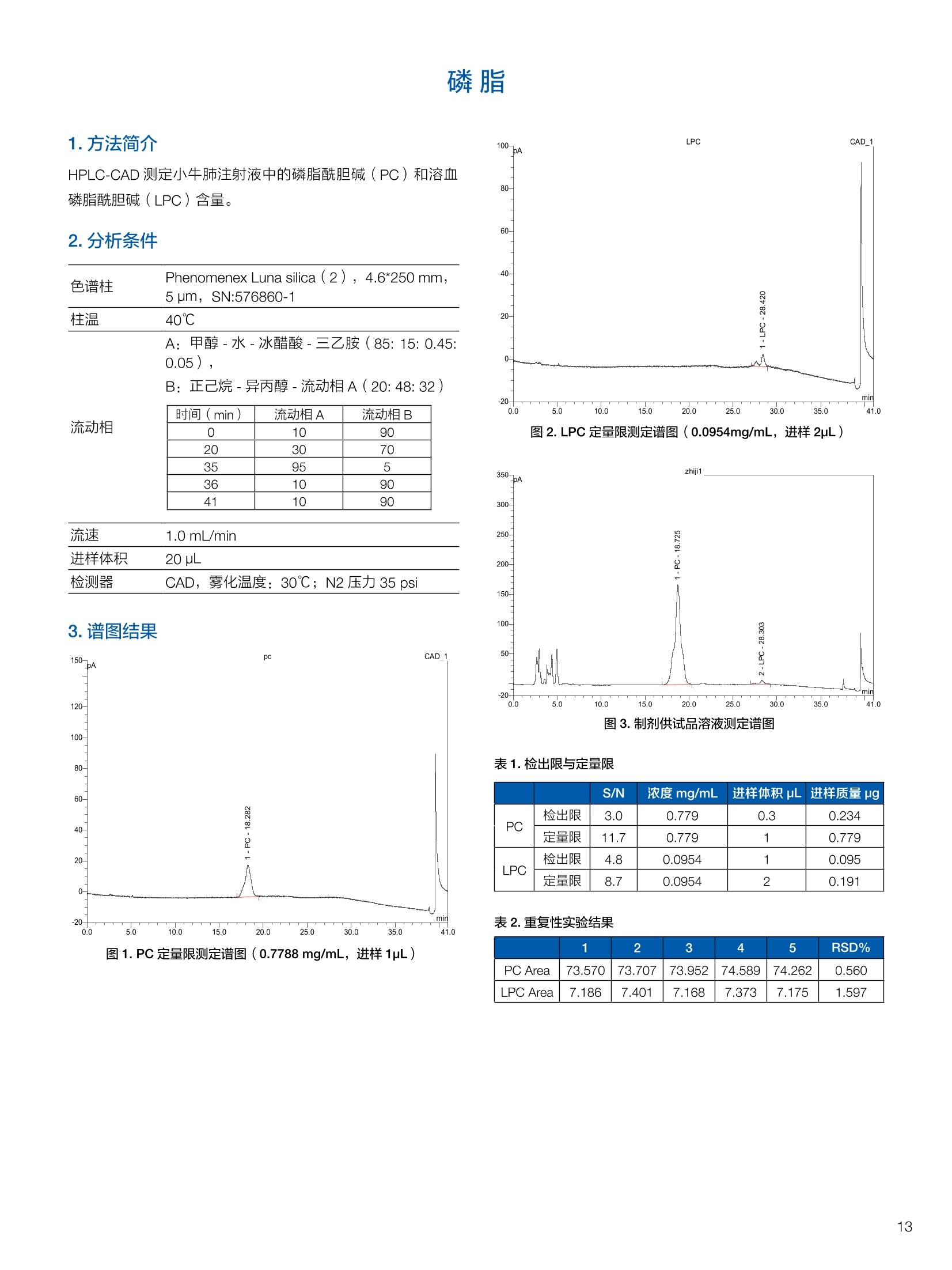
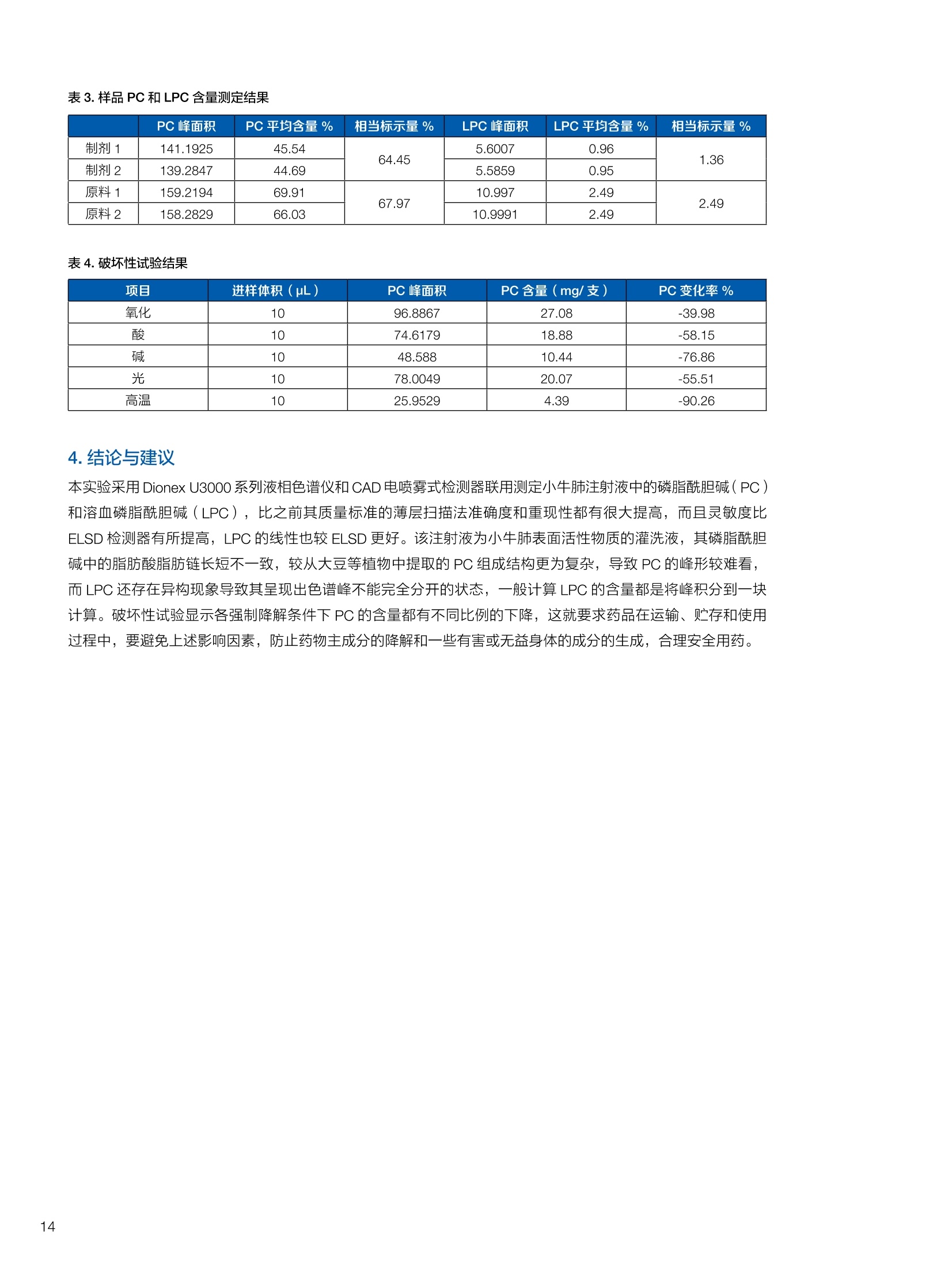
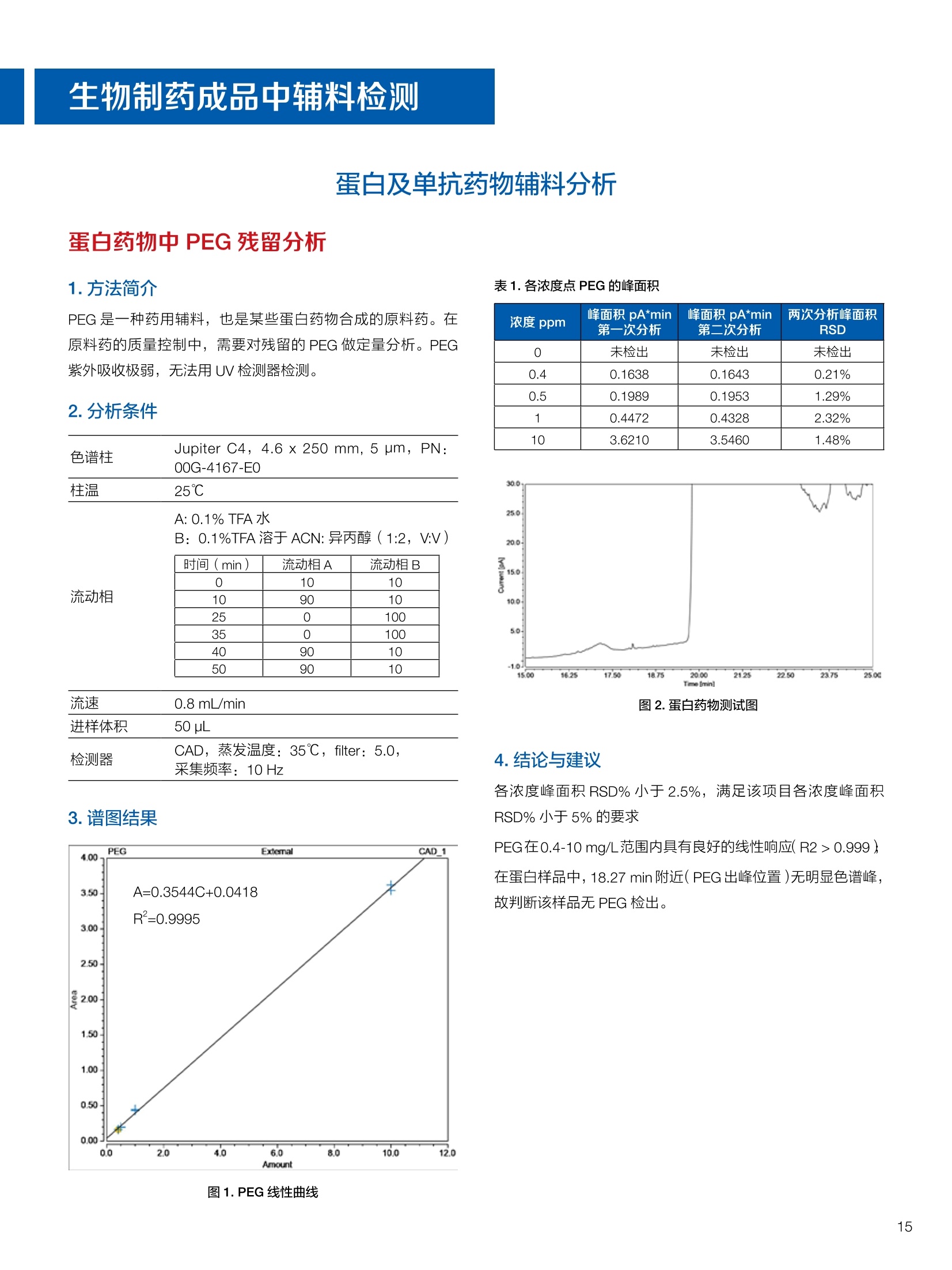
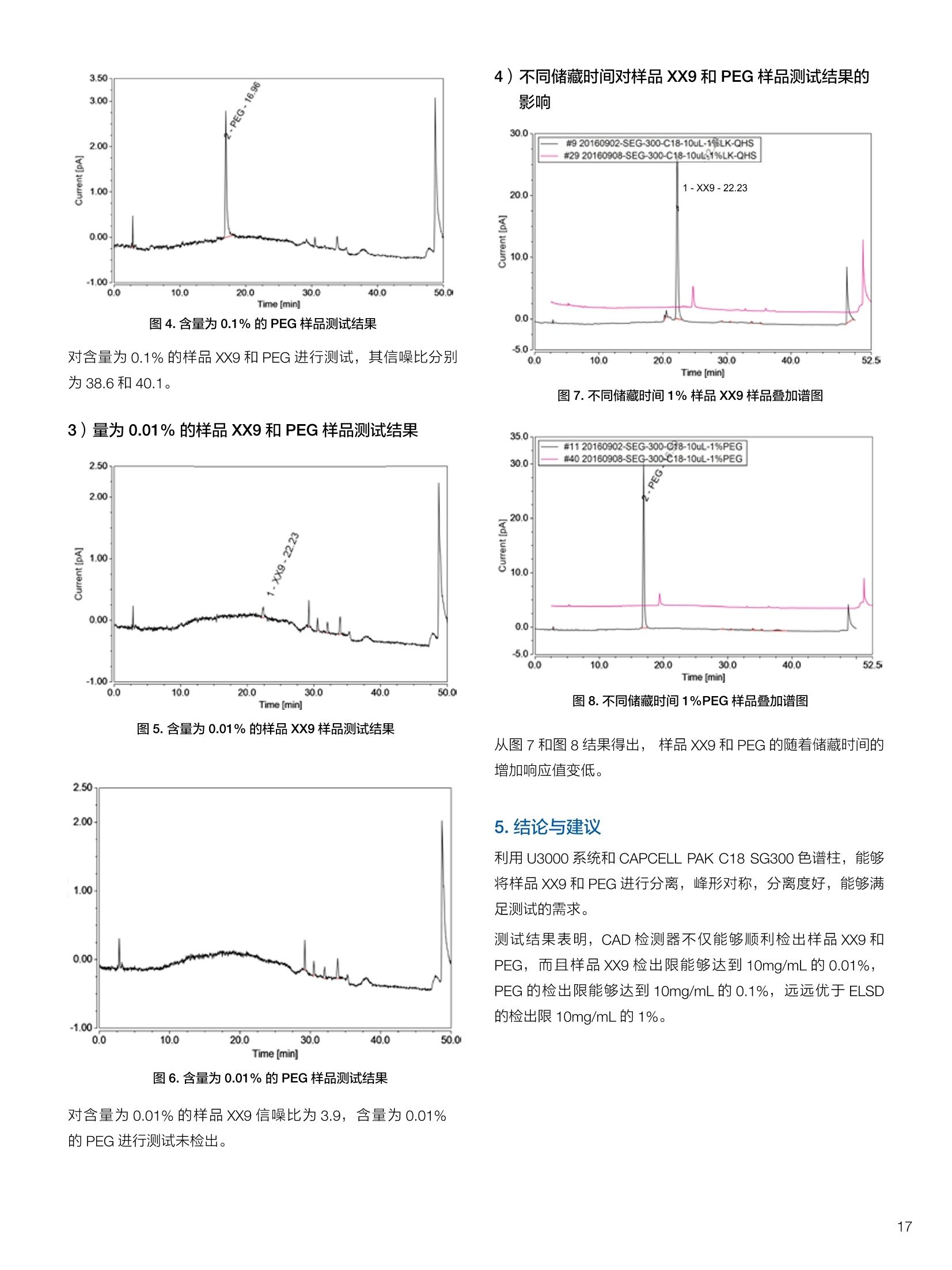
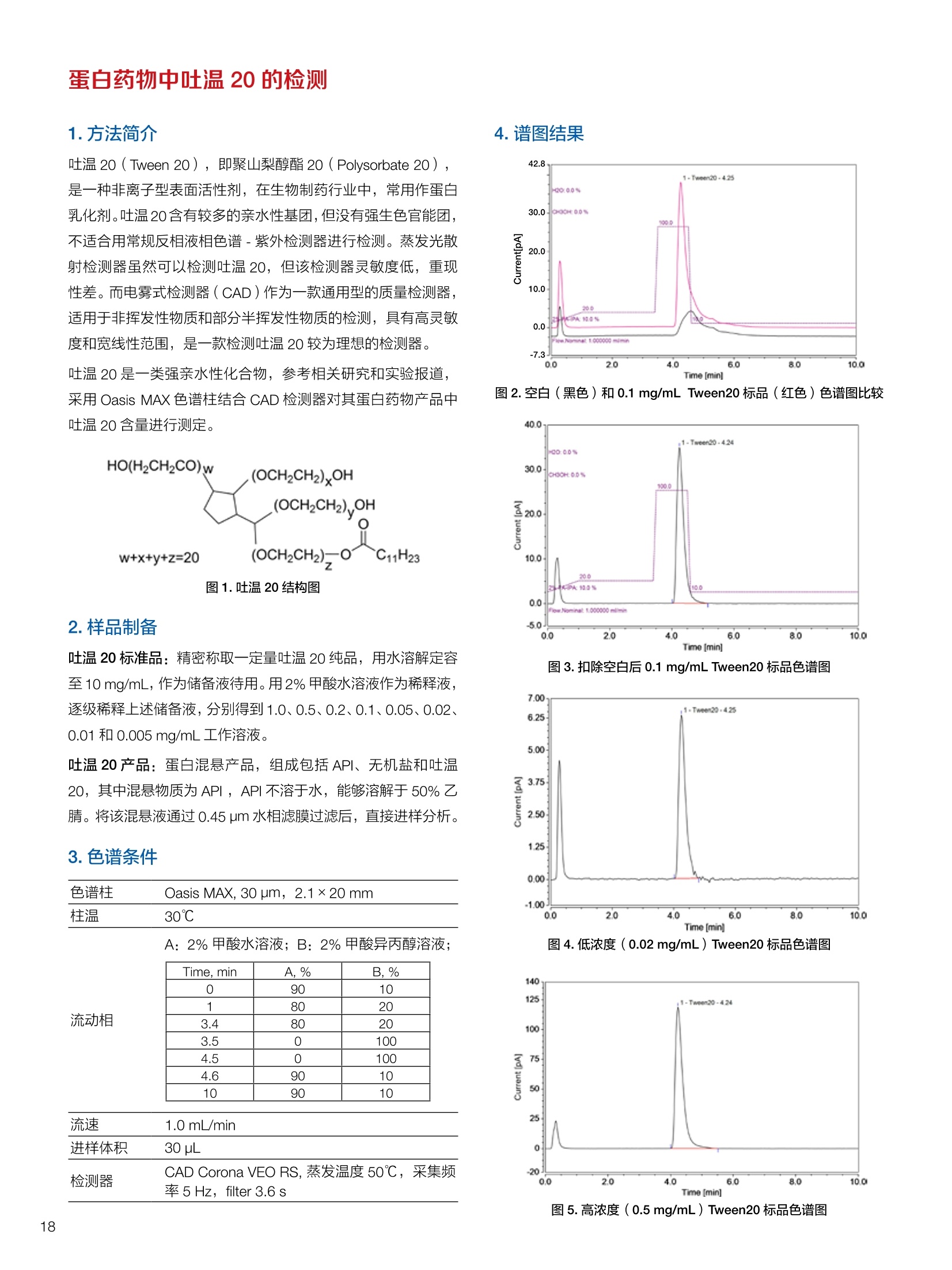
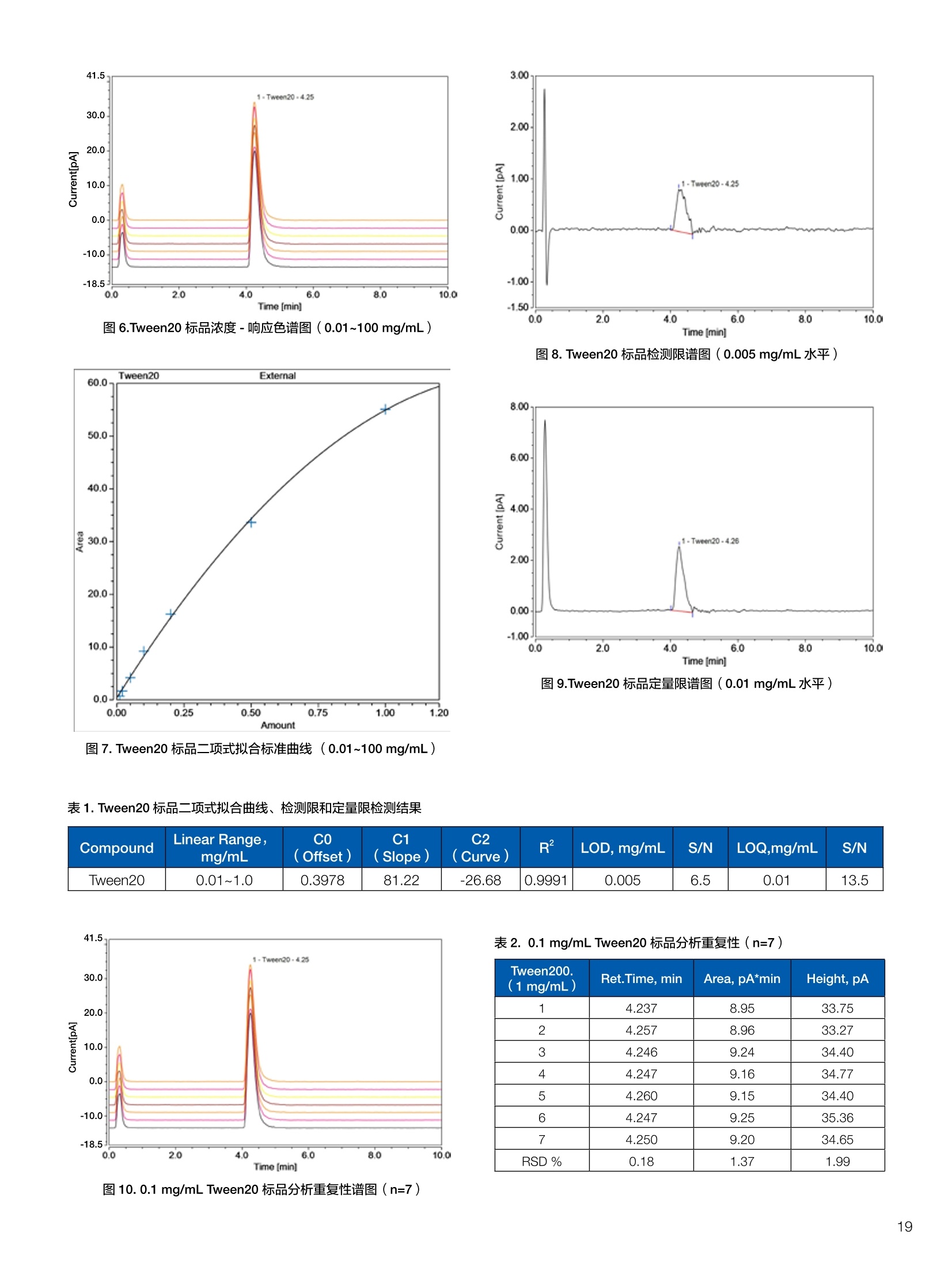
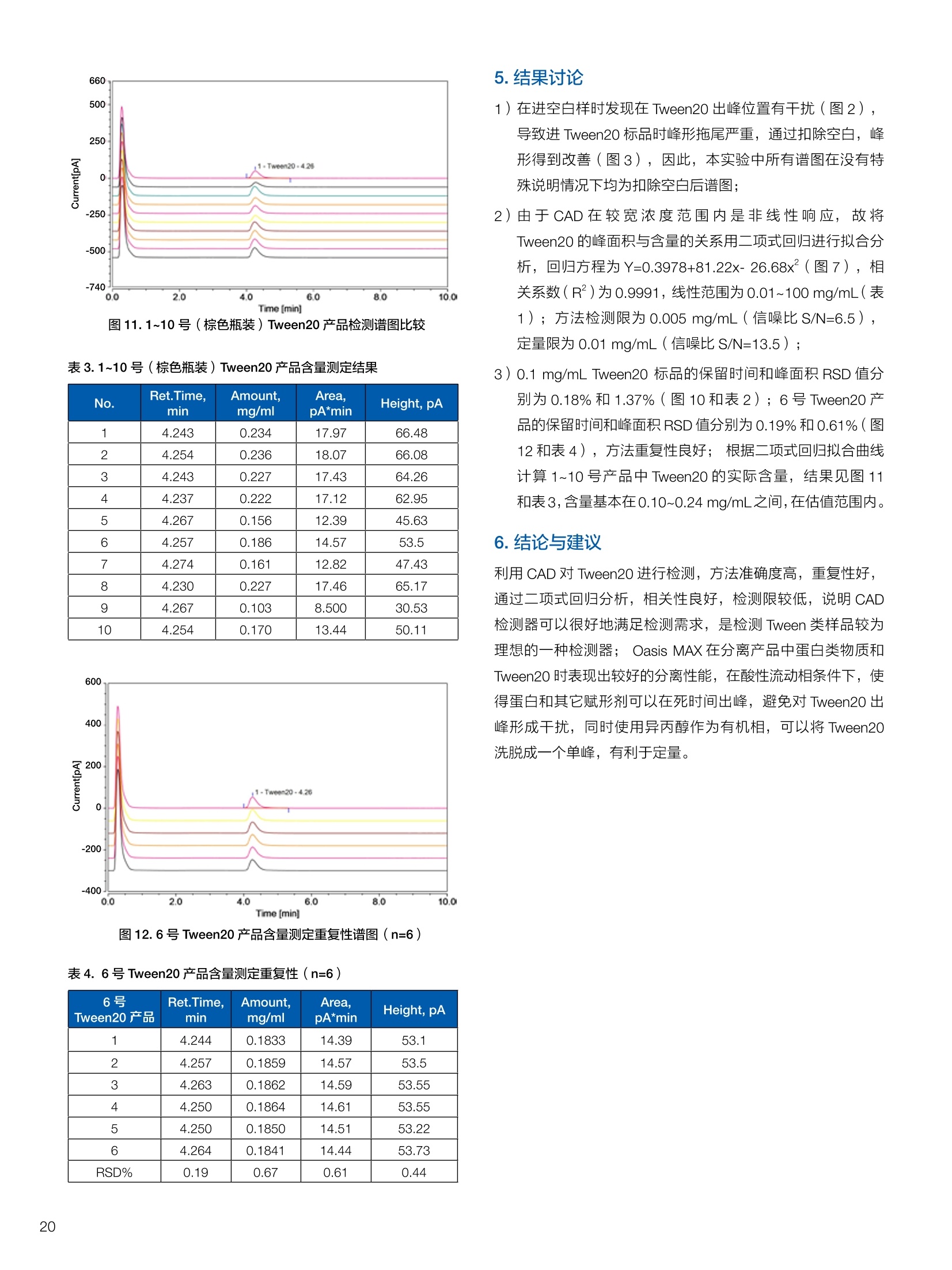
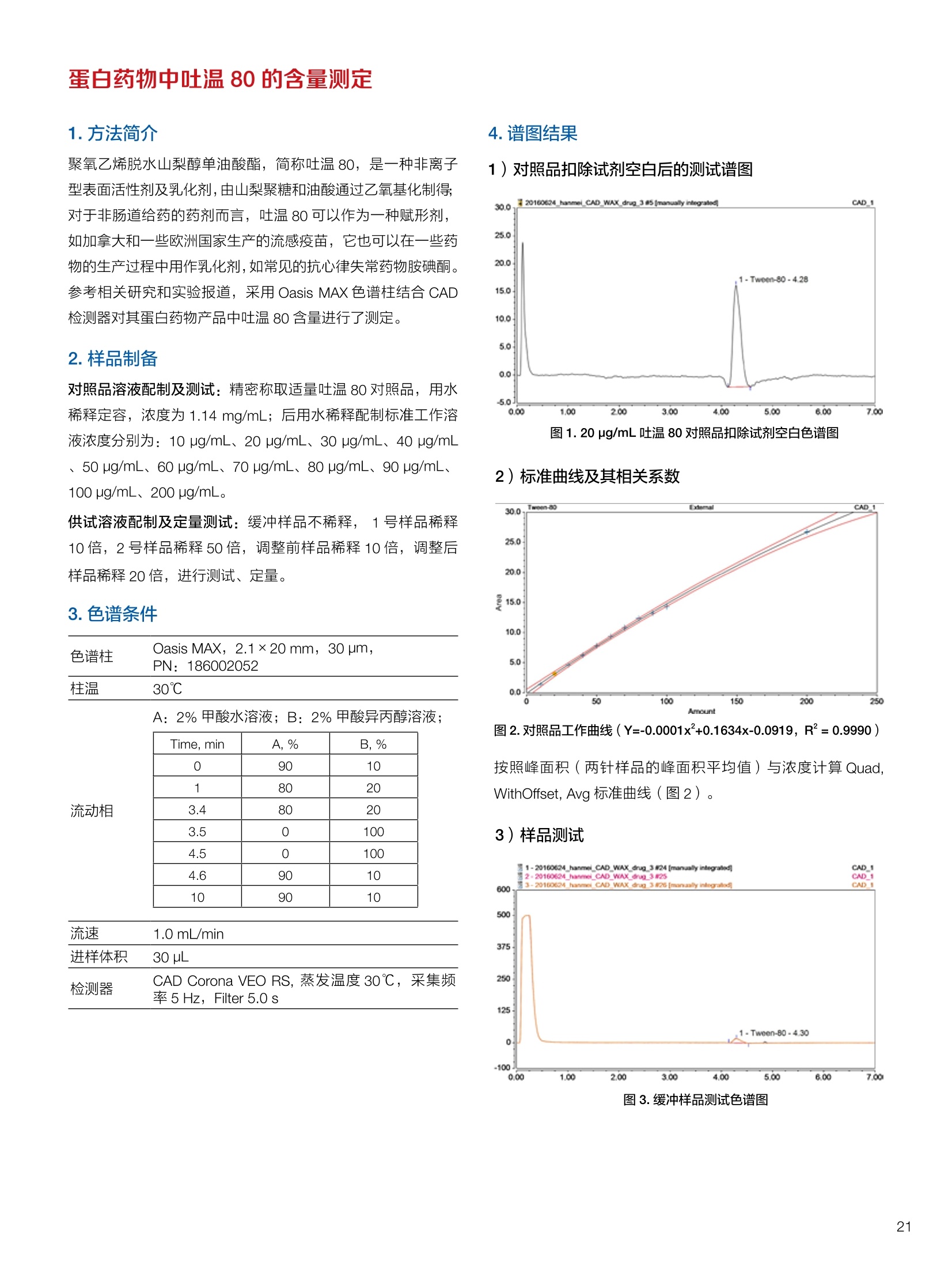
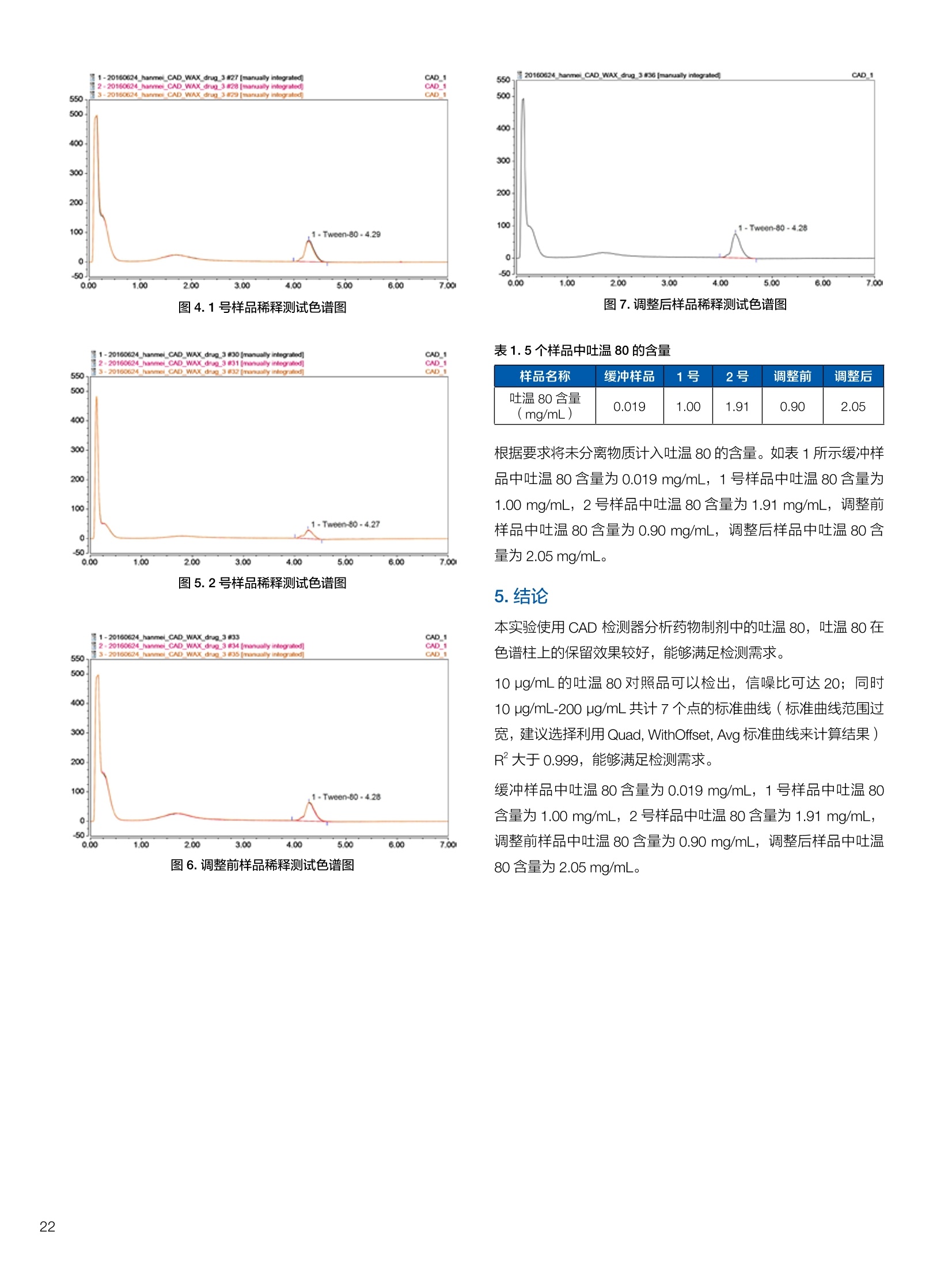
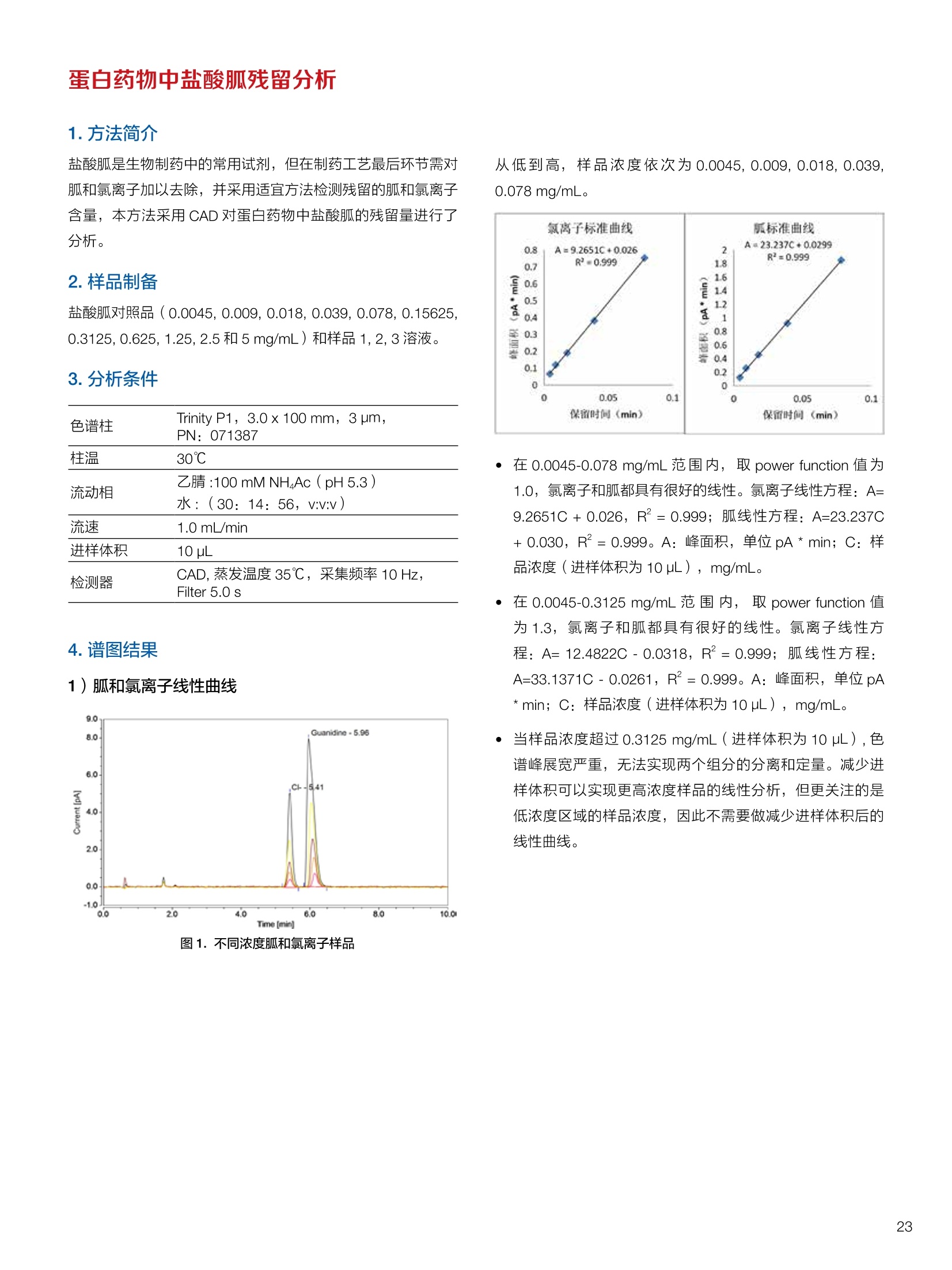
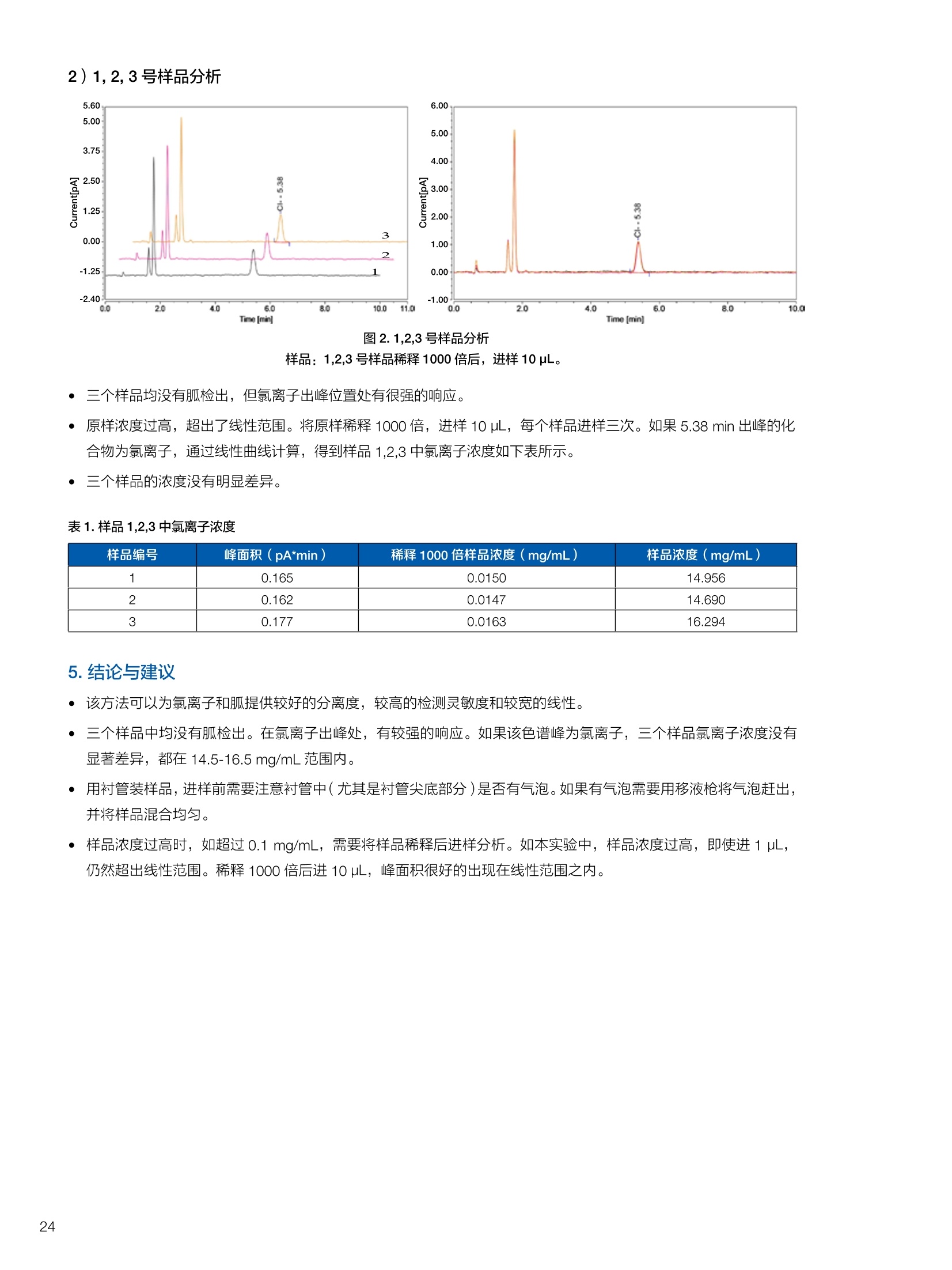
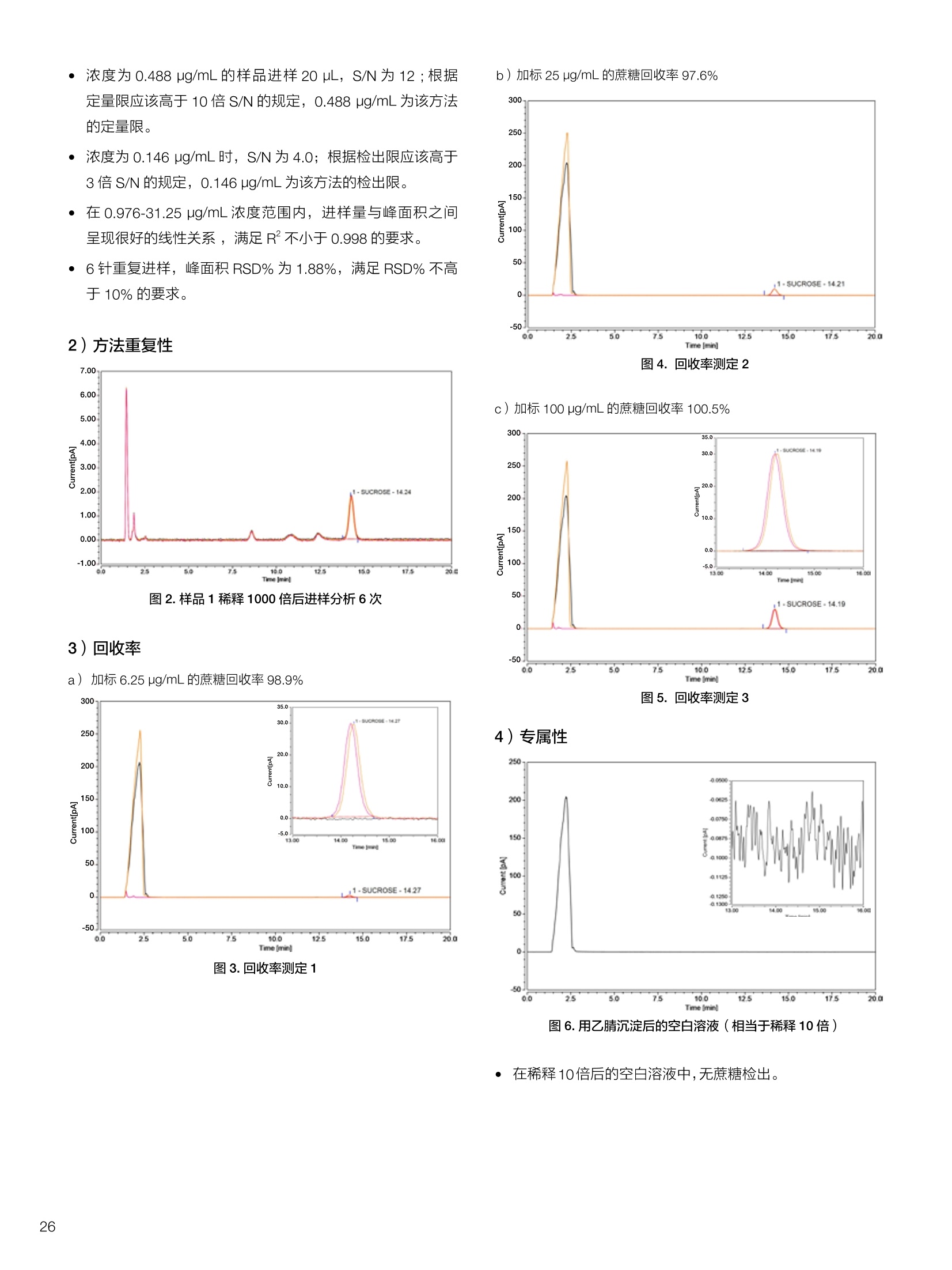
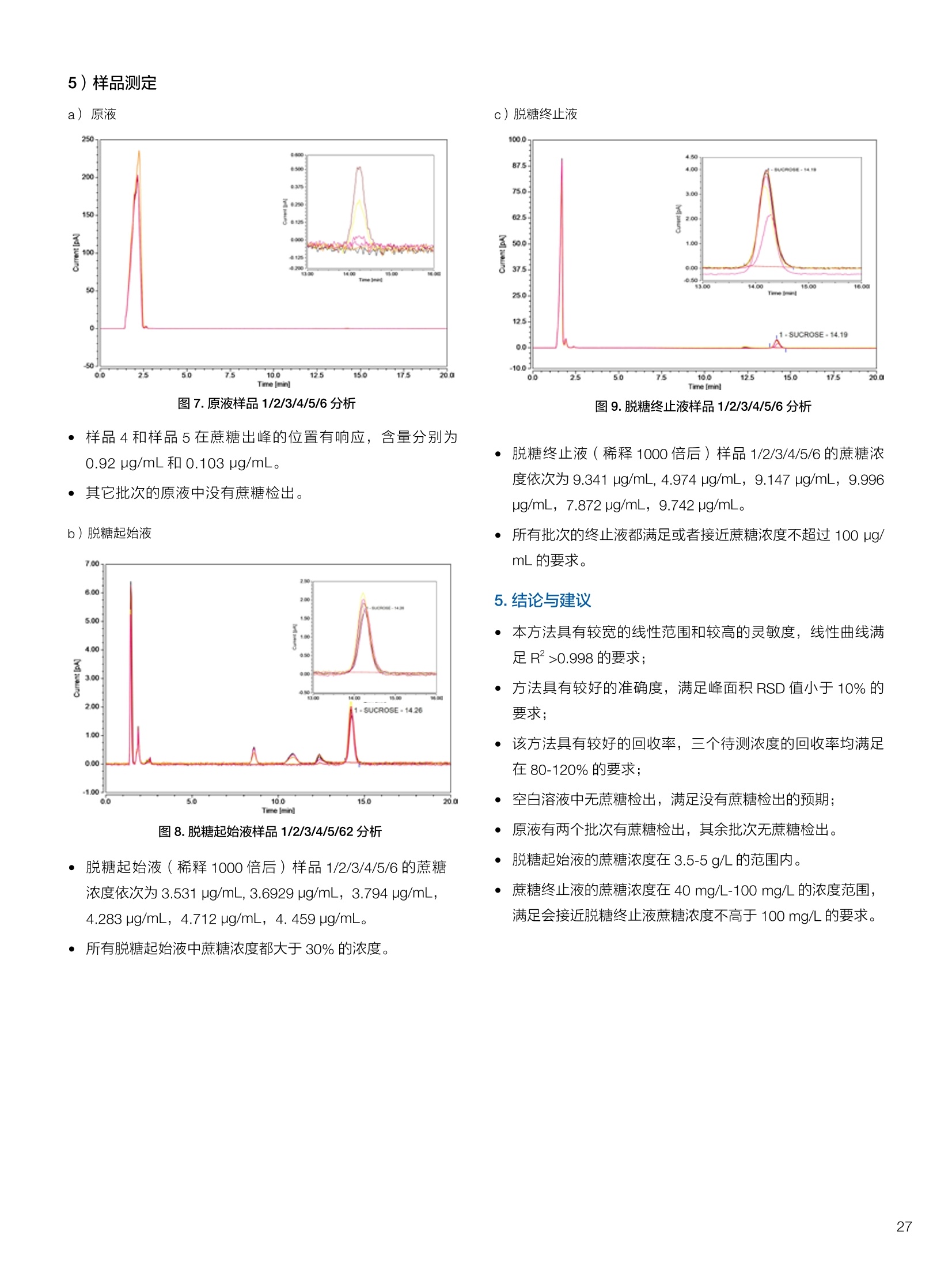
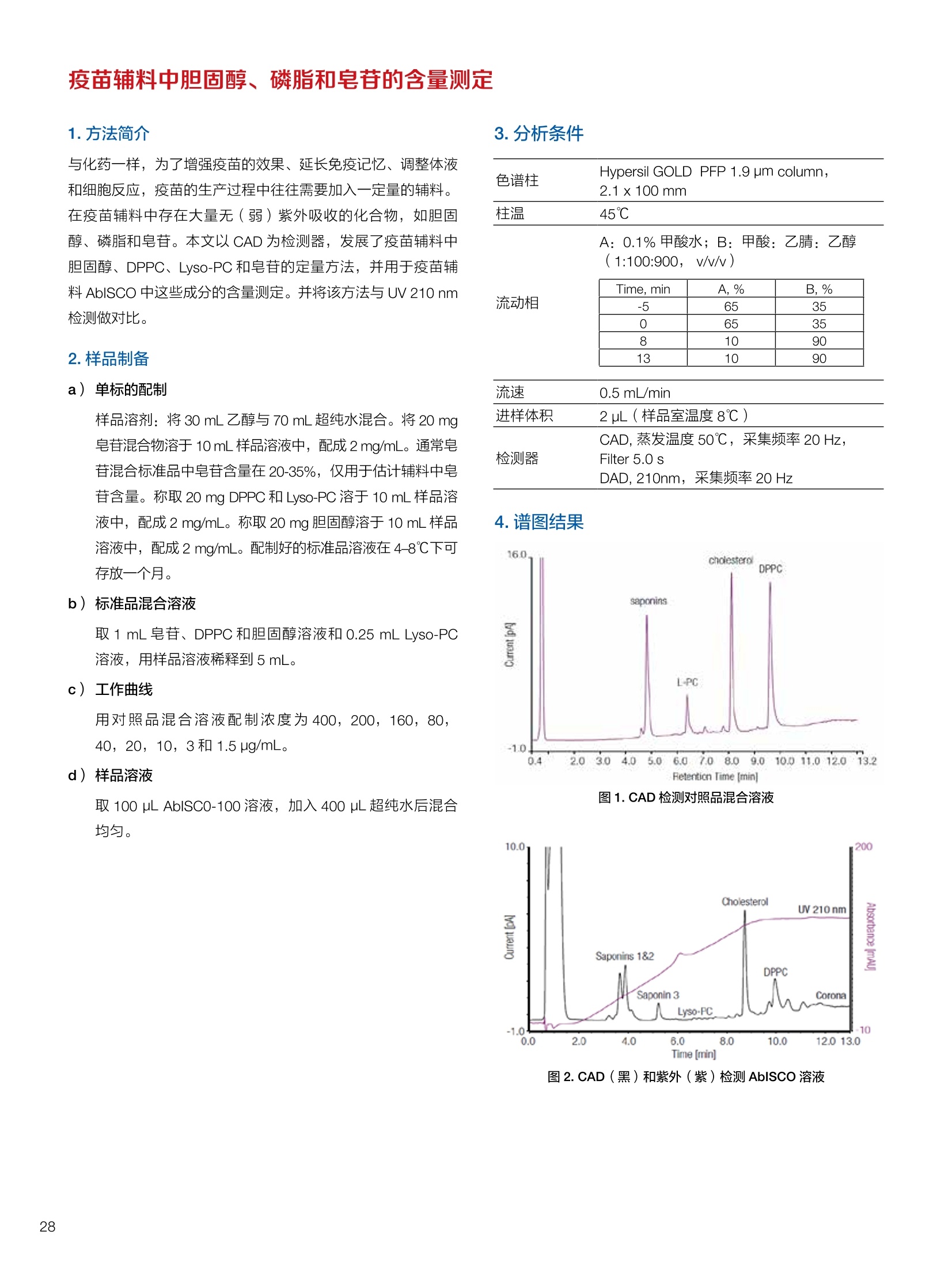
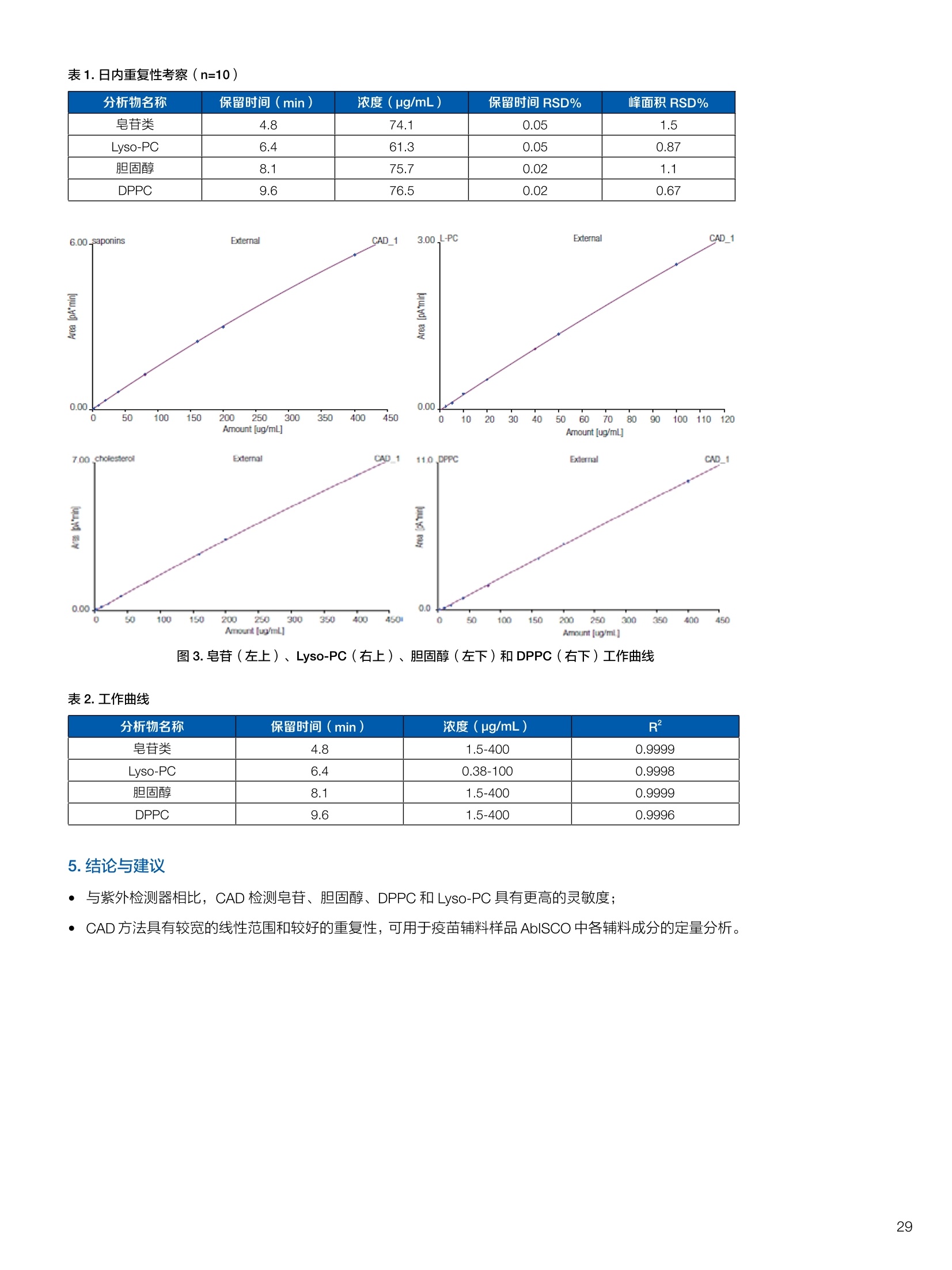
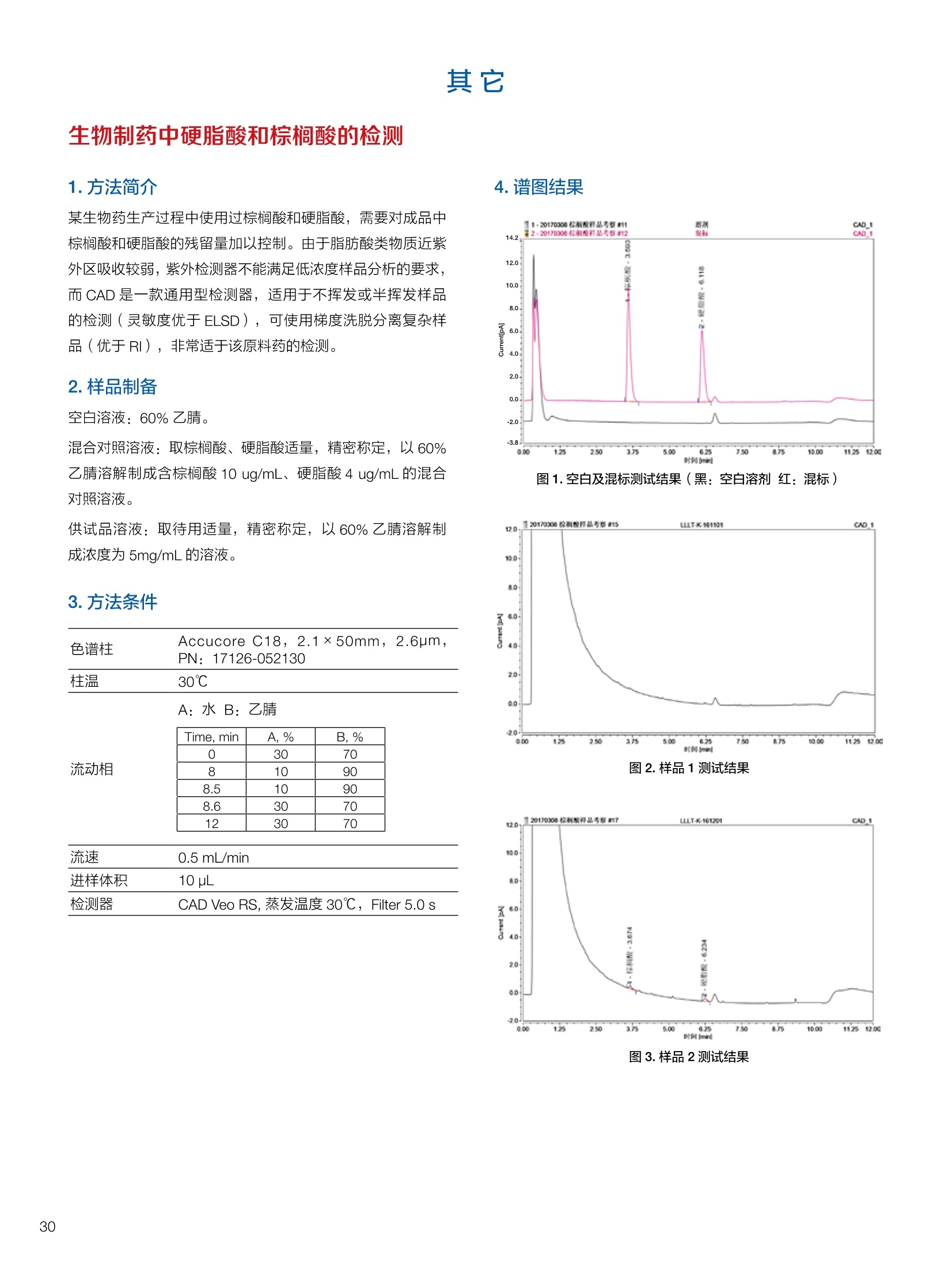
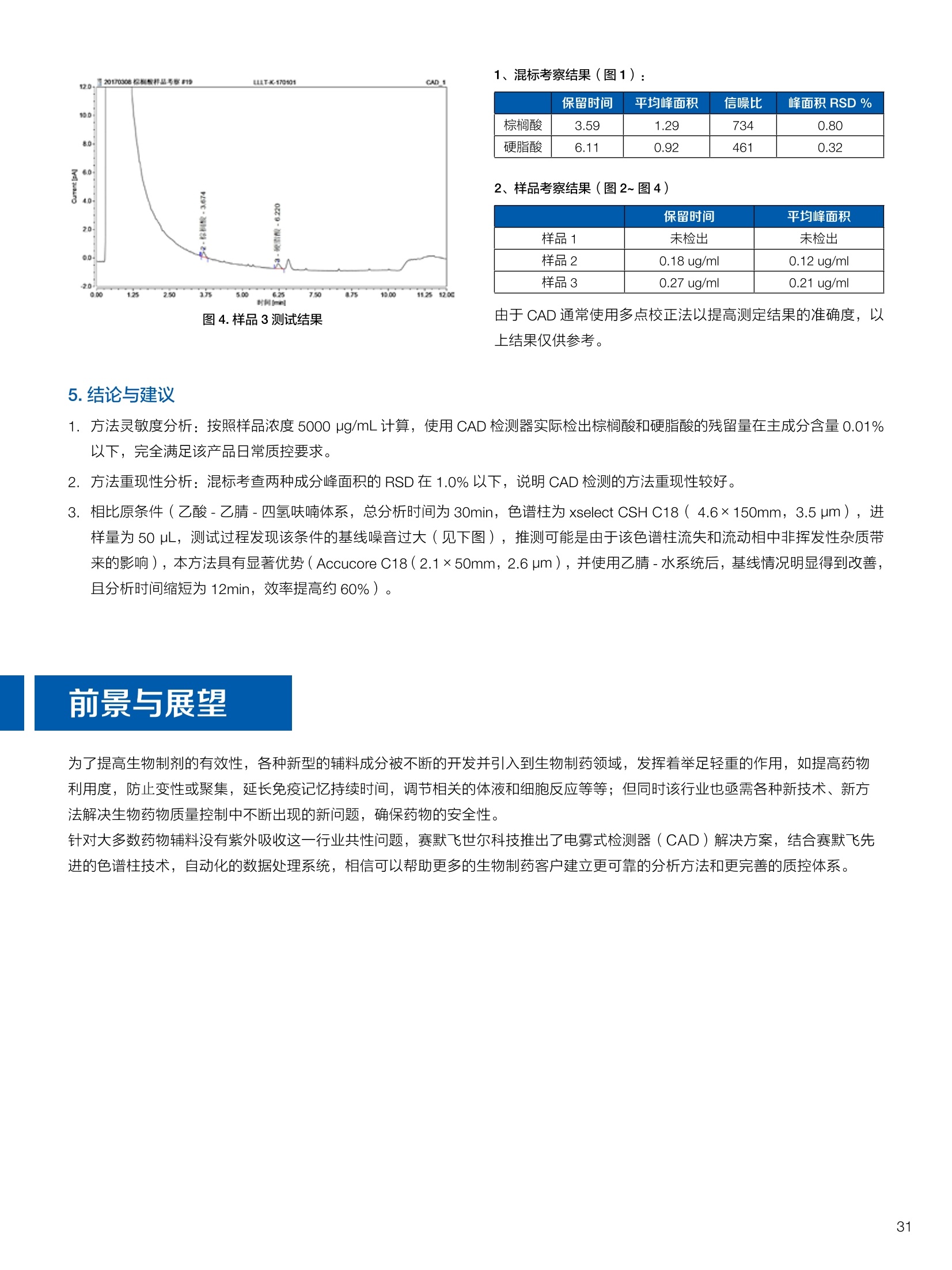
生物制药常用辅料质量评价 脱氧胆酸 液相色谱法电雾式检测器 UHa3000 40 10 .1.300932 00m 8 160/0 B-835000 三 1050 254 生物制药辅料应用文集 目录 O一 HC 1.前言 .3.1脂肪酸.. .6 3.2脱氧胆酸.. 7 3.3吐温, Triton-X100. 7 .3.4PEG 8 3.5泊洛沙姆P188.....mm 9 3.6乳糖....... 10 3.7硬脂酸镁.. 1 3.8磷脂.. 13 4.生物制药成品中辅料检测 .4.1蛋白及单抗药物辅料分析....... .15 4.1.1蛋白药物中PEG 残留分析.. 15 4.1.2 PEG 修饰药物中 PEG 的残留分析....... 16 4.1.3蛋白药物中吐温20的检测.. 18 .4.1.4蛋白药物中吐温80的含量测定, 2 4.1.5蛋白药物中盐酸胍残留分析... 23 4.2疫苗辅料分析解决方案.... 25 4.2.1疫苗中蔗糖的含量测定 25 4.2.2疫苗辅料中胆固醇、磷脂和皂苷的含量测定.. 28 .4.3其它....... .30 4.3.1生物制药中硬脂酸和棕榈酸的检测 30 前言 辅料是生物制剂中的重要组成部分,其组成和含量影响蛋白类药 物的稳定性和安全性,并在一定程度上影响着药物的治疗效果。例如,蔗糖和麦芽糖的含量影响蛋白药物的蓬松程度和复溶效果。吐温(吐温20或80)的含量影响蛋白药物的溶解性和稳定性。蛋白药物中吐温(吐温20或80)浓度过低无法实现助溶的作用,浓度过高将引起溶溶等副作用。PEG 是常见的蛋白药物修饰剂,残留的 PEG 影响蛋白药物的安全性。盐酸胍是蛋白增溶剂,残留的胍离子影响蛋白的安全性和有效性。辅料含量的高低对蛋白药物的有效性和安全性有明显的影响,但中国药典和药用辅料手册均未提供蛋白药物中辅料的含量测定方法。因此,急需建立蛋白药物中药用辅料的含量测定方法。 蔗糖、麦芽糖、吐温、PEG 和盐酸胍均为弱紫外(或无紫外)吸收化合物,难以使用紫外检测器直接测定;虽然示差折光检测器(RID)可用于该类化合物的检测,由于蛋白药物基质较复杂,往往需要梯度洗脱,而 RID 却不适合梯度洗脱;蒸发光散射检测器(ELSD)可兼容梯度洗脱,但ELSD 又存在灵敏度较低且重复性较差的问题。电雾式检测器(CAD)是一种新型的通用型检测器,可兼容梯度洗脱,比 ELSD 和 RID 具有更高的灵敏度,更好的日内和日间重复性,更好的结构响应一致性。 本应用文集以 CAD 为检测器,发展了生物制药中蔗糖、麦芽糖、吐温20(吐温80)、PEG和盐酸胍等常见辅料的检测方法。 赛默飞世尔科技(中国)应用中心 2020年5月 CAD 是一款设计独特、技术先进、灵敏度高、且重现性较好的通用型检测器,用于非挥发和半挥发性的化合物定量或半定量分析。图1所示是两款 CAD 检测器。CAD 的工作过程(见图2所示):HPLC 洗脱液经与雾化器中氮气流碰撞作用而雾化,其中较大的液滴经废液管流出,较小的溶质(分析物)液滴在雾化温度下干燥,形成溶质纳米颗粒。同时,分流的第二路氮气流经过电晕式放电装置(含高压铂金丝电极)形成带正电荷的氮气粒子,与溶质颗粒反向相遇时经碰撞使溶质颗粒带上正电。为了消除由带有过多正电荷的氮气所引起的背景电流,在含溶质颗粒的气流流入静电检测计之前,通过一种称之为离子阱的装置(带有低负电压)使迁移率较大的颗粒(即带正电荷的氮气粒子)的电荷中和,而迁移率小的带电颗粒把它们的电荷转移给一个颗粒收集器,最后用一个高灵敏度的静电检测计测出带电溶质的信号电流,由此产生的信号电流与溶质(分析物质)的含量成正比。 图1.电雾式检测器 CAD外观 左: Corona Veo 系列 CAD 右: Vanquish 系列 CAD 图2.电雾式检测器的构造及工作示意图 CAD 的分析步骤如下: 第一步:雾化与干燥 HPLC 洗脱液进入 CAD 雾化室,在氮气流作用下,进行雾化去溶剂,使洗脱液中的目标化合物变成颗粒,颗粒量的多少与进入雾化室的目标化合物质量有关。没有雾化完的大液滴直接进入废液管,雾化的超细小液滴进入干燥管,因其粒径较小,所含溶剂在此被迅速蒸发,干燥后的目标化合物颗粒随气流直接进入混合腔。因此,和大多数基于雾化原理的检测器一样, CAD 雾化效率也受流动相中有机相含量的影响显著,当有机相比例逐渐增加时,雾化效率增加,响应值也随之增加,当有机相比例达到80%时,雾化效率趋于稳定。 第二步:使目标颗粒物带电 另一路氮气经过高压电晕放电针,变成带正电的氮气,在碰撞室与干燥的目标化合物颗粒迎面碰撞对流流合后,电荷随之被转移到目标化合物颗粒表面。扩散带电的过程对颗粒材料的依赖性很小。如果颗粒物越大,球面积也越大,大致上带电量也就越多,实际上在很宽的粒径范围单极扩散带电正比于d(粒径)1.133。经过碰撞后,带电颗粒和多余的带电氮气离开碰撞室,其中,速度较快的带电氮气在迁移途中被低压离子阱捕集移除,而迁移速度较慢的多电荷目标化合物颗粒则通过后端的离子捕集阱,并撞向一个颗粒物过滤网。 第三步:检测带电目标化合物 颗粒物撞击收集器后,把电荷转移到过滤网上,由此产生的电流将被高灵敏度的静电计探测到,并被放大输出至到检测器,最终产生的信号强度与目标化合物的量成比例。离子肼可以捕集多余带电氮气,从而降低背景电流,因此,即使很少的电荷也能被检测器检测到,使得 CAD 的检出限较低,灵敏度较高。同时,由于 CAD 的响应不依赖于化合物的结构,其对大部分的化合物的响应因子也基本一致。蒸发光散射检测器由于其散射受到化合物的空间结构的影响,即使是同分异构体,同样的浓度其响应值也会出现较大的差异。 CAD的主要特点: 1)基于设计原理与结构,该检测器灵敏度高,如在分析葡萄糖、蔗糖和乳糖时,能检测到 0.5 ng的柱上样量; 2)响应因子一致,不依赖于化合物结构,重现性非常好,如对24种化合物在相同色谱条件下分别直接进样1ug(不接色谱柱)测定,其响应的峰面积的 RSD 值小于10%; 3)动态检测范围宽,达3-4个数量级; 4)应用较广泛,能分析小分子、大分子化合物,如氨基酸、蛋白、聚合物等; 5)使用操作直观简单,维护十分简便,工作流速0.2-2.0 mL/min, 完全兼容 UHPLC 超快速分析。 CAD 使用注意事项: CAD 由于需要对流动相进行雾化,所以当需要使用酸或盐来调节流动相时要使用挥发性的酸和盐,如甲酸、乙酸和三氟乙酸等,有机盐建议使用铵盐;推荐 pH值范围2-7.5,更高的pH值可能会增加背景和噪音值。 1.方法简介 2.分析条件 混合脂肪酸是一种常见药用辅料,作为栓剂等制剂的载体,其应用符合医药“低毒、高效”的基本发展原则和民众医疗保健的意愿,近年来发展较快。脂肪酸紫外吸收弱,用传统UV方法无法检测,本实验采用 HPLC-CAD 方法检测辅料中的常见脂肪酸取得了较好的分析结果。 色谱柱 PRP-1,4.1×250mm, 7pm (Hamilton, P/N: 79422) 流动相 乙腈-四氢呋喃-60mM 醋酸溶液 =60:5:35, 15min 内变化到 90:10:0 流速 1.0 mL/min 柱温 45℃ 进样量 25 uL 检测器 CAD, 雾化温度 15℃ CAD_1 时间 [min] 图1.辅料中脂肪酸分析图谱 表1.辅料中脂肪酸分析结果 供试品中组分名称 保留时间 min 峰面积 pA*min 塔板数Plates 分离度 Resolution 拖尾因子USP Tf 月桂酸 Lauric Acid min 峰面积 13070 8.11 1.11 肉豆蔻酸 Myristic Acid pA*min 塔板数 15153 6.86 1.06 棕榈酸 Palmitic Acid Plates 分离度 15989 1.81 1.09 油酸 Oleatic Acid Resolution 拖尾因子 16794 3.91 1.07 硬脂酸 Stearic Acid USP Tf 20.818 22488 n.a. 1.05 4.结论与建议 本方法使用 CAD 检测器结合 Hamilton 的一款色谱柱,对多种脂肪酸同时进行分析,分离度高,色谱峰形好,有较高实用价值。 参考文献来源:感谢 USP 中国研发中心提供谱图。 1.方法简介 脱氧胆酸及其盐为表面活性剂,为化妆品和药剂中安全有效的乳化剂,有抗真菌和抗炎作用,可用于治疗牙根疾患。脱氧胆酸通常来源于合成成动物, FDA 不允许动物来源的脱氧胆酸作为药物基质。本实验检测合成样品中脱氧胆酸的含量以及杂质检测。 2.分析条件 色谱柱 Acclaim C18 4.6×150 mm, 3 umA: 0.1%甲酸水溶液;B:0.1%甲酸乙腈溶液; Time (min) Mobile Phase A(%) Mobile Phase B(%) 0.0 75.0 25.0 2.0 55.0 45.0 14.0 42.0 58.0 24.0 0.0 100.0 35.0 0.0 100.0 35.0 75.0 25.0 38.0 75.0 25.0 流速 1.0 mL/min 柱温 30℃ 进样量 25 uL 检测器 CAD, 雾化温度50℃, Filter: 5.0 s, PF: 1.2 图1.脱氧酸分析图谱 4.结论与建议: 杂质检测,即使在杂质较低水平时也能实现。 参考文献来源: USP 40-NF 35, Monographs/Desoxycholic ( 8259, AN-72600-LC-CAD-Method-Transfer-Deoxycholic-Acid (内部资料) ) 吐温, Triton-X100 吐温20(聚山梨醇酯20)、吐温80(聚山梨醇酯80)和TritonX100作为非离子表面活性剂,具有低毒性和高表面活性,在药物制剂领域有广泛应用。这些表面活性剂没有生色团,紫外吸收弱,对于它们的测定,传统方法为比色法和薄层色谱法,但准确性较差。本方法利用通用型的质量型检测器 CAD 来测定,具有很好的可行性和推广意义。 2.分析条件 分析柱 MD150, 3.2x150mm, 3 um 柱温 室温 检测器 CAD, N2压力35 psi, 输出范围:500pA 流动相 65%水:35%甲醇 流速 0.5 mL/min 进样量 10 pL 图 3. Triton X100 图1.聚山梨醇酯20 4.结论与建议 本实验建立了药物及制剂中吐温20、吐温 80和 Triton X100的含量测定方法,取得了较理想的结果,可推广应用于含有该类辅料的药物检测。 ( 参考文献来源: AN 7 0 -6809 Non-lonic Surfactants- Polysorbate_2 0 ,_Polysorbat e _80(内部资料) ) 1.方法简介 PEG 具有良好的水溶性,并与许多有机物组份有良好的相溶性。它们具有优良的润滑性、保湿性、分散性,用作粘接剂、抗静电剂及柔软剂等,在化妆女、制药、化纤、橡胶、塑料、造纸、油漆、电镀、农药、金属加工生物工程及食品加工等行业中均有着极为广泛的应用。本实验比较超临界系统分析条件下 CAD 与 ELSD 色谱法定量 PEG 的性能。 2.分析条件 色谱柱 SFCpak SIL-5 silica gel column, 4.1×250 mm, 5 pm 流动相 超临界二氧化碳与90%甲醇水混合溶液, 二氧化碳流速为2ml/min 流速 1.0 mL/min 柱温 50℃ 进样量 25 pL 检测器温度 CAD, 雾化温度15℃ 3.谱图结果 Degree of Polymerization n 图1. CAD、ELSD 条件下 PEG 聚合化程度 4.结论与建议 在测定 PEG 系列实验中, CAD 测定 PEG分子量分布与实际值更接近,同时 CAD 具有更好的重复性、信噪比与灵敏度。 ( 参考文献来源: Kayor i Takahashi,etc, Qu a ntitative comparison of a CAD and ELSD for polymer. JCA. ) P 188是聚氧乙烯聚氧丙烯醚嵌段共聚物,用作发酵液中的辅料,也可用作增溶剂和乳化剂。 Time (min) A% B% Curve 0 80 20 5 6 80 20 6 11 50 50 2 15 10 90 2 18 10 90 6 18.1 80 20 6 20 80 20 5 图1.P188标准品色谱图(5 pg/mL-100 pg/mL) 表1.P188标准品积分表 浓度/ug*mL 保留时间 /min 信噪比 5 8.435 13.0 15 8.437 53.9 25 8.419 81.2 50 8.440 110.8 100 8.444 157.2 4.结论与建议 经考察,在5-100 pg/mL浓度范围内, P188的峰面积与浓度之间的线性关系良好,线性方程为 A=0.0947C+0.5123; 图2.不同样品中P188含量测定色谱图 (从上到下,分别为 S1、S2和S3) 表2.不同样品中 P188含量测定积分表 样品编号 保留时间 /min P188 浓度/ug*mL S1 8.435 N.D S2 8.435 N.D S3 8.435 N.D 5.结论与建议: 由表2可知,三个样品中, P188均未检出。采用 CAD 加Surfactant Plus 柱的模式对P188进行分析,信噪比高,定性和定量结果良好。 1.方法简介 乳糖 (lactose) 是一种二糖C12H22O11,是哺乳动物乳汁中特有的一种还原糖。在食品行业中,乳糖主要用于婴幼儿食品、炼乳品、糖果和人造奶油等。在医药行业中,用作药用辅料,主要是作为填充剂或稀释剂用于片剂和胶囊的生产,也可用于冻干产品和吸附剂等。此外,还可作细菌培养基。本实验建立HPLC-CAD 法测定原辅料及制剂中乳糖百分含量。 2.分析条件 色谱柱 聚合物氨基柱, Shodex Asahipak NH2P-50 4E,4.6×250mm, 5 um 柱温 35℃ 流动相 乙腈-水(70:30) 流速 1.0 mL/min 进样体积 25 pL 检测器 CAD, 雾化温度:30℃,采样频率:10Hz, 过滤常数:3.6s,幂率:1.20; 表1.样品分析结果 样品名称 保留时间 /min 峰面积/fA*min 峰高/fA 含量/% 理论塔板数(EP) S1 9.588 722.96 2615.9 99.65 8204 S2 9.594 735.95 2671.9 100.79 8250 S3 9.592 731.25 2652.6 100.75 8059 平均值 9.592 730.05 2648.8 100.39 8117 RSD/% 0.056 0.90 1.07 0.65 0.83 图1.制剂样品色谱图 4.结论与建议 本实验建立 HPLC-CAD法测定注射用乳糖辅料及其相关制剂中乳糖含量。经过精密度、重复性、线性等方法学考察,表明本方法准确度高,精密度、重现性较好,在1.0~100 pg/mL范围内,线性相关较好(r=0.9998),定量限达0.5 pg/mL, 可作为原辅料及制剂中乳糖的含量测定方法。CAD 作为质量型检测器,当需要检测更低浓度样品,可以通过适当增大进样体积,或进行柱后有机相补偿,提高化合物的响应,降低定量检出限。同时,由于该检测器响应因子一致,可以通过乳糖的浓度同步对其它糖类药物进行初步半定量分析。总体而言,该方法设计巧妙,原理新颖,操作使用方便,取得了较理想的结果,因因具有较好的推广与借鉴意义。 硬脂酸镁为白色无砂性的细粉;微有特臭;在直接压片中用作助流剂,还可作为助滤剂、澄清剂和滴泡剂,以及液体制剂的助悬剂、增稠剂。由于紫外吸收极弱,无法用紫外吸收检测器检测。本文采用电雾式检测器(CAD)开发了片剂中PEG4000 和硬脂酸镁的检测方法。 2.分析条件 Time, min A, % B,% 0 20 80 20 100 0 25 100 0 图1.PEG4000 和硬脂酸镁对照品分析(上:PEG4000,下:硬脂酸镁) 硬脂酸镁辅料是棕榈酸和硬脂酸镁的混合物,因此可以检测到两个色谱峰。 图2.棕榈酸二次拟合曲线(左)和线性回归(右) 图3.硬脂酸二次拟合曲线(左)和线性回归(右) 图4.PEG4000二次拟合曲线(左)和线性回归(右) 日由于没有棕榈酸和硬脂酸的单标。以硬脂酸镁的浓度做棕榈酸和硬脂酸镁的浓度。●栈棕榈酸:二次曲线拟合,浓度范围:0.449-460 ppm, 相关系数0.999;一次方程拟合,浓度范围:0.449-230 ppm,相关系数0.999; LOQ: 0.449 ppm. 硬脂酸:二次曲线拟合,浓度范围:0.449-460 ppm,相关系数0.999;一次方程拟合,浓度范围:0.449-115 ppm 范围内,相关系数 0.999. LOQ: 0.449 ppm。 PEG4000:):二次曲线拟合,浓度范围:0.278 ppm-285ppm, 相关系数0.999;一次方程拟合,浓度范围:0.278-35.6 ppm, 相关系数 1.000。 LOQ: 0.278ppm。 图5.酸乙腈提取物分析 棕榈酸和硬脂酸的分离检测不受其他化合物的干扰,故该方法可用于药片中硬脂酸镁的测定。以棕榈酸组分计算,药片中硬脂酸镁的含量为0.216 mg;以硬脂酸组分计算,药片中硬脂酸镁的含量为 0.127 mg, 药片中理论的硬脂酸镁含量为0.8 mg。因此,总棕榈酸镁提取率为27%,硬脂酸提取率为15.8%。需要再次优化药片中这两种化合物的提取方法。 ·该方法用于酸乙腈提取物中 PEG4000 的检测,不受其它化合物干扰,可实现其含量测定。用二次曲线方程计算测得药片中羟丙甲纤维素的含量为 0.342 mg(二次方程和一次方程计算结果近似),药片中 PEG4000 的理论含量为0.4 mg,提取率85.5%。 HPLC-CAD 测定小牛肺注射液中的磷脂酰胆碱(PC)和溶血磷脂酰胆碱(LPC)含量。 2.分析条件 Phenomenex Luna silica(2),4.6*250 mm, 进样体积 20pL 流动相A 流动相B 检测器 CAD, 雾化温度:30℃;N2压力 35 psi 10 90 20 30 70 35 95 5 36 10 90 41 10 90 图1. PC定量限艮定谱图(0.7788 mg/mL, 进样1pL) 图2. LPC 定量限测定谱图(0.0954mg/mL, 进样2pL) 图3.制剂供试品溶液则定普图 表1.检出限与定量限 S/N 浓度mg/mL 进样体积uL| 进样质量pg PC 检出限 3.0 0.779 0.3 0.234 定量限 11.7 0.779 1 0.779 LPC 检出限 4.8 0.0954 1 0.095 定量限 8.7 0.0954 2 0.191 表2.重复性实验结果 1 2 3 4 5 RSD% PC Area 73.570 73.707 73.952 74.589 74.262 0.560 LPC Area 7.186 7.401 7.168 7.373 7.175 1.597 表3.样品PC和LPC 含量测定结果 PC峰面积 PC平均含量% 相当标示量% LPC峰面积 LPC 平均含量% 相当标示量% 制剂1 141.1925 45.54 64.45 5.6007 0.96 1.36 制剂2 139.2847 44.69 5.5859 0.95 原料1 159.2194 69.91 67.97 10.997 2.49 2.49 原料2 158.2829 66.03 10.9991 2.49 表4.破坏性试验结果 项目 进样体积(uL) PC峰面积 PC含量(mg/支) PC变化率% 氧化 10 96.8867 27.08 -39.98 酸 10 74.6179 18.88 -58.15 碱 10 48.588 10.44 -76.86 光 10 78.0049 20.07 -55.51 高温 10 25.9529 4.39 -90.26 4.结论与建议 本实验采用 Dionex U3000 系列液仪色谱仪和CAD电喷雾式检测器联用测定小牛肺注射液中的磷脂酰胆碱(PC)和溶血磷脂酰胆碱(LPC),比之前其质量标准的薄层扫描法准确度和重现性都有很大提高,而且灵敏度比ELSD 检测器有所提高,LPC的线性也较 ELSD 更好。该注射液为小牛肺表面活性物质的灌洗液,其磷脂酰胆碱中的脂肪酸脂肪链长短不一致,较从大豆等植物中提取的 PC 组成结构更为复杂,导致PC的峰形较难看,而LPC 还存在异构现象导致其呈现出色谱峰不能完全分开的状态,一般计算 LPC 的含量都是将峰积分到一块计算。破坏性试验显示各强制降解条件下PC 的含量都有不同比例的下降,这就要求药品在运输、贮存和使用过程中,要避免上述影响因素,防止药物主成分的降解和一些有害或无益身体的成分的生成,合理安全用药。 1.方法简介 PEG是一种药用辅料,也是某些蛋白药物合成的原料药。在原料药的质量控制中,需要对残留的 PEG 做定量分析。PEG紫外吸收极弱,无法用 UV 检测器检测。 2.分析条件 流动相 时间(min) 流动相A 流动相B 0 10 10 10 90 10 25 0 100 35 0 100 40 90 10 50 90 10 3.谱图结果 表1.各浓度点 PEG 的峰面积 浓度ppm 峰面积 pA*min 第一次分析 峰面积 pA*min 第二次分析 两次分析峰面积RSD 0 未检出 未检出 未检出 0.4 0.1638 0.1643 0.21% 0.5 0.1989 0.1953 1.29% 1 0.4472 0.4328 2.32% 10 3.6210 3.5460 1.48% 图2.蛋白药物测试图 4.结论与建议 各浓度峰面积 RSD%小于2.5%,满足该项目各浓度峰面积 RSD%小于5%的要求PEG在0.4-10mg/L范围内具有良好的线性响应(R2>0.999) 在蛋白样品中,18.27 min附近(PEG出峰位置)无明显色谱峰,故判断该样品无 PEG 检出。 1.方法简介 将 PEG聚合物通过共价键接到小分子、大分子药物,以及脂质体、聚合物表面等的化学修饰是延长蛋白质药物半衰期的有效途径之一,例如 PEG 修饰能降低外源蛋白质的免疫原性,改善可溶性和生物学利用度,增加抗蛋白水解作用等。但残留的游离PEG具有一定毒性,需严格控制药物成品中PEG的残留量。PEG紫外吸收较弱,无法用紫外检测器获得高灵敏度检测。ELSD可实现弱(无)紫外吸收化合物的检测,但ELSD 灵敏度较低,且重复性较差。如 PEG 修饰的蛋白药物样品XX9中PEG 的残留检测,以 ELSD 为检测器, 检测限只能到1%,而国家标准的要求是0.1%。大量的研究表明,CAD 作为一种新型的通用性检测器具有比 ELSD 更高的检测灵敏度和重复性。本文以 CAD 为检测器,发展 PEG修饰药物样品XX9中残留PEG 的检测。 2.样品配制 分别称取 10 mg样品XX9 和 PEG样品,用乙腈定容至10mL,然后用乙腈分别将其稀释100、1000和10000倍,得到含量分别为1%、0.1%和0.01%的样品,上机测试。 CAPCELL PAK C18 SG300 4.6*250 mm, 色谱柱 流速 0.8 mL/min 流动相B 进样体积 10 pL 70 检测器 CAD, 蒸发温度:30℃,filter: 5.0, 70 15.00 采集频率:5Hz 50 25.00 90 10 45.00 90 10 45.01 30 70 50.00 30 70 1)含量为1%的样品 XX9和PEG样 图1.含量为1%的样品XX9样品测试结果 图2.含量为1%的PEG样品测试结果 对含量为1%的样品XX9和PEG 进行测试,其信噪比分别为170.5和230.1. 2)含量为0.1%的样品XX9和PEG样品测试结果 图3.含量为0.1%的样品 XX9样品测试结果 4)不同储藏时间对样品 XX9和PEG样品测试结果的影响 图4.含量为0.1%的 PEG样品测试结果 对含量为0.1%的样品XX9和 PEG进行测试,其信噪比分别为38.6和40.1。 图7.不同储藏时间1%样品XX9样品叠加谱图 3)量为0.01%的样品 XX9和 PEG 样品测试结果 图8.不同储藏时间1%PEG样品叠加谱图 图5.含量为0.01%的样品XX9样品测试结果 从图7和图8结果得出,,样品XX9 和 PEG 的随着储藏时间的增加响应值变低。 5.结论与建议 利用 U3000 系统和 CAPCELL PAK C18 SG300色谱柱,能够将样品XX9和 PEG进行分离,峰形对称,分离度好,能够满足测试的需求。 测试结果表明, CAD检测器不仅能够顺利检出样品XX9和PEG, 而且样品XX9检出限能够达到 10mg/mL的0.01%,PEG 的检出限能够达到 10mg/mL的0.1%,远远优于ELSD的检出限10mg/mL的1%。 图6.含量为 0.01%的 PEG样品测试结果 对含量为0.01%的样品XX9信噪比为3.9,含量为0.01%的 PEG进行测试未检出。 1.方法简介 吐温20 (Tween20),即聚山梨醇酯20 (Polysorbate 20),是一种非离子型表面活性剂,在生物制药行业中,常用作蛋白乳化剂。吐温20含有较多的亲水性基团,但没有强生色官能团,不适合用常规反相液相色谱-紫外检测器进行检测。蒸发光散射检测器虽然可以检测吐温20,但该检测器灵敏度低,重现性差。而电雾式检测器(CAD)作为一款通用型的质量检测器,适用于非挥发性物质和部分半挥发性物质的检测,具有高灵敏度和宽线性范围,是一款检测吐温20较为理想的检测器。 吐温20是一类强亲水性化合物,参考相关研究和实验报道,采用 Oasis MAX 色谱柱结合 CAD 检测器对其蛋白药物产品中吐温20含量进行测定。 图1.吐温20结构图 2.样品制备 吐温20标准品:精密称取一定量吐温20纯品,用水溶解定容至10 mg/mL,作为储备液待用。用2%甲酸水溶液作为稀释液,逐级稀释上述储备液,分别得到1.0、0.5、0.2、0.1、0.05、0.02、0.01和0.005 mg/mL 工作溶液。 吐温20产品:蛋白混悬产品,组成包括API、无机盐和吐温20,其中混悬物质为API, API不溶于水,能够溶解于50%乙腈。将该混悬液通过 0.45 pm 水相滤膜过滤后,直接进样分析。 流速 1.0 mL/min A,% B,% 进样体积 30 pL 90 10 CAD Corona VEO RS, 蒸发温度50℃,采集频 检测器 率5 Hz, filter 3.6 s 80 20 3.4 80 20 3.5 0 100 4.5 0 100 4.6 90 10 10 90 10 图2.空白(黑色)和0.1 mg/mL Tween20标品(红色)色谱图比较 图3.扣除空白后0.1 mg/mL Tween20标品色谱图 图4.低浓度(0.02 mg/mL) Tween20标品色谱图 图5.高浓度(0.5mg/mL)Tween20标品色谱图 图 6.Tween20 标品浓度-响应色谱图(0.01~100 mg/mL) 图8. Tween20标品检测限谱图(0.005 mg/mL水平) 图 9.Tween20 标品定量限谱图(0.01 mg/mL水平) 图7. Tween20标品二项式拟合标准曲线(0.01~100 mg/mL) 表 1. Tween20标品二以式拟合曲线、检测限和定量限检测结果 Compound Linear Range, mg/mL C0 (Offset) C1 ((Slope) C2 (Curve) B2 LOD,mg/mL S/N LOQ,mg/mL S/N Tween20 0.01~1.0 0.3978 81.22 -26.68 0.9991 0.005 6.5 0.01 13.5 表2. 0.1mg/mL Tween20标品分析重复性(n=7) Tween200.(1 mg/mL) Ret.Time,min Area, pA*min Height, pA 1 4.237 8.95 33.75 2 4.257 8.96 33.27 3 4.246 9.24 34.40 4 4.247 9.16 34.77 5 4.260 9.15 34.40 6 4.247 9.25 35.36 7 4.250 9.20 34.65 RSD% 0.18 1.37 1.99 图10. 0.1 mg/mL Tween20标品分析重复性谱图(n=7) 图11.1~10号(棕色瓶装) Tween20产品检测谱图比较 表3.1~10号(棕色瓶装)Tween20 产品含量测定结果 No. Ret.Time, min Amount. mg/ml Area, pA*min Height, pA 1 4.243 0.234 17.97 66.48 2 4.254 0.236 18.07 66.08 3 4.243 0.227 17.43 64.26 4 4.237 0.222 17.12 62.95 5 4.267 0.156 12.39 45.63 6 4.257 0.186 14.57 53.5 7 4.274 0.161 12.82 47.43 8 4.230 0.227 17.46 65.17 9 4.267 0.103 8.500 30.53 10 4.254 0.170 13.44 50.11 图12.6号Tween20 产品含量测定重复性谱图(n=6) 表4. 6号 Tween20 产品含量测定重复性(n=6) 6号Tween20 产品 Ret.Time, min Amount. mg/ml Area, pA*min Height, pA 1 4.244 0.1833 14.39 53.1 2 4.257 0.1859 14.57 53.5 3 4.263 0.1862 14.59 53.55 4 4.250 0.1864 14.61 53.55 5 4.250 0.1850 14.51 53.22 6 4.264 0.1841 14.44 53.73 RSD% 0.19 0.67 0.61 0.44 1)在进空白样时发现在 Tween20 出峰位置有干扰(图2),导致进 Tween20标品时峰形拖尾严重,通过扣除空白,峰形得到改善(图3),因此,本实验中所有谱图在没有特殊说明情况下均为扣除空白后谱图; 2) 由于 CAD 在较宽浓度范围内是非线性响应,故将Tween20 的峰面积与含量的关系用二项式回归进行拟合分析,回归方程为 Y=0.3978+81.22x-26.68x²(图7),相关系数(R²)为0.9991,线性范围为0.01~100 mg/mL(表1);方法检测限为0.005 mg/mL(信噪比S/N=6.5),定量限为0.01 mg/mL (信噪比 S/N=13.5) ; 3) 0.1 mg/mL Tween20 标品的保留时间和峰面积RSD值分别为0.18%和1.37%(图10和表2);6号 Tween20 产品的保留时间和峰面积RSD 值分别为 0.19%和0.61%(图12和表4),方法重复性良好;根据二项式回归拟合曲线计算1~10号产品中 Tween20 的实际含量,结果见图 11和表3,含量基本在0.10~0.24 mg/mL之间,在估值范围内。 利用 CAD 对 Tween20 进行检测,方法准确度高,重复性好,通过二项式回归分析,相关性良好,检测限较低,说明 CAD检测器可以很好地满足检测需求,是检测 Tween 类样品较为理想的一种检测器; Oasis MAX 在分离产品中蛋白类物质和Tween20 时表现出较好的分离性能,在酸性流动相条件下,使得蛋白和其其赋形剂可以在死时间出峰,避免对 Tween20 出峰形成干扰,同时使用异丙醇作为有机相,可以将 Tween20洗脱成一个单峰,有利于定量。 1.方法简介 聚氧乙烯脱水山梨醇单油酸酯,简称吐温80,是一种非离子型表面活性剂及乳化剂,由山梨聚糖和油酸通过乙氧基化制得;对于非肠道给药的药剂而言,吐温80可以作为一种赋形剂,如加拿大和一些欧洲国家生产的流感疫苗,它也可以在一些药物的生产过程中用作乳化剂,如常见的抗心律失常药物胺碘酮。参考相关研究和实验报道,采用Oasis MAX 色谱柱结合 CAD检测器对其蛋白药物产品中吐温80含量进行了测定。 2.样品制备 对照品溶液酒制及测试:精密称取适量吐温80对照品,用水稀释定容,浓度为 1.14 mg/mL;后用水稀释配制标准工作溶液浓度分别为:10 pg/mL、20 pg/mL、30 pg/mL、40 pg/mL、50 pg/mL、60 pg/mL、70 pg/mL、80 pg/mL、90 pg/mL、100 pg/mL、200 pg/mL。 供试溶液配制及定量测试:缓冲样品不稀释,1号样品稀释10倍,2号样品稀释50倍,调整前样品稀释10倍,调整后样品稀释20倍,进行测试、定量。 Oasis MAX, 2.1×20mm, 30 um, Time, min A,% B, % 0 90 10 1 80 20 3.4 80 20 3.5 0 100 4.5 0 100 4.6 90 10 10 90 10 1)对照品扣除试剂空白后的测试谱图 图1.20 pg/mL 吐温80对照品扣除试剂空白色谱图 2)标准曲线及其相关系数 图2.对照品工作曲线(Y=-0.0001x²+0.1634x-0.0919, R²=0.9990) 按照峰面积(两针样品的峰面积平均值)与浓度计算 Quad,WithOffset, Avg标准曲线(图2)。 3)样品测试 图3.缓冲样品测试色谱图 图4.1号样品稀释测式色谱图 图5.2号样品稀释测试色谱图 图6.调整前样品稀释测试色谱图 图7.调整后样品稀释测试色谱图 表1.5个样品中吐温80的含量 样品名称 缓冲样品 1号 2号 调整前 调整后 吐温80含量(mg/mL) 0.019 1.00 1.91 0.90 2.05 根据要求将未分离物质计入吐温80的含量。如表1所示缓冲样品中吐温80含量为0.019 mg/mL, 1号样品中吐温80含量为1.00 mg/mL,2号样品中吐温80含量为1.91mg/mL, 调整前样品中吐温80含量为 0.90 mg/mL, 调整后样品中吐温80含量为2.05 mg/mL。 5.结论 本实验使用 CAD 检测器分析药物制剂中的吐温80,吐温80在色谱柱上的保留效果较好,能够满足检测需求。 10 pg/mL 的吐温80对照品可以检出,信噪比可达20;同时10 pg/mL-200 ug/mL共计7个点的标准曲线(标准曲线范围过宽,建议选择利用 Quad, WithOffset, Avg标准曲线来计算结果) R²大于0.999,能够满足检测需求。 缓冲样品中吐温80含量为 0.019 mg/mL,1号样品中吐温80含量为 1.00 mg/mL, 2号样品中吐温80含量为 1.91 mg/mL,调整前样品中吐温80含量为 0.90 mg/mL,调整后样品中吐温80含量为 2.05 mg/mL。 1.方法简介 盐酸胍是生物制药中的常用试剂,但在制药工艺最后环节需对胍和氯离子加以去除,并采用适宜方法检测残留的胍和氯离子含量,本方法采用 CAD 对蛋白药物中盐酸胍的残留量进行了分析。 2.样品制备 盐酸胍对照品(0.0045,0.009, 0.018, 0.039, 0.078, 0.15625,0.3125,0.625,1.25,2.5和5 mg/mL) 和样品1,2,3溶液。 3.分析条件 色谱柱 Trinity P1, 3.0x 100 mm, 3 pm, PN: 071387 柱温 30℃ 流动相 乙:100 mM NHAc ( pH 5.3) 水:(30:14:56,v:v:v) 流速 1.0mL/min 进样体积 10uL 检测器 CAD, 蒸发温度35℃,采集频率10 Hz, Filter 5.0 s 1)胍和氯离子线性曲线 图1.不同浓度胍和氯离子样品 从低到高,样品浓度依次为0.0045,0.009, 0.018,0.039,0.078 mg/mL。 ·在0.0045-0.078 mg/mL范围内, 取 power function 值为1.0,氯离子和胍都具有很好的线性。氯离子线性方程: A=9.2651C+0.026, R²=0.999;胍线性方程:A=23.237C+0.030,R²=0.999。A:峰面积,单位 pA *min; C:样品浓度(进样体积为 10 pL), mg/mL. ( · 在 0.0045-0.3125 mg/mL范围内,1 ,取 power function 值 为1.3,氯离子和胍都具有很好的线性。氯离子线性方 程: A=12.4822C-0.0318, R²=0.999;胍线性方程:A=33.1371C -0.02 6 1, R²=0.999 。 A:峰面积 , 单位 pA*min;C:样品浓度(进样体积为10pL), mg/mL。 ) ·当样品浓度超过 0.3125 mg/mL (进样体积为10pL),色谱峰展宽严重,无法实现两个组分的分离和定量。减少进样体积可以实现更高浓度样品的线性分析,但更关注的是低浓度区域的样品浓度,因此不需要做减少进样体积后的线性曲线。 图2.1,2,3号样品分析 样品:1,2,3号样品稀释1000倍后,进样10pL。 ·三个样品均没有胍检出,但氯离子出峰位置处有很强的响应。 。原样浓度过高,超出了线性范围。将原样稀释1000倍,进样10pL,每个样品进样三次。如果5.38 min出峰的化合物为氯离子,通过线性曲线计算,得到样品1,2,3中氯离子浓度如下表所示。 三个样品的浓度没有明显差异。 表1.样品1,2,3中氯离子浓度 样品编号 峰面积(pA*min) 稀释1000倍样品浓度(mg/mL) 样品浓度(mg/mL) 1 0.165 0.0150 14.956 2 0.162 0.0147 14.690 3 0.177 0.0163 16.294 5.结论与建议 。该方法可以为氯离子和胍提供较好的分离度,较高的检测灵敏度和较宽的线性。 ·三个样品中均没有胍检出。在氯离子出峰处,有较强的响应。如果该色谱峰为氯离子,三个样品氯离子浓度没有显著差异,都在 14.5-16.5 mg/mL范围内。 ·用衬管装样品,进样前需要注意衬管中(尤其是衬管尖底部分)是否有气泡。如果有气泡需要用移液枪将气泡赶出,并将样品混合均匀。 样品浓度过高时,如超过 0.1 mg/mL, 需要将样品稀释后进样分析。如本实验中,样品浓度过高,即使进1pL,仍然超出线性范围。稀释1000倍后进10uL, 峰面积很好的出现在线性范围之内。 疫苗辅料分析解决方案 蔗糖作为低端而廉价的冻干保护剂广泛用于疫苗制品中。冻干保护剂的组成对疫苗质量有重大影响,因为保护剂不仅关系到冻干疫苗的稳定性,而且影响到疫苗复溶后的效价、渗透压等于疫苗质量息息相关的因素,因此对冻干疫苗中蔗糖组分进行定量分析对疫苗的质量控制具有重要意义。——杨烨等,中国生物制品学杂志,2015,411。 2.样品制备 ·线性、LOQ、LOD:用1 mg/mL蔗糖对照品溶液用75%乙腈水稀释成以下浓度:500,250,125,62.5,31.25,15.63,7.81,3.91,1.95,0.49,0.146 pg/mL。 供试品溶液和重复性: 1.脱糖起始始:取脱糖起始液300 pL,加乙腈2700 pL,涡旋 1 min 后,用10000 r/min 离心 10 min。取上清液过0.22pm滤膜,透过液用75%乙腈水稀释100倍(相当于原溶液稀释了1000倍),进样分析。取其中一批(BV-1603-005)分析6次。 2.脱糖终止液:取脱糖终止液300 pL, 加乙腈2700 pL,涡旋1 min 后,用10000 r/min 离心 10 min。取上清液过0.22 um滤膜,透过液用75%乙腈水稀释10倍(相当于原溶液稀释了100倍),进样分析。 3.原液:取原液300uL, 加乙腈2700 uL, 涡旋 1 min 后,用10000 r/min 离心 10 min。取上清液过 0.22 pm滤膜,进样分析。 ●准准确度: 1)稀释液:原液1mL,加乙腈9 mL, 涡旋 1 min 后,用10000 r/min 离心10 min。取上清液过 0.22 um 滤膜,作为稀释液。 2)样品溶液:取浓度为1000 pg/mL,2250 ug/mL, 62.5pg/mL的蔗糖溶液各100pL,用稀释液分别稀释到1mL。 ( 3)对照溶液:取浓 度 为 1000 pg/mL, 2 5 0 pg/mL, 6 2.5 pg/mL 的蔗糖溶液各100pL,用75%乙腈水分别稀释到1mL。 ) 4)回收率计算: (样品溶液中蔗糖峰面积-稀释液中蔗糖峰面积)除以对照溶液中蔗糖峰面积,再乘以100%。 ·专属性:取空白溶液300pL,加乙腈2700 pL, 涡旋1min 后,用10000 r/min 离心 10 min。取上清液过0.22um滤膜,进样分析。 3.分析条件 色谱柱 Shodex NH2 (4.6x250 mm, 5um); PN: F7630001; SN:N1610109 柱温 30℃ 流动相 乙腈:水(75:25,V:V) 流速 1.0 mL/min 进样体积 20 pL 检测器 CAD, 蒸发温度55℃,采集频率10 Hz, Filter 5.0 s 4.谱图结果 1)蔗糖工作曲线、LOQ和LOD 图1.以A=aC+b拟合, 得蔗糖工作曲线 样品浓度从高到低:31.25,15.63,7.81,3.91, 1.95,0.976 ug/mL 。浓度为0.488 pg/mL的样品进样20 pL, S/N 为12;根据定量限应该高于10倍S/N 的规定,0.488 pg/mL 为该方法的定量限。 ·浓度为 0.146 pg/mL 时, S/N 为4.0;根据检出限应该高于3倍S/N 的规定, 0.146 pg/mL 为该方法的检出限。。·在0.976-31.25 ug/mL浓度范围内,进样量与峰面积之间呈现很好的线性关系,满足R²不小于0.998的要求。 6针重复进样,峰面积RSD%为1.88%, 满足RSD%不高于10%的要求。 2)方法重复性 图2.样品1稀释1000倍后进样分析6次 3)回收率 a)加标6.25 pg/mL的蔗糖回收率98.9% 图3.回收率测定1 b)加标25 pg/mL 的蔗糖回收率97.6% 图4.回收率测定2 c)加标100 pg/mL 的蔗糖回收率100.5% 图5.回收率测定3 4)专属性 图6.用乙腈沉淀后的空白溶液(相当于稀释10倍) 在稀释10倍后的空白溶液中,无蔗糖检出。 a)原液 图7.原液样品1/2/3/4/5/6分析 。样品4和样品5在蔗糖出峰的位置有响应,含量分别为0.92 pg/mL 和0.103 pg/mL。 其它批次的原液中没有蔗糖检出。 b)脱糖起始液 图8.脱糖起始液样品1/2/3/4/5/62分析 脱糖起始液(稀释1000倍后)样品1/2/3/4/5/6的蔗糖浓度依次为3.531 pg/mL, 3.6929 ug/mL, 3.794 pg/mL,4.283 pg/mL, 4.712 ug/mL, 4. 459 pg/mL. ( ·所有脱糖起始液中蔗糖浓度都大于30%的浓度。 ) 图9.脱糖终止液样品1/2/3/4/5/6分析 脱糖终止液(稀释1000倍后)样品1/2/3/4/5/6的蔗糖浓度依次为9.341 ug/mL, 4.974 ug/mL, 9.147 pg/mL, 9.996ug/mL, 7.872 pg/mL, 9.742 pg/mL。 ·所有批次的终止液都满足或者接近蔗糖浓度不超过 100 pg/mL的要求。 ·本方法具有较宽的线性范围和较高的灵敏度,线性曲线满足R²>0.998的要求; 。方法具有较好的准确度,满足峰面积RSD 值小于10%的要求; 。该方法具有较好的回收率,三个待测浓度的回收率均满足在80-120%的要求; 。空白溶液中无蔗糖检出,满足没有蔗糖检出的预期; ·原液有两个批次有蔗糖检出,其余批次无蔗糖检出。 ●脱糖起始液的蔗糖浓度在3.5-5g/L 的范围内。 房蔗糖终止液的蔗糖浓度在40 mg/L-100 mg/L的浓度范围,满足会接近脱糖终止液蔗糖浓度不高于 100 mg/L 的要求。 1.方法简介 与化药一样,为了增强疫苗的效果、延长免疫记忆、调整体液和细胞反应,疫苗的生产过程中往往需要加入一定量的辅料。在疫苗辅料中存在大量无(弱)紫外吸收的化合物,如胆固醇、磷脂和皂苷。本文以 CAD 为检测器,发展了疫苗辅料中胆固醇、DPPC、Lyso-PC 和皂苷的定量方法,并用于疫苗辅料AblSCO 中这些成分的含量测定。并将该方法与 UV 210 nm检测做对比。 2.样品制备 a)单标的配制 样品溶剂:将30 mL乙醇与 70 mL 超纯水混合。将20 mg皂苷混合物溶于 10 mL样品溶液中,配成2mg/mL。通常皂苷混合标准品中皂苷含量在20-35%,仅用于估计辅料中皂苷含量。称取20 mg DPPC 和Lyso-PC 溶于 10mL样品溶液中,配成2 mg/mL。称取 20 mg 胆固醇溶于 10 mL样品溶液中,配成2 mg/mL。配制好的标准品溶液在4-8℃下可存放一个月。 b)标准品混合溶液 取1mL皂苷、DPPC和胆固醇溶液和 0.25 mL Lyso-PC溶液,用样品溶液稀释到5 mL。 c)工作曲线 用对照品混合溶液配制浓度为400,200,160,80,40, 20, 10,3和1.5 pg/mL。 d)样品溶液 取 100 pL AbISC0-100 溶液,加入400 pL 超纯水后混合均匀。 流速 0.5 mL/min B,% 进样体积 2uL(样品室温度8℃) 35 0 CAD,蒸发温度50℃,采集频率20 Hz, 35 检测器 Filter 5.0s DAD,210nm,采集频率20 Hz 90 13 10 90 4.谱图结果 图 1. CAD检测对照品混合容液 图2.CAD(黑)和紫外(紫)检测 AblSCO 溶液 表1.日内重复性考察(n=10) 分析物名称 保留时间(min) 浓度(pg/mL) 保留时间 RSD% 峰面积 RSD% 皂苷类 4.8 74.1 0.05 1.5 Lyso-PC 6.4 61.3 0.05 0.87 胆固醇 8.1 75.7 0.02 1.1 DPPC 9.6 76.5 0.02 0.67 Amount [ug/mL] Amount [ug/ml] 图3.皂苷(左上)、Lyso-PC(右上)、胆固醇(左下)和 DPPC(右下)工作曲线 表2.工作曲线 分析物名称 保留时间(min) 浓度 (ug/mL) B² 皂苷类 4.8 1.5-400 0.9999 Lyso-PC 6.4 0.38-100 0.9998 胆固醇 8.1 1.5-400 0.9999 DPPC 9.6 1.5-400 0.9996 5.结论与建议 与紫外检测器相比, CAD 检测皂苷、胆固醇、DPPC 和 Lyso-PC具有更高的灵敏度; · CAD方法具有较宽的线性范围和较好的重复性,可用于疫苗辅料样品 AbISCO中各辅料成分的定量分析。 生物制药中硬脂酸和棕榈酸的检测 1.方法简介 某生物药生产过程中使用过棕榈酸和硬脂酸,需要对成品中棕榈酸和硬脂酸的残留量加以控制。由于脂肪酸类物质近紫外区吸收较弱,紫外检测器不能满足低浓度样品分析的要求,而 CAD 是一款通用型检测器,适用于不挥发或半挥发样品的检测(灵敏度优于ELSD),可使用梯度洗脱分离复杂样品(优于RI),非常适于该原料药的检测。 2.样品制备 空白溶液:60%乙腈。 混合对照溶液:取棕榈酸、硬脂酸适量,精密称定,以60%乙腈溶解制成含棕榈酸 10 ug/mL、硬脂酸4 ug/mL的混合对照溶液。 供试品溶液:取待用适量,精密称定,以60%乙腈溶解制成浓度为 5mg/mL 的溶液。 进样体积 10uL B,% 检测器 CAD Veo RS, 蒸发温度30℃, Filter 5.0 s 70 8 10 90 8.5 10 90 8.6 30 70 12 30 70 图1.空白及混标测试结果(黑:空白溶剂红:混标) 图2.样品1测试结果 图3.样品2测试结果 图4.样品3测试结果 1、混标考察结果(图1): 保留时间 平均峰面积 信噪比 峰面积RSD% 棕榈酸 3.59 1.29 734 0.80 硬脂酸 6.11 0.92 461 0.32 2、样品考察结果(图2~图4) 保留时间 平均峰面积 样品1 未检出 未检出 样品2 0.18 ug/ml 0.12 ug/ml 样品3 0.27 ug/ml 0.21 ug/ml 由于 CAD 通常使用多点校正法以提高测定结果的准确度,以上结果仅供参考。 5.结论与建议 1.方法灵敏度分析:按照样品浓度 5000 pg/mL计算, 使用 CAD 检测器实际检出棕榈酸和硬脂酸的残留量在主成分含量0.01%以下,完全满足该产品日常质控要求。 2.方法重现性分析:混标考查两种成分峰面积的 RSD 在1.0%以下,说明 CAD 检测的方法重现性较好。 3.相比原条件(乙酸-乙腈-四氢呋喃体系,总分析时间为 30min,色谱柱为 xselect CSH C18 ( 4.6×150mm, 3.5um), 进样量为50 pL, 测试过程发现该条件的基线噪音过大(见下图),推测可能是由于该色谱柱流失和流动相中非挥发性杂质带来的影响),本方法具有显著优势( Accucore C18 (2.1×50mm, 2.6pm),并使用乙腈-水系统后,基线情况明显得到改善,且分析时间缩短为 12min, 效率提高约60%)。 前景与展望 为了提高生物制剂的有效性,各种新型的辅料成分被不断的开发并引入到生物制药领域,发挥着举足轻重的作用,如提高药物利用度,防止变性或聚集,延长免疫记忆持续时间,调节相关的体液和细胞反应等等;但同时该行业也亟需各种新技术、新方法解决生物药物质量控制中不断出现的新问题,确保药物的安全性。 针对大多数药物辅料没有紫外吸收这一行业共性问题,赛默飞世尔科技推出了电雾式检测器(CAD)解决方案,结合赛默飞先进的色谱柱技术,自动化的数据处理系统,相信可以帮助更多的生物制药客户建立更可靠的分析方法和更完善的质控体系。 赛默飞世尔科技 上海 南京 上海市浦东新区新金桥路27号3,6,7号楼 南京市中央路201号南京国际广场南楼1103室 邮编201206 邮编210000 电话021-68654588*2570 电话021-68654588*2901 生命科学产品和服务业务 上海市长宁区仙霞路99号21-22楼 邮编200051 西安 电话021-61453628/021-61453637 西安市高新区科技路38号林凯国际大厦 1006-08单元 邮编710075 北京 电话029-84500588*3801 北京市东城区北三环东路36号环球贸易 中心C座7层/8层 邮编100013 昆明 电话+86 10 8794 6888 成都成都市临江西路1号锦江国际大厦1406室邮编610041电话 028-65545388*5300沈阳沈阳市沈河区惠工街10号卓越大厦3109室邮编110013电话 024-31096388*3901武汉武汉市东湖高新技术开发区高新大道生物园路生物医药园C8栋5楼邮编430075电话027-59744988*5401 云南省昆明市五华区三市街6号柏联广场写字 楼908单元 邮编650021 电话0871-63118338*7001 广州 广州国际生物岛寰宇三路36、38号合景 星辉广场北塔204-206单元 邮编510000 电话 020-82401600 欲了解更多信息,请扫描二维码关注我们的微信公众账号 赛默飞世尔科技在全国有共21个办事处。本资料中的信息,说明和技术指标如有变更,恕不另行通知。 热线8008105118 赛默飞 赛默飞色谱 电话4006505118 官方微信 口 与质谱中国 www.thermofisher.com The world leader in serving science 本实验建立HPLC-CAD法测定注射用乳糖辅料及其相关制剂中乳糖含量。经过精密度、重复性、线性等方法学考察, 表明本方法准确度高,精密度、重现性较好,在 1.0 ~ 100 μg/mL 范围内,线性相关较好(r 2 =0.9998),定量限 达 0.5 μg/mL,可作为原辅料及制剂中乳糖的含量测定方法。CAD 作为质量型检测器,当需要检测更低浓度样品, 可以通过适当增大进样体积,或进行柱后有机相补偿,提高化合物的响应,降低定量检出限。同时,由于该检测 器响应因子一致,可以通过乳糖的浓度同步对其它糖类药物进行初步半定量分析。总体而言,该方法设计巧妙, 原理新颖,操作使用方便,取得了较理想的结果,因此具有较好的推广与借鉴意义。
确定







还剩30页未读,是否继续阅读?
赛默飞色谱与质谱为您提供《乳糖中蛋白药物检测方案(液相色谱仪)》,该方案主要用于其他中蛋白药物检测,参考标准--,《乳糖中蛋白药物检测方案(液相色谱仪)》用到的仪器有赛默飞Vanquish Flex液相色谱二元系统、赛默飞Corona CAD电喷雾检测器
推荐专场
色谱检测器/蒸发光检测器/紫外检测器
更多
相关方案
更多
该厂商其他方案
更多
















