方案详情
文
使用大曹三耀中等极性色谱柱CAPCELL PAK C18 MGII色谱柱,按照《GB 5009.86-2016》方法微调进行分析可得到分离度为1.28的良好分离(大于客户要求的0.90);同时,开发了不添加离子对试剂的新方法,使用MGII、AQ、ADME三款色谱柱均能实现良好分析结果。
方案详情

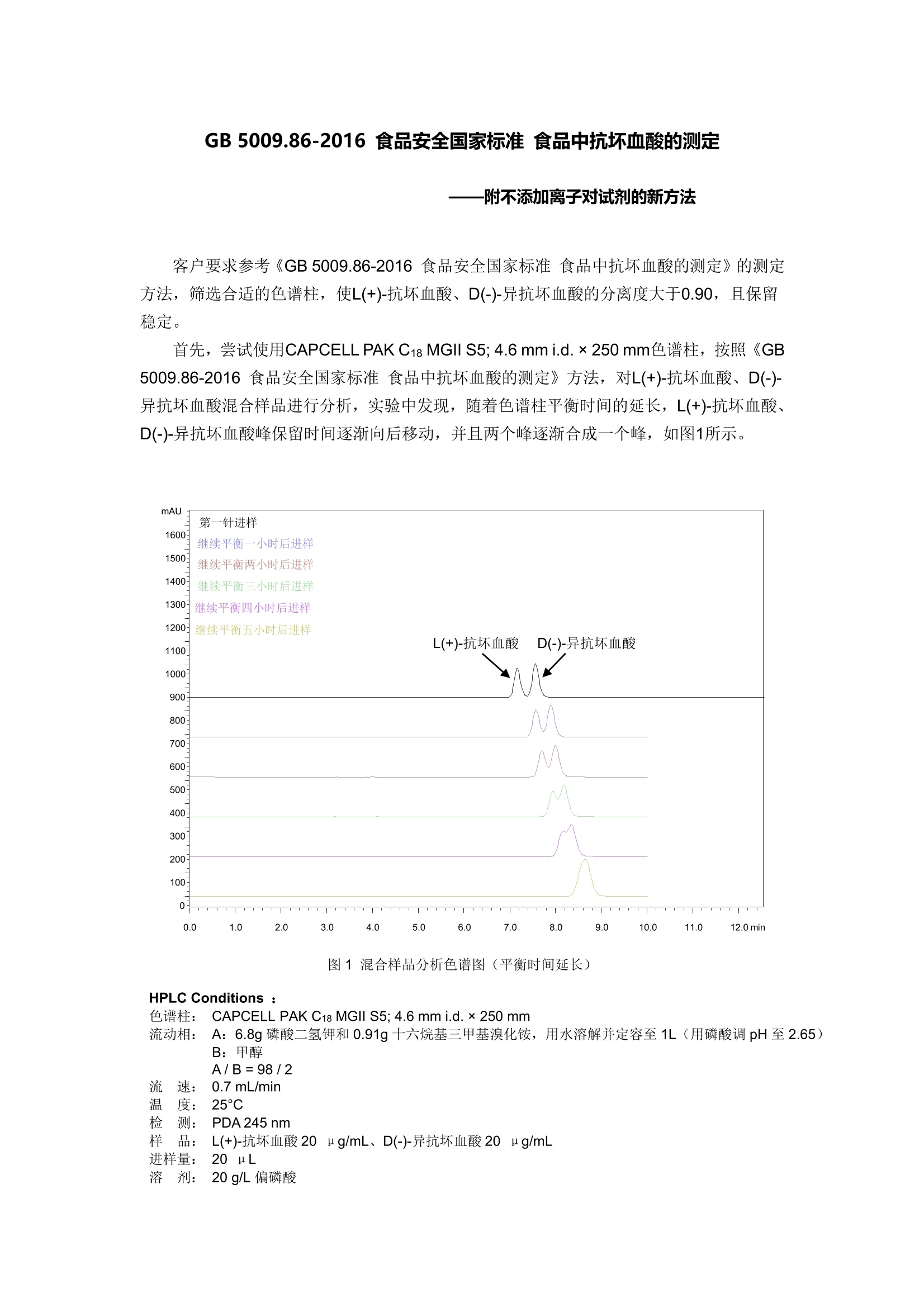
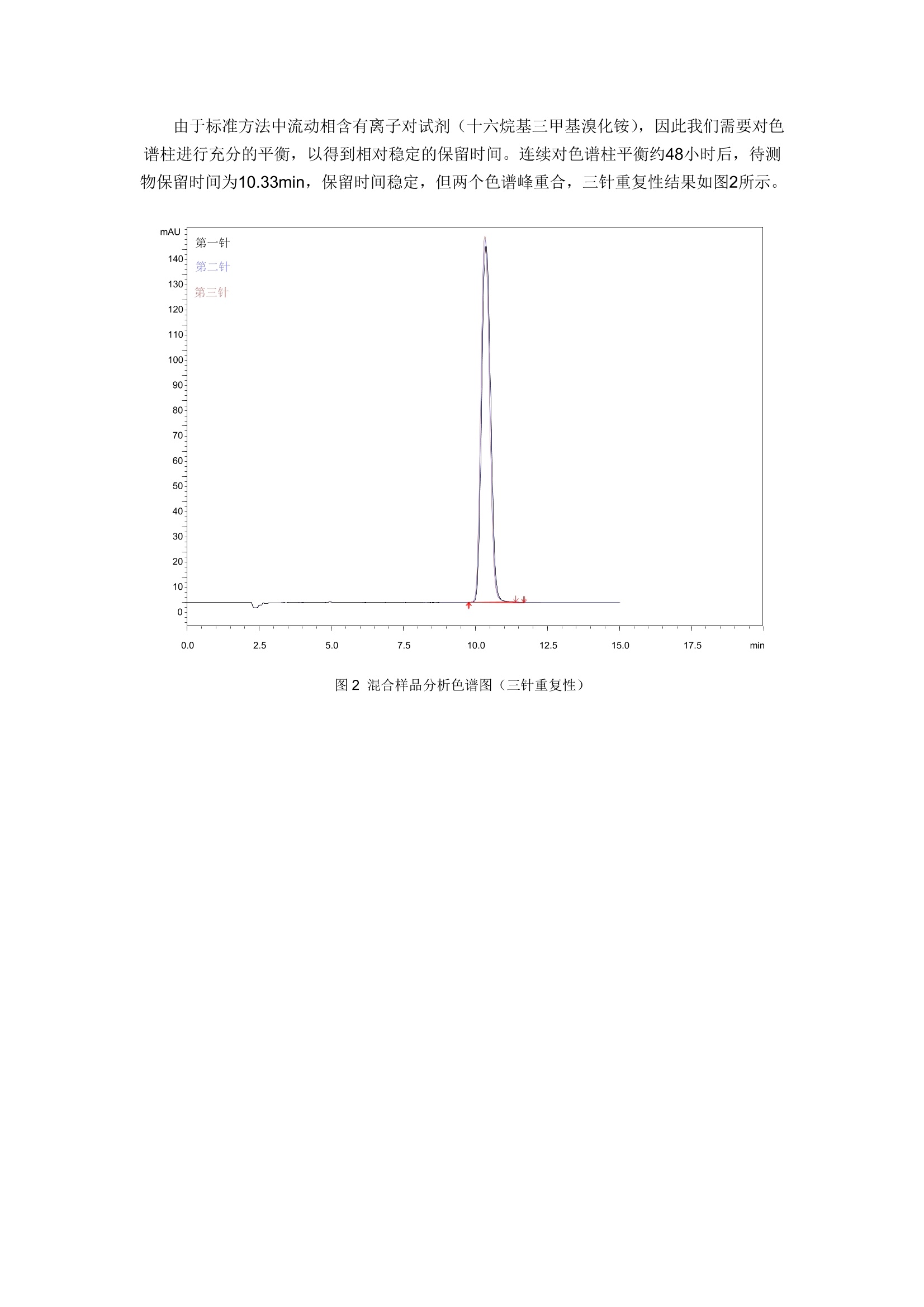
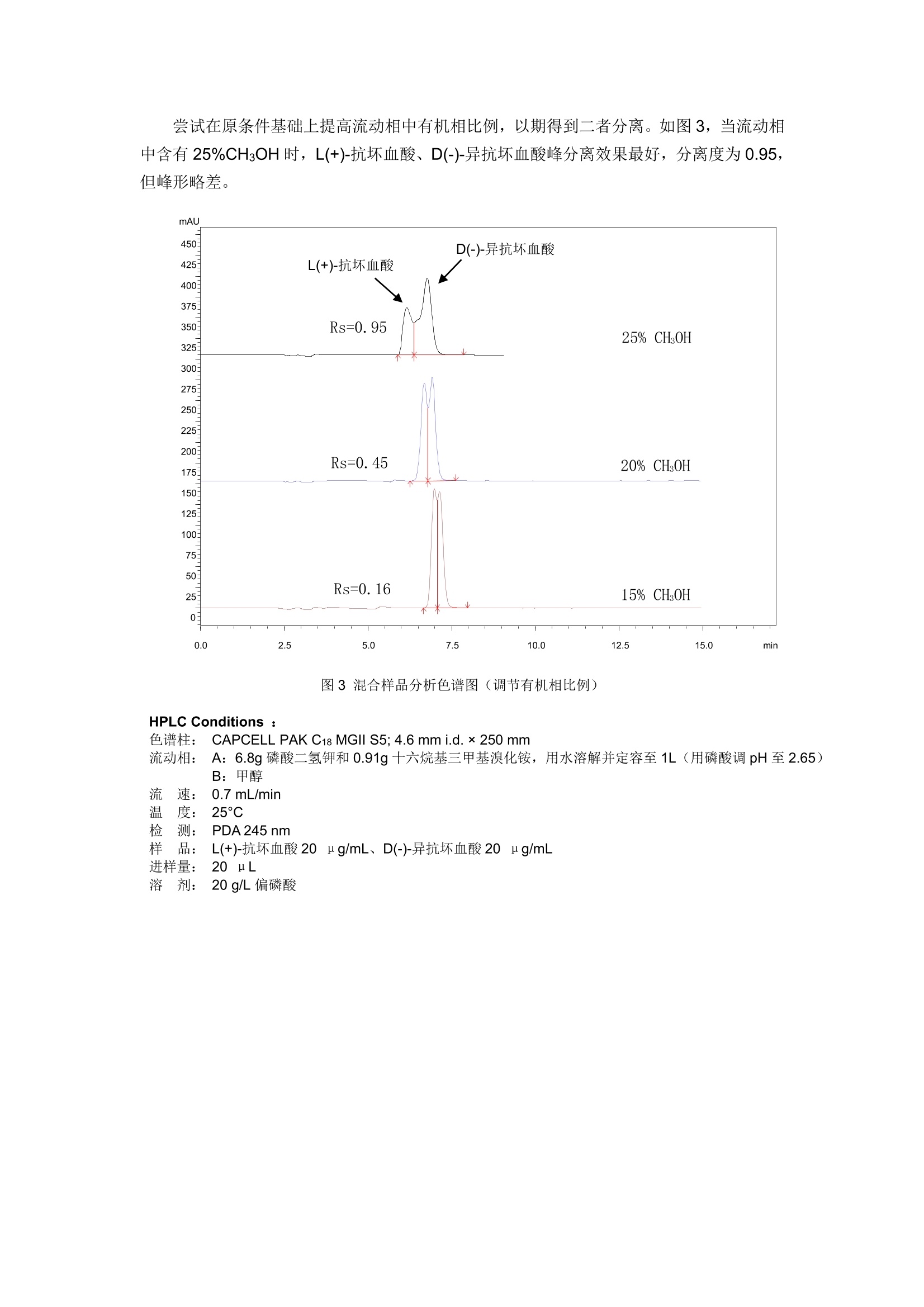
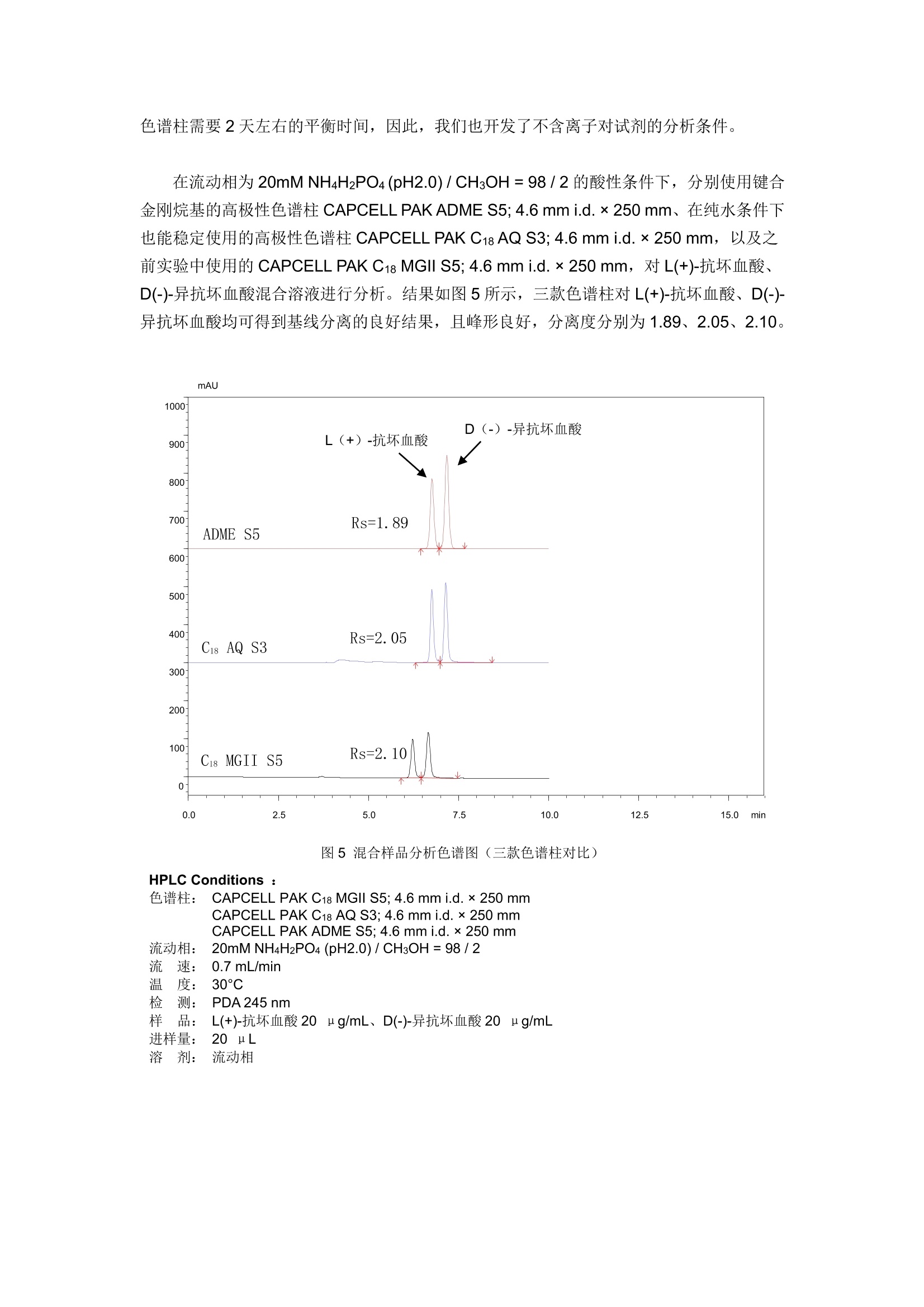
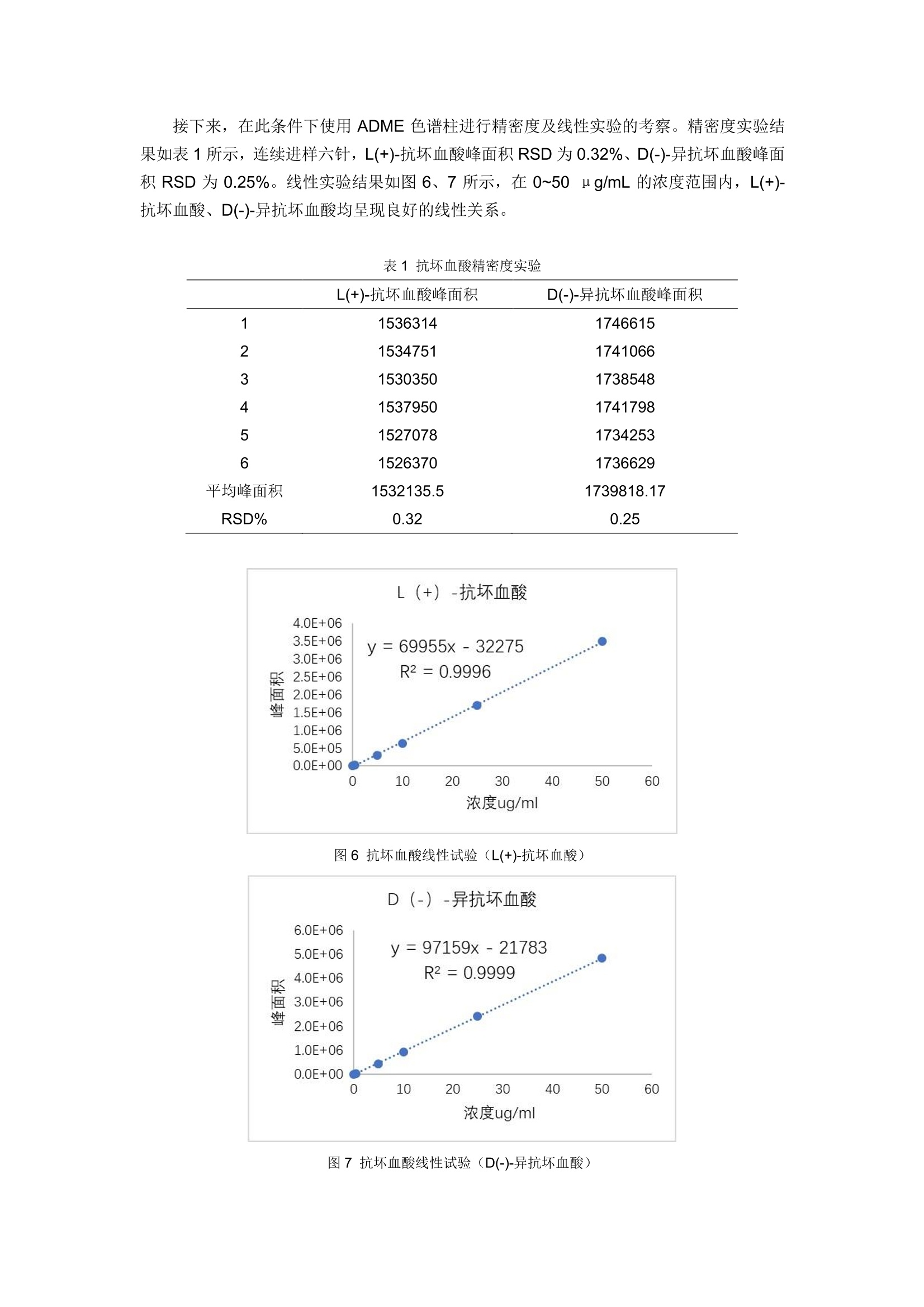
GB 5009.86-2016食品安全国家标准食品中抗坏血酸的测定 —-附不添加离子对试剂的新方法 客户要求参考《GB 5009.86-2016 食品安全国家标准食品中抗坏血酸的测定》的测定方法,筛选合适的色谱柱,使L(+)-抗坏血酸、D(-)-异抗坏血酸的分离度大于0.90,且保留稳定。 首先,尝试使用CAPCELL PAK C18 MGII S5; 4.6 mm i.d.×250 mm色谱柱,按照《GB5009.86-2016食品安全国家标准食品中抗坏血酸的测定》方法,对L(+)-抗坏血酸、D(-)-异抗坏血酸混合样品进行分析,实验中发现,随着色谱柱平衡时间的延长, L(+)-抗坏血酸、D(-)-异抗坏血酸峰保留时间逐渐向后移动,并且两个峰逐渐合成一个峰,如图1所示。 图1混合样品分析色谱图(平衡时间延长) HPLC Conditions : 色谱柱: CAPCELL PAK C18 MGII S5; 4.6 mm i.d. ×250 mm C流动相:AA: 6.8g磷酸二氢钾和0.91g 十六烷基三甲基溴化铵,用水溶解并定容至1L(用磷酸调pH至2.65)B:甲醇 A/B=98/2 流0.7 mL/min温 检样 25°C PDA245 nm L(+)-抗坏血酸20 ng/mL、D(-)-异抗坏血酸20 ng/mL 进样量: 20uL 溶 剂: 20 g/L 偏磷酸 由于标准方法中流动相含有离子对试剂(十六烷基三甲基溴化铵),因此我们需要对色谱柱进行充分的平衡,,以得到相对稳定的保留时间。连续对色谱柱平衡约48小时后,待测物保留时间为10.33min,保留时间稳定,但两个色谱峰重合,三针重复性结果如图2所示。 图2混合样品分析色谱图(三针重复性) 尝试在原条件基础上提高流动相中有机相比例,以期得到二者分离。如图3,当流动相中含有 25%CH3OH时, L(+)-抗坏血酸、D(-)-异抗坏血酸峰分离效果最好,分离度为0.95,但峰形略差。 图3混合样品分析色谱图(调节有机相比例) HPLC Conditions : 色谱柱:CCAPCELL PAK C18 MGII S5; 4.6mm i.d.×250 mmA 流动相: A: 6.8g磷酸二氢钾和0.91g 十六烷基三甲基溴化铵,用水溶解并定容至1L(用磷酸调pH至2.65)B:甲醇 流0.7 mL/min温 检样 25°C PDA 245nm L(+)-抗坏血酸20 ng/mL、D(-)-异抗坏血酸 20 ng/mL 进样量: 20uL 溶 剂: 20 g/L 偏磷酸 为改善峰形,尝试将柱温由25℃提高到30℃,结果如图4所示。L(+)-抗坏血酸、D(-)-异抗坏血酸峰形得到明显改善,二者分离度为1.28,大于客户要求的0.90。我们也尝试进一步提高流动相中有机相比例、温度以及改变有机相种类,未得到更好的分析结果。 图4混合样品分析色谱图 (25%CH3OH 30℃) HPLC Conditions : 色谱柱:CAPCELL PAK C18 MGII S5; 4.6 mm i.d. ×250 mm 流动相:AA: 6.8g磷酸二氢钾和0.91g 十六烷基三甲基溴化铵,用水溶解并定容至1L(用磷酸调pH至2.65)B:甲醇 A/B=75/25 流速0.7 mL/min温度检测样品 30C PDA 245 nm L(+)-抗坏血酸20 ng/mL、D(-)-异抗坏血酸20 ug/mL 进样量: 20uL 溶 剂: 20 g/L 偏磷酸 此外我们还尝试使用保留能力较 MGII 稍弱的 CAPCELL PAK C18 UG120 S5; 4.6 mmi.d.×250 mm色谱柱,经流动相充分平衡后,在同样条件下对 L(+)-抗坏血酸、D(-)-异抗坏血酸混合溶液进行分析,也未得到更好的分离结果。 上述实验中,我们在原条件基础上将流动相中有机相比例及柱温调整为25%CH3OH、30℃, 使用 MGII色谱柱进行分析,可得到L(+)-抗坏血酸、D(-)-异抗坏血酸分离度为1.28的最佳分离结果,但二者仍未达到基线分离。且使用添加离子对试剂的流动相进行分析时, 色谱柱需要2天左右的平衡时间,因此,我们也开发了不含离子对试剂的分析条件。 在流动相为20mMNH4H2PO4(pH2.0)/CH3OH=98/2的酸性条件下,分别使用键合金刚烷基的高极性色谱柱 CAPCELL PAK ADME S5; 4.6 mm i.d.×250 mm、在纯水条件下也能稳定使用的高极性色谱柱 CAPCELL PAK C18 AQ S3; 4.6 mm i.d.×250 mm,以及之前实验中使用的CAPCELL PAK C18 MGII S5; 4.6 mm i.d.×250 mm, 对L(+)-抗坏血酸、D(-)-异抗坏血酸混合溶液进行分析。结果如图5所示,三款色谱柱对 L(+)-抗坏血酸、D(-)-异抗坏血酸均可得到基线分离的良好结果,且峰形良好,分离度分别为1.89、2.05、2.10。 图5混合样品分析色谱图(三款色谱柱对比) HPLC Conditions : 色谱柱: CAPCELL PAK C18 MGII S5; 4.6 mmi.d.×250 mm CAPCELL PAK C18 AQ S3;4.6 mm i.d.×250 mm CAPCELL PAK ADME S5;4.6 mm i.d.×250mm 流动相: 20mM NH4H2PO4 (pH2.0)/CH3OH=98/2 流0.7 mL/min温 检样 30°C PPDA 245 nm L(+)-抗坏血酸 20 ng/mL、D(-)-异抗坏血酸20 ng/mL 进样量: 20uL 溶 剂: 流动相 接下来,在此条件下使用 ADME 色谱柱进行精密度及线性实验的考察。精密度实验结果如表1所示,连续进样六针, L(+)-抗坏血酸峰面积 RSD 为 0.32%、D(-)-异抗坏血酸峰面积 RSD 为 0.25%。线性实验结果如图6、7所示,在0~50 ng/mL 的浓度范围内, L(+)-抗坏血酸、D(-)-异抗坏血酸均呈现良好的线性关系。 表1抗坏血酸精密度实验 L(+)-抗坏血酸峰面积 D(-)-异抗坏血酸峰面积 1 1536314 1746615 2 1534751 1741066 3 1530350 1738548 4 1537950 1741798 5 1527078 1734253 6 1526370 1736629 平均峰面积 1532135.5 1739818.17 RSD% 0.32 0.25 图6抗坏血酸线性试验(L(+)-抗坏血酸) 图7抗坏血酸线性试验(D(-)-异抗坏血酸) 综上,在不添加离子对试剂的酸性条件下,使用键合金刚烷基的 ADME 色谱柱及 MGII、AQ S3 两款 C18色谱柱进行分析,均可对L(+)-抗坏血酸、D(-)-异抗坏血酸得到基线分离的良好结果,其中, CAPCELL PAK C18 MGII 色谱柱的分离效果最好,分离度为2.10。 此外,在实验中我们发现使用流动相(20mM NH4H2PO4(pH2.0)/CH3OH=98/2)作为样品溶剂时,随着分析时间的延长, L(+)-抗坏血酸、D(-)-异抗坏血酸的峰面积有逐渐减小趋势;而当样品溶剂为20 g/L 的偏磷酸时,L(+)-抗坏血酸、D(-)-异抗坏血酸峰面积基本保持稳定,但死时间处的溶剂峰较大。建议客户在进行长时间进样分析时,使用偏磷酸作为溶剂,避免样品氧化引起峰面积降低等现象,进而影响实验结果。 在《GB 5009.86-2016》方法基础上,将有机相调整为25%(2%),柱温调整为30°C(25°C),使用CAPCELL PAK C18 MGII色谱柱进行分析,L(+)-抗坏血酸、D(-)-异抗坏血酸之间的分离度为1.28,大于客户要求的0.90。上述实验中,我们在原条件基础上将流动相中有机相比例及柱温调整为25%CH3OH、30°C,使用MGII色谱柱进行分析,可得到L(+)-抗坏血酸、D(-)-异抗坏血酸分离度为1.28的最佳分离结果,但二者仍未达到基线分离。且使用添加离子对试剂的流动相进行分析时,色谱柱需要2天左右的平衡时间,因此,我们也开发了不含离子对试剂的分析条件。在流动相为20mM NH4H2PO4 (pH2.0) / CH3OH = 98 / 2的酸性条件下,分别使用键合金刚烷基的高极性色谱柱CAPCELL PAK ADME S5; 4.6 mm i.d. × 250 mm、在纯水条件下也能稳定使用的高极性色谱柱CAPCELL PAK C18 AQ S3; 4.6 mm i.d. × 250 mm,以及之前实验中使用的CAPCELL PAK C18 MGII S5; 4.6 mm i.d. × 250 mm,对L(+)-抗坏血酸、D(-)-异抗坏血酸混合溶液进行分析。结果如图5所示,三款色谱柱对L(+)-抗坏血酸、D(-)-异抗坏血酸均可得到基线分离的良好结果,且峰形良好,分离度分别为1.89、2.05、2.10。接下来,在此条件下使用ADME色谱柱进行精密度及线性实验的考察,在0~50 μg/mL的浓度范围内,L(+)-抗坏血酸、D(-)-异抗坏血酸均呈现良好的线性关系。
确定


还剩5页未读,是否继续阅读?
三耀精细化工品销售(北京)有限公司为您提供《异抗坏血酸,抗坏血酸中异抗坏血酸,抗坏血酸检测方案(液相色谱柱)》,该方案主要用于其他食品中营养成分检测,参考标准--,《异抗坏血酸,抗坏血酸中异抗坏血酸,抗坏血酸检测方案(液相色谱柱)》用到的仪器有
相关方案
更多
该厂商其他方案
更多









