方案详情
文
应用循环伏安和紫外光谱法研究杨梅酮氧化还原性质及其稳定性. 结果表明:在B2R缓冲溶液中玻碳电极上,杨梅酮的氧化还原表现为两步氧化反应和两步还原反应. 氧化反应对应于B环4′2 OH和C环32OH的氧化,还原反应对应于C环4位羰基还原为中间体自由基之后再进一步还原生成羟基. 以上各步反应均为
单电子单质子电极过程. 杨梅酮的氧化还原反应与溶液pH关系密切,但其原因来自于去质子化作用,并导致它的抗氧化能力增强,但其最终氧化产物没有电化学活性,并吸附在电极表面,阻碍了电极过程电子传递. 在pH 7. 45~12. 00范围内,杨梅酮也因去质子化作用导致紫外光谱Ⅰ带和Ⅱ带随pH增加,而发生红移,分解作用加剧. 同时分解作用还与放置时间有关.
方案详情

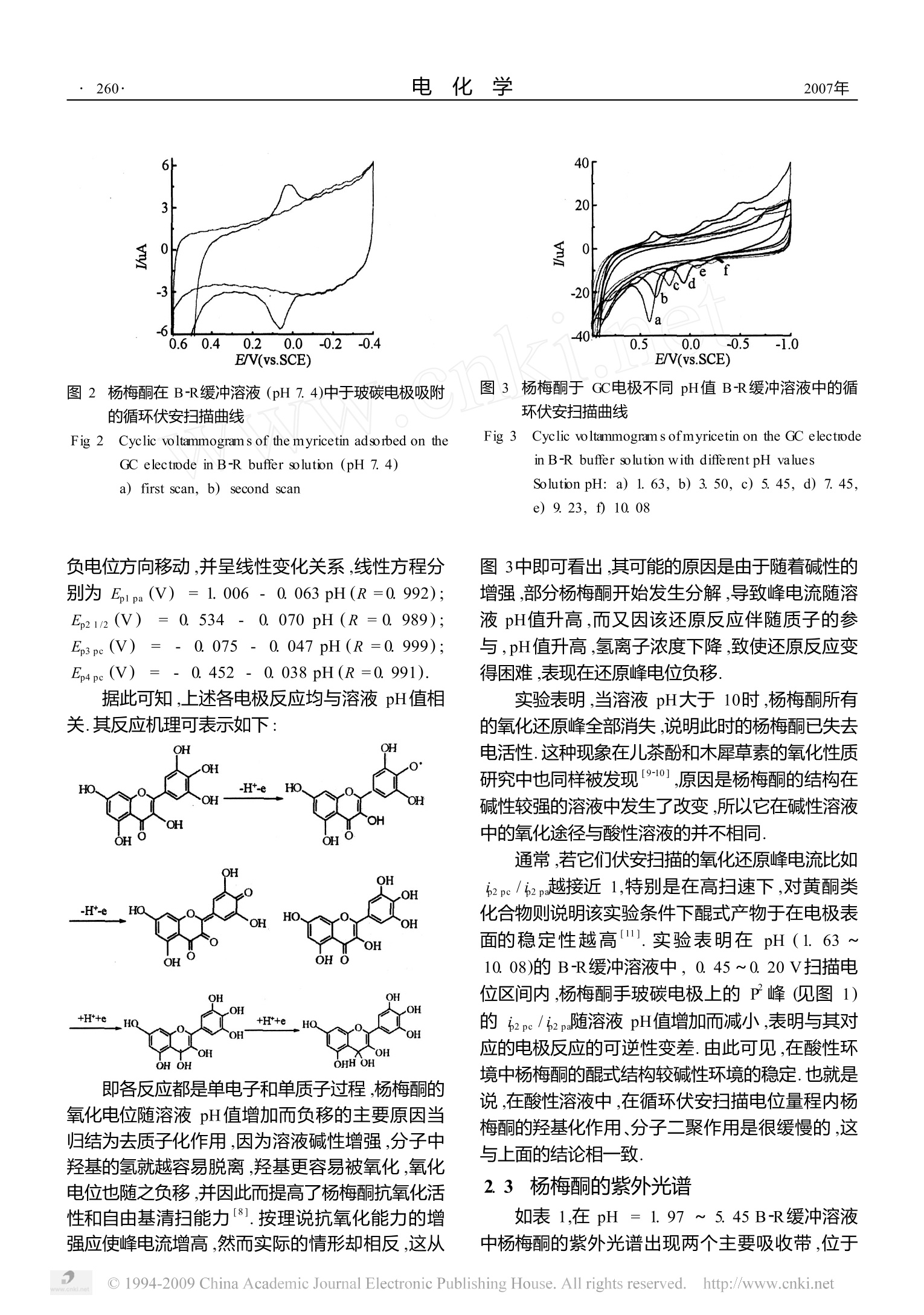
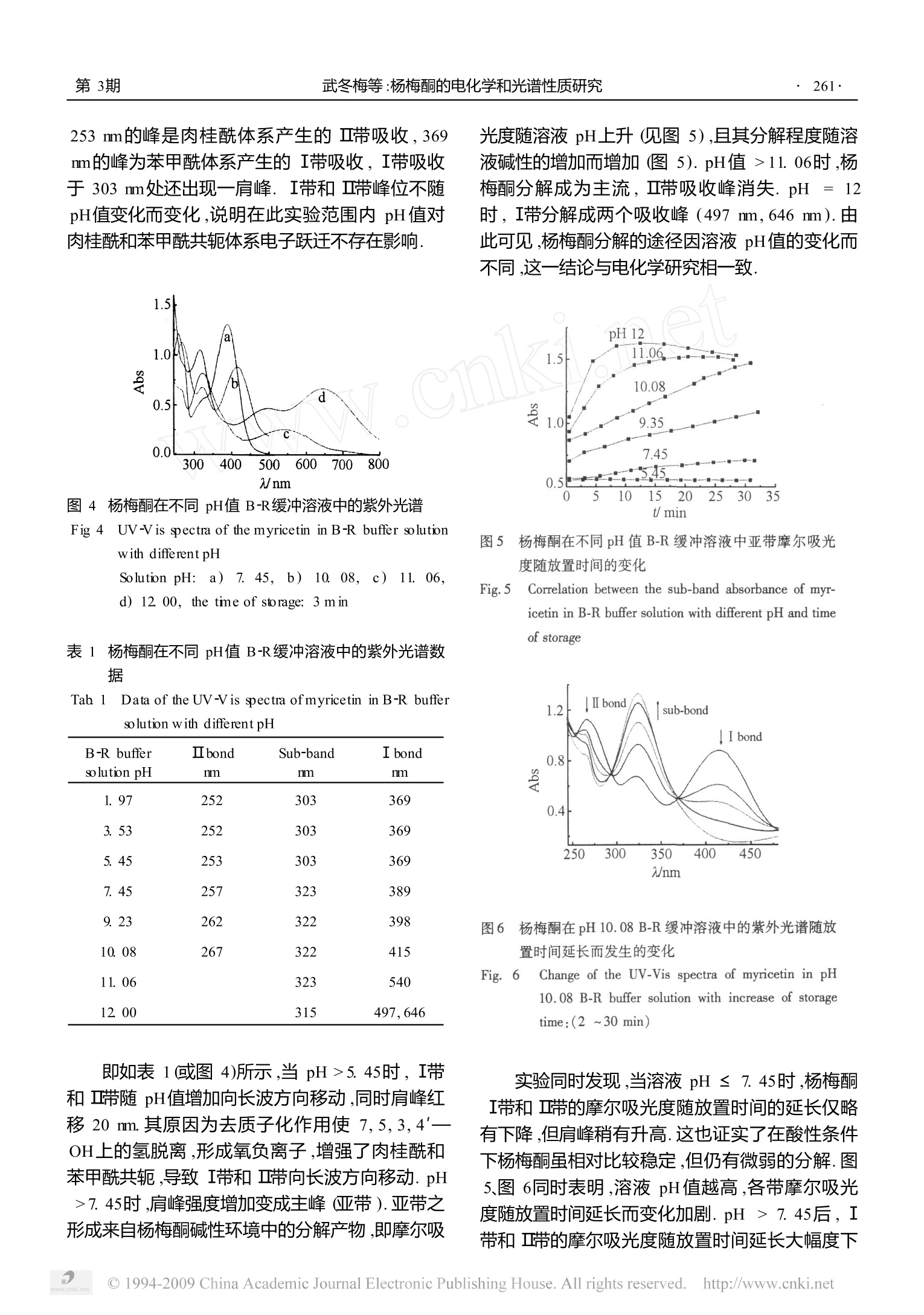
电化学ELECTROCHEM ISTRYVol 13 No 3Aug 2007第13卷 第3期2007年8月 第3期武冬梅等:杨梅酮的电化学和光谱性质研究·259 · 杨梅酮的电化学和光谱性质研究 武冬梅,刘 爽1.2..高洪福,李锦莲,刘海燕,梁启超1,2 (1.佳木斯大学化学与药学院,黑龙江佳木斯 154007: 2.黑龙江乌苏里江佳大制药有限公司,黑龙江佳木斯154005) 摘要: 应用循环伏安和紫外光谱法研究杨梅酮氧化还原性质及其稳定性.结果表明:在BR缓冲溶液中玻碳电极上,杨梅酮的氧化还原表现为两步氧化反应和两步还原反应.氧化反应对应于B环4'OH和C环30H的氧化,还原反应对应于C环4位羰基还原为中间体自由基之后再进一步还原生成羟基.以上各步反应均为单电子单质子电极过程.杨梅酮的氧化还原反应与溶液 pH关系密切,但其原因来自于去质子化作用,并导致它的抗氧化能力增强,但其最终氧化产物没有电化学活性,并吸附在电极表面,阻碍了电极过程电子传递.在pH 7.45~1200范围内,杨梅酮也因去质子化作用导致紫外光谱I带和Ⅱ带随pH增加,而发生红移,分解作用加剧.同时分解作用还与放置时间有关. 关键词: 杨梅酮;电化学;pH;紫外可见光谱 中图分类号:(0657.1 文献标识码: A 杨梅酮(3,5,7,3',4',5'六羟基洞酮)又名杨梅素,属六羟基黄酮类化合物,其结构如下所示. 杨梅酮主要来自于杨梅树的皮和叶中,具有极高的抗氧化和清除自由基的活性.此外,还有抗炎、抗血栓、抗肿瘤、改善微循环、降血糖、肝保护、解轻乙醇中毒等药理作用,广泛应用于医药、食品、保健品和化妆品等领域,美国保健品药 FYI杨梅酮作为添加剂用于预防关节炎和治疗各种炎症,更加适合于妊娠及哺乳期妇女和婴儿.虽然,有关杨梅酮的生物活性及其提取方法等已有许多研究,但涉及它的的电化学/光谱性质还未见报道.本文应用循环伏安法和紫外光谱研究了杨梅酮的电 化学性能,以及溶液 pH值对杨梅酮的稳定性和氧化还原反应的影响,揭示杨梅酮的抗氧化活性与其结构的内在关系. 1 实验部分 1. 1 仪器与试剂 LK2005电化学分析仪(天津兰力科),三电极体系:工作电极为玻碳电极,饱和和汞电极(SCE)为参比电极,铂丝为对电极.UV757CRT型紫外可见分光光度计(上海精密科学仪器公司).PB-20标准型 pH计(德国塞多利斯).室温下实验,高纯氮气除氧. 杨梅酮(sigma公司)用无水乙醇配成1×10mol/L储备液.B-R缓冲溶液(0.04 mol/L磷酸、0.04mol/L醋酸、0.04mol/L硼酸)用0.1mol/L氢氧化钠调节所需 pH值.所用试剂均为分析纯,溶液用三次蒸馏水配置. 1.2 实验方法 用微量移液器移取3mLB-R缓冲溶液注入电 ( 收稿日期:2007-03-06,修订日期:2007-04-18 *通讯作者,Tel: 1 (86-454) 8 610818,Email: w udmei@yahoo com. cn ) ( 黑龙江省教育厅科技项目(No 10541221)、浙江省自然科学基金(No Y205706)、黑龙江省自然科学基金项目(No B200609)、佳木斯大学科研项目 (No L2007-90)资助 ) 解池或标准比色杯中,再加入适量杨梅酮储备液使其浓度为5X10mol/L,分别测定该体系循环伏安曲线和紫外可见光谱. 2 结果与讨论 2.1 杨梅酮的循环伏安行为 图1示出杨梅酮在 pH3.5的B-R缓冲溶液中的循环伏安曲线.如图可见,在正电位区,杨梅酮显示两个氧化峰(P和P),负电位区出现两个还原峰(P和P). 图1 杨梅酮在 pH 3.5B-R缓冲溶液中的循环伏安曲线 Fig 1 Cyclic voltammograms of myricetin in pH 3. 5 B-Rbuffer so lutionscan rate: 100 mV/s, potential rangea)1.0~-1.0V,b)0.45~-0.20V 文献「3]提出,黄酮B环上的羟基比A环和 C环羟基更容易被氧化,其中4'—OH最容易被氧化形成半醌式自由基.据此可将图1中在正电位区出现的第1氧化峰 P(E,1/2=0.300V)指认为杨梅酮B环4'一OH被氧化成半醌式自由基的反应,该峰与其还原峰峰电位差▲E,2=65mV,而p2pc /52pa=0.20,可见该过程当为不可逆的单电子反应.P的氧化峰电位相当低,峰电流明显地高于其它峰,表明杨梅酮的连苯三酚结构更容易发生氧化反应,从而具有很高的抗氧化和清扫自由基的能力. 黄酮类化合物存在两种不同的药效基团,一个是 B环上的羟基.另一个是A环和C环上的羟基.A环上的5—OH和7—OH的推电子作用增强了C环上3—OH的电化学活性,5—OH和7—OH的氧化电位高于3—OH的氧化电位.图1中第2个氧化峰P(Ep:=0.824V)被认为对应于杨梅酮C 环上3—OH的氧化反应.但与5—OH和7—OH相对应的氧化峰却未在电位扫描区间内出现.3—OH的氧化反应也是不可逆的,并且峰电流很小. 黄酮类化合物C环上4位羰基C=0具有电化学活性,能够经过还原生成中间体自由基,中间体自由基再进一步还原生成羟基4-51.所以,图1P峰 (E3p=-0.248Ⅴ)可归因为杨梅酮C环4位羰基被还原成中间体自由基的不可逆反应,而P峰(E4pc。=-0.609V)则对应于间体自由基还原生成羟基的不可逆反应. 实验表明,P、P和P的峰电位与扫速对数lgv存在线性关系,线线方程分别为:Elna(V)=0913+0.0801logv(V/s)(R=0.981), E,3pa(V)=-0209-00718 lgv(V/s)(R=0.992), Ep4pa(V)=-0.599-0.0692 logv(V/s) (R =0. 992).由方程直线斜率161可算出 P、P和P的反应电子转移数都为1.P和P的峰电流对数也与扫速v对数呈线性关系: logp2pa(哈A)=--0. 0685 +0.776 lg v(V/s) (R =0. 996),logp2pe(uA)=-1.136+0.962 logv(V/s)(R=0. 996).可见,二者直线斜率都小于1,表明该氧化还原的电极过程既受扩散控制又受吸附控制. 从图1b可见,如将伏安扫描电位区间缩小,以便把P、P和P峰的出现都排除在外,则P的阴极峰电流相应增高,阳极峰电流下降,降2c2m由0.2增加到0.8,显示该过程由不可逆反应转变为可逆反应.这一现象在槲皮素的电化学研究中也被发现. 实验表明,在B-R缓冲溶液中杨梅酮于玻碳电极上经多圈循环伏安扫描后,其第2圈及其后的峰电流与第1圈相比强度均大幅度下降,这说明杨梅酮在玻碳电极表面发生吸附作用,并且吸附产物阻碍了电极表面的电子传递.将多圈扫描后的玻碳电极用三次蒸馏水洗净,放在 pH7.4的B-R缓冲溶液再进行循环伏安扫描,发现在0.040V处出现一对可逆的氧化还原峰(见图2),该峰为杨梅酮B环4—OH的氧化反应,但在第2圈扫描时氧化还原峰消失,说明在玻碳电极表面杨梅酮的吸附作用是很弱的. 2.2 溶液 pH对伏安扫描的影响 图3表明,在玻碳电极上,杨梅酮所有的氧化还原峰电位都随B-R缓冲溶液pH值的增加而向 图 2 杨梅酮在B-R缓冲溶液(pH7.4)中于玻碳电极吸附的循环伏安扫描曲线 Fig 2Cyclic voltammogram s of the myricetin adsorbed on theGC electrode in B-R buffer solution (pH 7.4)a) first scan, b) second scan 据此可知,上述各电极反应均与溶液 pH值相关.其反应机理可表示如下: 即各反应都是单电子和单质子过程,杨梅酮的氧化电位随溶液pH值增加而负移的主要原因当归结为去质子化作用,因为溶液碱性增强,分子中羟基的氢就越容易脱离,羟基更容易被氧化,氧化电位也随之负移,并因此而提高了杨梅酮抗氧化活性和自由基清扫能力.按理说抗氧化能力的增强应使峰电流增高,然而实际的情形却相反,这从 图3 杨梅酮于 GC电极不同pH值B-R缓冲溶液中的循环伏安扫描曲线 Fig 3 Cyclic voltammogram s ofmyricetin on the GC electrodeinB-R buffer solution with different pH valuesSolution pH: a) 1. 63, b) 3. 50, c) 5. 45, d) 7.45,e) 9. 23, f) 10.08 图3中即可看出,其可能的原因是由于随着碱性的增强,部分杨梅酮开始发生分解,导致峰电流随溶液 pH值升高,而又因该还原反应伴随质子的参与,pH值升高,氢离子浓度下降,致使还原反应变得困难,表现在还原峰电位负移. 实验表明,当溶液 pH大于10时,杨梅酮所有的氧化还原峰全部消失,说明此时的杨梅酮已失去电活性.这种现象在儿茶酚和木犀草素的氧化性质研究中也同样被发现19-10],原因是杨梅酮的结构在碱性较强的溶液中发生了改变,所以它在碱性溶液中的氧化途径与酸性溶液的并不相同. 通常,若它们伏安扫描的氧化还原峰电流比如p2pc/2pa越接近1,特别是在高扫速下,对黄酮类化合物则说明该实验条件下醌式产物于在电极表面的稳定性越高.实验表明在 pH(1.63~10.08)的B-R缓冲溶液中,0.45~0.20V扫描电位区间内,杨梅酮手玻碳电极上的P峰(见图1)的i21i随溶液pH值增加而减小,表明与其对应的电极反应的可逆性变差.由此可见,在酸性环境中杨梅酮的醌式结构较碱性环境的稳定.也就是说,在酸性溶液中,在循环伏安扫描电位量程内杨梅酮的羟基化作用、分子二聚作用是很缓慢的,这与上面的结论相一致. 2.3 杨梅酮的紫外光谱 如表1,在 pH =1.97~5. 45 B-R缓冲溶液中杨梅酮的紫外光谱出现两个主要吸收带,位于 253 nm的峰是肉桂酰体系产生的Ⅱ带吸收,369mm的峰为苯甲酰体系产生的Ⅰ带吸收,I带吸收于 303mm处还出现一肩峰. I带和Ⅱ带峰位不随pH值变化而变化,说明在此实验范围内pH值对肉桂酰和苯甲酰共轭体系电子跃迁不存在影响. 图4 杨梅酮在不同pH值B-R缓冲溶液中的紫外光谱 Fig 4 UV-V is spectra of the myricetin in B-R buffer solutionwith different pHSolution pH:a)77. 45,b)110.08,c) 11.06.d) 12.00, the tie of storage: 3 min 表1 杨梅酮在不同pH值BR缓冲溶液中的紫外光谱数据 Tab 1 Data of the UV-V is spectra of myricetin in B-R buffersolution with different pH B-R buffer Ⅱ bond Sub-band I bond solution pH mm nm nm 1.97 252 303 369 3.53 252 303 369 5.45 253 303 369 7.45 257 323 389 9.23 262 322 398 10.08 267 322 415 11.06 323 540 12.00 315 497,646 即如表1(或图4)所示,当 pH>5.45时,I带和Ⅱ带随 pH值增加向长波方向移动,同时肩峰红移20mm.其原因为去质子化作用使7.5,3.4一OH上的氢脱离,形成氧负离子,增强了肉桂酰和苯甲酰共轭,导致I带和Ⅱ带向长波方向移动.pH>7.45时,肩峰强度增加变成主峰(亚带).亚带之形成来自杨梅酮碱性环境中的分解产物,即摩尔吸 光度随溶液 pH上升(见图5),且其分解程度随溶液碱性的增加而增加(图5).pH值>11.06时,杨梅酮分解成为主流,Ⅱ带吸收峰消失.pH=12时,I带分解成两个吸收峰(497 nm,646 nm).由此可见,杨梅酮分解的途径因溶液 pH值的变化而不同,这一结论与电化学研究相一致. 图5 杨梅酮在不同 pH 值B-R缓冲溶液中亚带摩尔吸光度随放置时间的变化 Fig.5 Correlation between the sub-band absorbance of myr-icetin in B-R buffer solution with different pH and timeof storage 图6 杨梅酮在 pH 10.08 B-R 缓冲溶液中的紫外光谱随放置时间延长而发生的变化 Fig..6 Change of the UV-Vis spectra of myricetin in pH10.08 B-R buffer solution with increase of storagetime:(2~30 min) 实验同时发现,当溶液 pH ≤7.45时,杨梅酮I带和Ⅱ带的摩尔吸光度随放置时间的延长仅略有下降,但肩峰稍有升高.这也证实了在酸性条件下杨梅酮虽相对比较稳定,但仍有微弱的分解.图5、图6同时表明,溶液pH值越高,各带摩尔吸光度随放置时间延长而变化加剧.pH>7.45后,I带和Ⅱ带的摩尔吸光度随放置时间延长大幅度下 降,亚带快速升高.当 pH=12.00时,亚带摩尔吸光度于放置10min后,停止上升而后略有下降.以上的现象说明杨梅酮分解主要由 pH决定,同时还受到放置时间的影响. 3 结 论 在玻碳电极上杨梅酮于B-R缓冲溶液中出现4个氧化还原峰,分别对应于B环4—OH和 C环3—OH的氧化反应,及C环4位羰基生成中间体自由基和中间体自由基生成羟基的还原反应,以上反应均为单电子单质子过程.由于去质子化作用导致杨梅酮的氧化还原电位与溶液 pH值密切相关,随着 pH值增增加杨梅酮抗氧化和清扫自由基能力增强.杨梅酮在玻碳电极上有吸附作用.杨梅酮的紫外光谱受 pH值影响,随溶液碱性的增加杨梅酮发生部分分解. ( 参考文献(References): ) ( [ 1 ] Lin CM, C h en C S, Chen C T, et al M o lecular mod- eling of flavonoids t hat i nhibits xanthine oxidase [J ] . B iochem ical and B iophysical Researc h Communications,2002, 2 94(1):1 6 7-172. ) ( [21 Zhang Yousheng (张友胜), Ning Zhengxiang (宁正),Hu Yanyong(胡勇). Research on flavonol ofdihydrom yricetin [J ] . Chinese TranditionalPatentMedi- cine(in Chinese),2002 , 24 ( 12): 9 70 -971. ) ( [3] Jovanovic SV, S teenken S, T o sicM, et al a l F lavonoids as antioxidants[J ] . J Am Chem Soc, 1994, 1 16(1 1 ): 4846-4851. ) ( [4] Zheng Jianbin (郑建斌),Dong Sheying(董社英) Y arSuihong(延绥宏), et al I nvestigation on t he electro- chem ical behavior of sodium 4 ' ,7-Dimethoxy-3'-isofla-vone s ulfonate[J]. Acta Chim Sinica, 2 004, 6 2 ( 1 1): 1071-1075. ) ( 151 Dong Sheying(董社英),Zheng Jianbin (郑建斌), Gao Hong(高鸿). I nvestigation o n the e l ectrochem ical b e -havior of sodium 4',7-dimethoxy-3-isoflavone sul f onate [J]. Acta Chim Sinica, 2003, 61 ( 4):487-491. ) ( [6] Anson F Ele c trochem istry and electroanalytical chem is- try [M ] . E d : H uang W Z, Be i jing: Beijing University Press, 1 981. 1 35. ) ( [71 B rett Oliveia A M, Ghica M E E l ectrochemical oxida-tion of quercetin [J]. ]Electroanalysis , 2003, 22(15):1745-1750. ) ( [8] OliveC C, Hapiot P, Pi n son J, et al Fr e e rad i cal chemistry of f l avan-3-ols: S: detemm ination of themmody- nami c p arameters a n d of ki n etic re a ctivity f i om sh o rt(ns) t to long (ms) tme s c ale [J] . J Am Chem Soc. 2002, 1 24(47):14027-14038. ) ( [9] Filip iak M. Electrochem ical o xidation of luteolin [J ].Anal Sci , 2001, 1 7(Suppl i ): 16 67. ) ( [10] Patricia P, B rett O liveia A M. Catechin electrochemi- cal oxidation mechanisms [ J ]. Anal C h imica Acta, 2004,518(1):109-115. ) ( [11] NematollahiD, Malakzadeh M. Electrochem ical oxida- tion of quercetin in the presence o f benzenesulfinic acids[J]. J Electroanal Chem, 2003, 547(2): 191- 195. ) Investigation on the Electrochem ical and Spectra PropertiesofM yricetin WU Dongmei,LU Shuang, GAO Hong-fu',LIJ in-lian7.LJ Hai-yan,L ANG Qi-chao (1. College of Chen istry and Phamn acy,Jiam usi University, Jiam usii 154007, Heilongjiang, China,(2 Heilengjiang wusulijiang and jiam usi University Pham aleutical Ca , L td ,Jiam usi 154005, Heilongjiang, China) Abstract: The electrochem ical mechanism of redox and stability ofmyricetin were investigated using cyclic vol-tammetry and electronic absoip tion spectraTwo oxidation reactions and wo reduction reactions were achieved inB-R buffer solutionThe oxidation reactionswere both due to oxidation of 4'OH on ring B and 3-OH on ring Cwithin a one electron one pro tonpiocessThe reduction reactions both correspond to the transfomation of 4-carbonyl group on ring C to intemmediate radical, and inteimediate radical to hydroxyl group within a one electronone proton piocess, respectively The redox ofmyricetin is pH dependent because ofdep rotonation, resulting inan increase of the antioxidant ability upon fomation of the dep rotonated fommsi The final oxidation product ofmyricetin without electroactivity adsorbs on the electrode surface, and blocks transfers ofelectron W ith increa seof pH (7. 45~12.00), I and Ⅱ bonds of electronic absoip tion spectra of myricetin are red-shifted due to thedep rotonation and the degradation of myricetin increases The tie of storage affects intensity of degradation ofmyricetin Key words:myricetin; electrochemistry; pH; electronic absorp tion spectra ◎China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net
确定




还剩4页未读,是否继续阅读?
天津市兰力科化学电子高技术有限公司为您提供《杨梅酮中电化学和光谱性质研究检测方案(电化学工作站)》,该方案主要用于其他中电化学和光谱性质研究检测,参考标准--,《杨梅酮中电化学和光谱性质研究检测方案(电化学工作站)》用到的仪器有LK2005A电化学工作站
推荐专场
相关方案
更多
该厂商其他方案
更多
















