
由于使用仪器的灵敏性不断提高,目前,分析检出 限在常规情况下可以达到ng/l(ppt)级,而在一定 条件下甚至能达到pg/l (ppq) 级。进行这些痕量分 析所获得的数据的可信度,主要依赖于对几个条件 和参数的控制情况。除了对仪器进行技术性操作 外,小心进行样品处理及试剂的纯度是能控制的主 要参数1。水是最重要的试剂之一,因为它在很多应 用情况下都被使用。液相色谱柱的清洗、空白对照 的准备、样品的稀释和准备,以及最后的洗脱都只 是水被使用的一些例子。因为水的大范围使用,而 且其使用的体积非常大,因此必须异常谨慎,确保 水的质量符合实验要求。尤其是在进行痕量离子分 析时,需要稳定的、可再生的高纯度水。
方案详情

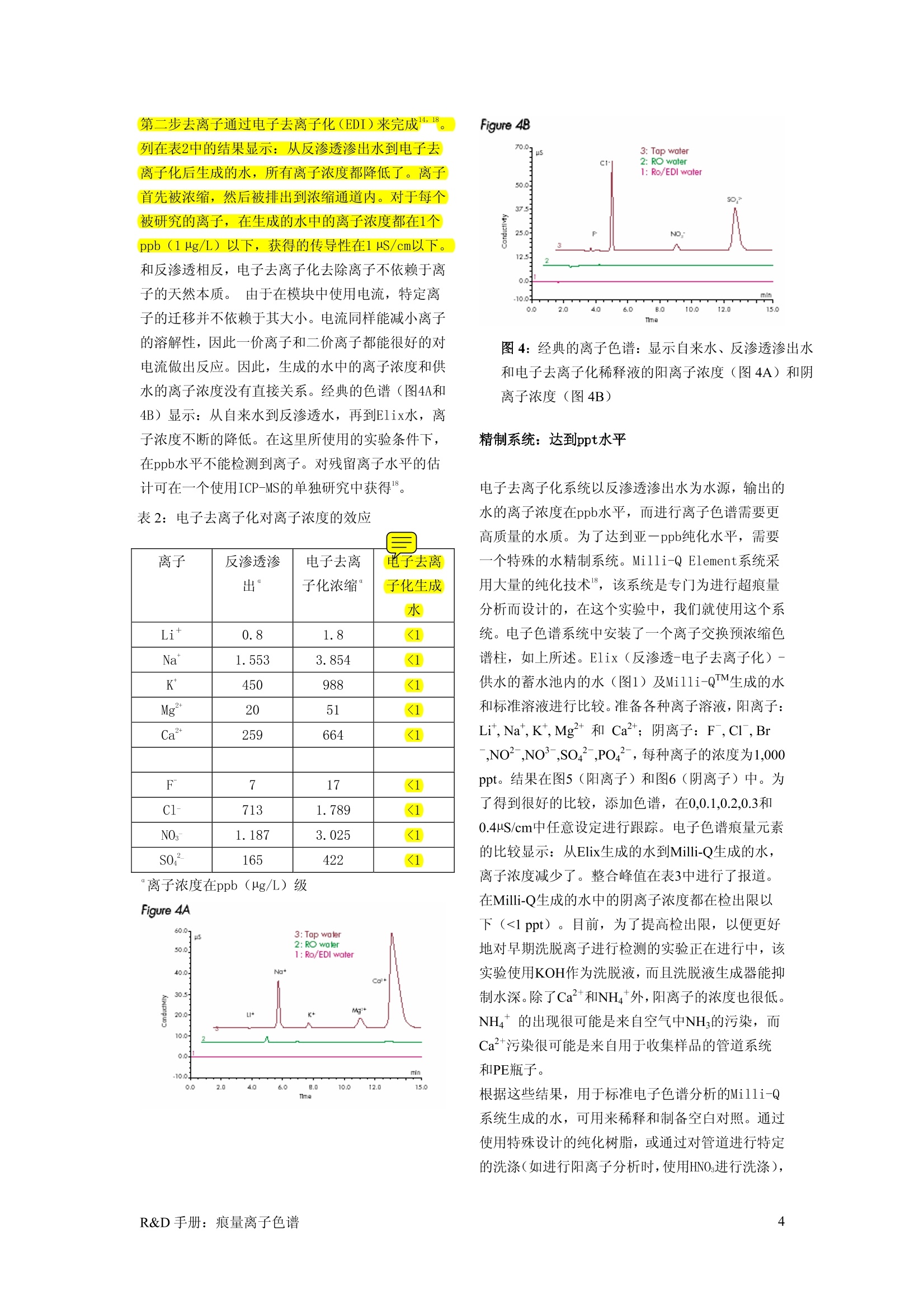
材料和方法 The R&D NotebookA publication of the Laboratory Water Division of Milliporelldi 痕量离子色谱 Stephane Mabic, Ichiro Kano, and Daniel Darbouret Research & Development, Laboratory Water Division, Millipore S.A., Saint-Ouentin-en-Yvelines, France This article is based on a paper presented at the International Ion Chromatography Symposium, September 11-14,2000,Nice, France. 摘要:根据从持续性研究和对不同类型使用仪器的开发工作获得的结果,离子色谱(IC)已经被认为是进行痕量分析最有竞争力的技术之一。进行超痕量分析需要使用异常清洁的试剂,包括水。在从自来水到超纯水的整个水纯化链过程中,通过离子色谱监控水中的离子浓度。阴离子和阳离子的浓度从自来水的ppm级降低到超纯水的ppt级。这个研究显示:从Milli-Q@系统获得的超纯水可用于离子色谱的痕量分析。 由于使用仪器的灵敏性不断提高,目前,分析检出限在常规情况下可以达到ng/l (ppt)级,而在一定条件下甚至能达到pg/l (ppq)级。进行这些痕量分析所获得的数据的可信度,主要依赖于对几个条件和参数的控制情况。除了对仪器进行技术性操作外,小心进行样品处理及试剂的纯度是能控制的主要参数。水是最重要的试剂之-—,因为它在很多应用情况下都被使用。液相色谱柱的清洗、空白对照的准备、样品的稀释和准备,以及最后的洗脱都只是水被使用的一些例子。因为水的大范围使用,而且其使用的体积非常大,因此必须异常谨慎,确保水的质量符合实验要求。尤其是在进行痕量离子分析时,需要稳定的、可再生的高纯度水。 有几种方法可用于进行离子分析,这些方法的灵敏 性各不相同:诱导偶联等离子体-光学发射光谱 (ICP-OES),诱导偶联等离子体-质谱 (ICP-MS) 23,火焰原子吸收光谱 (FAAS),带电原子吸收 光谱 (GFAAS)“和整合了UV-Vis光谱或电子导电计的离子色谱(IC)。离子色谱,和传导性测量结合使用,已经成为一个分析稀释样品中各种阴离子和阳离子的可靠的流行方法6.7。这种方法已经在几种研究领域中得以开发和使用,如在南极冰的研究中8、在半导体工厂中,在分析研究领域中也对这种方法进行了开发使用,如在空气10、土壤''和水12的环境分析中。为了符合新的标准和规定,饮用水也需要进行水质的分析和确证,这些要求使得离子色谱的使用更加广泛,并且鼓励开发新的分析技术。水纯化系统需要达到以下要求:能产生可进行痕量分析的水;在需要的情况下,可对水的质量进行监控;并且符合良好实验室操室规定 (GoodLaboratory Practices)。开发这样的一个水纯化系统确实是一个极大的挑战。在这个研究中,在自来水中检测出的主要离子,在水纯化链的各种阶段,通过离子色谱对这些离子浓度进行研究。 水纯化链 用来产生分析用水的水纯化链使用了几种技术的组合。这个水纯化链可以分成两个主要部分:预处理,包括一个起起的纯化系统,如Elix@系统,该系统产生的纯净水流到一个蓄水池中;最后的精制单元,如Milli-Q系统,该系统以蓄水池的水生产超纯水4(图1)。这里所使用的预处理系统为Elix 10 系统,结合使用了通过过滤/吸收的序列水纯化、反渗透(RO)和电子去离子化(EDI)。在Elix系统的起始纯化步骤中使用了ProgardM预处理包,由于几种重要的原因,这个预处理包应该放置在反渗透膜前。在Progard柱中的活性炭球珠能有效的防止自来水中的氯气对反渗透膜的损坏作用,并通过吸附作用去除一些溶在水中的有机物。多磷酸盐是一种聚合沉淀作用的抗缩放比例试剂,可作为一种Ca和Mg离子的有效螯合剂,从而保护缩放比例过程中的反渗透膜和电子去离子化模块。最后,一个孔大小为 0.5um的聚丙烯深度过滤器能有效的去除大的胶体物质、残渣和颗粒性物质。然后,这种预处理后的水通过一个螺旋形薄膜、复合反渗透膜处理,这样能显著减少离子浓度。将反渗透预处理的水引向一个电子去离子化模块,这个模块由离子交换膜、离子交换树脂和--个直流电组成,有效的去除水中的离子"。电流使系统中的离子交换数值不断的再生,避免更换数值的需要。这些实验中使用的Elix单元,每小时能向蓄水池中输入10升由自来水生成的纯化水。这个蓄水池,用专门挑选的聚乙烯材料制成,可以向最后的精制单元供水,在最后的精制单元中,残留的痕量离子将被除去。在这里,我们使用Milli-QElement 系统作为最后的精制系统,并通过顺序的光致氧化、离子交换,和过滤后,输出超纯水(参见图2)17,18。在光致氧化过程中使用一个紫外灯(入=185 nm和254 nm),该波长能引起有机物螯合分子断裂,并诱导螯合离子释放。有机物断裂同样有助于避免有机物在树脂球珠表面形成污垢。然后用由低渗漏物质制成的混床树脂将离子顺序去除。在使用精制系统时,放置一个微孔滤膜,进行微粒的去除和防止外部环境带来的反相污染。图1描述的流程图显示纯化链和各种取样口。在每个纯化步骤,将样品收集到聚乙烯(PE) 瓶子°中,这种瓶子在使用前要用超纯水进 行彻底的清洗。在下面几个位置中选择取样口,以监控每个纯化步骤的有效性:自来水、反渗透排斥和预处理的水、电子去离子化浓缩和生成的水、蓄水池的水,和最后的超纯水。 图1:水纯化链和取样口 图2: Milli-Q Element 超纯水系统 (UHMWPE 过滤器-超高分子量聚乙烯, PVDF 最后过滤器- 聚乙二烯氟化物) 离子色谱 使用Dionex@ DX 500仪器进行离子分析,该仪器有一个GP50泵和一个AS40自动取样器,和一个有peaknet 软件的CD20传导计相连。对于50到5,000ppb范围,使用25m1样品,对于5到1,000 ppb范围,使用200u1样品。对于阴离子色谱,使用AS12A/AG12A层析斤、2.7mM Na2C03 / 0.3 mMNaHC03的洗脱液,流速为1.5 mL/min。选择一个ASRS 超级抑制物,采用100 mA循环模式,外部水供应。对于阳离子分析,使用CS12A/CG12A色谱柱,20 mM 甲基磺酸洗脱液,流速为1.0 ml/min。在这种情况下,使用一个CSRS超级抑制剂,采用50 mA循环模式。对于痕量分析,使用相同的色谱柱和抑制剂,但是预先要安装一个预浓缩柱子。进行阴离子痕量分析时,使用一个Dionex@ TAC-2预浓缩柱子,进行阳离子痕量分析时,使用Dionex TCC-2预 浓缩柱子。为了避免由空气带来的污染,将样品保留在PE瓶子中,并放置在一个充满2-bar N压力的房间内。在一定的压力条件下,向预浓缩柱子中压入7ml样品,流速为1ml/min。在开始收集样品前,将PE瓶子清洗3次,并且在收集样品前用1升水冲洗系统。通过混合及稀释标准溶液(从SpexCertiprep公司购买, c.a.1,000 ppm)来制备为进行每种离子的痕量分析所用的标准溶液。使用Milli-QElement系统纯化的水进行稀释。 结果 预处理纯化单元:达到ppb水平如上所述,使用活性炭球珠和抗缩放比例试剂对自来水进行的起始处理步骤,不能有效的减少自来水中总的离子的数量,但是能有效的保护水纯化链,使其免受氯气和缩放比例的损坏。反渗透是用于消除离子的第一个处理过程(图1)。自来水中主要离子的浓度((Li+, Na+, K+, Mg2+, Ca2+,F,C1-,NO, and SO),以及这些离子在反渗透预处理中的各自浓度列在标1中。每种离子的排出百分比也一起被报道,如通过反渗透清除的离子百分比。显然,反渗透系统在去除自来水中的大部分离子上非常有效(87%到99%,依各种离子而定)。选择性渗透能力是特定离子所带电荷、离子大小,以及离子的溶解性的一个功能。因此,二价离子的清除(对于Mg2+,Ca2+和SO,清除率>99%)比一价离子的清除(87%到93%)更加有效。和离子浓度平行,传导性也下降,从自来水的 569 pS/cm降到反渗透后的12.3 IS/cm,相对应于97.8%的排出率。因为离子的排出是起始时总的离子浓度的百分比,因此,在反渗透后水中的离子浓度和供水相关。在第二个实验中,在20分钟过程中监控离子的浓度(ca.3.3L)显示:系统在5分钟内,或在0.8L后,达到最后的浓度(图3A和3B)。更重要的是:对于所有被研究的离子,只要供水质量维持稳定,那么这个离子浓度就维持稳定。可以预期的是,传导性读数也和这些结果平行,并在5分钟内达到一个稳定的值。因此,可以从这些结果得出如下的结论:反渗透是持续清除所有类型离子的一个非常有效的方法。在一个完整的水纯化链的起始纯化处理中,这样的系统尤其适用。 表1:反渗透对离子浓度的效应 离子 自来水° 反渗透渗出 %排出 Li+ 2. 9 0.19 93.4 Na 14599 1868 87.2 K* 3138 371 88.2 Mg" 6438 20 99.7 Ca 106502 584 99.5 F 578 6 99.0 Cl- 45477 831 98.2 NOs- 13843 1756 87.3 SO 117546 232 99.8 “离子浓度在ppb (Hg/L)级 图 3A 图3B 图3:阳离子(图3A)和阴离子(图3B)排出的反渗透操作 第二步去离子通过电子去离子化(EDI)来完成:14,18列在表2中的结果显示:)从反渗透渗出水到电子去离子化后生成的水,所有离子浓度都降低了。离子首先被浓缩,然后被排出到浓缩通道内。对于每个被研究的离子,在生成的水中的离子浓度都在1个ppb (1Hg/L) 以下,获得的传导性在1 rs/cm以下。和反渗透相反,电子去离子化去除离子不依赖于离子的天然本质。 由于在模块中使用电流,特定离子的迁移并不依赖于其大小。电流同样能减小离子的溶解性,因此一价离子和二价离子都能很好的对电流做出反应。因此,生成的水中的离子浓度和供水的离子浓度没有直接关系。经典的色谱(图4A和4B)显示:从自来水到反渗透水,再到Elix水,离子浓度不断的降低。在这里所使用的实验条件下,在ppb水平不能检测到离子。对残留离子水平的估计可在一个使用ICP-MS的单独研究中获得。 表2:电子去离子化对离子浓度的效应 离子 反渗透渗出" 电子去离子化浓缩 电子去离 子化生成 水 Li* 0.8 1.8 <1 Na 1.553 3.854 <1 K 450 988 <1 Mg 20 51 <1 Ca 259 664 <1 F 7 17 <1 Cl- 713 1.789 <1 NOs 1.187 3.025 <1 SO- 165 422 <1 "离子浓度在ppb (Hg/L) 级 Figure 4A 图4:经典的离子色谱:显示自来水、反渗透渗出水和电子去离子化稀释液的阳离子浓度(图4A)和阴离子浓度(图4B) 精制系统:达到ppt水平 电子去离子化系统以反渗透渗出水为水源,输出的水的离子浓度在ppb水平,而进行离子色谱需要更高质量的水质。为了达到到亚ppb纯化水平,需要一个特殊的水精制系统。Milli-Q Element系统采用大量的纯化技术8,该系统是专门为进行超痕量分析而设计的,在这个实验中,我们就使用这个系统。电子色谱系统中安装了一个离子交换预浓缩色谱柱,如上所述。Elix(反渗透-电子去离子化)-供水的蓄水池内的水(图1)及Mil1i-QM生成的水和标准溶液进行比较。准备各种离子溶液,阳离子:Li,Na,K,Mg和 Ca ;阴离子: F,Cl,Br,NO,NO,SO4,PO,每种离子的浓度为1,000ppt。结果在图5(阳离子)和图6(阴离子)中。为了得到很好的比较,添加色谱,在0,0.1,0.2,0.3和0.4uS/cm中任意设定进行跟踪。电子色谱痕量元素的比较显示:从Elix生成的水到Milli-Q生成的水,离子浓度减少了。整合峰值在表3中进行了报道。在Milli-Q生成的水中的阴离子浓度都在检出限以下(<1ppt)。目前,为了提高检出限,以便更好地对早期洗脱离子进行检测的实验正在进行中,该实验使用KOH作为洗脱液,而且洗脱液生成器能抑制水深。除了Ca²+和NH*外,阳离子的浓度也很低。NH4*的出现很可能是来自空气中NH;的污染,而Ca²+污染很可能是来自用于收集样品的管道系统和PE瓶子。 根据这些结果,用于标准电子色谱分析的Milli-Q系统生成的水,可用来稀释和制备空白对照。通过使用特殊设计的纯化树脂,或通过对管道进行特定的洗涤(如进行阳离子分析时,使用HNOs进行洗涤), 或通过专门的色谱结构和色谱柱,将特定的离子浓度进行改进。 图5: Elix(反渗透-电子去离子化)供水的蓄水池内的水、Milli-Q系统生成的水和标准阳离子溶液(1,000)的电子色谱 . 1000 ppt 图6: Elix(反渗透-电子去离子化)供水的蓄水池内的水、Milli-Q系统生成的水和标准阴离子溶液(1,000)的电子色谱 表3: Elix 供水的蓄水池内的水、Milli-Q Element系统生成的水的离子浓度 (ppt) 离子 蓄水池的水 Milli-Q生成的水 Li <1 <1 Na 286 5 K 50 <2 Mg 6 2 Ca 64 35 F <1 <1 C1 254 <1 NO 369 <1 SO 238 <1 ( 参考文献 ) Kocherlakota, N.; Lamothe,D. ; Obenauf, R.; Noonan, J. “Standard requirements for pptanalysis of trace metals”Amer. Environ. Lab.,(11),26-27,(1995). 2 “Analysis of major, minor and trace elements in NIST biological reference materials 0ptima3000,ICP Application Study N° 62,、((1992). 3 Lanza, F.; Trincherini, P.R. “The determination of cadmium, lead and vanadium by highresolution ICP-MS in Antarctic snow samples” Annali di Chim. 90, 61-71 (1999). 4 Kojima, I.;Katsuzaki, M.66“Selective extraction and“one-drop” flame atomic absorptionspectrometric determination of silver in biological standard reference materials”Anal.Sciences, 13,1021-1023,(1997). 5 Liu, C.-Y.; Lee, N. -M. ; Wang, T.-H. “Chelation ion chromatography as a technique for traceelemental analysis in complex matrix samples”Analytica Chimica Acta, 337,(2),173-182,(1997). 6 Lopez-Ruiz, B. “Advances in the determination of inorganic anions by ion chromatography"J. Chromatogr. A, 881,607-627,((2000). 7 Nesterenko, P.N. “Simultaneous separation and detection of anions and cations in ionchromatography” Trends in Anal. Chem., 20, 311-319,(2001). ( 8 Curran, M. A. J.; Palmer, A. S. “Suppressed ion chromatography methods for the routinedetermination of u ltra- l ow l evel a nions and cations in ice cores” J. Chromatogr. A, 91 9 , 107-1 1 3, (2001). ) ( 9 Vanatta,l L.E. “ A pplication o f ion chromatography in the s emiconductor industry” Trends in Anal. Chem., 20,336-345, ( 2001). ) ( 10 Rahmalan, A .; A bdullah, M . Z.; Sanagi, M.M.; Rashid, M. “Determination of heavy m etals inair particulate matter b y ion c hromatography” J. Chromatogr. A , 739, 233-239, ( 1996). ) ( 11 Woods, C . ; Rowland, A . P. “Applications of a nion chromatography in terrestrial environmental research” J. C hromatogr. A , 789, 287-299, (1997). ) ( 12 Gros, N. ; Gorenc, B. “Performance of ion chromatography in the determination of anions an d cations in various natural waters wit h elevate d mineralization” J. Chromatogr. A, 7 70, 119-124, ( 1997). ) 13 Singh, R.P.; Abbas, N.M. ; Smesko, S. A. “Suppressed ion chromatographic analysis of anionsin environmental waters containing high salt concentrations” J. Chromatogr. A, 733, 73-91,(1996). ( 14 Darbouret, D.; Stewart, B. M. “Advancement i n t he production of ul t rapure water for ICP-MS metals analysis” Amer. L aboratory News, 3 0,( 9) ,(1 99 8). ) 15 Cheng, P.T.; Pritzker, K.P.“Pyrophosphate, phosphate ion interaction: effects on calciumpyrophosphate and calcium hydroxyapatite crystal formation in aqueous solutions”Rheumatol.,(10),769-77,(1983). 16 Darbouret, D.; Kano, I.; Youf, E. ; Stewart, B. “Optimizing storage of purified water forlaboratory applications"22 R&D Notebook, Millipore,RD001,(1999). 17 Darbouret, D. ; Kano, I. “Ultrapure water for elemental analysis down to ppt levels”RR&DNotebook, Millipore, RD002,,(1999). 18 Darbouret, D. ; Kano, I. “Ultrapure water for boron and silica sensitive laboratoryapplications”R&D Notebook, Millipore, RD003,(1999). 19 U. S. Environmental Protection Agency. Sample preservation in Methods for Chemical Analysisof Water and Wastes, EPA-600/4-79-020. U.S.E.P.A., Cincinnati, Ohio, USA, (1983). Lit.号: RD007EN00.2001年在法国印制 版权2001, Millipore 有限公司, Bedford, MA, U.S. A. Millipore, Milli-Q and Elix 是 Millipore 有限公司的注册商标。 Milli-Q 和 Progard 是 Millipore有限公司的商标 Dionex 是 Dionex 有限公司的注册商标。 版权所有,违者必究! www.millipore.com/H20 R&D手册:痕量离子色谱
确定





还剩4页未读,是否继续阅读?
彤迪科学仪器(上海)有限公司为您提供《超纯水中痕量离子色谱分析检测方案 》,该方案主要用于其他中痕量离子色谱分析检测,参考标准--,《超纯水中痕量离子色谱分析检测方案 》用到的仪器有
相关方案
更多








