方案详情
文
液相色谱仪常用检测器主要分为选择性检测器和通用型检测器,其中选择性检测器包括紫外 / 可见光吸收检测器(UVD)、二极管阵列检测器(DAD)、荧光检测器(FLD)等,通用型检测器主要指示差折光检测器(RI)、蒸发光散射检测器(ELSD)和质谱检测器(MS)等。质谱检测器(MS)尽管价格较昂贵,但是由于其在选择性、灵敏度、
分子量及结构信息等方面的优势,把它与各种分离手段联用,将定性、定量结果有机地结合在一起,近年来越来越广泛被应用于科研、制药、生物制药、化工合成等各个领域的分析。
方案详情

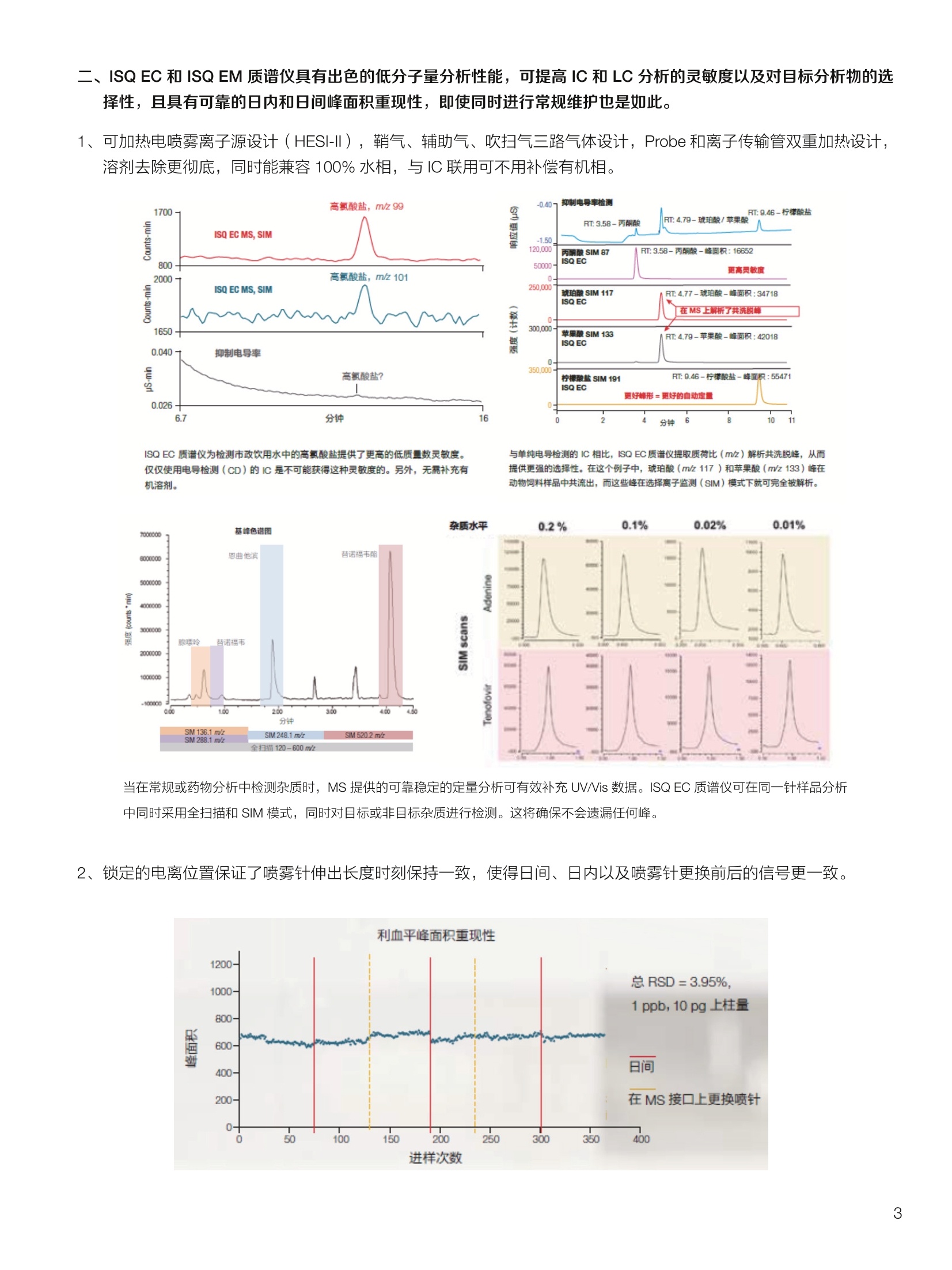
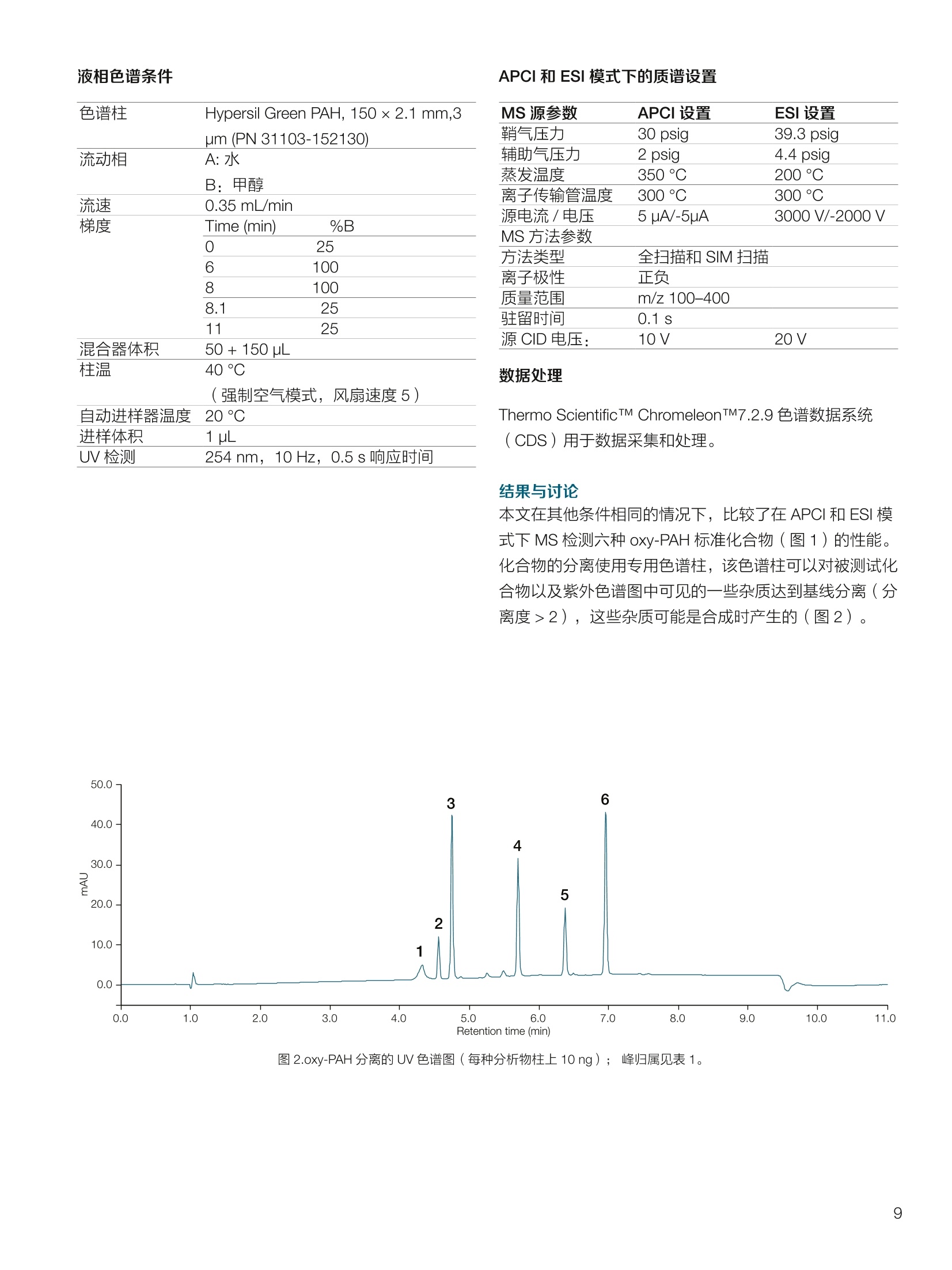
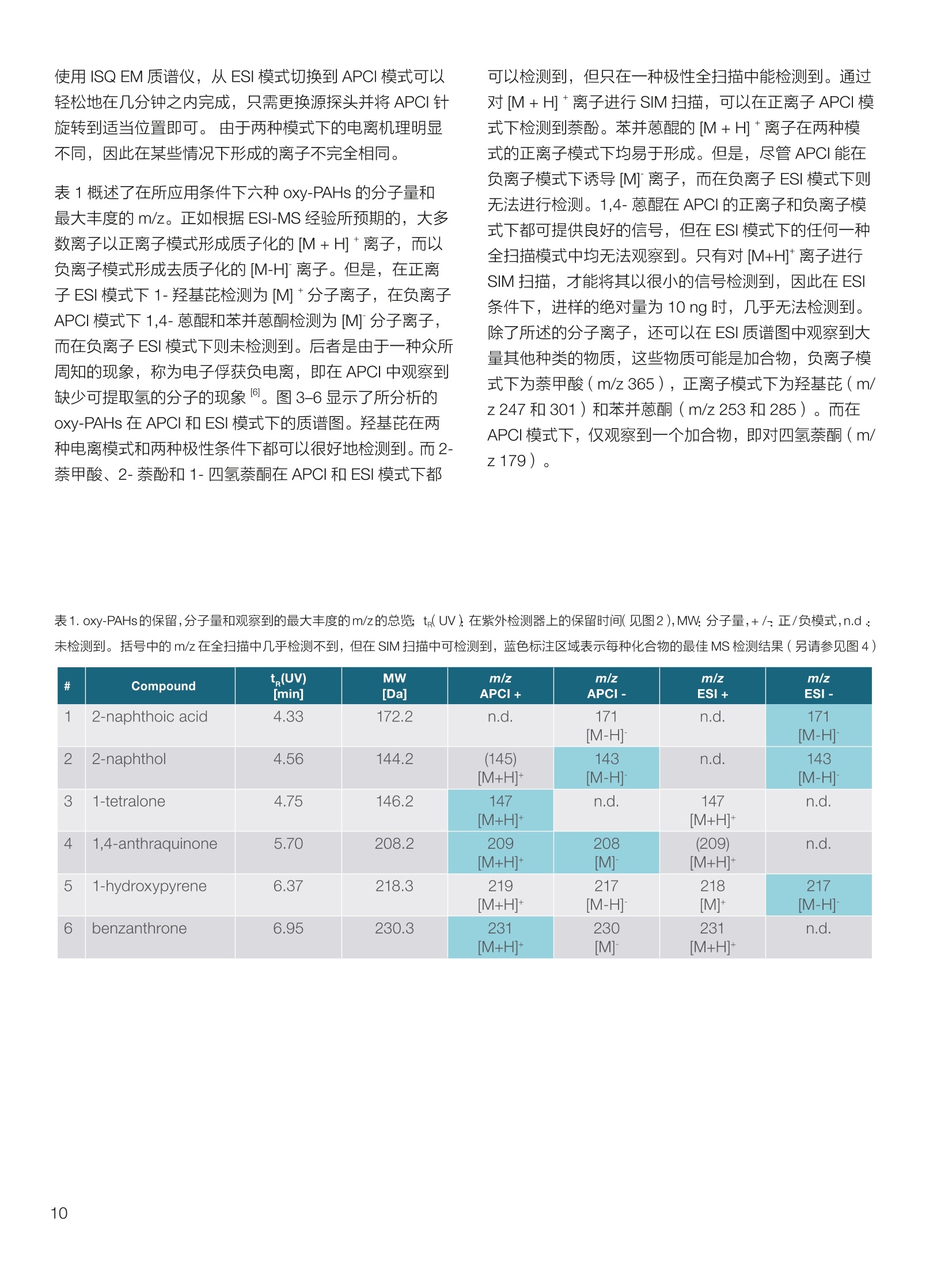
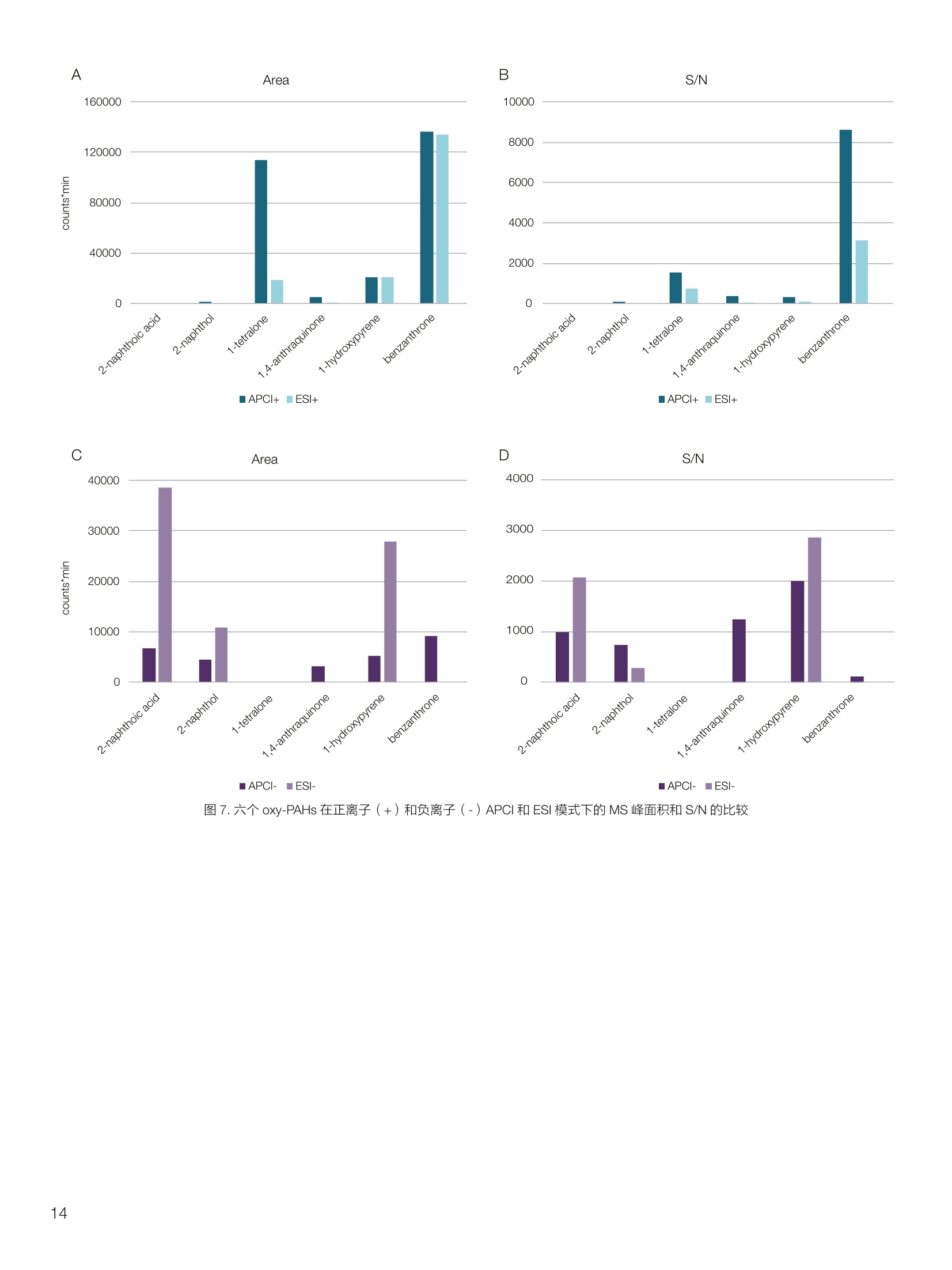
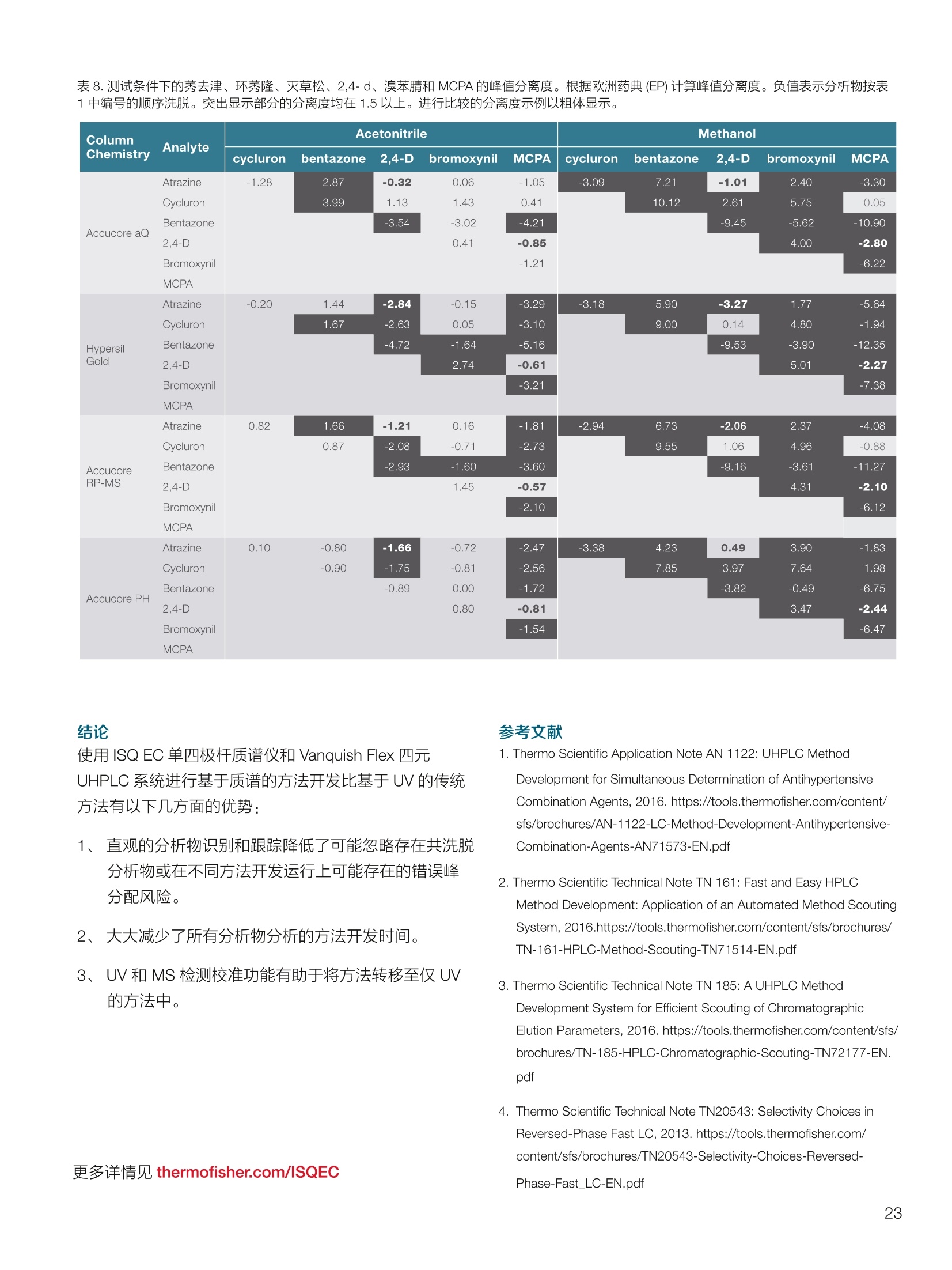
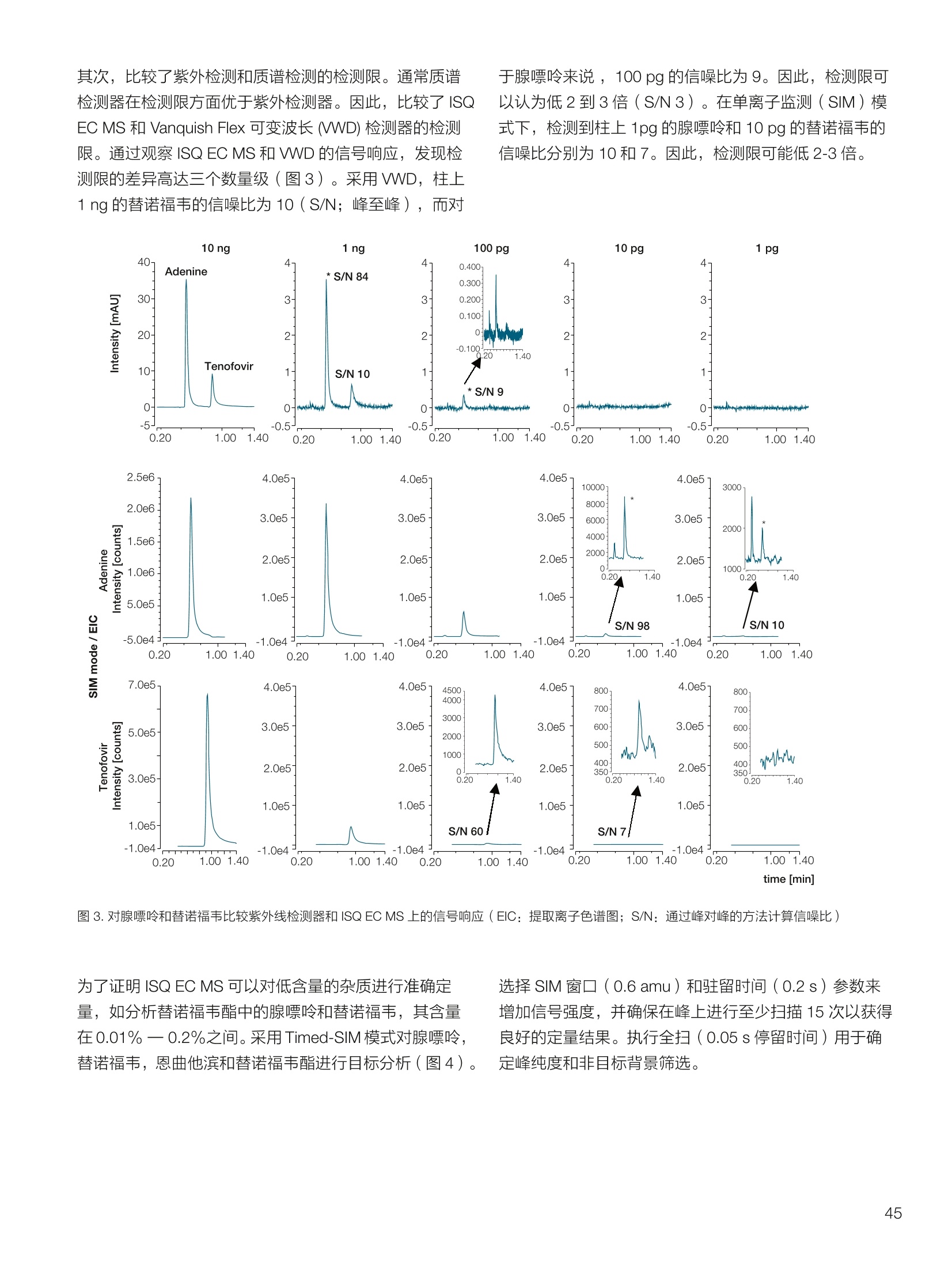
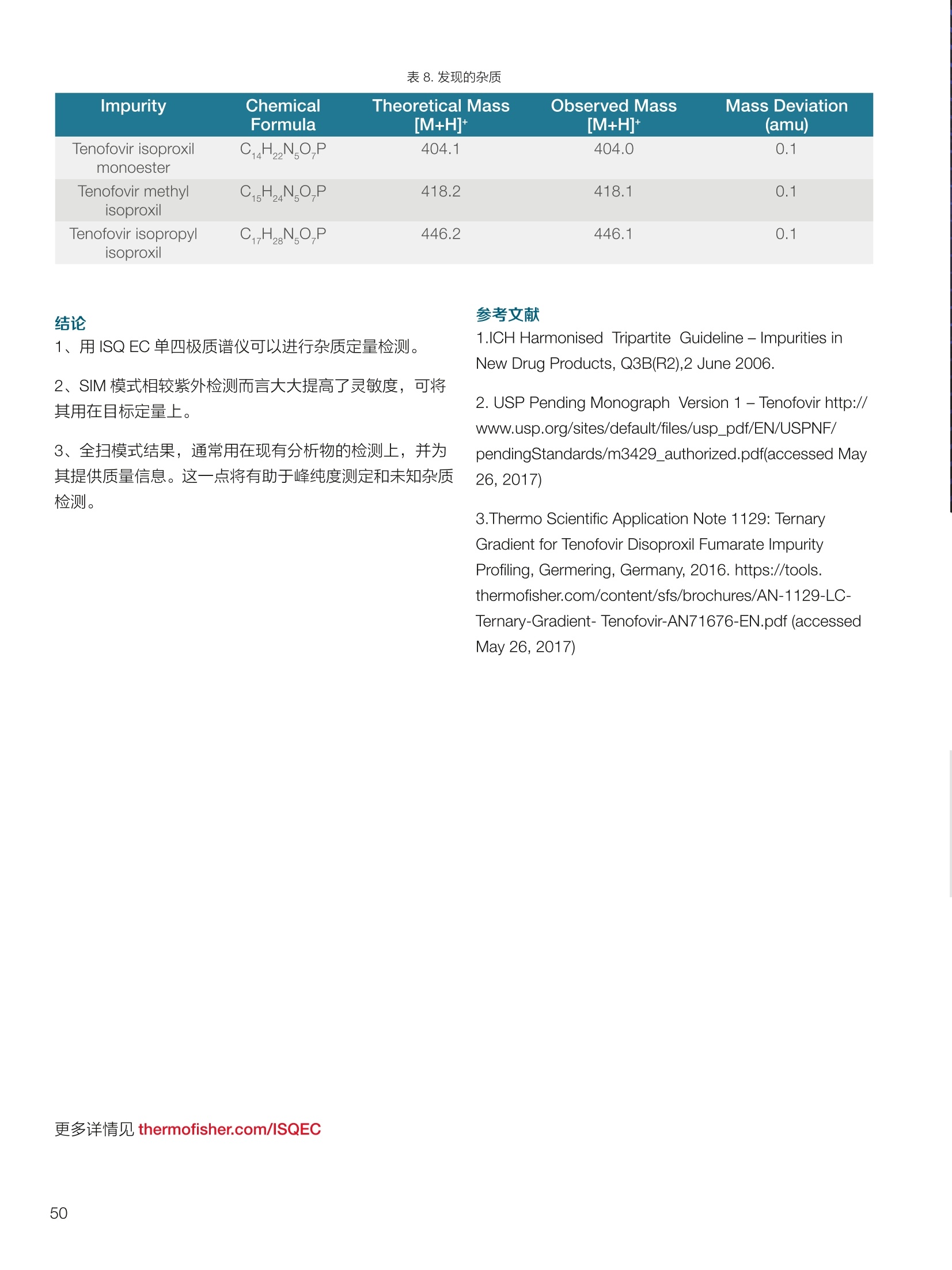
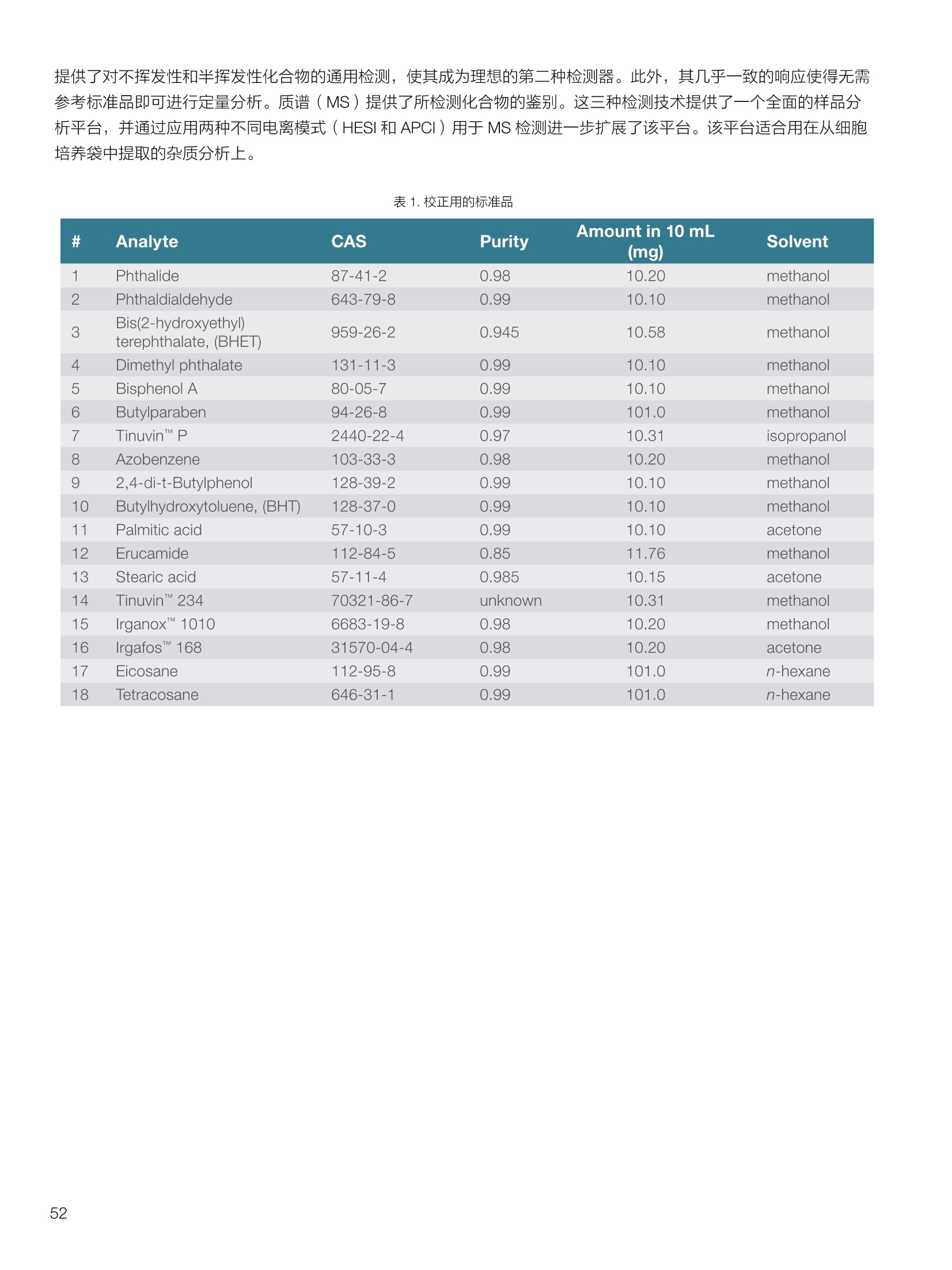
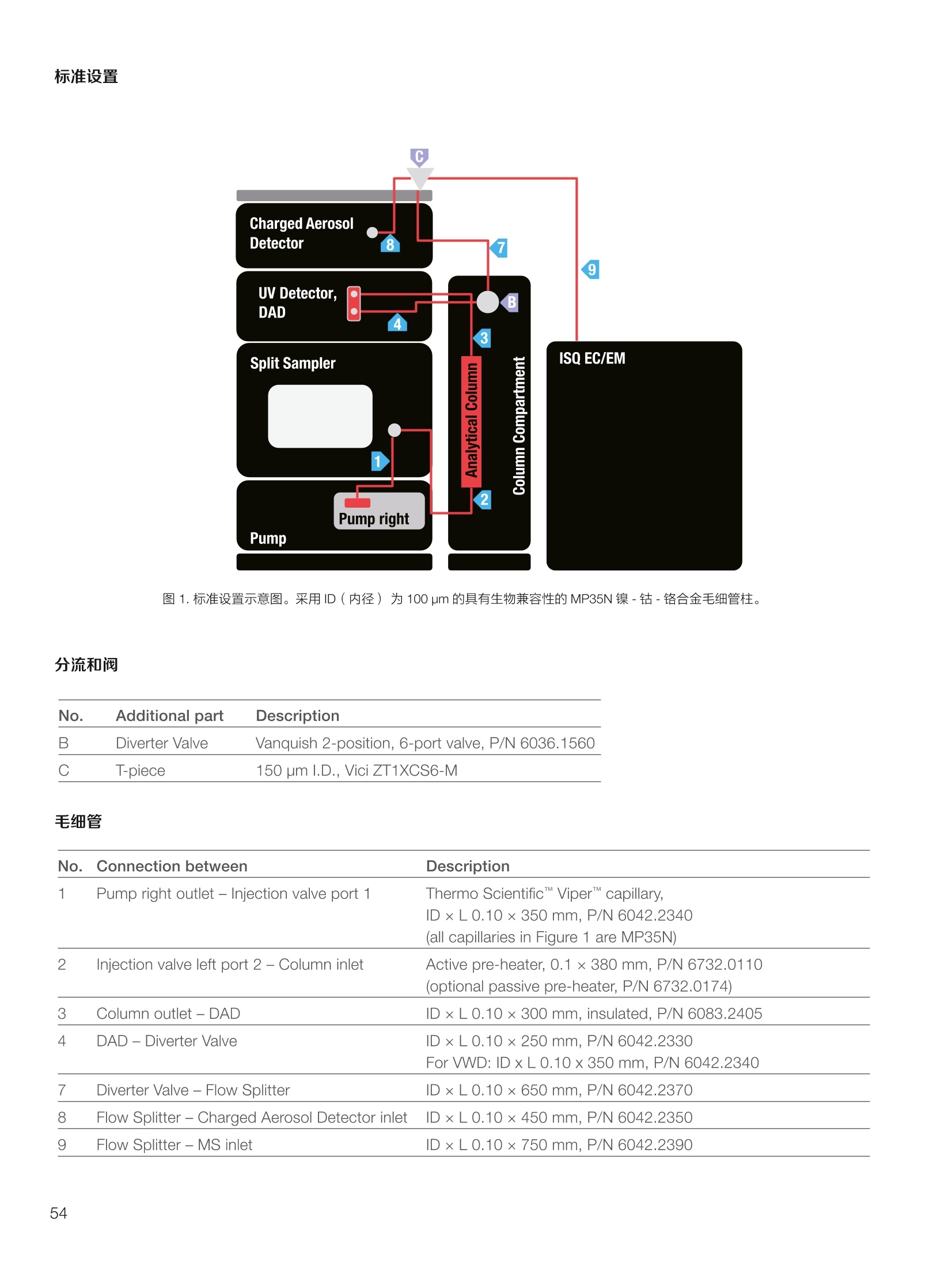
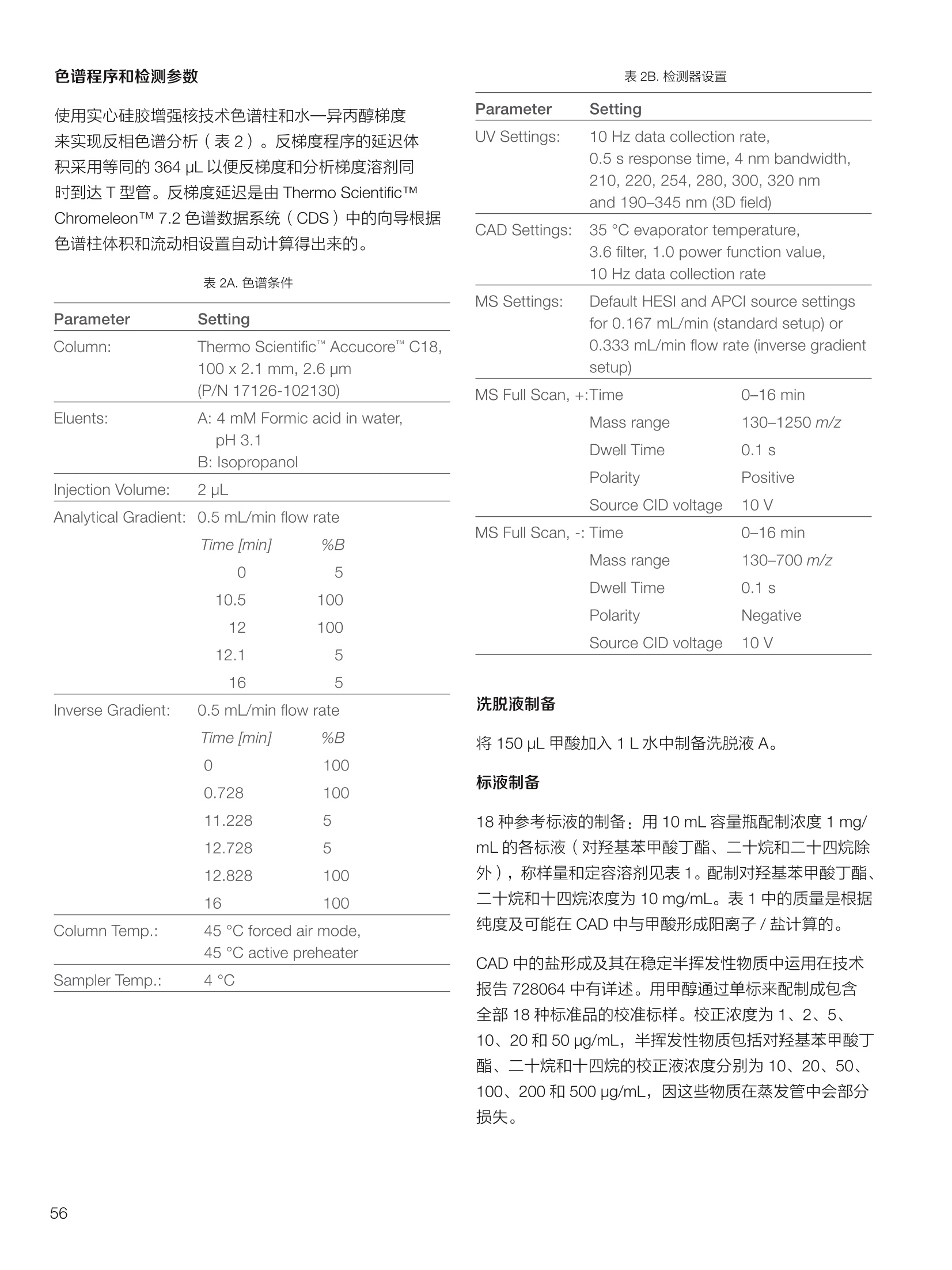
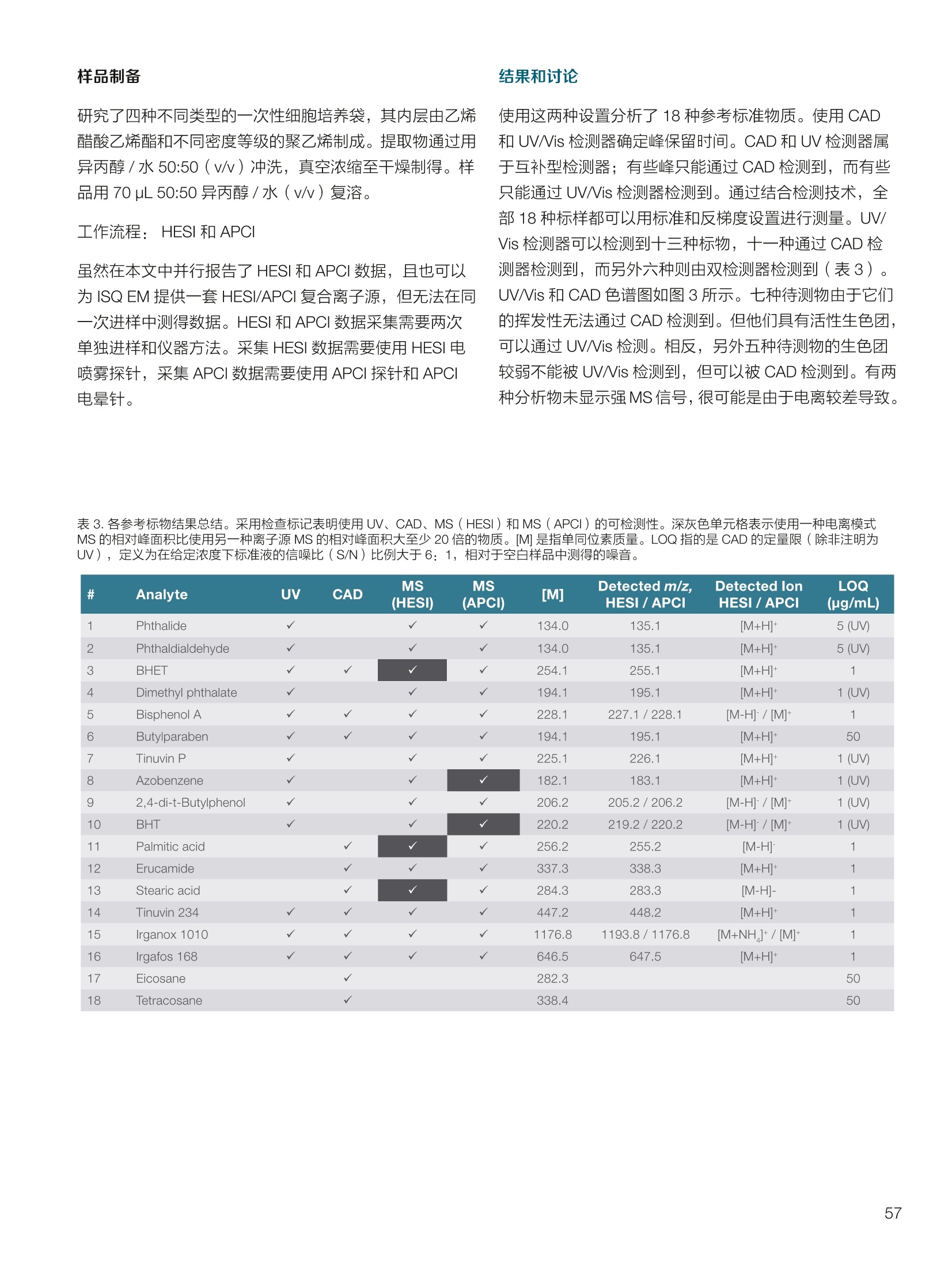
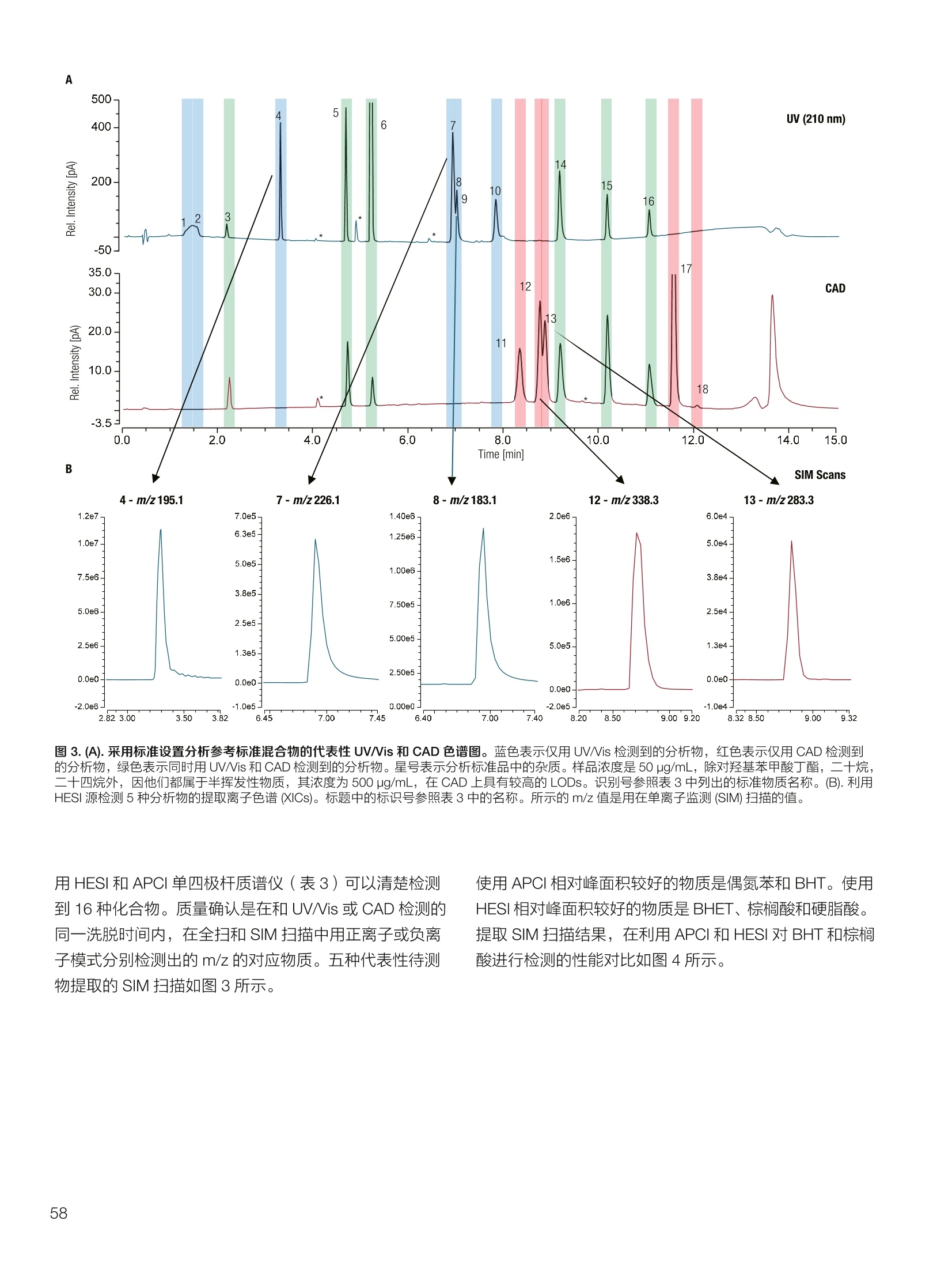
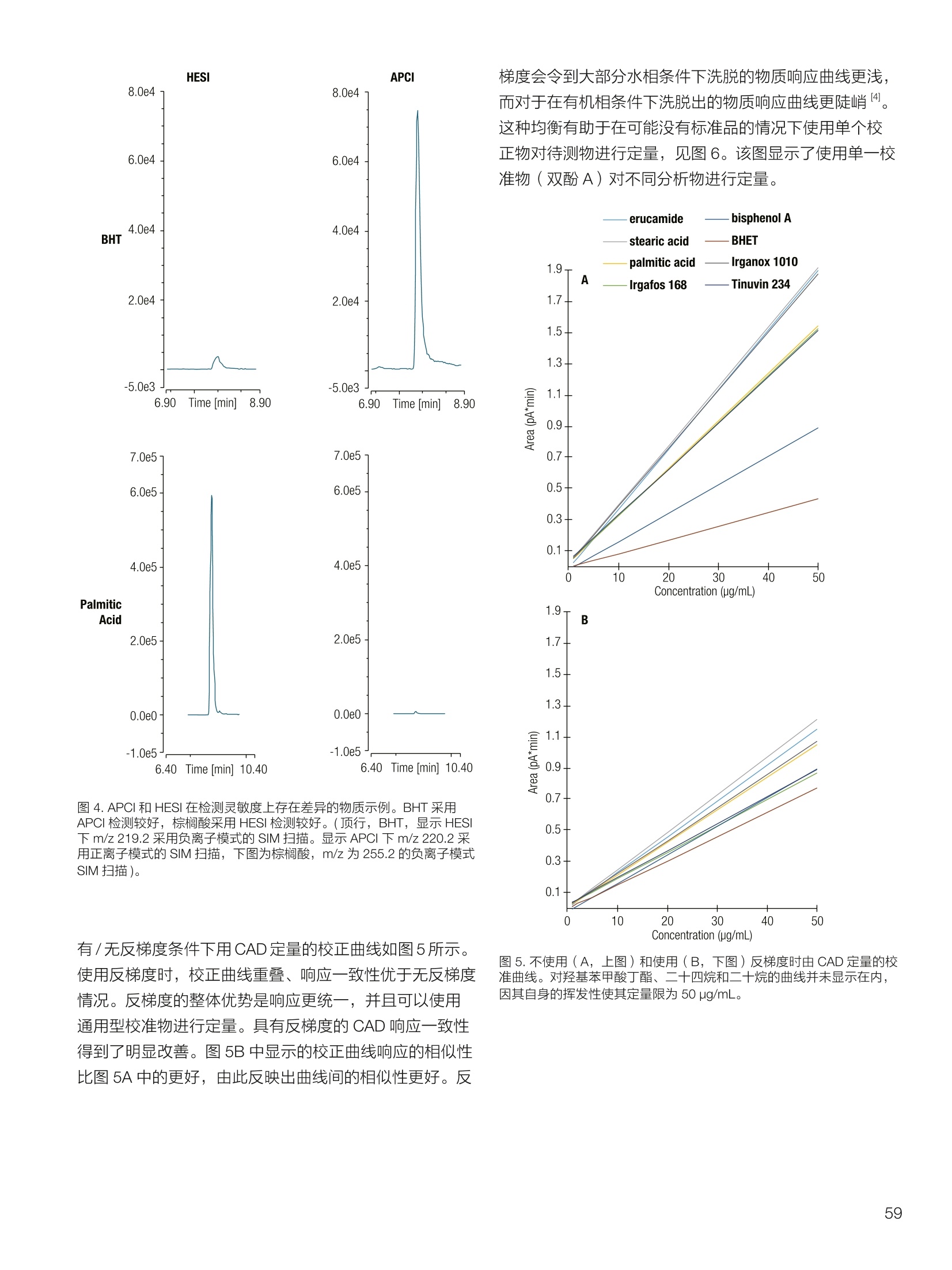
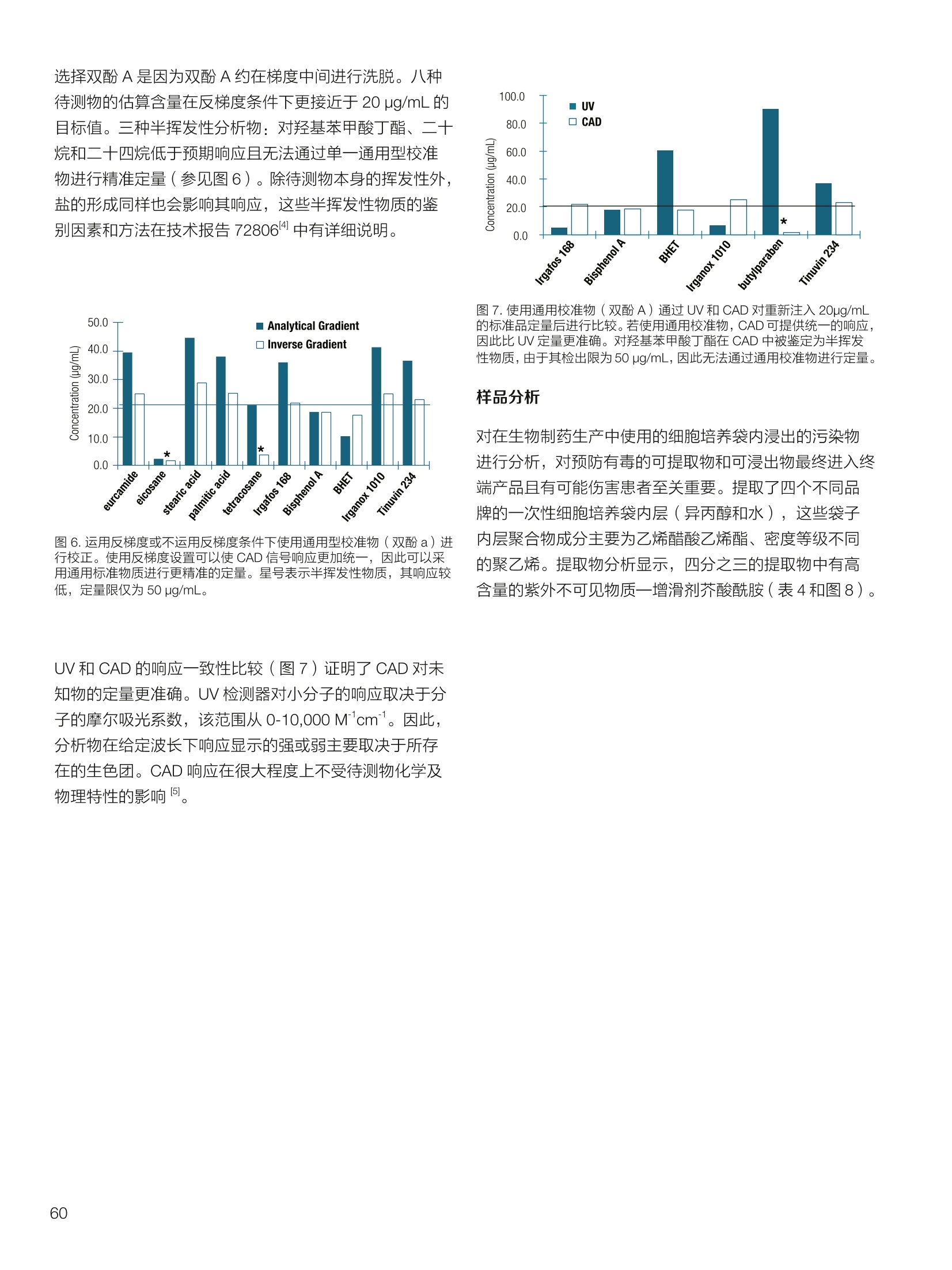
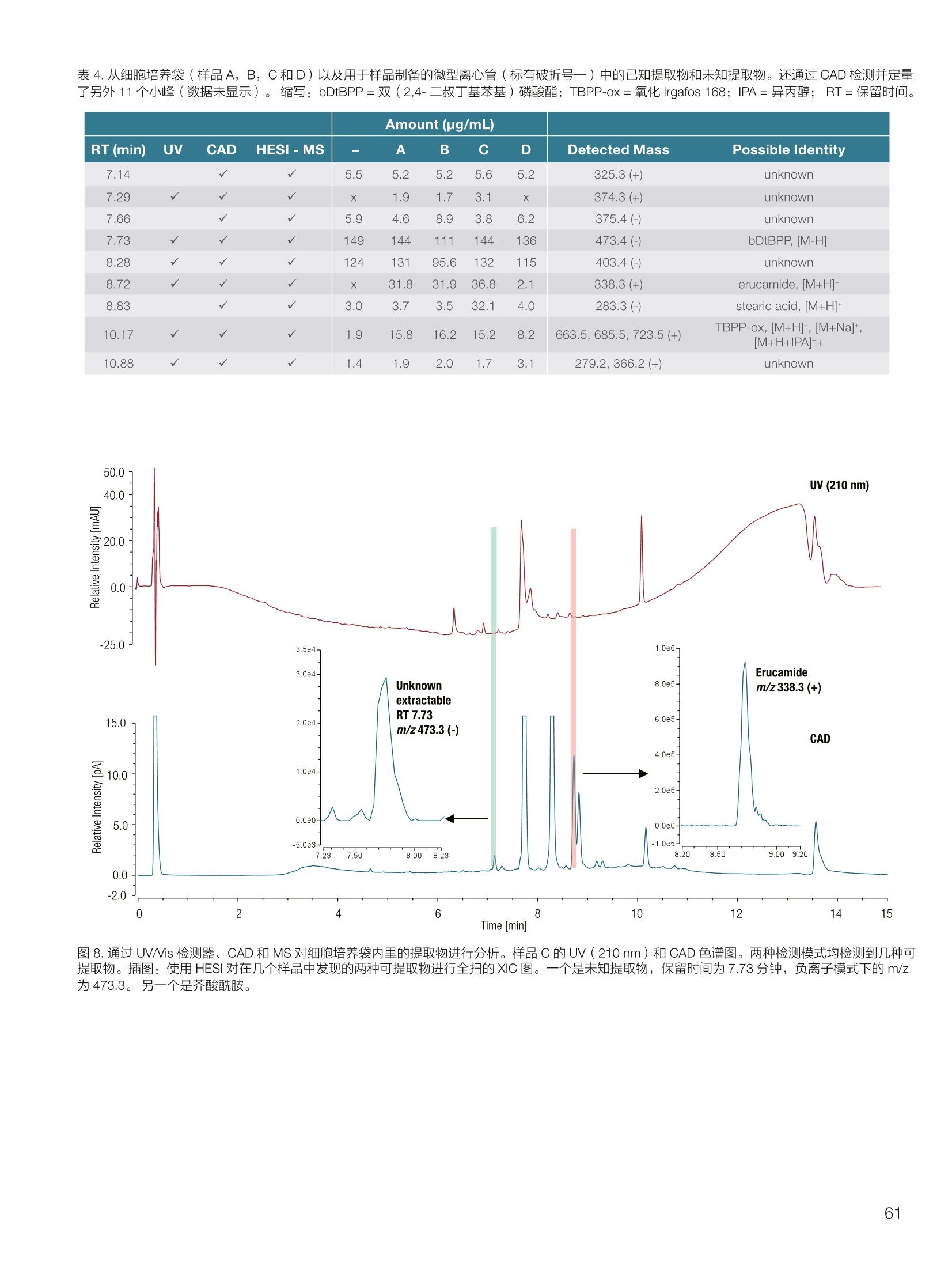
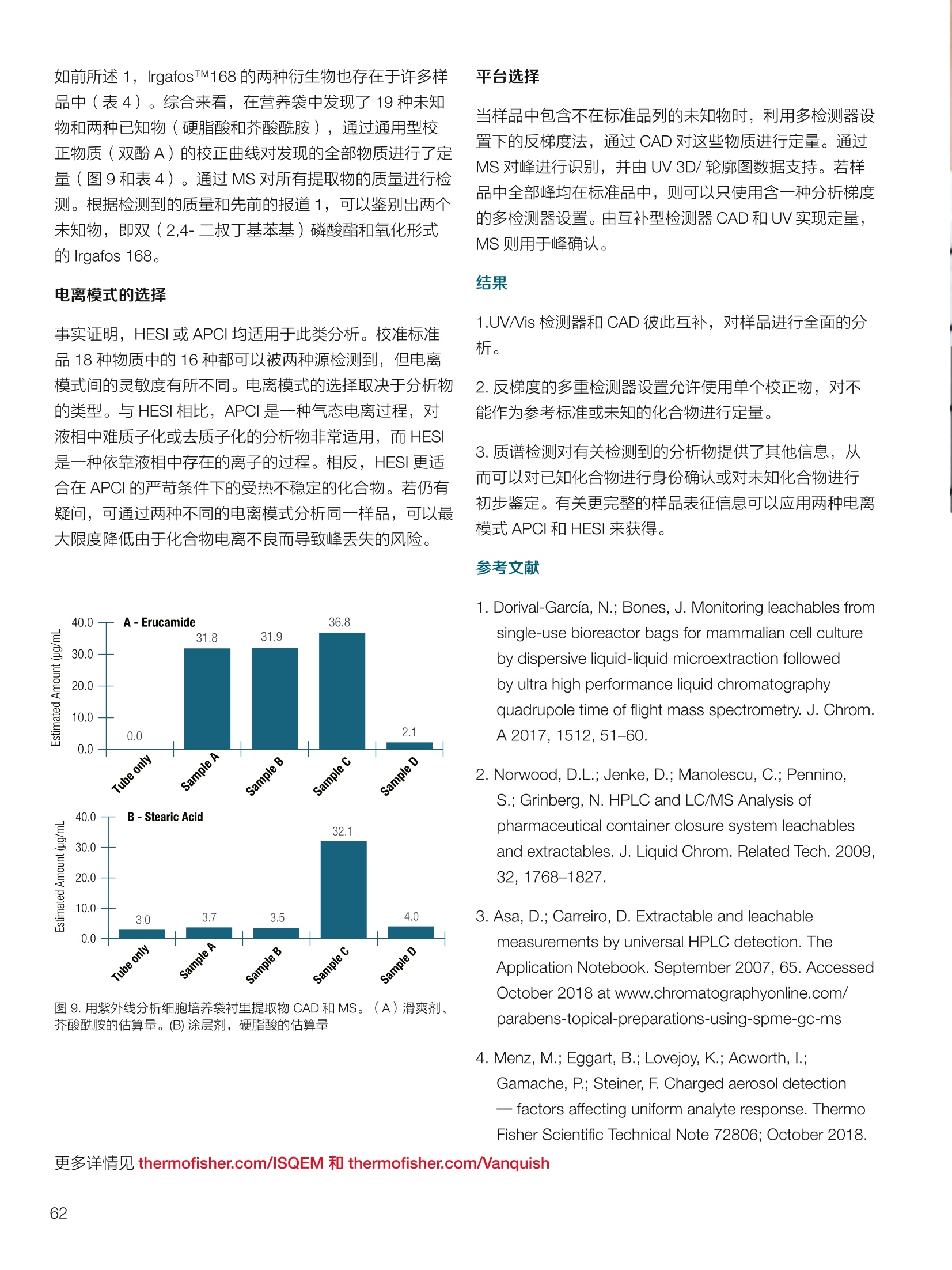
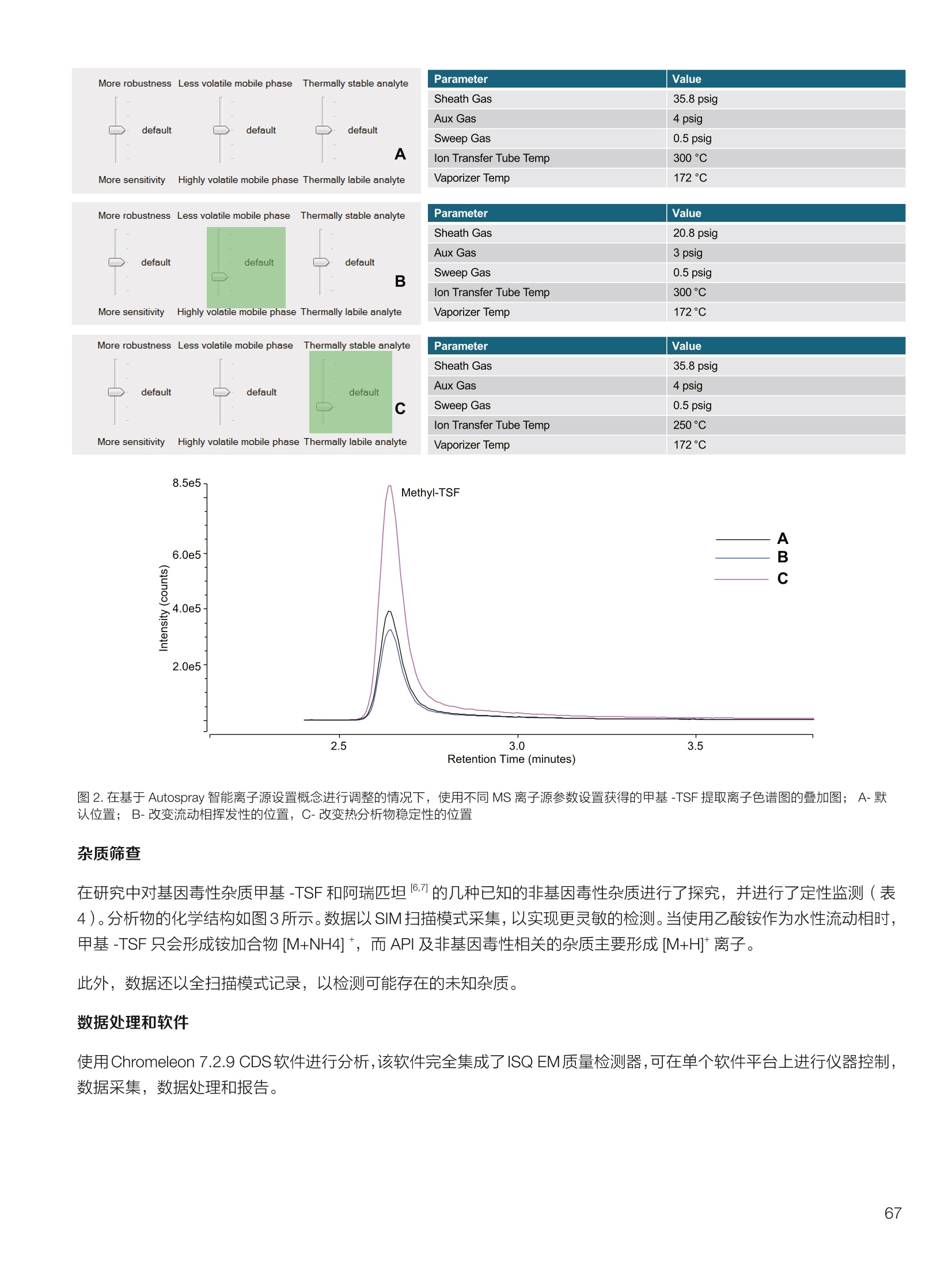
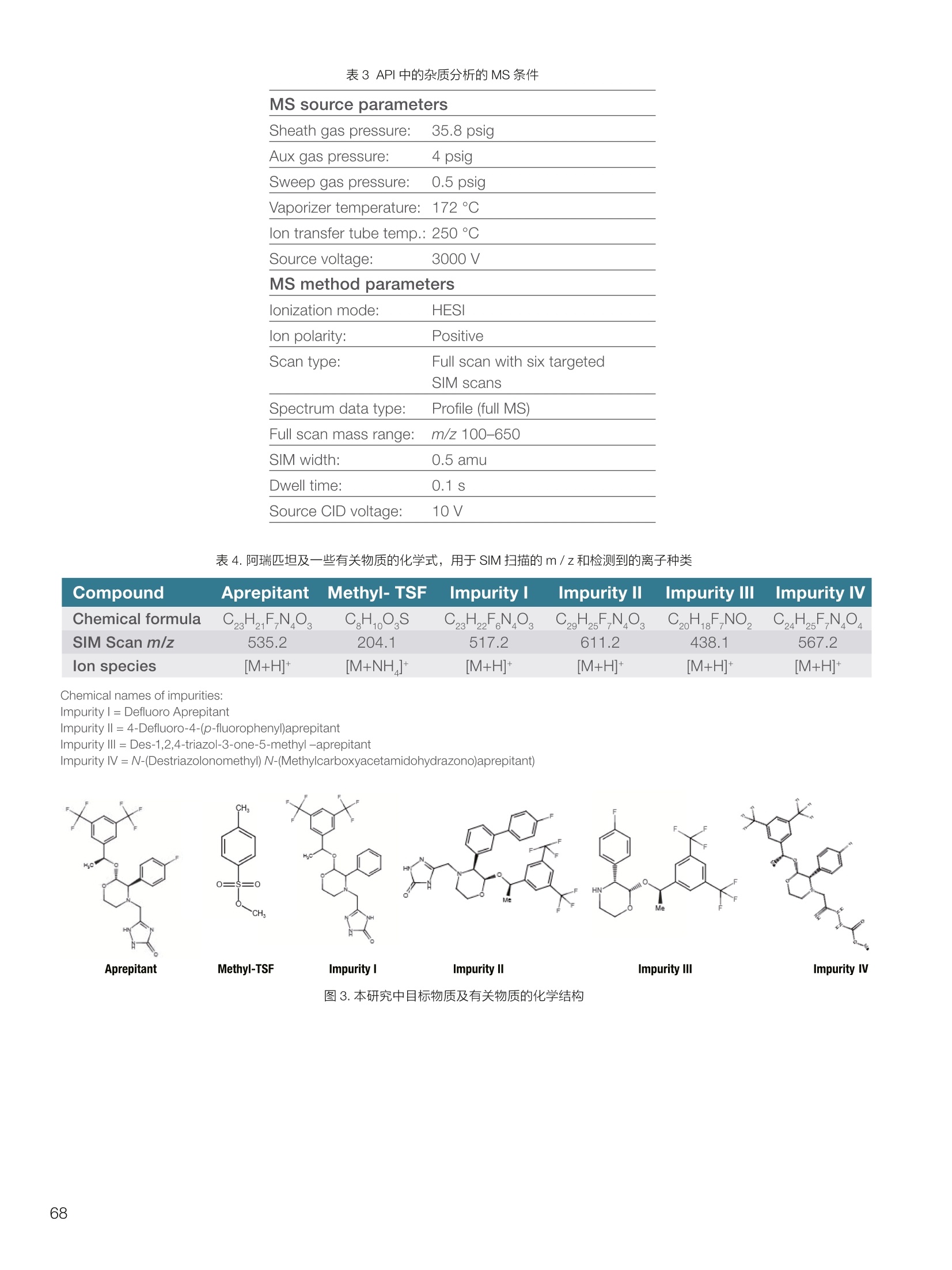
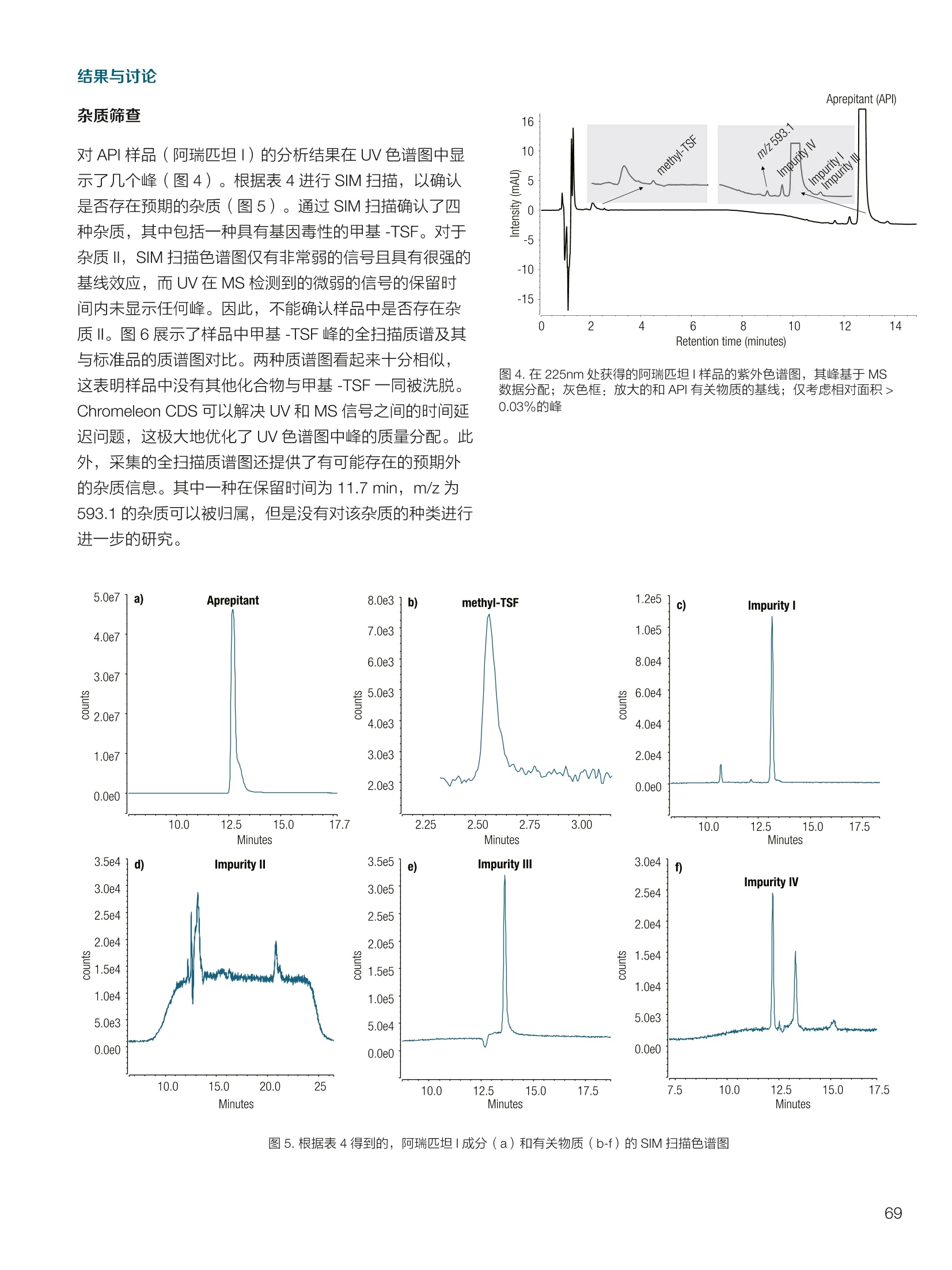
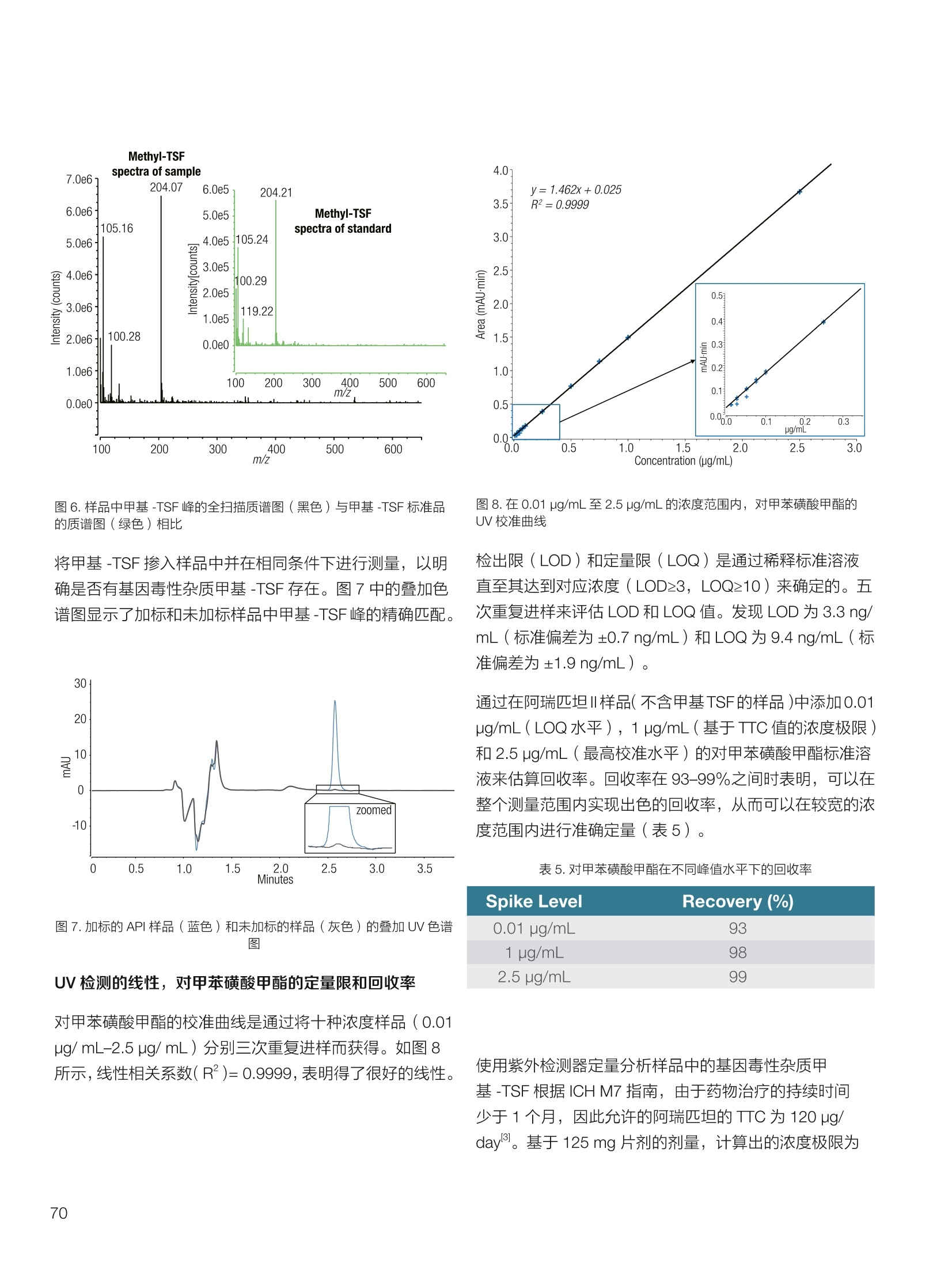
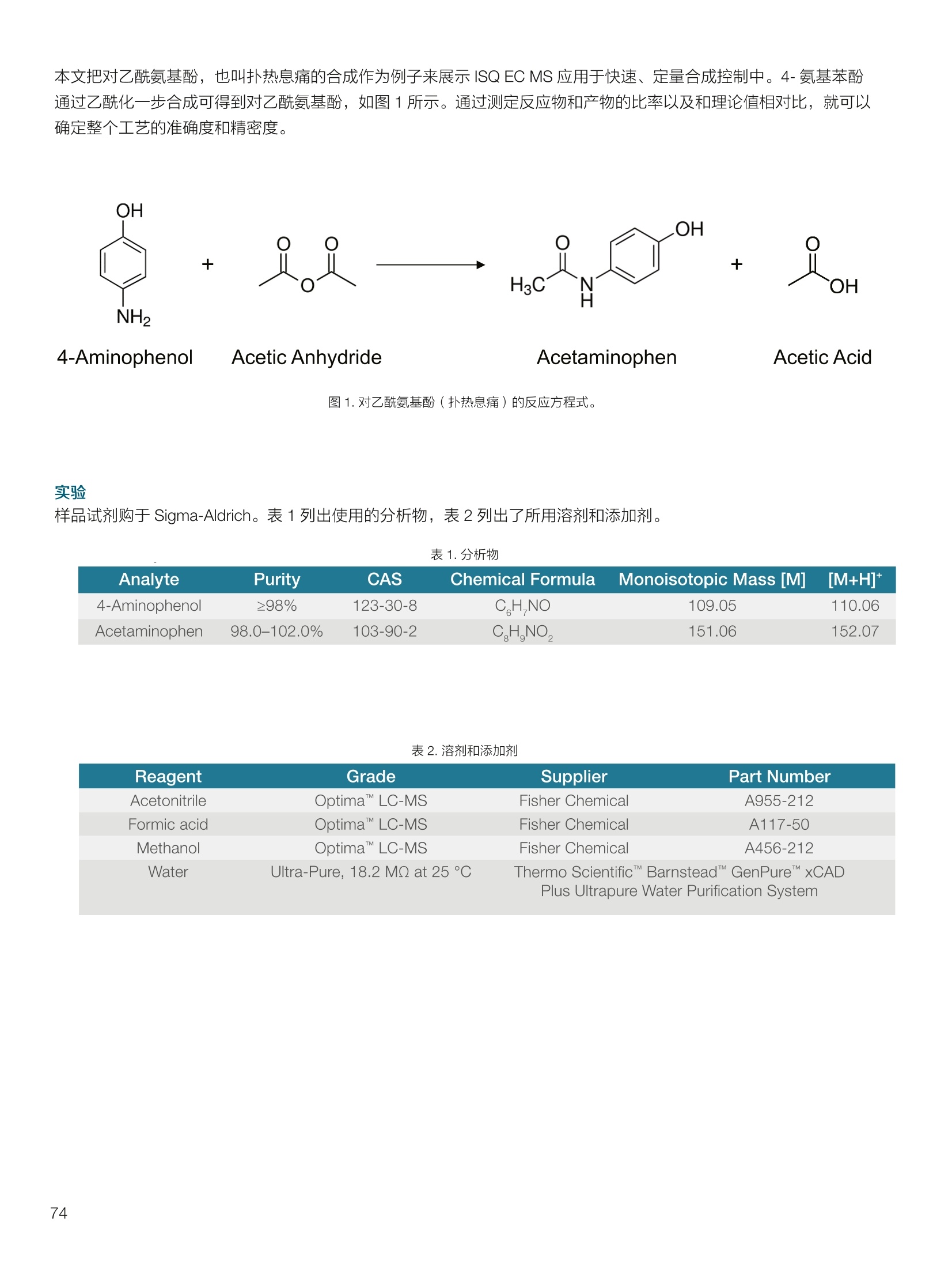
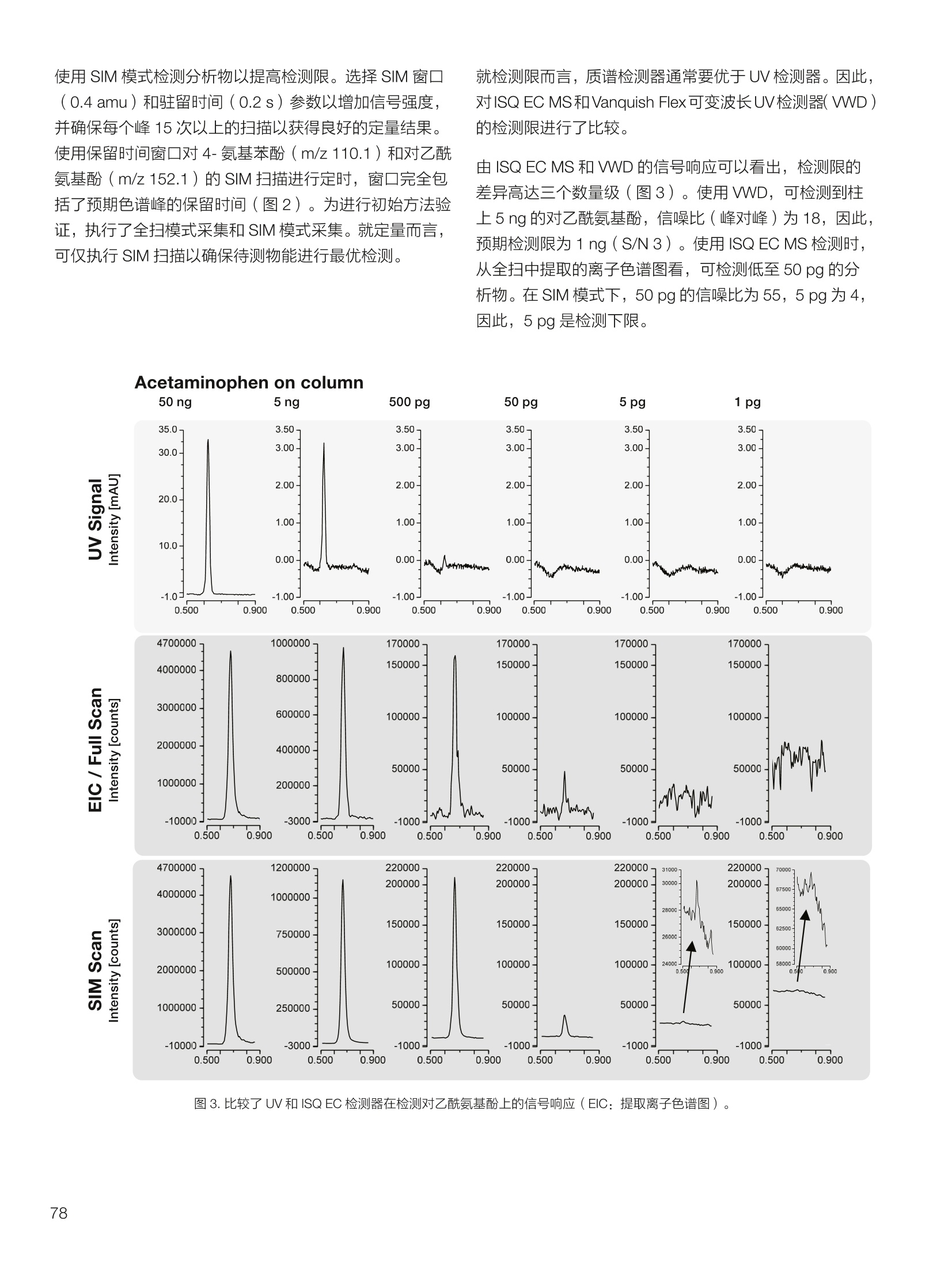
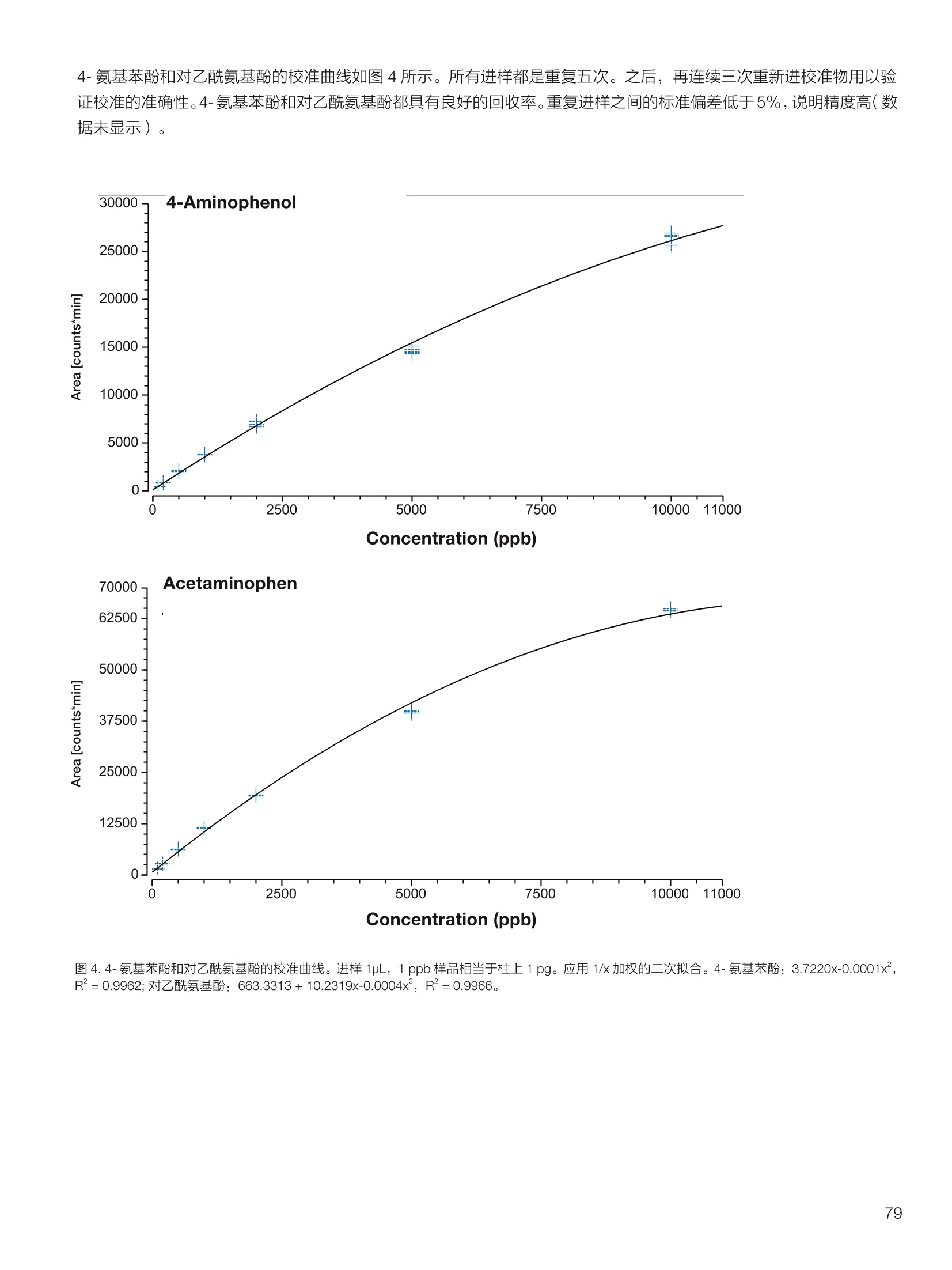
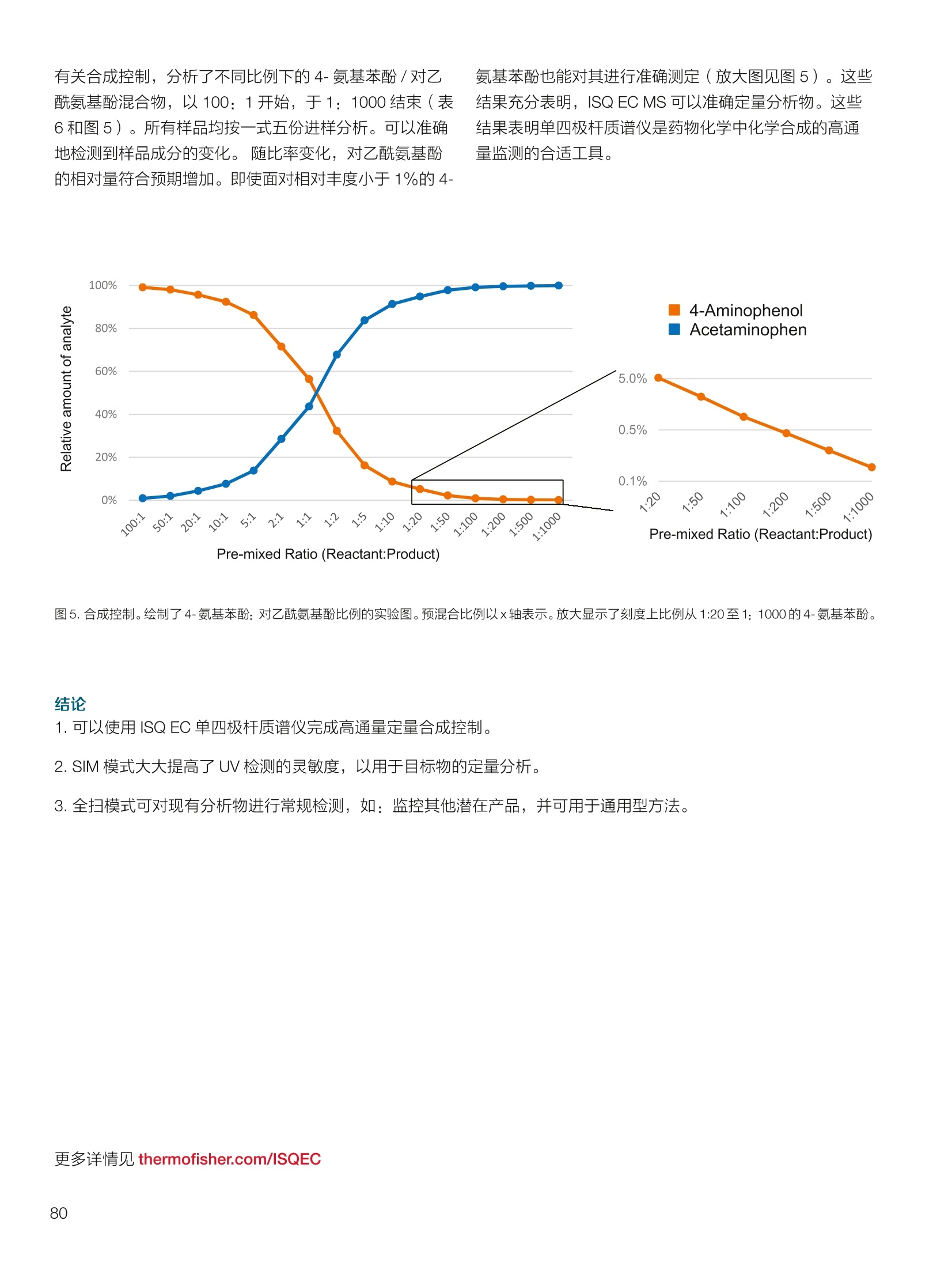
thermoscientific 1.0e6 Thermo Scientific 单四极杆质谱仪 ISQ EC&EM 应用文集 目录 第一部分前言....... .1 第二部分 ISQ单四杆杆质谱仪产品技术简介 .2 第三部分应用文摘 环境检测.. .6 AN72819::Detection of oxygenated polycyclic aromatic hydrocarbons (oxy-PAHs)in APCl mode with a single quadrupole mass spectrometer 使用单四极杆质谱仪APCI 模式检测氧化多环芳烃(oxy-PAHs) .7 AN72503: Accelerate method scouting with the Thermo Scientific ISQ EC singlequadrupole mass spectrometer and the Thermo Scientific Vanquish Flex QuaternaryUHPLC 使用 Thermo Scientific ISQEC单四极杆质谱仪和 Thermo ScientificVanquish Flex 四元 UHPLC 系统加快了方法筛选...... .16 生物制药.... .24 AN72818:Impurity profiling of the synthetic peptide LL-37 using high-performance liquid chromatography with combined UV and single quadrupole massspectrometric detection 采用高效液相色谱结合紫外和单四极杆质谱检测技术分析LL-37 合成肽中的杂质. .25 AN 72820: Oligonucleotide characterization for quality control and increasedproductivity by single quadrupole mass spectrometer with extended mass range 质量范围扩大的单四极杆质谱仪应用于寡核苷酸表征以进行质量控制和提高生产效率...... .32 制药.mmm .39 AN72391: Achieve confident impurity detection with the Thermo Scientific ISQ ECsingle quadrupole mass spectromete,r利用赛默飞 ISQ EC 单四极杆质谱实现可靠.的杂质检测. .40 AN72869:: AA multi-detector platform comprising UV/Vis, charged aerosol, andsingle quadrupole mass spectrometric detection for comprehensive sampleanalysis 集合UV/Vis、CAD 和单四极杆质谱的多检测器平台应用于样品全面分析.51 AN72976: Identity confirmation and accurate quantitation of a genotoxic impurity inan active pharmaceutical ingredient by UHPLC-UV coupled to a single quadrupolemass detector 通过 UHPLC-UV结合单四极杆质量检测器对活性药物成分中的基因毒性杂质进行定性和准确定量... .63 合成控制.. .72 AN72385: Achieve confident synthesis control with the Thermo Scientific ISQ ECsingle quadrupole mass spectrometer 利用 Thermo Scientific ISQ EC 单四极杆质谱仪实现可靠的合成控制... .73 液相色谱仪常用检测器主要分为选择性检测器和通用型检测器,其中选择性性测器包括紫外/可见光吸收检测器(UVD)、二极管阵列检测器(DAD)、荧光检测器(FLD)等,通用型检测器主要指示差折光检测器(RI)、蒸发光散射检测器(ELSD)和质谱检测器(MS)等。质谱检测器(MS)尽管价格较昂贵,但是由于其在选择性、灵敏度、分子量及结构信息等方面的优势,把它与各种分离手段联用,将定性、定量结果有机地结合在一起,近年来越来越广泛被应用于科研、制药、生物制药、化工合成等各个领域的分析。 赛默飞 ISQ EC 和 ISQ EM 单四极杆质谱仪集易用性和耐用性为一体,可与色谱系统无缝连接,让客户更加轻松地使用质谱仪去分析各种复杂的样品,获得更多的样品信息。本文集结合了 ISQ EC 和 ISQ EM 的设计特点,收集的典型应用文摘涉及环境检测、制药、生物制药、化学合成等领域,希望能对相关科研工作者和色谱分析人员提供一定的参考和借鉴。 赛默飞世尔科技(中国)应用中心 2020年4月 全面了解您所分析的样品始终是一项具有挑战性的工作。尽管质谱(MS)联用技术具有明显的分析优势,但是,我们都知道需要熟练掌握不是件容易的事。这个时候您一定在想:如果有一款质谱仪能让从样品分析到获取样品信息都最简便就好了!这就是为什么我们要设计 Thermo Scientific MISQTM EC 和 Thermo ScientificM ISQTM EM单四极杆质谱仪的初衷,集耐用性和易用性于一体。 ISQ EC 质谱仪与 IC 和 LC系统集成使用,为常规单四极杆 MS 提供出色的耐用性和性能。 ISQ EM 质谱仪将应用范围拓展到大分子,具有 HESI 和 APCI 两种电离模式,用于分析极性和非极性化合物,大大扩充了单四极杆质谱仪的应用范围。 一、ISQ EC 和 ISQ EM 质谱仪可用于分析各种复杂样品基质,具有无与伦比的耐用性。 1、ISQ EC 和 ISQ EM 质谱仪配备正交离子源,专门用于分析具有挑战性的样品基质。离子源通过节省维护时间,提供更长时间的不间断操作。 2、ISQ EC 和 ISQ EM 质谱仪配备S型预杆,过滤中性粒子和噪音,在提高仪器信噪比的同时,大大提高质量分析器的耐用性。 二、ISQ EC 和 ISQ EM 质谱仪具有出色的低分子量分析性能,可提高 IC 和 LC分析的灵敏度以及对目标分析物的选择性,且具有可靠的日内和日间峰面积重现性,即使同时进行常规维护也是如此。 1、可加热电喷雾离子源设计(HESI-II),鞘气、辅助气、吹扫气三路气体设计, Probe 和离子传输管双重加热设计,溶剂去除更彻底,同时能兼容100%水相,与IC联用可不用补偿有机相。 ISQ EC 质谱仪为检测市政饮用水中的高氨酸盐提供了更高的低质量数灵敏度。仅仅使用电导检测(CD) 的 IC是不可能获得这种灵敏度的。另外,无需补充有机溶剂。 与单纯电导检测的 IC 相比, ISQ EC 质谱仪提取质荷比(m/z)解析共洗脱峰,从而提供更强的选择性。在这个例子中,球珀酸(m/z 117) 和苹果酸(m/z 133) 峰在动物饲料样品中共流出,而这些峰在选择离子监测(SIM)模式下就可完全被解析。 当在常规或药物分析中检测杂质时, MS提供的可靠稳定的定量分析可有效补充 UV/Vis 数据。 ISQ EC 质谱仪可在同一针样品分析中同时采用全扫描和 SIM 模式,同时对目标或非目标杂质进行检测。这将确保不会遗漏任何峰。 2、锁定的电离位置保证了喷雾针伸出长度时刻保持一致,使得日间、日内以及喷雾针更换前后的信号更一致。 三、ISQ EC 和 ISQ EM 质谱仪配备真空互锁模式,无需卸真空即可进行日常维护,使得仪器的日常维护变得更简便快速,大大提高仪器的连续运行时间。 四、ISQ EC 和 ISQ EM 质谱仪通过单一变色龙数据处理系统控制,无需任何插件并依从合规性。通过快速访问质谱仪界面控件中内置的实验信息,快速获得高品质结果。配备Easy Mode和Advanced Mode两种模式进行参数设置,无论是质谱新手还是专业分析人员的需求都可满足。当然,也可以通过 Thermo ScientificTM ChromeleonTMXPSOpenAccess 用户界面进行直观的常规分析工作流程,简化分析流程即可得到分析结果。 Easy Mode 通过直观的离子源技术工具帮助您根据以上三个参数选择适合的 MS 条件。 Vaporizer temperature: 338 Sheath gas pressure: 56.9 psig lon transfer tube temperature: 300 ℃ Aux gas pressure: 6.5 psig Source voltage positive ions: 3000 v Sweep gas pressure: 0.5 psig 五、ISQ EM 质谱仪能够在一个比较宽泛的质量数范围内对大分子和小分子做定量检测,同时使用 HESI和 APCI(大气压化学电离)两种模式检测极性和非非性化合物。 图(TIC)示例中,目标37氨基酸合成肽LL-37(活性药物成分,4500Da)及其两个相关碎片在2分钟内得到分离。 进行其他实验,是不可能实现峰归属的。 ISQ单四极杆质谱相关指标参数 应用文摘 一环境检测 应用文章72819 使用单四极杆质谱仪以APCI模式检测氧化多环芳烃(oxy-PAHs) 作者 Maria Grubner; Thermo Fisher Scientific, Ger-mering, Germany 关键词 APCI, 大气压化学电离,质谱,单四极杆质谱仪,高效液相色谱,ESI, 电喷雾电离,氧化多环芳烃,oxy-PAHs, ISQ EM, Vanquish Flex UHPLC, LC-MS, UHPLC 目标 证明了用Thermo ScientificTMISQTMEM单四极杆质谱仪对oxy-PAHs进行检测时,使用APCI-MS检测相较于ESI-MS检测的优势。 应用优势 1、APCI为像 oxy-PAHs 等电离性差的化合物提供了可替代标准ESI的电离模式。 2、使用APCI时,信噪比通常更高,并且形成的加合物更少。 简介 多环芳烃(PAHs)是水、植物、食物、土壤和大气中普遍存在的环境污染物1-3。这些化合物至少包含两个稠合的芳环,其是由人为和自然界中的不完全燃烧过程产生的。多环芳烃以及伴随的衍生物,如氧化多环芳烃(oxy-PAHs), 也是通过燃烧或在二次反应中形成的,其表现出严重的毒性和致癌性。由于其有害性以及人体不可避免的会通过皮肤吸收、吸入以及最关键的摄入而引起的暴露,因此大量的环境和营养研究专注于各种材料中此类化合物的分析以及其对人与自然的风险评估1-3。 气相色谱分离与质谱(MS)联用是一种常用的 PAH分析技术1.3.4。但是,极性官能团会降低化合物的挥发性,因此该法在检测 oxy-PAHs 时的灵敏度较低,或者需要对其进行衍生化。另一种是基于高效液相色谱(HPLC)的技术,这种技术适用于光学(UV和/或荧光)或 MS检测4.5。虽然在大多数 LC-MS应用中,电喷雾电离(ESI)通常是首选的电离技术,但是大气压化学电离源(APCI)已被证明是应用于 oxy-PAHs分析的更好的电离模式14,6] 本应用文摘展示了 ISQ EM 单四极杆质谱仪使用 APCI-MS模式对六种 oxy-PAHs 标准化合物进行检测的能力(结构如图1所示),并与使用同一仪器的 ESI-MS模式进行检测进行了对比。使用 Thermo ScientificTMVanquishTMFlex二元 UHPLC 系统和 Thermo Scientific TMHypersilTMGreenPAH LC 色谱柱进行分离,该色谱柱的固定相专为此类分析物定制。 .OH 图1.本文中分析的六个 oxy-PAHs 的结构 实验 试剂 ( ·去离子水,电阻率18.2MQ·cm或更高(P/NN/A) ; ) ( ·Fisher ScientificTM 甲醇, OptimaTMLC / MS 级 (P/N A456-212); ) ( ·慕尼黑工业大学(Thomas Letzel)友善提供2-萘甲酸、 2-萘酚、苯并蒽醌、1-羟基芘、1,4-蒽醌和1-四氢萘酮的合成标准品。 ) 仪器 使用配备 ISQ EM 单四极质谱仪的 Vanquish Flex BinaryUHPLC 系统进行分析。 ·Thermo ScientificTMVanquishTM 色谱系统 VanquishHorizon / Flex( P/N VF-S01-A-02) · Thermo ScientificTMVanquishTM 二元泵 F (P/N VF-P10-A-01) Thermo ScientificTMVanquishTM分流进羊器 HT(P/NVH-A10-A-02) · Thermo ScientificTMVanquishTM 柱温箱H(P/NVH-C10-A-02) 。 Thermo ScientificTMVanquishTM 可变波长检测器F(P/NVF-D40-A-01) ·Flow Cell Semi-Micro, 2.5pL, 7mm 光程长度(SST)(P/N 6077.0360) ·ISQ EM质谱普(P/NISQEM-ESI-APCI) 标准配制 使用甲醇配制浓度为1 mg /mL的标准化合物储备溶液。注射入 UHPLC-MS系统的工作溶液是通过将各储备溶液混合后,用甲醇进一步稀释而得。工作溶液的最终浓度为每种分析物 10 pg/mL. MS源参数 APCI设置 ESI设置 鞘气压力 30 psig 39.3 psig 辅助气压力 2 psig 4.4 psig 蒸发温度 350°C 200°C 离子传输管温度 300°℃ 300 °C 源电流/电压 5 pA/-5pA 3000V/-2000V MS方法参数 0 25 方法类型 全扫描和 SIM 扫描 100 离子极性 正负 100 质量范围 m/z 100-400 25 驻留时间 0.1s 25 源 CID电压: 10V 20V 柱温 40°C (强制空气模式,风扇速度5) 自动进样器温度 20°C 进样体积 1uL UV检测 254 nm, 10 Hz, 0.5 s响应时间 使用 ISQ EM 质谱仪,从ESI模式切换到 APCI 模式可以轻松地在几分钟之内完成,只需更换源探头并将 APCI针旋转到适当位置即可。由于两种模式下的电离机理明显不同,因此在某些情况下形成的离子不完全相同。 表1概述了在所应用条件下六种 oxy-PAHs 的分子量和最大丰度的 m/z。正如根据 ESI-MS 经验所预期的,大多数离子以正离子模式形成质子化的[M+H]+离子,而以负离子模式形成去质子化的[M-H]离子。但是,在正离子ESI模式下1-羟基芘检测为[M]+分子离子,在负离子APCI 模式下 1,4-蒽醌和苯并蒽酮检测为[M]分子离子,而在负离子 ESI模式下则未检测到。后者是由于一种众所周知的现象,称为电子俘获负电离,即在APCI中观察到缺少可提取氢的分子的现象象。图3-6显示了所分析的oxy-PAHs 在 APCI和 ESI模式下的质谱图。羟基芘在两种电离模式和两种极性条件下都可以很好地检测到。而2-萘甲酸、2-萘酚和1-四氢萘酮在 APCI和ESI模式下都 可以检测到,但只在一种极性全扫描中能检测到。通过对[M+H]+离子进行 SIM 扫描,可以在正离子 APCI 模式下检测到萘酚。苯并并醌的[M+H]+离子在两种模式的正离子模式下均易于形成。但是,尽管 APCI 能在负离子模式下诱导[M]离子,而在负离子ESI模式下则无法进行检测。1,4-蒽醌在 APCI 的正离子和负离子模式下都可提供良好的信号,但在ESI模式下的任何一种全扫描模式中均无法观察到。只有对[M+H]* 离子进行SIM 扫描, 才能将其以很小的信号检测到,因此在ESI条件下,进样的绝对量为10 ng时,几乎无法检测到。除了所述的分子离子,还可以在 ESI 质谱图中观察到大量其他种类的物质,这些物质可能是加合物,负离子模式下为萘甲酸(m/z365),正离子模式下为羟基芘(m/z247和301)和苯并蒽酮(m/z253和285)。而在APCI 模式下,仅观察到一个加合物,即对四氢萘酮(m/z179)。 表1.oxy-PAHs的保留,分子量和观察到的最大丰度的m/z的总览; t(UV)在紫外检测器上的保留时间(见图2),MW:分子量,+/:正/负模式,n.d:未检测到。括号中的 m/z 在全扫描中几乎检测不到,但在 SIM 扫描中可检测到,蓝色标注区域表示每种化合物的最佳 MS 检测结果(另请参见图4) # Compound t(UV) [min] MW[Da] m/zAPCI+ m/zAPCI- m/zESI+ m/zESI- 1 2-naphthoic acid 4.33 172.2 n.d. 171 [M-H]- n.d. 171 M-HI 2 2-naphthol 4.56 144.2 (145)TM+H1 143 M-HF n.d. 143 M-H] 3 1-tetralone 4.75 146.2 147 M+HH n.d. 147 M+H]+ n.d. 4 1,4-anthraquinone 5.70 208.2 209 [M+H]+ 208[M (209)M+H]+ n.d. 5 1-hydroxypyrene 6.37 218.3 219 [M+H]+ 217 [M-H] 218 [M+ 217 M-H 6 benzanthrone 6.95 230.3 231 [M+H+ 230 [M] 231 M+H]+ n.d. 2-naphthoic acid 图3.在正(+)和负(-) APCI 和 ESI模式下分析的三种 oxy-PAH 化合物的背景扣除质谱图;标记了丰度最高的离子的m/z;背景光谱从对应峰旁边的空白区域获得。 图4.正(+)和负(-)APCI 和 ESI模式下 1,4-蒽醌的背景扣除质谱图;标记了丰度最高的离子的m/z;2;背景光谱从对应峰旁边的空白区域获得。 图5.在正(+)和负(-)APCI和ESI模式下苯并蒽醌的背景扣除质谱图;标记了丰度最高的离子的m/z;;背背景光谱从对应峰旁边的空白区域获得。 6.0e5- 图6.在正(+)和负(-)APCI和ESI模式下苯并酮酮的背景扣除质谱图;标记了丰度最高的离子的m/z;背景光谱从对应峰旁边的空白区域获 ,得 图7给出了 MS 峰面积和最大丰度的 m/z 的信噪比(S/N)的比较。从图7的C和D部分可以清楚地看出,负离子模式的 ESI 在灵敏度方面比 APCI 更具优势。在ESI负离子模式下检测到的三种化合物的峰面积均高于 APCI负离子模式下的峰面积。但是,这三个组分中只有两个组分的 S/N比较高,而使用 APCI时,在负离子模式下多检测到两个分析物。同一图的A部分和B部分展示了 APCI 在正离子模式下的巨大优势。APCI 中所有检测到的化合物的信号响应与ESI 相似或更高,而信噪比更好。总之,对于这些种类的分析,应首选 APCI 而不是标准 ESI模式。 尽管标准ESI模式对某些负极性分析物具有更高的检测灵敏度,但由于以下原因, APCI模式是当前应用中的首选MS模式: 1、在APCI模式下很容易检测到所有六个 oxy-PAHs,而在ESI模式下有一种化合物几乎无法在S/N_12 的情况下检测到。 2、缺乏酸性氢的分子,不能通过负离子ESI电离,但可以通过负离子 APCI 中的电子捕获来电离。 3、对于大多数分析物来说, APCI 的信噪比更好。 4、在 APCI模下下形成的加合物较少。 ( 参考文献 ) ( 1 . L undstedt, S. et al., F irst intercomparison study on theanalysis of oxygenated polycyclic aromatic hydrocarbons(oxy-PAHs) and nitrogen heterocyclic polycyclic aromaticcompounds (N-PACs) in contaminated soil. Trends Anal.Chem. 2014, 57,83-92. ) ( 2. S ingh, L., Agarwal, T., P olycyclic aromatic hydrocarbons indiet: Concern for public health. Trends Food Sci. Technol. 2018,79,160-170. ) ( 3. Walgraeve, C. et a l., Development o f an analytical method todetermine oxy- P AHs and PAHs in Taxus baccata leaves, Anal.Bioanal. Chem. 2017,409,335-347. ) 4. Cochran, R.E., Smoliakova, I.P., Kubatova, A., Detection ofnitrated and oxygenated polycyclic aromatichydrocarbonsusing atmospheric pressure chemical ionization high-resolution mass spectrometry. Int. J. Mass Spectrom. 2016,397-398,6-17. ( 5. K umar, S.,Negi, S., Maiti, P . , B iological and analyticaltechniques used for detection of polyaromatic hydrocarbons.Environ. Sci. Pollut. Res. 2017,24,25810-25827. ) 6. Grosse,S., Letzel, T., Liquid chromatography/atmosphericpressure ionization mass spectrometry with post-columnliquid mixing for the efficient determination of partially oxidizedpolycyclic aromatic hydrocarbons. J. Chrom. A 2007, 1139,75-83. 150- 100- -5 4e67 2e6o -1e5= 2e6- 1e6 -1e4 1.52.0 4.0 使用Thermo Scientific ISQ EC单四极杆质谱仪和ThermoScientific Vanquish Flex四元UHPLC系统加快方法筛选 Stephan Meding, Katherine Lovejoy, Martin Ru-ehl Thermo Fisher Scientific, Germering, Germa-ny 关键词 单四极杆质谱仪、UHPLC、方法开发、方法 建立、自定义变量 证明了与 UV 检测方法相比,基于质谱检测的方法减少了方法开发时间。 简介 进行 LC 方法开发主要是为了得一一个最优化方法,以提供足够的色谱峰分离和尽可能短的运行时间。分离方法的开发通常很耗时,从而限制了生产率。在确定方法要求之后,通常,寻找方法是 HPLC 方法开发过程中的第一步。对于方法开发而言,需要评估不同的色谱柱、溶剂、流动相添加剂、温度、pH值或梯度,!以确定哪一组参数满足给定的要求。之前,我们已经演示过了如何通过硬件和软件的提升来简化此过程1-3)。目前,最常用的方法是在方法开发过程中根据UV 检测进行峰定性分析,待测物根据其紫外光谱进行识别。所以,可靠的鉴别依靠的是几个先决条件,需要了解分析物的图谱,以确保即使在共洗脱情况下也能鉴别出来。若无法满足这些前提条件,则必须单独测量分析物标准品,这将使得方法开发更加耗时。 若添动质谱检测便可以轻松地克服这一挑战。除 LC为分析物提供的分离外,质谱为分析物鉴别提供了独特信息。对于小分子而言,各分析物可以通过其特有的分子量、同位素模式以及(若需要)碎片模式进行鉴别。所以,所有分析物都可以同时进行分析,甚至在共洗脱情况下也可以选择性地可视化。由于对各峰进行了跟踪,所以可以轻松确定最佳的方法参数。因此,质谱提供了更多选择性,显著减少了成功方法开发所需的运行次数。 质谱检测使用受限的原因是认为方法开发复杂且难以使用。Thermo ScientificTM ISQTM EC单四极杆质谱仪(ISQEC MS) 是专为色谱工作者开发的。全面集成到ThermoScientificTM ChromeleonTM 7.2色谱数据系统(CDS)和Thermo ScientificTM AutoSprayTM 智能方法设置,使LC-MS操作变得简单、直观。 ISQ EC MS可以在全扫和单离子监测(SIM)模式下运行,既可以对检测的化合物进行一段质量范围扫描,也可以对特定化合物进行选择性扫描。它可以以适合快速 UHPLC 应用程序的扫描速率运行,同时提供皮克级检测限。新型正交源的设计即使面对的是复杂基质也能提供高水平的仪器耐受性。 本文介绍了使用 ISQ EC MS 进行方法开发的优势。。一一个包含了18种杀虫剂的样本用以展示基于 MS 的工作流程能以简单直观的方式实现。本文测试了四种不同的色谱柱和两种不同的有机洗脱液。UV 检测也包括在设置中,因为结合 MS 和UV检测有助于后续方法转移到仅基于 UV的设置中。 实验 Thermo ScientificTM QC 杀虫剂混标见表1(各杀虫剂浓度100pg/mL), LC-MS级溶剂见表 2, ThermoScientificTM VanquishTM Flex 四元 UHPLC 系统见表3。该系统使用 Vanquish 自动方法开发组件(P/N6036.2807)配置,该组件包含了一个柱温箱和两个6位7通色谱柱切换阀。流速设置在之前的出版物中进行了描述。长75 cm, 内径为 100 um 的 MP35N毛细管柱(P/N 6042.2390)用于连接 UHPLC 系统和 ISQ EC MS。本文采用四种不同的色谱柱(表4)和两种不同的有机洗脱液对18种杀虫剂混合物进行了分析。 ISQ EC MS 功能已完全集成到 Chromeleon 7.2 CDS 中,以用于系统操作和后续数据分析。这就允许在自定义变量中选择不同的柱子进行简单的序列设置。 色谱条件和 MS 采集设置列于表5和表6中。 表1.从QC杀虫剂混标参数页得到的各分析物概况。 Chemical Molecular Monoisotopic Detected m/z # Analyte CAS Green: [M+H]+ Red: [M-H]- Formula Weight Mass [M] 1 Omethoate 001113-02-6 C,H12NOPS 213.19 213.02 214.03 2 Propamocarb 024579-73-5 CH20NO, 188.27 188.15 189.16 3 Dicrotophos 000141-66-2 CHNO,P 237.19 237.08 238.09 4 Vamidothion 002275-23-2 CHNOPS, 287.34 287.04 288.05 5 Schradan 000152-16-9 CHNO.P, 286.25 286.13 287.14 6 Atrazine 001912-24-9 CHCIN, 215.69 215.09 216.10 7 Cycluron 002163-69-1 C22N0 198.31 198.17 199.18 8 Azoxystrobin 131860-33-8 CHNO, 403.39 403.12 404.13 9 Spirotetramat 203313-25-1 C21H27NO, 373.45 373.19 374.20 10 Sulfotep 003689-24-5 C2095P2S, 322.32 322.02 323.03 11 Pirimiphos-methyl 029232-93-7 C.HoN9PS 305.33 305.10 306.11 12 Trifloxystrobin 141517-21-7 C2H1FN,O 408.37 408.13 409.14 13 Bentazone 025057-89-0 CoH2NO.S 240.28 240.06 239.05 14 2,4-D 000094-75-7 CH.co 221.04 219.97 218.96 15 Bromoxynil 001689-84-5 C,HBr,NO 276.92 274.86 273.85 16 MCPA 000094-74-6 C,H,clo, 200.62 200.02 199.01 17 Hexaflumuron 086479-06-3 CHCFNO 461.14 459.98 458.97 18 Fluazinam 079622-59-6 CHCFNO 465.09 463.95 462.94 表2.溶剂和添加剂。 Reagent Grade Supplier Part Number Acetonitrile OptimaLC-MS Fisher Chemical A955-212 Formic acid OptimaLC-MS Fisher ChemicalM A117-50 Methanol OptimaLC-MS Fisher Chemical A456-212 Water Ultra-Pure, 18.2 MQ at 25°C Thermo ScientificM Barnstead"M GenPure"MxCAD Plus Ultrapure Water Purification System 表 3. Vanquish Flex Quaternary UHPLC 系统模块。 Module PartNumber Vanquish System Base F VF-S01-A Vanquish Quaternary Pump F (with 200 pL mixer) VF-P20-A (6044.5110 and 6044.5026) Vanquish Split Sampler FT VF-A10-A Vanquish Column Compartment H (6-position 7-port Column Switching Valves) VH-C10-A (6036.1570) Vanquish Variable Wavelength Detector F (2.5 pL SST flow cell) VF-D40-A (6074.0360) Stationary Phase Particle Size Dimension Part Number Thermo ScientificAccucoreaQ 2.6 pm 2.1×100 mm 17326-102130 Thermo Scientific" Hypersil GOLDM 1.9 um 2.1×100mm 25002-102130 Thermo ScientificAccucoreRP-MS 2.6 um 2.1×100 mm 17626-102130 Thermo ScientificAccucore Phenyl Hexyl 2.6 pm 2.1×100mm 17326-102130 表 5.UHPLC 条件。 Parameter Value Source Settings A: Water with 0.1%formic acid Mobile Phase B: Acetonitrile with 0.1% formic acid C: Methanol with 0.1% formic acid Time 0-0.5 min: 2% B or C Gradient 0.5-10 min: 2-98% B or C Dwell Time 10-15 min: 2% B or C Flow Rate 0.4 mL/min Column 40°C,forced air mode Temperature Passive pre-heater, 40℃ Injection Volume 0.1pL UV detection 220nm, 100 Hz Source CID Voltage 20V 结果与讨论 在方法开发工作流程中利用 MS 检测将获得更多有关样品信息。分析物通常呈电离状态,大部分要么是质子化阳离子 [M+H]*要么是去质子化阴离子 [M-H]。由于需要一种通用的方法来进行工作流程开发,所以进行全扫模式下MS采集,并进行正/负离子极性切换。极性切换时间仅为 25 ms。除MS数据外,还采集了220 nm波长下的紫外数据。通过从 MS 的全扫数据上提取表1中列出的各自的质荷比(m/z),生成单个分析物对应的峰谱图。随后将这些提取离子色谱图(EICs)用于色谱参数计算上,如保留时间,峰宽或分离度。 使用MS检测,所有杀虫剂都可以使用默认设置清楚地检测到。其中,有十二种是以正离子模式检测,另外六种以负离子检测模式检测(图1)。所有待测物检测到的质 表6.MS条件。 量数与理论值的偏差不超过 0.1 Da(数据未显示)。紫外检测仅显示了十个峰,说明可能有几种化合物共洗脱了或在 220 nm 处为无 UV吸收状态(图1)。通过调整 UV色谱图和EICs, 可以在 UV色谱图中进行峰归属分析。这表明六种杀虫剂(氧化乐果、霜霉威、蚜灭多、八甲磷、环莠隆和治螟磷)在波长为220 nm 的UV检测下未检测到。检测到其他十二种杀虫剂,其中有三个共洗脱(莠去津、2,4-D和溴苯腈)。这充分显示了 MS 数据明显好于UV数据。质谱信息的选择性可对全部分析物直接鉴别以及分辨出所有化合物,即使是共洗脱的情况。虽然 UV数据提供的信息比MS数据少,但在方法开发过程中结合UV和 MS检测方法将对后续开发过程步骤有利。若分析人员想要仅使用 UV 执行更简单的检测方法,则根据方法开发结果还是可以了解其可行性和有关的测试参数。 图1.18种杀虫剂分析物的UV色谱图和 MS 谱图。UV色谱图显示在上图。下方为正离子模式和负离子模式的 MS 谱图。均显示了两种模式下的EICs图。根据表1对分析物进行编号。对未通过 UV 检测到的杀虫剂都采用带框数字进行标记。所提供的数据,使用的是 Accucore aQ色谱柱及使用乙腈作为流动相。 到目前为止,仅将单同位素质量的 m/z 比率用于分析物确认。通过将测得的同位素模式与理论同位素模式进行比较,以提高对分析物鉴别的置信度。使用 Chromeleon 7.2CDS, 可以自动生成EICs 峰尖、峰前或峰尾质谱图,从而可以快速查看分析物的同位素模式。某些杀虫剂所含的元素具有非常独特的同位素模式(表7)。对于所有的杀虫剂而言,其理论模式都可以与所测的杀虫剂完全匹配, 表7.所选的示范性元素的同位素分布。 Element Atomic Weight Relative of Isotopes [u] Abundance[%] 12C 12.00000 98.93 13C 13.00335 1.07 35CI 34.96885 75.78 37C\ 36.96590 24.22 79Br 78.91834 50.69 81Br 80.91629 49.31 进一步证实了它们是正确鉴定(数据未显示)。图2显示了两种包含两个(2,4-D)氯原子或两个(布罗姆林)溴原子的共洗脱分析物。根据所测定的同位素模式,这两种共洗脱分析物可被鉴定出并轻松对它们进行可靠鉴定。 在方法开发中,我们测试了四种色谱柱和两种不同的有机洗脱液。从色谱图上可以清晰看出不同色谱柱之间选择性的差异及有机洗脱液对选择性的影响(图3)。这与报告中描述的这些固定相的化学性质一致4。通常对所有色谱柱而言,甲醇提供的峰分离度优于乙腈,对于某些分析物而言,有机洗脱溶剂变化时,洗脱方式将相反,如用于嘧菌酯(#8)和螺虫乙酯(#9)(图3,蓝色框)。几个峰洗脱相近,甚至重叠,如如去津(#6),环莠隆(#7),灭草松(#13),2,4-D(#14),溴苯腈(#15)和MCPA(#16)(图3,红色框)。这些分析物不能仅通过紫外检测分离出来。通过 MS检测,可以对所有分析物进行检测并分别对他们的分离度进行准准计算(表8)。 图2.根据共洗脱分析物2,4-D和溴苯腈的同位素模式进行可靠的分析物鉴定。EIC 显示在左侧,然后是质谱图,放大的分析物测试的同位素模式图以及理论同位素分布图显示在右侧。 在实际方法开发实验中,需要预先定义色谱需求。如,莠去津(#6)和2,4-D(#14)的分离度至少达到1.5,那么 Hypersil GOLD 和 Accucore Phenyl Hexyl 作为固定相结合有机溶剂乙腈或 Hypersil GOLD 和 AccucoreRP-MS 作为固定相结合有机溶剂甲醇一起使用比较合适(表8)。若2,4-D(#14)和 MCPA(#16)两者的分离度至少达到1.5,则所有的测试色谱柱与甲醇结合使用都很合适(表8)。注意:为了保持应用案例的简明,影响固定相的选择性参数,如柱温或 pH值并未进行测试。 综上所述,基于 MS 的方法开发可对色谱分离参数进行快速直观的评估,如分离度。因其利用了质谱检测的选择性进行可靠地识别分析物,即使处于共洗脱情况下也能完全解析。这简化并加速了方法开发过程。不再需要进行单个样品分析,而是可以使用包含所有分析物的标液。 圆网一田可Accucore PH Accucore RP-MS Hypersil Gold可浒可#义呐瞬心可泊。氏米画应六3#斗6亦m一6网义网3知C八C氏米。斗浒眾游。。 Negative Positive UV Negative Positive UV Negative Positive UV Negative Positive UVMode Mode Signal Mode Mode Signal Mode Mode Signal Mode Mode Signal 言 高 8 5 -N N 心 O 二5 c co 00 00 DO 00 一 二 寸 二 . oo Negative Positive UV Negative Positive UV Negative Positive UV Mode Mode Signal Mode Mode Signal Mode Mode Signal g 一 8 己 u L 一5 .5 N N 叮 云 cn DO 寸 0.10 Acetonitrile Methanol -5.64 -0.88 -0.20 1.44 -2.84 -0.15 MCPA -3.29 -3.18 5.90 -3.27 1.77 Atrazine -1.28 1.67 -2.63 0.05 -1.05 -3.10 9.00 0.14 4.80 -1.94 1.13 1.43 0.41 10.12 -12.35 -4.72 -1.64 -4.21 -5.16 -9.53 2.74 -0.85 5.01 -2.27 -3.21 -7.38 0.82 1.66 -1.21 0.16 -1.81 -2.94 6.73 -2.06 9.55 1.06 0.87 -2.08 -0.71 -2.73 -2.93 -1.60 -3.60 -9.16 1.45 -0.57 -2.10 -6.12 -0.80 -0.90 -1.66-1.75 -0.72 -2.47-2.56 -1.72 -3.38 4.23 0.49 3.90 -1.83 -0.81 7.85 3.97 -0.89 0.00 -3.82 0.80 -0.81 -2.44 -1.54 3.47 -6.47 使用 ISQ EC 单四极杆质谱仪和 Vanquish Flex 四元UHPLC 系统进行基于质谱的方法开发比基于 UV 的传统方法有以下几方面的优势: 1、直观的分析物识别和跟踪降低了可能忽略存在共洗脱分析物或在不同方法开发运行上可能存在的错误峰分配风险。 2、大大减少了所有分析物分析的方法开发时间。 3、 UV和 MS检测校准功能有助于将方法转移至仅UV的方法中。 ( 参 考 文献 ) ( 1 . Thermo Scientific Application Note AN 1122: UHPLC MethodDevelopment for S imultaneous Determination of AntihypertensiveCombination Agents, 2 0 16. https://tools.thermofisher.com/content/sfs/brochures/AN-1 1 22-LC-Method-Development-Antihypertensive-Combination-Agents-AN71573-EN.pdf ) ( 2. Thermo Scientific Technica l Not e TN 161: Fast an d Easy HPLCMethod Development: Application of an Automated Method ScoutingSystem, 2016.https://tools.thermofisher.com/content/sfs/brochures/TN-161-HPLC-Method-Scouting-TN71514-EN.pdf ) ( 3. Thermo Scientific Technical Note T N 185: A UHP L C Method Development System for Efficient Scouting of ChromatographicElution Parameters, 2016. https://tools.thermofisher.com/content/sfs/brochures/TN-185-HPLC-Chromatographic-Scouting-TN72177-EN. pdf ) 4. Thermo Scientific Technical Note TN20543: Selectivity Choices inReversed-Phase Fast LC, 2013. https://tools.thermofisher.com/content/sfs/brochures/TN20543-Selectivity-Choices-Reversed-Phase-Fast_LC-EN.pdf 应用文摘 一生物制药 采用高效液相色谱结合紫外和单四极杆质谱检测技术分析LL-37合成肽中的杂质 Sylvia Grosse, Martin Samonig, Mauro De Pra,Frank Steiner; Thermo Fisher Scientific, Ger-mering, Germany 关键词 杂质分析、合成肽、单四极质谱仪 ISQ EM 、高效液相色谱、Vanquish Flex Binary UHPLC、LL-37、质控、LC-MS、UHPLC 目的 借助 UV检测来确定杂质水平和质谱检测对活性药物成分(activepharmaceutical ingredient, API) 及其他产品有关物质进行鉴定,利用一种快速方法对合成肽杂质进行分析。 应用优势 1.使用结合紫外和单四极杆质谱仪快速检测合成肽中的杂质。 2. Thermo ScientificM单四普质谱仪 ISQMEM 的质量数范围高达 m/z2000,可检测低电荷肽类并提高鉴定可信度。 简介 为保证合成肽高质量生产,则需要简单、快速和可靠的分析方法来帮助确定所生产肽的纯度。通常采用配有紫外检测器(UV)的高效液相色谱(HPLC)进行分析。但是,因为在生产过程中随主要成分一起形成的这些杂质的浓度很低,且往往结构非常相似,所以有时对生产过程及产品相关的杂质的分离和检测是很有挑战的。此外,与产品相关的杂质通常都是未知的,必须加以鉴定,这就导致需要更先进的分析技术,如质谱(MS)。合成肽主要有两种不同的合成方法,分别是固相多肽合成法(SPPS)或液相多肽合成法(SPS)。现今首选固相多肽合成法(SPPS)进行合成,因该过程可以通过完全自动化来实现。 简单来说,在 SPPS中,一个氨基酸与另一个氨基酸缩合,之间通过冲洗,然后重复该过程,直到完成所需肽合成为止“。了解相关的化学物质,包括树脂、氨基酸以及用于缩合和去保护的试剂,这有助于评估生产过程中产生的杂质。 本文对人源抗菌肽 LL-37 进行了肽杂质分析和基于质量的化合物确认,证明了该化合物因其抗菌、抗真菌、抗病毒、伤口愈合、抗癌和免疫调 节活性作用而具有很高的医学价值2。序列包括了37个氨基酸,肽质量数约为4500 Da。通过紫外检测确定杂质含量,同时借助质谱对其鉴定。新型的单四极杆质谱仪ISQ EM 拓宽了质量数范围,使其能检测所选肽的低电荷态,并提升了鉴定可信度。 实验耗材 ·去离子水,18.2 MQ·cm 的电阻率或更高 (P/N N/A) ( ·Fisher ScientificTM 乙腈, OptimaTM LC/MS级(P/N 10001334) ) ( · Fisher ScientificTM E 甲酸, OptimaTM L C/MS 级 (P/N 10596814) ) ( · Thermo Scientific T M Acclaim T M RSLC 120 C18 柱50× 2.1 mm, 2.2 pm (P/N 068981) ) ( 合成肽 LL-37(活性药物成分; API)和两个相关片段LL-37 RKS 和 LL-37 SKE (购于知名供应商)。 ) 标准品制备 表1为本研究所用肽氨基酸序列的概述。用流动相A(水+0.1%甲酸)制备1mg/mL 的肽溶液。将肽片段 LL-37RKS(片段1)和 LL-37 SKE(片段2)分别以 150 pg/mL和 50 pg/mL 的浓度加标到 500 pg/mL LL-37 (API)的肽溶液中以模拟包含产品相关杂质的样品。 ( 采用 Thermo ScientificTM VanquishTM F lex Binary UHPLC 系统,并配有单四极杆的 ISQ EM 质谱仪进行分析。 ) ( ·Thermo ScientificTM VanquishTM S ystem Base VanquishHorizon/Flex (P/N VH-S01-A-02) ) ( · Thermo ScientificTM VanquishTM Binary Pump F (P/N VF-P10-A-01) ) ( ·Thermo ScientificTM VanquishTM Split Sampler FT (P / N VF-A10-A-02) ) ( · Thermo ScientificTM VanquishTM Column Compartment H (P/N VH-C10-A-02) ) ( ·Thermo ScientificTM VanquishTM Variable WavelengthDetector F (P/N VF-D40-A) ) ( ·Flow Cell Semi-Micro, 2.5 pL, 7 mm light path (SST) (P/ N6077.0360) ) ( · ISQ EM Mass Spectrometer (P/N ISQEM - ESI) ) 表1.多肽氨基酸序列和理论分子量 Theoretical Theoretical Theoretical mostabundantisotope mass[Da] Compound Amino acid sequence average monoisotopic mass mass [Da] [Da] LL-37 (API) LLGDFFRKSKEKIGKEFKRIVQRIKDFLRNLVPRTES 4493.299 4490.565 4492.582 LL-37 RKS RKSKEKIGKEFKRIVQRIKDFLRNLVPRTES 3800.488 3798.211 3799.225 (fragment 1) LL-37 SKE SKEKIGKEFKRIVQRIKDFLR 2619.130 2617.544 2618.558 (fragment 2) 液相色谱条件 Column Acclaim RSLC 120 C18. 50×2.1 mm, 2.2 pm Mobile phase A: Water +0.1% formic acid B: Acetonitrile + 0.1% formic acid Flow rate 0.5 mL/min Gradient Time (min) %B 0 2 Mixer volume 10 + 25 pL Column 50°℃ temperature (forced air mode, fan speed 5) Autosampler 4°C temperature UV wavelength 214 nm UV data collection 10 Hz rate UV response time 0.5 s 质谱条件 MS source parameters Sheath gas pressure 49.9 psig Aux gas pressure 5.7 psig Sweep gas pressure 0.5 psig Vaporizer temperature 282°C Ion transfer tube temperature 300°℃ Source voltage 3000V MS method parameters Method type Full Scan Ion polarity Positive Mass range m/z 500-2000 Dwell time 0.2 s Source CID voltage 10V 数据处理 采用 Thermo ScientificTM ChromeleonTM 7.2.9色谱数据系统 (CDS) 进行数据采集和处理。 结果和讨论 在本项研究中,紫外数据用于确定合成肽样品中的杂质含量,而MS数据则主要用于合成肽样品中产品有关物质的鉴定。根据人用药品注册技术要求国际协调会(ICH)公布的指南对有关物质的相对峰面积(Rel. Area)进行计算和评估。所以,对UV、总离子流(TIC)和提取离子色谱图(XIC)获得的相对峰面积(Rel. Area) 都进行了比较。该方法还可筛查未知杂质,并增加了结果的可信度。 图1显示了肽LL-37的UV色谱图和扫描范围 m/z 500-2000对应的TIC色谱图。肽LL-37可在保留时间(RT)1.7分钟处检测到。仅从 UV色谱图中未观察到其他峰,表明样品中并没有主要杂质存在。但是,仅凭紫外色谱图并不能排除共洗脱杂质可能。使用 MS 质谱数据的主要优势在于可以通过运行全扫模式来确定峰纯度。但是,获得的质谱图显示没有明显的其他质谱峰来说明API与其他杂质共洗脱(图4)。 Chromeleon CDS 提供了使用序列列表中自定义列的功能,通过输入肽序列或化学式来计算肽和其他化学组分的理论质量数。它还允许计算不同电荷态和不同质量加合(图2)。这是一个非常有用的工具,用于鉴定肽质谱和其它生物分子质谱的多电荷状态。 图1. a)在波长为214nm 处的紫外色谱图和 b) 将多肽 LL-37 放大到基线的色谱图 # TIC Name *API_peptide_sequence *Fragment_1_peptide_sequence #Fragment_1_Calculatedmost abundant Mass [M] IDal #Fragment_2_Calculatedmost abundant Mass [M][Da] #Fragment_2_Calculatedmost abundant Mass [M+4H][m/Z] abundant Mass [M][Da] most abundantMass [M+4H] [m/z] most abundant Mass[M+4H][m/Z] Fragment_2_peptide_sequence 1 None Blank n.a. n.a n.a. n.a. n.a. n.a. 2 None API+fragments LLGDFFRKSKEKIGKEFKRIV.. 4492.58213 1124.15281 RKSKEKIGKEFKRIVQRIKDF. 3799.22542 950.81363 SKEKIGKEFKRIVQRIKDFLR 2618.55776 655.64672 3None API+fragments LLGDFFRKSKEKIGKEFKRIV.. 4492.58213 112415281 RKSKEKIGKEFKRIVQRIKDF. 3799.22542 950.81363 SKEKIGKEFKRIVQRIKDFLR 2618.55776 655.64672 4None API+fragments LLGDFFRKSKEKIGKEFKRIV. 4492.58213 1124.15281 RKSKEKIGKEFKRIVQRIKDF. 3799.22542 950.81363 SKEKIGKEFKRIVQRIKDFLR 2618.55776 655.64672 5None Blank n.a. En.a. n.a. n.a. n.a. n.a. 图2.添加自定义列的 Chromeleon 进样列表截图,用于目标组分的理论质量数计算(淡蓝色: API;浅绿色:片段1;亮红色:片段2) 为模拟产品杂质分析,将两个不同的肽段分别加入到 LL-37肽溶液中,并在相同条件下测试。用一个2分钟的短梯度法即可实现基线分离,如图3所示。 由于与 ISQ EM 质谱仪连接,可以通过比较理论质量和实测到的质量将峰分配给相应的肽。若没有其他实验,仅凭紫外信号是不可能实现峰值分配的。 Retention time (min) 图3模拟肽杂质分析波长为214nm处的紫外色谱图 扩展了质量数范围的 ISQ EM 质谱仪可用于研究肽在2至8的多电荷态(图4)检测。低分辨率质谱仪,如四极杆在高电荷态下不能分辨出同位素质量,因而,使用平均质量代替在高分辨质谱中很常见的单同位素质量。 表2总结了 LL-37肽及其两个片段的所有电荷态下 m/z 的测量值和理论值(平均和最大丰值同位素)。理论值和实测平均值之间的质量偏差(△m/z)在所有电荷态下均≤0.4。使用方程式1计算出各电荷态下的不带电荷平均质量,并将其平均,得到完整的去卷积平均质量。所有肽的完整分子质量偏差均≤0.5 Da。 方程1.从 m/z 值和相应的电荷状态计算出不带电质量 图4获得API和两个碎片的质谱图 表2比较图4中各肽谱所有配有电荷态的理论质量和测量质量以及对应的绝对质量量差 LL-37 (API) Measured Measured most Theoretical Calculated Delta Charge state abundant mass Mass deviation to theoretical mass [Da] LL-37 RKS (Fragment 1) 2618.4 [M] average mass 2618.1 3800.5 average mass [M+1H]1+ 一 [m/z] 3801.5 [m/z] [Da] [M+2H]2+ — 1901.3 — [M+3H]3+ 1267.5 1268.3 1267.8 0.3 3799.5 [M+4H]4+ 950.9 950.9 951.1 0.2 3799.6 [M+5H]5+ 761.2 761.2 761.1 -0.1 3801.0 [M+6H]6+ 634.5 634.5 634.4 -0.1 3801.0 [M+7H]+ 544.1 544.1 543.9 -0.2 3801.6 [M+8H]8+ 750.0 750.0 476.1 -0.1 4494.0 [M+7H]7+ 643.0 643.0 642.9 -0.1 4493.9 [M+8H]8+ 562.8 562.8 562.7 -0.1 4494.3 4493.3 Deconvoluted average mass (n=4) [Da] 2618.6 通常,UV 信号响应被用于杂质分析中的相对定量,因MS 信号高度依赖于各分析物的离子化效率,且还必须考虑离子抑制,这可能导致分析物浓度高估或低估。尽管如此,质谱因其高灵敏度, MS数据被常用于较低浓度水平的定量。表3显示了通过 UV、TIC 和 XIC图比较获得的相对峰面积。结果的变化清晰地说明了产品有关物质的定量的挑战性。UV信号响应是基于214nm处的强肽键吸收。但是,由于这三种多肽序列的差异较大,其紫外响应并不一致。因此,从相对峰面积计算而得的结果与理论计算值有所不同,片段1为30%,片段2为10%,只能作粗略估计。为利用UV进行准确定量,应对各单独分析物进行外标校准,或者需要确定响应因子。在质谱定量情况下,由于质谱响应不一致,并且可能会发生离子抑制,需要用同位素标记标物进行准确定量。 1、由于可以得到有关峰纯度和基于化合物确认质量等分析物的补充信息,所以紫外结合质谱检测的方法更有助于肽杂质分析。 2、质量数范围扩大到 m/z 2000, 使其可以检测低电荷物质,并可进行中型生物分子的完整电荷态检测分析。 3、快速梯度法可在2分钟内完成 LL-37 肽杂质分析。 ( 1. Wu, L. C .; Chen, F . ; Lee, S.L . ; Raw, A . ; Y u ,L.X.Bu i lding p arity between brand and generic p eptide products: R egulatory and s c ientific considerations for qualityof synthetic peptides. I n ternational Journal ofPharmaceutics 2017,518,320-334. ) ( 2.Chen, Y.; Yang, S .; Ho, E .A. D evelopment of anAnalytical Method f or the Rapid Quantitationof Peptides U sed i n Microbicide Formulations.Chromatographia 2014,77(23-24), 1713-1720. ) 表 3 LL-37 SKE (片段2) m/z 525.0, LL-37 RKS(片段1) m/z 634.5 和LL-37 (API) m/z 643.0处模拟杂质通过比较 UV、TIC 和XIC 图获得的相对峰面积、保留时间和分辨率的数据 Compound RT Resolution UV trace TIC trace XIC trace [min] Rel. Area[%] Rel. Area[%] Rel.Area[%] LL-37 SKE 0.9 3.54 4.4 4.3 5.9 fragment 2) LL-37 RKS 1.2 4.16 16.5 21.9 25.1 fragment 1) LL-37 (API) 1.7 100 100 100 质量范围扩大的单四极杆质谱仪应用于寡核苷酸表征以进行质量控制和提高生产效率 Katherine Lovejoy, Sylvia Grosse, Mauro de Pra,Martin Samonig, Frank Steiner; Thermo FisherScientific, Germering, Germany 关键词 单四极质谱仪、ISQEM、UHPLC、ssDNA、寡核苷酸、质量控制、扩大质量范围、LC-MS、高效液相色谱法、Vanquish Flex 目的 通过将 Thermo ScientificTM ISQTM EM 单四极杆质谱仪结合到基于UV的质量控制方法中,可以提高分析长度在29至40个碱基对之间的合成寡核苷酸的分析效率。 应用优势 1、扩展了 UV 质量控制方法到质谱,提供了质量确认和杂质鉴定。 2、常用的 DNA 离子对试剂的使用有助于现有 QC方法的转移。 简介 寡核苷酸合成的质量控制(QC)要求需要对寡核苷酸进行可靠的质量确认,并使用快速有效的方法对产量和杂质水平进行粗略定量。由于在波长260 nm处有很强的 DNA吸收,所以可轻松地通过 UV检测进行定量。需要使用质谱仪对杂质进行粗略估算,因为在快速QC方法中, N-1序列通常不能从色谱上与全序列N分离出来。质谱仪还可进行明确的低聚物鉴定。质谱(MS)通常被认为是复杂的,在常规质量控制应用中难以使用。但 ISQ EM 单四极杆质谱仪是专为色谱工作者开发的。其功能完全集成到 Thermo Scientific TMChromeleonTM 7.2数谱数据系统(CDS)中, 加上 ThermoScientificTM AutoSpray 智能方法设置,使LC-MS 操作和数据分析变得简单而直观。扩大了质量范围(m/z 10-2000) 的 ISQ EM 质谱仪, 使色谱工作者可收集到多个电荷态下的数据。 正交源的设计可提供高水平的仪器耐受性,即使在极具挑战性的离子对色谱条件下也是如此,通常用于确保 DNA 低聚物的保留。本应用文摘描述了寡核苷酸的质量控制,包括通过质谱的质量确认和杂质水平评估,以及紫外定量。 寡核苷酸(表1)由位于 California, Pleasanton 的Thermo Fisher Scientific 遗传科学部门提供。使用 FisherChemicalTMOptimaTM LC/MS 级(P/N A454)甲醇。从Sigma-Aldrich购买离子对试剂1,1,1,3,3,3-六氟-2-丙醇(HFIP, P/N 105228)和三乙胺(TEA, P/N T0886)。使用由 Thermo ScientificTMBarnsteadTMGenPurexCADTMPlus 超纯水净化系统生产的超纯水。 仪器 采用配有 ISQ EM 单四极杆质谱仪的 ThermoScientificTMVanquishTM Flex UHPLC 系统进行分析。 ( ·Thermo ScientificTM VanquishTM Binary Pump F (P/NVF- P10-A) ) ·35 uL mixer (P/N 6044.3870) ( ·Thermo ScientificTM VanquishTM Split Sampler FT (P/N VF-A10-A) ) ( · Thermo ScientificTM VanquishT M Column Compartment H (P/N VH-C10-A) ) ( · Thermo ScientificTM VanquishTM Variable WavelengthDetector F (P/NVF-D40-A) ) ( ·2.5uL standard stainless steel flow cell(P/N 6077.0360) ) ·ISQ EM Mass Spectrometer (P/N ISQEM-ESI) 色谱过程和检测参数 反相离子对色谱法是使用专为寡核苷酸分析而设计的独特的聚(二乙烯基苯)色谱柱进行的。通常采用离子对流动相洗脱低聚物以进行质谱分析,尤其是 TEA/HFIP。在 10mm色谱柱(表2)上使用未分离N和N-1低聚物简短质控方法。优化CID电压,令到-9电荷态下最大丰度质量相关的峰面积最大。仪器在实验开始前使用Chromeleon CDS 中的操作验证(OQ)向导进行调谐。 洗脱液A的制备 在250mL量筒中将 3.36 g纯 HFIP 添加到 90 mL水中来制备洗脱液A。并在边搅拌边添加下加入112 uL 的纯TEA, 然后加水至100 mL。将洗脱液超声处理 15 min,然后静置至用前达到室温。 样品的制备 将冻干、脱盐、去三苯甲基化的样品在不含脱氧核糖核酸酶的水中重构至100 uM的浓度,并储存在-20℃下。用移液枪和超纯水将其稀释至文中所述的浓度后进行分析。 校正样的制备 使用移液枪和超纯水配制50、20、10、5、2、1、0.5、0.2、0.1和0.05 pM 来制备37个碱基样品。 色谱数据系统 ISQ EM 质谱仪功能完全集成到 Chromeleon 7.2.9 CDS中,以用于系统操作和后续数据分析。 表1.低聚物样品分析。 Length Sequence Average Mass (Da) 40 CTCTCTGACACAATTAAGGGATAAAATCTCTGACGGAATG 12,306.1 37 CAGGAAACAGCTATGACCCGCGCTCACCTCGCCTCTG 11,234.9 31 ATGATATTATGATTAGGAGCCGCGCAGGGAG 9659.6 29 TGAAGGAITGCACTGAAAGGCAGGCTAAT 9024.9 Parameter Setting Column Thermo ScientificDNAPac"RP 2.1×10 mm, 4 um(P/N 088925) Eluents A: 200 mM HFIP, 8.0 mM TEA, pH 8.0 B:Methanol Injection volume 1pL Analytical gradient 0.5 mL/min flow rate Time (min) %B 0 15 0.5 15 1 60 1.3 60 1.4 15 6 15 Column temperature 50℃ forced air mode, 50°C active preheater Autosampler temperature 4°C UV settings =260 nm, 10 Hz data collection rate, 0.5 s response time MS settings HESI source type, easy ESI source settings for 0.5 mL/min flow rate, specifically: Sweep gas pressure 0.5 psig Sheath gas pressure 49.9 psig Aux gas pressure 5.7 psig Vaporizer temperature 282°C Ion transfer tube temperature 300°℃ MS Full Scan Time 0-6 min Mass range m/z 600-2000 Dwell time 0.2 s Polarity Negative Source CID voltage 15 V Spectrum type Profile 结果和讨论 ISQ EM 质谱仪的质量范围扩展到 m/z 2000, 对具有多个电荷态的长链低聚物分析适用。该功能已应用到质量控制工作流程中,分别注入长度为 29-40的寡核苷酸,并经过梯度洗脱,,以以便每个寡聚物都能与其他所有寡核苷酸一样以相同的保留时间快速洗脱。紫外检测器用于定量,质谱仪用于质量确认和杂质鉴定。在质谱检测中通常使用离子对试剂 TEA 和 HFIP1对寡核苷酸进行检测。虽然这些试剂会相对长久存留,但正交源的设计即使在经过100多次注射后也还不需要清洗。 常出色的质量精度。观察到的质量均在 ISQ EM 质谱仪的质量精度指标范围内≤±0.1 Da。结果的重复性极好,相对标准偏差(RSD)为0.02%或更小。 所有低聚物均观察到多种电荷态。为了对 m/z 600-2000白所有电荷态进行质量确认,重复进样四次 50 pmol的37个碱基寡核苷酸。37个碱基的电荷态如表4所示。用各寡核苷酸的平均分子量来计算各电荷态的预期质量。除-13电荷态外,观察到的质量都在质量精度范围内。观测值的重复性极好, RSD 为 0.02%或更小(除-14电荷态的 RSD为0.07%以外)。较高电荷态下相关的仪器误差更高,进一步说明了电荷态13、14和15的结果稍差的原因。 图1.值为0.05、0.1、0.2、0.5、1、2、5、10、20、50 uM 上的UV校准曲线确定系数为 0.9996,y轴截距0.099,斜率0.539 采用平均质量进行质量确认。单四极杆质谱仪是一种低分辨率质谱仪,在我们考虑的电荷态下,许多同位素的峰会聚到平均质量上。 质量确认 重复进样三次5 pmol 的29个碱基、31个碱基、37个碱基和40个碱基寡聚物,以通过质量确认进行鉴定。表3中显示了这些低聚物各自-9电荷态下的质量确认,表明在柱上质量相对较低的各长度的寡核苷酸分析上具有非 表3.使用相对高丰度的[M-9H]9-电荷态对29个碱基、31个碱基、37个碱基和40个碱基进行质量确认 Length Average Average Found Found Found Mean Mass Std. Dev. RSD Mass Mass. Mass, Mass, Mass, (n=3) Accuracy (n=3) (Da) [M-9H19- Trial 1. Trial 2, Trial 3. Observed [M-9H19- [M-9H19- [M-9H19- 40 12312.0 1367.0 1367.1 1366.9 1366.9 1367.0 0.0 0.12 0.01% 37 11240.3 1247.9 1247.9 1247.8 1247.8 1247.8 -0.1 0.06 0.00% 31 9664.3 1072.8 1072.9 1073.0 1072.8 1072.9 0.1 0.10 0.01% 29 9024.9 1001.8 1001.6 1001.7 1002.0 1001.8 0.0 0.21 0.02% 表4.计算并发现37个碱基的电荷态(TIC,扫描m/z 600-2000, CID 15,驻留时间0.2s,负离子模式,柱上50 pmol)。实测值和标准偏差(标准偏差)和RSD 来自四次进样的平均值 6 7 8 9 10 11 12 13 14 15 Expected 1872.4 1604.8 1404.0 1247.9 1123.0 1020.9 935.7 863.6 801.9 748.4 Found 1872.4 1604.8 1403.8 1247.9 1122.9 1020.7 935.7 864.0 802.1 748.6 Mass Accuracy -0.0 -0.0 -0.2 -0.0 -0.1 -0.2 -0.0 +0.4 +0.2 +0.2 Std. Dev. (n=4) 0.16 0.20 0.15 0.10 0.15 0.10 0.10 0.21 0.56 0.17 RSD 0.01% 0.01% 0.01% 0.01% 0.01% 0.01% 0.01% 0.02% 0.07% 0.02% 由于杂质的因素,如中止序列(N-1)、脱嘌呤产物、2-氰乙基修饰和异丁酰基修饰在快速质控方法中通常不能通过色谱从完整序列(N)中分离出来,需要使用质谱仪进行杂质鉴定及其水平的粗略估计。基于峰面积、加合物大致总量及-9电荷态下的相对所有加合物面积总和的杂质识别如表5所示。潜在的杂质和加合物使用同行评审文献来源进行鉴别1.2)。低含量(<10%)的杂质鉴定包含了中止序列N-1。痕量(<5%)级杂质鉴定包括了2- 氰基乙基杂质、异丁酰基杂质和氯醛N-碱基杂质。为确认这些痕量级杂质的存在,提取离子色谱图(XIC)检测很有帮助。-9电荷态下的37碱基和其他杂质的 XIC如图2所示。在1.05分钟时明显出现了峰,包括与主峰质量相对应的[M-9H]9,N1中止序列峰,单钾盐峰[M+K+-10H]9,脱嘌呤峰和2-氰基乙基杂质峰。·一些峰不太明显,包括与质量峰对应的三氯乙醛杂质和异丁酰基杂质。这些杂质的存在需要由高分辨率质谱证实。 Time (min) Time (min) Time (min) 图2.使用负离子模式进行全扫, [M-9H]9电荷态下37个碱基的 XIC 和鉴定出的其他杂质的 XIC (m/z 600-2000,停留时间为 0.2 s, CID 为15,使用高斯函数进行平滑并在 Chromeleon CDS 中设置11个点)。A)[M-9H]°, m/z 1247.9。B)-9电荷态下中止序列, N-1, m/z 1211.3。C)[M+K+-10H]9, m/z 1252.2。D)-9电荷态脱嘌呤导致失去一个腺嘌呤碱, m/z 1232.9。E)-9电荷态的2-氰基乙基杂质, m/z 1253.5。F)-9电荷态三氯乙醛杂质, m/z 1263.8。G)-9电荷态的异丁酰基杂质, m/z 1255.4。 表5.基于针对37个碱基寡核苷酸-9电荷态而鉴定的所有加合物的峰面积之和,进行杂质鉴定及水平的粗略估计 脱嘌呤,即腺嘌呤或鸟嘌呤碱基的损失源于酸水解,而酸水解通过用于质谱分析过程中通过加热或者源内裂解去除三苯甲基保护基团。脱嘌呤占所有加合物峰面积总和的8.5%。腺嘌呤丢失的 XIC 如图 2D 所示。通过对[M-xH]*的最大丰度电荷态的峰面积最大化来优化此应用的CID电压,但另一种优化方式是选择一个生成最小脱嘌呤的 CID 电压。 峰面积较大的原因归功于37个碱基与溶剂添加剂 HFIP加合。加合 HFIP与非加和37个碱基的比率对 CID 电压无响应。发现了极少量的甲醇和 TEA 加合物。钾盐及其HFIP加合物占总峰面积的14.4%,而钠盐仅占总峰面积的2.0%。钾和钠离子的可能来源包括了洗脱液、洗脱瓶、样品瓶、、样品缓冲液,或寡核苷酸生产过程。 色谱人员经常根据泵压的变化曲线来确定进样之间系统平衡所需的时间。一旦泵压力信号已恢复到初始值时,开始下一次进样。但是当使用离子配对试剂时,最短平衡时间延长三倍可大大提升峰面积重现性。如图3所示,全扫模式下平衡时间从1分钟增加到4.5分钟时,六次进样1uL(5uM37个碱基样品)的峰面积的 RSD 从15.4%改善善8.1%。 质谱仪在现有的UV工作流程中可提供质量确认和杂质鉴定信息。质量范围扩大的质谱仪 ISQ EM 允许使用8种电荷态对37个碱基低聚物进行精确的质量确认。即使通过进样100次三乙胺和六氟-2-丙醇的传统离子对反相液相色谱流动相后,由于正交源的设计并不需要对仪器进行清洁。与仅根据泵压力曲线的还原情况进行调整的较短平衡相相比,略微延长进样之间的平衡相能大幅提升峰面积的重现性。基于 ISQ EM MS 工作流程相较于一个基于UV的简单质控工作流程来说,提升了生产率,因其通过高效且易于使用的界面进行 MS 控制和数据处理,在相同的时间内提供了更多的附加信息。 ( 1.Apffel, A.; Chakel, J .A.; Fischer, S .; L i chtenwalter, K .;Hancock, W.S. Analysis of oligonucleotides by HPLC-electrospray ionization mass spectrometry. Anal. Chem.1997,69, 1 320-1325. ) ( 2.Nikcevic, I .; Wyrzykiewicz, T .K.; L i mbach, P . A.Detecting low-level synthesis impurities i n modifiedphosphorothioate oligonucleotides using liquidchromatography—high resolution mass spectrometry.Int. J. Mass Spectrom.2011,304,98-104. ) 应用文摘 一制药 利用赛默飞ISQ EC单四极杆质谱实现可靠的杂质检测 作者 Stephan Meding, Katherine Lovejoy, MartinRuehl Thermo Fisher Scientific, Germering,Germanv 关键词 单四极杆质谱仪、杂质分析、峰纯度、定量 LC MS、富马酸替诺福韦酯 目的 使用 Thermo ScientificTM 单四极杆质谱仪 ISQTM ECTM 进行杂质定量分析,实验证明了其在药物开发和质量控制方面的优势。 简介 化学品生产过程的杂质分析对于小分子药物开发或质量控制是至关重要。根据国际协调人类使用药物注册的技术规定会议(ICH)的指南,首先必须对高于某一阈值的所有副产物进行表征,然后进行监测。鉴定合格阈值取决于每天的量,范围在0.1%一1.0%之间“。分析通常由一系列不同的检测方法来实现的。在质量控制方面,基于 UV的检测仍然是标准,但是MS检测由于其明显的优势而受到认可。除了较低的检测限外,它还可以基于其质量数进行质谱分析,并根据质谱图进行简单的峰纯度分析。另一方面,基于UV的识别通常是模棱两可可,因为其对分析物的识别是根据保留时间和UV吸收来推断的。 现代单四极质谱仪,如 ISQ EC 单四极质谱仪(ISQ ECMS), 是为常规应用而设计的可靠产品。 ISQ EC MS 可以在全扫或单离子监测(SIM)模式下运行,以扫描所有可检测分析物的质量范围或着眼于特定化合物。它可以适合快速 UHPLC 应用的扫描速率运行,同时提供皮克级检测限。新型的正交离子源设计即使在具有挑战性的基质条件下也可提供高水平的仪器稳定性。完全集成到 ThermoScientificTMChromeleonTM 7.2色谱数据系统(CDS) 和 ThermoScientificTMAutoSpray TM 智能方法设置,使LC-MS操作和数据分析变得简单直观。 本文以富马酸替诺福韦酯为例,说明了基于 ISQ EC MS 的杂质分析方法的优势。该药物通常用在 HIV治疗上,与其他的抗逆转录病毒药物联用。与恩曲他滨联用时,吉利德将其作为 TruvadaQ 上市销售。美国药典(USP)描述了几种杂质②。选择了其中两种,腺嘌呤和替诺福韦用于展示基于 ISQ EC MS 的杂质分析流程。两者在结构上均与替诺福韦酯(图1)相关。每一种杂质含量上限相当于替诺福韦酯含量的0.15%。在先前发表的论文中开发了具有挑战性的色谱分离方法。 图1.替诺福韦酯、恩曲他滨、腺嘌呤和替诺福韦的化学结构。前两者肓 Truvada 的活性药物成分(APls)结构,后两者是相关替诺福韦酯杂质的结构 实验 使用 Fisher ScientificTM ACROS OrganicsTM。其他样品试剂均按USP 参考标准采购。 表1.分析物的概述。替诺福韦酯与富马酸盐1:1 制备。色色谱分析过程中,检测到分离的复合物和替诺福韦酯。因此,此处和下列只提及替诺福韦酯 Analyte CAS Chemical Molecular Monoisotopic Mass [M] [M+H]+ Formula Weight Tenofovir 201341-05-1 CH3oNOP 519.44 519.17 520.18 disoproxil (fumarate) Emtricitabine 143491-57-0 CHFNO.S 247.25 247.04 248.05 Adenine 73-24-5 CHN, 135.13 135.05 136.06 Tenofovir 147127-20-6 CH4N,OP 287.21 287.08 288.09 表2.溶剂和添加剂 Reagent Grade Supplier Part number Acetonitrile OptimaLC-MS Fisher Chemical A955-212 Acetic acid Optima LC-MS Fisher Chemical A113-50 Methanol Optima LC-MS Fisher Chemical A456-212 Water Ultra-Pure, 18.2 MQ Thermo Scientific"M BarnsteadTM GenPureMxCAD at 25°C Plus Ultrapure Water Purification System 采用 Thermo ScientificTM VanquishTM Flex Quaternary UHPLC 系统进行色谱分离(表3)。用一根内径为100 um,长75 cm 的 MP35N毛细管柱 (P/N 6042.2390) 连接至 ISQ EC MS 上。LC 和 MS条件分别见表4和表5。 表 3. Vanquish Flex Quaternary UHPLC 系统模块 Module Part Number Vanquish System Base F VF-S01-A Vanquish Quaternary Pump F VF-P20-A (with 200 uL mixer) (6044.5110 and 6044.5026) Vanquish Split Sampler FT VF-A10-A Vanquish Column Compartment H VH-C10-A Vanquish Variable Wavelength Detector F VF-D40-A (2.5 uL SST flow cell) (6074.0360) 表 4. HPLC 条件 Parameter Value Column Thermo ScientificAccucore aQ, 2.6 pm, 2.1 x 100 mm (P/N 17326-102130) Mobile phase A: Water with 0.1% acetic acid B: Methanol with 0.1% acetic acid C: Acetonitrile with 0.1% acetic acid Gradient 0-4 min: 0-70% B, 0-15% C 4-4.5 min: 70% B, 15%C 4.5-5 min: 70-25% B, 15-70% C 5-6 min: 25% B, 70%C 6-6.1 min: 25-0% B, 70-0% C 6.1-15 min: 0% B, 0% C Flow rate 0.6 mL/min Column temperature Still air, 40 °C Active pre-heater, 40 °℃ Injection volume 1 pL or 10 pL UV detection 260 nm, 100 Hz, easy mode 表5.MS条件 Parameter Value Vaporizer temperature 450°C lon transfer tube temperature 350°C Source voltage +750V SIM scan Compound Adenine Time 0-1.5 min Mass 136.1m/z Source CID voltage 20 V Compound Tenofovir Time 0-1.5 min Mass 288.1m/z Source CID voltage 25V Compound Emtricitabine Time 1.5-3.0 min Mass 248.1m/z Source CID voltage 10V Compound Tenofovir disoproxil Time 3.0-4.0 min Mass 520.2 m/z Source CID voltage 10V Full Scan Time 0-15 min Mass range 120-600 m/z Source CID voltage 10V ISQ EC MS完全集成到 Chromeleon 7.2 CDS 中,用于系统操作和后续数据分析。 用5%的甲醇水溶液逐级稀释 10 ppm 腺嘌呤和替诺福韦以配制校准标样(10 ppb-10 ppm)。用5%的甲醇水溶液稀释1000 ppm 替诺福韦酯、1000 ppm 恩曲他滨和10 ppm腺嘌呤/替诺福韦溶液,以配制用于测量杂质含量的样品。配制的样品列于表6中。 表6.杂质样品和所用的样品浓度(1 ppm=1 ng/uL) Impurity Level Adenine Tenofovir Emtricitabine Tenofovir Disoproxil (ppm) (ppm) (ppm) (ppm) 1% 1 1 66.7 100 0.2% 0.2 0.2 66.7 100 0.1% 0.1 0.1 66.7 100 0.02% 0.02 0.02 66.7 100 0.01% 0.01 0.01 66.7 100 首先考察杂质分析的系统适应性。在先前出版物中采用了USP参考方法来减少循环时间,并将色谱柱从4.6 mm转换为2.1 mm。本文对方法进行了进一步修改。溶剂A为0.1%的乙酸水溶液,溶剂B为0.1%的乙酸甲醇溶液和溶剂C为0.1%的乙酸乙腈。由于修改,该方法与USP 方法并不等同。 不过,所开发的方法预计满足 USP 规定的色谱要求,即替诺福韦酯的峰拖尾≤2.0,相对标准偏差≤10%,以及腺嘌呤和替诺福韦的分离度≥1.5。USP 适用性要求是通过质谱检测法确定的,该检测方法是在色谱柱上重复进样10 ng 腺嘌呤和替诺福韦,及100 ng 的替诺福韦酯和66.7 ng的恩曲他滨(图2)。 图2.腺嘌呤,替诺福韦,恩曲他滨和替诺福韦酯的色谱图。A)10 ng 腺嘌呤和替诺福韦的UV色谱图(上)和SIM扫描(下图)。B)100ng 富马酸替诺福韦酯和 66.7 ng 恩曲他滨的UV色谱图(上)和SIM 扫描图(下)。 替诺福韦酯的拖尾因子为 1.7, RSD 为 4.0%。腺嘌呤和替诺福韦的分离度为4.0(根据公式1计算)。因此,满足了所需的适用性阈值。因此,认为该方法适用于杂质分析。 于腺嘌呤来说,100 pg的信噪比为9。因此,检测限可以认为低2到3倍(S/N3)。在单离子监测(SIM)模式下,检测到柱上1pg的腺嘌呤和10 pg 的替诺福韦的信噪比分别为10和7。因此,检测限可能低2-3倍。 其次,比较了紫外检测和质谱检测的检测限。通常质谱检测器在检测限方面优于紫外检测器。因此,比较了 ISQEC MS 和 Vanquish Flex 可变波长 (VWD) 检测器的检测限。通过观察 ISQ EC MS 和 VWD的信号响应,发现检测限的差异高达三个数量级(图3)。采用VWD, 柱上1ng的替诺福韦的信噪比为10(S/N;峰至峰),而对 图3.对腺嘌呤和替诺福韦比较紫外线检测器和 ISQ EC MS 上的信号响应(EIC:提取离子色谱图; S/N:通过峰对峰的方法计算信噪比) 为了证明 ISQ EC MS 可以对低含量的杂质进行准确定量,如分析替诺福韦酯中的腺嘌呤和替诺福韦,其含量在0.01%一0.2%之间。采用 Timed-SIM模式对腺嘌呤,替诺福韦,恩曲他滨和替诺福韦酯进行目标分析(图4)。 选择 SIM窗口(0.6amu)和驻留时间(0.2s)参数来增加信号强度,并确保在峰上进行至少扫描15次以获得良好的定量结果。执行全扫(0.05s停留时间)用于确定峰纯度和非目标背景筛选。 图4.富马酸替诺福韦酯/恩曲他滨(100 ppm/67 ppm)中的1%腺嘌呤和替诺福韦(各1ppm)的色谱图分析。上图:基峰色谱图。中间: SIM扫描。下图: SIM扫描的 SIM 窗一一采集窗口。 相关样品浓度范围内的腺嘌呤和替诺福韦的校准曲线如图5。所有样品均按一式五份进行进样。然后,一式三份地重新注入校准样以验证校准的准确性。腺嘌呤和替诺福韦具有良好的回收率,在最低浓度下的偏差小于10%, 其他所有浓度下的偏差小于5%。重复进样间的标准偏差低于10%,说明精度很高(数据未显示)。 图5.腺嘌呤和替诺福韦的校准曲线。采用 1/x加权进行二次拟合。腺嘌呤:80.7655+32.6257x-0.0126x²,R²=0.9994;替诺福韦:-43.5406+4.0614x+0.0001x,R²=0.9996。 对杂质进行重复进样五次。可以很轻松地对腺嘌呤和替诺福韦定量低至0.01%(图6)。两种化合物均达到了良好的准确性(表7)。大多数杂质水平的标准偏差小于5%,即实现了高精度。最低的一个标准偏差也小于10%。 time [min] 图6-用于杂质水平定量分析的腺嘌呤和替诺福韦 SIM 扫描的提取离子色谱图。 表7.腺嘌呤和替诺福韦在不同杂质水平下的回收率和标准偏差(SD)。注入1pL试样对腺嘌呤进行定量分析,注入10 pL试样进行替诺福韦定量分析,为进行准确定量获得足够的信号响应 Impurity Level Adenine Recovery ± SD Tenofovir Recovery ± SD 0.2% 105.1%±0.8% 100.5%±2.0% 0.1% 111.3%±2.2% 93.7%±2.4% 0.02% 111.7%±3.7% 92.9%±4.4% 0.01% 103.7%±6.2% 100.0%±9.4% 可使用与 SIM 数据同步采集的全扫数据来评估与 API共洗脱的其他组分的存在。检查替诺福韦酯峰的前端、顶端和尾部的质谱图中是否存在其他物质(图7)。替诺福韦酯以[M+H]+为主导峰。另外,检测到钠加合物[M+Na]*(m/z 542.0)。未检测到其他峰,表明了峰纯度。 图7.替诺福韦酯的峰纯度分析。图中显示了替诺福韦酯的峰前、峰尖和峰尾的质谱图。峰前和峰尾采用15%的峰高。以主峰的1%作为检测阈值 杂质分析的另一个重要方面是检查样品中是否存在其他意外或未知杂质。这可以通过查看全扫的数据来完成。本文检测到了恩曲他滨和替诺福韦酯之间的其他杂质洗脱(图8)。将质谱信息与 USP提供的杂质信息相结合,可以对两种杂质进行质量确认:替诺福韦吡呋单酯和替诺福韦二吡呋酯,可以确定第三个为替诺福韦甲基酯,三种化合物的观测质量均偏离理论质量0.1 amu(表8)。 time [min] 图8.用质谱确证法鉴定未知杂质。下图:替诺福韦酯/恩曲他滨中1%的腺嘌呤和替诺福韦的基峰色谱图。检测到三个其他峰与恩曲他滨和替诺福韦酯共洗脱。上图:通过这些峰的质谱图将其鉴定为替诺福韦吡呋单酯,替诺福韦甲基酯和替诺福韦二吡呋酯 Impurity Chemical Theoretical Mass Observed Mass Mass Deviation Formula [M+H]+ [M+H]+ (amu) Tenofovir isoproxil C4H22N,,P 404.1 404.0 0.1 monoester Tenofovir methyl C5H24N5O,P 418.2 418.1 0.1 isoproxil Tenofovir isopropyl CH28N,O,P 446.2 446.1 0.1 Isoproxil 结论 1、用 ISQ EC 单四普质谱仪可以进行杂质定量检测。 2、SIM模式相较紫外检测而言大大提高了灵敏度,可将其用在目标定量上。 3、全扫模式结果,通常用在现有分析物的检测上,并为其提供质量信息。这一点将有助于峰纯度测定和未知杂质检测。 ( 1.ICH H armonised Tripartite Guideline - Impurities inNew Drug Products, Q3B(R2),2 June 2006. ) ( 2.USP Pending Monograph Ver s ion 1 - T enofovir http://www.usp.org/sites/default/files/usp_pdf/EN/USPNF/pendingStandards/m3429_authorized.pdf(accessed May26,2017) ) 3.Thermo Scientific Application Note 1129: TernaryGradient for Tenofovir Disoproxil Fumarate ImpurityProfiling, Germering, Germany, 2016. https://tools.thermofisher.com/content/sfs/brochures/AN-1129-LC-Ternary-Gradient- Tenofovir-AN71676-EN.pdf (accessedMay 26,2017) 集合 UV/Vis、CAD和单四极杆质谱的多检测器平台应用于样品全面分析 作者 Stephan Meding, Katherine Lovejoy, RemcoSwart, Frank Steiner, and Martin Ruehl, ThermoFisher Scientific, Germering, Germany 关键词 Vanquish UHPLC, ISQ EC/ISQ EM 单四极杆质谱仪,电雾式检测器(CAD),可提取物,浸出物 目的 对样品中存在的其他化合物进行确认和定量,如杂质、降解物或可提取物和浸出物。 应用优势 1、多种互补型检测器能发现在标准 UV-MS 设置中可能被忽略的峰。 2、未知样由 CAD 定量后由 MS 进行识别。已知物质通过 CAD 或 UV定量。 3、大气压化学电离(APCI)为不易离子化的化合物(例如某些可提取物和可浸出物)提供了一种可替代加热电喷雾电离(HESI)的离子化模式。 简介 色谱仪只有在检测器产生响应时才能分析样品含量。若样品组成明确,则检测器的选择会比较容易。例如,若已知组分都具有发色团,则非常适合使用UV检测器。对于组成不明确的样品,例如带有杂质、降解产物或被可提取物和浸出物污染的样品,单个检测器可能会漏检某些组分,因此需要使用多个检测器来对样品进行全面的分析。使用多重互补型检测器进行全面的样品分析对于确定未知样或非预期存在的化合物至关重要。除单纯的检测需求外,实验室还经常需要对这些化合物进行定性和定量来确定其特性及它们是否在可接受的浓度限值下。紫外检测器可准确定量含发色团的物质。电喷雾检测器(CAD) 提供了对不挥发性和半挥发性化合物的通用检测,使其成为理想的第二种检测器。此外,其几乎一致的响应使得无需参考标准品即可进行定量分析。质谱(MS)提供了所检测化合物的鉴别。这三种检测技术提供了一个全面的样品分析平台,并通过应用两种不同电离模式(HESI和APCI) 用于 MS 检测进一步扩展了该平台。该平台适合用在从细胞培养袋中提取的杂质分析上。 表1.交正用的标准品 # Analyte CAS Purity Amount in 10 mL Solvent (mg) 1 Phthalide 87-41-2 0.98 10.20 methanol 2 Phthaldialdehyde 643-79-8 0.99 10.10 methanol 3 Bis(2-hydroxyethyl) terephthalate, (BHET) 959-26-2 0.945 10.58 methanol 4 Dimethyl phthalate 131-11-3 0.99 10.10 methanol 5 Bisphenol A 80-05-7 0.99 10.10 methanol 6 Butylparaben 94-26-8 0.99 101.0 methanol 7 TinuvinTM P 2440-22-4 0.97 10.31 isopropanol 8 Azobenzene 103-33-3 0.98 10.20 methanol 9 2,4-di-t-Butylphenol 128-39-2 0.99 10.10 methanol 10 Butylhydroxytoluene, (BHT) 128-37-0 0.99 10.10 methanol 11 Palmitic acid 57-10-3 0.99 10.10 acetone 12 Erucamide 112-84-5 0.85 11.76 methanol 13 Stearic acid 57-11-4 0.985 10.15 acetone 14 Tinuvin" 234 70321-86-7 unknown 10.31 methanol 15 Irganox1010 6683-19-8 0.98 10.20 methanol 16 Irgafos" 168 31570-04-4 0.98 10.20 acetone 17 Eicosane 112-95-8 0.99 101.0 n-hexane 18 letracosane 646-31-1 0.99 101.0 n-hexane 文献报道的存在于细胞培养袋11-3]上的可提取物中 的18种化合物的标准品。表1列出了等级和纯度。Fisher ScientificTM OptimaTM LC/MS 级乙腈(P/N A955-212),甲酸(P/NA117-50),异丙醇(A461-212),丙酮(P/NA949),正己烷(P/N H306)和甲醇(P/NA456-212)。使用的超纯水是通过 Thermo ScientificTMBarnsteadTM GenPureTM xCAD Plus 超纯水净化系统生产的。 系统 Thermo ScientificTM VanquishTM Flex UHPLC 系统以两种不同配置进行色谱分析(图1和图2)。在标准设置(图1)中,四元低压混合泵提供分析梯度。在反梯度(图2)设置中,泵模块包含了双三元低压泵,提供分析梯度和反梯度。反梯度使 CAD 和MS检测过程中溶剂组成恒定,从而改善了检测器响应的一致性。 CAD 的一致性响应在技术文摘728064中有详细说明。加热电喷雾电离(HESI)和大气压化学电离(APCI)这两种互补的电离模式提升了检测范围。 在反梯度设置中,采用标准的100 pm 内径的 Vanquish毛细管柱将分析梯度溶剂输送至分析柱和流通池(见图2)。高粘度的异丙醇需要在流通池后端使用内径为 130um的毛细管以保持流通池的背压小于120 bar。虽然尽可能使用最小内径的毛细管来减少峰展宽,但在此情况下只能使用较大的毛细管才能应用于合适的流速。反梯度流路采用130 um 内径的毛细管。通过采用T型管、MS端的背压是 CAD 端的背压的两倍来实现 CAD 和 MS之间的分流比(2:1)。 柱温箱中的2位/6通阀用于清洗色谱柱时将废液排出,减少质谱仪和 CAD 检测器的污染。 根据MS应用需要,使用200 uL 混合器代替标准 350 uL混合器。更小的混合器减少了梯度延迟体积,从而实现了更快的分析方法。 ( 标准设置: ) ( ·Thermo ScientificTM VanquishTM Q uaternary Pump F (P/N VF-P20-A)200 uL s tatic mixer (P/N 6044.5110) ) ( 反梯度设置: ) ( ·Thermo ScientificTM VanquishTM D ual Pump F to replaceQuaternary Pump (P/N VF-P32-A)Two 200 pL staticmixers (P/N 6044.5110) ) ( ·Thermo ScientificTM VanquishTM Split Sampler FT ( P/N VF-A10-A) ) ( ·Thermo ScientificTM VanquishTM Column CompartmentH (P/N VH-C10-A) 2-position/6-port valve (P/N 6036.1560) ) ( · Thermo ScientificTM VanquishTM Diode Array DetectorFG (P/N VF-D11-A)2.5 uL titanium flow cell (P/N 6083.0550) ) ( ·Thermo Scientific TM VanquishTM Charged AerosolDetector F (P/N VF-D20-A) ) ( ·Thermo ScientificTM VanquishTM ISQ EC/EM SingleQuadrupole Mass Spectrometer (P/NISQEC-LC/ ISQEM-ESI-APCI) ) ( · Thermo ScientificTM VanquishT M System Base F (P/N VF-S01-A) ) ( 色谱数据系统 ) ( ISQ EC/ISQ EM 质谱仪功能完全集成到 Chromeleon 7.2.9 CDS中 , 以用于系统操作和后续数据分析。 ) 图1.标准设置示意图。采用ID(内径)为100 um 的具有生物兼容性的 MP35N镍-钴-铬合金毛细管柱。 分流和阀 No. Additional part Description B Diverter Valve Vanquish 2-position, 6-port valve, P/N 6036.1560 C l-piece 150 um l.D., Vici ZT1XCS6-M 毛细管 No. Connection between Description 1 Pump right outlet - Injection valve port 1 Thermo Scientific Vipercapillary, ID×L0.10×350 mm, P/N 6042.2340 (all capillaries in Figure 1 are MP35N) 2 Injection valve left port 2- Column inlet Active pre-heater,0.1×380 mm, P/N 6732.0110 (optional passive pre-heater, P/N 6732.0174) 3 Column outlet- DAD ID×L0.10×300 mm, insulated, P/N 6083.2405 4 DAD -Diverter Valve ID ×L 0.10×250 mm, P/N 6042.2330 For VWD: IDxL 0.10x350 mm. P/N 6042.2340 7 Diverter Valve- Flow Splitter ID×L0.10×650 mm, P/N 6042.2370 8 Flow Splitter-Charged Aerosol Detector inlet ID×L0.10×450 mm, P/N 6042.2350 9 Flow Splitter - MS inlet IDxL0.10×750 mm, P/N 6042.2390 图2.反梯度设置示意图。使用100 um 内径的毛细管将分析梯度输送至分析柱和流通池。在流通池后段,使用了 130 um ID 的毛细管柱。在流通池的后段使用了 100 um ID 的毛细管(8)以确保合适的分流比。反梯度流路使用 130 pm 内径的毛细管。 分流器和阀 No. Additional part Description A T-piece 500 pm ID, P/N 6263.0035 B Diverter Valve Vanquish 2-position, 6-port valve, P/N 6036.1560 C T-piece 150 um l.D., Vici ZT1XCS6-M 毛细管 No. Connection between Description 1 Pump right outlet - Injection valve port 1 Viper capillary, ID×L 0.10×350 mm, MP35N, P/N 6042.2340 2 Injection valve left port 2 - Column inlet Active pre-heater, 0.1×380 mm, MP35N, P/N 6732.0110 3 Column outlet - DAD ID×L0.10×300 mm, MP35N, P/N 6083.7950 4 DAD -Diverter Valve ID×L 0.13×250 mm, SST, P/N 6040.2325 5 Diverter Valve-T-piece ID×L0.13×65 mm, SST, P/N 6040.2307 6 Pump left outlet -T-piece ID×L0.13×950 mm, SST, P/N 6040.2340 7 T-piece- Flow Splitter ID×L0.13×350 mm, SST, P/N 6040.2335 8 Flow Splitter - Charged Aerosol Detector inlet ID×L0.10×350 mm, MP35N, P/N 6042.2340 9 Flow Splitter-MS inlet ID×L0.13×750 mm, SST, P/N 6040.2320 使用实心硅胶增强核技术色谱柱和水一异丙醇梯度来实现反相色谱分析(表2)。反梯度程序的延迟体积采用等同的364 uL以便反梯度和分析梯度溶剂同时到达T型管。反梯度延迟是由 Thermo ScientificTMChromeleonTM 7.2色谱数据系统(CDS)中的向导根据色谱柱体积和流动相设置自动计算得出来的。 表 2A.色谱条件 Parameter Setting Column: Thermo ScientificAccucoreC18, 100x2.1 mm, 2.6 um Eluents: (P/N 17126-102130) A: 4 mM Formic acid in water, pH 3.1 B: Isopropanol Injection Volume: 2 puL Analytical Gradient: 0.5 mL/min flow rate Time [min] %B 0 5 10.5 100 12 100 12.1 16 5 Inverse Gradient: 0.5 mL/min flow rate Time [min] %B 0 100 0.728 100 11.228 5 12.728 5 12.828 100 16 100 Column Temp.: 45°C forced air mode. 45℃ active preheater Parameter Setting UV Settings: 10 Hz data collection rate. 0.5 s response time, 4 nm bandwidth, CAD Settings: MS Settings: 210,220,254,280,300, 320 nm and 190-345 nm (3D field) 35℃ evaporator temperature, 3.6 filter, 1.0 power function value, 10 Hz data collection rate Default HESI and APCI source settings for 0.167 mL/min (standard setup) or 0.333 mL/min flow rate (inverse gradient setup) MS Full Scan, +:Time 0-16 min Mass range 130-1250 m/z Dwell Time 0.1 s Polarity Positive Source CID voltage 10V MS Full Scan, -: Time 0-16 min Mass range 130-700 m/z Dwell Time 0.1s Polarity Negative 10V 洗脱液制备将150 uL甲酸加入1L水中制备洗脱液A。 ( 标液制备 ) 18种参考标液的制备:用10mL容量瓶配制浓度 1 mg/mL 的各标液(对羟基苯甲酸丁酯、二十烷和二十四烷除外),称样量和定容溶剂见表1。配制对羟基苯甲酸丁酯、二十烷和十四烷浓度为10 mg/mL。表1中的质量是根据纯度及可能在 CAD中与甲酸形成阳离子/盐计算的。 CAD 中的盐形成及其在稳定半挥发性物质中运用在技术报告728064中有详述。用甲醇通过单标来配制成包含全部18种标准品的校准标样。校正浓度为1、2、5、10、20和 50 pg/mL, 半挥发性物质包括对羟基苯甲酸丁酯、二十烷和十四烷的校正液浓度分别为 10、20、50、100、200和500 pg/mL,因这些物质在蒸发管中会部分损失。 研究了四种不同类型的一次性细胞培养袋,其内层由乙烯醋酸乙烯酯和不同密度等级的聚乙烯制成。提取物通过用异丙醇/水50:50(v/v)冲洗,真空浓缩至干燥制得。样品用70 uL 50:50异丙醇/水(v/v) 复溶。 工作流程:HESI和 APCI 虽然在本文中并行报告了 HESI 和 APCI数据,且也可以为ISQ EM提供一套 HESI/APCI复合离子源,但无法在同一次进样中测得数据。HESI 和 APCI 数据采集需要两次单独进样和仪器方法。采集 HESI 数据需要使用 HESI电喷雾探针,采集 APCI 数据需要使用 APCI 探针和APCI电晕针。 使用这两种设置分析了18种参考标准物质。使用 CAD和UV/NVis 检测器确定峰保留时间。CAD 和 UV检测器属于互补型检测器;有些峰只能通过 CAD 检测到,而有些只能通过UV/Vis 检测器检测到。通过结合检测技术,全部18种标样都可以用标准和反梯度设置进行测量。UV/Vis 检测器可以检测到十三种标物,十一种通过 CAD 检测器检测到,而另外六种则由双检测器检测到(表3)。UV/Vis 和 CAD 色谱图如图3所示。七种待测物由于它们的挥发性无法通过 CAD 检测到。但他们具有活性生色团,可以通过 UV/Vis 检测。相反,另外五种待测物的生色团较弱不能被 UV/Vis 检测到,但可以被 CAD 检测到。有两种分析物未显示强MS信号,很可能是由于电离较差导致。 表3.各参考标物结果总结。采用检查标记表明使用UV、CAD、MS(HESI) 和 MS (APCI)的可检测性。深灰色单元格表示使用一一电离模式MS 的相对峰面积比使用另一种离子源 MS的相对峰面积大至少20倍的物质。[M]是指单同位素质量。LOQ 指的是 CAD 的定量限(除非注明为UV),定义为在给定浓度下标准液的信噪比(S/N)比例大于6:1,相对于空白样品中测得的噪音。 # Analyte UV CAD MS (HESI) MS APCI) [M] Detected m/z, HESI/APCI Detected Ion HESI/APCI LOQ (ug/mL) 1 Phthalide √ √ 134.0 135.1 [M+H]+ 5 (UV) 2 Phthaldialdehyde √ 134.0 135.1 [M+H]+ 5 (UV) 3 BHET √ √ √ 254.1 255.1 [M+H]+ 1 4 Dimethyl phthalate √ √ √ 194.1 195.1 [M+H]+ 1 (UV) 5 Bisphenol A √ 228.1 227.1/228.1 [M-H]/[M]+ 1 6 Butylparaben √ / √ √ 194.1 195.1 [M+H]+ 50 7 Tinuvin P √ 225.1 226.1 [M+H]+ 1 (UV) 8 Azobenzene √ √ √ 182.1 183.1 [M+H]+ 1(UV) 9 2,4-di-t-Butylphenol √ √ 206.2 205.2/206.2 [M-H]/[M]+ 1(UV) 10 BHT √ 220.2 219.2/220.2 [M-H]/[M]+ 1 (UV) 11 Palmitic acid / √ 256.2 255.2 [M-H]- 1 12 Erucamide √ / √ 337.3 338.3 [M+H]+ 1 13 Stearic acid √ √ √ 284.3 283.3 [M-H]- 1 14 Tinuvin 234 √ √ √ √ 447.2 448.2 [M+H]+ 1 15 Irganox 1010 √ √ √ √ 1176.8 1193.8/1176.8 [M+NHJ+/[M]+ 1 16 Irgafos 168 √ √ √ √ 646.5 647.5 [M+H]+ 1 17 Eicosane √ 282.3 50 18 Tetracosane √ 338.4 图3.(A).采用标准设置分析参考标准混合物的代表性 UV/Vis 和 CAD 色谱图。蓝色表示仅用 UV/Vis 检测到的分析物,红色表示仅用 CAD 检测到的分析物,绿色表示同时用 UV/Vis 和 CAD 检测到的分析物。星号表示分析标准品中的杂质。样品浓度是50 pg/mL,除对羟基苯甲酸丁酯,二十烷,二十四烷外,因他们都属于半挥发性物质,其浓度为500 pg/mL, 在 CAD 上具有较高的LODs。识别号参照表3中列出的标准物质名称。(B).利用HESI源检测5种分析物的提取离子色谱 (XICs)。标题中的标识号参照表3中的名称。所示的 m/z 值是用在单离子监测 (SIM) 扫描的值。 用 HESI和 APCI单四极杆质谱仪(表3)可以清楚检测到16种化合物。质量确认是在和UV/Vis 或 CAD 检测的同一洗脱时间内,在全扫和 SIM 扫描中用正离子或负离子模式分别检测出的 m/z的对应物质。五种代表性待测物提取的 SIM 扫描如图3所示。 使用APCI 相对峰面积较好的物质是偶氮苯和 BHT。使用HESI相对峰面积较好的物质是 BHET、棕榈酸和硬脂酸。提取 SIM 扫描结果,在利用 APCI 和 HESI 对 BHT和棕榈酸进行检测的性能对比如图4所示。 HESI APCI 8.0e4- 8.0e4 - 梯度会令到大部分水相条件下洗脱的物质响应曲线更浅,而对于在有机相条件下洗脱出的物质响应曲线更陡峭。这种均衡有助于在可能没有标准品的情况下使用单个校正物对待测物进行定量,见图6。该图显示了使用单一校准物(双酚A)对不同分析物进行定量。 图 4. APCI 和 HESI 在检测灵敏度上存在差异的物质示例。BHT采用APCI检测较好,棕榈酸采用 HESI 检测较好。(顶行, BHT, 显示 HESI下 m/z 219.2采用负离子模式的 SIM 扫描。显示 APCI 下 m/z 220.2采用正离子模式的 SIM 扫描,下图为棕榈酸, m/z 为255.2的负离子模式SIM 扫描)。 有/无反梯度条件下用CAD 定量的校正曲线如图5所示。使用反梯度时,校正曲线重叠、响应一咥性优于无反梯度情况。反梯度的整体优势是响应更统一,并且可以使用通用型校准物进行定量。具有反梯度的 CAD 响应一致性得到了明显改善。图5B中显示的校正曲线响应的相似性比图5A中的更好,由此反映出曲线间的相似性更好。反 图5.不使用(A,上图)和使用(B,下图)反梯度时由 CAD 定量的校准曲线。对羟基苯甲酸丁酯、二十四烷和二十烷的曲线并未显示在在,因其自身的挥发性使其定量限为 50 pg/mL。 选择双酚A是因为双酚A约在梯度中间进行洗脱。八种待测物的估算含量在反梯度条件下更接近于20 pg/mL的目标值。三种半挥发性分析物:对羟基苯甲酸丁酯、二十烷和二十四烷低于预期响应且无法通过单一通用型校准物进行精准定量(参见图6)。除待测物本身的挥发性外,盐的形成同样也会影响其响应,这些半挥发性物质的鉴别因素和方法在技术报告728064中有详细说明。 图6.运用反梯度或不运用反梯度条件下使用通用型校准物(双酚a)进行校正。使用反梯度设置可以使 CAD 信号响应更加统一,因此可以采用通用标准物质进行更精准的定量。星号表示半挥发性物质,其响应较低,定量限仅为 50 pg/mL。 UV和 CAD 的响应一致性比较(图7)证明了 CAD 对未知物的定量更准确。UV 检测器对小分子的响应取决于分子的摩尔吸光系数,该范围从 0-10,000M^'cm²。因此,分析物在给定波长下响应显示的强或弱主要取决于所存在的生色团。CAD 响应在很大程度上不受待测物化学及物理特性的影响向。 图7.使用通用校准物(双酚A)通过 UV和 CAD 对重新注入20pg/mL的标准品定量后进行比较。若使用通用校准物, CAD 可提供统一的响应,因此比 UV定量更准确。对羟基苯甲酸丁酯在 CAD 中被鉴定为半挥发性物质,由于其检出限为 50 pg/mL, 因此无法通过通用校准物进行定量。 样品分析 对在生物制药生产中使用的细胞培养袋内浸出的污染物进行分析,对预防有毒的可提取物和可浸出物最终进入终端产品且有可能伤害患者至关重要。提取了四个不同品牌的一次性细胞培养袋内层(异丙醇和水),这些袋子内层聚合物成分主要为乙烯醋酸乙烯酯、密度等级不同的聚乙烯。提取物分析显示,四分之三的提取物中有高含量的紫外不可见物质一增滑剂芥酸酰胺(表4和图8)。 Amount (ug/mL) RT (min) UV CAD HESI-MS A B C D Detected Mass Possible Identity 7.14 √ √ 5.5 325.3(+) unknown 7.29 √ √ √ 374.3(+) unknown 5.9 4.6 8.9 3.8 6.2 375.4(-) unknown 7.73 √ √ √ 149 144 111 144 136 473.4(-) bDtBPP,[M-H] 8.72 124 131 95.6 132 115 403.4(-) unknown √ / / 31.8 31.9 36.8 2.1 338.3(+) erucamide,[M+H]+ 8.83 3.0 3.7 3.5 283.3(-) stearic acid, [M+H]+ 10.17 √ √ 1.9 15.8 16.2 15.2 663.5,685.5,723.5(+) TBPP-ox,[M+H]+,[M+Na]+, [M+H+IPA]*+ 10.88 √ √ 1.4 1.9 2.0 3.1 279.2,366.2(+) unknown 图 8.通过 UV/Vis 检测器、CAD和 MS对细胞培养袋内里的提取物进行分析。样品C的UV(210nm)和 CAD 色谱图。两种检测模式均检测到几种可提取物。插图:使用HESI 对在几个样品中发现的两种可提取物进行全扫的 XIC图。一个是未知提取物,保留时间为7.73分钟,负离子模式下的 m/z为473.3。另一个是芥酸酰胺。 如前所述1, IrgafosTM168 的两种衍生物也存在于许多样品中(表4)。综合来看,在营养袋中发现了19种未知物和两种已知物(硬脂酸和芥酸酰胺),通过通用型校正物质(双酚A)的校正曲线对发现的全部物质进行了定量(图9和表4)。通过 MS 对所有提取物的质量进行检测。根据检测到的质量和先前的报道1,可以鉴别出两个未知物,即双(2,4-二叔丁基苯基)磷酸酯和氧化形式的Irgafos 168。 电离模式的选择 事实证明, HESI或APCI 均适用于类类分析。校准标准品18种物质中的16种都可以被两种源检测到,但电离模式间的灵敏度有所不同。电离模式的选择取决于分析物的类型。与 HESI相比, APCI 是一种气态电离过程,对液相中难质子化或去质子化的分析物非常适用,而 HESI是一种依靠液相中存在的离子的过程。相反, HESI 更适合在APCI 的严苛条件下的受热不稳定的化合物。若仍有疑问,可通过两种不同的电离模式分析同一样品,可以最大限度降低由于化合物电离不良而导致峰丢失的风险。 图9.用紫外线分析细胞培养袋衬里提取物 CAD 和MS。(A)滑爽剂、芥酸酰胺的估算量。(B)涂层剂,硬脂酸的估算量 当样品中包含不在标准品列的未知物时,利用多检测器设置下的反梯度法,通过 CAD 对这些物质进行定量。通过MS对峰进行识别,并由UV3D/轮廓图数据支持。若样品中全部峰均在标准品中,则可以只使用含一种分析梯度的多检测器设置。由互补型检测器 CAD 和 UV实现定量,MS则用于峰确认。 结果 1.UV/Vis 检测器和 CAD 彼此互补,对样品进行全面的分析。 2.反梯度的多重检测器设置允许使用单个校正物,对不能作为参考标准或未知的化合物进行定量。 3.质谱检测对有关检测到的分析物提供了其他信息,从而可以对已知化合物进行身份确认或对未知化合物进行初步鉴定。有关更完整的样品表征信息可以应用两种电离模式 APCI 和 HESI 来获得。 ( 1 . Dorival-Garcia , N.;Bones, J. Monitoring leachables fromsingle-use bioreactor bags for mammalian cell cultureby dispersive liquid-liquid microextraction followedby ultra hig h performance liquid chromatographyquadrupole time of flight mass spectrometry . J.Chrom.A2017,1512,51-60. ) ( 2. Norwood, D.L.; Jenke, D.; Manolescu, C.; P ennino,S.; Grinberg, N. HPLC and LC/MS Analysis ofpharmaceutical container closure system l e achablesand extractables. J . Liquid Chrom. Related Tech. 2009, 32,1768-1827. ) 3. Asa, D.; Carreiro, D. Extractable and leachablemeasurements by universal HPLC detection. TheApplication Notebook. September 2007, 65. AccessedOctober 2018 at www.chromatographyonline.com/parabens-topical-preparations-using-spme-gc-ms 4. Menz, M.; Eggart, B.;Lovejoy, K.; Acworth,I.;Gamache, P.; Steiner, F. Charged aerosol detection一 factors affecting uniform analyte response.ThermoFisher Scientific Technical Note 72806; October 2018. 通过UHPLC-UV结合单四极杆质量检测器对活性药物成分中的基因毒性杂质进行定性和准确定量 作者 Sylvia Grosse, Mauro De Pra, Frank Steiner ThermoFisher Scientific, Germering, Germany 关键词 基因毒性杂质,对甲苯磺酸甲酯,阿瑞匹坦, ISQEM,单四极杆,质量检测,UV检 测, Autospray功能 应用优势 1、质谱检测可简单可靠地对峰定性确认。 2、、灵敏的UV检测可定量检测低于 ng/mL 浓度量级的基因毒性杂质 3、、使用 Autospray 功能可以简单方便地调节离子源参数的设置 目的 通过单四极杆质量检测器对原料药中有关物质和基因毒性杂质进行定性确认。通过 UV 检测器对基因毒性杂质进行准确定量。 简介 与生产过程和产品相关的杂质的分析是整个药物生命周期中必不可少的步骤。迄今为止,具有紫外光(UV)检测器的高效液相色谱(HPLC)是用于评估活性药物成(API)纯度最常用的技术。通常都是根据保留时间来评估鉴定。为此,必须对单一杂质的标准品分分进行测试。在药物开发的早期阶段,通常无法获得杂质的标准品,因此很难简单的对峰定性确认。基因毒性杂质是一类特殊的杂质,因为它们具有致癌性,因此会对患者健康带来比药物本身更大的风险。被鉴定为药物潜在污染物的基因毒性杂质必须依据比其他杂质更严格的规则进行监测和准确定量。美国食品药品监督管理局(U.S.FDA) 和欧洲药品管理局(EMEA)已将使用该类药物产品进行长期治疗的毒理学关注阈值(TTC)设置为 1.5 pg/天1。此外,人用药物注册技术要求国际协调会(ICH) M7提出的基于药物暴露持续时间的分阶段 TTC 如表1所述图。 根据 TTC的值,可以根据对患者给药的预期每日剂量,使用以下公式计算浓度极限值值: 对甲苯磺酸盐是一种基因毒性杂质。它们会作为药物合成的副产物出现,比如对甲苯磺酸与醇(例如甲醇,乙醇或异丙醇)反应。由于对甲苯磺酸经常被用作形成盐的平衡离子,因此对甲苯磺酸盐是常见的基因毒性杂质4。对甲苯磺酸盐的鉴定很容易,因为已有现成的标准品。然而,在药物开发的早期阶段,如果 HPLC 方法能够一次鉴别出基因毒性杂质和其他有关物质,而无需单独运行标准品是实用且合乎需求的。这可以通过将 HPLC 与 UV和质量检测器串联使用来实现,其中UV检测提供定量信息,质量检测器提供定性信息。对合成途径的理解通常可以扣除掉许多预期的杂质,这些杂质可以汇总在完整的质量清单中。然后可以通过单四极质谱仪普 SIM 模式下进行筛选,从而进行可能杂质的推定。 本研究的目的是开发一种对原料药中的对甲苯磺酸甲酯以及其他有关物质监测和定量的方法。本研究中选择的API是阿瑞匹坦。阿瑞匹坦是一种止吐药,用于预防化疗期间的恶心和呕吐。由于在不同的合成步骤中对甲苯磺酸和甲醇都有应用,因此具有基因毒性的对甲苯磺酸甲酯可能会污染阿瑞匹坦[4.5]。 实验 试剂 去离子水,电阻率18.2MQ·cm以上 ( Fisher Scientific 乙 腈 , OptimaTMLC / MS级 ( P/N A955- 212) ) ( Fisher Scienti f ic甲醇, OptimaTMLC / MS 级(P/N A456- 212) ) ( Fisher ScientificTM 醋酸铵, LC /MS级(P/NA114-50) ) ( Fisher ScientificTM 对甲苯磺酸甲酯(P/N AAA11088130)从供应商处购买了两种阿瑞匹坦的样品。 ) ( 设备 样品瓶(棕色, 2mL) , Fisher Scientific ( P/N 11545884) ) 带有隔垫的卡扣盖(硅胶/PTFE), Fisher Scientific (P/N 10547445) 标准品制备 用乙腈配制浓度为 1 mg/mL 的对甲苯磺酸甲酯(甲基-TSF)储备溶液。 通过将 100 uL 的储备溶液转移到 10 mL的容量瓶中并用水/乙乙50/50(v/v)的溶液定容,来制备 10 pg/mL的标准溶液。根据该溶液,制备浓度为0.01 pg/mL, 0.025ug/mL, 0.05 pg/mL, 0.075 pg/mL,0.1 pg/mL, 0.25 pg/mL, 0.5 pg/mL, 0.75 pg/mL, 1 pg/mL, 和 2.5 pg/mL 的校准标样。 另外,准备0.005 pg/mL的标准溶液,用于确定检测限(LOD)。 Duration of exposure <1 month >1-12 months >1-10 years >10 years Acceptable daily intakes for an individual impurity(ug/day) 120 20 10 1.5 Acceptable total daily intakes for multiple impurities (ug/day) 120 60 30 5 用水/乙乙,50/50(v/v)的溶液制备 1 mg/mL的每种阿瑞匹坦样品(阿瑞匹坦1和阿瑞匹坦Ⅱ)母液溶液。 把含有甲基-TSF的阿瑞匹坦1样品作为杂质,用于杂质筛选实验和定量。 阿瑞匹坦Ⅱ样品不含甲基-TSF,因此通过在1 mg/mL阿瑞匹坦Ⅱ样品中掺入0.01 pg/mL, 1 pg/mL 和2.5 pg/mL的甲基-TSF 用于测定回收率。 仪器 配备 Thermo ScientificTMISQTMEM 单四极杆质谱仪的Thermo ScientificTMVanquishTMFlex 四元 UHPLC 系统用于实验分析: ·Thermo ScientificTMVanquishTM 色谱系统 VanquishHorizon/Flex(P/N VH-S01-A) ( ·Thermo ScientificTMVanquishTM进样器 FT (P/N VF- A10-A) ) ( · Thermo ScientificTMVanquishTM 柱温箱H(P/NVH- C10-A) ) ( ·Thermo ScientificTMVanquishTM 二极管阵列检测器F (P/N VF-D11-A)带半微量流通池,2. 5 uL (P/N 6083.0550) ) ( · Thermo Scientific ISQ EM 质谱仪(P/N ISQEM-ESI) ) 表2.用于杂质分析的LC条件 Column: Thermo ScientificAcclaim Polar Advantage ll, 150×2.1 mm, 2.2 pm (P/N 071401) Mobile phase: A: 15 mM ammonium acetate B: methanol Flow rate: 0.3 mL/min Gradient: Time [min] %B 0 60 4.5 60 6.0 73 21.0 73 21.5 60 35.0 60 Active pre-column heater temp.: 35°℃ Column temp.: 35℃ (forced air mode, fan speed 5) Autosampler temp:. 4°C JV wavelength: 225 nm 3D scan: 190-280 nm UV data collection rate: 10 Hz UV response time: 0.5 s Injection volume: 10 uL 利用 Thermo ScientificTM 变色龙色谱数据系统(CDS)软件中已有的功能,可以对 ISQ EM 质量检测器的离子源参数进行自动调整。 该软件允许使用进样列表中的序列自定义变量来自动优化源 CID电压(请参阅“变色龙7软件操作手册”帮助-自定义变量)。只需要创建一种仪器方法,仪器就可以在进样序列内的自定义变量窗口中定义所有的 CID电压值并自动运行(图1)。 对信号强度进行比较,以确定甲基-TSF的最佳 CID 电压。实验表明 CID 电压为 10V时是最佳设置。 此外, Autospray 智能离子源的设置允许根据色谱方法中使用的流速简便地自动调整离子源的气流和温度。有三个方面需要单独考虑:耐受性/灵敏度,流动相的挥发性和分析物的热稳定性。 图2显示了使用不同滑块位置时 Autospray 离子源设置的选择以及对气体和温度值的影响。 最佳结果等就可以通过叠加对比提取离子色谱图(XIC)来选择,如图2所示。使用图2-C的设置可获得最高的信号强度。如果由于灵敏度问题等原因需要对方法进行离子源参数的全面优化,则可以从 Autospray 给的设置作为起点开始。 More robustness Less volatile mobile phaseThermally stable analyte Parameter Value Sheath Gas 35.8 psig Aux Gas 4 psig Sweep Gas 0.5 psig Ion Transfer Tube Temp 300°C Vaporizer Temp 172°℃ Parameter Value Sheath Gas 20.8psig Aux Gas 3 psig Sweep Gas 0.5 psig Ion Transfer Tube Temp 300°C Vaporizer Temp 172°C Parameter Value Sheath Gas 35.8 psig Aux Gas 4 psig Sweep Gas 0.5 psig Ion Transfer Tube Temp 250°C Vaporizer Temp 172°℃ Retention Time (minutes) 图2.在基于 Autospray 智能离子源设置概念进行调整的情况下,使用不同 MS 离子源参数设置获得的甲基 -TSF提取离子色谱图的叠加图;A-默认位置;B-改变流动相挥发性的位置,C-改变热分析物稳定性的位置 杂质筛查 在研究中对基因毒性杂质甲基 -TSF和阿瑞匹坦16.71的几种已知的非基因毒性杂质进行了探究,并进行了定性监测(表4)。分析物的化学结构如图3所示。数据以SIM 扫描模式采集,以实现更灵敏的检测。当使用乙酸铵作为水性流动相时,甲基-TSF只会形成铵加合物[M+NH4]*, 而 API 及非基因毒性相关的杂质主要形成 [M+H]*离子。 此外,数据还以全扫描模式记录,以检测可能存在的未知杂质。 数据处理和软件 使用 Chromeleon 7.2.9 CDS软件进行分析,该软件完全集成了 ISQ EM质量检测器,可在单个软件平台上进行仪器控制,数据采集,数据处理和报告。 表3API中的杂质分析的 MS 条件 MS source parameters Sheath gas pressure: 35.8 psig Aux gas pressure: 4 psig Sweep gas pressure: 0.5 psig Vaporizer temperature: 172°C lon transfer tube temp.: 250 ℃ Source voltage: 3000V MS method parameters lonization mode: HESI Ion polarity: Positive Scan type: Full scan with six targeted SIM scans Spectrum data type: Profile (full MS) Full scan mass range: m/z 100-650 SIM width: 0.5 amu Dwell time: 0.1s 10 V Source CID voltage: 表4.阿瑞匹坦及一些有关物质的化学式,用于 SIM 扫描的m/z和检测到的离子种类 Compound Aprepitant Methyl- TSF Impurity I Impurity ll ImpurityIl Impurity lV Chemical formula C23H2FN40 C。19,S C2925FN9 C20H18FNO, C24H25FNO4 SIM Scan m/z 535.2 204.1 517.2 611.2 438.1 567.2 lon species [M+H]+ [M+NH]* [M+H]+ [M+H]+ [M+H]+ [M+H]+ Chemical names of impurities: Impurity1= Defluoro Aprepitant Impurity ll=4-Defluoro-4-(p-fluorophenyl)aprepitant Impurity Ill=Des-1,2,4-triazol-3-one-5-methyl-aprepitant Impurity IV= N-(Destriazolonomethyl) N-(Methylcarboxyacetamidohydrazono)aprepitant) 图 3.本研究中目标物质及有关物质的化学结构 杂质筛查 对API样品(阿瑞匹坦1)的分析结果在 UV 色谱图中显示了几个峰(图4)。根据表4进行 SIM 扫描,以确认是否存在预期的杂质(图5)。通过 SIM 扫描确认了四种杂质,其中包括一种具有基因毒性的甲基-TSF。对于杂质I, SIM 扫描色谱图仅有非常弱的信号且具有很强的基线效应,而UV在 MS检测到的微弱的信号的保留时间内未显示任何峰。因此,不能确认样品中是否存在杂质Ⅱ。图6展示了样品中甲基-TSF 峰的全扫描质谱及其与标准品的质谱图对比。两种质谱图看起来十分相似,这表明样品中没有其他化合物与甲基-TSF 一同被洗脱。Chromeleon CDS 可以解决 UV 和 MS 信号之间的时间延迟问题,这极大地优化了 UV 色谱图中峰的质量分配。此外,采集的全扫描质谱图还提供了有可能存在的预期外的杂质信息。其中一种在保留时间为 11.7 min, m/z为593.1的杂质可以被归属,但是没有对该杂质的种类进行进一步的研究。 图4.在225nm处获得的阿瑞匹坦1样品的紫外色谱图,其峰基于MS数据分配;灰色框:放大的和API有关物质的基线;仅考虑相对对积>0.03%的峰 图5.根据表4得到的,阿瑞匹坦1成分(a)和有关物质(b-f)的 SIM 扫描色谱图 图6.样品中甲基-TSF峰的全扫描质谱图(黑色)与甲基-TSF标准品的质谱图(绿色)相比 将甲基-TSF掺入样品中并在相同条件下进行测量,以明确是否有基因毒性杂质甲基-TSF存在。图7中的叠加色谱图显示了加标和未加标样品中甲基-TSF峰的精确匹配。 图7.加标的API样品(蓝色)和未加标的样品(灰色)的叠加UV色谱图 UV检测的线性,对甲苯磺酸甲酯的定量限和回收率 对甲苯磺酸甲酯的校准曲线是通过将十种浓度样品(0.01ug/mL-2.5 ug/mL)分别三次重复进样而获得。如图8所示,线性相关系数(R²)=0.9999,表明得了很好的线性。 图8.在0.01 pg/mL 至2.5 pg/mL的浓度范围内,对甲苯磺酸甲酯的UV校准曲线 检出限(LOD)和定量限(LOQ)是通过稀释标准溶液直至其达到对应浓度(LOD>3, LOQ≥10)来确定的。五次重复进样来评估 LOD 和 LOQ值。发现 LOD 为 3.3 ng/mL(标准偏差为±0.7 ng/mL)和 LOQ 为 9.4 ng/mL(标准偏差为±1.9 ng/mL)。 通过在阿瑞匹坦Ⅱ样品(不含甲基TSF的样品)中添加0.01ug/mL(LOQ水平), 1 pg/mL ( 基于 TTC值的浓度极限)和2.5 ug/mL(最高校准水平)的对甲苯磺酸甲酯标准溶液来估算回收率。回收率在 93-99%之间时表明,可以在整个测量范围内实现出色的回收率,从而可以在较宽的浓度范围内进行准确定量(表5)。 表5.对甲苯磺酸甲酯在不同峰值水平下的回收率 Spike Level Recovery (%) 0.01 ug/mL 1 pg/mL 2.5 pg/mL 使用紫外检测器定量分析样品中的基因毒性杂质甲基-TSF 根据 ICH M7 指南,由于药物治疗的持续时间少于1个月,因此允许的阿瑞匹坦的 TTC 为 120 ug/day3。基于125 mg 片剂的剂量,计算出的浓度极限为 960 ppm。使用上述方法算得,对于1 mg/mL的阿瑞匹坦样品,其浓度为 0.96 pg/mL。 API样品(阿瑞匹坦)的定量分析是通过3次进样得到的。如表6所示,通过回收率校正后的计算结果为0.010ug/mL, 相对标准偏差(RSD) 为5.05%。结果表明,样品中发现的基因毒性杂质远低于基于 TTC 值的浓度极限(0.96 pg/mL),而接近该方法的 LOQ。 表6.阿瑞匹坦1样品中对甲苯磺酸甲酯的定量结果 Measured Recovery Calculated RSD amount (%) amount (%) (ug/mL) (ug/mL) 0.009 93 0.010 5.05 结论 ( 1.UV和单四极杆质量检测器的组合对于开发早期阶段的API分析是很强大的工具,其可以对预期的杂质进行确认。 ) ( 2. Autospray 智能离子源设置能使没有经验的 MS用户也可以轻松快速地调节 MS 离子源参数。 ) ( 3.与基于960 ng/mL 的TTC值的浓度极限相比, L OQ值 要低10倍,因此可以证明 UV 法对对甲苯磺酸甲酯的 测定的灵敏度高。 ) ( 4.证明了对基因毒性杂质具有出色的检测线性和回收率。 ) 1. European Medicines Agency (EMEA), Committee forMedical Products for human use (CHMP), Guidelineson the limits of genotoxic impurities, 2006, EMEA/CHMP/QWP/251344/2006 2. U.S. Department of Health and Human Services, Foodand Drug Administration, Center for Drug Evaluationand research (CDER), Guidance for Industry, Genotoxicand Carcinogenic Impurities in Drug Substances andProducts: Recommended Approach, December 2008 3. International Council for Harmonisation of TechnicalRequirements for Pharmaceuticals for Human Use(ICH) , ICH Harmonised Guidline M7 (R1), Assessmentand Control of DNA Reactive (Mutagenic) Impurities inPharmaceuticals to Limit Potential Carcinogenic Risk,31 March 2017, current Step 4 version 4. Zacharis, C.K., Vastardi, E. Application of analyticalquality by design principles for the determination ofalkyl p-toluenesulfonates impurities in Aprepitant byHPLC. Validation using total-error concept, Journal ofPharmaceutical and Biomedical Analysis,2018, 150,152-161,https://doi.org/10.1016/j.jpba.2017.12.009 5. Elati, C.R., Kolla, N., Gangula, S., Naredla, A.,Vankawala, P.J., Avingiri, M.L., Chalamala, S.,Sundaram, V., Mathad,V.T., Bhattacharya, A.,Bandichhor, R. A. Convergent approach to thesynthesis of aprepitant: a potent human NK-1 receptorantagonist, Tetrahedron Letters, 2007, 48,8001-8004,https://doi.org/10.1016/j. tetlet.2007.09.051 6. United States Pharmacopeia, Aprepitant, USP PendingMonograph- Version 1, 2012 7.TRC website,https://www.trc-canada.com/products-listing/, accessed February 2019 应用文摘 一合成控制 应用文章72385 利用Thermo Scientific ISQ EC单四极杆质谱仪实现可靠的合成控制 Stephan Meding, Katherine Lovejoy, Martin Ru-ehl, Thermo isher Scientific, Germering, Germa-ny 关键词 单四极杆质谱仪、药物化学、合成控制、LC-MS定量、高通量 目的 使用 Thermo ScientificTM 单四极质谱仪 ISQTM EC 展示定量合成控制并证明了其对药物化学研究的好处。 简介 药物化学在药物发现、先导药物优化和药物研发中具有重要地位。它能使制药公司研究和开发新的活性药物化合物甚至一系列化合物。需要建立成功的方法来合成有机新型分子或分离天然来源化合物。,一个非常重要的工具就是 LC-MS, 它可以通过质量数确认来验证分析物,从而确定反应的产率,并在同一分析中检测与拟定的候选药物有关的杂质。另一个需求是需要快速的分析方法以实现高通量。通常,需要对候选药物进行大量筛查,这给LC-MS资源带来了压力。 现代化的单四极杆质谱仪,如 Thermo ScientificTM ISQTM EC 单四极杆质谱仪(ISQECMS),是为常规应用而设计的可靠产品。ISQ ECMS 可以进行全扫和单离子监测(SIM)模式操作,以对所有可检测到的分析物进行质量范围扫描或聚焦于某一特定化合物。它可以以适合快速 UHPLC 应用程序的扫描速率运行,同时提供皮克级检测限。新型正交源的设计即使面对的是复杂基质也能提供高水平的仪器耐受性。全面集成到 Thermo ScientificTM ChromeleonTM 7.2色谱数据系统(CDS) 和 Thermo ScientificTM AutoSprayTM 智能方法设置,使LC-MS 操作变得简单、直观。 本文把对乙酰氨基酚,也叫扑热息痛的合成作为例子来展示 ISQ EC MS 应用于快速、定量合成控制中。4-氨基苯酚通过乙酰化一步合成可得到对乙酰氨基酚,如图1所示。通过测定反应物和产物的比率以及和理论值相对比,就可以确定整个工艺的准确度和精密度。 图1.对乙酰氨基酚(扑热息痛)的反应方程式。 实验 样品试剂购于 Sigma-Aldrich。表1列出使用的分析物,表2列出了所用溶剂和添加剂。 表1.分析物 Analyte Purity CAS Chemical Formula Monoisotopic Mass [M] [M+H1+ 4-Aminophenol ≥98% 123-30-8 CHNO 109.05 110.06 Acetaminophen 98.0-102.0% 103-90-2 CHNO, 151.06 152.07 表2.溶剂和添加剂 Reagent Grade Supplier Part Number Acetonitrile Optima" LC-MS Fisher Chemical A955-212 Formic acid Optima" LC-MS Fisher Chemical A117-50 Methanol Optima" LC-MS Fisher Chemical A456-212 Water Ultra-Pure, 18.2 MQ at 25°℃ Thermo ScientificM BarnsteadM GenPurexCAD Plus Ultrapure Water Purification System 色谱分离是在 Thermo ScientificTM VanquishTM Flex Binary UHPLC 系统上运行,包含二元泵、自动进样器、柱温箱和可变波长检测器(表3)。内径100 um , 长75 cm 的 MP35N 毛细管柱(P/N 6042.2390)用于连接 ISQ EC MS。 表4列出了 HPLC条件,而MS条件在表5中列出。 表3. Vanquish Flex Binary UHPLC 系统模块 Module Part number Vanquish System Base F VF-S01-A Vanquish Binary Pump F VVF-P10-A (with 35 uL mixer) (6044.3870) Vanquish Split Sampler FT VF-A10-A Vanquish Column Compartment H VH-C10-A Vanquish Variable Wavelength Detector F VF-D40-A (2.5 uLSST flow cell) (6074.0360) 表4.HPLC条件 Parameter Value Column Thermo Scientific" Hypersil GOLD, 1.9 um, 2.1 x 50 mm (P/N 25002-052130) Mobile phase A: Water with 0.1% formic acid B: Acetonitrile with 0.1% formic acid Gradient 0-2 min: 5-50% B 2-3 min: 50% B 3-5 min: 5% B Flow rate 0.6 mL/min Column temperature Forced air, 40°℃ Active preheater, 40°C Injection volume 1pL UV detection 280 nm, 50 Hz, easy mode 表5. MS条件 Parameter Value Vaporizer temperature 550°C lon transfer tube temperature 350°C Source voltage +1000V SIM scan Compound 4-Aminophenol Time 0-0.5min Mass 110.1m/z Source CID voltage 20V Compound Acetaminophen Time 0.5-1.18 min Mass 152.1m/z Source CID voltage 20V Full Scan Time 0-5 min Mass range 105-250 m/z Source CID voltage 20 V ISQ EC MS 功能已完全集成到 Chromeleon 7.2 CDS中,以用于系统操作和后续数据分析。 通过在5%的甲醇水溶液中连续稀释储备溶液方法(在50:50甲醇:水溶液中1 ug/uL 的4-氨基苯酚和对乙酰氨基酚)来制备校准准样(10 ppb-10 ppm)。用于测定反应物和产物比率的样品通过用5%的甲醇水稀释储备液而得。配制的样品列表如表6。 表6.样品分析比率和使用的样品浓度(1 ppm=1 ng/pL) Theoretical Ratio 4-Aminophenol (ppm) Acetaminophen (ppm) (Reactant:Product) 100:1 10 50:1 5 20:1 2 10:1 1 5:1 0.5 2:1 0.2 0.1 1:1 0.1 1:2 0.2 1:5 0.5 1:10 1 1:20 2 1:50 5 1:100 1:200 0.05 1:500 0.02 1:1000 0.01 结果与讨论 合成控制要求对不同比率的反应物和产物进行快速、定量的分析。在该工作中,按100:11:1000(反应物与产物)比率预先混合并定量,以模拟对乙乙氨基酚从开始到基本完成合成。为确保定量结果最佳,开发了一种高通量方法,为4-氨基苯酚和对乙酰氨基酚达到基线分离(图2)。 5.0e6--Total lon Chromatogram from Full Scan 2.00 2.50 Time [min] 图2.全扫模式采集4-氨基苯酚和对乙酰氨基酚(50pg)的总离子流色谱图。图显示了高通量方法的梯度部分。梯度从5%B开始,然后增加到50%B。 SIM 扫描的采集窗口以橙色和蓝色表示。 使用 SIM 模式检测分析物以提高检测限。选择 SIM 窗口(0.4amu)和驻留时间(0.2s)参数以增加信号强度,并确保每个峰15次以上的扫描以获得良好的定量结果。使用保留时间窗口对4-氨基苯酚(m/z 110.1)和对乙酰氨基酚(m/z 152.1) 的 SIM 扫描进行定时,窗口完全包括了预期色谱峰的保留时间(图2)。为进行初始方法验证,执行了全扫模式采集和 SIM 模式采集。就定量而言,可仅执行 SIM 扫描以确保待测物能进行最优检测。 图3.比较了 UV 和 ISQ EC 检测器在检测对乙酰氨基酚上的信号响应(EIC:提取离子色谱图)。 4-氨基苯酚和对乙酰氨基酚的校准曲线如图4所示。所有进样都是重复五次。之后,再连续三次重新进校准物用以验证校准的准确性。4-氨基苯酚和对乙酰氨基酚都具有良好的回收率。重复进样之间的标准偏差低于5%,说明精度高(数据未显示)。 图4.4-氨基苯酚和对乙酰氨基酚的校准曲线。进样1pL, 1 ppb样品相当于柱上1 pg。应用1/x加权的二次拟合。4-氨基苯酚:3.7220x-0.0001x,R²=0.9962;对乙酰氨基酚:663.3313+10.2319x-0.0004x², R²=0.9966。 有关合成控制,分析了不同比例下的4-氨基苯酚/对乙酰氨基酚混合物,以100:1开始,于1:1000结束(表6和图5)。所有样品均按一式五份进样分析。可以准确地检测到样品成分的变化。随比率变化,对乙酰氨基酚的相对量符合预期增加。即使面对相对丰度小于1%的4- 氨基苯酚也能对其进行准确测定(放大图见图5)。这些结果充分表明, ISQ EC MS可以准确定量分析物。这些结果表明单四极杆质谱仪是药物化学中化学合成的高通量监测的合适工具。 图5.合成控制。绘制了4-氨基苯酚:对乙酰氨基酚比例的实验图。预混合比例以x轴表示。放大显示了刻度上比例从1:20至1:1000的4-氨基苯酚。 结论 1.可以使用 ISQ EC 单四极杆质谱仪完成高通量定量合成控制。 2. SIM 模式大大提高了UV检测的灵敏度,以用于目标物的定量分析。 3.全扫模式可对现有分析物进行常规检测,如:监控其他潜在产品,并可用于通用型方法。 北京 广州上海市浦东新区新金桥路27号3,6,7号楼 北京市东城区北三环东路36号环球贸易中心C座7层/8层 广州国际生物岛寰宇三路36、38号合景星辉广邮编201206 邮编100000 场北塔204-206单元电话021-68654588*2570 电话010-87946888 邮编510000电话020-82401600沈阳 西安成都市临江西路1号锦江国际大厦1406室 沈阳市沈河区惠工街10号卓越大厦3109室 西安市高新区科技路38号林凯国际大厦邮编610041 邮编110013 1006-08单元电话028-65545388*5300电话024-31096388*3901 邮编710075电话029-84500588*3801武汉 昆明南京市中央路201号南京国际广场南楼1103室 武汉市东湖高新技术开发区高新大道生物园路 云南省昆明市五华区三市街6号柏联广场写字邮编210000 生物医药园C8栋5楼 楼908单元电话021-68654588*2901 邮编430075 邮编650021电话027-59744988*5401 电话0871-63118338*7001 赛默飞世尔科技在全国有共21个办事处。本资料中的信息、说明和技术指标如有变更,恕不另行通知。 本文在其他条件相同的情况下,比较了在 APCI 和 ESI 模 式下 MS 检测六种 oxy-PAH 标准化合物(图 1)的性能。 化合物的分离使用专用色谱柱,该色谱柱可以对被测试化 合物以及紫外色谱图中可见的一些杂质达到基线分离(分 离度 > 2),这些杂质可能是合成时产生的。
确定






































还剩83页未读,是否继续阅读?
赛默飞色谱与质谱为您提供《环境中氧化多环芳烃检测方案(气质联用仪)》,该方案主要用于环境水(除海水)中有机污染物检测,参考标准--,《环境中氧化多环芳烃检测方案(气质联用仪)》用到的仪器有赛默飞ISQ™ 7000单四极杆GC-MS
推荐专场
相关方案
更多
该厂商其他方案
更多
















