推荐厂家
暂无
暂无




 400-629-8889
400-629-8889
 留言咨询
留言咨询

 400-886-5615
400-886-5615
 留言咨询
留言咨询

 400-805-0826
400-805-0826
 留言咨询
留言咨询



药物MTT实验步骤(贴壁细胞)----个人改进版by sssholy (2012-10-22) 1. 边缘孔用无菌PBS充填。收集对数期细胞,调整细胞悬液浓度为50000个/ml,每孔加入100ul细胞悬液(每孔5000个细胞)。注:⑴每次加入细胞都使枪头贴着孔底边缘(最好相同位置),缓慢加入100ul细胞悬液。孔加入顺序:可从上到下,从左到右依次加入。⑵为了保证细胞密度均匀,最好每加3-5列细胞混匀一下细胞悬液,避免因重力沉降导致细胞密度不均。⑶每块96孔板加完细胞后,应拿起板子前后左右水平摇晃几下(勿旋转摇晃),使细胞均匀分散。⑷一般设6个复孔(B-G行),对照孔非常重要,且变异大,故设2列(2,3列为对照孔),4-10或4-11列为给药孔。⑸边缘孔用无菌PBS充填, 2-11列均可加入细胞。因为要设置调零孔(即不加细胞孔),所以可将第11列设为调零孔,也可将第12列的无菌PBS孔在第2天加药时改为调零孔。2. 细胞放入培养箱培养,待贴壁后第二天给药(通常前一天下午或晚上铺板,第2天上午给药)。给药方法:先配好药(用EP管配好药),再拿出96孔板,弃去原有培养液(可不用PBS洗,太麻烦了),加入药物。注:⑴MTT加药时都是先配药再弃去原培养液,最后加入药物。切勿先弃去原有培养液再配药,因为配药一般要花较长时间,若先弃去培养液再配药会导致细胞无营养液体而死亡。⑵药物是用母液溶于无血清培养基配成工作液,事先算好对照孔,药物孔,调零孔如何配制,如何设置加药顺序。一般越靠中央的孔变异越小,故最重要的给药孔一般放在最中间,次要孔放边缘,调零孔可用第11或12列。⑶如果某个给药孔需加入2种药物,一般需要一种药物先预处理1-2h(预处理药物可用Ep管配好后再分别加入各孔),1-2h再加入另一种药物(直接加入各孔)。3.细胞放入培养箱培养24h(或其他指定时间)。4. 药物作用结束后,每孔加入20ul---MTT(5mg/ml),培养3-4h。若药物能与MTT反应,可先弃去原培养液,再加入含MTT的培养液(无血清培养液:MTT=5:1配制)。注:MTT使用前预先解冻。MTT对光敏感,故一般保存于负20℃,配好5mg/mlMTT后我习惯分装于EP管中。5.终止培养,小心吸去孔内培养液。每孔加入150ul---DMSO(DMSO可预先算好所需体积加入15ml离心管中),37℃温箱孵育10分钟或摇床低速振荡10分钟。之后用酶标仪检测OD—490nm(也有测570nm的)各孔的吸光度(A)值。6.同时设置调零孔(无血清培养基, MTT, DMSO),对照孔(细胞,最大浓度的药物溶解介质,无血清培养基, MTT, DMSO)。7.细胞活力(cell viability):细胞活力(cell viability of control)=(药物组A值-调零孔A值)/(对照孔A值-调零孔A值)*100%0 http://img.dxycdn.com/upload/2012/10/22/48/88256443.snap.jpg药物MTT实验步骤----原版:0 http://img.dxycdn.com/upload/2012/10/22/45/66035574.snap.jpg

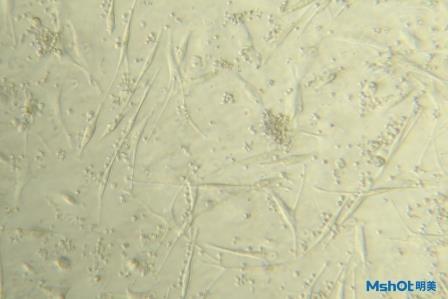
293T/17(人胚肾细胞)293T/17(人胚肾细胞)培养条件:DMEM(PM150210)+10% FBS (164210-500)+1% P/S (PB180120)由衷地感谢您对我们公司的信任与支持! [img=,557,423]http://ng1.17img.cn/bbsfiles/images/2017/07/201707311556_01_3250905_3.png[/img]注意事项:1、首先,观察细胞培养瓶是否完好,培养液是否有漏液、浑浊等现象。若有,请拍照,并及时与技术支持联系(所拍照片将作为后续服务依据)。2、用75%酒精擦拭细胞培养瓶表面,显微镜下观察细胞状态。因运输问题,部分贴壁细胞会有少量从瓶壁脱落;先不要打开培养瓶盖,将细胞置于细胞培养箱内静置培养2-4小时,以便稳定细胞状态。3、仔细阅读细胞说明书,了解细胞相关信息,如贴壁特性(贴壁/悬浮)、细胞形态、所用基础培养基、血清比例、所需细胞因子、传代比例、换液频率等。4、静置完成后,取出细胞培养瓶,镜检、拍照,记录细胞状态(所拍照片将作为后续服务依据);建议细胞传代培养后,定期拍照、记录细胞生长状态。5、贴壁细胞:若细胞生长密度超过80%,可正常传代;若未超过80%,移除细胞培养瓶内培养基,预留5ml左右继续培养,直至细胞密度达80%左右再进行传代操作,瓶盖可稍微拧松。6、悬浮细胞:将细胞培养瓶内液体全部转移至50ml无菌离心管内,1200rpm离心5min,离心后上清培养基可收集备用,管底细胞沉淀加入5ml培养基吹打、重悬。镜检时,若细胞密度超过80%,可将细胞悬液分至2个细胞培养瓶内培养,补加培养基至5ml;若细胞密度未超过80%,将细胞悬液移至原瓶继续培养,直至细胞密度达80%左右时再进行传代操作。 [img=,557,425]http://ng1.17img.cn/bbsfiles/images/2017/07/201707311556_02_3250905_3.png[/img]温馨提醒:1、可将培养瓶内多余的培养基转移至50ml无菌离心管中,备用;细胞首次传代时,可以将该培养基按照一定比例和客户自备的培养基混合使用,让细胞逐渐适应培养条件。2、确认细胞状态良好后,应及时将部分细胞冻存,再进行后续的实验,避免后期实验失误可能发生细胞污染或死亡而导致的细胞丢失,影响后续实验。3、建议客户收到细胞后前3天,100X、200X、400X各拍3张细胞照片,记录细胞状态,便于后续和技术支持沟通交流。 更多咨询中国微生物菌种查询网 网址:www.biobw.org
大家还记得我吗?好久好久没有来发帖了,肯定都快被遗忘了。一直在忙着养细胞,这次过来给大家分享一些自己的心得体会。↓↓↓养了很久的细胞,有一些经验和体会总结一下,和大家分享一下。关于如何把细胞养的形态很好更漂亮。1.不同的细胞,喜欢的环境是不一样的。这个不仅仅是说培养基的不同,还有就是细胞生长的空间密度问题。有一些细胞是数量多一点比较好生长,生长状态也比较好。这种一般是属于生长速度慢的细胞。譬如内皮细胞。而有一些是细胞是数量少一点细胞状态会生长的比较好,譬如巨噬细胞和某些肿瘤细胞。尤其是巨噬细胞,生长速度非常得快,贴壁速度很快,所以传代时就应该留很少量的细胞,这样细胞状态会比较好。并且巨噬细胞比较喜欢扎堆生长,而堆与堆之间是有空间的。如果长成相连在一起的一满片的时候,细胞形态基本上就会差了,老化的会比较多,对后期实验结果是不好的。所以在养细胞的时候应该摸索该细胞喜欢的生长空间密度问题。2.对于有些人总是会遇到养的细胞形态怎么都不好的问题。这个其实是有一个方法可以改善的。对于贴壁细胞,如果细胞形态不好,(或者细胞形态不清晰,表面似有异物等)可以在传代的时候进行如下操作:首先,倒掉旧的培养基,加入3ml新的培养基(有无血清的都可)洗涤一次,用滴管吸走,然后再加入3ml的培养基,进行预吹打,控制吹打力度,轻轻地大概沿着瓶底过一遍,然后吸走。这时侯再开始正式的消化、吹打。(巨噬细胞我们只吹打,不消化的)其次,把吹打下来的细胞悬液加入到新的培养瓶内,培养瓶事先加入培养基,放入培养箱内培养,按时间点观察细胞贴壁情况。10分钟观察一次,20分钟,30分钟观察一次。选择一个时间点,已经有部分细胞贴壁的情况下,重新置于洁净台,底面朝上迅速倒出其中的培养基,加入3ml新培养基再轻轻洗一次。然后加入完全培养基培养。后续观察细胞生长情况以及形态。我称之为“二传”。呵呵。如果一次效果还不理想,可重复多次。直到找到细胞完美形态。其中要注意,结合细胞喜欢的生长情况。喜欢多一点数量长得好的细胞你就等贴壁细胞比较多点的时候再传。反之亦然。这个是我师兄发明的,谢谢他了。这个方法真的很好用!3.关于培养瓶内加入培养基的量的问题。这个是要靠自己去摸索你所养的细胞的。并不是小的玻璃方瓶12ml,大方瓶14ml的。有些细胞反而是培养基少一点相反细胞形态会长得比较好。(可能也是竞争很大,有优胜劣汰吧。呵呵。)对于生长速度快的细胞,易生长的细胞加少一点培养基细胞形态会更好。但是要注意换液掌握。4.关于选择培养瓶的问题。个人发现生长速度快的细胞在玻璃瓶内生长的状态会比一次性塑料瓶相对好一些。而对于同一种细胞,在其生长旺盛快速的时期在玻璃瓶内的生长状态也比塑料瓶内好。这可能是因为塑料瓶比玻璃瓶更容易贴壁。生长速度快的细胞在塑料瓶这种相对“更安逸”的环境里反而长得状态不如玻璃瓶好。所以对于生长速度慢的细胞如果想要更漂亮的细胞状态,塑料瓶比玻璃瓶会好,对于生长速度慢的细胞,玻璃瓶则会更好。同样,对于同一种细胞,在其生长速度慢的时候,塑料瓶会好一点,比如刚刚复苏的时候,或者原代培养的时候。而在其生长旺盛的时候,玻璃瓶则相对会好一点。今天就先分享到这里吧,等下次有时间来逛帖的时候再来分享。大家一定要注意:要想把细胞养的漂亮,一定要保持实验室干净整洁。至于怎么保持,方法很重要,更重要的是要有责任心。方法的话,可能每个人都会有自己的一套方法,不过能走捷径的还是可以走的。像我们实验室,现在很多都是利用软件来管理的。还记得之前给你们推荐的那款软件吗?我们实验室现在还在用,倒是真的蛮好用的,至少大家做实验的时候不会再乱堆乱放了(因为有领用记录)可能新朋友不知道,或者没有看过我上篇帖子的人不了解,如果相信我的推荐,可以看下我上一篇帖,谢谢,希望能帮到大家!差点忘了,那款软件更新成了iLab,不叫Mr.F了。其他不多说,省得被当成打广告的!