







热爱生命科学


荧光显微成像技术对人们理解神经科学起了非常关键的作用。而最近一些年出现的各种超分辨显微成像技术和专门的荧光探针能够以超过以往普通光学显微镜的分辨率直接观察神经元亚细胞结构和蛋白质排列。并以直观可视方式揭示了神经细胞骨架组成、分布、运动和膜蛋白信号传导、突触下结构和功能,以及神经元−胶质细胞相互作用。同时超高分辨显微成像技术(Super Resolution,SR,下文中出现SR均指超高分辨率显微成像技术)对于许多自身免疫和神经退行性疾病模型中的分子靶点研究也提供了全新的强大工具。
今年春,Werner等科学家在美国化学学会会刊(ACS)上最新发表了一篇综述,比较详实系统介绍了超高分辨率显微技术在神经科学上的最新应用进展。我们在此文基础上进行了编译整理。因文章较长,我们将分三期陆续介绍。本期接着上期的第一部分超高分辨率显微技术在神经科学中的应用(一) ,为第二部分内容。
4.荧光标记与样品制备
4.1. 荧光标记
神经元和脑片的超分辨率成像是用适当的荧光团标记感兴趣的生物分子,理想情况下是以定量和化学计量的方式。虽然SIM和其他超分辨方法的成像质量取决于信号背景(S/B)比,但SIM对荧光团没有特殊要求。另一方面,STED显微镜可达到的分辨率在很大程度上取决于所用荧光团的光稳定性。RESOLFT显微镜使用可逆光开关FPs,具有两个稳定状态,因此可以使用较低的激光照射强度。所有SMLM方法的定位精度取决于每个事件检测到的光子数。dSTORM需要光开关有机荧光团,包括菁、罗丹明和恶嗪染;而PALM则需要使用光开关、光转换和光激活FPs。与此相反,DNA-PAINT理论上适用于所有荧光团,因为开/关速率由对接链和成像链序列和缓冲条件决定,而其中 Cy3B和ATTO 643效果最好。、为了获得一张好的超分辨率图像,除了成像方法以外,样品制备也非常关键。使用荧光探针进行高效和特异的标记,并且使标记误差(荧光团和目标之间的距离)达到最小。为了通过荧光成像进行结构解析,标记密度(即荧光探针之间的距离)必须显著高于所需的分辨率。另一方面,特别是对于接近几乎分子分辨率的超分辨率成像方法,标记误差必须尽可能小,以达到高精度成像。
对于活细胞标记而言,在合适的表达载体中融合感兴趣的蛋白质的基因编码FPs无疑成为首选。然而,FPs的亮度较低,与有机染料相比,其图像分辨率较低。理想的标记方法是使用荧光染料标记基因编码的蛋白质、肽标签或单一氨基酸。
在模式生物如果蝇或秀丽隐杆线虫的应用得益于基因编码工具,通过转座子、操纵二分体Gal4/UAS表达系统或Crispr/Cas9方法引入或去除突触蛋白和荧光蛋白。由于瞬时转染的细胞表现出不同的蛋白质表达水平,蛋白质的分布和功能不一定反映野生型的情况。
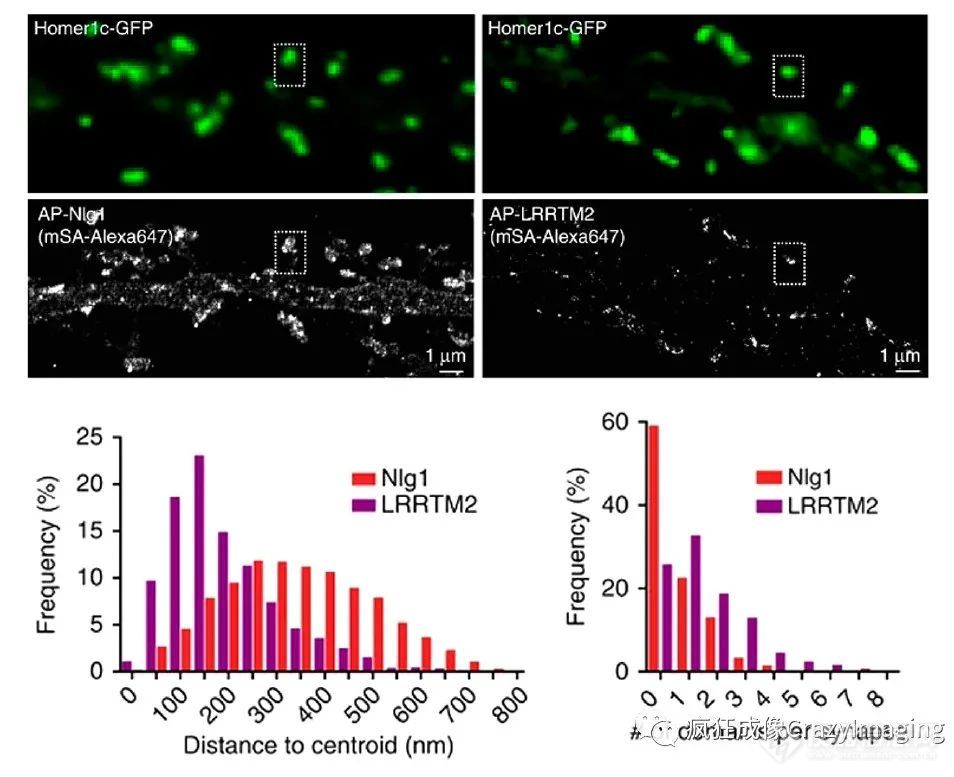
图5 通过单体链霉亲和素结合AP标记的突触蛋白成像结果显示Nlg1和LRRTM2的差异分布(dSTORM成像)。上排:Homer 1c GFP作为突触后室的参考。第二排:Nlg1和LRRTM2(dSTORM成像)。左下:频率分布直方图,用于显示相对于Homer 1位置中心的信号分散情况。右下:列出比较两种蛋白质的突触结构域数量的直方图。
然而,通过构建优化表达,稳定表达的细胞或CRISPR基因敲入等方法可以产生从内源性到强过表达的蛋白质表达水平。根据不同的转染策略,可以采用不同的方法转染神经元。传统的磷酸钙共沉淀法和脂质体法在大多数实验室都可实施,但这两种技术的转染效率很低。而病毒转染的效率比较高,允许注射到大脑区域,但需要实验者具备病毒生产方面的专业知识,并需要考虑生物安全问题。此外,还必须考虑病毒类型、插入片段大小、毒性和差异表达等因素。
要达到高转染效率,可以使用高压脉冲将核酸直接输送到细胞核,进行核转染。然而其缺点是,当这种方法应用于小鼠原代神经元时,会导致细胞存活率较低,并且实验设备昂贵,还需要根据神经元密度和物种对脉冲参数进行多次测试。另外,也可以使用细胞附着式高电阻管,在完整神经元网络(如器官型切片)中进行单细胞电穿孔。利用这种方式,结合CRISPR基因敲入获得了接近内源性的蛋白质表达水平。基于CRISPR基因敲入,在神经元发育的不同时间点通过脂质感染、核感染或病毒转染在神经元中实现。
如前所述,FPs光稳定性和荧光光子输出较低,这降低了图像质量。另外,连接大小为2−5nm的FP后,蛋白质功能可能会受到影响。因此,首先必须清楚感兴趣的蛋白质在野生型的功能表现。而有机染料比FPs小得多,有更高的光子产率和光稳定性,但需要与其它能与感兴趣分子结合的分子进行连接耦合。对于固定细胞,使用一抗和二抗进行免疫染色仍然是标记内源性蛋白质的首选方法。缺点是由两个大小17.5 nm左右的IG抗体间接免疫标记有可能导致标记误差。使用直接法免疫荧光或Fab片段可以减少标记误差。另外针对GFP或转基因短肽标签的更小(1.5×2.5 nm)的骆驼“纳米抗体”已应用于dSTORM成像。
此外,耦合了链霉亲和素的荧光染料可用于神经元和器官型组织中靶蛋白的特异性标记。使用这种标记方法,研究了神经氨酸酶-1ß、神经肽原-1和富含亮氨酸的重复跨膜蛋白2的动力学和纳米级结构,并揭示了跨突触粘附结构的形成(图5)。
另外可以使用生物正交肽或自标记蛋白质标签,例如FlAsH tags, SNAP-tags, and Halo-tags。这些标签蛋白与目标蛋白共表达,并以共价和特异性结合其各自的荧光标记试剂或配体。对于肌动蛋白和微管的标记,可以使用小肽药物,如双环七肽-鬼笔环肽和紫杉烷类药物,如紫杉醇。膜和细胞器的标记可以通过荧光脂质和细胞器的追踪试剂来实现。此外,小肽或配体可以直接用荧光团标记,并特异性结合生物分子,例如,显示抑制性突触后位点的超结合肽。要达到最小的标记误差,可以通过单个非天然氨基酸的特定位点标记实现。通过基因编码导入设计的非天然氨基酸,并用四嗪染料进行生物正交点击化学标记。
显然,神经元和组织切片必须根据要成像的结构进行透膜和固定。与所使用的标记方法无关,特别注意所用的试剂必须能保留自然细胞环境中生物分子的超微结构。通过化学试剂固定交联蛋白质,可能会影响结合亲和力,也可能削弱分子间的相互作用。在大多数情况下,多聚甲醛(PFA)和戊二醛已成功用于神经科学的超分辨率成像。此外,还引入了乙二醛等新型固定剂。膜分子应始终使用4%的PFA和0.2%戊二醛固定,以尽量减少残余流动性并避免伪影,例如抗体结合诱导的簇形成。
4.2. 神经元的多色遗传标记
荧光蛋白彻底改变了神经元的活细胞成像方式,因为荧光蛋白可以与感兴趣的蛋白质融合,并且在假定不影响野生型功能的前提下,用于双色和三色成像。神经系统具有非常高密度的轴突和树突相互作用结构,需要使用更多不同颜色的标记来区分不同的神经元连接。
2007年,随着一种名为Brainbow的转基因方案的开发,这一问题得到了解决,该策略能够对神经元进行多色标记。结合单细胞分辨率成像技术,Brainbow技术可以用来创建大脑图谱,详细描述神经元如何形成回路,其连接体以及它们投射到何处。Brainbow利用了三原色,即可见光谱的所有颜色都可以由三种原色的不同混合物生成,即红色、绿色、蓝色(RGB)或转化为荧光蛋白,例如RFP、YFP和CFP。为了实现这一想法,应用了Cre/lox重组系统,该系统可以通过DNA切除、反转或染色体重组启动基因表达,使三个荧光蛋白基因中的一个在转基因中随机表达。转基因盒的多个拷贝的引入导致三个不同拷贝数的基因在每个细胞中组合表达,从而产生几十种颜色,使相邻神经元分化并观察其相互作用。Brainbow技术非常适合绘制不同神经元类型之间的连接模式,追踪轴突,并识别大脑中远距离的神经元连接。此外,已经证明Brainbow表达可以成功地用于研究周围神经损伤后的轴突再生,并检测大脑发育过程中的重要阶段。
为了进一步改进Brainbow在包括突触蛋白在内的大脑和连接图谱中的应用,SRM的应用是显而易见的。最近通过结合Brainbow、顺序免疫染色和ExM同时研究同一脑切片上的形态、分子标记和连接,成功地证明了这一点(图6)。将这项技术应用到全脑研究一直是一个挑战,直到最近才成功应用。
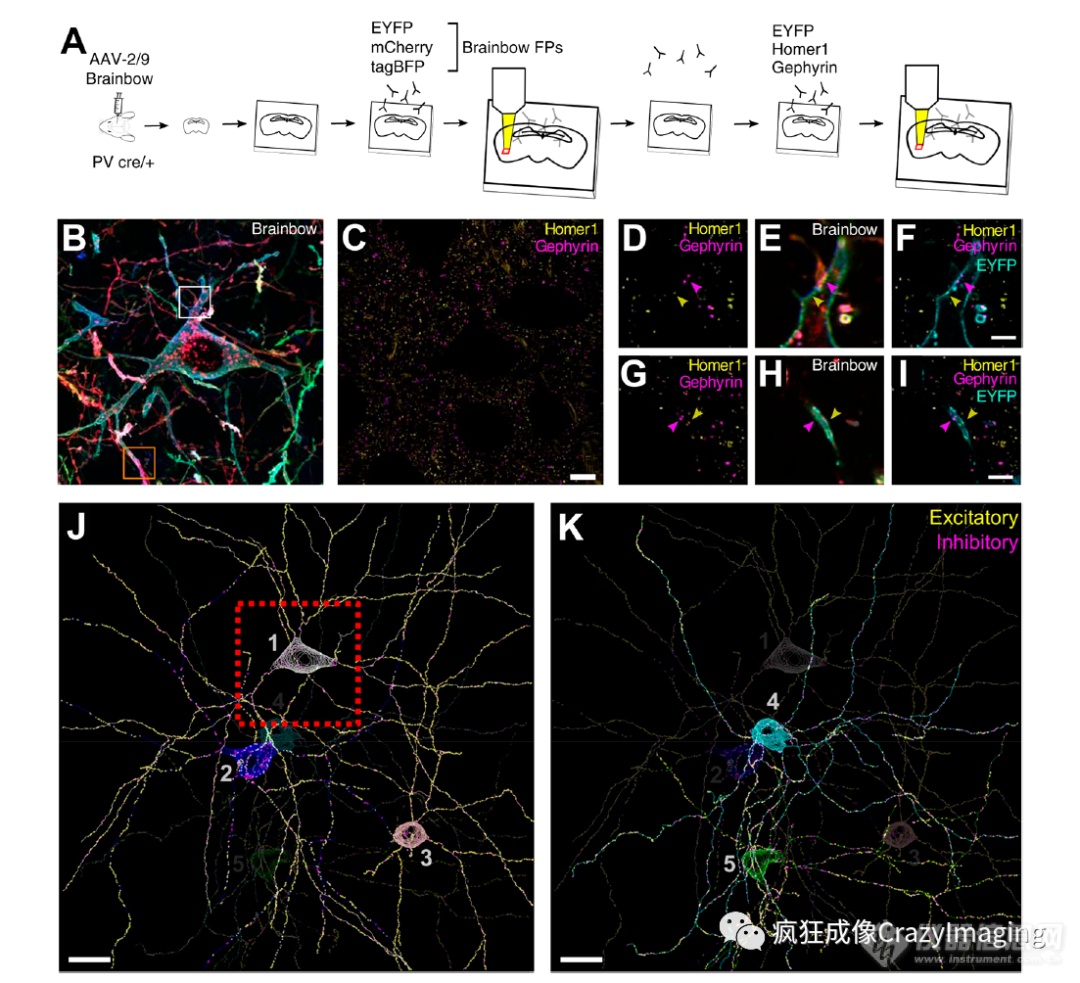
图6 结合Brainbow和ExM的多轮免疫染色和ExM(miriEx)成像。(A) 实验方案:在Parvalbumin cre/+ 小鼠的脑切片中,Parvalbumin蛋白阳性中间神经元通过Brainbow进行观察,并在下一轮应用4倍ExM成像。使用EYFP信号对Homer1和Gephyrin进行免疫染色来观察突触。(B) Brainbow 信号的免疫染色。(C) 分别通过突触后标记homer1和Gephyrin的免疫染色来区分抑制性和兴奋性突触。
插图(D)−(F)和(G)−(I) 显示图像的更多细节图。(J)和(K)神经元的形态重建(使用ImageJ软件插件nTracer),包括其各自传入的特征。虚线框表示(B)和(C)中所示的区域。重建的神经元按顺序编号。标尺(膨胀前的):10μm(B/C)、2.5μm(I)、20μm(J/K)。
4.3. 神经科学中的光电联合显微镜
电子显微镜(EM)和电子断层扫描具有光学显微镜无法达到的空间分辨率,可以获得细胞和细胞器的超微结构信息。然而,EM和电子断层扫描不能标记特定的分子,因此难以识别未知的细胞结构或具有相似形态特征的结构。用胶体金标记结合抗体可以实现蛋白质的纳米级定位,但抗原的标记效率低下,这意味着胶体金颗粒的数量仅占抗原总数量的1%到20%。
而另一方面,荧光显微镜虽然分辨率较低,但可以进行大视场成像和对活细胞中蛋白质进行定位。对固定样本细胞中的各种分子进行高效和特异的分子标记后,结合超分辨率荧光显微镜方法,达到的空间分辨率可以远低于衍射极限。
因此,光电联合显微镜(CLEM)作为一种通用的方法,在电子显微镜提供的细胞超微结构背景下,通过超分辨率成像来可视化蛋白质的定位和相互作用。然而,将超分辨率成像与EM结合起来更为困难,因为乍一看,这主要是由于两种方法的样品制备流程不同且不兼容。例如,EM中保存超微结构所需的固定和染色会引入很强的自发荧光。而且荧光蛋白还会在固定和聚合物包埋所需的脱水和氧化条件下淬灭。此外,这两幅图像必须在纳米精度下精确叠加,首先需要使用在荧光成像和EM中都表现出极好的对比度的固定对准标记物,如裸金微球。
另外,样品脱水引起的结构变形会严重破坏两幅图像的正确叠加。所以必须在超微结构和荧光保存之间找到折衷方案。例如,已经证明,对于某些周期性分子结构,如核孔复合体,无需使用对准标记,dSTORM和EM扫描图像可以以<20 nm的精度叠加。
光电联合显微镜的流程是先对轴突和树突进行荧光实时成像后,再使用透射电镜观察。例如,表达GFP的脑组织在荧光成像后进行化学固定,再使用电子密度标记进行免疫标记,例如EM金。或者采用更成熟的方法,如过氧化物酶或胶体金标记。最后,可以通过光转化在荧光团处局部生成二氨基联苯胺(DAB)聚合物。
为了克服标记问题并确保超微结构的保存,已经开发了用于EM (NATIVE)的纳米体辅助组织免疫染色。NATIVE能够高效标记蛋白质,无需苛刻的渗透步骤、特殊树脂、锇替代物或透明化试剂。随着方法的改进和技术的发展,光电联合显微镜已被证明是研究不同种类突触和定位突触蛋白的理想选择。
5.超分辨显微镜观察神经元隔室/突触以及神经元−胶质细胞相互作用
下面我们将展示通过超高技术获得的有关细胞骨架组成和动力学、突触前室和突触后室对神经传递准确性至关重要的分子组装,以及形成神经元功能的星形细胞结构的调节和构建的最新数据。
5.1. 细胞骨架
神经元的极化性质以及树突和轴突的长度都需要结构和功能性支架来支持它们的稳定性、适应可塑性和物质运输,这些特性对神经元的存活和信号传递是必不可少的。因此,神经细胞骨架的结构在过去几十年中引起了神经科学家的注意,并在其它文献中进行了详细的回顾。20世纪70年代的电镜研究表明,神经细胞骨架由三种主要类型的神经纤维组成:大小约为20−30 nm的微管,直径为10 nm的神经纤维和5−10 nm大小的肌动蛋白丝。微管是由异二聚体在GTP依赖性组装过程中结合α和β微管蛋白单体组装而成的圆柱体,称为原丝,再由13个这样的原丝形成一个微管单元。轴突的微管成束状组织,并根据其相对于神经元胞体的位置显示不同的方向。它们的极化通过快速增长的正端和缓慢增长的负端体现。
STED显微镜揭示了快速生长极依赖钙锚定在肌动蛋白皮质上。使用dSTORM对发育中的神经元进行活细胞成像证明了神经元极性和轴突具有方向一致的、平行的由TRIM46驱动的微管束,而树突微管的特征是混合极性。用Motor-PAINT方法进行纳米跟踪发现稳定和乙酰化的微管显示负端向外的方向,而动态和酪氨酸酶化的微管则显示相反的方向(图7)。例如轴突起始节中微管密集地聚集在束簇中,由于密集的重叠定位,使用SMLM方法具有挑战性。这个问题可以通过两种实验方法来解决:第一,设计更小的标记探针,如微管蛋白纳米抗体,这不需对神经元微管更详细的观察。第二,一种降低群聚密度的超分辨率方法,如ExM,可用于胞体和树突中微管亚群的可视化。
神经纤维是在轴突中形成的广泛平行网络的异质聚合物,它为轴突提供稳定性并调节轴突直径和传导速度,其组成包括低、中、高分子量神经纤维、中间蛋白和外周蛋白的三联体。它们的自组装首先形成平行的异二聚体,然后半交错地结合成反平行的四聚体。最后,八个四聚体横向聚集成单位长度的神经纤维,进一步拉长并径向压缩至最终的神经纤维外观。用电镜观察到在神经纤维之间的交界面,形成3−5 nm大小的交叉桥,但对其功能及其与神经纤维的分子相互作用仍不清楚。在这里,ExM与SMLM的结合或DNA-PAINT的应用可能有助于研究密集神经纤维中的这种相互作用。神经纤维动力学已经通过光转换和光活化SRM实验进行了研究,显示了端到端蛋白合成中的退火和切断过程。
肌动蛋白最初被认为与一组更集中的短肌动蛋白丝结合在一起,在轴浆中形成斑点状的膜下层。在原代神经元和脑切片中使用phalloidin Alexa Fluor 647进行STORM成像,揭示了轴突肌动蛋白的新的组成原理。这些实验揭示了轴突中存在圆周式肌动蛋白环,每190 nm固定重复间隔绕一圈,并进一步表征了轴突中具有类似尺寸的ßII血影蛋白和钠通道的周期性条带,而树突状腔室内显示出更细长的肌动蛋白组织。此外,通过STORM成像发现,并通过STED显微镜的研究得到证实,这种肌动蛋白组织模式的普遍性也存在于树突中。进一步的报告发现,尽管树突中也存在基于肌动蛋白血影蛋白的周期性膜骨架,树突中这种结构的形成倾向和发育速度低于轴突。此外,本文还显示了肌动蛋白和血影蛋白在胞体和部分树突中的二维多边形晶格结构,类似于红细胞中的膜骨架结构。此外,使用SiR-actin,可通过STED显微镜在活的原代神经元中观察到这种周期性结构。最后,最近的CLEM方法结合铂金复原电镜(PREM)和STORM研究了无顶轴突中的肌动蛋白组织,并提供了轴突编织状肌动蛋白结构与周期性肌动蛋白超微结构相关的证据(图8)。
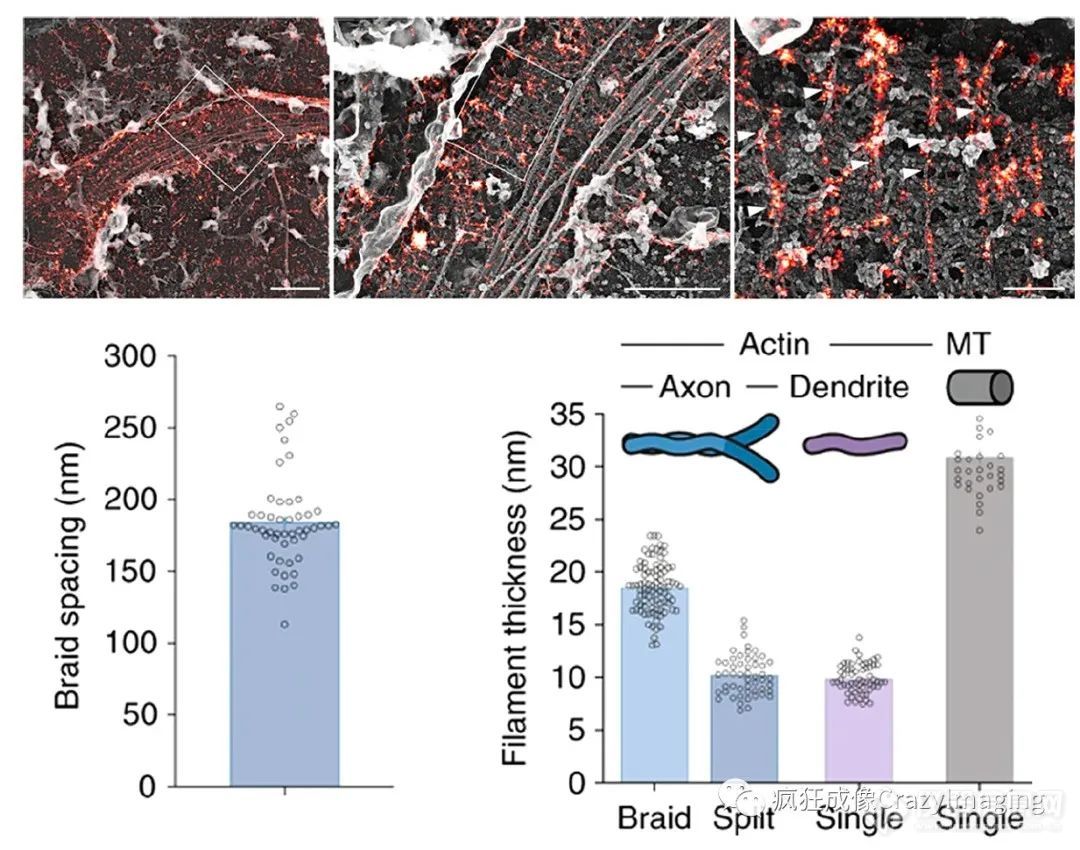
图8。原代神经元无顶轴突(unroofed axons)的CLEM成像(结合铂复型电子显微镜和STORM的光电联合成像)。用铂复型电镜(PREM)(灰色)显示的轴突辫状条带(箭头)被叠加到大鼠原代神经元的超分辨肌动蛋白环(伪彩)上,比例尺=2, 1, 0.2μm(从左到右)。中间:轴突辫状条带间距测量后显示出与周期肌动蛋白间距相似的尺寸。右图:在铂复型电镜(PREM)中记录的神经纤维厚度,未分裂(交织在一起)和分裂(分裂开)的轴突肌动蛋白辫状条带为蓝色,树突中的单个肌动蛋白神经纤维为紫色,微管为灰色参考。采用平均值和标准误显示数据。Copyright 2019 Springer Nature.
ßII 血影蛋白基因敲除导致周期性肌动蛋白环结构破坏,同时细胞器的双向轴突运输受损。SMLM结果显示,与轴突相比,轴突起始节中的分子组织其特征是轴突起始节(AIS)蛋白ankyrin-G和ßIV-血影蛋白,这种基于肌动蛋白-血影蛋白的细胞骨架与远端轴突相似。此外,在AIS中存在ßIV-血影蛋白和Ankyrin G,而在远端轴突中存在ßi--血影蛋白和Ankyrin B。SMLM显示与肌动蛋白环相连的纵向头对头ßIV血影蛋白和Ankyrin的二价取向有助于建立紧凑的AIS超微结构,该超微结构甚至对针对肌动蛋白和微管的药物治疗具有抵抗力。进一步显示Ankyrin-G会聚集到亚结构域,增强神经元活性,而成为精神疾病的主要风险基因。随后的SMLM研究还阐明了αII血影蛋白与ßIV血影蛋白共同在AIS提供强健的周期性细胞骨架组织以及防止AIS装配不完全和神经变性的重要性。一份相关报告显示,αII 血影蛋白丰度随有髓鞘轴突直径的增加而增加,表明大直径轴突更容易发生神经退行性病变。在免疫标记II血影蛋白后,将其连接到一种可膨胀的聚合物,并在水中膨胀后,通过ExM研究ßII spectrin沿轴突的周期性模式。这一新方法证实了如前所述的细胞骨架内部的组织原理。
不幸的是,在ExM过程中,phalloidin探针在膨胀过程中被冲掉。有两种策略解决这一问题:一方面,携带甲基丙烯酸基团的phalloidin三功能抗体被设计用于与凝胶的有效标记;另一方面,最近的一份报告使用荧光团结合抗体,类似于常规免疫染色,将荧光团靶向phalloidin探针与凝胶连接。在中枢神经系统的几种神经细胞类型和动物物种中,肌动蛋白和附属蛋白的强大超微结构组织也得到了证实。外周神经系统(PNS)中,STED显微镜也显示在梳理的神经纤维样本上有重复的细胞骨架成分。最后,SMLM揭示了肌动蛋白-血影蛋白骨架的一个重要生物学功能:它可以作为一个信号平台,通过组织跨膜信号蛋白,包括G蛋白偶联受体(GPCR)、细胞粘附分子(CAM)和受体酪氨酸激酶(RTK),在神经元中进行信号转导从而实现GPCR-和CAM介导的RTK信号。
5.2. 突触前室
为了确保有效的神经化学传递,突触前膨大参与突触囊泡循环、神经递质填充以及与突触前膜在活性区(特殊蛋白质密集分布的纳米隔室)的融合,以最终释放神经递质。在这里,我们关注SRM如何扩展我们对突触前功能的理解。
早期只能使用EM对化学固定神经元里的小直径突触小泡进行研究,但随着SRM的出现,应用快速STED显微镜,通过免疫标记位于突触前室突触小泡上的钙传感器突触标记蛋白1(SYT1)来观察突触小泡的活动。STED显微镜进一步显示,突触小泡融合后Syt1分子似乎驻留在突触膜上,也支持胞吐后突触小泡蛋白的清除过程。此外,在突触小泡融合过程中,当暴露于细胞外空间时,靶向Synaptobevin 2 pHluorin的荧光团结合纳米体后,亚衍射追踪显示了突触小泡的异质性迁移。一种类似的方法使用vGlut1 pHluorin在原代神经元中的表达来观察单个神经元突触小泡,定位精度为27 nm,并揭示了突触小泡的多个不同释放位点。作为一项方法学的进步,为了对主动循环的小泡成像,设计了一种名为mCLING的亲脂膜探针,该探针可对突触膜进行染色,通过内吞作用和固定,可以进行免疫标记,且和SRM相结合。
突触小泡的胞吐过程需要一组属于突触前细胞基质的突触前蛋白质的高度可靠的相互作用,使突触小泡接近和暂时驻留在所谓活动区的膜上,并最终释放突触小泡。黑腹果蝇易于遗传,有助于精确定位果蝇幼虫神经肌肉接头(NMJ)活动区的第一个重要蛋白质。Bruchpilot(Brp)是一种必不可少的活性区成分,是一种大的、卷曲的螺旋蛋白,对于钙通道聚集和突触囊泡定位到突触释放位点至关重要。除了通过Brp研究钙通道聚集外,STED显微镜还证明了该蛋白细长的组织结构,并揭示了与Brp相互作用的蛋白(如syd-1α、liprin和rim结合蛋白(RBP))的定位。定量dSTORM方法研究了果蝇活动区Brp丝的数量,并显示了Brp的结构组织与其功能之间的强相关性。接下来的研究通过dSTORM评估Syt1敲除后的活动区(CAZ)电生理学和细胞基质参数。这项研究表明,在果蝇NMJs 1b型突触膨胀中,Syt1基因的敲除导致更高的Brp计数和簇内Brp图谱的改变。
在哺乳动物突触中,突触前支架蛋白bassoon 和 piccolo参与突触囊泡释放的调节。据报道,bassoon蛋白通过与RBP的相互作用来控制CaV2.1型钙通道的定位。此外bassoon蛋白能加速囊泡释放,因为其丢失导致小脑苔藓纤维到颗粒细胞突触中的突触囊泡数量显著减少和突触抑制。STED显微镜显示bassoon 和 piccolo蛋白是一个夹心三明治结构,两侧为piccolo蛋白,bassoon蛋白居中。STORM成像通过距离测量显示bassoon蛋白相对于突触前和突触后室中其他相关突触蛋白质的方向。囊泡胞吐过程由一组可溶性ethylmaleimide敏感因子附着受体(SNARE)蛋白质进一步协调。位于突触膜上的囊泡SNAREs (v-SNAREs) 蛋白和 t-SNARES蛋白的复杂形成导致突触囊泡成功融合。在质膜上的突触体相关蛋白25(SNAP-25)和突触融合蛋白聚集首先通过STED显微镜进行研究。这项研究表明,大约75个突触融合蛋白分子被堆积成50- 60 nm大小的纳米团簇。
在之后的研究中,SMLM以更高的精度对SNAP-25和突触融合蛋白的分布进行成像。在这里,描述了Syntaxin簇内的分子密度梯度。dSTORM成像显示,未聚集的分子紧密地定位于聚集区域。最近的一项研究显示了一种以syntaxin或SNAP-25为靶点的纳米抗体。这使密集的突触前区域更好的标记,并显示突触外突触融合蛋白可在增强突触活动后进入突触室。SNARE结合蛋白tomosyn被证明定位于突触融合蛋白簇,据报道,其ß-螺旋结构域的突变是SNAP-25复合物形成的关键。此外,tomosyn与v-SNARE突触结合蛋白竞争,与突触融合蛋白和SNAP-25形成复合物,因此被认为下调了胞吐过程。
相反,rim结合蛋白2(RBP2)可根据所研究的突触类型在调节突触可塑性方面发挥多种作用。SRM显示RBP2通过调节CaV2.1钙通道相对于释放位点的纳米定位来调节释放概率。此外,STED显微镜显示海马脑片中RBP2对锥体CA3-CA1突触的神经传递只有轻微的影响,它通过控制munc-13-1的定位,在苔藓纤维突触中强烈调节囊泡启动和释放概率。
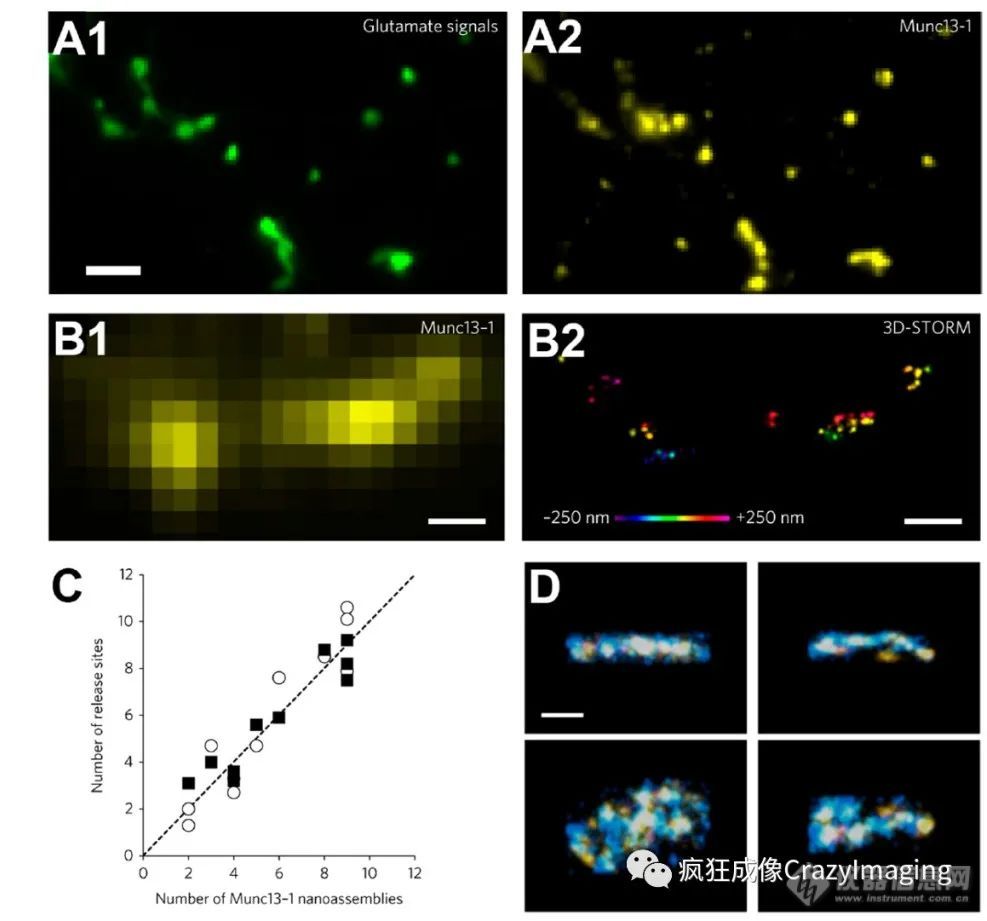
图9。与突触释放位点相关的Munc-13-1纳米组装体。上排:应用高钙溶液和钾通道阻滞剂(A1)以及相应的munc-13-1信号(A2)激活突触后eEOS(增强型谷氨酸光学传感器)的荧光反应图像。注意主动释放条件下的紧密空间相关性。比例尺:5μm。第二行:常规显微镜图像(B1)与munc-13-1(B2)的3D STORM成像。比例尺:500nm。(C) 释放位点数量与munc-13-1纳米团数量的相关性。(D) munc-13-1(黄色)和syntaxin-1A(蓝色)的超分辨双色图像。比例尺:2μm。侧面(顶部)和正面(底部)视图。比例尺:200nm。Copyright 2017 Springer Nature.
Munc-13是unc-13的哺乳动物直系同源物,是引发突触小泡释放的另一个不可或缺的成分。Munc-13-3被证明能够将钙通道募集到活动区,3D-STORM成像提供了证据,证明Munc-13-1聚集在突触释放位点,并与突触融合蛋白分子相关(图9)。通过活体成像和STED显微镜对果蝇中显示不同突触前钙通道距离的两种munc-13亚型进行研究,发现unc-13亚型由CAST/ELK同源物Brp和RIM结合蛋白定位,导致释放部位相对于钙通道的不同超微结构。在神经元发育过程中改变不同Unc-13亚型的比率,通过改变其与钙通道的纳米结构域耦合,导致神经传递增强。Unc-13 A定位通过突变分析表明C末端部分调控释放位点的产生,而蛋白质的N末端部分参与活性区靶向调节。
在活性区内,钙通道的纳米定位和潜在的动力学对于有效调节神经传递至关重要。钙通道和突触小泡之间的纳米域耦合可以是紧密的,也可以是松散的,并以这种方式决定神经传递的精确性。小脑突触中的免疫金电镜定量显示,强突触的耦合距离约为10nm,但其钙通道数量是弱突触的三倍,弱突触的特征是耦合距离较长且低效。一项结合电生理学的免疫金冷冻断裂EM研究提供了证据,证明释放部位随突触前钙通道数量的增加而增加。为了研究电压门控钙通道的活动性,应用单粒子跟踪PALM(sptPALM)对原代神经元成像。研究表明,集中在突触前部位的60%的通道是可变的。此外,通过应用BAPTA钙缓冲降低了钙通道的扩散。结果表明,突触小泡和钙通道之间的纳米域偶联保证了神经传递的精确度,并可根据需要通过突触前钙通道的扩散进行精细调节。
在融合和递质释放后,内吞机制诱导循环产生新的囊泡,从而重建可释放的囊泡池并为持续的神经传递提供基础。囊泡循环的主要机制由网格蛋白介导的内吞作用组成。使用光遗传学和”闪光冷冻”电镜的研究也报道了比超快的内吞快200倍的过程。如双色iso-STED显微镜所示,通过摄取针对囊泡内膜结合位点的Syt 1抗体,将内吞位点定位到活性区外周。此外,在神经内分泌细胞中,STED显微镜也揭示了囊泡只能部分与突触前膜融合释放递质,形成一个“Ω”形状的结构,而没有完全融入膜中,因此有利于“接触后即脱离”(kiss and run)的模式。与网格蛋白介导的内吞作用相比,它会产生更快囊泡再循环率的递质释放模型。依赖于活性的大量内吞作用进一步增加了可能涉及的机制的复杂性,有人提出,根据突触类型和活动,多种内吞模式可能并行运作。
本文由超高显微技术应用工程师郭连峰、黄梓彤编译
[来源:疯狂成像CrazyImaging]

2022.07.12

2024.07.17

超23亿!北京首批医疗设备购置项目公布,涉及CT、DR、基因序列仪等
2024.07.16

3i流式快讯|凯普瑞生物完成数千万Pre-A+轮融资!聚焦流式诊断
2024.07.15

2024.07.15

2024.07.15
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~