如何完成eCTD格式的递交免费网络专题讲座
尊敬的老师,您好! 从2017年5月5日开始,所有递交到美国FDA的新的DMFs以及任何现有的DMFs的补充递交,都必须以eCTD格式进行递交。不少国家和地区正采取全面或部分实现eCTD递交。CFDA发布的《2015年全国药品注册管理工作会议精神》中,也指出要“制定统一的注册申请规范,扩大CTD格式在药品注册申报中的作用,逐步实现药品注册申请的电子递交”。那么如何完成符合各国法规的eCTD格式的递交呢? 创腾科技诚邀您参加免费的网络研讨会“eCTD电子递交专题讲座(US DMF and EU ASMF)” 讲座主题:如何完成eCTD格式的递交(US DMF and EU ASMF)讲座时间:2017年2月24日 14:00-15:00,持续时间:60分钟主讲人:Silke Nolkemper Fernanda Manhaes参加办法:免费注册 (注册请登入创腾科技网站) 讲座内容: 网络讲座将为您提供一个独特的机会,让您更好的了解即将推行的法规、正在进行的变革以及如何去克服这些挑战,在讲座上您更可以准确地了解到关于US DMF 和EU ASMF是如何通过eCTD的格式进行建立、查看、验证及提交的。讲座之后,演讲者将在问答环节回答您的问题。 讲座提纲:1.US DMF2.EU ASMF3.问答环节 eCTDmanager:eCTDmanager能够使您容易的使用CTD、eCTD、NeeS、eCopy、IMPD、CTA、VNeeS、DMF、ASMF以及其他提交结构的格式进行创建、查看、验证和发布提交。 讲师简介:Silke Nolkemper女士是德国海德堡大学的制药生物学博士,在制药企业有超过7年的法规注册经理经验,曾在PharmaLex公司,Sandoz/HEXAL公司担任法规部注册经理,针对的市场有欧盟、亚太地区、拉丁美洲、中东地区。同时Silke女士在CRO企业的临床注册领域也有多年的工作经验。从2014年加入EXTEDO至今,Silke女士一直致力于注册咨询服务,对于电子申报格式十分熟悉(eCTD, NeeS, eCopy,VNeeS, ASMF, DMF),此外,Silke女士还是一位专业的培训讲师。 Fernanda Manhaes女士有超过5年的法规注册经验,曾帮助过巴西、法国、意大利等多个国家的公司完成eCTD递交,特别是API和FDA方面,是Fernanda女士擅长的专项。 >>讲座注册请登入创腾科技网站
厂商
2017.02.13
Discovery Studio 2017 R2 新版本发布会
作为全球最大的科学计算软件提供商BIOVIA公司在生命科学领域的核心产品,Discovery Studio是一款应用于生命科学预测领域的综合性分子模拟软件,集成了目前分子模拟领域的各种经典、先进算法,通过用户体验友好的操作界面以及高质量的图形显示,在计算生物学和药物设计领域都有着广泛的应用。Discovery Studio构建于BIOVIA Pipeline Pilot之上,为研究队伍的合作与信息共享提供了优秀的平台。 Discovery Studio 2017 R2是Discovery Studio软件的最新版本,由BIOVIA公司向全球正式发布。新版本的Discovery Studio在性能和效率上都得到了加强,并加入新方法,使其功能更加完善。新特性简介:■ 与最新发布的BIOVIA Pipeline Pilot 2017 R2相兼容;■ 小分子设计: · 新!新增Generate Analog Conformations模块,在给定以蛋白结合口袋为参照系具有明确3D几何构象的先导化合物时,可获得其同系化合物的3D几何构象,且可采用in-situ MM-GBSA对配体结合进行打分排序; · 新!新增Set Up Relative FEP Calculation、Free Energy Perturpation (NAMD)、Analyze FEP Results模块,可基于自由能微扰(FEP)精确预测配体相对结合自由能; ■ 抗体理性设计 · Model Full Length Antibody模块支持双特异性抗体全长结构的模建; · Model Full Length Antibody模块支持将抗体Fab区结构移植到抗体全长模板结构中以获得更合适的起始结构进行抗体建模; · Antibody Modeling Cascade模块现支持将抗体Fab区模型嫁接到全长抗体结构模板中以获得更准确的抗体全长结构模型; · Loop Refinement模块改进了looper算法,提高了loop区从头预测的准确性;■ 力场 · 完全支持CHARMM力场的补丁机制; · charmm36力场的更新;■ 客户端 · 支持将分子以COLLAborative Design Activity (DAE)文件格式保存输出;■ 第三方程序的更新 · CHARMm 40b1 · MODELER 9v17 · DMol3 2017 R2 · NAMD 2.10 · 支持CCDC GOLD 5.5■ 数据库的更新 · Anitibody数据库 · BLAST数据库 若您想对以上新功能做进一步了解和获取更多Discovery Studio 2017 R2新功能信息, 详情了解:请关注创腾科技官网
新品
2017.01.03
创腾科技“Materials Studio奖学金”收稿倒计时
2016年第四季度奖学金计划投稿截止日期:2016年12月31日别忘了参与活动,获得更多交流学习机会和奖品 四季度奖品一等奖苹果平板电脑二等奖kindle电子书 创腾科技materials studio奖学金是什么? 创腾科技“materials studio奖学金”为ms软件的所有使用者构建一个交流模拟研究工作,学习模拟研究思路和方法的公益奖学平台。各领域的研究人员将基于materials studio发表的sci文章以中文精简版的形式发送到prize@neotrident.com, 我们将定期统计和更新各人投送文章的影响因子积分总和(文章影响因子积分总和=文章影响因子总和+文章数目),并按排名先后发送对应奖品。 2016年度奖学金计划有哪些新规则值得关注: ? 按季度统计个人投送文章的影响因子积分总和并评奖 ? 投送不同数目文章获得对应数目的礼品 ? 有机会受邀做面向全国的学术报告>>更多详情请登录官网查看
厂商
2016.12.28
CIMS 4.0 & CMS 4.0 管理系统新版本发布会
尊敬的客户, 您好! 非常高兴地宣布由创腾科技有限公司自主创新产品 (neosuite cms) v4.0思为特化合物注册管理系统,和(neosuite cims) v4.0思为特试剂库存管理系统,新版本将于2017年初正式发布。 neosuite cims v4.0 (试剂库存管理系统)是创腾科技10年专注于化学试剂信息化管理经验的结晶,对化学实验室试剂耗材从查询,采购,入库,申领,出库,使用,退库,报废进行全生命周期管理。提升试剂库存管理水平,减少试剂浪费,缩短申领周期,降低危化品管理安全风险。 neosuite cms v4.0(化合物注册管理系统)是创腾科技10年化合物信息管理经验的积累,发布的最新的化学制药企业研发成果管理平台。一站式管理化合物研发数据,包括项目信息,化学信息、样品信息、反应路线、生物信息集中管理。采用最先进的工业标准的化学结构式处理模块,严格的注册审批发布流程,灵活的审批流程,为化学制药研发机构建立规范的私有化合物知识库。 以上仅仅是新版本简单介绍,如果您想进一步了解产品详细功能,我们诚邀您出席在2017年1月13日(周五)通过网络形式召开的新版本发布会。届时我们会向大家详细介绍并进行新版本演示,点击下面注册链接,免费获取发布会登录地址,非常欢迎感兴趣的企业注册参加。 发布会主题:neosuite cims & cms——化学制药实验室的管理变革发布会时间:2017年1月13日(周五)下午14:30-16:30发布会讲师:市场产品总监 徐博士发布会形式:网络发布会【免费】(通过网络链接即可参加发布会,手机端和pc端均可登录) >>立即注册 (请登录创腾科技有限公司的官网,提交注册后您会收到发布会链接地址,建议会议开始前30分钟登录) neosuite cims v4.0的主要功能特点如下: 1. 采用b/s构架,支持主流的ie,firefox和谷歌浏览器,部署管理方便 2.采用最新的html5技术开发,用户界面更友好。 3. 试剂耗材全生命周期管理,支持移动端和条码管理,提高效率,降低库管难度 4. 十年化学试剂管理的最佳实践,开箱即用,实施周期短。 5. 完善的安全策略和加密技术,保证系统安全。 6. 采用web service api设计,方便与其他系统进行整合,消除信息孤岛 neosuite cms v4.0的主要功能特点如下: 1. 规范便捷的化合物信息注册功能: 批量导入/导出功能,提高数据维护效率,唯一性检测,严格的审批流程,保证数据的可靠性。与eln系统规范的接口,支持一键注册功能。 2.成熟的化学及生物数据模板: 精心设置的化合物、合成路线、样品、谱图信息、以及体外、药效、药理、毒理信息管理模板,满足化学药物研究全方位需求 3. 高度灵活的模板自定义: 复杂多变而无法预测的化合物信息字段的完美解决方案,满足不同企业的使用需求 4. 高效的协作任务管理: 合成部门与测试部门自动信息流转,提升协作效率 详情了解登录创腾科技官网
新品
2016.12.23
学生特惠 | Discovery Studio分子模拟【寒假特训】
培训主题:12月DS分子模拟【寒假特训】培训时间:2016年12月27日-29日,共三天培训地点:苏州创腾科技培训中心经典模拟方法在药物设计以及计算生物学领域的应用—— 同源建模、分子对接、蛋白设计、药效团等尊敬的老师和同学,您好! 创腾科技有限公司将于2016年12月27日-29日特别举办一期生命科学分子模拟寒假特训课程。本次课程的培训主题是 “经典模拟方法在药物设计以及计算生物学领域的应用”,共为期三天。本次课程将重点介绍Discovery Studio中以下几种在药物设计和计算生物学领域常用的计算方法:同源建模、小分子对接、大分子对接、蛋白设计以及药效团。借助DS中这些经典模拟技术,您可以进行药物的虚拟筛选、药物分子的优化与改造,药物潜在靶标的搜寻,药物靶标蛋白三维结构的预测与评估、蛋白-小分子作用机制的解释、蛋白-蛋白(核酸/多肽)作用模式的预测与分析、蛋白的理性设计与改造等工作。 培训相关信息如下:培训时间:2016年12月27-29日,共三天培训地点:苏州创腾科技培训中心(江苏省苏州市工业园区东长路88号2.5产业园A2栋301室) 培训主旨:本次培训班旨在帮助学员快速了解并掌握Discovery Studio2017中多种经典的模拟技术——同源建模、分子对接、药效团模型、蛋白设计,包括核心原理、参数设置技巧、结果分析、热点问题的解决并快速上机操作。 培训对象:从事药物研发相关领域的科研工作者,从事蛋白质结构与功能关系研究相关领域的科研工作者,对分子模拟和Discovery Studio软件感兴趣、希望系统掌握软件使用技巧、能够快速上机模拟操作相关课题的老师和同学。 培训内容:本次培训课程将会围绕Discovery Studio2017软件中多种小分子对接算法、全方位的药效团模型构建方法及应用策略、基于目前市场上最大最全药效团模型数据库的反向找靶、基于行业标准同源建模程序的蛋白结构预测与分析、以及业内认可度和使用率最高的大分子对接方法、独特灵活的蛋白虚拟氨基酸突变等技术方法展开介绍。 培训价格:培训费用1人参加特惠价格及条件(符合任一条件即可):1、在12月19日确认报名并汇款;2、同一单位,≥2人参加 。学生(凭学生证)3500/人2500/人教师或企业客户3500/人3000/人 培训形式:1、通过文献案例分析讲解每一种模拟技术方法的应用以及原理介绍;2、上机操作(培训现场配有电脑,无需自带):讲解每一种模拟技术方法的具体操作流程及参数设置(提供完整的培训教程);3、学员交流与讨论,工程师进行现场答疑答疑。 欢迎感兴趣的老师及同学登入创腾学院网站报名网址:http://training.neotrident.com/course/course_nr.aspx?id=172
厂商
2016.12.09
浙江海正药业股份有限公司“牵手”北京创腾科技有限公司共建QC实验室信息管理系统
2016年10月17日星期一,由北京创腾科技有限公司所承接的浙江海正药业股份有限公司[600267]实验室管理系统开工会在海正药业总部台州顺利召开,包括北京创腾科技CEO曹总、CTO冯总、海正药业质量副总裁王总、海正药业质量副总温总在内的双方多名高管均参加了本次会议。 浙江海正药业股份有限公司[600267]是国内外顶尖的原料药和制剂供应商,主营抗肿瘤、抗感染、心血管、内分泌、免疫抑制、抗抑郁、骨科等领域的原料药、制剂的研产销业务,业务遍及全球70多个国家和地区,在特色原料药产业化和高端制剂产业化等形成了自己的特色和优势。然而,随着国内外的法律法规对包括数据完整性、计算机化系统验证等众多因素在内的要求越来越严格,海正药业面正在并还将临着巨大的QC实验室合规性挑战。经过大半年的实验室信息管理系统供应商甄选,海正药业最终“牵手”北京创腾有限公司进行合规化QC实验室建设,希望借助创腾科技在该领域丰富的项目经验,按时保质的完成项目建设 北京创腾科技有限公司是业界领先的面向生命科学行业提供综合研发、过程、检测、生产信息化平台及咨询服务的高新技术企业,在合规化QC实验室建设,有着丰富的经验和独一无二的解决方案。北京创腾科技的合规性实验室管理系统方案由赛默飞 SampleManager LIMS 和Dassault Systèmes BIOVIA LES整体解决构成。SampleManager LIMS系统稳定、配置简单、拓展性灵活、系统功能完备、适合于分析领域,Dassault Systèmes BIOVIA LES在药企GMP领域有很高的权威性,能够完全保障QC检测的数据完整性和可靠性。这样的产品组合将共同组成了一个覆盖海正药业药业质量部管理需求和业务需求的完整解决方案,在海正药业的总体质量战略和质量方针指导下,将实验室的样品检验流程、环境、人员、仪器设备、标物标液、化学试剂、标准方法、文件、实验记录等要素有机结合起来,建立先进、高效合规的实验室信息化管理平台。该解决方案也相继在四川科伦药业、协和发酵麒麟、国药集团、药明康德等国内多家顶尖药企和CRO企业由北京创腾科技建设并成功上线运行。 北京创腾科技目前拥有超过60人的咨询、实施、验证和开发队伍,是国内实施基于GCP/GLP/GMP/17025规范的信息系统最多的企业。所有实施、验证团队成员均来自于国内外著名医药公司和实验室,并都通过相关的计算机验证方法学培训。实施团队熟悉GxP行业法规的要求,了解FDA等政府部门对计算机系统的审查重点,熟悉验证方法学——GAMP5,了解医药企业客户的实际业务流程,有丰富的系统整合的经验 (ELN/LIMS/ERP/CMS/CIMS)和计算机化系统验证经验。
厂商
2016.11.02
干货分享:药品eCTD(电子申报)实践交流活动(12月. 北京)
如何让最安全、有效和高质量的药品以最经济高效的方式得到批准和上市是药品监管部门、制药企业的共同心愿。从2008年起,FDA开始鼓励以eCTD(electronic Common Technical Document电子通用技术文件)格式提交相关新药申请材料。这一申请无纸化进程逐渐在全世界各地的生物医药管理部门得到推广。近十年来,eCTD递交以其在创建、传输、复制、审阅、检索、存档以及文件生命周期管理等方面的优势已成为全球药品注册申报的大势所趋。2015年FDA正式宣布,到2017年中旬前大部分药物的申请将被要求采用eCTD提交。在这一期限之后,FDA将不再受理要求范围之内文件的纸质申请。 所以药品的eCTD申请,将是获取国际市场准入的必经之路,注册文件的质量将对企业优先抢占目标市场起到了决定性作用。我们希望通过本次研讨活动,快速提升广大药企面向欧美高端市场,编写及申报注册文件的水平,为更多医药企业,原料药,制剂出口创造更高的效益。活动中专家将介绍eCTD的标准并解释eCTD申报的结构和生命周期中的细节; 如何递交DMF和ASMF eCTD档案至US FDA,EMA和NCAs;申报中最常见的验证问题和如何解决这些问题,以及对公司及申请人的建议等关键性问题。 诚邀并欢迎医药企业的研发管理、项目管理、QA/QC、注册专员等相关技术人员参加本次交流研讨活动。 研讨会时间:2016年12月1日(周四)研讨会地点:中国科技会堂研讨会地址:北京市海淀区复兴路3号会议注册费:无报名方式:填写回执并于11月28日前反馈到以下信箱market@neotrident.com研讨会日程演讲者: dr. silke nolkemper, mr. stefan horneborg, mr martin schmid(ceo)以及其他特邀嘉宾09:00 – 9:30案例分析介绍 (针对中国企业)09:30-10:30有关ectd介绍· ctd 与ectd:纸质材料和电子材料间的差异· ectd的大体结构· 对公司及申请人的建议o 硬件/软件规格o it知识,申请人能力及其他10:30 – 11:00 茶歇11:00 – 12:30ectd-结构的细节· 元数据· 签及超链接· xml-backbone类库, 信封· e-ctd在欧洲生命周期属性经验:多个药用规格和剂型如何在一个ectd材料中被管理(特殊章节的管理)12:30 – 13:30午餐13:30 – 15:00 ectd 生命周期管理· 申报生命周期,如变量和申报线延长· 文档生命周期(新加、替换,删除,附件文档)· 标准:eu,us及其他地区· 特殊格式: asmf, dmf· e-ctd准备时间和将被使用的格式15:00 – 15:30茶歇15:30 – 16:30ectd 最佳实践:· do & don't· 最常见的验证问题和如何解决这些问题16:30 – 17:00问答时间 ü会议酒店信息:酒店:中国科技会堂地址:北京市海淀区复兴路3号电话:010-68518822ü报名方式:填写word版报名回执>并于11月28日前发送发送到market@neotrident.com信箱。工作人员将在2个工作日内发给您报名成功的确认回复。 ü会议联系:北京创腾科技有限公司会务电话:021-51821768转242(曹小姐); 021-51821768转233(陈女士);email:market@neotrident.com;web:www.neotrident.com;
厂商
2016.11.02
关于eCTD格式电子申报的介绍及最佳实践-eCTD研讨会邀请函
尊敬的各位专家及老师们, 在此我们诚挚的邀请您参加“关于ectd格式电子申报的介绍及最佳实践”的研讨会,研讨会将于2016年9月21日在上海举办。在这一天的活动中我们的专家将介绍ectd(electronic common technical document电子通用技术文件)的标准并解释ectd申报的结构和生命周期中的细节,以及如何递交dmf和asmf ectd档案至us fda,ema和他们的ncas。 时间:2016年9月21日(周三)地点:上海皇廷世际酒店地址:上海市浦东新区唐安路588号会议注册费:无报名方式:填写回执并于9月18日前反馈到以下信箱huiyu@neotrident.com 或xutao@neotrident.com 研讨会日程演讲者: dr. silke nolkemper, mr. stefan horneborg, mr. li zhong 以及其他特邀嘉宾9:00 –9:30 案例分析介绍 (针对中国企业)9:30-10:30 有关ectd介绍 ? ctd 与 ectd:纸质材料和电子材料间的差异 ? ectd的大体结构 ? 对公司及申请人的建议 ? 硬件/软件规格 ? t知识,申请人能力及其他10:30 – 11:00 茶歇11:00 – 12:30 ectd-结构的细节 ? 文件及文件夹 ? 元数据 ? 书签及超链接 ? xml-backbone类库, 信封 ? e-ctd在欧洲生命周期属性经验:多个药用规格和剂型如何在一个ectd材料中被管理 (特殊章节的管理)12:30 – 13:30 午餐13:30 – 15:00 ectd 生命周期管理 ? 申报生命周期,如变量和申报线延长 ? 文档生命周期(新加、替换,删除,附件文档) ? 标准:eu,us及其他地区 ? 特殊格式: asmf, dmf ? e-ctd准备时间和将被使用的格式15:00 – 15:30 茶歇15:30 – 16:30 ectd 最佳实践 ? do & don't ? 最常见的验证问题和如何解决这些问题16:30 – 17:00 问答时间 会议酒店信息? 酒店:上海皇廷世际酒店三层水晶厅? 地址:上海市浦东新区唐安路588号? 电话:021-20650158 周边住宿(住宿需自行预定)? 上海皇廷世际酒店 浦东新区唐安路588号;电话021-20650158; 住宿费: 650元/天(含早) ? 如家快捷酒店 浦东新区唐安路695弄11号(靠近高科东路);电话021-68790156;住宿费: 约250元/天 交通路线? 虹桥火车站&虹桥机场 → 地铁2号线(徐泾东-广兰路)到达广兰路 → 地铁2号线东延伸段(广兰路-浦东国际机场)途径1站到达唐镇 → 步行约709米到达酒店? 上海火车站 → 地铁1号线(富锦路-莘庄)途径3站到达人民广场 → 地铁2号线(徐泾东-广兰路)到达广兰路 → 地铁2号线东延伸段(广兰路-浦东国际机场)途径1站到达唐镇 → 步行约709米到达酒店。报名方式请填报名回执并于9月18日前反馈到以下信箱huiyu@neotrident.com或 xutao@neotrident.com 会议联系北京创腾科技公司 惠女士电话:021-51821768转284;13564882594
厂商
2016.08.29
药品美国市场准入”独家专题讲座 邀请函
尊敬的老师,您好! 为生命科学专业人才提供的药品美国市场准入独家专题讲座开始啦!本次为期一天的独家专题讲座,通过深入了解药品美国市场准入项目,您可以获取fda最新要求和gmp法规要求,并应用到贵司的实际,降低贵司的风险,加速贵司的产品进入美国市场。我们将分享行业中的最佳案例,阐述在生命科学领域中会对贵司的盈利造成负面影响的各种挑战和趋势,为您介绍其他企业如何应对这些问题。我们还将把此领域专家积累的丰富经验分享给您,为您介绍一套综合性的实际操作方案。同时您也有机会与业内的同行互相交流。 本次专题讲座由北京创腾科技公司与全球产品安全事业的领导者ul公司联合举办,将于2016年9月20日(周二)在上海皇廷世纪酒店进行。 专题讲座的各项筹备工作正在按计划顺利进行。我们真诚地邀请您参加。现将专题讲座邀请函发给您,请您仔细阅读后,尽快完成相关的注册手续,并抽空将所附回执填好并在报名截止日期前寄给我们。 同时欢迎您对专题讲座提出宝贵的意见和建议,关于报名或讲座内容的任何问题,请联络会务人员。 一、专题讲座时间和地点时间:2016年9月20日(周二), 1天地点:上海皇廷世界酒店 三层水晶厅 地址:浦东新区唐安路588号 (距离地铁2号线唐镇站约709米) 二、会议日程(9月20日,周二,为期一天)时 间内 容9:00-9:15欢迎致辞9:15-10:30进入美国市场之前的战略规划和正式审查准备期望进入美国等规范市场的企业,必须了解fda的法规更新对您的产品设计、工艺流程、质量体系和员工能力等要求的影响。始终保持具有前瞻性的战略规划,企业可以降低由无法达到当地市场要求或者产品上市延迟所带来的风险。本报告将重点介绍企业如何设计一个满足fda合规要求的战略路线图,如何建立一个良好绩效表现同时保证合规的质量文化和员工能力培养计划。本报告还将结合相关指南和注意事项,介绍企业如何利用信息技术来优化流程,促进审查准备、提高效率和降低成本。报告要点:· 为什么战略规划和路线设计对贵司的产品获得市场准入非常重要· 如何用战略路线图来排兵布阵,结合贵司实际所处的阶段,排列获得市场准入各项需求的优先级· 如何顺利实现产品注册,通过fda检查并在新的市场始终保持合规· 如何通过优化流程、充分利用资源和信息技术,为成功获得市场准入做准备10:30-10:45茶歇10:45-11:30企业自身准备程度评估为审查做充分的准备非常重要,尤其是当前全球各监管机构的质量体系法规正在日趋复杂化和重叠化。为多国市场提供服务的生命科学企业,或者供应链遍布全球的生命科学企业,经常面对来自监管机构的合规挑战,这些挑战主要来自美国fda、欧盟委员会和中国药监局。本报告将介绍如何帮助贵司减少监管审查,并在fda审查通过后,始终保持合规状态。报告要点:教育:帮助贵司员工做好接受审查员面试的准备评估:根据fda相关要求,进行模拟审查,对业务流程、技术体系和员工能力做差距分析和风险评估审核:通过审核发现差距和风险造成的影响整改:实施整改计划,以通过最终模拟审查保持:随时做好检查准备11:30-12:15如何响应和应对fda的审计和后续整改无论企业收到的是来自监管机构审查、内部审查还是第三方模拟审查的不符合项,都需要对所有的审查不符合项建立和实行整改计划。本报告将介绍企业如何向监管机构的审查不符合项提供必要的响应和整改措施,并在复审以前成功修复所有已发现的问题;如何撰写对审查不符合项和纠正预防措施建议的客观有逻辑的响应内容,降低进一步监管审查的风险。报告要点:· fda审查行为的几种类型——对企业意味着什么· 如何响应fda和向fda报告的流程· 对整改有帮助的工具和解决方案——电子化管理和专业知识· qms(电子质量管理系统),lms(电子培训系统),dms(电子文档系统)对企业合规有何帮助12:15-13:30午餐和交流13:30-14:15fda等监管机构对产品注册和测试的要求本报告将介绍fda等监管机构对产品注册和测试的要求。介绍产品测试计划和测试开发,如何支持产品注册和认证。除了美国市场准入要求以外,还将讨论iso13485、加拿大cmdcas、欧盟公告机构、巴西– inmetro和风险管理iso 14971的系统注册要求。报告要点:· 如何确定贵司产品获得市场准入的fda要求· 制定测试计划以满足fda要求· 全球市场的监管方案· iso 13485认证和其他市场要求14:15-15:30现代化制药企业集成信息技术的基础构架行业中的成功案例表明,企业具备了集成化的信息技术基础,不仅能满足监管机构的合规要求,还能创造更高质量的产品和更优化的业务流程,从整体上提升企业的商业绩效。本报告将讨论建立一套自动化集成的质量管理体系基础结构的重要性,并介绍如何用业内最好的网络技术为贵司建立基础结构,实现点对点的流程自动化,同时保证合规。报告要点:· 集成的信息技术基础结构态系中包含哪些要素· 根据贵司当前在市场准入路线图中所处的阶段和问题,正确的部署集成信息技术基础结构· 如何为集成的信息技术基础结构的开发和可持续发展进行战略投资15:30-15:45茶歇15:45-17:00讨论和回答 三、讲师风采linda m. chatwin 博士简介:已经有30多年医疗产品法规事务方面的从业经历,包括在医疗器械公司多年担任法规事务工作以及在ul多年的法规咨询经验。她的专长包括:通过对监管领域发展和变化的多年观察为医疗器械产品符合全球市场准入监管破解迷津,制定国际法规事务战略,提交美国fda 510(k)文件及其他监管文件,实施fda模拟审查及其他外部审查,改正从审查中发现的错误,质量体系建设和改进以及基于fda qsr质量体系规范、风险管理、《关于限制在电子电器设备中使用某些有害成分的指令》(rohs)认证和安全标准培训,编制和维护风险管理文件,对各种认证标准的差距评估,制定及实施设计控制工艺,以及实施医疗器械唯一标识(udi)程序等深度咨询服务。她已帮助很多企业获得广泛领域的产品批准,并且始终参与了解世界范围内对医疗器械不断变化的要求。 linda也为很多企业提供美国食品药品监督管理局(fda)的现场检查辅导,以及协调与fda的沟通并获得有利的结果。linda 持有威斯敏斯特大学的工商管理学位,以及犹他大学法学院的法学博士(jd)学位。她还拥有国际法规事务认证证书,并且在美国境内是一名律师。victoria amann简介:维多利亚是ul eduneering咨询团队负责人,有超过15年的行业经验。她最常咨询的领域为培训流程梳理、学习管理制度开发、在现有的学习环境中嵌入合规流程等。维多利亚曾参与制定美国等监管机构的检查员培训计划,美国先进医疗技术协会advamed的质量培训计划,以及国际医疗器械生产商和制药企业的培训计划,她熟悉质量体系规范qsr和质量体系审核技术qsit,她帮助这些机构和企业超越合规培训、达到能力培养。在加入ul以前,维多利亚曾就任雅培公司的合规培训经理,是ul线上培训平台compliancewire的全球系统管理员,协助开发了雅培的质量体系培训课程,培训系统验证和其他系统集成。她同时也是雅培公司认证的纠正预防措施capa培训师。维多利亚还曾就任强生公司的质量培训专家,结合精益化管理和卓越设计方法开发了全球质量培训的标准。再此前,她曾担任field sales技术公司的培训师,基于网络培训技术制定一套培训计划和材料,培训了该公司超过250名员工。 四、讲座费用注册费用:rmb 1000/人(费用包括场地、授课、资料、中餐、茶歇费; 学员住宿费及交通费自理)优惠条件: 1、若同一单位超过两人(包括两人)报名,可以享受rmb 800/人的优惠价格; 2、9月1日前报名并付款可享受rmb 800/人的优惠价格 注:开具发票内容可以为‘培训费’或“会议费”,发票将在会期间发给您,若对发票开具内容有特殊要求,请在报名回执中说明。 收费方式: 1、银行汇款信息(请备注:“参会人姓名+美国市场准入”) 户 名:北京创腾科技有限公司上海分公司 开户行:招商银行上海晨晖支行 账 户:1219197075105012、现场支付:培训现场可收取现金或刷卡。五、住宿推荐(住宿需自行预定)=上海皇廷世际酒店 浦东新区唐安路588号;电话021-20650158; 住宿费: 650元/天(含早) =如家快捷酒店 浦东新区唐安路695弄11号(靠近高科东路);电话021-68790156;住宿费: 约250元/天 六、交通及地图路线参考:=虹桥火车站&虹桥机场 → 地铁2号线(徐泾东-广兰路)到达广兰路 → 地铁2号线东延伸段(广兰路-浦东国际机场)途径1站到达唐镇 → 步行约709米到达酒店=上海火车站 → 地铁1号线(富锦路-莘庄)途径3站到达人民广场 → 地铁2号线(徐泾东-广兰路)到达广兰路 → 地铁2号线东延伸段(广兰路-浦东国际机场)途径1站到达唐镇 → 步行约709米到达酒店。七、报名方式:请填写报名回执并提交到以下报名信箱,成功报名后您会收到确认邮件。报名截止日期9月15日,最大容纳人数为100人,额满为止。 八、会议联系人北京创腾科技有限公司上海分公司 杨先生(信息事业部)联系电话:021-51821768转454, 15001765869报名信箱:yangliuqing@neotrident.com 或 market@neotrident.com公司官网:www.neotrident.com
厂商
2016.08.29
“计算机化系统验证培训班”即将开班
尊敬的企业科研人员、管理者: 为了帮助企业解决在执行计算机化系统验证中存在较多的困惑,指导企业自主找出数据完整性方面的缺陷,建立数据完整性质量体系,由北京创腾科技有限公司主办为期一天的“计算机化系统验证培训”将于2016年5月21日(周六)在北京凤凰会议中心(国家蛋白质科学研究中心)举办。我们诚挚地邀请您参加本次培训。 随着CFDA颁布并执行2010版GMP法规的新附录《计算机化系统》,随着国内GMP的监力度显著增强,越来越多的企业意识到能不能满足《计算机化系统》法规的要求将起着至关重要的作用。本届培训将围绕此命题,对计算机化系统法规进行深入的解读,理解法规对计算机化系统合规的要求及其重要性,对计算机化系统验证内容及流程进行详细阐述,并帮助企业识别生命科学行业。法规具体适用的计算机化系统验证法规以及实战解释相关规例和成功验证系统的指南。 我们邀请到具有计算机系统验证资质的资深培训师Shannon女士为嘉宾进行深入系统的培训,以下是培训详情,请您仔细阅读,我们诚邀您的参与!一、培训时间和地点:培训时间:2016年5月21日(周六)8:30-17:00培训地点:北京凤凰会议中心 小会议室北京市昌平区北清路中关村生命科学园(国家蛋白质科学研究中心)二、参加对象:企业管理人员和技术人员,包括质量保证部门、质量控制部门、IT部门、验证实施部门、技术支持部门等需要掌握CSV基础知识的管理人员、以及计算机系统的供应商等。三、培训专家介绍:Shannon Wang个人简介: 具有超过 15 年的经验,为政府机构、 电信、 建筑、 电子商务以及医疗行业提供有效应对技术挑战的解决方案。非常熟悉医药行业,按照监管要求及GAMP5指南提供完整的计算机化的系统实施和验证解决方案。 项目包括,ERP验证、 MES实施和验证、BMS/EMS 系统验证、 LIMS 系统实施和验证、WMS系统验证等。具有国际制药工程协会(ISPE) 中国培训委员会成员及ISPE中国GAMP培训师,以及中国食品药品查验审核中心(CFDI)计算机化系统验证培训师资质。为中国本地制药公司提供计算机化系统验证培训。四、培训详细议程:点击查看五、培训费用:培训费用:RMB 1000元/人 (包括:专家费、资料、中餐、证书,住宿和交通费自理)优惠费用及条件: RMB 800元/人,只限于参加“第三届数字化实验室建设与应用研讨会“的代表。收费方式:A、银行汇款信息(请在汇款时务必注明用途“培训费+姓名“) 户 名:北京创腾科技有限公司上海分公司 开户行:招商银行上海晨晖支行 账 户:121919707510501B、现金支付:会议现场注册,支持刷卡支付方式。六、报名方式:请您填写报名回执,并将回执以邮件、传真或邮寄方式于5月15日前提交会务组(报名信箱:huiyi@neotrident.com),以便我们在培训举办前,为您安排好相关培训事宜。收到您的报名回执后,会务组将用邮件方式与您确认。七、住宿与交通:梧桐苑商务酒店会议价格:RMB 328/晚 (含早,标准间)宾馆地址:北京市昌平区北清路中关村生命科学园内宾馆电话:010-61777200海诺康会馆会议价格:RMB 298 /晚(含早,标准间)宾馆地址:北京市昌平区生命科学园路 16 号(中关村生命科学园内)宾馆电话:010-80728999转8178会议地址:凤凰会议中心小会议室(北京昌平区中关村生命科学园入口东侧大楼)八、培训联系:北京创腾科技有限公司电话: 021- 51821768转233(陈女士); 13916858963 021-51821768转219 (崔小姐) 010-82676188转213(杨小姐)传真: 021- 51821758邮箱:huiyi@neotrident.com网站:www.neotrident.com
会展
2016.05.10
大会报告抢先看:第三届(2016)数字化实验室建设与应用研讨会
第二轮通知“第三届数字化实验室建设与应用研讨会”第一轮通知发出后,得到了众多企业研发及管理人员和相关领域专家学者的积极响应和热情支持。本届会议将于2016年5月19日至20日在北京凤凰会议中心举行。会议主题为探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。大会将邀请到来自药监、药检系统的相关领导、国际国内临床试验专家、和医药、石油、材料等领域研发与生产部门的高层管理人员与会进行全面和有针对性的研讨。会议的各项筹备工作正在按计划顺利进行,我们真诚地邀请您参加本次大会。现将会议筹备情况及第二轮通知寄给您,请您仔细阅读。5月5日前报名可以享受优惠价格,报名截至日期为5月15日,请在此时间前提交您的参会回执,以便我们在会议召开之际,为您安排好相关参会事宜。我们热忱欢迎您的参与,并期待在北京与您相聚。 大会议题: 探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。??? 材料研发及检测信息化 ? 【报告题目】化学技术研发型企业知识平台建设浅谈 代志龙 主任,中国航天科技集团公司四院四十二所【报告题目】实验室管理系统在军工研究所的实施与应用 严蕊 高级工程师,西安近代化学研究所【报告题目】万华化学实验室信息化系统的应用 乙志静 经理,万华化学集团股份有限公司【报告题目】信息化驱动的研究创新在中国石油化工股份有限公司的应用和展望 周涵 总工,中国石油化工股份有限公司石油化工科学研究院 药企研发及检测信息化 【报告题目】制药实验室信息化系统如何满足法规要求 林淘曦 部长,广东东阳光药业有限公司【报告题目】天士力制药试剂与仪器信息化管理方案建设及实践 刘锐 部长,天津天士力制药股份有限公司【报告题目】 从CFDA临床数据核查看如何规范化管理实验室数据 沈晓航 博士【报告题目】实验室信息化助力海思科新药研发 苏桂转 经理,四川海思科制药有限公司【报告题目】信息化技术助力科伦全面质量管理 徐华林 部长,四川科伦药业股份有限公司【报告题目】LIMS+LES在国药化学试剂生产的应用 郑琦,质量经理,国药集团化学试剂有限公司 政府检测信息化 【报告题目】药检系统的报送和数据挖掘 胡康 高级工程师,中国食品药品检定研究院【报告题目】如何成功实施一个数据分析系统? 蒋受军 主任药师,广西壮族自治区药品不良反应监测中心【报告题目】中检院检定流程管理系统的建设 李健 高级工程师,中国食品药品检定研究院【报告题目】检测实验室的数据挑战 周霖 高级工程师,浙江省食品药品检验研究院 学术研究信息化 【报告题目】数字化实验室建设过程中的推广和培训 陈浩宇 教授,军事医学科学院【报告题目】PMS在高校的使用推广 罗彤 经理【报告题目】基于云平台的生物数据中心 朱云平 教授,军事医学科学院放射医学研究所 其他企业信息化&计算机化系统验证 【报告题目】Managed Innovation leveraging a Science-aware Platform (基于科学智能信息平台的创新管理)Reza S. Sadeghi,Dassault Systèmes BIOVIA【报告题目】Unified Laboratory and Knowledge management for Research Development, Production and Compliance (统一的数字化实验室信息平台和知识管理系统在研发、生产及合规领域的应用)Michael Doyel,Dassault Systèmes BIOVIA【报告题目】Innovation through Laboratory Informatics(实验室信息化进程中的革新) Matt Grulke 高级总监,赛默飞世尔科技公司【报告题目】unique online FDA regulatory and compliance training plateform UL Eduneering【报告题目】计算机法规附录解读及计算机系统验证介绍 YI (SHANNON) WANG 圆桌主题:针对国家CFDA一系列的相关政策,如7-22事件,讲述如何通过Watson LIMS满足生物分析实验室的法规要求,邀请用户介绍Watson LIMS的应用,和出席嘉宾共同讨论如何通过信息化使生物分析实验室更加满足国家法律法规要求。【报告题目】 新形势下电子信息化系统的作用 郑维义 董事长,江苏诺佰奥生物医药股份有限公司【报告题目】Watson LIMS - Reviewing the tools to improve productivity and ensure compliance and data integrity(Watson LIMS - 评估提高生产力及确保合规和数据完整性的工具)Matt Gruver 产品经理,赛默飞世尔科技公司会议时间: 2016年5月19日至20日(周四至周五)会议地点: 北京凤凰会议中心,二层报告厅北京市昌平区北清路中关村生命科学园(国家蛋白质科学研究中心)报到时间:2016年5月18日(周三)下午14:00-20:00 2016年5月19日(周四)上午07:30-08:30 地点:北京凤凰工程梧桐苑会议中心(二层)进行报到和注册。注册费用:包含所有会议资料、用餐及茶歇;参会人员住宿费及交通费自理。国内代表 RMB 2400/人 国外代表 USD 500/人 注: 5月5日前报名并汇款,可以享受 RMB 1800/人或USD400/人的优惠价格。 收款方式:A、银行汇款信息(请在汇款时务必注明用途“会议注册费+参会人姓名“) 户 名:北京创腾科技有限公司上海分公司 开户行:招商银行上海晨晖支行 账 户:121919707510501B、现金支付:会议现场注册,支持刷卡支付方式。报名方式:请填写与会代表参会回执,并将回执以邮件、传真或邮寄方式于5月15日前提交会务组,以便我们在会议召开之际,为您安排好相关参会事宜。收到您的参会回执后,会务组将用邮件方式与您确认。会议住宿:梧桐苑商务酒店会议价格:RMB 328/晚 (含早,标准间)宾馆地址:北京市昌平区北清路中关村生命科学园内宾馆电话:010-61777200海诺康会馆会议价格:RMB 298 /晚(含早,标准间)宾馆地址:北京市昌平区生命科学园路 16 号(中关村生命科学园内)宾馆电话:010-80728999转8178会议交通:会议地址:凤凰会议中心(北京昌平区中关村生命科学园入口东侧大楼)交通路线:1、首都国际机场乘坐出租车:全程约 37.7 公里,用时 1 小时 13 分钟 ,打车费用约 120 元;地铁/公交:步行至 T2 航站楼,乘坐机场线,在东直门站下车,乘坐地铁13 号线,在西二旗站下车(A2 北出口出),乘坐运通 112 路,在小牛坊桥东站下车,步行至中关村生命科学园。2、北京西站乘坐出租车:全程约 28.3 公里,用时 48 分钟,打车费用约 87 元。地铁/公交:步行至北京西站乘坐地铁 9 号线,在国家图书馆站下车,乘坐地铁 4 号线在西直门站下车,乘坐地铁 13 号线,在西二旗站下车(A2 北出口出),乘坐运通 112 路,在小牛坊桥东站下车,步行至中关村生命科学园;3、北京南站乘坐出租车:全程约 36.8 公里,用时 1 小时 1 分钟,打车费用约 117 元。地铁/公交:步行至北京南站乘坐地铁 4 号线,在西直门站下车,乘坐地铁13 号线,在西二旗站下车(A2 北出口出),乘坐运通 112 路,在小牛坊桥东站下车,步行至中关村生命科学园;注:组委会不安排车辆接送。请代表自行乘地铁、出租车等交通工具抵达报到地点。 会务联系:北京创腾科技有限公司电话: 021- 51821768转233(陈女士); 021-51821768转219 (崔小姐) 010-82676188转213(杨小姐)传真: 021- 51821758邮箱:huiyi@neotrident.com; 网站:www.neotrident.comhttp://www.neotrident.com/upload/edit/files/20164/计算机化系统验证培训通知.pdf?附件一:【计算机化系统验证培训通知】?附件二:【参会代表报名回执】??
商机
2016.05.10
第一轮通知:第三届(2016)数字化实验室建设与应用研讨会
第三届(2016)数字化实验室建设与应用研讨会The 3rd symposium of the construction of digital laboratory applications第一轮通知 由北京创腾科技有限公司主办的“第三届数字化实验室建设与应用研讨会”将于2016年5月19至20日在北京召开。大会每年举办一次,截止2015年已成功举办两届,每届会议规模超过百人。本届会议依然秉承“加强数字化实验室建设整体水平,提高研发及生产等环节的质量管理与控制能力,加快企业管理水平与国际先进标准接轨步伐”的理念,邀请来自药监、药检系统的相关领导、国际国内临床试验专家、和医药、石油、材料等领域研发与生产部门的高层管理人员与会进行全面和有针对性的研讨。本届大会主题是探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。 伴随着信息化在国内医药、材料、化工等领域企业及研发机构的发展要求,信息化在企业的研发、过程、生产及检测管理方面已经在国际上得到了广泛的应用,国内主要的材料和医药研发企业以及主要的研发机构也在构建和应用信息化平台方面进行了有益的探索并取得了较大的进展。提高企业管理效率、进行信息化管理模式的探索和创新将是一个永恒的主题。 本届会议将邀请到来自国内外众多高水平研究机构的专家学者,以及企业相关部门的管理人员,将共同交流信息化技术在企业中的应用;分享信息化建设中的经验与体会;探讨如何利用最新的信息技术搭建研发智能、检验检测、生产质控管理平台以提高企业管理水平、研发能力、经营水平、市场竞争力。会 议 组 织 机 构会议组织委员会:· 主 任:沈竞康 陈 为· 副主任:冯 华 · 委员会成员:(以姓氏拼音排序) 陈 为 陈浩宇 成双红 代志龙 邓炳初 冯 华 郭殿武 郭洪祝 郭志杰 韩 昆 胡 康 胡齐悦 贾 宁 江 骥 李 川 李 健 李可欣 李 杨 林淘曦 刘万卉 罗 彤 罗卓雅 马国栋 阮 斌 沈陵陵 沈晓航 涂 健 沈竞康 徐华林 徐筱杰 杨治旻 袁 征 张哲民 赵玉明 周 涵 周 霖 会 议 基 本 信 息会议时间: 报到时间:2016年5月18日下午(周三) 会议时间:2016年5月19日至20日(周四至周五)会议地点: 北京(具体地点待定) 大会报告邀请名单(截止3月15日确认)军事医学科学院陈浩宇副处长中国航天科技集团公司四院四十二所代志龙主任中国食品药品检定研究院胡康高级工程师广西壮族自治区药品不良反应监测中心蒋受军副主任中国食品药品检定研究院李健高级工程师天津天士力制药股份有限公司刘锐部长国药集团化学试剂有限公司罗彤经理TBD沈晓航博士四川海思科制药有限公司苏桂转经理四川科伦药业股份有限公司徐华林部长西安近代化学研究所严蕊高级工程师万华化学集团股份有限公司乙志静经理中国食品药品检定研究院标化所尹利辉主任协和发酵麒麟(中国)制药有限公司 张丽英高级主管江苏诺佰奥生物医药股份有限公司郑维义董事长中国石油化工股份有限公司石油化工科学研究院 周涵总工BIOVIAMichael Wang 总监赛默飞世尔科技公司Dave Leitham 副总裁赛默飞世尔科技公司Matt Gruver 产品经理北京创腾科技有限公司冯华技术副总注:报告情况将会持续更新,敬请关注!大 会 议 程5月18日(周三)14:00-20:00注册报到 地点:北京 5月19日(周四)9:00-18:00 大会报告 地点:北京 大会议题: 探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。议程安排:07:30-09:00 报到注册(所有参会代表需佩带会议胸卡入场) 09:00-09:10 会议开幕式09:10-10:00 大会报告 (每个报告30分钟)10:00-10:30 茶歇10:30-12:00 大会报告 (每个报告30分钟)12:00-12:30 大会照相12:30-13:30 午餐13:30-15:30 大会报告(每个报告30分钟)15:30-16:00 茶歇16:00-18:00 大会报告(每个报告30分钟)18:00-20:30 欢迎晚宴 5月20日(周五)9:00-12:00 大会报告 地点:北京 议程安排:09:00-10:00 大会报告 (每个报告30分钟)10:00-10:30 茶歇10:30-12:00 大会报告 (每个报告30分钟)12:00-13:30 午餐 5月20日(周五)13:30-16:00 生物分析圆桌会议 地点:北京 会议主题:针对国家CFDA一系列的相关政策,如7-22事件,讲述如何通过Watson LIMS满足生物分析实验室的法规要求,邀请用户介绍WatsonLIMS的应用,和出席嘉宾共同讨论如何通过信息化使生物分析实验室更加满足国家法律法规要求。议程安排:13:30-16:00 圆桌讨论说明:参加本届会议的代表,可以选择参加5月20日下午的圆桌讨论会其 它 会 务 信 息会议费用:1)会议注册费:(包含会议资料、会议用餐;参会人员住宿费及交通费自理)· 国内代表:RMB2400元/人· 外宾代表:USD500 /人2)优惠条件: 2016年5月 5日前报名并交纳注册费可享受RMB1800/人或 USD400/人的优惠价格。3)收费方式:A、银行汇款信息(请在汇款时务必注明用途“会议注册费”,以及参会人员姓名) 户 名:北京创腾科技有限公司上海分公司 开户行:招商银行上海晨晖支行 账 户:121919707510501B、现金支付:会议现场注册,支持刷卡支付方式。 报名方式:请填写与会代表参会回执,并将回执以邮件、传真或邮寄方式于5月15日前提交会务组,以便我们在会议召开之际,为您安排好相关参会事宜。收到您的参会回执后,会务组将用邮件方式与您确认。 会务联系:北京创腾科技有限公司电话: 021- 51821768转233(陈女士) 021-51821768转219 (崔小姐) 010-82676188转213(杨小姐)传真: 021- 51821758邮箱:huiyi@neotrident.com网站:www.neotrident.com说明:大会地点、报告详情将在4月中旬发布的第二轮通知中公布,敬请关注!期待您的参与!更多会议信息及报名回执请登入创腾科技网站查询,详情:http://www.neotrident.com/news/detail.aspx?id=947
会展
2016.04.07
2016年分子模拟学习体验日(免费)
尊敬的老师和同学,您好! 近20年来,诺贝尔化学奖已两次授予计算化学学科(1998年度和2013年度),这充分说明了理论计算和模拟在科学研究中的重要性,不仅在化学和生命科学领域,科学计算和模拟结合高性能计算机,已经成为认识和解决所有复杂的科学和工程问题的重要方法。Discovery Studio(简称DS),作为面向生命科学领域的综合性分子模拟平台,通过高质量的图形界面、经多年验证的科学算法以及集成的环境,为科研工作者提供了易用高效的药物设计与大分子模拟技术和工具,从而得到了广大用户的认可与青睐。 2015年创腾科技有限公司在北京成功举办了Discovery Studio4.5体验日,共吸引超过120多位相关领域的科研工作者。为满足更广大客户的学习需求,我们计划于2016年在全国(暂定五大区:成都、沈阳、武汉、西安、南京)继续举办该学习体验活动,为更多科研人员提供一个免费交流学习Discovery Studio软件在药物设计和生物大分子模拟领域应用的机会与平台,帮助更多的科研人员了解Discovery Studio软件的应用并学以致用。 随着Discovery Studio2016版本的正式发布,本年度活动将以Discovery Studio2016软件为依托,介绍Discovery Studio2016新功能,并围绕经典的模拟技术手段进行介绍和案例分享,内容涵盖:基本界面和入门操作、分子对接、药效团模型、蛋白质理性设计等,从而帮助大家系统了解该模拟技术并应用于蛋白(核酸)-小分子相互作用机理解释、化合物的虚拟筛选、化合物构效关系的分析、反向找靶、抗体设计和酶设计等方面。活动具体信息如下: 一、活动城市和时间:二、活动日程安排: 详情见创腾科技网站活动页面(www.neotrident.com)三、参加对象: 对分子模拟感兴趣、希望了解分子模拟并将模拟技术应用于药物研发、蛋白结构功能研究、抗体研究或酶研究领域的高校或企业科研人员;对Discovery Studio软件感兴趣、希望了解Discovery Studio软件的高校或企业科研人员。 四、活动费用:免费活动(食宿交通等费用自理) 五、学习电脑: 学习体验日现场涉及上机操作,需自带电脑(具体会有后续通知)。请在活动开始前自行下载并安装DS软件。学员可根据自己手提电脑配置自行下载所对应的版本: Windows 32bit下载 链接: http://pan.baidu.com/s/1i4ho54x 密码: 4n4u Windows 64bit 下载 链接: http://pan.baidu.com/s/1qXtR8SG 密码: qh5m Linux 64bit下载 链接: http://pan.baidu.com/s/1qXiwsby 密码: bixs 六、报名方式:请填报名回执并发送到market@neotrident.com信箱,提交回执后3个工作日内会收到一封确认邮件,敬请留意!注:1)自通知发布后接受报名,以报名先后顺序安排座位,因场地名额限制,额满为止! 2)若临时取消报名,务必提前通知工作人员;活动当日请提早报到,若活动开前5分钟仍不到现场,为您预留的座位将由旁听席学员顶替。 报名邮箱:market@neotrident.com
百态
2016.02.29
如何通过化学品信息化方案提高实验室安全管理?
天津港爆炸事件余温还未散去,又惊闻清华大学化学系某实验室火灾事件。据传,事故系由危险化学品叔丁基锂引发。如何建立并执行规范的实验安全制度,确保科研人员在有安全保障的环境下工作,是当下整个科研环境都要深刻反思的问题。 NeoSuite CIMS是创腾科技基于通用化学信息管理平台开发的网页版的化学品库存、采购管理系统,能够完成对化学试剂进行申领、申购、订购、跟踪、审核、入库、出库、盘库、精确称量分装、配送等相关化学品库存管理功能。B/S架构方便多地区办公地点同时使用,专业的库存管理流程,精细化的管理方式,灵活的配置和审批机制,便于信息共享,提高库存管理效率,减少试剂耗材浪费从而降低使用成本,便于库存统计及项目成本核算,为研发机构试剂高效流通及安全存储提供了有力保障。 对于研发人员来说,准确、高质量、高效率地获取实验所需试剂对自己的实验进行十分重要。很多研发人员反映,订购试剂到货期难控制,流程相对繁琐,影响实验进程。有些研发试剂具有易燃易炸性、氧化性、放射性、毒性,带来一定的安全隐患,需要安全分类管理。试剂分散存放无从进行试剂信息的共享,导致研发人员重复订购试剂;或因项目暂停或结束无从处理相关试剂,造成试剂浪费。NeoSuite CIMS的特点 支持全中文的界面和环境,客户端基于浏览器界面,便于操作和使用; 系统开发基于中国国内真实的客户需求,适用于中国客户的具体情况,满足大部分中国客户的需求; 系统具有严格的安全机制的可配置功能,可针对客户需求,对安全机制进行严格和灵活的配置,确保所有数据在安全可靠的基础上,能够发挥最有效的应用; 实施周期短,Out-of-box的解决方案; 丰富的报表生成功能,方便管理人员对库存数据随时进行统计和报告; 可进行客户化,使系统完全符合客户独特的需求; 满足现在和将来的需求:系统易于维护和拓展,能够适应需求的变化;可与其他软件或管理系统(如ERP)进行整合,形成企业级整体信息解决方案。NeoSuite CIMS应用价值 NeoSuite CIMS在企业的应用,将为企业的研发、物流和财务管理相关的工作人员带来很多的便利性。 对于实验人员来说,他可以使用最便捷、最习惯的化学结构检索的方式来查找化合物,而且可以通过相似性结构检索来查找替代化合物;可以很快的了解仓库里化合物库存的情况,包括准确的库存量、纯度、过期时间等详细信息;可以随时在线提交化合物申领和试剂申购请求,并随时了解配送和采购的进度。 对于库存管理人员来说,他可以即时响应实验人员的化合物配送请求,并对库存试剂和样品进行精细化管理,保证化合物的库存量和库存位置都十分精确;另外可以随时跟踪每瓶化合物的使用历史,跟踪没有退库的或即将过期的化合物;简化化合物出入库和盘点的操作,提高效率并减少错误。 对于财务人员来说,在线申购请求和审批可以加快审批和采购的进度;可以避免重复采购,减少浪费;长期合作的供应商及其产品目录信息可以进行集中管理;订单的管理和财务统计也将十分的方便。了解NeoSuite CIMS产品请登入创腾科技网站:www.neotrident.com
厂商
2015.12.23
科伦药业实现对样品检测的最佳质量控制(LIMS系统)
药品的质量和安全日益受到广大消费者的关注,政府监管机构也出台严格的措施以确保药品的安全和维护消费者的权益,因此,药品生产企业面临着许多挑战和困难,比如,要遵从越来越多的法律法规,要在保证企业效益的情况下不断提高药品质量,要在众多制药企业中脱颖而出等等,在这种情况下,药品生产企业必须主动采取快速有效的措施来提高产品质量才能在激烈的竞争中生存下来。 四川科伦药业股份有限公司成立于1996年,是拥有32家子(分)公司的现代化药业集团,科伦药业生产和销售包括输液、粉针、冻干粉针、小水针、片剂、胶囊剂、颗粒剂、口服液、透析液以及原料药、医药包材、医疗器械等共计551个品种912种规格的产品。科伦药业的生产基地分布于四川、湖南、黑龙江和云南等14个省区,并已在哈萨克斯坦投资建厂。挑战: 科伦药业急需一个先进、高效的实验室信息化管理平台来对质量部进行规范化管理,而对方对这个系统的需求是:1. 先进性:能保证大并发量的访问和数据的安全性,系统应当基于当前最先进的软件信息技术进行开发,确保系统有足够长的生命周期。2. 易用性:友好简洁的用户界面设计,便于用户的快速理解和使用。3. 开放性和可扩展性:系统具有开放性,应充分考虑网络、硬件的扩展,方便与其他厂家的应用系统进行数据交换。4. 灵活性:系统必须具备灵活的用户业务设计功能,允许用户根据实际业务需求对系统功能进行适当的定制。当业务扩展和业务流程发生变动时,能通过简单的方法即可满足新的业务流程需求。5. 安全性和真实性:系统必须提供身份验证、访问控制、电子签名、多角度的保密手段等严密的措施,确保系统的安全性和完整性。数据的授权修改应有审计跟踪的机制,便于追溯。6. 法规符合性:系统在管理实验室的人员、文件、数据、样品、仪器设备等各要素时应完全符合ISO/IEC 17025准则和GxP等相应的法规要求。 2012年经过广泛的市场调研,科伦药业最终选择了Thermo Scientific SampleManager LIMS +Accelrys LES这种整体解决方案,科伦药业看重的主要是SampleManager LIMS系统稳定、配置简单、拓展性灵活、系统功能完备、适合于分析领域, Accelrys LES在GMP领域有很高的权威性,这种组合方式规避了单一的大而全的系统带来的资源上的浪费和技术上的不精湛。 实施: 历时9个多月的实施工作,北京创腾科技有限公司提供的SampleManager LIMS+Accelrys LES软件整合方案,与科伦药业现有ERP进行集成,共同组成了一个覆盖科伦药业质量部管理需求和业务需求的完整解决方案,将实验室的样品检验流程、环境、人员、仪器设备、标物标液、化学试剂、标准方法、文件、实验记录等要素有机结合起来,建立先进、高效的实验室信息化管理平台。 结果: SampleManager LIMS+Accelrys LES软件与科伦药业集团现有的ERP系统整合起来,实现了通过ERP系统实时传送请验数据进入LIMS系统,质量部门根据导入LIMS系统中的样品信息,将样品相关的测试任务提交给LES系统,LES系统负责完成具体的测试工作并记录原始数据,最后将最终的试验结果提交给LIMS, 经过LIMS系统,产品终审后自动同步到ERP系统。LIMS与ERP的整合意味着在LIMS中产生的试验结果经审核后,此信息能迅速为高层管理人员和一线分析人员提供可靠、准确和及时的质量信息,从而指导生产、降低产品不合格率、提高企业效益。 系统提供了许多便利的功能,如快速锁定样品、查看任意样品原始记录、原始图谱,通过电子签章、电子签名等安全有效的方式进行COA报告、原始记录单的审核工作,稳定性趋势分析、移动极差分析的数据统计等,在很大程度上解放了实验室人员繁重的工作;严格遵从药品管理行业cGMP法规的同时,规范了实验室管理,确保了数据的及时、有效性。 对国内医药行业来说信息化是一个新兴事物,科伦药业在信息化上是走在前列的,相信在SampleManager LIMS + Accelrys LES的帮助下,科伦药业能向公众提供始终如一的高质量产品,也必将成为国内医药行业竞争力最强的企业之一。
商机
2015.11.25
立足信息化建设,确保数据真实完整性,让临床试验数据值得信赖!
随着国家食品药品监督管理总局对药物临床试验数据现场核查越来越严格,医药界也越来越关注临床试验条件和设计合规性以及临床试验数据真实性和完整性。尤其是近期国家食品药品监督管理总局公布了对部分已经提交自查资料的药品注册申请的临床试验数据现场核查结果,8家药企11个药品注册申请不予受理。根据发布不予批准的公告,惨剧主要与临床试验数据真实完整性有致命关系,一时间又掀起了关于临床试验数据合规性的腥风血雨。 根据国家食品药品监督管理总局关于药品注册申请不予批准公告,汇总不予受理的药品注册申请临床试验数据存在的问题主要与数据真实完整性有关:一、临床试验部分数据的真实性完整性:原始记录缺失;试验数据不完整;试验记录与实际不符;试验数据不可靠;修改调换试验数据;试验数据不可溯源;不良事件记录不完整。二、人体生物等效性(BE)/人体药代动力学(PK)试验生物样本检测数据的真实完整性:分析测试系统无稽查轨迹;分析测试过程不完整;试验用药品未留样,部分血样丢失;部分图谱真实性高度存疑;分析测试数据存疑。三、II、III期临床实验数据数据库真实性:隐瞒弃用试验数据;选择性使用数据等。 数据完整性是2015年制药圈最热词之一,这个概念其实在中国GMP中早已有相关要求,也是最基本的要求,因此并不是一个新的概念。然而自号称医药界“七二二惨案”,即国家食品药品监督管理总局下发《关于开展药物临床试验数据自查核查工作的公告》之后,数据完整性的概念被迅速炒热。如何建立一个有效的证据链,保证其记录的真实完整性,成为医药界亟待解决的重大问题。 如何能够分类管理我们不同的研究项目,设计合理的受试者或实验动物的分组和给药方案,并根据实验人员的不同身份进行工作的安排?如何能够保证DMPK实验室数据的安全管理,数据不会被随意改动?如何能够保证对样品的管理准确有效?如何能够让负责DMPK工作的CRO企业与制药公司互相沟通?如何保证DMPK工作的数据信息能够通过严格FDA审核,提高制药公司DMPK的研究效率,增加CRO企业的国际竞争能力?这些挑战,只有专注于DMPK实验室应用的信息管理系统,才能真正解决。 Watson LIMS实验室信息化解决方案——数据真实性完整性保障的王牌 Watson LIMS 就是这样一个满足独特要求的标准化系统。它是专门为制药公司和CRO企业的DMPK实验室定制的产品。Watson LIMS 属于商业成品LIMS,与普通的需要大量定制化工作的通用LIMS来说,其配置时间短,验证速度快,临床研究机构能够从高效率中快速受益。 Watson LIMS专门为DMPK的生物分析工作流程而设计:图表化的临床方案设计能够清楚直观地反映出临床试验方案的受试对象组、受试对象、给药方式、取样类型和取样时间点的关系,确保临床试验设计的合理性;生命周期式的样品跟踪和管理,支持多层次的样品存储位置设计(可以细化至冰箱层架、储存盒、孔位等),用户在初始化存储地址后,系统将基于条形码记录样品流转的时间和操作信息,形成完整的样品追踪报告, 为样品管理的法规准从性提供了保证;具有与各类常见分析设备的电子接口,支持仪器产生的原始数据(如峰面积、峰高、OD值等)和经过处理的结果(如浓度),保证仪器数据的真实性可靠性;内置各种回归计算功能,对具有电子接口的仪器所产生的原始数据都可以进行分析计算,在一定程度上提高了数据处理的一致性和对法规的准从性。 除此之外,Watson LIMS内置了150多种实验报告的模版,用户可以进行定制化,进行数据的查看和分析。Watson LIMS内置的独特的文档管理系统,能够系统地管理研究结果的报告,高效率地读取数据,生成统一的最终报告。 Watson LIMS 内置的数据管理形式完全符合GLP和21 CFR PART 11的规范。其安全设置功能能够保证数据的绝对安全性。每个使用者在系统内部具有自己的角色和权限,对实验方法和实验数据的任何改动都必须经过授权,电子签名,并且任何改动都可以进行审计审核。这些安全性的设定能保证客户在向CFDA提交新药注册申请时,DMPK的数据能够被信任。全球顶尖的20家制药公司中的19家都选择了Watson LIMS应用于其DMPK实验室,众多的CRO企业同样选择了Watson LIMS ,二者在进行项目交流和数据转移的过程中能够实现无缝连接。 只有致力于寻求解决临床试验设计、试验数据记录、样品管理、数据库信息真实完整等问题的方案,才能从根本上满足越来越严格的数据核查要求。Waston LIMS信息化的解决方案,具备专业数据管理的科学性和有效性,不仅解决了严格的管理制度的难题,同时建设和积累研究机构内部真实完整的大数据,从而使研究机构找到自己独特临床治疗的优势和产品特色,造福百姓生命健康,承担医药界为人类健康服务的崇高使命! >>点击查看Watson LIMS产品
商机
2015.11.18
中药研发科学化、现代化——屠呦呦获诺贝尔生理学或医学奖为中医药发展迎来新的契机
2015年10月5日,瑞典斯德哥尔摩,诺贝尔委员会举办新闻发布会,宣布2015年诺贝尔生理学或医学奖得主。中国药学家屠呦呦,爱尔兰科学家威廉·坎贝尔、日本科学家大村智分享该奖项。图1 2015诺贝尔生理学或医学奖得主 至此,屠呦呦成为首位获得诺贝尔科学类奖项的中国科学家、首位获得诺贝尔生理医学奖的华人科学家。屠呦呦发现的对抗疟疾的神药青蒿素也引起举世瞩目。 青蒿素的发现表明,中医药是一个伟大的宝库,有宝贵的财富,需要我们去发现、挖掘和研究。而屠呦呦此次因其发现青蒿素的突出贡献获得诺贝尔奖也为中药发展迎来新的契机。图2 中国药学家屠呦呦肖像照和其工作描述图 创腾科技作为国内资深的生命科学信息提供商,基于数据库、分子模拟与分子设计平台Discovery Studio以及强大的信息整合和流程定制的科学平台Pipeline Pilot,能够为中药研发的科学化和现代化助上一臂之力。 中药化合物数据信息的提供· 中药化学数据库 (Traditional Chinese Medicines Database , TCMdb)是创腾科技有限公司和中国科学院过程工程研究所联合开发的综合性中药数据库,是支持新药研发和中药现代化研究的有力工具。 TCMdb目前收集了化合物23033种,每种化合物下列12项数据:唯一代码、CAS登录号、中文名称、英文名称、别名、分子式、分子量、二维结构式、植物来源、药理活性(即药理模型实验结果,近8000多种化合物有此数据)、物理化学性质(晶体形态、熔点、沸点、旋光度等,14000多种化合物有此数据)和参考文献。TCMdb涉及到的中药药用植物有6735种,使用的参考文献有5507篇。图3 TCMdb数据库中收集的青蒿素信息 · 中国天然产物数据库(Chinese Natural Product Database,CNPD)是创腾科技有限公司和中国科学院上海药物研究所联合开发的综合性天然产物数据库。CNPD收集、整理、分析了从中国国产的植物中分离鉴定出的天然产物的物理性质、生物活性剂化学结构等信息,为中国的新药、天然产物及相关领域的研究与开发工作提供了一个不可多得的好工具。 CNPD目前共收集了五万七千多个天然产物,涵盖天然产物的三十七个类别,有70%的分子是类药性分子。同时CNPD还收集了天然产物相关的各类信息,主要包括:天然产物的二维分子结构及三维分子结构;天然产物的名称、分子式、分子量、熔点、旋光度等理化性质、天然产物的CAS号;天然产物的生物活性信息及其参考文献;天然产物的自然来源及其参考文献;原植物或其同属重要在中国传统医药中的应用等。图4 CNPD数据库中收集的青蒿素信息 特定靶标中药的虚筛 针对特定的药物靶标,筛选新的活性化合物是药物科研工作者和各大制药公司奋斗的目标。获得先导化合物的一个重要来源就是天然产物。我国在天然产物的药物发现研究中做出了杰出的贡献,典型的例子就是抗疟药物青蒿素。但是要收集这些天然产物需要大量的经费和时间,随着计算机在药物发现中逐渐发展成为不可缺少的手段,在计算机上利用软件针对某靶标从中药化学数据库或者天然产物数据库中用虚拟筛选(virtual screening,VS)方法搜寻活性化合物,继而集中提取几个至几十个化合物进行药理筛选,是发现新型先导化合物结构的一种经典且高效的途径。 Discovery Studio (简称DS),作为权威的药物设计与模拟平台,通过高质量的图形界面、经多年验证的科学算法以及集成的环境,为科研工作者提供了易用高效的药物设计与优化工具。 对于中药的虚拟筛选,DS可以提供多种不同的虚筛方法:· 以靶标结构为基础,通过分子对接技术和片段设计技术,模拟中药数据库与靶标分子间相互作用,从而虚拟筛选出潜在活性分子· 以已知同一靶标的活性化合物为基础,通过构建药效团模型并以此作为检索模式来筛选潜在活性化合物· 联合不同模拟技术进行虚拟筛选。 针对上述每种虚拟筛选策略,DS都能提供多种算法以供研究者根据不同的研究体系进行选择,同时对于活性的评价也提供多种打分函数。结合TCMD和CNPD,DS为中药的虚拟筛选提供有力的保证。图5 中药的虚拟筛选示意图 中药的成药性评价 中药成药性评价方面,Discovery Studio提供专业的类药性评价工具和ADME/T性质预测工具,可快速、准确预测化合物相关的各项成药性指标。· 类药性评价工具。主要包含两种常用半经验方法,类药五规则和veber规则,从氢键供体、氢键受体、分子量、LogP等方面来进行类药性的判定;· ADME/T 性质预测工具。提供多种ADMET性质预测模型,可以对中药的吸收、代谢、分布、排泄、毒性等性质进行预测。· 化合物的水溶性· 血脑屏障穿透性· 人细胞色素P450 2D6抑制性· 肝毒性· 人肠吸收性质· 血浆蛋白结合能· 潜在发育毒性(Developmental Toxicity Potential,DTP)· 致突变型(Mutagenicity(Ames test))· 啮齿动物致癌性(Rodent Carcinogenicity)包括 NTP及FDA 数据集· 大鼠长期口服最低毒副反应水平(Rat Chronic Oral Lowest Observed Adverse Effect Level, LOAEL)· 皮肤致敏性(Skin Sensitization (GPMT))· 皮肤刺激性(Skin Irritancy )· 大鼠口服LD50(Rat Oral LD50 )· 大鼠最大耐受剂量(Maximum Tolerated Dosage)· 黑头呆鱼LC50(Fathead Minnow LC50 )· 大型溞EC50(Daphnia Magna EC50 )· VlogP· 眼刺激性(Ocular Irritation)· 大鼠吸入LC50(Inhalational LC50)· 好养生物降解性能(Aerobic Biodegradability)图6 青蒿素的ADMET Descriptors预测结果图7 青蒿素的TOPKAT预测结果 中药靶向原理、有效成分的预测中药的现代化,应该是真正理解其有效成分、药效机理、靶向原理,知其然并知其所以然。图8 青蒿素潜在靶标的预测示意图 对于未知靶标的中药有效成分,可以基于如下三种方法进行反向找靶,从而预测其作用机制。· 药效团模型搜索( Compound Profiling )Discovery Studio为研究者提供基于受体或基于受体-配体相互作用构建代表受体活性口袋化学和几何信息的药效团模型的算法。 图 9 基于受体 - 配体复合物产生药效团 基于药效团模型来搜索潜在靶标的方法,就是将中药有效成分与多个代表各靶标蛋白的药效团模型相互匹配,最终按照匹配打分的高低来判定潜在作用靶标。Discovery Studio中包含目前市场上最大的受体-配体复合物药效团数据库 PharmaDB,该数据库是基于scPDB(2012)中7028个复合物晶体结构构建的,共含117423个药效团模型,并且这些模型已根据不同的靶标类型进行了分类。Discovery Studio中自带的流程Ligand Profiler可自动实现多个分子和多个药效团模型的快速匹配并进行匹配度打分排序。因此,结合PharmaDB,Discovery Studio可以快速有效且全面地进行靶标搜寻、中草药有效成分的确定以及毒副作用评价。图 10 基于药效团模型的反向找靶示意图,“对号”代表命中的模型 · 反向分子对接( Target Fishing ) 传统的分子对接方法可以帮助科研工作者预测靶标分子与待研化合物的相互作用模式,并借助打分函数评价分子的构效关系。然而,借助计算流程编辑与管理平台Pipeline Pilot以及分子模拟平台Discovery Studio中的分子对接算法、打分函数,创腾科技为国内医药研究者提供基于分子对接方法的化合物反向找靶策略。图 11 基于分子对接的化合物反向找靶计算流程图整个设计思路分为三个步骤:1. 读取用户的小分子结构· 读入的文件格式可能不同:sdf、mol、mol2、skc等· 实现读入小分子的二维/三维结构转化,结构标准化,加氢,结构优化等2. 反向对接及打分(等于多个正向对接)· 遍历蛋白数据库文件,获得每个蛋白的文件路径和结合位点· LibDock参数自动设置和填写(图示流程整合了DS中的LibDock对接模块,如需要,也可替换其它对接程序)· 自动循环,使小分子与每个蛋白受体对接· 打分、筛选和排序3 结果报表输出· 柱状图显示靶标打分和最终排序· 对接结构和打分情况 图 12 基于 DS+PP 反向找靶流程的结果示意 其中,靶标可来源于scPDB数据库(http://bioinfo-pharma.u-strasbg.fr/scPDB ),该数据库收集了标准PDB数据库中含有药物结合位点的蛋白,可根据配体、蛋白、结合方式为特征进行搜索。· 基于 小 分子相似性分析 (Ligand Similarity Search) Discovery Studio为研究者提供基于分子指纹的分子结构相似性搜索,即DS可以计算中药活性成分与已包含化合物生物活性以及靶标注释的化合物数据库中小分子化合物的Tanimoto系数等,从而进行相似性评价,进而预测其潜在靶标。如果输入的分子能够在数据库中搜索到它本身,则可以获得其已知靶标;如果输入的分子能够在数据库中搜索到与其相似的化合物,则根据与其结构相似的分子靶标可推测输入分子的靶标信息。图13 根据同已有靶标分子相似性的分析进行未知分子靶标的预测流程示意图
百态
2015.11.04
浅谈研发领域信息化知识库建设方案
现如今新药、生物技术、仿制药公司都面临着前所未有的挑战,提高产品质量、生产率、投资回报率和法规依从性。这些挑战随着未来医药产品专利过期,在新兴市场企业面临更大的压力的情况下将持续增长。为此,企业组织机构重新评估从研发到商品生产整个产品生命周期,从信息技术(IT)系统着眼,以应对不断变化的新供应链商业生态环境。也就是说,寻求行业内IT系统发展提供的综合解决方案以提高生产率,大大降低成本,提高基础设施动力。那么,这种挑战主要存在哪些方面呢?当然,核心是数据,R&D和QC数据的获取、存储、处理和利用成为最重要的需求。传统的纸质版的数据记录(仪器工作站单独工作等原因)和手工管理方式使得各部门的数据都是一个个的孤岛,使得数据的获取和分析变得尤为困难。因此,创建一个高效的信息平台,将各种数据集变为信息,形成一个企业级的知识库,为研发和生产提供有力的支持尤为重要。 这一高效信息平台的创建往往需要三层架构,即企业资源管理系统(ERP),实验室信息管理系统(LIMS),电子实验记录本(ELN)或实验室执行系统(LES)、库存管理系统(CIMS),三层体系的协同合作有效加强了内部信息分享与协作,同时更好地控制了与外部合作伙伴(如CRO/CMO)的工作流。据报道,这种综合的系统战略降低了20%的成本提高了生产效率,产品生命周期缩短50%以上,转变了纸质记录方式并且保证了文档的合规性。R&D ELNs& CIMS, QC LES, LIMS 系统再加上与仪器和设备的整合,直接将数据传输到ERP系统,保证能够电子化获取和访问到从早期的研发到商业化过程中产生的一致的信息,能够控制产品开发生命周期完整的数据历史。 在检测、制药、化工、医疗等领域的研发机构、企业,研发型和生产型两种环境分别有不同的解决方案。今天,我们主要从医药研发行业来探讨研发管理系统信息化知识库建设方案。对于研发型的机构,知识的循环利用非常重要。实验室获取信息的过程是一个循环的过程是由实验或实验室产生一系列数据,有效地使用这些数据进行分析产生信息,将与研发相关的各部门的信息形成自己内部机构的知识库,根据积累的知识来支持进一步项目或研发方向的决策,以利于下一步研发的进行,并优化数据的产生。国内采用的实验记录信息化解决方案主要是各类ELN产品,实验室资源管理主要是LIMS产品。实验记录产生的知识是研发管理知识库建立的核心,除此之外与研发实验工作相关的管理也尤为重要,例如研发所用试剂、耗材等化学品的库存管理是保障科研工作顺利进展的前提条件,规范、可追溯的、高度自动化的库存管理方案(例如NeoSuite CIMS)便于科研工作者申领、申购所需试剂和物品并及时掌握状态和进度以利于合理安排工作时间;高效出/入库、自动化盘库改善库存管理水平的同时提高库存管理工作的效率;维护常用高性价比的供应商和产品信息也是服务于实验工作试剂、物品来源积累的重要方便,为科研工作提供可靠的保障。 电子实验记录信息化解决方案 电子实验记录本协会(CENSA)对ELN(Electronic Lab Notebook,ELN)的定义:ELN是一个能够创建、储存、检索和分享实验信息的平台,满足法律、法规、技术和科学的需要,主要在研发机构使用,以完整记录每一个实验的过程。ELN系统的功能根据科研领域和任务而有所不同,其主要功能包括实验设计、实验数据记录、实验模板设计、数据存档、数据检索、报告导出、数据挖掘与可视化、实验结果分析、科研工作流支持与协作、电子签名等等。对记录的数据进行存储和管理。一般来说ELN主要处理非结构化数据和信息、管理研发合作。 ELN的概念提出最早是在二十世纪九十年代末。开始主要应用于制药和化学领域,在过去的5-10年中,ELN已经拓展到生物相关的学科领域,例如药理学,药物代谢学、药物动力学,流程驱动(process-drived disciplines)的领域例如生物分析、药物制剂、分析和工艺。所以ELN支持结构化和非结构化的数据的存储、共享查询、数据分析。支持跨临床前研究部门的工作流整合。每个学科领域对于ELN的需求各不相同。药物制剂需要获取样品、流程和剂型,计算,测试结果和样品批记录,跨领域汇报给项目组。分析团队需要管理测试请求,获取方法,验证细节,整合临床数据系统(CDS),实验室信息管理系统LIMS,提供结构化数据的获取和结果汇报。药代动力学需要将研究、剂量、样品收集整合在一起,录入和管理数据,提供综合分析并和与专业工具整合(如WinNonlin)。在研发领域,ELN平台的建设意味着各部门的解决方案可以构成综合的化学、生物研究进展的视图。当然通过权限配置也允许每个学科的成员不仅可以看到自己部门的数据,也能看到其他部门的相关信息。使用企业级的ELN,数据的获取和视图都可以根据不同部门的需求来定制。例如配方设计师可能从样品的角度看结果,而生物学家会从检测的角度进行工作。这意味着好的数据管理非常重要。系统必须对数据的使用如获取一样重要,因为数据的使用与其他部门的工作实践息息相关。ELN通过提高数据质量,支持数据重复利用,支持数据挖掘从而在整个临床前研究过程中进行数据提供和知识管理。 ELN市场充满活力,已经实施的组织机构正在体会到它在实验室工作效率和更好的保护知识产权方面的显著效益。大约94%的潜在用户拟将ELN同现存的其他系统整合,最常见的是LIMS、文档管理系统、仪器数据采集系统、数据归档以及科学数据库等。25%科学家们可能将ELN作为“所有实验室管理系统的门户”,23.5%的人认为他们是“应用于多学科领域的通用实验室杂志”。 实验室资源信息化解决方案 实验室信息管理系统( Laboratory Information Management System,LIMS),是基于计算机局域网,专门针对一个实验室的整体环境而设计,是一个包括了信号采集设备、数据通讯软件、数据库管理软件在内的高效集成系统,能够完成实验室数据和信息的收集、分析、报告和管理。以实验室为中心,将实验室的业务流程、环境、人员、仪器设备、标物标液、化学试剂、标准方法、图书资料、文件记录、科研管理、项目管理、客户管理等等因素有机结合。商业化LIMS产品已有20多年历史,尽管每个LIMS产品应用的领域各不相同,但都成为在实验室信息化平台建设方面的主要元素。纯粹数据管理型这类的LIMS 软件主要功能一般包括:数据采集、传输、存储、处理、数理统计分析、数据合格与否的自动判定、输出与发布、报表管理、网络管理等模块。样品进入实验室或者说进入整套流程后,需要对其进行编号,划分测试方法,并再次对子样品名进行编号(或者根据实验室具体需要成批编号),然后选择适当的方法生成适合不同仪器使用的样品序列,进入仪器分析,最后分析结果由系统进行相应的采集,并将数据自动填写在相应报告模板上,最后出具电子报告。这是一个LIMS基本流程,LIMS的信息是围绕着样品展开的,目前很多LIMS拥有更多其他功能,如实验室标准品静态数据管理,实验室仪器校核管理,QA数据统计信息管理,实验人员培训管理等。同时对于每个流程都是可以设置电子签名的,并实时跟踪。适用于检测环境,如药检所、CMO等企业。LIMS应用于跟踪检测、生产过程中的各个阶段,包括采样与重新采样、分析,样品的接收、状态,产生与接收条形码,跟踪样品信息等实现以样品为中心的分析管理工作流。分析数据的中间计算和传输是由计算机自动进行,消除了人为误差和时间延误。根据产品的多级指标检查结果,可进行产品等级(规格)的判定及拒绝超指标的结果输入,可使用声音等多媒体技术进行报警,同时可对结果进行趋势分析。在线提供最新数据和历史数据,这使得实验室管理人员以及有关生产人员可以很快地得到及时而准确的信息。实验室将管理的更加有序和有效,能很快调整去适应新的变化和更高的要求。 库存管理解决方案 库存管理解决方案(Chemical Inventory Management System,NeoSuite CIMS),主要是解决实验人员、库管人员、财务人员等不同的问题提供的专业的库存管理解决方案。对于生命科学领域和材料科学领域来说,化学品库存管理有一定的特殊性,专业的化学品库存管理软件支持化学试剂精确结构检索、子结构结构检索、组合检索、其他字段检索等各种检索功能,快速便捷的帮助实验人员在线提交申领、申购请求,并对申领申购的过程进度进行查看,提高了实验人员获取试剂、耗材等物品的效率。能够完成对试剂、样品、耗材等物品进行申领、申购、订单生成、跟踪、审核、入库、出库、盘库、精确称量分装、库存统计等相关库存管理功能,极大节约了盘库所需的时间,条码扫描枪的使用以及天平关联自动称量重量信息使得入库、退库、盘库工作效率更高且信息更准确。精细化库存管理,实时准确的库存信息,保证实验人员查询到准确的数量、位置信息;最低库存量预警,库存管理人员能够及时采购和备库,保证备库试剂充足的需求量。企业内部化学品信息共享,减少重复采购同类试剂的现象,极大的节约采购成本;由于回收试剂再利用率高,也减少了因试剂浪费增加的成本。试剂存储使用的风险性降低,对于毒性试剂、放射性试剂等危险性化学品种,系统管理加线下双人双管制度,在符合国家管理法规情况下,降低危险性系数。 随着制药技术的发展和监管部门带来的压力,研发型企业更加注重覆盖研发全流程的解决方案。实验的设计,实验的执行,结果的分析,研究报告的产生,实验室资源的管理以及仪器原始数据的管理等等繁杂的内容,在漫长的科技创新生命周期中起着至关重要的作用和价值。统筹规划整体的研发信息化解决方案,避免一个一个信息系统成为数据孤岛,以积累企业数据、信息、知识为核心目的,切实可行的改善企业对知识和组织的管理模式,通过信息技术带动研发管理和决策模式的变革和创新,才能真正提高产品质量、生产率、投资回报率和法规依从性,应对当下研发企业所面临的巨大挑战。
百态
2015.10.29
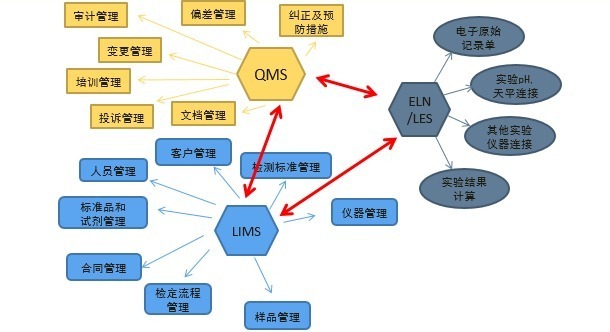
现代无纸化检测实验室(LIMS系统)
相信无纸化实验室的概念在每个医药以至检测行业人员的工作中会被经常的提起,那么检测实验室无纸化仅仅是为了节约纸张,或者让实验室人员摆脱手写工作的繁琐吗? 答案必然是否定的,只有全面了解现代检测实验室无纸化即信息化整体解决方案,才能更清晰了解信息化能够给检测实验室带来的好处,以及现有信息化前进的方向。 提到实验室信息化,最耳熟能详的就是 LIMS 系统(Lab Information Management System)实验室信息管理系统,早在 20 世纪 60 年代末,LIMS 系统受到当时计算机硬件条件限制,仅能单机完成简单的数据处理,到 20 世纪 80 年代随着实验室仪器的自动化水平大大增强,实验室在单位时间内能完成的测试任务量得以大大增加,同时计算机数据处理能力及数据吞吐量的极大提高,使得采用计算机信息系统来自动管理实验室成为可能。1982 年世界上第一套商品化的 LIMS 被推出市场并获得成功。进入 20 世纪 90 年代随着 Internet 的发展,LIMS 实现了跨地域的全球部署,为大型跨国企业提供了统一的质量管理支持平台。 LIMS 系统实现了检测样品的录入,分配,检测,判定,审批,报告发布以及数据分析整个流程的自动化和统一化,改进了实验室工作方式,将人员从繁琐的重复工作中解放出来,更加关注企业以及公司质量的提升。于此同时实验室运转必不可少的人机料法环也被 LIMS 系统统一管理。 除了样品流转过程的中文件和数据,实验室中大量的文件和原始数据产生于测试过程中,如何将检测过程实现无纸化,分析仪器的数据采集是关键,仪器中分析数据能否自动准确又便捷的传入实验室信息化系统中,直接影响着实验室工作效率和测试结果的准确性。实验室仪器连接和数据采集问题不能很好的解决,所谓无纸化实验室也只能流于表面,只是一句空话。针对实验室原始记录的电子化,电子实验记录本 ELN/LES(Electronic Lab Notebook/Lab Execution System)应运而生。电子实验记录本模拟所有检测实验员习惯的纸质文档操作流程,同时提供计算机系统自动化所带来的所有便利优势:在网络中安全访问最新审批过的方法,直接读取仪器数据至系统中,避免誊抄错误,实验终点即为原始记录终点,保证原始记录及时性。 在检测过程中会用到大量的质量文件,从质量手册到测试方法 SOP 各类文档,同时在检测过程中有相应的质量事件产生,如检测结果超标,偏差产生,以及客户投诉等等,在处理质量活动时,有可能会触发重新测试,SOP 升版以及人员再培训,在质量活动管理系统 QMS(Quality Management System)中,以上活动都被集中并与上述 LIMS,ELN/LES 系统无缝集成,完成整个质量活动的闭环处理。 LIMS,ELN/LES 和 QMS 系统三者无缝整合,实现对检测实验室从样品流程,检测过程及原始记录,以至实验室质量活动的全面管理,构成完整的无纸化实验室信息化管理解决方案。检测实验室无纸化管理可以带来以下显著成效: 1.规范实验室管理: 通过改进管理手段,系统严谨的程序控制可以防止人的随意性和惰性,保证产生的实验数据真实、完整、可靠,不易更改,消除有痕迹,可追朔性和多重关联性,从而提高管理效率,实现标准化规范化管理。 2.提高实验室工作效率: 通过改革工作模式,通过全息数据、多重关联和系统时序性自动记录,整个系统通过发挥机械特性,提高工作效率和水平,实现自动化和无纸化。 3.实现实验室数据共享: 改善数据管理状态,通过数据集中储存和数据筛选分析,提高检验数据的利用率,挖掘分析数据潜在价值,实现质量预警和质量数据在企业范围内共享。并且通过与 SAP 等企业资源管理系统提供友好的灵活界面,便于组织内统一质量信息的分发,提高运作效益。 4. 提高合规性: 实验室活动以及质量活动被记录在经过验证的计算机系统中,系统在符合 GxP 要求下,提供综合的功能以利于符合美国联邦法规第 21 章第 11 部分(21CFR Part11)、优良自动化制造规范(GAMP)和 ISO 17025 标准。 实验室信息化系统给检测实验室带来的不仅仅是无纸化的工作方式,它将随着科技的发展日新月异给企业发展带来持续不断的支持!
商机
2015.10.22
信息化助力四川科伦药业 当选2015全国工业企业质量标杆
近日,工业和信息化部发布了“2015年全国工业企业质量标杆”名单,33家工业企业的典型经验被确定为今年的全国质量标杆,在仅有的2家制药企业中,四川科伦药业股份有限公司的“推行质量管理体系信息化的经验”成功入围。此次质量标杆企业的评选活动代表着国内两化融合的又一次成功实践。 “两化融合”即信息化和工业化高层次的深度结合,2014年国家工信部先后颁布了《信息化与工业化深度融合专项行动计划(2013-2018年)》(工信部[2013]317号),以及《信息化与工业化融合管理系统要求》(试运行)等文件,号召并鼓励企业以国家标准认定的形式落实“两化融合”战略。 科伦药业的子(分)公司遍布全国各地和海外,为了克服地域上的分散性,避免管理碎片化,保证质量管理活动数据的一致性,同时让公司总部能及时获知所有子(分)公司质量活动数据和信息,从2014年开始,公司逐步在全集团范围内推广实施实验室信息管理系统(LIMS)和质量管理信息系统(QMS)。北京创腾科技有限公司作为科伦药业的实验室管理系、质量管理信息系统的供应商和实施方,从2012年开始便与集团信息部门及各业务部门紧密合作,相继在新都基地、湖南科伦、江西科伦等多地成功实施实验室信息管理系统,为集团“量化融合”提供基础支持。 2015年,北京创腾科技在原有实验室信息管理系统(LIMS)的基础上,将更进一步为科伦药业提供质量管理信息系统QMS的服务,为科伦药业打造无断裂、无障碍的封闭型质量管理体系。 值得一提的是,本次标杆仅有的两家制药企业的另外一家天士力制药集团,也正在使用北京创腾科技有限公司自主研发的试剂库存管理系统NeoSuite CIMS,该信息系统针对天士力制药部门的实验人员、库管人员、财务人员的不同问题,提供了完整的解决办法,对于实验人员来说,提供了简洁的检索和申领界面,方便即时提出申领申购请求,并对申领申购的过程进度进行查看;对于库管人员来说,提供了查询和处理申领请求的全部功能模块,并在试剂和样品出入库,配送,试剂和样品自动化盘库方面提供了全面的支持。相信随着系统的实施和上线,NeoSuite CIMS将推进了天士力信息化与工业化建设,大大提升了集团精益制造水平。
厂商
2015.09.17
天津港爆炸 危化品运维何去何从
截止今日,天津港爆炸事件共造成上百人死亡,其中包括大量的公安消防官兵,现场如战场,浓烟滚滚,一片狼藉。将近700人受伤住院,五六家物流公司全部被炸毁,8000多辆刚刚组装下线的新车被损毁。天津港爆炸这场事故在同类事故中堪称情况最复杂、伤亡和损失最严重。 令人心痛的消息不断传来,悲痛欲绝的家人和关切的群众不停的质问,究竟是什么原因导致的,为什么会有这么多无辜的民众、消防员受重伤甚至丧失性命?北京军区参谋长史鲁泽说,爆炸地点瑞海仓库现场集装箱堆积如山,各种集装箱、物品混杂在一起。由于危险品数量和内容存储方式不明,救援工作只能通过现场情况和瑞海公司近期出口数据来判断可能存在氰化钠、硫酸铵、硫化钠等多种危险品。现场的混乱为危险品的寻找带来一定难度,通过与氰化钠来源的河北诚信有限公司确认了现场存在700多吨氰化钠,可怕的是,一旦地下水或附件海域受到这些剧毒品的化学成分的污染,后果不堪设想。而瑞海公司的人也说不清楚氰化钠具体堆放在哪里。经过专业人员多次冒着生命危险进行现场勘察才基本确定了位置。 复杂的情况加大了事故处理的难度,现场多种化学品遇湿遇水容易发热并爆炸,化学反应会导致爆炸情况的加重。情况及其复杂和危险,然而由于没有及时给予消防人员专业的指导,从而导致了惨剧的加重。危险品仓储管理混乱,缺乏有效的追踪 瑞海公司资质的获得、危化品仓储的选址、危化品储存的操作流程等领域所可能存在的“不专业”甚至于违法行为,都可能是此次事故发生的原因所在。危化品堆放场所不符合危化仓库的标准,更像是危化品堆积场所,一般化工品与危化品码放在一起,品种太多太杂,外人根本无法辨认区分。堆场中的禁忌物料都在一起,很容易顾此失彼,救了一个点了另一个,施救根本就没地方下手,即便是专业的救援的来了也只能听之任之。 具幸存的员工反映,他们没有经过任何危化品的培训,根本不知道如何处理进入港内的危化品,甚至不了解其危险程度。严格管理危化品物流公司资质,提高信息化监控水平 如果危化品的存储位置、存储数量、出入库记录都可通过信息化的手段追踪,当地拥有专业的危化品事故处理团队或应对措施,第一时间到达现场的消防员能获得仓储信息和处理方法,事故的损失也能大大降低。 目前,中国“物流体系”中每年有两亿吨危化品在运输路上或者仓储之中,如何提升危化品生产使用、仓储运输和事故应对等领域运营和监管的水平?恐怕除了严格审核危化品物流公司的资质、选址,专业的进行仓库建设之外,只有通过信息化手段实时监控危化品的仓储管理。 精细到准确的仓储位置、数量、出入库动作,保证能够实时监控仓库管理信息;异地备份信息化数据库,即使现场通讯障碍的情况下也能有备选方案查询和追踪危化品位置、数量以及处理办法信息。(如果你感兴趣,想要了解NeoSuite CIMS能为你提供什么帮助,请联系我们获取更多的信息) 甚至对于所有接触危化品的员工进行专业的培训严格考核,做好风险控制措施,在应对突发的危险事故时有专业的指导方案,专业的事故处理团队,准确的定位、迅速找到合适的解决方案,才能最大限度避免悲剧重演。 创腾科技官方微信北京创腾科技有限公司联系人:张小姐 电话:021-58353866转255邮件: zhangjinjin@neotrident.com; market@neotrident.com
百态
2015.08.18
"2015 Phoenix技术与应用中国行" 研讨会邀请函
美国Certara公司与北京创腾科技有限公司(以下简称“创腾科技”)在过去的三年中携手为中国地区Phoenix软件用户提供了优质的服务与技术支持,并在国内不同城市举办系列Phoenix培训班,得到国内用户的广泛欢迎和高度评价。为了回馈中国地区Phoenix用户,同时也向国内广大的从事DMPK、PKPD研究的科研人员分享Phoenix系列软件的最新动态和发展方向,美国Certara公司与创腾科技计划于2015年10月16日(周五)在北京东方君悦大酒店举办Phoenix Road Show活动,本次活动不收取任何费用,我们诚邀各位专家学者的参与! Phoenix系列软件包括了Phoenix WinNonlin、Phoenix NLME、IVIVC toolkit for Phoenix WinNonlin、Phoenix Connect与Phoenix Validation Suite等,其业已成为工业界的金标准。在世界范围内,大型制药与新药研发企业无一例外的选择了Phoenix系列软件。事实上,全球已有超过1500家企业与学术机构正在使用Phoenix WinNonlin与其他Phoenix工具。更重要的是,包括FDA在内的主要药物监管与评审机构也在使用Phoenix对新药进行检查与审批。在本次Road Show活动中,我们将与大家分享来自Certara公司咨询团队的专业经验与经典案例。 Phoenix Road Show活动将为来宾传递最及时、有效的信息,无论是初学者或者高级专家、实际用户或者管理层,不论你在新药研发流程中的角色如何,都将从本次Road Show活动中获益。会议主要内容包括:· 学习如何使用最新版Phoenix的向导及模板功能来简化工作流程· 了解更多有关如何遵从即将到来的CDISC-SEND标准以及药品监管机构的动向· 构建一个更加紧密的PK/PD研究策略,为临床前、毒理/安评、以及临床研究组之间建立桥梁· 学习如何根据需要组织一个全面的研究项目,如“首次人体试验”· 我们的知名顾问为您介绍如何构建一个定量药理学策略,以及PK/PD最新的法规指南· 从业界同行的实例中学习并扩展Phoenix新的使用方法与思路 我们还将邀请北京协和医院临床药理中心胡蓓教授及其研究团队参与到本次Phoenix Road Show。该团队是Phoenix系列软件多年的用户,在定量药理学研究领域有着极其深厚的实力与非常丰富的研究经验。胡蓓教授及其团队将在活动中带来精彩的报告与案例分享,并与参会来宾共同就热点问题与领域交流探讨。会议详情及参与方式会议时间:2015年10月16日(周五)全天会议地点:北京东方君悦大酒店 ( Grand Hyatt )会议地址:东长安街1号东方广场会议费用:免费主 办 方:美国Certara公司、北京创腾科技有限公司参会对象制药企业(公司)的新药研发人员,医院、医药科研院(所)、药检单位和医药高等院校中从事药代动力学与药效动力学、群体药代动力学、定量药理学的科研人员,或对该领域有研究兴趣的药物研发工作者。参与方式· 参加费用:免费· 报名时间:2015年7月20日-10月15日· 报名人数:会议最大规模80人,以报名先后顺序排位,额满截止!· 报名方式:以下两种方式任选其一。 1)邮箱报名:登入创腾科技网站:www.neotrident.com下载word版报名回执 ,发送到market@neotrident.com信箱。 2)手机报名: a、扫描并识别以下二维码后点击‘我要报名’ b、或关注公众微信“创腾科技服务号”(微信号:market-NT), 点击研讨会专栏中‘立即报名’。 * 微信分享有礼:将活动分享到朋友圈,并积齐5个点赞,您就可以在参会现场凭借截图领取一个保温杯!· 报名说明: 1). 每个单位最多2~3个人; 2). 因为要预约会场及午餐,请务必确保报名人员出席; 3). 若临时取消报名: a. 通过手机报名的客户请务必在手机报名页面点击‘取消报名’。 b. 通过邮箱报名的客户务必通知到会务组工作人员。交通路线地铁:乘坐1号地铁,从王府井站或东单站A出口出站,步行到酒店的距离约300米。会务联系:创腾科技有限公司电话:021-58353866转242(曹小姐); 021-58353866转233(陈女士) 13911435596(张先生)Email:market@neotrident.com;Web:www.neotrident.com
会展
2015.07.27
辉瑞消费保健品部门LIMS系统的成功迁移
从LabManager转换为SampleManager LIMS1 项目背景 辉瑞消费保健品部(简称为PCH部门), 为Warner-LambertLLC公司旗下一个部门, 该公司为辉瑞的全资子公司。辉瑞选择在其位于新泽西州Morris Plains的消费保健品总部的负责多元化业务的分析实验室使用Thermo FisherSampleManagerLIMS系统来替代原有的LabManagerLIMS。该部门的主要产品为Benadryl?,Neosporin?,Sudafed?和Visine?,拥有35亿美金的效益。本文将着重介绍辉瑞PCH部门如何顺利地将原系统迁移到Sample ManagerLIMS,包括稳定性的数据以及活性物质的研究的迁移。 2 系统状况 2002年辉瑞PCH研发部门在位于Morris Plains的负责多元化业务的实验室中开始使用Lab Manager 8.4a系统,约有70个系统用户。该系统于1998年完成版本更新,较早版本于1990年代初期完成部署使用。 基于以下原因辉瑞PCH部门决定升级其实验室信息管理系统: · 原有LabManagerOpen VMS系统支持变得日渐困难且该系统面临淘汰的处境 · 原有LabManager系统不再能满足PCH研发部门日渐增长的业务需求,包括安全性,网络接口,以及电子通讯方面的需求 · PCH研发部门强烈需要在统一的系统中追溯稳定性数据 基于以上原因,PCH 研发部门决定制定一个新的LIMS产品的选择标准,他们组织了一系列的人员来起草用户系统需求,从而保证系统可以更好的支持他们将来的工作。核心团队来自于分析实验室,稳定性及校准部门,实验工厂,制剂和产品研发部门,原辅料部门,质量保证部,以及IT部门。在这之前整个LabManagerLIMS运行是由分析实验室人员来负责的,没有任何PCH全球商业技术的参与。在新的LIMS项目中PCH全球商业技术将会参与负责整个项目管理和持续进行的系统维护。新的LIMS系统将会在全球商业技术的支持下满足所有PCH全球商业技术提出的系统开发标准。 3 新解决方案的可接受标准 PCH研发部门在寻找一个可高度配置的LIMS并附带尽可能多的额外功能来避免客制化LIMS而带来的额外费用,资源,以及时间。这个解决方案需要同时满足PCH研发部门的业务需求并能对终端用户有吸引力。 细化的需求由系统用户提出,涵盖了业务,技术,安全以及法规方面的各项需求。 负责PCH 研发部门实验室信息系统的经理Eric Kopp说道:我们没有提出任何关于系统可以完成哪些任务的设想,我们只是很清晰的表达了我们需要什么。 4 选择ThermoFisher的Sample Manager LIMS 通过业界领先的LIMS供应商ThermoFisher的演示,以及根据系统针对相应用户需求的符合程度来评分,Sample Manager LIMS成为了辉瑞PCH部门的首选解决方案。 Kopp提到:任何一家LIMS供应商的系统最终都能满足我们的需求,但是我们需要的LIMS系统能在最少的客制化前提下满足我们的需求。SampleManagerLIMS高度集成了开箱即用的功能。作为一个系统用户的角度来看,SampleManagerLIMS直观的界面特别受人喜欢,它一点儿都不复杂,很容易就可以上手使用并找到你所需要的数据。 VincentCantarella,负责PCH全球商业技术的项目经理,他说道:SampleManagerLIMS的高度可配置化可以在系统的长期使用中降低用户的管理成本,例如系统维护费用以及后续的系统升级费用。 SampleManagerLIMS满足PCH部门的所有技术需求,包括符合PCH部门制定的标准,操作系统以及数据库的兼容性。其中审计追踪,电子签名以及21CFR PART 11的符合性都是PCH部门标准的一部分。此外,PCH部门关键的业务需求如稳定性,原料,研发等等的需求也在最少的配置下得到满足。 另外Kopp也说道,辉瑞PCH部门很高兴选择了ThermoFisher作为系统供应商,ThermoFisher公司作为财富500强公司之一,在业界有良好的声誉。 VincentCantarella和Erik Kopp分别代表PCH全球商业技术和商业项目领导,共同提出了项目的提议,该提议包含了系统实施的商业理由,经费来源,可支配的资源以及大致的项目周期。 系统项目的投资和SampleManagerLIMS账号的批准于2003年3月完成。 5 实施和验证 辉瑞PCH部门选择了第三方供应商来负责系统的集成,验证,迁移以及培训。系统集成和验证用时13个月,系统于2004年4月上线。在SampleManagerLIMS上线运行的过程中,PCH部门面临着稳定性项目的转移以及从原系统LabManagerLIMS至SampleManagerLIMS转移数据。 6 数据转移 在项目前期,PCH研发部门评估了数据迁移的以下可能性: 1. 不做历史数据迁移,在SampleManager LIMS中录入新的研究项目; 2. 只迁移已完成的稳定性研究数据(从LabManager到SampleManager); 3. 或者迁移已完成和进行中的稳定性研究数据到SampleManager LIMS中。 项目背景调查表明全部数据迁移并不是一件容易的事情。尽管如此,PCH部门还是研究了哪些迁移是有可能性的并发现了PowerCenter by informatica,一款Thermo Fisher旗下的工具型软件,该软件是为用户从原有LIMS系统到新LIMS系统进行数据迁移而量身打造。这样PCH部门将可以将所有已完成和进行中的稳定性研究静态和动态数据成功导入SampleManager LIMS系统中。同时也可以完成仪器相关信息的迁移,不再需要人工录入大量数据。 辉瑞PCH部门之所以决定迁移所有的稳定性数据,是因为稳定性研究一般都会持续3-5年,并且在原有系统中存在着大量的正在进行中的稳定性研究数据。考虑到原LIMS系统的运行寿命且系统维护难度的增大,且PCH部门想要在单一系统中追溯数据。PCH作为一个卫生保健用品的研发实验室有着对稳定性研究整个生命周期相关数据的管控需求,所以PCH的目标是在一个单一的系统数据库中维护实验数据,以便能轻松地,持续不断地出具报告,同时避免维护旧的,孤立的,只能用作数据储存的系统而产生的额外费用。 在2003年12月到2004年9月间,当正式的数据迁移开始时,PCH部门经历了相当从容的过程,包括概念论证,开发,测试以及验证。核心团队以验证从原有LabManager系统到SampleManager数据迁移是否合格为目的而编写了相应的验证测试脚本。验证的目的是为了确认迁移的数据是否被转移到了正确的位置,迁移的数据量是否准确,和迁移后的数据和报告是否和从前一致。同时也验证了SampleManager LIMS系统是否能够处理迁移进来数据,并且和处理在SampleManager中直接生成的数据没有差别。 LabManager和SampleManager LIMS曾在几个月时间内在实验室同时运行,但这种网络效应被Kopp显示称赞为“最佳的方案…因为我们做了更好的质量保证工作并在一开始就做对了”。 真正的数据迁移发生在一个周末,整个迁移过程没有对任何一个用户产生影响。 “我们做了如此之多的计划和测试,我们确信它会成功“Kopp先生说道。数据成功迁移之后没有系统发生任何故障,SampleManager LIMS系统在PCH部门研发实验室按照客户预期运行良好,而且受到了辉瑞PCH部门系统用户的广泛接受。
厂商
2015.07.03
蛋白质理性设计学术研讨会 暨Discovery Studio 4.5软件培训(免费)
尊敬的老师和同学,您好! 创腾科技有限公司将联合华南理工大学生物科学与工程学院于2015年7月3日在广州举办为期1天的“蛋白质理性设计学术研讨会暨Discovery Studio4.5软件培训”,将为大家提供一个蛋白质理性设计领域面对面讨论与交流的机会与平台。 随着2013年诺贝尔化学奖的揭晓,美国三位科学家Martin Karplus, Michael Levitt与Arieh Warshel因其发展的分子模拟方法对生命科学领域发展的贡献而获奖,这从根本上承认了计算机模拟预测在生物学领域的贡献,分子模拟工具已经成为了生命科学家不可或缺的预测工具。Discovery Studio(简称DS)作为面向生命科学领域的综合性分子模拟平台,在生物制药、生物领域的应用已日趋成熟与完善,也为蛋白质理性设计提供了最先进的分子模拟工具。 研讨会将邀请中国科学院广州生物医药与健康研究院的刘劲松研究员和暨南大学生命科学技术学院的姚冬生教授分享他们在蛋白质理性设计领域的成果、经验与最新进展。同期的培训会,创腾科技技术支持专家将以Discovery Studio4.5软件的基础操作和应用为核心,以蛋白质理性设计为基础,针对蛋白质理性设计中所涉及的技术进行介绍与上机操作,包括:基于蛋白的一级序列预测蛋白的三维结构、蛋白-小分子/蛋白相互作用预测、通过虚拟氨基酸突变设计亲和力更高或稳定性更高的蛋白、预测并引入新的二硫键提高蛋白酶的稳定性、预测蛋白结构表面易聚集的位点并进行突变优化等等。会议基本信息会议时间:2015年7月3日(周五)会议地点:华南理工大学生物科学与工程学院1楼机房具体地址:广州市番禺区外环东路382华南理工大学大学城校区会议主题:蛋白质理性设计日程安排详情请登入创腾科技网站:www.neotrident.com 培训电脑参加7月3日下午培训的学员需自带手提电脑,手提电脑推荐配置如下:DS4.5安装所需的系统环境:Windows 7 (Professional & Enterprise完整版)64位;硬件要求:- Processor: Intel-compatible processor ≥2 GHz with x86_64 architecture- RAM: ≥4 GB of memory- Disk space: ≥20 GB disk space - Graphics card: ati or nvida independent graphics recommended- Mouse: Standard Microsoft 3-button mouse or 2-button wheel mouse关于软件安装、卸载的特别说明此次安装的DS4.5软件仅限于2015年7月3日培训使用! 7月2日下午 14:00-17:00,7月3日上午8:00-13:00,由北京创腾科技有限公司的工程师在华南理工大学生物科学与工程学院1楼机房,负责为下午参加培训的学员安装DS4.5软件,并在培训结束后统一卸载。 对于安装过软件的学员,在培训结束后,需积极配合工程师的卸载工作,并承诺不将软件用作文章发表或者其它任何商业用途,对于不配合软件卸载工作、将软件用于文章发表或者其它任何商业用途的学员,北京创腾科技有限公司将保留追究其法律责任的权利。 对于确认报名参加此次培训的学员,均视作已阅读、知晓并同意以上全部内容。报名方式报名详情请登入创腾科技网站:www.neotrident.com 额有限,报名从速,额满为止。为保证研讨会质量,广州学术研讨会计划招生40名学员,额满为止。
会展
2015.06.17
Discovery Studio软件暑期基础培训班通知
尊敬的老师和同学,您好! 创腾科技有限公司主办的Discovery Studio软件技术应用暑期培训班至今已举办过十三次,培训班得到了来自全国各行业各领域企业和高校的专家、老师和学生的积极响应和热情支持!根据广大Discovery Studio用户和其他从事生命科学研究人员的要求,创腾科技将于2015年暑期再次在上海(7月13-17日)和北京(8月10-14日)各举办一场计算机辅助药物设计和大分子模拟技术基础培尊敬的老师和同学,您好! 创腾科技有限公司主办的Discovery Studio软件技术应用暑期培训班至今已举办过十三次,培训班得到了来自全国各行业各领域企业和高校的专家、老师和学生的积极响应和热情支持!根据广大Discovery Studio用户和其他从事生命科学研究人员的要求,创腾科技将于2015年暑期再次在上海(7月13-17日)和北京(8月10-14日)各举办一场计算机辅助药物设计和大分子模拟技术基础培训班,每班各为期五天。 随着2013年诺贝尔化学奖的揭晓,分子模拟技术终于修成正果,分子模拟工具已成为生命科学家不可或缺的预测工具,分子模拟技术也将会得到越来越多的认可和更为广泛的应用。如果您对分子模拟技术和分子模拟平台Discovery Studio感兴趣,想要全面了解DS中各种模拟技术的基础原理与应用,并能快速进行上机操作,那么您可以趁暑期参加我们的基础培训班,培训安排如下: 培训基本信息 上海基础班 课程时间:2015年7月13日-7月17日(周一至周五训班,每班各为期五天。 随着2013年诺贝尔化学奖的揭晓,分子模拟技术终于修成正果,分子模拟工具已成为生命科学家不可或缺的预测工具,分子模拟技术也将会得到越来越多的认可和更为广泛的应用。如果您对分子模拟技术和分子模拟平台Discovery Studio感兴趣,想要全面了解DS中各种模拟技术的基础原理与应用,并能快速进行上机操作,那么您可以趁暑期参加我们的基础培训班,培训安排如下: 培训基本信息 上海基础班 课程时间:2015年7月13日-7月17日(周一至周五) 课程地点:上海创腾科技培训中心(上海浦东新区芳甸路1088号紫竹国际大厦2104室) 北京基础班 课程时间:2015年8月10日-8月14日(周一至周五) 课程地点:北京大学计算中心二层2号机房 培训主旨 在基础培训班中,您将了解和上机操作Discovery Studio新版本4.5的所有模拟技术,整个培训的技术专题包括:蛋白序列分析、翻译后后修饰位点预测(New!)、线性抗原表位预测(New!)、蛋白质结构预测、抗体结构预测(New!)、抗体人源化改造、酶-底物作用机制预测(Update!)、蛋白-蛋白(核酸/多肽)相互作用预测、蛋白质设计、抗体设计&优化、蛋白质工程、分子动力学模拟、分子力学(New!)/量子力学模拟、基于靶标结构的药物设计(分子对接)(Update!)、虚拟筛选、全新药物设计、Me too/me better药物设计、骨架跃迁、基于小分子配体的药物设计(药效团模型)、组合化学及组合化物库分析、QSAR和ADMET性质预测等。 培训内容 针对Discovery Studio4.5在药物设计和计算生物学领域的每个应用技术专题,完整的培训内容包括三大部分: 1、 基础方法和技术原理的讲解 2、 软件的基础操作与上机练习 3、 该模拟技术与实际科研工作的结合(文献案例的简单讲解) 每位培训学员有充分的时间对培训班的每个技术点进行软件的上机操作(提供完整的培训教程),我们的工程师将全程提供技术服务。培训班结束后,我们将向每一位学员颁发创腾科技有限公司的生命科学模拟软件技术认证证书。 培训费用 培训注册费:RMB 4000元/人 优惠条件: 1. 若同一单位同时有四人或超过四人参加同一培训; 2. 上海基础班在7月1日前汇款; 3. 北京基础班在8月1日前汇款; 符合以上任何一个条件, 均可享受优惠价格RMB 3200元/人 注: 1、培训费包含听课费、资料费、上机费、午餐、晚餐。住宿和交通费自理。 2、统一开据发票内容为 “培训费”,发票将在培训期间发给学员,若您对发票内容有特殊要求请务必在回执中注明。 报名方式 报名请登入创腾学院网站:http://training.neotrident.com/ 欢迎感兴趣的老师和同学踊跃报名。名额有限,报名从速!
厂商
2015.06.12
互联网时代实验室的数字化革命
互联网时代实验室的数字化革命 转载中国信息化周报 近日,第二届数字化实验室建设与应用研讨会在上海召开,会议围绕在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、质量保障、数据分析以及效益收率等关键问题进行探讨。 如今药品的质量和安全日益受到广大消费者的关注,政府监管机构也出台严格的政策办法一确保药品安全和维护消费者权益,药品生产企业竞争日益激烈,药品质量需要不断提高,各企业面临着许多挑战和困难。同样在材料研究、石油、化工等企业里,这些问题也都存在。近日,第二届数字化实验室建设与应用研讨会在上海召开,会议围绕在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、质量保障、数据分析以及效益收率等关键问题进行探讨。大会还邀请到来自药监、药检系统的相关领导、国际国内临床试验专家和医药、石油、材料等领域研发与生产部门的高层管理人员。与会的各级领导和企业代表嘉宾踊跃发表各自观点,进行了全面并且有针对性的研讨,为研讨会的成功举办添上了浓墨重彩的一笔。大会现场嘉宾提问 数字化实验室建设任重道远 数字化实验室建设任务艰巨,一方面工作人员要在很枯燥的过程中持之以恒地长期坚持。数字化的价值不能立竿见影的体现,数字产生价值需要积累和沉淀。只有当数字积累到一定程度时它的价值才会体现出来。同时要改变一些传统的工作习惯,这对从业人员是一项挑战也是一种考验,所以,数字化实验室建设应用过程是艰难的。北京创腾科技有限公司总经理曹凌霄表示,“一个新系统如果能上线并且能够成功应用其实是一件非常不容易的事情,这里面凝结了许多人的心血,包括知识的传承、经验的积累、教训的积累等,而系统是千差万别的,很多单位和很多公司的系统各不相同,但是其中也会有很多共享的地方,我们希望搭建一个平台,大家能在这样的平台里做一些充分的交流,使我们信息化的建设能够走得更快一点。” 另一方面,数字化实验室建设与应用往往取决于领导对此的重视程度。制度的建设对于数字化实验室、大数据应用有重要意义。很多样品和数据库的进步与否,关键问题是在规范积累和共享。将此作为“一把手”工程有利于制度的建设,利于数字化实验室迅速准确的找准方向,少走弯路绕路,提高数字化实验室建设与应用的规范度。中国石油化工股份有限公司石油化工科学研究院信息中心主任周涵明确说道:“这是一把手的工程,尤其是涉及到核心的机密,涉及到核心实验数据时,没有领导的高度重视那么项目是不可能成功的。” 药业、科研数字化实验室建设 现在国家在深度进行两化融合,也在提倡工业4.0。什么是两化融合呢?四川科伦药业股份有限公司总监徐华林说:“对于我们来说实际上就是将业务和信息化高度融合。比如我们将供应链同信息化高度融合,将财务系统与信息化高度融合,将质量工作同信息化高度融合等。实际上是包含了我们实验室信息化,也包含了其他的质量工作的信息化。”他还表示,“公司的信息化建设是本着按照总体规划、分步实施、目标导向、持续改进的原则进行。” 实验室信息化是公司信息化的一个重要的组成部分,也是同其他公司信息系统的高度集成,是其将质量工作与信息化工作高度融合的具体体现。比如,随着业务的流程和进度,对系统的重要结点在于所有的数据实行了审计追踪,系统可靠确保了操作的有迹可查。徐华林总监报告称:“上新系统,对管理人员来讲,要掌握样品的状态以及完成情况都可以在系统里得到清晰和明确的结果,整体效率得到了大幅度的提升;对于成品的企业来讲,从原始检验记录报告的生成,审核放行效率大大提高了,提高了25%。”中国石油化工股份有限公司信息中心主任 周涵 药明康德新药开发有限公司分析和药政CMC服务部助理主任印勇在提到实验室信息化应用时,强调要调整实验室的流程,实现实验室的必要部分无纸化,同时确保数据质量。“因为在与客户交流的过程中,特别是一些欧美大的制药企业,他们一直在强调一个问题,就是实现过程控制。如果过程控制的非常好,他相信我们的结果肯定不会差的。所以我们想通过实验室的标准化流程,通过加强过程控制,确保所有的数据的产生都是在监管下,而且都是高质量的。” 而对于科研机构而言,科研创新支撑平台是一大重点,首先是实验记录的规范化和标准化。原来纸质的实验记录,这是目前电子的实验记录,这是规范化。其次是结构化,这是催化剂开发的环节,每一个环节都有相应的模板,高度结构化的同时也可以相互搭配,灵活性较强,数据易于提取,检索也很容易,为之后的数据挖掘提供了良好基础。“我们实现了现有相关信息化系统的数据整合,科研数据的关联性和完整性,多类型数据的综合展示等。通过系统的建设能够确保数据的完整性、安全性、可追溯性,数据真实性是有保障的。同时可以通过数据流处理的工作流,分析数据,通过可视化的工具可以提高综合利用率。”周涵主任这样说。 行业信息化建设展望 我国医药产业与国际接轨的步伐越来越快,在积累的过程中,如何保证药品的研发、生产、监督、检验领域里的实验数据的完整性、准确性、安全性、可追溯性等要求,是目前的重要课题。中国食品药品检定研究院陈为处长表示,“从理念上和观念上来讲,我认为我们这个领域,特别是药品食品检验检测机构,我们这个领域对实验室信息化整体的、全面的了解和对新技术、新理念的了解总体看来是欠缺的。”他表示希望大家互相交流,有更多学习和探讨的机会。 数字化实验室对数字的规范化起到至关重要的作用。数字化是信息化与大数据研究的基础,数字化建设将推动大数据研究和信息进一步的推广和应用。达到规范、优化、可控、可靠、高效的效果。周涵主任展望未来:“通过电子实验记录系统希望未来逐步形成标准化长期化的管理体制,有助于建设符合国际和国内标准的一流实验室。借助电子实验记录系统有助于科研数据的规范化和长期收集,为后续的数据挖掘和科研创新提供支撑。再有借助电子实验记录系统有助于实现工作流程的规范化,人员协作的无障碍化,提高效率,对课程进行监控。另外,借助电子实验记录系统有助于科研装备、分析仪器试剂和备建的统一管理,提高仪器设备利用率、投资采购效率及管理水平。” 医药产业本身极具特性,是以过程指导的行业,整体生产过程非常复杂,比汽车、飞机这种装配行业复杂得多。曹凌霄对此表示:“行业信息化的水平,相对来讲比较慢,因为我们是以实验为主,我们生产也是以过程为主。所以,这方面的工作我们要做很多非常非常辛苦的努力。”徐华林总监也说道,“如果把公司所有的信息系统生态组合起来,有质量的数据,有生产的数据,有消费的数据,这样维度比较多,如果还加上我们的社交数据,就真正是一个大数据系统。我们的愿景是通过整个公司信息化体系的建设,将所有的数据转换成公司的资产,为公司的决策和战略提供参考依据。” 北京大学徐筱杰教授对本次会议评价十分中肯:“数字化实验室建设与应用研讨会从去年开始,非常及时的关联了大数据时代。” 在“互联网+”时代,数字化实验室应需而出,会议有效提高了实验室数字化建设应用水平,有助于建设符合国际和国内标准的一流实验室。转载中国信息化周报
会展
2015.06.03
大会报告抢先看——“第二届数字化实验室建设与应用研讨会”第二轮通知
“第二届数字化实验室建设与应用研讨会” 第一轮通知发出后,得到了众多企业研发及管理人员和相关领域专家学者的积极响应和热情支持。本届会议将于2015年5月21日至22日在上海浦东御龙宴大酒店(御龙宴会中心)举行。会议主题为探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。大会将邀请到来自药监、药检系统的相关领导、国际国内临床试验专家、和医药、石油、材料等领域研发与生产部门的高层管理人员与会进行全面和有针对性的研讨。会议的各项筹备工作正在按计划顺利进行,我们真诚地邀请您参加本次大会。现将会议筹备情况及第二轮通知寄给您,请您仔细阅读。5月5日前报名可以享受优惠价格,报名截至日期为5月18日,请在此时间前提交您的参会回执,以便我们在会议召开之际,为您安排好相关参会事宜。大会演讲嘉宾介绍 徐华林 信息部部长,四川科伦药业股份有限公司 【报告题目】:科伦药业实验室信息管理系统应用与实践 作为国内第一个在医药生产QC检测环节实现无纸化的实验室,科伦药业将会分享信息化技术 给QC检测实验室带来的合规性及 效率的提升。周涵 信息中心主任,中国石油化工股份有限公司石油化工科学研究院 【报告题目】:信息化驱动的研究创新在中国石油化工股份有限公司的应用和展望分享如何通过信息化系统提升创新研究袁征 科技部处长,军事医学科学院 【报告题目】:数字化实验室圆梦科学创新 分享在大型科研院所建立数字化实验室平台的经验,通过该平台的建设,军事医学科学院各实验室逐渐形成标准化、程序化的管理体制,建设成为符合国际和国内标准的一流实验室。龚佑祥 分析和药政CMC服务部副总裁,药明康德新药开发有限公司 【报告题目】:CRO三方检测实验室信息化应用与展望 实验室信息化新系统在药明康德检测实验室的应用,总结和展望CRO三方检测实验室数字化、信息化的特点 Dr. Reza S. Sadeghi Managing Director Managing Director-Portfolio & Product Management, Dassault Systèmes BIOVIA 【报告题目】:Innovation by digital lab / 数字化实验室驱动科学创新 Share successful experience of BIOVIA solutions in helping science driven company to accelerate innovationWarren Perry Compliance Consultant, Dassault Systèmes BIOVIA 【报告题目】:Quality Management empowered by QUMAS 制药企业质量管理解决方案 Share experience and scucessfucl cases in how QMS system help life science company to meet the critical regulations of FDAIsaacs Mark Sr. Account Director , Dassault Systèmes BIOVIA 【报告题目】:Intelligent Process Product Operation Solutions企业工艺及生产过程管理智能化信息解决方案 The process development, manufacturing and quality functions generate an abundance of data, which needs to be utilized in a more user-friendly, organized (contextualized) form for improved process knowledge and production operations. Traditional manual methods, such as spreadsheets, are error-prone and waste valuable time. As organizations generate more data through implementation of QbD (Quality by Design), PAT (Process Analytical Technology), PR (Process Robustness), and CPV (Continued Process Verification) initiatives along with new manufacturing and measurement technologies, they need better ways to access and use their data. We will share experience, as well as successful cases, in process product operation, which provides process development, quality, and manufacturing users with self-service, on-demand access to process and quality data from disparate databases and paper records, automatically aggregates and contextualizes the data and enables hoc statistical investigations and analysis with automated validation-ready workflows to provide browser-accessible outputs for teams of observational users.李健 信息中心高级工程师,中国食品药品检定研究院信息中心 【报告题目】:药检系统实验室质量管理现状、及信息化应用展望 总结药检系统实验室的质量管理现状及问题,展望数字化技术和信息化技术在药检系统各方面的应用。沈晓航 生物分析服务执行主任,药明康德新药开发有限公司 【报告题目】:生物分析实验室电子数据管理分享如何通过信息化系统满足 GLP 分析实验室的严格要求代志龙 信息中心主任,中国航天科技公司第42研究所 【报告题目】:Sample Manager在研产结合性企业的应用分享军工研究所实验室信息化建设经验贾宁 行政物流部高级主任,药明康德新药开发有限公司 【报告题目】:Neosuite CIMS在医药研发企业的应用分享试剂库存管理系统给企业带来的收益李川 科研处副处长,中国科学院上海药物研究所?【报告题目】:基于风险防控的实验室采购网络化管理系统? 作为国内药物研发的顶尖学术单位,基于风险防控原则,分享实验室信息化在上海药物所实验室采购管理方面的应用。胡康 高级工程师,中国食品药品检定研究院信息中心【报告题目】: 药检系统数据整合、数据分析的若干应用实例 大数据分析背景下,介绍科学数据整合和数据分析在药检系统的若干成功应用案例,结合药检系统的信息化建设思路,展望智慧药检。尹利辉 主任,中国食品药品检定研究院 标化所【报告题目】:国家药品快速检测信息平台的建设国家药品快检数据库网络平台的建设背景、规划与设计、建设目标、关键技术、应用情况。李杨 院长助理,浙江省食品药品检验研究院 【报告题目】:浙江药检院LRP平台经验分享分享浙江食品药品检验研究院信息化LRP平台的建设经验及应用郭志杰 IT部主任,三角轮胎股份有限公司【报告题目】:三角轮胎信息化与LIMS——研发大数据应用分享管理系统在三角轮胎中研发数据的应用经验沈陵陵 信息部副总监,诺华(中国)生物医学研究有限公司【报告题目】:Informatics for local Analytical Platform / 信息技术在NIBR分析平台的应用 NIBR Shanghai Analytical Science (AS) is a group focus on biological targets characterizing, hits validating, MOA understanding, and leading compounds analyzing through collaboration with biology, chemistry, and translational science group. NIBR Shanghai Informatics (NX) facilitates research in the use of IT resources and tools, as well as provide leadership by introducing researchers to the best new IT resources that are available. Here we present 3 projects which was delivered through close collaboration between AS and NX, from which scientists has been released from heavy manual tracking and calculations. This developing workflow also provide more opportunities for NX to collaborate with other scientific groups.Here is the 3 projects in brief summary: (1) AWM : automatically report processing tool for small molecule characterization. (2) ADC : tracking and data archiving of macro molecules experiments. (3) HIS : tracking and visualization of compound treated histone profiling experiments.涂健 分析测试中心主任,西安近代化学研究所(204所)【报告题目】:数字化理化检测实验室建设方案初探分享实验室管理系统的建设经验熊茵 主任,药明康德新药开发有限公司【报告题目】:实验室内部及不同实验室间电子数据的传递和对接 分享不同实验室或不同平台间电子数据的传递和对接;CRO和客户之间的数据转移;实验室内部不同平台间的数据传递的经验。刘兴东 高级客户经理,Thermo Fisher【报告题目】: 法规依从性下的变色龙CDS 变色龙色谱数据系统不仅遵循诸如GLP、GMP 、21CFR Part 11等规范的要求,且拥有丰富智能的功能,并已延伸至质谱领域。报告将围绕法规依从性主题,介绍新形势下CDS工作站面临的挑战和基于,阐述变色龙CDS如何满足上述法规要求。冯华 技术部副总,北京创腾科技有限公司【报告题目】:数字化实验室4.0介绍国内生命科学、材料科学的数字化实验室建设的阶段及4.0版本会议日程安排5月20日(周三)下午:注册报到 地点:万信酒店5月21日(周四)全天:大会报告 地点:御龙宴会中心6层大会议题: 探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。议程安排:07:30-08:30 报到注册(所有参会代表需佩带会议胸卡入场) 08:30-09:00 会议开幕式09:00-10:00 大会报告 (每个报告30分钟)10:00-10:30 茶歇10:30-12:00 大会报告 (每个报告30分钟)12:00-12:30 大会照相12:30-13:30 午餐(御龙宴餐厅)13:30-15:30 大会报告(每个报告30分钟)15:30-16:00 茶歇16:00-18:00 大会报告(每个报告30分钟)18:00-20:30 欢迎晚宴(御龙宴餐厅)5月22日(周五)上午半天:大会报告 地点:御龙宴会中心6层大会议题: 探讨在研发、检测、生产质控等环节建立数字化实验室过程中有关创新性、协作性、适用性、合规性、质量保障、数据分析、知识挖掘、产权保护以及效益收率等关键问题。议程安排:07:30-08:30 报到注册(所有参会代表需佩带会议胸卡入场)08:30-09:00 会议开幕式09:00-10:00 大会报告 (每个报告30分钟)10:00-10:30 茶歇10:30-12:00 大会报告 (每个报告30分钟)12:00-13:30 午餐(御龙宴餐厅)说明:报名参加本届会议的代表,可以免费参加5月22日下午专家培训(价值1500元/人) 5月22日(周五)下午: 专家培训 地点:御龙宴会中心6层 培训主题:“信息化技术助力药品合规性、提高药品质量、降低生产风险”培训 培训专家: Warren Perry, Compliance Consultant \ Issac Mark, Sr. Account Director 会务信息 1、会议时间:报到时间:2015年5月20日下午(周三)会议时间:2015年5月21日全天-22日上午(周四至周五) 2、会议地点:会议地点:上海浦东御龙宴大酒店(御龙宴会中心,紧邻万信酒店)会议地址:上海浦东新区杨高中路2112号(南洋泾路578号) 3、会议报到:5月20日:下午13:00-20:00,万信酒店大堂进行报到和注册,并在万信酒店下榻。5月21日:上午07:30-08:30,御龙宴会中心6层报到和注册。 4、注册费用:1)会议注册费:(包含会议资料、会议用餐;参会人员住宿费及交通费自理) · 国内代表:RMB2000元/人 · 外宾代表:USD400 /人2)优惠条件:2015年5月 5日前报名并交纳注册费可享受8折优惠(RMB1600/人或 USD320/人)3)收费方式: A、银行汇款信息(请在汇款时务必注明用途“会议注册费”,以及参会人员姓名) 户 名:北京创腾科技有限公司上海分公司 开 户 行:中国工商银行上海市分行浦东开发区白杨路支行 账 户:1001154119006907319 B、现金支付:会议现场可以刷卡,不能享受优惠价格。 5、报名方式:请填写与会代表 参会回执,并将回执以邮件、传真或邮寄方式于5月18日前提交会务组,以便我们在会议召开之际,为您安排好相关参会事宜。收到您的参会回执后,会务组将用邮件方式与您确认。(详情请登入:www.neotrident.com) 6、会议住宿:万信酒店价格:商务大床330元/间(含早);商务双床 350元/间(含早)万信酒店地址:上海浦东新区南洋泾路578号(近杨高中路,紧靠御龙宴大酒店)万信酒店电话:021-68669999说明:会期间房间数量非常紧张,以上价格为会议协议价,会务组将按回执先后顺序安排房型,若您确认参会,烦请尽早提交参会回执,以便会务组协助您预留房间。 7、会议交通:交通路线图如下:乘坐地铁:6号线北洋泾路站下,2号出口,步行约15分钟; 9号线杨高中路站下,3号出口,步行约15分钟 8、会务联系:北京创腾科技有限公司(上海分公司)地址:上海浦东新区芳甸路1088号紫竹国际大厦2104室,201204电话: 021-58353866转233,13916858963(陈小姐);021-58353866转219(崔小姐)传真: 021-50158556报名邮箱:huiyi@neotrident.com北京创腾科技有限公司2015年4月27日
会展
2015.04.27
Hollister股份有限公司采用QUMAS 质量管理系统在全球范围实行合规性管理
1 公司简介 Hollister股份有限公司是一家私有的跨国公司,主要从事造口术、可控性、造瘘护理相关产品的开发、生产和营销。Hollister产品遍布全球超过90多个国家。全球有7个场地主要坐落于美国、爱尔兰、丹麦和印度。2 遇到的挑战 1998年,Hollister得知IBM用来进路控制组织机构内电子文档的主机要被淘汰了,这迫使他们来寻找替代的解决方案。分析了内部需求评估后,Hollister确定新的替代方案必须具备以下功能:支持电子签名,符合FDA 21CFR Prat11法规要求支持文档的生命周期管理支持文档版本控制具有快速搜索所存储文档的能力基于角色控制的文档访问权限管理支持多种语言支持全球范围内多种设备的24×7可用性3 QUMAS的选型过程 通过彻底地评估文档管理方案可行性后,Hollister选择了QUMASDocCompliance。自1998年开始,Hollister一直持续的更新版本至现在使用的V4.4版本。7个场地总共超过700名员工使用QUAMS DocCompliance。应用部门主要有质量部门、监管事务部门、研发部门、生物相容性研究部门、灭菌部门、技术服务部门,继而被应用于全球的工程、包装及IT部门(合规流程管理带头人Dawn Porter陈述)。管理Hollister所有的文档:包括生产规范和操作说明,以及监管政策和程序。 2008年,Hollister做了一个全面的解决方案评估,评估一些关键的内部业务流程包括产品注册追踪和CAPA自动化管理。自从Hollister在不同国家进行产品注册追踪后,监管事务部门也需要自动化的解决方案,来追踪当产品的注册到期时提交一个新的数据包重新注册。此外,Lotus Notes 平台即将退休,基于Lotus Notes 平台建立的CAPA管理系统需要升级。 在评估不同的业务流程管理解决方案后,Hollister选择了QUMASProcessCompliance。 “选择ProcessCompliance的一个重要的原因在于它能够与DocCompliance密切协作,使文档和流程关联起来”Dawn Porter说,“并且因为两个产品有相同的外观和风格,所以最终用户的培训会工作会降到最低程度”。 2011年,Hollister推广了QUMASComplianceUnity,一个综合的业务智能解决方案——MyQUMAS,通过统一的界面来访问所有的文档、流程、培训和报告。4 QUMAS的解决方案QUMAS为Hollister提供以下主要功能特点和利益:功能特点带来的利益集中存储所有规范性文档减少了信息搜索时间可配置的仪表板形成合规活动的集成视图追踪和监控完整的文档和流程生命周期为整个组织的可视化提供最佳支持电子审核、批准和文档流转加速审批周期,减少了因打印和快递方式流转文件的成本先进的流?程管理自动化的业务流程并确保了所有场地流程的一致性综合的报告功能允许用户创建临时报告 “QUMAS产品帮助Hollister成为一个更灵活的公司”,Dawn Porter说,“我们现在对于整个公司的合规活动能够有更好的可视性,能够看到一个场地存在的问题以及对其他场地产生的影响,然后采取所需的步骤来防止这一问题在全球范围内的发生。” Hollister目前开始允许合作制造商(CMO)访问QUMAS系统,下载最新的技术规范和图纸。而在此之前,CMO都必须等待快递服务派送的纸质文档。5 关于QUMAS QUMAS是企业合规性管理方案领先的软件供应商,拥有超过260家的全球客户,在生命科学领域有二十年的经验。QUMAS为您提供一个闭环的合规平台,允许您整合共同的合规元素,包括整个组织内的内容、流程、人员和系统的管理。QUMAS解决方案的文档、质量、事前管理,提交和监管批准,使得您能够加速产品上市的时间,降低合规风险,提高运营效率,降低整体质量成本。QUMAS是微软的金牌合作伙伴,提供QUMAS合规管理平台,SharePoint 2010,Documentum,Oracle及SQL。更多解决方案可登陆创腾科技网站www.neotrident.com查看
百态
2015.04.17
杨森制药(Janssen) QUMAS质量管理系统案例
1 公司简介 杨森公司是世界上最大的、综合性的医药保健公司,也是世界上产品最多元化的公司之一。杨森制药创立于1953年,总部位于比利时,不是作为化工厂的子公司,而是以药理研究为唯一目的的医药公司。 杨森制药是世界上最具创新力的制药公司,有超过80种药品,主要应用于人类用药,在中枢神经系统治疗、疼痛症状缓解、消化系统治疗、流行病、女性健康护理领域占据全球领导地位。2 遇到的挑战 医药行业一般会通过不同的软件供应商来提供内容解决方案和过程解决方案,杨森制药也走到了这样的十字路口,公司准备实施一个合规的解决方案,需要覆盖多方面的法规问题而不只是一个具体的规定。杨森制药需要一个综合的合规管理解决方案,确保方案随着组织机构变得更加全球化,实现企业级效率最大化。 杨森制药选择了QUMAS供应商提供合规管理的解决方案,实现文档管理和流程管理。通过选择QUMAS,杨森制药也意识到在医药行业中选择一个成熟的合规管理方案是必要的。3 QUMAS解决方案 杨森制药选择QUMAS作为合规管理解决方案,保障其在欧洲的医药制造工厂和全世界的化学制造工厂的法规需求。杨森制药是全世界领先的制药公司中第一个采用了单一的供应商方案来解决文档管理和过程管理。 QUMAS合规管理套件,是一个完整的合规管理框架,允许公司在高度监管的行业发起企业级合规管理项目,通过单个的解决方案覆盖多种法规要求。QUMAS合规套件规避了多个方案解决单个问题的风险,提供给公司一个可扩展的合规管理框架,使得能够在多个部门快速推广。 “我们选择QUMAS是因为它综合的合规管理套件是唯一允许我们只安装单个供应商提供的解决方案,而我们之前调研的方案可能需要选择两个或者更多的供应商才能满足所有法规需求。”杨森制药公司QA信息管理部门的欧洲制药主管Bert Jacobs反馈。4 关于QUMAS QUMAS拥有超过二十年的行业经验,是全球唯一为受监管的企业提供完整解决方案的合规软件供应商。在企业风险和合规管理方面被公认为领导地位,是行业创新和卓越奖的长期获得者。 QUMAS合规管理套件中的合规管理方案应用于受监管的企业,能够确保企业全球监管符合法规要求,包括Act 38a-1,USA PATRIOT,Sarbanes Oxley,21CFR Part11以及GxP法规要求。 QUMAS提供高度可配置的应用程序,在受监管的环境下支持验证和部署。基于开发的系统平台,QUMAS可以与企业现有的来自于其他所有的不同供应商的数据库、应用程序、操作系统以及硬件无缝集成。 QUMAS全球总部在爱尔兰的科克,美国总部在新泽西州弗洛勒姆帕克,其他场地遍布美国和欧洲。更多解决方案可登陆创腾科技网站www.neotrident.com查看
百态
2015.04.17
如何为生物分析实验室选择合适的LIMS系统
生物分析实验室有其独特的工作模式和一系列要遵从的法规,当一个机构在选购LIMS系统时,如何在众多的LIMS产品中选出适合自己的LIMS系统,是选择通用型的LIMS还是专业型的LIMS,机构在做决策时需要对产品的功能、市场情况、风险等进行评估,这样才能做出最合适的选择。 功能 在考虑功能时首选要明确自己的需求,要认识到机构的核心工作和核心职能是什么。对于生物分析实验室来说,最核心的工作和职能是依据法规和客户的要求获得生物分析实验数据,从管理职能上来说就是确保生物分析实验完全依据法规和客户要求来完成。真正好的LIMS系统是关心核心工作和核心职能的系统,是将先进工作方式和管理理念融入到系统中的系统。核心工作以外的功能有最好,没有也无伤大雅,或者可采用与其他系统互补的形式。当明确自己的需求后,就可以根据自己需求、产品的功能及二者的符合程度来选择合适的产品。对于生物分析实验室来说目前行业标准的LIMS系统是Watson LIMS,与通用性的LIMS不同,Watson LIMS是专门针对生物分析实验室的一款LIMS产品,设计旨在适应生物分析工作流,处理一些深度的业务流程(如:项目管理、实验方案设计、样品管理、仪器接口、数据拟合、统计分析、样品重分析、PK参数计算等)。由于Watson LIMS自诞生以来即专注于生物分析的流程,其成熟度相较与通用型LIMS更有优势,另外,由于供应商在此行业积累了数十年的经验,相较于新涉及生物分析领域的厂商来说更能应对快速变化的业务需求并为客户提供相应的解决方案。 市场状况 一套LIMS在全球的市场占有量是很重要的,只有达到一定的市场占有量,产品才会很安全地发展下去,否则,该产品有随时被停止开发的危险。另外,行业内LIMS的占有量也是很重要的,因为行业内的用户多,交流就会更方便,否则用户太少,使用交流则不方便。更重要的是,使用相同的LIMS系统有利于同行之间项目合作和交流,保证了大家都在同一个平台上对话。 全球顶尖的20家制药公司中有18家使用Watson LIMS管理生物分析实验室,如辉瑞、礼来、阿斯利康、强生、罗氏、诺华等等,在国内,已有超过20家的用户,如像药明康德、睿智化学这样的CRO公司,像北京医院、协和医院这样的I期临床研究机构,像上海药物所、成都安评中心、上海交通大学这样的科研院所,还有像山东绿叶、默克雪兰诺这样的制药企业。因此,Watson LIMS在生物分析领域有着很高的行业认可度。 风险 风险方面主要考虑供应商的实力、技术支持和服务能力以及系统实施验证风险 虽然不能说公司越大就代表产品越好,但公司较大时说明其抗风险的能力强。 在技术支持和服务方面,一套好的LIMS系统同样需要高水平的本土化技术服务队伍才能真正发挥其价值,否则也是一纸空谈。 Watson LIMS的国内实施团队均具有生物分析行业背景,来自各大生物分析的CRO公司或跨国公司,并都通过赛默飞世尔公司提供的全球统一的计算机验证方法学培训,成功实施案例达20多个,在软件实施、验证和通过法规部门审计方面具有明显的专业优势。 对于需要对软件系统进行验证的单位,系统验证的风险也是考虑因素之一,如果一套系统在验证方面存在高风险性,不仅意味着投入的成本增加,同时也意味着系统验证会有达不到相关法规要求的可能,那么由系统产生的数据也会受到质疑。 与通用性的LIMS不同,Watson LIMS不接受定制开发,通过简单配置实现不同客户的需求,因此实施周期短。通用性的LIMS只是提供一个平台,用户的需求均需要基于这个平台通过软件开发来实现,因此实施周期长。按照国际软件验证指南GAMP5的要求,通过编码方式实现的功能必须从Design和Coding阶段开始验证,验证的风险高,负担重,后续系统变更的验证工作也更复杂。而Watson LIMS提供现成的标准化验证测试脚本,验证方便,风险小,实施包括全验证两个月左右即可完成。 基于以上讨论,如果机构希望在生物分析领域里增加自身的竞争力,提高项目数据管理水平,加强法规依从性,降低风险,更多的和国际客户交流,那么Watson LIMS则是最合适的选择。更多解决方案可登陆创腾科技网站www.neotrident.com查看
百态
2015.04.17