推荐厂家
暂无
暂无
 银牌2年
银牌2年
 400-860-5168转5943
400-860-5168转5943
 留言咨询
留言咨询
 银牌8年
银牌8年
 400-860-5168转3999
400-860-5168转3999
 留言咨询
留言咨询
 留言咨询
留言咨询

 400-633-0963
400-633-0963
 留言咨询
留言咨询

 400-877-0075
400-877-0075
 留言咨询
留言咨询

 400-860-5168转4646
400-860-5168转4646
 留言咨询
留言咨询
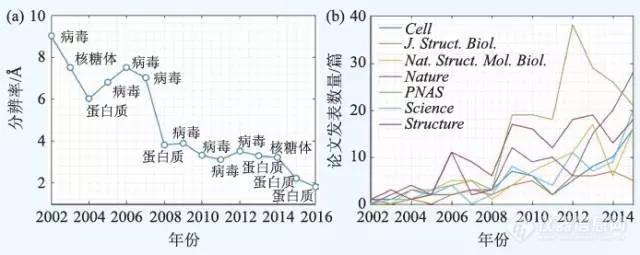





近日,清华大学施一公研究组通过单颗粒冷冻电子显微技术(冷冻电镜)解析了酵母剪接体近原子分辨率的三维结构,并在此结构的基础上进行了详细分析,相关文章发表在《科学》周刊上。这一重要研究成果再次让冷冻电镜技术进入了大家的视野。 施一公表示,如果没有冷冻电镜,就完全不可能得到剪接体近原子水平的分辨率。而早在2007年清华大学采购冷冻电镜时,也没想到冷冻电镜会出现飞跃性的进展。 确实自从2013年以来,随着单电子计数探测相机的问世,以及图像处理算法的发展,冷冻电镜技术在结构生物学研究中的应用越来越多,其重要性也日益凸显,吸引了许多以前从事X射线晶体学研究的研究人员关注。那么冷冻电镜技术未来的发展前景如何呢? 2015年4月,单电子计数探测相机的研发人员之一华人学者程亦凡(Yifan Cheng) 在Cell杂志刊登了《Single-Particle Cryo-EM at Crystallographic Resolution》,其中有一个部分专门介绍了单颗粒冷冻电镜技术未来的发展。现将原文翻译如下,与版友们共享。~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~ 毫无疑问,单颗粒冷冻电镜(single-particle cryo-EM)不再是‘‘blobology’’,而是一种可与X射线晶体学方法分辨率相媲美的新方法。然而,与X射线晶体学不同的是,单颗粒冷冻电镜总是产生一些信息(尽管并不都是原子分辨率级别的信息),甚至对分辨率并不是很高的图像进行重构,也能够获得如何改进样品制备的信息,以及宝贵的生物学见解。因此,在大分子研究方面,单颗粒冷冻电镜技术比X射线晶体学更具吸引力。 然而,单颗粒冷冻电镜技术还远非完美,而且技术发展仍然非常快。目前单颗粒冷冻电镜技术的分辨率水平,依然无法满足许多方面的应用要求。例如,如果分辨率能够突破3埃,这样就能清楚的看到离子的位置,同时不仅能观察到小分子,还能观察到小分子配体与目标蛋白是如何结合在一起的,这一点对于制药公司来说颇具吸引力,因为它能够为基于结构的药物设计和优化提供便利。 最近有一篇综述文章详细探讨了单颗粒冷冻电镜技术的局限性,尤其是在获取更高的分辨率方面,并介绍了可能的解决方法(Agard et al., 2014))。由于分辨率不足,建立新模型和精修所花费的时间常常远远超过了三维重构本身。尽管许多X射线晶体学工具可以被应用在冷冻电镜密度图模型的建立和精修,它也需要显著的改进(Amunts et al., 2014; Brown et al., 2015)。此外,X射线晶体学传统的验证准则,例如自由R-因子,对于建立冷冻电镜密度图的模型并不适用。因此,对于单颗粒冷冻电镜技术来说,建立、精修和验证有效的模型的工具和方法都需要进一步的发展。 除了提高技术本身,还有其他一些因素限制单颗粒冷冻电镜技术的广泛应用。首先,单颗粒冷冻电镜技术并不是一个“交钥匙”方法。即使有自动数据采集技术和流程化数据处理、图像采集和加工处理等,它依然是一个十分复杂的技术,对于一个新手来说,很难通过短时间的培训或使用说明书就能学会操作。其次,必要的基础设施需要价值不菲的投资,包括功能齐全的冷冻电镜设备,用于数据处理和存储的计算机资源等。另外,除了最初的投资,目前高端冷冻电镜设施运行所需要的投资也是巨大的。第三,目前几乎没有类似同步辐射光源向社会大众开放的、致力于高通量数据采集的冷冻电镜设施。 这些限制使得进入冷冻电镜领域的门槛太高,要想有所改变,将需要多方面的努力。 因此,使得冷冻电镜技术更加可靠耐用,并且相对容易掌握,降低设备和运行成本,提供现成的设备及专家,也是促使冷冻电镜技术能够像X射线晶体学技术广泛应用的重要步骤。尽管,单颗粒冷冻电镜技术的未来是光明的,但是需要科学界以及政府投资机构的大力支持,才能使得单颗粒冷冻电镜技术能够像X射线晶体学技术一样受欢迎。
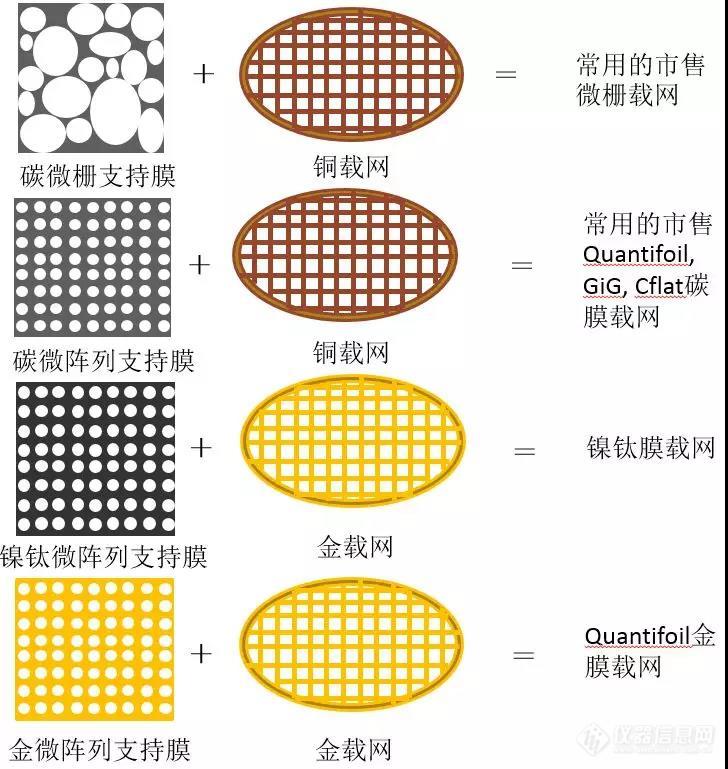
冷冻电镜技术是现今结构生物学里最常用的解析生物大分子三维结构的技术之一。虽然其样品制备过程比另一种同样非常常用的技术——X射线晶体学简便,但成功制备出一个适合进行高分辨数据收集的样品仍然是经验、运气、努力与创新相结合的结果。为了承载样品,使其能送入透射电镜进行观察,样品需要与带支持膜的载网接触并冷冻固定在一起。目前,可供选用的载网支持膜大体分两种:一种是有孔支持膜,包括常用的微栅碳支持膜、碳微阵列支持膜(如Quantifoil,GiG,Cflat等)、金属微阵列支持膜(如Quantifoil金膜,镍钛膜等)等,可直接购买使用。另一种是在有孔支持膜上再加一层连续超薄支持膜,添加的超薄支持膜常用的为超薄碳膜,近期又出现了氧化石墨烯膜等基于石墨烯的超薄膜类型。这种通常需要使用者对市售的有孔支持膜再加工,在其表面多加一层超薄支持膜。无论使用哪种膜,由于提供支撑的有孔膜较厚引入的噪音很高,数据收集都发生在孔内。[align=center][img=,690,728]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260954438579_6129_3224499_3.jpg!w690x728.jpg[/img][/align][align=center]图1.常用有孔支持膜类型[/align][align=center][img=,690,550]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260954588204_7034_3224499_3.jpg!w690x550.jpg[/img][/align][align=center]图2.有孔支持膜加连续超薄支持膜类型[/align]适合单颗粒技术数据收集的冷冻电镜样品需符合以下要求:①生物大分子群体主要为同种分子或者组分相同的复合体,且它们稳定在一种或有限的几种彼此能被计算机图像处理分类技术区分的构象;②样品颗粒彼此分离,同时分布密度又能满足在一次数据采集区域内获得足够的颗粒数量;③样品颗粒的空间取向随机分布。[align=center][img=,690,262]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260955256336_8129_3224499_3.jpg!w690x262.jpg[/img][/align][align=center]图3.理想化的样品颗粒在冰层中的分布示意图[/align]这些要求看似与载网支持膜的选用无太大关联,但实践经验告诉我们,有时同一个样品使用不同的载网支持膜进行样品制备,其数据收集质量有区别。导致这种差别的原因之一是支持膜表面性质的不同对进孔样品分布密度的影响。使用有孔碳支持膜常见的一个问题是样品大部分粘附在支持膜上,而在孔内的样品数量很少。根据经验,碳支持膜对部分样品的吸附性能相当强,溶液中的样品会优先吸附到碳膜上,以至于游离的样品颗粒浓度大大降低,而分布在支持膜孔内的样品来源于游离的样品颗粒群体。使用添加了连续超薄膜的载网则少有这个问题,毕竟孔内孔外都有碳膜,同时由于碳膜对样品的吸附在一定程度上具有样品富集效应,还可降低制样时所需样品浓度。此外,使用金属材质的有孔支持膜(如金膜,镍钛膜等)能缓解这种情况,因为金属支持膜表面性质与碳支持膜有区别,其对样品的吸附也可能有差异。[align=center][img=,690,263]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260955370487_1473_3224499_3.jpg!w690x263.jpg[/img][/align][align=center]图4.连续碳膜上的样品颗粒在冰层中的分布示意图[/align]导致这种差别的原因之二是冷冻样品制备时气液界面对样品的影响。由于电子能穿透的样品厚度很有限,样品被冻住前必须先进行减薄。目前最简单也最通用的减薄法是使用滤纸移除大部分液体而仅剩厚度在几十至上百纳米范围的水膜。根据现今通用的制样方式,从水膜的形成到它被快速冷冻成非晶态冰膜的时长在秒的量级。水膜的上下两层气液界面之间的距离如此短,水膜中样品被冷冻固定前的时间如此长,以至于样品颗粒有成千上万次机会与气液界面接触。每次接触样品颗粒都机率变性,或变成无定形的多肽链,或解体成更小的亚基组合。最终我们看到的样品颗粒或是被“已牺牲”的变性样品所保护而未能接触气液界面,或是幸运地多次接触气液界面而仍未变性。更多关于气液界面对样品影响的介绍,可参考孙飞(2018)以及Glaeser 和Han (2017)发表的综述。[align=center][img=,690,285]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260955485024_3909_3224499_3.jpg!w690x285.jpg[/img][/align][align=center]图5.现实的样品颗粒在冰层中的分布示意图[/align]使用有孔支持膜无可避免地会受到来自上下两层气液界面的影响,某些样品会因此而在冷冻后无法观察到完整颗粒。而使用连续超薄支持膜一面由气液界面转换为固液界面,另一面由于支持膜对样品的吸附而远离气液界面,有效地降低了气液界面对它的影响。既然添加连续超薄支持膜的载网有这么多好处,为什么很多样品仍然使用有孔支持膜呢?原因之一是长期使用的超薄碳支持膜对于小蛋白(特别是分子量小于500kDa)仍然太厚,引入的噪音太多,导致小蛋白数据取向搜索结果不够精确,影响重构分辨率提升。而石墨烯类超薄支持膜理论上为单分子层,比超薄碳膜更薄,在这方面可以帮上忙。但石墨烯类支持膜添加到载网上的方法仍在发展中,目前使用上仍不及有孔支持膜便利。[align=center][img=,690,541]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260956026943_9251_3224499_3.jpg!w690x541.jpg[/img][/align][align=center]图6.样品直径与碳膜厚度的选择(感谢友情出镜的大蛋黄颜值担当评审嘉宾)[/align]原因之二是添加超薄支持膜更大机率引起样品的取向优势,导致某些取向数据采集量远远不足,同样影响重构分辨率提升。[align=center][img=,690,396]https://ng1.17img.cn/bbsfiles/images/2018/11/201811260956143795_3302_3224499_3.jpg!w690x396.jpg[/img][/align][align=center]图7.样品颗粒取向优势示意(感谢友情出镜的大蛋黄实力客串样品颗粒)[/align]纯有孔支持膜与添加超薄支持膜两种方案可谓各有优缺。有孔支持膜的缺点很明显,在于受气液界面的两面夹击。如果有一种方法能缩短样品减薄到冷冻固定的时长至毫秒级别,那么样品颗粒将没有足够的时间多次接触气液界面,同时也减少与支持膜本身的接触,从而使用有孔支持膜的各种问题将可能迎刃而解。Bridget Carragher实验室研发了一种特殊的载网,命名为纳米线载网(nanowire grids)。这种载网具有自减薄功能,即载网孔内多余的液体会被固定在载网梁上的纳米线所吸走,留在载网孔内的液体厚度自然下降。当然纳米线吸附液体体积是有上限的,需要配合他们实验室研发的微量加样设备(Spotiton robot)加注皮升级别的样品量。虽然目前还未得到普及,但这种设置可以实现将减薄步骤的时长降低到百毫秒级别的水平。目前该文章未正式发表。推荐阅读文献:Fei Sun. Orienting the future of bio-macromolecular electronmicroscopy. Chin. Phys. B. 2018, 27(6): 063601Glaeser RM, Han BG. Opinion: hazards faced by macromolecules whenconfined to thin aqueous films. Biophys Rep. 2017, 3(1):1-7Noble AJ, Wei H, Dandey VP, Zhang Z, Potter CS, Carragher B.Reducing effects of particle adsorption to the air-water interface in cryoEM.doi: https://doi.org/10.1101/288340Palovcak E, Wang F, Zheng SQ, Yu Z, Li S, Bulkley D, Agard DA, ChengY. A simple and robust procedure for preparing graphene-oxide cryo-EM grids.doi: http://dx.doi.org/10.1101/290197Russo CJ, Passmore LA. Electron microscopy: Ultrastable goldsubstrates for electron cryomicroscopy. Science. 2014, 346(6215):1377-80.Sader K, Stopps M, Calder LJ, Rosenthal PB. Cryomicroscopy ofradiation sensitive specimens on unmodified graphene sheets: reduction ofelectron-optical effects of charging. J Struct Biol. 2013, 183(3):531-536来源:【生物成像中心】欢迎大家分享讨论使用过的载网支持膜[img]https://simg.instrument.com.cn/bbs/images/default/em09505.gif[/img]
近期学院里有位老师看文献里用到了冷冻蚀刻技术,或者叫冷冻复型技术。原理是这样的,由于要分析的样品是原油里面的沥青成分,常温下是固体,但是都是些高沸点大分子的物质,在高温下有可能会融化,不能直接到TEM里面做,所以先把一点沥青放到冷冻蚀刻机的样品室内,然后液氮冻住,在以45度角往上面喷一层Pt或者C的颗粒,叫做投影,然后再垂直喷一层C膜。最后把样品取下来,把沥青用溶剂溶解掉,剩下的那层碳膜做TEM分析,可以得到沥青表面颗粒分布的复型图像。原理罗嗦了半天,估计各位有搞生命科学或者医学的朋友早就看明白了,这个方法好像需要专用的冷冻复型机器,不知道各位有没有用过的或者了解的,方便的话提供一下品牌、价位,或者哪位可以做合作分析的,提供个联系方式给我,谢谢了。我的邮箱:jeffrylee@126.com


