推荐厂家
暂无
暂无

 400-873-7896
400-873-7896
 留言咨询
留言咨询

 400-860-8560
400-860-8560
 留言咨询
留言咨询

 400-860-5168转2233
400-860-5168转2233
 留言咨询
留言咨询



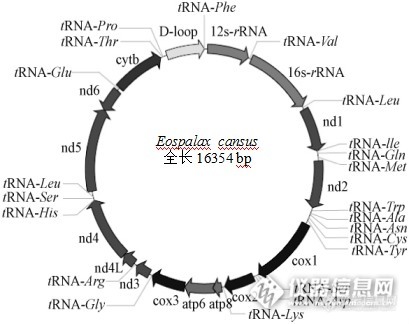
[b][/b][align=center]鼢鼠([i]Eospalax[/i])线粒体基因组测定及注释分析[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]安平中心:李瑞[/align][b]摘要【[/b]目的】获得鼢鼠线粒体基因组全序列,为线粒体基因组功能标记及进化生物学等研究提供基础资料。【方法】参考鼹型鼠等动物的线粒体基因组序列,设计出可覆盖鼢鼠线粒体基因组的16对引物,采用[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]产物直接测序法测得甘肃鼢鼠线粒体基因组全序列,分析其基因组的特点和基因结构。并结合GenBank中发表的啮齿类动物基因组全序列,探讨啮齿类动物的系统进化关系。【结果】鼢鼠线粒体基因组全长16354bp,其中包括22个tRNA基因、13个蛋白质编码基因、2个rRNA基因和2个D-loop区。碱基组成为33.5%A、24.2 %C、12.3 %G、30.0 %T。【结论】鼢鼠线粒体基因组结构及其信息和其他啮齿类动物的结构一致,线粒体变异保守。研究结果为鼢鼠的低氧适应、系统发育关系等提供了基础资料。[b]关键词 [/b]鼢鼠;线粒体基因组;序列分析 鼢鼠([i]Eospalax[/i])是分布于我国的主要啮齿类动物之一,其体型较小,栖息于洞穴内有挖掘活动,扩散能力强,数量波动大,是生态系统中重要的初级消费者,处于生态系统中的中心位置,草原生态系统中其能流比重很大[sup][/sup]。动物线粒体([color=#333333]Mitochondrion[/color])基因组为双链闭合环状分子[sup][/sup],少数也有线性的,它们具有分子量相对较小、结构简单、缺少重组、母性遗传和进化速率快等特点,已成为动物系统发育与进化、群体遗传学、分子生态学以及疾病机理研究等领域的理想材料[sup][/sup]。甘肃鼢鼠是仅分布于我国西北部的土著物种,其外形似中华鼢鼠,主要分布于甘肃临潭县及其附近地区。目前对线粒体DNA的研究主要在动物分子遗传学、分子生态学、种群遗传结构分析、遗传多样性、物种和品系鉴定、保护遗传学等方面得到了广泛应用[sup][4[/sup][sup],[/sup][sup]5][/sup]1. [b]实验材料和方法[/b]1.1 实验材料鼢鼠:采集于天祝(经度102.84、纬度 37.2)1个群体;鼢鼠解剖采集肝脏及肌肉组织样品,-20℃保存备用。1.2 线粒体DNA的提取用剪刀将肝脏及肌肉材料剪成小块,取0.1cm左右的小块肝脏及肌肉材料,采用常规的SDS/蛋白酶K裂解,酚氯仿提取DNA[sup][/sup],使用琼脂糖凝胶电泳检测其完整性。1.3 引物设计和[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]扩增通过Clustal X1.83比对,寻找相对应保守区域位置,用Primer Premier5.0引物设计软件设计引物,并对每条引物进行评价和修改,最终确定16对引物。以所提取的DNA为模板,用16对引物扩增覆盖整个线粒体基因组。利用引物进行[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]扩增,反应体系总体积为50μL,其中含有6μL [url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] buffer、3μL MgCl[sub]2[/sub](1.5mmol)、MgCl[sub]2[/sub],2μL dNTPs (100μL mol)、上下游引物各2μL (0.25μL mol)、Taq DNA聚合酶2μL (1U)、总DNA约为2μL (25ng)、去离子水31μL。反应程序为:94℃预变性4 min,94℃变性50s,48-45℃退1min,72℃延伸1 min 30s,循环30次,之后72℃延伸10min,并根据不同引物的退火温度和扩增反应的实际效果进行优化。取 5 μL [url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]扩增产物,和2 μL DNA marker 2000,进行1.0%琼脂糖凝胶(1×TBE)5V/电泳,用紫外观察[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]产物扩增情况,凝胶成像仪扫描记录结果。1.4 纯化、测序和序列拼接 在[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]产物中加入5 U SAP和2 U ExoⅠ,震荡混匀,37℃保温1 h,然后75℃保温15 min以灭活SAP和ExoⅠ酶,纯化好的模板可以在4℃保存24 h或-20℃长期保存。将纯化后的引物送往上海生工生物技术服务有限公司用ABI-3730序列自动分析仪进行双向测序。利用DNASTAR和测序峰图结果分析软件Chromas 2.22校对测序图,DNAMAN拼接序列。得到甘肃鼢鼠线粒体全基因组全序列。2. [b]结果[/b]2.1 鼢鼠线粒体基因组基因定位2.2.1 鼢鼠线粒体2个rRNA的分析哺乳动物线粒体的rRNA具有高度的保守性,它们的位置固定,12S rRNA位于tRNA-phe 和tRNA-Val之间,16S rRNA位于tRNA-Val和 tRNA-Leu之间,12S rRNA起始位置为68,终止位置为1019,长度为952bp,16S rRNA起始位置为1086,终止位置为2651,长度为1566。同时我们比对了鼢鼠和中华鼢鼠的rRNA基因和蛋白质基因,12S rRNA和16S rRNA的相似性分别为91.0%和87.3%,高于蛋白质编码基因之间的相似性。2.2.3 鼢鼠线粒体基因组结构 除NADH脱氢酶亚基6外均在H链上,虽然鼢鼠染色体数目少、染色体大,但与其它哺乳动物线粒体全基因组相比,它的线粒体基因组的结构与其它哺乳动物是十分相似的。甘肃鼢鼠线粒体基因组结构见图1。[align=center][img=,409,324]http://ng1.17img.cn/bbsfiles/images/2017/09/201709081454_02_2904018_3.png[/img][/align]注:ND: NADH脱氢酶亚基(NADH dehydrogenase subunit)、Cox:细胞色素氧化酶亚基(cytochrome oxidase subunit)、Atp:ATP合成酶亚基(ATP synthase F0 subunit)、Cyt b:1个细胞色素b编码基因(cytochrome b)。[align=center][b]图1[/b] 甘肃鼢鼠线粒体基因组结构简图[/align][align=center]Fig.1 The gene organization of [i]Eospalax cansus[/i] mitochondrial genome[/align]3. [b] 讨论[/b] 甘肃鼢鼠线粒体基因组的D-loop区,长度为933bp,比中国地鼠D-loop区(867bp)长。D-loop区对目的基因是不可缺少的,虽然D-loop区不能编码蛋白质但对于遗传信息表达是不可缺少的,在它上面有调控遗传信息表达的核苷酸序列,具有遗传效应的,比如RNA聚合酶结合位点是具有遗传效应的。8只甘肃鼢鼠中有5个单倍型:3只临潭群体共享1个单倍型,2只天祝群体独享单倍型;其余个体均独享单倍型,表明了甘肃鼢鼠线粒体DNA D-loop区碱基变异快、进化快的特性,符合啮齿动物线粒体变异大的现象。随着研究的深入,以线粒体DNA中完整的基因序列或多个基因序列协同而获得遗传信息来探讨物种的系统进化关系,将是以后研究发展的主要方向[sup][/sup]。目前,线粒体DNA已经在许多哺乳类动物的起源进化的研究中取的了重大进展,而对甘肃鼢鼠的起源进化的研究却很少,并且存在着甘肃鼢鼠属于[url=http://baike.baidu.com/view/113192.htm][color=#000000]瞎鼠科[/color][/url]和仓鼠二者之争,因此,为了更好的阐明甘肃鼢鼠的起源,还需要做更多、更深入的研究。
1971年Kleppe等人在Journal of molecular biology上发表文章首次准确、精炼、客观的阐述了PCR方法,1976年一种从嗜热水生菌(Thermus aquaticus)分离得到的热稳定的DNA依赖的DNA聚合酶的应用大大增加了PCR的效率。而现今所发展出来的PCR则是源于由Saiki和Mullis等人于1988年发表在Science上的一篇论文,Mullis当时服务于Perkin Elmer(PE)公司,因此PE公司在PCR界有着特殊的地位。后来PE被Applied Biosystems Inc.(ABI)公司收购、分拆、再转卖,而PCR的专利和倍受信赖的PCR仪器生产和销售就留在ABI名下。到如今,PCR方法愈发趋向自动化,并从中衍生出更多的新技术方法,可以说,PCR技术是支撑现代分子生物学发展的一块重要基石。这种技术的广泛应用催生了一个庞大的市场,多个公司均有各种类型的商品化PCR仪出售。PCR的专利目前依然掌握在ABI和Roche(罗氏)两大公司手中,去年业界颇为引人瞩目ABI诉MJ公司侵犯侵犯PCR仪知识产权案最终以MJ败诉并宣布破产、最终被Bio-rad收购暂告一段落。其后还会不会有后继的故事还需拭目以待。 PCR原理 DNA的半保留复制是生物进化和传代的重要途径。双链DNA在多种酶的作用下可以变性解链成单链,在DNA聚合酶的作用下,以单链为模版,根据碱基互补配对原则复制成新的单链,与模版配对成为双链分子挎贝。在体外实验中发现,DNA在高温时也可以发生变性解链,当温度降低后又可以复性成为双链。因此,通过温度变化控制DNA的变性和复性,并设计与模板DNA的5’端结合的两条引物,加入DNA聚合酶、dNTP就可以完成特定基因的体外复制,多次重复“变性解链—退火—合成延伸”的循环就可以以几何级数大量扩增特定的基因。 发现耐热DNA聚合酶对于PCR的应用有里程碑的意义,该类酶可以耐受90℃以上的高温而不失活,不需要每个循环加酶,使PCR技术变得非常简捷、同时也大大降低了成本,PCR技术得以大量应用,并逐步应用于临床。 从PCR原理可以看出,PCR仪的关键是升降温的步骤。现在偶尔还能听到一些前辈们笑谈早年的PCR实验如何在3个水浴锅中完成的趣闻。经过不断改进,今天的PCR已经越来越完善和智能化。出于市场推广的战略需要,各厂家的PCR仪型号不同,着力宣传的技术指标和参数也不尽统一,编者在这里简单列出选购时我们认为应该考虑的常用指标,希望有助于大家选购PCR仪的选购技巧。PCR仪介绍及其选购 PCR仪的种类总体来说可以分为两大类:PCR扩增仪和实时荧光定量PCR仪,普通的PCR扩增仪又衍生出带梯度PCR功能的梯度PCR仪、和带原位扩增功能的原位PCR仪等等。1996年由ABI公司首先推出将扩增和检测融为一体的实时荧光定量PCR仪,此后很多公司如Eppendorf、ROCHE、Corbett、MJ等等都先后推出不同款式的定量PCR仪。
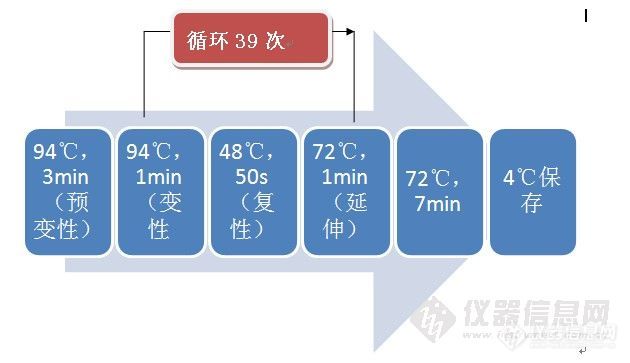
原创大赛进行得好快啊·~转眼就到9月份了,正好将暑期的实验总结下,来参加大赛了~~~~大家轻拍板砖~~~ 奖品许愿:容我再想几天哈~~~摘 要:本实验用酚—氯仿抽提的经典方法从动物心脏中提取总DNA,电泳检测后进行分离纯化,获得总DNA样品。以D-loop序列为引物,用提取的总DNA作为模板,在适宜条件下PCR快速扩增mtDNA D-loop区,获得了大量的目的片段。 线粒体(mitoch ondria)是真核细胞核外唯一的遗传物质,哺乳动物mtDNA是约16.5kb的闭环双链分子,线粒体DNA的结构上有一个独特的D—Loop环(displacement loop region):位于tRNA—Pro和tRNA—Pile的基因之间,由少数碱基构成一个突出结构。在线粒体DNA上,D—Loop环是整个线粒体基因组序列和长度变异最大的区域,其进化速度最快,一般用于种内种群间的系统进化分析。线粒体作为真核生物胞质遗传的重要组成部分,mtDNA是由卵细胞传递给后代,被认为属于典型的母性遗传。 有关生物进化的研究一直是科学家关注的问题,现在国内外很多学者利用mtDNA D-loop区研究生物进化,采用Neighbor-joining算法,绘制生物系统进化树。哺乳动物线粒体DNA的D-loop区是其复制和转录的起始区域,是一个高度多态性和突变性的区域,其中D—loop重链RNA(DH-RNA)与复制和转录功能密切相关。目前有关mtDNA D-Loop的遗传变异分析的研究已在人、牛、猪、马、鸭、鱼类、昆虫类、两栖类等多种动物中开展。为了探讨动物的分类地位,我们以位于D - loop 两端的tRNApro和12S rRNA 基因内的部分序列设计的2 对引物通过聚合酶链式反应(Polymerase Chain Reaction , PCR) 扩增mtDNA D - loop ( P1 和P2) ,通过测定产物序列,相关比较,进一步分析其分类地位,以及mtDNA D环多态性,为以后进一步研究线粒体D—Loop区的多态性与疾病的关系以及分析物种之间的进化规律奠定了基础。 1 材料与方法 1.1.1实验试剂 提取DNA:生理盐水(去除组织中的淤血)、 TES液(抑制DNA酶作用)、SDS(表面活性剂,抑制DNA酶)、饱和酚(将蛋白质变性)、酚∶氯仿∶异戊醇(体积比为25∶24∶1)、氯仿∶异戊醇(除去酚)、无水乙醇(预冷,沉淀DNA)、预冷的乙醇(洗涤DNA)、 TE(降解DNA)、蛋白酶K(降解蛋白质) 电泳: TBE缓冲液(pH8.0)、TBE缓冲液、琼脂糖(凝胶介质)、溴化乙啶(EB,荧光染料)、溴酚蓝(指示剂)、标准λDNA(48kb,Mark)、上样液(蔗糖+溴酚蓝) PCR扩增:引物P1:5’-TATGTACCATGAGGACAAATATC-3’,P2:5’-ATTACACCTCCTAATTTATTAGGAATC-3’ 、dNTP(2.5mmol·L-1)、10×Buffer溶液、TaqDNA聚合酶(2.5U·μl-1)、超纯水、Marker(DL2000)、PCR产物回收试剂盒等。 1.1.2仪器 微量移液器、Eppendorf离心机、微波炉、DYCp31型电泳仪、凝胶成像系统、恒温水浴锅、PCR仪 1.2 实验方法 1.2.1 总DNA的提取(总的说来采取的步骤图示为:)http://ng1.17img.cn/bbsfiles/images/2010/09/201009021539_241030_1915361_3.jpg 1.2.1.1 将材料解块,用NaCl洗去血污。剪一小块组织,剪碎,放入-20℃预冷的研钵中加入TES充分研磨。 1.2.1.2吸取匀浆液到离心管中,再加入SDS及蛋白酶K(20mg/ml)充分混匀后于56℃保温,每2小时摇一次。放置室温,加入等体积的饱和酚,颠倒混匀呈乳浊液,10000rpm离心10min(液体分层,上层为黄色,下层无色)。分离水相和有机相小心吸取上层含核酸的水相到一个新的离心管中。 1.2.1.3加入等体积酚∶氯仿∶异戊醇(25∶24∶1)380μl,颠倒混匀15min,10000rpm离心10min,取上清液移到一个新的离心管中。再加入等体积氯仿∶异戊醇(24∶1)颠倒混匀15 min。这时液体分层,10000rpm离心10min,取上清液移到一个新的离心管中。 1.2.1.4加入2.5倍体积-20℃的预冷无水乙醇沉淀DNA。于12000rpm离心15min,用乙醇快速洗涤沉淀,离心,弃上清,干燥。加入TE于40C冰箱中保存备用。 1.2.2 电泳检测总DNA 1.2.2.1称取0.24g琼脂糖于三角瓶中加入30ml0.5×TBE缓冲液配成0.8%的胶;用微波炉加热,煮沸,振荡,反复加热振摇2~3次,使糖充分融化。用医用胶布将胶床两端粘好,注意不要超过底部以免放置不平。 1.2.2.2等胶冷却至约60℃时,将融化的琼脂糖小心地倒入已插好梳子的胶床中,再使其自然冷却,直至完全凝固。小心向上方拔出梳子,去掉制胶槽两边的胶带,小心地将胶和胶床放入电泳槽。向电泳槽中加入TBE缓冲液,液面高于胶面1~2mm,以使其全部处于电场内。 1.2.2.3取8μlλDNA,加2μl上样液,混匀后,小心点入上样孔中。取4μl样品DNA,加2μl上样液在parafilm上混匀,同样点入上样孔中。将电压调至100V,接通电源,打开开关,开始电泳。大约20分钟后,待指示剂迁移到距上样孔1.5cm以外时终止电泳,切断电源,取出凝胶,放入含EB的染色液中染色20分钟。凝胶取出后,于凝胶成像系统中观察分析。 1.2.3总DNA的纯化 提取的总DNA加TE补到50μl,加0.5μl的RnaseA,37℃温浴1h;加50μl氯仿:异戊醇,颠倒均匀,大约10次;10000rPm,离心10分钟,取上清夜;加150μl无水乙醇,轻微晃动;12000rPm离心10分钟,弃乙醇;加300μl70%乙醇洗涤DNA,弃乙醇控干,55℃干燥DNA;加25μlTE溶解DNA 1.2.4 PCR扩增线粒体DNAD-LOOP基因 1.2.4.1 引物的设计 扩增引物为昆虫通用引物,引物设计参考Simon等,引物由上海生工生物工程有限公司合成。 1.2.4.2 扩增体系的建立 每一样品的扩增体积均为25μl。将下列试剂按表1的顺序加入0.2mL的EP管中。http://ng1.17img.cn/bbsfiles/images/2010/09/201009021448_241016_1915361_3.jpg 1.2.4.3 PCR扩增 对上述加好试剂的0.2mL的Ep管短暂离心,灭气泡后放入PCR仪。扩增共运行35个循环,每一循环包括:http://ng1.17img.cn/bbsfiles/images/2010/09/201009021550_241036_1915361_3.jpg 扩增产物用1.0%的琼脂糖凝胶电泳检测其大小、纯度及浓度。 1.2.4 PCR扩增产物的电泳检测 称取0.3g琼脂糖于三角瓶中加入30ml的1×TBE缓冲液配成1.0%的凝胶。 从PCR仪中取出已经扩增的样品.用微量取液器取3μl溴酚蓝加入EP管,反复抽吸以混匀,再从中吸取3μl,加入上样孔.吸取6ulMarker点样.插好电极,接通电泳仪电源,调节电压120V,电泳20min,以指示剂迁移位置判断.将凝胶取出置于EB液中染色20min. 凝胶取出后在凝胶成像系统中拍照观察,从中检测其大小、纯度和浓度。 1.2.5 PCR产物的回收、纯化与测序 1.2.5.1 PCR产物的回收 称取0.3g琼脂糖于三角瓶中加入30ml的1×TBE缓冲液配成1.0%的胶。用微量取液器取3μl溴酚蓝加入Ep管,反复抽吸以混匀,再从中吸取25μl,加入上样孔。另外,吸取6μlMark点样。然后插好电极,接通电泳仪电源,调节电压90V或更低,电泳时间1h,将凝胶取出,在紫外灯下观察结果。 在紫外灯下割下目的胶条,按比例加入S1液300μl,50℃水浴10min,使胶块融化,每隔2 min摇匀一次。加100μl的异丙醇,混匀,50℃水浴5 min,混匀之后短暂离心。将溶好的Agarose胶移入吸附柱,12000rpm离心30S,倒掉收集管中的液体。将吸附柱放入同一管中,然后加入W1500μl,12000rpm离心15 S,倒去管中液体,再加入W1500μl后静置1min,离心15S,倒去液体离心1min。 1.2.5.2 纯化 将吸附柱放入一个干净的1.5mlEp管中,加20μl无菌水,37℃保温5 min溶解。 再于12000rpm离心,DNA溶于液体中。 1.2.5.3 PCR回收产物的检测 使用1.0%的胶,用微量取液器取2μl溴酚蓝加入2μlDNA溶液,加入上样孔。另外,吸取4μlMark点样。然后插好电极,接通电泳仪电源,调节电压