推荐厂家
暂无
暂无




 400-860-8560
400-860-8560
 留言咨询
留言咨询

 400-877-2799
400-877-2799
 留言咨询
留言咨询

 400-860-5168转2128
400-860-5168转2128
 留言咨询
留言咨询



抗氧化剂检验方法的发展趋势是各类食品中抗氧化剂的多组分同时测定。色谱技术如高效液相色谱、气相色谱、离子色谱已成为抗氧化剂分析的主要手段。其中高效液相色谱法占主导地位,基本上能进行所有抗氧化剂的分析,气相色谱法主要应用于脂溶性抗氧化剂的分析,离子色谱法主要应用于水溶性抗氧化剂的分析。
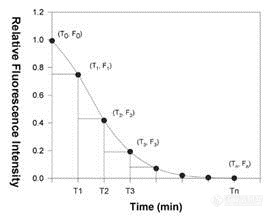
酒中抗氧化能力ORAC分析1.实验原理ORAC反应是一个经典的氢原子转移(HAT)的氧化过程。在实验条件下,一分子的AAPH失去一分子氮气,生成两分子AAPH自由基(方程1)。在空气中,生成的AAPH自由基很快与O2反应(方程2)生成相对稳定的过氧自由基ROO· 。荧光素的荧光衰退曲线表明过氧自由基对荧光素的破坏程度,在没有抗氧化剂存在的情况下,ROO·从FL获得一个氢原子(方程3),致使荧光素的荧光衰退;在有抗氧化剂(ArOH)存在的情况下,ROO·从抗氧化剂获得一个氢原子,生成ROOH和一个稳定的抗氧化剂自由基ArO· (方程4),致使荧光素被过氧自由基破坏的速率受到抑制(见图1)。R-N=N-R 2R· + N2 (1)R·+O2 ROO· (2)ROO· + probe (荧光素) ROOH + oxidized probe (失去荧光) (3)ROO·+ArOH(抗氧化剂) ArO· + ROOH (4)http://ng1.17img.cn/bbsfiles/images/2013/10/201310141626_470806_1613776_3.gif图1 ORAC检测示意图2.实验方法ORAC法即氧自由基吸收能力(又称为抗氧化能力指数),是一种测量不同食品抗氧化能力的国际通用标准单位,检测数值愈高代表其抗氧化能力就愈强。ORAC法适合抗氧化剂的高通量筛选,是目前评价抗氧化物质抗氧化活性的最为准确、灵敏度高、应用范围广的方法之一,目前国际上已经有很多商品的标签注明抗氧化能力(ORAC值)。将空白、样品以及标准抗氧化物(Trolox)各20μL,分别与160μL荧光素溶液混合后37℃保温30min,然后再加入AAPH溶液20μL,迅速开始测定,利用荧光酶标仪配备软件记录荧光强度,初始荧光强度值记为f0,以后每隔一段时间测定一个点,荧光强度分别记为f1, f2 …,抗氧化剂作用下荧光衰减曲线下的积分面积,扣除无抗氧化剂的空白曲线下面积,得出抗氧化剂的曲线下净面积(Net AUC)。抗氧化剂的ORAC值是通过其荧光衰退曲线的曲线下净面积与标准抗氧化物质Trolox的曲线下净面积相比得出的,ORAC值以Trolox当量μmol Trolox equivalent/g (μmol TE/g)或μmol Trolox equivalent/L (μmol TE/L)表达。我们将以ORAC方法来验证,包括线性(定量限与检测限)、精密度与准确度、重复性与稳定性、回收率等。通过验证方法的可行性,以此来评价保健酒的抗氧化能力。3.试剂溶液的制备3.1磷酸盐缓冲溶液3.1.1缓冲溶液储备液0.75 M K2HPO4:130 g K2HPO4溶于1 LddH2O;0.75 M NaH2PO4:90 g NaH2PO4溶于1 LddH2O 3.1.2缓冲溶液工作液分别量取K2HPO4贮备液81 mL,NaH2PO4贮备液19 mL,混合后用ddH2O定容至1000 mL,这样得到75 mM,pH 7.4的缓冲溶液,冰箱下贮存。3.2荧光素钠盐溶液荧光素钠盐贮备液1:称取0.0456g荧光素钠盐定容到100 mL磷酸缓冲液,4℃黑暗贮存;荧光素钠盐贮备液2:1000μL贮备液1用磷酸缓冲液定容至100mL,4℃黑暗贮存;荧光素钠盐工作液:800μL贮备液2用磷酸缓冲液定容至100mL,4℃黑暗贮存。3.3 Trolox标准溶液的配制0.0125 g Trolox定容到50 ml磷酸缓冲液中,得到1000μM的贮备液,−20℃ 贮存。然后用磷酸缓冲溶液依次稀释成100,50,25,12.5,6.25μM的工作液。3.4 AAPH溶液0.414g AAPH完全溶于10mL pH7.4,75mM的磷酸缓冲溶液,即得153mM的溶液,冰浴保存。(8h的有效期,现配现用)3.5
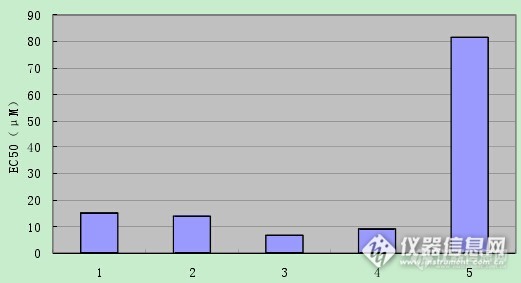
九味中药的抗氧化能力活性筛选 衰老的自由基学说最早1956年提出, 并逐步发展为自由基一氧化应激学说。此学说认为在生命活动过程中产生的自由基对生物大分子、细胞器、细胞等累积性氧化损伤,导致组织损伤和器官功能衰退,诱导及加速机体衰老。在病理条件下或随着年龄的增加,各种内外因素导致自由基大量、过多产生,超过了机体的抗氧化能力,便产生氧化应激,过多自由基通过损伤细胞核及线粒体DNA、生物膜脂质过氧化、蛋白质交联变性等多种方式引起细胞损伤,氧化损伤逐渐累积,最后导致各种老年性疾病的发生和发展。 本实验室通过大量调研文献,筛选出具有潜在抗氧化作用的中药,只在通过实验最终筛选出具有抗氧化作用比较强的药味,进一步开发利用! DPPH(二苯基苦味酰基自由基,)在有机溶剂中是一种稳定的以氮为中心的自由基,其单电子在517 nm附近有最大吸收。甲醇溶液呈紫色,其浓度与吸光度呈线性关系。当甲醇溶液中有自由基清除剂存在时,的单电子被配对而使ESR信号减弱,溶液颜色变浅,直至达到稳定。因此,可以通过在517nm波长处检测不同待测样品对自由基的清除效果,从而评价样品的抗氧化能力。本实验参照相关文献用紫外分光光度计筛选了九味中药的DPPH自由基清除活性,并测定了半效应浓度(EC50)。一、试剂与仪器二苯代苦味酰自由基(DPPH)、2,6-二叔丁基-4-甲基苯酚;氯仿、甲醇均为分析纯;紫外可见分光光度计为上海产S54A型分光光度计。二、实验方法2.1样品的制备 待测样品:九味中药分别采用水煎煮的方法提取浓缩成每1g提取液相对于10g原药材。每份提取液以最适溶剂溶解后,配成1μg/ml、5μg/ml、10μg/ml、25μg/ml、50μg/ml、100μg/ml六个浓度的溶液待测。2.2 DPPH标准曲线的制备 精密称取DPPH标准品12.62 mg,加入200 ml无水甲醇,配制成浓度为0.16 mmol/L的储液。分别精密移取1.00 mL各个样品的六个浓度的待测溶液,依次迅速加入1.00 mL DPPH甲醇溶液。在选定最大吸收波长(517 nm)的条件下,分别测定其吸光度。2.3样品的自由基清除能力测定 DPPH[


