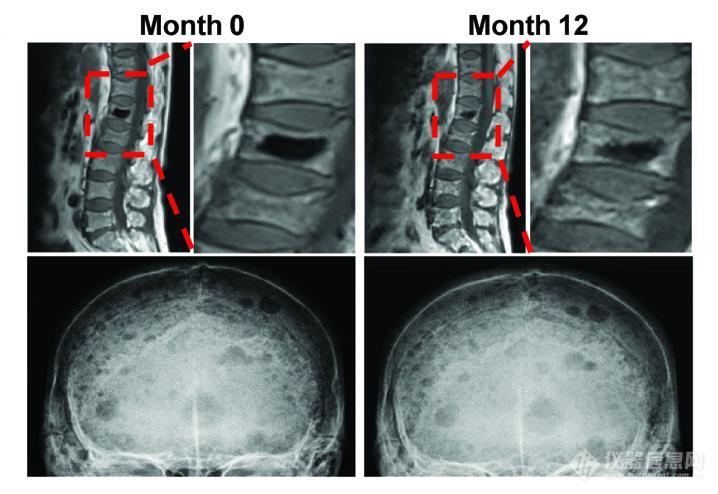
每天睡眠时间变化仅超过1小时,代谢异常风险就有可能增加27%!
一项发表在《Diabetes Care》杂志的研究将不规则睡眠模式与代谢紊乱联系了起来:不遵守规律的就寝时间和起床时间会使人更容易患上肥胖、高胆固醇、高血压、高血糖和其他代谢紊乱。事实上,上床睡觉时间和睡眠总量每变化1小时,一个人经历代谢异常的风险将增加高达27%。 一项发表在《Diabetes Care》杂志的研究将不规则睡眠模式与代谢紊乱联系了起来:不遵守规律的就寝时间和起床时间会使人更容易患上肥胖、高胆固醇、高血压、高血糖和其他代谢紊乱。事实上,上床睡觉时间和睡眠总量每变化1小时,一个人经历代谢异常的风险将增加高达27%。研究由国家心、肺和血液研究所(National Heart, Lung, and Blood Institute,NHLBI)资助。“许多以前的研究称,睡眠不足与肥胖、糖尿病和其他代谢紊乱高风险之间有联系,”文章作者、波士顿Brigham和妇女医院网络医学部的流行病学家Tianyi Huang说。“但我们对睡眠不规律、睡眠持续时间和日复一日的高变化性的影响知之甚少。我们的研究表明,考虑到一个人的睡眠量和其他生活方式因素,每晚每增加一个小时的睡眠差异(入睡时间或睡眠总量)就会使代谢不良效应成倍增加。”研究人员调查了2003年参与NHLBI动脉粥样硬化多民族研究(MESA)的45至84岁男性和女性,对参与者进行了中位数为6年的跟踪研究,目的是找出睡眠规律性与代谢异常之间的关系。为了确保对睡眠时间和质量的客观测量,参与者都佩戴了密切跟踪睡眠情况的腕表(可连续监测7天),还记录了睡眠日记,并对有关睡眠习惯和其他生活方式和健康因素的标准调查问卷作出了回应。参与者在2010年至2013年陆续完成了体动记录仪跟踪部分,随后调查研究一直跟踪到2016年至2017年。NHLBI国家睡眠障碍研究中心主任Michael Twery博士说:“客观指标和大而多样的样本量是这项研究的优势。这项研究不仅着眼于当前的因素,而且也有前瞻性分析,使我们能够评估不规则睡眠模式是否与未来的代谢异常有关。”研究人员假设关联存在,而调查结果也证明确实如此。就寝时间和睡眠时间差异较大的个体代谢问题的发生率较高,在调整了平均睡眠时间后,这些关联仍然存在。在6.3年的随访中,研究对象出现代谢紊乱的情况也与之相符。前瞻性结果显示,睡眠时间和就寝时间的变化对代谢功能障碍发展具有可预见性。根据作者的说法,这提供了一些支持不规则睡眠和代谢功能障碍之间因果关系的证据。睡眠时间变化超过一小时的参与者更有可能是非裔美国人、非白班工作者、吸烟者,并且他们的睡眠持续时间普遍更短。他们也有较高的抑郁症状、总热量摄入和睡眠呼吸暂停指数。然而,增加睡眠时间或入睡时间波动与多种代谢和随之出现的问题(如低HDL胆固醇、高腰围、血压、总甘油三酯和空腹血糖)密切相关。“我们的研究结果表明,保持规律的睡眠时间对新陈代谢有好处,”合著者、Brigham和妇女医院睡眠和昼夜节律紊乱部的高级医师Susan Redline医学博士说。“这一信息将丰富当前代谢性疾病的预防策略,主要集中于促进充足的睡眠和其他健康的生活方式。”
厂商
2019.06.10
肠道微生物群是健康老年人的秘密吗?
要点: 移植年轻小鼠的粪便可以增强老年小鼠的肠道免疫系统。由于年龄增长,肠道免疫反应下降并不是不可逆转的,肠道细菌可以促进老年个体肠道免疫反应。肠道微生物群可能是治疗一系列衰老相关症状以促进健康老龄化的目标。剑桥Babraham研究所免疫学家的一项研究表明,移植幼鼠粪便给老年小鼠可以刺激肠道微生物群并恢复肠道免疫系统。这项研究发表在《 Nature Communications》杂志上。肠道是受衰老影响最严重的器官之一,人类肠道微生物群的年龄依赖性变化与虚弱、炎症和肠道疾病易感性增加有关。这些肠道微生物群的年龄依赖性变化与肠道免疫系统功能的下降同时发生,但直到现在,还不知道两者变化是否有联系。“我们的肠道微生物群由数百种不同类型的细菌组成,这些细菌对我们的健康至关重要,在我们的新陈代谢、大脑功能和免疫反应中发挥着作用,”主要研究人员Marisa Stebegg博士解释说。“我们的免疫系统不断地与胃肠道中的细菌相互作用。作为免疫学家,我的研究课题是为什么衰老后,我们的免疫系统就不能好好工作?我们也有兴趣探索肠道微生物群的组成是否影响肠道免疫反应的强度。”混合饲养年轻和老年小鼠(小鼠天生喜欢从其他小鼠的粪便中摄取营养!)或者更直接地,转移年轻小鼠粪便给老年小鼠,都可以增强老年小鼠的肠道免疫系统,部分纠正与衰老相关的身体机能下降。“令我们惊讶的是,共同居住拯救了老年小鼠肠道免疫反应的降低。观察所涉及的免疫细胞数量,老年小鼠的肠道免疫反应几乎与年轻小鼠的肠道免疫反应不可区分,”Babraham 研究所免疫计划小组负责人Michelle Linterman博士评论道。结果表明,不良的肠道免疫反应并不是不可逆转的,并且可以通过适当的刺激来增强这种反应,这项研究暗示基本上可以通过将肠道免疫系统时钟调回更接近幼鼠的状态。研究结果与治疗衰老相关症状有关,证实了免疫系统老化的影响与肠道微生物群年龄相关变化之间的联系。通过证明对肠道微生物群组成具有积极影响的干预措施的有效性,本研究表明,粪便移植、益生菌、共同居住和饮食都可能是促进健康老龄化的方法。
厂商
2019.06.10
可复制的微型人脑3D模型开辟神经科学新领域
哈佛大学和Broad研究所斯坦利精神病研究中心的科学家们在人类大脑“类器官”的发展方面取得了重大进展:加入病人自己脑细胞的微型3D组织培养物。他们的新方法发表在《Nature》杂志,这一进展将会改善神经精神疾病研究和药物测试的有效性。人类神经系统疾病背后的遗传学是复杂的,有关疾病发生和发展的基因组跨度很大。再加上人脑的独特性,研究其他动物为神经疾病相关发现提供的机会有限。类器官是一个好的方向,但到目前为止,有一个非常关键的问题还没有攻克。“我们可以使用不同的大脑(细胞),但是,大脑连接和基本细胞类型是相同的,”哈佛大学干细胞和再生生物学教授、斯坦利中心成员、文章通讯作者Paola Arlotta解释说。“这种一致性很重要,而且除了极少数例外,人类大脑在子宫中形成时,这种一致性就会被复制。就我们大脑中的细胞类型和结构而言,我们人与人之间只有非常小的差异。”然而,现在的类器官做不到如此。虽然它们确实能产生人类的脑细胞,但每一个都是独一无二的。这意味着它们不能轻易地用来比较患病和对照脑组织之间的差异。“类器官大大提高了我们研究人类大脑发育的能力,”Arlotta说。“但到目前为止,每个类器官都是独一无二的,以一种从一开始就无法预测的方式制造自己独特的细胞类型组合。现在,我们解决了这个问题。”在干细胞生物学家Yoshiki Sasai领导的开创性工作基础上,该团队创造了即使在实验室连续生长超过6个月也几乎没有差别的类器官。此外,在特定培养条件下,类器官是健康的且能够发育足够长的时间来产生人类大脑皮层中发现的广泛的细胞类型。这些进展意味着,脑类器官现在可以作为一种直接研究患者组织中疾病并比较不同药物对人脑组织的影响的可行实验系统。同样的细胞,同样的方式研究人员重点研究了大脑皮层类器官:这里负责认知、语言和感觉。大脑皮层在自闭症谱系障碍和精神分裂症等神经精神疾病中起着关键作用。文章主要作者、哈佛大学和Broad研究所的研究科学家Silvia Velasco解释说:“我们从多个来自男性和女性的干细胞系中提取了类器官,所以它们的遗传背景是不同的。”人脑组织生长非常缓慢。在这项研究中,六个月类器官的直径增长到了三毫米。在这项迄今为止最大的脑类器官单细胞RNA测序实验中,研究人员根据不同阶段表达的基因对细胞进行了分组。利用大数据分析的计算模型,他们将每一组与胚胎大脑皮层发育的细胞类型进行了比较。“尽管有不同的遗传背景,我们发现每个类器官中相同的细胞类型都是以相同的方式和正确的顺序组织的,”Velasco说。“我们真的很兴奋,因为这个模型给我们提供了非常好的一致性。”疾病调查新方法诞生了利用该优化方法,研究人员可以从患者的干细胞中提取类器官,或者设计含有与特定疾病相关突变的细胞。Arlotta实验室目前正在利用CRISPR/CAS9基因编辑技术探索自闭症大脑类器官。“现在有可能将‘对照’类器官与我们已知的疾病相关突变进行比较。这将使我们更加确定哪些差异是有意义的,哪些细胞受到影响,哪些分子路径出错,”Arlotta说。“拥有可复制的类器官将帮助我们更快地走向具体干预,它们将指导我们找到引起疾病的特定遗传特征。在未来,我设想我们将能够就精神疾病提出更为准确的问题。”“在很短的时间内,我们对人脑中许多不同类型的细胞有了大量了解,”共同作者Aviv Regev说,他是Broad研究所的核心研究所成员和教授,同时也是人类细胞图集项目的共同主席。“这些知识为我们创造了复杂器官模型奠定了基础。克服再现性问题为研究人类大脑打开了大门。”
厂商
2019.06.10
港大学者Nature子刊培养出猪扩增潜能干细胞
这项研究在干细胞领域取得突破性发展,为胚胎发育、再生医学、生物科技及农业的研究开拓了新途径。生物通报道:来自香港大学李嘉诚医学院(港大医学院)的研究人员发表了题为“Establishment of porcine and human expanded potential stem cells”的文章,在全球首次成功获得猪的扩增潜能干细胞(EPSCs),这是一类保留有胚胎最初发育潜能的细胞,这为研究胚胎发育,基因组学、再生医学、生物科技及农业的转化研究带来新突破。这一研究发现公布在6月3日的Nature Cell Biology杂志上,文章的通讯作者为港大医学院刘澎涛教授和德国汉诺威医学院的Heiner Niemann。EPSCs是什么?迄今为止,胚胎干细胞一般都是来自于数十个细胞的植入前胚胎(又称囊胚)。在囊胚形成前,胚胎细胞仍然具备分化成不同种类细胞的可能性,因此具有全能性特征。2017年,当时还在英国Sanger研究院的刘澎涛博士第一次在小鼠中生成了一类新型干细胞:Expanded Potential Stem Cells (EPSCs,扩增潜能干细胞),这类细胞比目前的干细胞系具有更大的扩增潜力,它们具有发育胚胎中第一细胞的特征,并且可以发育成任何类型的细胞。研究表明,EPSCs源自囊胚形成前的植入前胚胎,而通用的标准胚胎干细胞则是在受精卵发育成大约100个细胞的胚囊阶段时提取的。因此研究人员认为,从发育最初期的胚胎细胞建立新型胚胎干细胞可能会进一步促进干细胞研究。猪扩增潜能干细胞刘教授表示,“几十年来,科学家们一直试图获得猪胚胎干细胞而没有取得多大成功,通过我们的扩增潜能干细胞技术,现在可以成功地从猪胚胎植入前胚胎中获得并鉴定了这种干细胞。我们还建立了类似的人类干细胞。”这项最新研究从猪和人类身上取得扩增潜能干细胞(EPSCs),其中猪EPSCs研究结果尤为重要,因为这是科研人员首次在猪早期胚胎中取得干细胞。猪具有重要的生物医学研究价值,其遗传基因、身体构造及生理机能(如器官大小)与人类相近。如果能够改造猪的干细胞基因,不但有利于动物健康及食物生产,而且也能促进生物医学研究 ,比如器官移植。当然,人体EPSCs研究也可为人体的发育成长及再生医学研究提供新的细胞来源。目前,刘澎涛教授团队已经成功从小鼠、猪和人类取得EPSCs。这些来自不同物种的干细胞,有相似的分子特性,可以进行多次基因编辑。人类的EPSCs除了可以分化为人体的所有细胞类型,用于人类疾病和再生医学研究,而且还由于人体EPSCs可以产生大量胎盘滋养层细胞,可以提供研究先兆子痫和流产等妊娠并发症提供了新机会文章第一作者,港大生物医学学院的高学飞博士表示,“这些EPSCs细胞具有传统胚胎干细胞或诱导多能干细胞不常见的发育潜能。它们可以产生所有胚胎和胚胎外细胞系,包括在胎盘和卵黄囊中出现的细胞类型。”科学家在上世纪70和80年代首次从小鼠囊胚建立胚胎干细胞系,但迄今为止,除了在一些啮齿类及灵长类动物以外,科学家很难从其他哺乳类动物建立胚胎干细胞株。刘澎涛教授和其团队在多年前提出了这个新的EPSC构想,他们认为从比囊胚期更早期的植入前胚胎建立干细胞体系十分重要。“越早在哺乳类动物胚胎发育初期取得干细胞,细胞中物种之间可能存在的差异越小,EPSC技术应用在多种哺乳类物种上的成功机会就越大。我们的目的是研究在什么条件下,可以在不同物种的胚胎发育的最早期取得干细胞,这个时期的胚胎细胞就像一张空白的纸,理论上说应该具有最大的发育潜力,而最新研究结果证明,这个构思和猜想基本上是正确的”,刘教授说。文章的另外一位一作,德国动物卫生研究院Monika Nowak-Imialek博士说:“我们从猪胚胎分离出来的EPSCs是全球首个拥有完整潜能的猪胚胎干细胞株。由于EPSC具有分化成所有类型细胞的发育潜能,它们将可以极大程度促进发育生物学、再生医学、器官移植、疾病模型,动物健康、农业及生物科技。”刘教授早年毕业于河南师范大学,1998年博士毕业于美国贝勒医学院,2003年加盟英国威康信托基金会桑格研究所研究员,2010年晋升为资深研究员和课题组长。2005年担任过包括辉瑞在内多家生物医药公司之科学顾问,后开始在港大组建实验室,擅长化学基因组研究,先后发表学术论文百余篇。
厂商
2019.06.05
贺建奎基因编辑婴儿出现致命缺陷!Nature子刊近40万人研究新发现
基因编辑CRISPR婴儿的预期寿命可能会缩短,一项对近50万人的研究将预防艾滋病毒感染的突变与早期死亡联系起来。 生物通报道:去年11月,何建奎宣布世界首例艾滋病免疫基因编辑婴儿的诞生,这一爆炸性新闻席卷了全球,包括科学界在内的社会各界对此表示了谴责,伦理学家认为他不应该随意改变个体基因,并将其传递给后代,而科学家们则质疑他对基因的选择,因为CCR5这种编码允许HIV进入免疫细胞的蛋白质的基因的缺失有可能造成人们更容易受到流感病毒和西尼罗河病毒的感染。而最新的一项研究也指出这一本来用于帮助编辑婴儿抵抗艾滋病毒的基因,有可能会缩短个体的预期寿命。来自加州大学伯克利分校的研究人员发现携带CCR5基因两个缺陷拷贝的个体虽然似乎能防御艾滋病毒感染,但是比较于携带至少一个正常拷贝基因的个体,前者的预期寿命要比后者的低:76岁之前死亡的可能性增加了21%。这一研究发现公布在6月3日的Nature Genetics杂志上。这项分析基于英国生物银行研究项目中41万人的遗传和健康数据,其中没有足够的数据来估计超过76年的生存概率。CCR5编码一种允许HIV进入免疫细胞的蛋白质,剔除其部分基因可以使其失效,模仿自然发生的突变,CCR5-Δ32,具有对HIV的抗性。而最新的研究引发了对于贺建奎编辑婴儿研究的更多质疑,毕竟目前的艾滋病治疗方法可以让许多患者过上老年生活。神秘的突变在贺建奎宣布基因编辑婴儿之时,加州大学伯克利分校的进化生物学家April Wei正在开发一种计算工具,利用英国生物银行的数据将基因突变与寿命联系起来。她和遗传学家Rasmus Nielsen决定用CCR5测试这个工具。“这本身就是一个有趣的基因,”Wei说。所有哺乳动物基因组都含有CCR5基因,表明它在这些动物生物学中具有重要作用。然而,在某些人群中,CCR5-Δ32突变也很常见。大约11%的英国人携带的CCR5基因出现了两个拷贝的突变,而且在部分地区甚至更高。一种功能性基因的删除突变很少如此普遍。CCR5-Δ32的流行表明,至少在某些情况下,CCR5基因缺失可以带来进化优势。但科学家们不知道那是什么。英国埃克塞特大学的流行病学家David Melzer表示,CCR5-Δ32突变与预期寿命之间的明显联系很有意思,但并不奇怪,Wei和Nielsen用于检测CCR5突变形式的遗传标记之一与自身免疫疾病相关,如克罗恩病和1型糖尿病,这会缩短一个人的生命。但Melzer认为,CCR5缺失与寿命之间联系的证据远不及许多其他基因对长寿影响的证据。也有科学家认为这项研究有局限性,因为它的数据来自41岁或以上的人,并且会排除任何先前死亡的人,或者没有报名参加英国生物银行的病人。但他表示,研究人员“在所掌握的信息方面做得非常出色”。未知的风险对Wei来说,这项研究发现强调了一个观点,那就是禁用人类胚胎中的基因是一个坏主意。“我认为很难证明基因是无条件有益的,这是值得考虑的事情,”她说,“即使我们解决了技术难题和道德问题,如果我们不知道它是否会产生有害影响,我们真的可以编辑基因吗?”加州大学洛杉矶分校的神经科学家Alcino Silva同意这一观点。他说:“从这一点出发,改变人类的基因,简直就是蛮干” 。“无论我们在设计这些遗传操作时我们的用意是多么善意,我们此时根本就不知道这样做是不是正确的。”Silva的团队还发现阻断CCR5似乎可以帮助人们从中风中恢复得更快,并提高小鼠的记忆力和学习能力。但他表示,禁用该基因类似于消除汽车刹车。“这辆车的速度会变得非常快,”Silva说,但风险会更高,正如修补大脑发育可能导致疾病一样。 “进化其实已经很努力,给我们提供了我们需要的基因。”
厂商
2019.06.05
《Cell》:皮肤和肝脏有独立于大脑的“时钟”!
白天,我们会经历一系列生理、心理和行为的变化,即昼夜节律。这些变化是由位于大脑中心,下丘脑的中央时钟控制的。这个时钟负责同步我们的组织,以确保它们的功能是协调的,并在同一个时钟下一起工作。生物医学研究所(IRB,巴塞罗那)的科学家的研究结果显示,尽管每个组织都从中央时钟接收信息以协调其功能,但每个组织也有能力独立地对光的变化做出反应,并感受白天和夜晚之间光强度的变化。这项研究发表在Cell杂志上的两篇论文中,证实了这种自主性,这使得我们的组织即使在身体另一个组织濒临衰竭的时候也能保持最小的功能。“这些研究结果可能与衰老和疾病特别相关,在这些疾病中,人们曾认为高度的组织依赖性将导致机体的普遍恶化,”巴塞罗那IRB干细胞和癌症实验室主任Salvador Aznar Benitah说。到目前为止,还没有合适的动物模型能够测试调节我们所有器官和组织的时钟是否由大脑协调,或者正如已经观察到的那样,这些器官和组织是否能够直接对每天发生的循环环境变化做出反应。这项研究是由巴塞罗那IRB与美国加州大学欧文分校的Paolo Sassone Corsi团队合作完成的,他们得益于一种使研究人员能够将每个组织的通讯与其他组织分隔开来的新小鼠模型。本文的第一作者,博士后学者Patrick Simon Welz和“La Caixa”博士生Valentina María Zinna(他们均在巴塞罗那IRB工作),比较了这种小鼠模型其中的健康小鼠和中央时钟受损小鼠的表皮和肝脏的昼夜节律,该模型不同组织之间没有交流。确认了这两个组织对随时间推移而发生变化的光照有自主性。中央时钟与整个身体通讯如前所述,虽然每个组织都是自主的,但这并不意味着没有与身体其他部分的交流。“我们证实了中枢时钟与大脑和身体其他部分的通讯,提供有用的信息来确保身体其它部分的正确功能,例如,通知胃肠道、肝脏和胰腺是时候吃饭了,并让它们为消化做好准备。但当这种交流失败时,每个器官都能知道现在是什么时间,从而自觉地完成它们的基本功能,”ICREA研究人员Salvador Aznar Benitah说。“我们的结果对健康有重要影响,”Aznar Benitah说。“我们现在的生活方式让黑夜暴露在光明中。鉴于每个器官都能独立地对光做出反应,白天应该发生的身体功能在晚上发生的话,这种每天的时段差或社会时差可能导致早衰和某些病理疾病。”
厂商
2019.06.05
破解“化骨绵掌”幕后黑手——叛变的脂肪细胞
一项对多发性骨髓瘤(multiple myeloma,MM)患者样本的研究已经证明了“重新编程”的脂肪细胞,即使在癌症已经得到缓解后,是如何导致长期的骨损伤的。一项对多发性骨髓瘤(multiple myeloma,MM)患者样本的研究已经证明了“重新编程”的脂肪细胞,即使在癌症已经得到缓解后,是如何导致长期的骨损伤的。以分子复合物作为靶标可减轻小鼠体内骨损害病变的严重程度,提示针对MM这种常见的且使人虚弱的并发症的可能治疗对策。当癌性浆细胞积聚在骨髓中并对其他血细胞的制造生产产生不利影响时,就会发生这种恶性肿瘤。超过80%的MM患者的骨骼也出现溶骨病变,这可能导致严重疼痛和骨折。即使成功治疗了癌症,这些损伤也无法愈合,从而导致骨愈合的长期缺陷和较低的生活质量。为了理解为什么溶骨病变不能愈合,Huan Liu和他的同事研究了活动期骨髓瘤患者、缓解期患者和健康对照组的骨髓样本。他们观察到,靠近溶骨病变的部位含有大量的骨髓脂肪细胞(脂肪细胞)。与骨髓瘤细胞一起培养的脂肪细胞“逆生长”为重新编程状态,释放抑制骨形成和促进骨分解的酶。进一步的分析显示,骨髓瘤细胞通过激活一种叫做PRC2的分子复合体来转化脂肪细胞,进而抑制一种叫做PPARγ的受体的活性。脂肪细胞中,PRC2复合体组分EZH2失活可阻止其重新编程,并降低MM缓解期小鼠模型中骨损伤的严重程度,这表明恢复PPARγ活性有助于治疗患者的骨损伤。
厂商
2019.06.04
阻挡高剂量放射辐射新方法
损伤健康肠细胞是放射治疗的主要缺点,导致癌症有效治疗中断和失败,还有可能导致肿瘤快速复发。现在,西班牙国家癌症研究中心(CNIO)生长因子、营养素和癌症研究小组的科学家在Science杂志上发表的一项发现可能有助于保护健康的肠道细胞免受辐射损伤。 放射治疗是常见的癌症治疗方法,可以破坏癌细胞,是缩小肿瘤的最有效方法之一。大约50%的胃肠道肿瘤患者(肝脏、胰腺、结肠、前列腺等)接受了这种治疗,在过去几十年中提高了癌症患者的生存率。然而,密集的放射治疗不仅会损伤肿瘤细胞,而且还会损伤健康的肠道细胞,导致60%的患者中毒。虽然在放射治疗结束后观察到,毒性损伤有所恢复,但10%的治疗患者出现胃肠道综合征,这是一种以肠道细胞死亡为特征的疾病,导致整个肠道的损坏和患者死亡。该小组的工作重点是URI,一种功能尚未完全理解的蛋白质。然而,该小组先前的研究发现,这种蛋白质在某些器官中的异常表达水平可以导致癌症。这项发表在Science杂志上的研究表明,高水平的URI蛋白可以保护小鼠免受辐射引起的肠道损伤,而低水平或无检测到的URI蛋白可能导致胃肠道综合征和死亡。损伤健康肠细胞是放射治疗的主要缺点,导致癌症有效治疗中断和失败,还有可能导致肿瘤快速复发。现在,西班牙国家癌症研究中心(CNIO)生长因子、营养素和癌症研究小组的科学家在Science杂志上发表的一项发现可能有助于保护健康的肠道细胞免受辐射损伤。他们在小鼠身上的研究结果可能会从根本上改变人类处理高水平辐射的方式;既适用于癌症研究和治疗,也适用于太空探索、核战争或核事故等其他领域。“还没有确定URI的准确功能,”西班牙国家癌症研究中心生长因子、营养素和癌症研究小组的负责人,该研究的Nabil Djouder说。“就像生物体需要维持在一定范围内的酸碱度或温度一样,URI水平也必须保持在一个很窄的窗口内,以调节其他蛋白质的正常功能。当URI水平高于或低于佳水平时,它们可能促进或保护肿瘤的发展以及其他疾病,这取决于不同的环境。”Djouder长期以来一直在研究URI,他开发了一个基因小鼠模型来研究这种蛋白质在哺乳动物中的功能。他的研究小组观察到高URI水平可以保护肠道细胞在培养过程中免受DNA损伤。因此,Djouder和博士生Almudena Chaves-Pérez认为他们需要研究URI的保护功能在体内是否有效,以及它是否能够减轻大剂量辐射的影响,和减轻由此导致的胃肠道综合征。为了解决这些问题,他们开发了三种基因小鼠模型。这是首次为了专门研究URI的作用和辐射对肠道的影响而创建的实验性基因小鼠模型。其中一个作为对照模型,用于确定肠中URI的确切表达位置;另一个小鼠模型在肠中表达的URI蛋白水平很高,第三个模型删除了该基因,以降低肠上皮中的URI水平。对照组小鼠显示,URI在位于肠隐窝的特定休眠干细胞群(称为Lieberkühn隐窝)中表达。URI保护这些细胞免受高剂量辐射引起的毒性。“我们发现,当放射治疗结束后,这些细胞会再生受损组织。”该文章的作者 Chaves-Pérez说,“最近有很多关于哪些干细胞群体负责这项工作的争论。”在接受大剂量辐射后,在肠道中表达高水平URI的小鼠在胃肠道综合征中存活下来,而在正常条件下,高达70%的小鼠死亡。相反,所有删除URI基因的小鼠都死于胃肠道综合征。Chaves-Pérez解释这个结果说,“这种特定的干细胞群体的区别在于,在正常情况下(当它们表达URI时),这些细胞是静止的,也就是说,它们不会增殖。因此,它们不会受到辐射损伤,而辐射损伤只会影响增殖细胞。然而,当这些干细胞中不存在URI时,众所周知的癌基因c-myc会过度表达,导致细胞增殖,增加这些细胞对辐射损伤的敏感性。结果,这些细胞死亡,肠道无法自我修复,随后小鼠死亡。”尽管他们的发现需要进一步的研究来证实,但Djouder相信c-myc抑制剂可能有助于减轻患者在辐射下引起的胃肠道综合征。“我们的研究为通过抑制或消除c-myc来治疗和预防胃肠道综合征开辟了新的途径。这种抑制剂将减少高剂量放射治疗的致命副作用,使放射剂量能够增加从而有效地治疗癌症并保护患者免受胃肠道综合征的影响。”Djouder说,“除了防止辐射的致命副作用外,c-myc抑制剂还用于癌症治疗,这意味着它们可能具有双重功效。”现在,了解其他具有再生能力的器官,如皮肤,是否具有高水平表达URI的特殊干细胞群,这将是一件有趣的事情。Djouder和他的团队目前正在研究这方面。Djouder相信除了它在癌症领域的重要性,这一发现可能对高剂量辐射的防护,例如在发生核事故、核战争或长时间的空间探索中暴露于宇宙辐射的防护方面具有重大意义。
厂商
2019.06.04
从肠道出发治疗神经疾病:肠道细菌可干涉小鼠自闭症样行为!
在现代这个社会,女性(而非男性)更多地被“受荷尔蒙影响的”或“受情绪影响的”等词语加以修饰,但这是一种对公共卫生构成重大问题的过时的刻板印象,东北大学心理学系神经解剖学与行为实验室助理教授Rebecca M. Shansky写道。在现代这个社会,女性(而非男性)更多地被“受荷尔蒙影响的”或“受情绪影响的”等词语加以修饰,但这是一种对公共卫生构成重大问题的过时的刻板印象,东北大学心理学系神经解剖学与行为实验室助理教授Rebecca M. Shansky写道。如今,认为循环系统中的卵巢激素使女性受试者的数据“更加混乱”的观点继续影响着动物实验设计。在Shansky所在的神经科学领域,受试动物通常仍主要是雄性,“当我们在雄性背景下观察雌性时,”Shansky说,“我们可能会错过雌性问题的关键所在,特别是在情绪和焦虑障碍有关的行为研究中尤为棘手,例如严重抑郁症和创伤后应激障碍这两种疾病在女性中的患病率是男性的2倍。”“周期性发情会使女性受试者的数据比男性受试者的数据更具易变性,纵观整个历史,这一观点似乎是合理的假设,”Shansky写道。但是始终缺乏科学检验。直至2014年一项神经科学荟萃分析发表文章指出,不管处于任何发情周期,雌鼠与雄鼠相比变化并不大,事实上,在某些情况下,雄鼠比雌鼠的变化更大,特别是种群中的雄性小鼠(而非雌性)建立起优势等级时,优势雄鼠的睾酮水平平均是从属雄鼠的5倍。直到2016年美国才要求所有受资助的动物研究同时使用两性,并将性别作为一个生物变量(SABV)。然而,由于SABV指令没有明确规定如何设计两性实验,一些神经科学家已经达成了“折衷共识”——先解决雄性问题,然后再利用他们的发现解决雌性的相同问题。Shansky说,折衷策略是危险的,“因为它延续了过时的、性别歧视的、科学上不准确的观念,认为雄性的大脑是‘标准的’,而雌性大脑则是其‘偏离版本’。”她说研究人员应该严格遵守SABV指令,不要让过时的性别歧视使科学研究偏离严谨。“女性并不比男性更复杂,荷尔蒙也并非‘只有雌性才有的问题’。我们需要停止用这样的态度来对待动物研究。”
厂商
2019.06.04
iScience:花粉管微丝高级结构控制新机制
论文综合生物化学、遗传学和活体成像技术揭示了在拟南芥花粉管中维持微丝成束因子FIM5和PLIM2a/PLIM2b之间的平衡对于产生正常的微丝结构至关重要。清华大学生命学院黄善金课题组在Cell期刊新推出的子刊iScience上在线发表了题为“微丝成束因子之间的平衡控制花粉管微丝结构”(The Balance between Actin Bundling Factors Controls Actin Architecture in Pollen Tubes)的研究论文。该论文综合生物化学、遗传学和活体成像技术揭示了在拟南芥花粉管中维持微丝成束因子FIM5和PLIM2a/PLIM2b之间的平衡对于产生正常的微丝结构至关重要。花粉管生长为两个不能运动的精细胞提供运输载体,最后将精细胞送到胚珠完成开花植物的双受精过程。花粉管生长非常快速,探讨花粉管生长调控机制一直是植物生殖生物学和细胞生物学领域重要的科学问题。与花粉管快速生长相匹配的是花粉管中存在着旺盛的由微丝骨架系统驱动的细胞质环流现象。目前对于花粉管胞质环流现象的认识如下:即一些囊泡或细胞器以微丝骨架为轨道在花粉管中产生运动。在这个理论框架中,产生和维持有序的微丝结构是推动胞质环流的基础。花粉管如何控制这些有序微丝结构的产生得到了人们的广泛关注,大部分的研究集中在解析某一个或某一类微丝成束因子的功能和作用机制上,对于不同类微丝成束因子如何协作调控花粉管微丝结构几乎一无所知。黄善金课题组前期的研究发现拟南芥FIM5作为重要的微丝成束因子在花粉管中稳定微丝并控制其空间排布,进而控制胞质环流和花粉管生长(Plant Cell, 2010; J Exp Bot., 2016; J Biol Chem., 2016)。但在研究的过程中发现缺失FIM5的花粉管中充满了大小比较均匀的微丝束,这个现象不太容易从丢失一个微丝成束因子的角度对fim5突变体花粉管中出现的微丝结构缺陷进行合理的解释。这项研究增进了人们对胞内微丝高级结构调控机制和花粉管生长调控机理的理解,并为未来深入解析不同微丝成束因子之间的功能协作和机制奠定了良好的基础。当时推测一些生化性质各异的微丝成束因子在fim5突变体花粉管中功能替代了FIM5产生了异常的微丝排布。为了找到这些功能替代的微丝成束因子,当时进一步的假设是那些与FIM5生化性质各异的微丝成束因子的转录水平在fim5突变体花粉中可能发生了改变。基于该假设,黄善金课题组对fim5突变体和野生型花粉的转录组进行了分析,发现微丝成束因子PLIMs的转录水平在fim5突变体花粉中显著上调。后续的实验证明PLIMs蛋白的功能上调确实是造成fim5突变体花粉管中微丝结构缺陷的其中一个重要的原因。综合论文中的研究结果,表明维持FIM5和PLIMs之间的平衡对于花粉管槽部产生正常的微丝束结构至关重要。清华大学生命学院黄善金研究员为本文的通讯作者,黄善金课题组已毕业博士张瑞辉、已出站博士后屈晓璐和已毕业博士张孟为本文的共同第一作者。本研究得到了清华大学生命学院王宏伟实验室以及首都师范大学于荣实验室的大力帮助。本课题得到了国家自然科学基金委和清华-北大生命科学联合中心的资助。
厂商
2019.06.03
从肠道出发治疗神经疾病:肠道细菌可干涉小鼠自闭症样行为!
自闭症谱系障碍(ASD)影响1/59的美国人,造成各种社会困难。包括遗传和环境影响许多因素被认为与症状有关,但是仍缺乏批准的治疗方法。现在,加州理工学院的研究人员利用老鼠模型发现,肠道细菌可直接导致老鼠的自闭症样行为。 这项工作主要由Sarkis Mazmanian实验室承担,论文发表在5月30日的《Cell》杂志。“近年来,许多研究表明,患有自闭症和神经病的人的肠道微生物群细菌组成存在差异。然而,虽然先前的研究确定了潜在的重要关联,但无法确定观察到的微生物群变化是ASD的结果还是会导致症状。”“我们的研究表明肠道微生物群足以促进小鼠的自闭症样行为。然而,这些发现并不表明肠道微生物会导致人类自闭症,”Mazmanian实验室的资深博士后学者、该研究的第一作者Gil Sharon强调说。“还需要进一步研究来解决肠道细菌对人体的影响。”人类肠道内的微生物群落称为微生物群(microbiota),它们的集体基因组称为微生物组(microbiome)。这些生物体与人类生活在一种共生状态。在肠道这个温暖和营养丰富的环境中,细菌帮助我们消化食物,影响新陈代谢,并训练我们的免疫系统。为了研究微生物群在小鼠自闭症样行为中的作用,研究小组使用了“无菌”小鼠——在没有微生物的情况下生长的实验动物。自闭症儿童的肠道微生物通过粪便移植被转移给这些小鼠,来自没有自闭症的人的样本被移植给其他动物组。患有自闭症个体的微生物群小鼠表现出自闭症样行为,而携带普通发育个体的微生物群的小鼠没有表现出这些症状。具体来说,“自闭症样”小鼠们花较少的时间与其他小鼠进行社交,较少发声,并且表现出重复的行为。这些症状类似于自闭症患者的行为特征。除了行为上的差异外,携带人类ASD微生物群的小鼠大脑中的基因表达也发生了改变,并且存在代谢物类型差异(代谢物是消化和微生物代谢的副产物)。在这些小鼠体内发现了两种较低含量的代谢物:5-氨基戊酸(5-aminovaleric acid,5AV)和牛磺酸。ASD的特点是大脑中的兴奋和抑制比例不平衡,因此研究人员对较低量的5AV和牛磺酸很感兴趣,因为两者都会影响抑制性神经受体——GABA受体。Sharon说:“我们很惊讶地看到这些影响有多么深远。”随后,研究小组转向其他不同自闭症模型的小鼠。一种被称为BTBR的小鼠自然表现出自闭症样行为。研究人员想看看用5AV或牛磺酸治疗这些小鼠是否能减轻这些行为症状。值得注意的是,经过治疗的小鼠确实表现出自闭症样行为的减少。此外,脑部检查显示,特别是5AV让小鼠们的神经兴奋性下降。有许多因素使得自闭症在人类中比在鼠身上更复杂。“在小鼠身上,我们可以模拟这种疾病的症状,但不能复制它,”Mazmanian说。“然而,这项研究为肠道微生物群在与自闭症相关的神经变化中的作用提供了线索。这表明,自闭症症状有一天也许能通过细菌代谢物或益生菌药物来治疗。此外,它还为自闭症以及其他典型的神经系统疾病提供了一种可能性,即通过针对肠道而非大脑的疗法来治疗自闭症,这似乎是一种更容易处理的方法。”
厂商
2019.06.03
《Cell》新发现:心脏存在未知小蛋白
由Norbert Hübner教授研究小组领导的一支研究团队观察正在工作的人类心脏细胞“蛋白质工厂”时,惊讶地发现了一个未知的小蛋白,而且它对未来心脏病治疗具有潜在意义。文章发表在《Cell》杂志。 人心容纳着许多秘密。不仅是在形象的、情感意义上,从理性的、科学角度来看,我们对这个为全身每个细胞提供氧气功能的肌肉器官知之甚少,也不知道它为什么有时失灵。现在,发表在科学杂志《Cell》上的一项研究对这个最重要的器官有了更多的了解。由MAX DELBRüCK分子医学中心(MDC)领导的一个由56名研究人员组成的国际小组检查了健康人和心脏病患者心脏细胞中的核糖体所产生的蛋白质。结果令人惊讶——新发现了大量以前完全未知的迷你蛋白质。DNA包含的蓝图比以前想象的要多得多储存在每个细胞核中的DNA包含了人体内产生的所有蛋白质的蓝图。蛋白质的产生是两步过程:转录和翻译。第一步,DNA片段的拷贝以信使RNA(mRNAs)的形式产生,然后离开细胞核。第二步,核糖体利用细胞中游离的单个氨基酸来产生相应的蛋白质。尽管我们对转录的科学研究比较多,但对翻译过程的了解却相对较少。MDC心血管疾病组、该研究的主要作者Sebastiaan van Heesch博士解释说:“借助一种被称为核糖体分析(Ribo-Seq)的相对较新技术,我们现在已经能够首次确定不仅是孤立细胞中的,而且是完整的人类心脏组织中,迁移到核糖体的mRNA。然后利用特殊算法,我们可以计算出在翻译过程中,心脏中产生的蛋白质。”利用这种策略,研究人员发现了一系列以前未知的微型蛋白质。van Heesch和研究小组的另一个令人惊讶的发现是,许多微蛋白质是由不被认为具有编码特性的RNA编码的,也就是说,过去它们不曾被认为携带构建蛋白质的指令。大多数迷你蛋白质被用来生产能量利用特殊的显微技术,科学家们随后观察到,一旦被生产出来,超过一半的这些迷你蛋白迁移到线粒体中。“意味着它们显然被用于了心脏的能量生产过程。由于许多心脏病都是由能量代谢不良引起的,我们对这个结果特别感兴趣。”为了检测疾病心脏和健康心脏的翻译本(反应形成的蛋白质总量)之间的可能差异,科学家们检查了65名扩张型心肌病(DCM)患者的组织样本。在预定的心脏手术期间,通过活检从患者身上提取样本,以及15例健康心脏组织。“DCM患者需要在生命中的某个时刻接受心脏移植,它是由titin基因突变引起的,titin基因是人类心脏中最大和最重要的蛋白质。该基因突变的结果是,在线粒体中产生一个停止信号,告诉核糖体在完成titin之前停止工作,”van Heesch解释说。“然而,并非所有携带这种基因突变的人都会发展成DCM。”治疗心脏病van Heesch和他的同事们现在正在调查背后的原因。“我们已经观察到核糖体有时可以简单地忽略这个停止信号,不受titin产生的影响,”研究人员说。“现在的目标是找出这种情况发生的条件,”van Heesch解释道。“这可能取决于基因突变在mRNA上的位置,但也可能是一个因素的结果,一旦确定,将扭转现有的治疗困境。”van Heesch和他的同事们还希望更密切地研究新发现的微结构的作用。“这些蛋白质在进化上似乎相当年轻。例如,我们在老鼠的心脏里找不到它们。”他声称“这些物质提供了进一步的证据,证明人类的心脏有多么特殊。”此外,科学家希望有朝一日能够利用这些蛋白质诊断心脏病,或者作为未来治疗的目标结构,能在治疗心脏能量代谢紊乱方面比以往更有效。
厂商
2019.06.03
我们有可能绊住“失控”的自身性免疫吗?
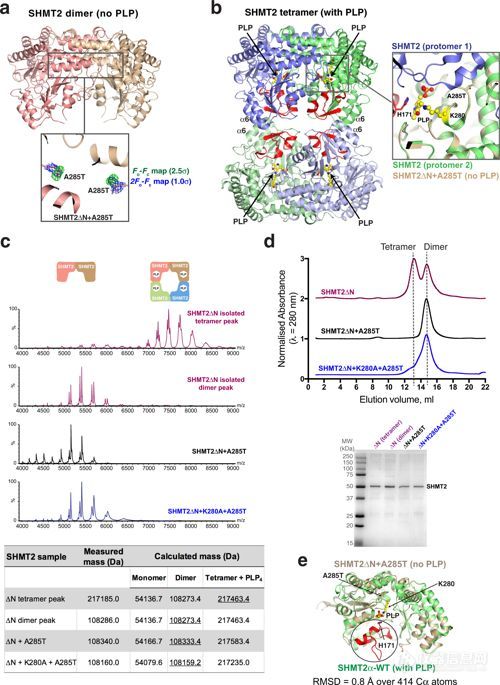
科学家们发现了一种新的,有助于控制人体对抗感染的反应的内部调节器。这一发现可能为治疗自身免疫性疾病(如狼疮和硬皮病)的新药开辟目标。 利兹大学的EltonZeqiraj博士说:“我们想给身体自身的免疫系统施加一个刹车,以阻止它自行启动。”“我们的发现有可能帮助我们找到一种针对这种调节器的新药,抑制免疫系统,在没有感染的情况下阻止机体破坏自身细胞。“我们要找到一种治疗自身免疫性疾病的新方法还有很长的路要走,但是我们很兴奋,因为这一发现可能为一种新药打开大门。”自身免疫性疾病包括许多难以治疗的疾病,如 1型糖尿病和类风湿性关节炎等。科学家们在利兹大学Astbury中心使用强大的低温电子显微镜来揭示这种调节器的结构,它由两种蛋白质组成,分别叫做BRISC和SHMT2,首次了解了它们如何在细胞中协同工作。蛋白质复合物的作用是增加细胞的免疫反应,当它们检测到入侵病原体时,就会发生这种反应。Elton Zeqiraj博士继续说:“显微镜使我们能够非常详细地了解这种蛋白质复合物的结构,通过建立一个精确的3D模型,我们发现它在调节免疫反应中起着完全意想不到的作用。“下一步是找到一种针对这种蛋白质的方法来抑制该过程,防止我们的免疫系统攻击健康的细胞。”结构被发现了,就有可能设计出这种蛋白质的基因工程版本,并绘制出复合物在细胞中的功能。科学家们还意外地发现,BRISC-SHMT2蛋白复合物可以通过维生素B6的活性形式进行调节。尽管实验表明维生素B6被证明对这种调节器的功能很重要,但科学家们警告说,仍需要进一步的研究来充分理解它所起的作用。这项发现已经发表在科学杂志《Nature》上,该团队创造了世界上该蛋白质复合体的一个视觉模型。这项研究是由利兹大学和宾夕法尼亚大学领导的由研究人员和临床医生组成的国际小组完成。共同主要作者,宾夕法尼亚大学的Roger Greenberg博士说:“我们现在对这种蛋白质复合体在原子分辨率下如何起作用了解。它揭示了代谢和免疫反应之间的分子基础交流,同时也指出了防止这种复合物在由过度活跃的炎症信号引起的疾病中发挥作用的新方法。”共同作者,来自利兹大学的Francescodel Galdo博士说:“靶向治疗已经彻底改变了我们控制免疫系统的方式,这一发现让我们对新陈代谢在调节先天免疫中的作用有了重要的认识。”SHMT2蛋白是一个小分子,但有证据表明越来越多的小分子参与细胞代谢和免疫反应,所以研究小组对他们的发现感到非常惊讶。Elton Zeqiraj博士于2010年在加拿大多伦多的Mount Sinai医院开始研究这种蛋白质复合物的结构,然后于2016年搬到利兹,在Astbury结构分子生物学中心工作。Zeqiraj博士说:“利兹的Astbury中心拥有世界上好的结构生物学设施之一,资源和专业知识缺一不可。如果没有大学先进的显微镜,这一突破是不可能实现的,因为显微镜使我们一次了解了这种蛋白质的结构。”科学家和临床医生的国际合作包括来自利兹的联合一作者Miriam Walden博士和来自宾夕法尼亚的Lei Tian博士,以及来自利物浦大学、Wistar研究所(费城)、Ubiq Bio BV(阿姆斯特丹)、华沙生命科学大学和隆德大学的研究人员。这项研究主要由威康信托基金会、皇家学会、国家癌症研究所、狼疮研究联盟、硬皮病和雷诺德英国资助。威康的感染和免疫生物学投资组合经理Sumi Subramaniam说:“这项研究使用技术来揭示两种蛋白质的基本生物学功能,以及它们如何相互作用来控制人体对感染的免疫反应。“破坏这些蛋白质可能是解决自身免疫疾病的一条令人兴奋的新途径。治疗自体免疫攻击健康细胞,我们很少有有效的方法,这些发现可以帮助研究人员找到控制免疫反应的新方法。”硬皮病和雷诺德英国资助公司(Raynaud's UK)的首席执行官Sue Farrington说:“英国数千人患有硬皮病等自身免疫性疾病,这可能导致严重的皮肤问题,从而大大降低生活质量。“我们非常自豪能够为这一重要的科学突破提供资金,我们希望这能为药物发现开辟一条新的途径,以便为自身免疫疾病创造更有效的治疗方法。”
厂商
2019.05.31
KRAS突变虽然被抑制,可细胞还有备胎啊
加州大学旧金山分校的研究人员近日利用CRISPR干扰(CRISPRi)功能基因组学平台系统鉴定了KARS G12C抑制剂与靶点的遗传相互作用,并发现了可增强抑制剂功效的组合疗法,有望防止耐药性的出现。 许多癌症的生长是由KRAS基因的突变引起的。尽管KRAS蛋白被认为是不可成药的,但一些新型的化合物(包括ARS-1620)能够结合并抑制特定KRAS突变体(G12C),在临床试验中表现出希望。加州大学旧金山分校的研究人员近日利用CRISPR干扰(CRISPRi)功能基因组学平台系统鉴定了KARS G12C抑制剂与靶点的遗传相互作用,并发现了可增强抑制剂功效的组合疗法,有望防止耐药性的出现。这项成果本周发表在《Science Signaling》杂志上。靶向KRAS G12C的抑制剂是一种大有潜力的癌症靶向治疗药物。当KRAS蛋白处于非活性状态时,突变蛋白上产生一个浅口袋。抑制剂以此口袋作为结合位点,与突变体半胱氨酸残基发生反应。然而,癌症可不是一般的聪明,在癌症驱动基因受到限制后,它们可能会寻找“备胎”,将之前的非必需基因变成必需基因。研究人员表示:“这些必需基因的丧失增强了细胞对KRAS G12C抑制的敏感性。我们将这些基因称为‘旁系依赖性’(CD),并确定了两类靶向这些CD的组合疗法,它们能够增加KRAS G12C靶点的参与度,或阻断体内残留的存活通路。”在临床前研究中,一种名为ARS-1620的抑制剂对KRAS G12C突变肿瘤表现出特异的抗癌活性,并且在小鼠中没有观察到剂量限制毒性。不过,研究人员表示,依赖KRAS G12C的癌细胞可能会召集之前非必需的基因和通路来维持生存和增殖。他们假设,这种可维持癌细胞存活的旁系信号通路可能与合成致死(SL)依赖性不同,并将其称为旁系依赖性(CD)。利用全基因组的CRISPRi功能基因组筛选平台,他们对含有KRAS G12C突变的肺癌和胰腺癌细胞模型进行分析,确定了癌基因失活后CD影响癌细胞生长的不同机制。“这种方法确定了RAS信号通路已知成分的特殊作用,并突出了参与转录调控的CD以及核心RAS通路以外的其他细胞过程,”作者们写道。“对于KRAS G12C驱动的许多种癌细胞,我们鉴定出的绝大多数CD都不是SL,因此证明CD在生物学上与SL不同。”研究人员随后利用药理学来分析治疗上可靶向的CD,发现一些RAS通路基因的抑制可导致KRAS G12C的抑制。在研究这些药物相互作用的机制时,他们进一步发现这些组合疗法要么与口袋抑制直接配合,增加KRAS G12C靶点的参与,要么独立阻断残留的存活通路。“我们检测的这两类组合疗法最终实现了常见信号节点的深度抑制,强调了致癌RAS信号网络的融合性质,”作者们写道。“我们的研究发现了在急性抑制KRAS G12C后,旁系的促癌信号蛋白通过何种机制维持突变KRAS依赖的癌症表型。”“过去认为单个癌基因的活性可驱动癌症表型,如今这个概念正在被修订,因为靶向疗法未能达到促进持久应答和治疗患者的承诺,”他们总结道。“我们认为CD是基本细胞过程,参与了癌症驱动基因的抑制,并限制了靶向疗法的功效。
厂商
2019.05.31
价值数十亿美元!人工智能已渗透入蛋白质组学
慕尼黑工业大学(TUM)的研究人员利用人工智能,成功地使任何有机体的蛋白质质量分析比以前快多了,而且几乎没有错误。这种新方法将引起蛋白质组学领域的巨大飞跃,因为它既可以应用于基础研究,也可以用于临床研究。任何有机体的基因组都包含了数千种蛋白质的蓝图,这些蛋白质几乎控制着生命的所有功能。蛋白质缺陷会导致严重的疾病,如癌症、糖尿病或痴呆症。因此,蛋白质也是药物最重要的靶点。为了更好地了解生命过程和疾病,开发更合适的治疗方法,有必要同时分析尽可能多的蛋白质。目前,使用质谱法测定生物系统中蛋白质的种类和数量。然而,数据分析环节仍然存在许多错误。TUM的一个研究小组,在生物信息学科学家Mathias Wilhelm和TUM蛋白质组学和生物分析学教授Bernhard Küster领导,下现在已经成功地利用蛋白质组学数据训练神经网络,使人工智能学会更快地识别蛋白质,并且能够识别蛋白质,几乎没有错误。解决一个严峻问题质谱仪不能直接测量蛋白质。它们用其多达多达30个构建基块分析的是由氨基酸序列组成的小部分。再将这些链的测量光谱与数据库进行比较,以便对应特定的蛋白质。然而,评估软件只能使用光谱包含的部分信息。因此,某些蛋白质不能被识别或容易被错误识别。“这是一个严重的问题,”Küster说。TUM团队开发的神经网络利用所有光谱信息进行识别。“我们错过的蛋白质更少,犯的错误也少了100倍。”适用于所有生物研究人员将该人工智能软件命名为“Prosit”,“( Prosit)适用于世界上所有的生物体,即使它们的蛋白质组以前从未被检测过,”Mathias Wilhelm解释说。“这使得以前无法想象的研究成为可能。”在1亿台质谱的帮助下,该算法得到了广泛的训练,无需任何额外的训练即可上手用于所有普通质谱仪,我们的系统是这个领域的全球,”Küster说。价值数十亿美元的市场诊所、生物技术公司、制药公司和研究机构都在使用这种高性能设备,市场价值已经达到数十亿美元。有了“Prosit”,未来还有可能开发出更强大的仪器。研究人员和医生也将更好、更快地在患者的血液或尿液中寻找生物标记物,或监测治疗的有效性。研究人员对基础研究也抱有很高的希望。“这种方法可以用来追踪细胞中新的调控机制。我们希望从中获得大量知识,从中长期来看,这些知识将反映在人类、动物和植物所患疾病的治疗上。”Wilhelm预计“Prosit等人工智能方法将很快改变蛋白质组学领域,因为它们几乎可以用于蛋白质研究的每个领域。
厂商
2019.05.31
Nature子刊:如何更有效地遏制致命的儿童癌症?
恶性横纹肌样肿瘤(Malignant rhabdoid tumor,MRT)是侵袭性和致死性的儿童癌症之一。 虽然在美国算是少见的,每年大约有20到25新病例被诊断出来,但是这种疾病缺乏标准有效的治疗方法,因为患者丢失了一种名为SNF5的抗癌蛋白。一个MRT患儿在确诊后存活一年的可能性很小。范德堡大学的研究人员发现,一种原癌基因编码蛋白MYC往往受到SNF5抑制。SNF5的缺失相当于移除了MYC“刹车”,从而加速了癌症的生长。5月《Nature Communications》杂志报道,阻断MYC在治疗MRT以及其他由SNF5失活引起的癌症方面可能“出乎意料地有效”。“治疗类似MRT这样的癌症的一个困难是,它被肿瘤细胞中一种特定蛋白质损失驱动,”细胞和发育生物学教授William Tansey博士说。“如果MYC是由SNF5受损而激活,意味着它将是这些癌症的一个理想靶标,”他说。本文的共同Tansey在MYC领域是一位国际知名专家。MYC家族有三个蛋白质成员,在美国每年因MYC而死亡的癌症患者高达10万例。MYC蛋白作为转录调节因子发挥作用,控制与细胞生长、增殖、代谢和基因组不稳定相关的数千个基因的表达。Tansey实验室致力于确定MYC工作的基本机制,从而在临床上针对MYC制定新的策略。在MRT细胞中,SNF5抑制MYC对靶基因的识别Tansey首先怀疑在MRT背景下,SNF5是否调节MYC与染色质的相互作用,因为SNF5丢失引起MYC靶基因被反复激活。研究人员采用shRNA介导的MYC基因敲除(慢病毒shRNA结构由赛业设计)MRT细胞,证实MYC对MRT细胞的重要性,从而强化了SNF5与MYC对疾病的关联影响。接下来,再建立一个系统,比较相同环境下,在MRT细胞中重新引入SNF5和抑制MYC的效果。将ChIP与下一代测序(ChIPSeq)结合,跟踪MYC在G401细胞基因组中的分布,对比表达EGFP的对照,研究人员发现了900个MYC结合峰,进而比较OmoMYC或SNF5表达的影响。结果显示,OmoMYC减少了可检测的全基因组MYC结合,更重要的是,SNF5也降低了MYC结合,且SNF5对MYC结合的影响是全基因组性的,结合强度平均约降低了三倍,但MYC稳态水平不受SNF5表达影响,排除了结合减少由MYC蛋白减少的可能性。 利用ATAC-seq、RNA-seq和PRO-Seq,Tansey和他的同事证明,SNF5与MYC的结合调节独立于SNF5在染色质重塑中的作用,而是因为控制了RNA聚合酶在MYC调节基因处的暂停释放。SNF5选择性地抑制MYC与DNA的结合,是其致瘤所必需的。这些发现为MRT肿瘤发生提供了一个新模型,其中SNF5的缺失使MYC去阻遏,因此,将SNF5重新导入MRT细胞可以将MYC从染色质中置换出来,从而抑制原癌基因表达程序。
厂商
2019.05.30
Cancer Cell:一种促进癌转移的调节蛋白
一组研究人员发现癌细胞扩散到机体新部位的时候,必须征服自己面对的环境才能继续生长。这种环境变化越迅速,癌细胞生长就越快。肿瘤周围的细胞和组织被统称为肿瘤微环境,这种环境与癌症的发生、生长和扩张有密切的关系。目前的癌症治疗主要以肿瘤本身为目标,实际上靶标肿瘤微环境也同样重要。癌细胞扩散(又称癌转移)能够侵袭更多的人体组织,最终导致整个机体发生崩溃。在许多癌症中,癌细胞扩散才是最致命的威胁。人们往往可以通过手术、药物、化疗或者放疗成功治疗原发瘤,然而一旦癌症扩散到机体的其他器官就很难再进行遏制。科学家们一直在尝试阻断癌细胞的转移途径,但目前成效并不理想。这项研究显示,扩散到机体新部位的癌细胞需要周围组织的帮助,才能建立起新的肿瘤。一旦这些癌细胞获得了自己所需的环境,就会开始蓬勃生长。研究人员通过小鼠研究向人们展示,容易扩散的癌细胞生产一个被称为THSB2的蛋白。该蛋白可以帮助癌细胞塑造适合肿瘤生长的怡人环境。进一步研究表明,THSB2的这种效果是通过激活成纤维细胞实现的。成纤维细胞在正常情况下建立机体组织,但它们也能为癌症生长提供支持。“如果我们能想办法阻断癌细胞适应新环境的能力,就可以延缓癌症向其他部位转移,”领导这项研究的Dr Ilaria Malanchi说。“细胞生产的THSB2蛋白越多,组织环境就会越快达到癌症发展的最佳条件。我们这项工作只是令人振奋的第一步,现在需要寻找药物阻止癌细胞生产THSB2蛋白,看看能否降低它们的扩散能力。”阻止癌细胞向机体其他部位扩散,是成功治疗癌症的最大挑战之一。癌转移是一个非常复杂的过程,进一步理解癌转移的发生,有助于拯救更多癌症患者的生命。
厂商
2019.05.30
单细胞测序技术揭示干细胞为什么与众不同
昆士兰大学Diamantia研究所的科学家利用基因测序技术揭示了干细胞和其他血管细胞的区别。领导皮肤癌和干细胞研究的Kiarash Khosrotehrani教授说,这些发现提供了干细胞如何表达基因的证据,而这些基因可以使干细胞在血管内被识别出来。 昆士兰大学Diamantia研究所的科学家利用基因测序技术揭示了干细胞和其他血管细胞的区别。领导皮肤癌和干细胞研究的Kiarash Khosrotehrani教授说,这些发现提供了干细胞如何表达基因的证据,而这些基因可以使干细胞在血管内被识别出来。“到目前为止,就我们所知,我们还不能准确地说出干细胞如何与其它细胞不同,”Khosrotehrani教授说。“我们假设干细胞表达的基因可以将它们与血管内的其他细胞区分开。”昆士兰大学高级讲师Jatin Patel博士进行这项研究,观察了大动脉(主动脉)中的每个细胞,并通过测序确定了每个细胞表达的基因。“这使得我们可以在检查每一个细胞时无需考虑误差或者它是否是干细胞,”Patel 博士说。这项研究使用单细胞RNA测序来检测每一个细胞的基因表达,并将正常细胞分组到不同的群体中。昆士兰大学分子生物科学研究所高级研究员Sam Lukowski博士进行了该分析。“我们使用专门的算法将表达相似基因的细胞分组成簇,”Lukowski博士解释说。“我们发现这些干细胞在血管内形成小的群体,这就是你如何将它们与其他细胞区分开来的方法。”了解干细胞的确切情况将有助于研究人员为皮肤癌、心脏病发作和伤口愈合等疾病制定新的治疗方案。“这将影响我们如何治疗由血管功能失调引起的疾病,”Khosrotehrani教授说。“我们知道,如果你能瞄准这些干细胞,那么你就可以减少血管形成,并有可能阻止像皮肤癌转移这样的疾病。”Khosrotehrani教授先前的研究发现,阻止黑色素瘤向身体其他部位扩散可能与切断癌症的血液供应一样简单。“血管是至关重要的,因为没有它们肿瘤就不能生长——它们喂养肿瘤并使肿瘤扩散,”Khosrotehrani教授说。“如果你去除了这些干细胞,那么血管就不会形成,肿瘤也不会生长或扩散到其他地方。”在血管缺失或堵塞的情况下,提供更多的干细胞可能会产生新的血管,并允许心血管疾病(如心脏病发作、中风或腿部缺血)中的氧气供应。Khosrotehrani教授曾假设这种干细胞鉴定方法,并说这些发现为科学争论提供了答案。“我们从事这类研究已经十多年了,我们发现的模型与我们以前的发现完全吻合,”他说,“这些数据的公开提供将使来自世界各地的科学家们有希望结束关于这些干细胞身份和定义的一些争论。”
厂商
2019.05.30
病毒感染导致阿尔兹海默的又一力证
斯德哥尔摩大学和卡罗林斯卡研究所的最新研究表明,病毒与宿主生物液体中的蛋白质相互作用,会在病毒表面形成一层蛋白质。这层蛋白质使病毒更具传染性,并有助于阿尔茨海默病等神经退行性疾病特征性斑块的形成。 斯德哥尔摩大学和卡罗林斯卡研究所的最新研究表明,病毒与宿主生物液体中的蛋白质相互作用,会在病毒表面形成一层蛋白质。这层蛋白质使病毒更具传染性,并有助于阿尔茨海默病等神经退行性疾病特征性斑块的形成。这些病毒是死的还是活的?两者都有。病毒只能在活细胞内繁殖,并利用宿主的细胞机制造福它们。然而,在进入宿主细胞之前,病毒只是纳米大小的颗粒,非常类似于用于诊断和治疗的人造纳米颗粒。斯德哥尔摩大学和卡罗琳斯卡研究所的科学家发现病毒和纳米粒子都具有另一个重要的特性——当它们在找到目标细胞之前遇到宿主的生物液体时,它们都会被一层蛋白质覆盖。表面的这层蛋白质显著影响它们的生物活性。“想象一个网球掉进一碗牛奶和谷类食品中。球立即被混合物中的粘性颗粒覆盖,当你把球从碗里拿出来时,这些物质仍然留在球上。当病毒与含有数千种蛋白质的血液或肺液接触时,也会发生同样的情况。其中许多蛋白质会立即粘附在病毒表面,形成所谓的蛋白冠,”斯德哥尔摩大学和卡罗琳斯卡学院的Kariem Ezzat解释说。KariemEzzat和他的同事研究了呼吸道合胞病毒(RSV)在不同生物液体中的蛋白冠。RSV是一种RNA病毒,经空气飞沫和密切接触传播。多见于新生儿和6 个月以内的婴儿,是全球婴幼儿急性下呼吸道感染最常见的原因,每年导致3400万例病例和196000人死亡。“血液中RSV的蛋白冠特征与肺液中的极为不同。人与其他物种(如恒河猴)之间也存在差异,恒河猴也能感染RSV,”Kariem Ezzat说。“病毒在遗传水平上保持不变。它只是根据环境的不同,在其表面积累不同的蛋白冠,从而获得不同的特征。这使得病毒可以利用细胞外宿主因子来发挥作用,而且我们已经证明许多不同的蛋白冠使RSV更具传染性。”斯德哥尔摩大学和卡罗琳斯卡研究所的研究人员还发现,诸如RSV和单纯疱疹病毒1型(HSV-1)等病毒可以结合一类特殊的蛋白质,称为淀粉样蛋白。淀粉样蛋白聚集成斑块,在阿尔茨海默病中起作用,导致神经细胞死亡。到目前为止,病毒与淀粉样斑块之间的联系机制还很难找到,但Kariem Ezzat和他的同事发现HSV-1能够加速可溶性淀粉样蛋白向线状结构转化,这些线状结构会形成淀粉样斑块。在阿尔茨海默病的动物模型中,他们发现小鼠在大脑感染HSV-1后48小时内患上了阿尔茨海默病。如果没有HSV-1感染,通常需要几个月。“本研究描述的新机制不仅让我们了解决定病毒传染性程度的新因素,而且对设计疫苗的新方法也有影响。此外,描述一种将病毒和淀粉样蛋白致病原因联系起来的物理机制,增加了人们对微生物在阿尔茨海默病等神经变性疾病中作用的研究兴趣,为这些疾病治疗开辟了新的途径。”Kariem Ezzat说。
厂商
2019.05.29
著名免疫学家最新PNAS发文:CAR-T可以用于实体肿瘤
十年前,研究人员宣布开发出了一种称为CAR-T(嵌合抗原受体)的癌症免疫疗法,患者利用自身基因修饰过的T细胞,这些T细胞具有强大的抗肿瘤作用,进行治疗。自此之后,CAR-T成为新型细胞免疫治疗工具的热点关键词,在所谓的“液体癌症”,如白血病和淋巴瘤的治疗中取得了重大成功。但实体瘤被证明对这些方法具有抵抗力,部分原因是工程化的T细胞一旦进入这些肿瘤,就会逐渐失去抗肿瘤能力。免疫学家称这种现象为T细胞“疲惫”或“功能障碍”。La Jolla免疫学研究所(LJI)研究人员Anjana Rao教授过去几年中一直致力于解开这其中的原因,其研究组发表了一系列论文,发现了一种调节基因表达的转录因子:NFAT能打开“下游”基因,削弱T细胞对肿瘤的反应,使T细胞衰竭。Anjana Rao教授作为美国科学院院士,在免疫研究领域功成名就,并且在表观遗传领域也取得了许多傲人的成绩。近期其研究组又报道了一组这些下游基因编码的转录因子——NR4A,Rao实验室之前的研究生Joyce Chen发现,肿瘤浸润的CAR-T细胞中NR4A蛋白被剔除,能改善肿瘤排斥。然而,在该途径中与NFAT和NR4A合作的其他参与者的身份仍然未知。最新一项研究中,Rao教授与Patrick Hogan博士完善了这一参与者列表,提出了一个更完整的分子机制。这个网络建立并维持T细胞衰竭。研究人员采用小鼠模型,指出遗传上剔除两个新因子:TOX和TOX2,可以改善了CAR-T模型中针对黑色素瘤的根除。这项工作表明,针对患者的NR4A和TOX因子的干预,可以将基于CAR-T的免疫疗法的应用范围扩展到实体瘤。这一研究小组首先比较了正常与“疲惫”T细胞样本中的基因表达谱,寻找与NR4A平行上调的因子作为T细胞出现功能障碍的共同作用因子。“我们发现两种称为TOX和TOX2的DNA结合蛋白与NR4A转录因子都会高表达,”文章一作,Rao实验室博士后研究员Hyungseok Seo博士说,“这一发现表明,类似NFAT或NR4A这样的因子可能调控着TOX的表达。”之后,研究人员在小鼠中重新尝试CAR-T方案,首先用黑素瘤肿瘤细胞接种动物,构建肿瘤小鼠模型,一周后给小鼠注射T细胞:一种来自正常小鼠的“对照”样品,一种来自经基因工程改造,缺乏T细胞中的TOX和TOX2表达的小鼠。结果发现,注入TOX缺陷的CAR-T细胞的小鼠出现了比注入正常细胞的小鼠更强烈的黑素瘤肿瘤消退。此外,用TOX缺陷的CAR-T细胞处理的小鼠表现出显著增加的存活率,表明TOX因子的缺失能对抗T细胞耗竭,而且允许T细胞更有效地破坏肿瘤细胞。研究人员进一步分析,表明TOX因子与NFAT和NR4A联合起来能促进PD-1抑制性受体的表达,PD-1可以修复耗竭T细胞表面,发送免疫抑制信号。PD-1可以通过检查点抑制剂这种单克隆抗体阻断,这些抗体可抵抗免疫抑制,激活先天性抗癌免疫反应。 PD-1与TOX,NFAT和NR4A的合作令免疫抗癌更有意义,而且可以结合细胞免疫疗法和抗体免疫疗法。“目前,CAR-T细胞疗法对患有白血病和淋巴瘤等液体肿瘤的患者表现出惊人的效果,”Seo说,“但是由于T细胞耗竭,它们仍然不能用于实体瘤患者。如果我们通过用小分子治疗CAR-T细胞来抑制TOX或NR4A,这种策略可能对黑色素瘤等实体癌症有很强的治疗作用。”
厂商
2019.05.29
上海科大,华中科大Nature Neuroscience解码捕食与进食的神经机制
研究人员揭示了大脑未定带(Zona Incerta,ZI)神经元在捕食与进食之中所起的关键作用。 进食与捕食行为是生物进化的主要驱动力之一,一直是神经科学研究的热门话题。这些行为与感觉特征提取、奖赏和动机息息相关。解码这些行为不仅是理解神经系统如何调控行为的重要窗口,也为理解临床肥胖症和厌食症的发生提供契机。两个研究团队利用光遗传学、在体电生理记录和钙信号光纤光度法等神经环路手段,发现ZI神经元介导了猎物的“感觉特征”提取、捕食的动机、捕食与进食的相互关联等内容。2019年5月24日,上海科技大学生命学院沈伟研究组与华中科技大学李浩洪研究组合作,在Nature Neuroscience杂志上长文发表了题为Zona incerta GABAergic neurons integrate prey-related sensory signals and induce an appetitive drive to promote hunting的文章,揭示了大脑未定带(Zona Incerta,ZI)神经元在捕食与进食之中所起的关键作用。ZI是大脑中的功能“未定”的区域,位于大脑神经轴中央位置,与多个脑区有丰富的神经连接,然而其功能仍然不够清晰(Mitrofanis J. Neuroscience, 2005.)。沈与李的团队发现ZI不仅对于小鼠提取猎物特征信息很关键,还编码奖赏性动机,促进捕食行为;另外ZI还促进奖赏性进食,且通过不同的下游环路来调控进食和捕食行为。同时,研究团队发现,光遗传学激活ZI的GABA(gamma-aminobutyric acid)γ-氨基丁酸神经元会引起小鼠的暴食性行为和啃咬食盘与垫料,说明这些神经元除了参与进食外,还可能参与捕食行为。实验过程还引入小鼠的天然猎物——蟋蟀,发现光遗传学激活的确能够大幅提高小鼠的捕食速度和成功率。那么猎物是如何被“特征”识别和诱发捕食行为的呢?两个研究团队通过多通道电生理记录发现食物、猎物与普通小物体激活不同的ZI神经元群。研究人员通过细致分析不同的感觉刺激发现,猎物相关的躯体感觉(猎物与小鼠胡须接触)、运动视觉刺激,以及声音刺激,都可以激活ZI神经元。令人意想不到的是,这些被激活的神经元相互重叠;换句话说,这些感觉刺激被ZI所“整合”了!研究人员通过对行为学和生理钙信号的分析发现,ZI的确利用这些信号来提高捕食效率。ZI是否介导了捕食与进食的奖赏与动机呢?通过实时位置偏好实验(RTPP),研究人员发现小鼠特别喜欢ZI被光激活侧,提示光刺激可能诱发奖赏。另外,在经典的鼻触测试中,为获得光刺激奖赏,小鼠表现出不断的和重复性的鼻触,提示光刺激诱发了强烈的正向动机。研究人员通过神经环路研究发现ZI投射至导水管周围灰质(PAG)脑区,引发捕食和奖赏;ZI投射至丘脑室旁核(PVT),引发进食与奖赏(图2,Zhang X, van den Pol A N. Science, 2017.)。综上,SC-ZI的神经环路负责提取猎物的特征信息,并促进捕食行为;ZI-PAG的神经环路负责编码奖赏性动机,促进捕食行为;ZI-PVT介导奖赏性进食行为。这些发现有助于理解动物对特征提取和动机编码的关键神经机制,或可解释临床上刺激ZI附近所诱发的暴食性行为和奖赏性动机改变,并为肥胖和厌食症的控制提供新的切入点。沈伟教授长期从事中枢对能量稳态调节机制的研究,先后作为通讯或共同通讯作者,在PNAS(2017)、Cell Research(2018)等期刊上阐明下丘脑对产热与体温调节、以及摄食调节的神经机制。在本论文中,赵政东(上科大生命学院和免疫化学研究所联合博士后)、陈宗明(上科大生命学院,2015级硕博连读生)、向心宽(华中科大)、胡孟娜(上科大生命学院,2015级硕博连读生)为共同作者;生命学院沈伟教授和华中科技大学李浩洪教授为本文的共同通讯作者;上科大生命学院已毕业本科生贾晓宁(2014级)、钱乐琛(2014级),和2016级在读本科生杨以清参与了这项工作。该研究工作得到了国家自然科学基金委员会“重大研究计划”代谢专项培育项目、面上项目,以及上海科技大学启动经费等的经费支持。上科大生命学院分子影像平台和分子细胞平台、国家蛋白质科学研究(上海)设施给予了平台支持。
厂商
2019.05.29
肠道如何在保证防御的同时最大化吸收营养
这项发表在《Nature》杂志上的研究结果提供了有关肠道如何最大限度地吸收营养物质,同时保护身体避免具有潜在危险的微生物入侵的新见解,这两种功能似乎相互矛盾。食物进入肠道,便开始了一段漫长旅程。对于大多数路径来说,周围环境似乎变化不大。但是,来自洛克菲勒大学的Daniel Mucida的最新研究表明,这些食品加工管道实际上由很多隔间组成,隔间可以调节免疫系统对通过的食品的反应——在吸收营养的第一程,攻击性防御力较低,而在最后一程,强火力集中消灭病原体。这项发表在《Nature》杂志上的研究结果提供了有关肠道如何最大限度地吸收营养物质,同时保护身体避免具有潜在危险的微生物入侵的新见解,这两种功能似乎相互矛盾。这项研究还有潜力改善胃肠道疾病药物,并为口服疫苗的开发提供信息。Mucida说:“乍一看,整个肠道看起来都很均匀。但我们发现,一个复杂的功能系统潜伏在表面之下,它由多个部分组成,允许不同的免疫系统在不同的位置发挥不同的功能。”肠道分水岭Mucida和他的同事通过检查肠道结构(肠道引流淋巴结)发现了小鼠的一个功能性分割,该结构协调了免疫反应。研究人员发现,肠道不同部位的节点有不同的细胞组成,当他们用沙门氏菌之类的病原体攻击小鼠时,他们看到了不同的免疫反应。Mucida说,将免疫反应按位置分开可能会增加免疫系统对通过的东西做出适当反应的机会。一旦大多数营养物质被吸收完毕,该系统就可以更积极地集中在消除病原体上,而不会干扰能量储藏。分段集中治疗根据Mucida的说法,肠道段与段之间的免疫差异可用于多种治疗目的。例如,通过将免疫抑制药物靶向对其影响最大的部分,可能可以抑制其副作用。此外,如果考虑到肠段之间的差异,更精确地切除部分肠的手术结果可能会有所改善。肠道免疫反应地图也可用于制造更好的口服疫苗。到目前为止,科学家们设计的口服疫苗都难以产生强大的免疫反应(除非免疫系统对疫苗产生足够强的反应,否则机体无法获得所需的病原体分子“记忆”,这阻碍了这些疫苗的研制)。据Mucida说,肠道开始时的弱免疫反应可能是口服疫苗不如注射疫苗有效的原因之一。他说:“理论上,瞄准肠道远端可以更有效地诱导所需的免疫反应。如果我们利用了正确的肠道区域,也许能看到一些以前失败的疫苗起作用。”
厂商
2019.05.28
Nature子刊:为何有些人更容易因为病毒感染而生病
人们一直认为,干扰素就是机体受到感染时做出的最早应答。发烧、肌肉酸疼等感冒症状,是免疫系统与病毒和细菌作战的典型特征。出现这些令人不快的身体表现,是因为机体生成了一种被称为干扰素的物质,这种物质能对入侵者展开攻击。但一项研究指出,机体其实有一个更早发生的防御机制。机体通过一个此前未知的机制对抗病毒和细菌,这才是免疫系统最早的防御应答。正因为这种防御的存在,我们在病毒包围之下才并没有一直生病。在病毒和细菌尝试建立感染的时候,机体粘膜会受到破坏,进而激活一种免疫反应。免疫系统识别病毒之后,生产中和这些不速之客的物质。这一过程在机体内持续发生,只是我们根本没有意识到。如果这种免疫反应不足以抑制病毒,感染在机体内建立起来,涉及干扰素的第二免疫反应就会触发。干扰素可以帮助机体对抗病毒,但这也意味着我们已经生病了。“这项研究从根本上改变了我们对机体一线免疫的理解。我们一直被病毒和细菌包围着,但整个免疫系统并没有持续激活,否则类似感冒的症状会更加频繁,”Aarhus大学的Soren Riis Paludan教授说。进一步研究表明,缺乏第一免疫反应的小鼠接触到疱疹病毒就会生病,而正常小鼠在这种情况下还能保持健康。“这些发现可以帮助我们理解,为何有些人更容易因为病毒感染而生病。这样的机制应该适用于那些对粘膜起作用的病毒,比如HIV和疱疹。我们正在分析与此有关的具体分子,这将帮助我们鉴定那些有缺陷的人,也有助于开发新型的疾病疗法。这一机制可能对非病毒疾病也很有意义,是很有潜力的研究方向,”Soren Riis Paludan说。
厂商
2019.05.28
Science新论文解释细菌如何完成耐药性这一壮举
一项新的研究显示,大多数细菌中发现的膜泵(membrane pump)有助于大肠杆菌从邻近细胞中获得耐药性,即使它们接触抗生素也是如此。一组法国研究人员发现,大肠杆菌即使在削弱细胞生长的抗生素存在下,也能够合成耐药性蛋白质。他们还发现了细菌是如何完成这一壮举的:一个保存完好的膜泵(membrane pump)将抗生素从细胞中运出,只要有足够长的时间就可以让细胞有时间接收来自相邻细胞的DNA,这些细胞可以编码一种耐药蛋白。这一研究成果公布在Science杂志上。新墨西哥大学的微生物学家Manuel Varela(未参与这项研究)表示,“这是一个重要的发现,这一发现将有助于解释细菌在遇到抗生素时如何设法传播抗素耐药性。”最初,里昂大学的细菌遗传学家,文章的通讯作者Christian Lesterlin等人是想要开发一个实时显微镜系统,希望能详细观察质粒转移(细菌细胞彼此共享DNA的过程),他们利用精心设计的荧光蛋白,跟踪质粒,将DNA从供体细胞穿梭到受体微生物,以及一旦它们在新宿主体内翻译后产生的蛋白质。研究人员利用大肠杆菌常见共享抗生素抗性基因作为案例研究,仔细观察细菌如何通过DNA编码TetA蛋白,这是一种通过将四环素分流出去,使细胞对四环素产生抗性的泵。不久之后,他们发现质粒DNA到达非抗性细胞一段时间后,受体细胞膜上出现了红色荧光,表明TetA蛋白被翻译,细胞对四环素产生了耐药性。抗生素通常用于家畜,但有时也用于治疗肺炎,呼吸道感染和其他疾病,可以关闭未携带TetA的细菌的生长,但许多细菌菌株会通过共享机制变得耐药。这个初始实验不存在四环素,因此,为了了解这一过程如何受到药物本身的影响,研究人员让细胞接触高浓度的四环素,并再次将它们置于显微镜下。正如所料,他们观察到质粒DNA到达新的非抗性细胞。这是预料之中的,因为四环素不会阻碍这一过程。相反,它旨在阻止蛋白质生产。令人惊讶的是,研究人员发现一些新的受体细胞中出现红色荧光,这些细胞以前没有TetA蛋白质:显然,尽管接触了四环素,它们仍然能够合成蛋白质,包括TetA。Lesterlin说:“我们花了很长时间才确认这个结果,这违反直觉,我们很难确信它确实发生了。”研究人员发现,当功能正常时,AcrAB-TolC泵可以通过保持抗生素浓度足够低,使细胞合成质粒DNA中编码的抗性蛋白来补充细菌时间。在这种情况下,它允许产生TetA蛋白,然后将更多的四环素分流出细胞。最终,细菌可以在抗生素的影响下变得耐药这一发现具有广泛的相关性,因为AcrAB-TolC在细菌中的保守性非常广泛,并且因为其机制不仅限于四环素。Lesterlin和他的同事证明,该泵还允许细菌在其他抗生素存在的情况下产生抗药性蛋白,这些抗生素旨在抑制基因表达,例如抑制翻译的氯霉素和抑制转录的利福平。Lesterlin补充说,这种机制与所谓的抑菌抗生素有关,它不会杀死但只能抑制细菌的生长。这些结果表明,细菌的AcrAB-TolC多药外排泵能减轻四环素的表达阻断作用,并同时令抗生素耐药性得到确立。
厂商
2019.05.28
J Thorac Oncol:饮酒和遗传交互作用增高食管鳞癌患病风险
这项研究首次将酒精代谢相关基因功能信息融入分析,是探索基因–饮酒交互作用对中国人群食管鳞癌发病风险影响的大型研究之一。 食管癌是全球范围内常见的消化系统恶性肿瘤,也是我国最为高发的恶性肿瘤之一。食管癌发病率、死亡率高,危害严重,在不少地区仍是威胁居民健康最严重的恶性肿瘤,造成了极为沉重的疾病负担。食管癌发病具有明显的地理差异和人种差异,西方国家人群以腺癌为主,而亚洲人群尤其是中国人群以鳞状上皮癌为主,占90%以上。食管鳞癌(Esophageal Squamous Cell Carcinoma,ESCC)的发病原因有很多,目前公认饮酒、吸烟对食管造成损伤的各类慢性刺激、环境因素及某些遗传因素是中国食管鳞癌发病的主要原因,因此全面具体地了解食管癌的危险因素对于其防治十分重要。复旦大学生科院青年研究员陈兴栋和遗传工程国家重点实验室索晨博士(现任公共卫生学院青年副研究员)等学者联合攻关,揭示了饮酒和酒精代谢相关遗传因素的交互作用能显著增加食管鳞癌的发病风险,强调了过量饮酒的危害性,特别是在体内缺乏乙醛脱氢酶的人群中,此风险更强。此重要研究成果于2019年4月正式发表在肿瘤学国际知名学术期刊《Journal of Thoracic Oncology》上,影响因子10.34。既往研究报道饮酒和遗传变异是食管鳞癌(esophageal squamous cell carcinoma,ESCC)的主要影响因素。然而,酒精与酒精代谢通路相关的遗传因素之间复杂的交互作用在增加ESCC发病风险方面尚未明确。这项研究在ESCC发病率较高的江苏泰州开展了一项以人群为基础的例对照研究,共纳入1190个例和1883个对照。该研究整合了单核苷酸多态性数据,详细的饮酒史,以及酒精代谢相关基因的生物学功能信息,阐述饮酒、酒精代谢酶基因变异和ESCC风险之间的复杂关系。据报道,ADH1B不同基因型(rs1042026)可影响ADH1B的活性,从而影响体内乙醛浓度。根据该位点的基因型分布,研究认为大多数中国人体内代谢酒精时,从乙醇氧化为乙醇速率过快,可导致乙醇堆积;这其中,1/4的人又同时携带ALDH2基因rs671AG基因型,导致乙醛脱氢酶活性较低,体内乙醛浓度升高。携带不同ALDH2和ADH1B基因型的健康个体也表现出多样化的饮酒行为:在携带不同基因型组合的个体中,饮酒者的比例可从23.7%变化至54.3%。研究证实了两个ESCC易感位点,乙醛脱氢酶家族成员基因(ALDH2)上的rs671和乙醇脱氢酶1B基因(ADH1B)中的rs1042026,与饮酒行为高度相关并修饰了饮酒和ESCC高风险之间的关联。该研究进一步评估了ADH1B和ALDH2变异与饮酒量对ESCC发病风险升高的交互作用。结果表明,在乙醇被迅速氧化的个体中,饮酒与乙醛氧化率有很强的相加交互作用和相乘交互作用。提示相关部门需加大力度,防止过度饮酒,特别是在携带ADH1B基因rs1042026AG/GG基因型和ALDH2基因rs1671AG基因型的个体中。这项研究首次将酒精代谢相关基因功能信息融入分析,探索基因 –饮酒交互作用对中国人群食管鳞癌发病风险影响的大型研究之一,是多团队多学科合作努力的结果。陈兴栋青年研究员为本文的通讯作者,并列第一作者是遗传工程国家重点实验室索晨、杨亚军和泰州健康科学研究院袁子宇。该论文得到了金力院士、卡罗林斯卡学院叶为民教授,复旦公共卫生学院张铁军副教授的支持,尤其是山东大学吕明教授的悉心指导,同时离不开复旦大学泰州健康科学研究院在数据收集和样品制备方面付出的努力,以及泰兴人民医院和泰兴市疾病预防控制中心的积极协助。
厂商
2019.05.27
Nature子刊:不仅癌症有性别差异,肿瘤扩散也有性别差异
历史上的解释——男性更可能吸烟和在工作环境中接触危险化学品——已被证明是不充分的,因为即使是吸烟率下降和职业模式发生了改变,男性发展多种癌症的概率仍然超过女性,包括一些与烟草使用相关的癌症,如肾癌、膀胱癌、口腔癌。不少科学家都认同癌症有性别差异,而来自Broad研究所、哈佛医学院等处的一项研究表明,不仅癌症有性别差异,而且肿瘤扩散也有性别差异。这一研究发现公布在Nature Genetics杂志上。研究人员发现女性在其细胞中携带某些保护性基因的一个额外副本——一抗击正在失控生长的癌细胞的另一道防线,这些副本虽然不是癌症对男性“偏爱”的全部原因,但是它们可能解释了一些失衡,包括某些类型的肿瘤有高达百分之80的男性患者。哈佛医学院Andrew Lane博士说:“在几乎每一种癌症中,男性的发生率都比女性高。在某些情况下,差异可能很小,只有几个百分点,但在某些癌症中,男性发病率比女性高出两倍或三倍。来自美国国家癌症研究所的数据显示,男性比女性患癌风险高出百分之20。这转化为每年新增的150000例男性癌症病例。”他与Broad研究所、麻省总医院的Gad Getz是本文共同通讯作者。尽管这个差距很大,但是这种分歧的原因一直都很难确定。Lane说,历史上的解释——男性更可能吸烟和在工作环境中接触危险化学品——已被证明是不充分的,因为即使是吸烟率下降和职业模式发生了改变,男性发展多种癌症的概率仍然超过女性,包括一些与烟草使用相关的癌症,如肾癌、膀胱癌、口腔癌。以前的研究发现,在白血病的一种形式中,癌细胞通常在一个称为KDM6A的基因中携带突变,该基因位于X染色体上——一条性染色体,决定一个人是男性还是女性。(女性细胞携带两条X染色体;男性细胞携带一条X染色体和一条更短更小的Y染色体)。如果KDM6A是一种抑癌基因——负责阻止细胞失控分裂,那么该突变就可能通过削弱这个约束系统而导致癌症。人们可能会认为,女性细胞一样易受到该突变的攻击。在胚胎形成过程中,女性细胞中的一条X染色体关闭,并终生保持关闭。因此,在活跃的那条X染色体上的一个KDM6A突变,将导致跟男性中一样混乱的细胞分裂。出乎意料的是,KDM6A突变更经常地是在男性癌症中被检测到。事实证明,在女性细胞中,失活的那条X染色体上的一些基因可“规避”这种休眠状态,并正常发挥功能。其中一个觉醒的基因恰好是KDM6A的一个工作副本。该基因的“好”副本足以防止细胞发生癌变。这项研究探讨了“在一条闲置的X染色体上存在功能完善的肿瘤抑制基因,这一现象是否是癌症偏爱男性细胞的原因?”。研究人员称这种基因为“EXITS”(Escape from X-Inactivation Tumor Suppressors)。Lane说:“根据这一理论,癌症在男性中更常见的一个原因是,男性细胞只需要一个EXITS基因一个副本中的一个有害突变,就能致癌。相比之下,女性细胞需要两个副本都突变才能致癌。”为了验证这一假设,Broad研究所的研究人员扫描了4000多份肿瘤样本的基因组,它们代表了21种不同类型的癌症,以寻找各种类型的异常,包括突变。然后,他们检测所发现的任何异常,是在男性细胞中更常见?还是在女性细胞中更常见?结果是惊人的。所发现的近800个基因只存在于X染色体上,六个基因频繁地在男性中发生突变并丧失功能。在其他18000多个基因中,没有一个基因表现出突变率的性别失衡。在6个更可能是在男性中发生突变的基因当中,有5个基因已知规避了X染色体失活,从而使它们成为EXITS基因的有力候选基因。Lane指出:“在男性中更经常突变的那些基因,被发现仅存在于X染色体上,它们中的一些已知是肿瘤抑制基因,并逃避了X失活,这个事实是我们这个理论的令人信服的证据。在女性细胞中这些基因的工作副本所提供的保护,可能有助于解释为什么许多癌症在女性当中的发病率较低。”这些结果的一个意义在于,在男性和女性中,许多癌症可能通过不同的分子途径而出现。为了规避女性细胞中对抗癌症的其他遗传预防措施,女性肿瘤可能会采用不同于男性的遗传回路。
厂商
2019.05.27
Neuron:干细胞发育路线图
视网膜是一种已充分研究的结构,其包含多种存在于神经系统的其他部分的细胞类型,因此可以作为一个极好的范例用于研究中枢神经系统发育。 约翰霍普金斯医疗集团的研究人员报告称,他们已开发出一种通过追踪细胞内表达的基因来描绘中枢神经系统发育的方法。这项技术在本研究的小鼠视网膜中得到证实,其跟踪了个体细胞在发育过程中使用的基因的活性,使研究人员能够以前所未有的详细方式来识别模式。研究人员表示,这种精确的路线图可用于在未来开发治疗致盲性疾病和其他神经系统疾病的再生疗法。“这无疑是我们在中枢神经系统细胞发育方面最全面的路线图”,约翰霍普金斯大学医学院神经科学教授兼细胞工程研究所成员Seth Blackshaw博士说道。“如果我们能够利用这种路线图来让干细胞制造某种类型的视网膜细胞,我们有朝一日便可以替换因黄斑变性和其他致盲性疾病而丧失的细胞”,Genevieve Stein-O Brien博士说道,其在约翰霍普金斯大学医学院的Elana Fertig博士实验室担任博士后研究员,Elana Fertig博士为约翰霍普金斯大学医学院肿瘤学副教授兼约翰?霍普金斯金梅尔癌症中心成员。该研究的描述于5月22日发布在《神经元》(Neuron)杂志的网络版。Blackshaw表示,视网膜是一种已充分研究的结构,其包含多种存在于神经系统的其他部分的细胞类型,因此可以作为一个极好的范例用于研究中枢神经系统发育。构成视网膜的各种细胞类型都是由神经祖细胞产生,神经祖细胞为干细胞样细胞,具有发育成几乎任何视网膜细胞类型的能力,这取决于在发育期间开启和关闭的基因。创造每种细胞类型所需的基因模式沿着严格的时间线出现。神经元如视网膜中的吸光视杆细胞和视锥细胞一样由较年轻的祖细胞产生,而支持性神经胶质细胞由较老的祖细胞产生。为了详细研究这一过程并构建路线图,研究人员首先对不同发育时间点的个体小鼠视网膜细胞的DNA进行了测序 - 从第一代祖细胞到成年视网膜细胞。研究人员随后将这些信息输入由Stein-O Brien开发的机器学习计算机程序中,该程序旨在快速压缩大量的遗传数据,将相似的细胞分组在一起,生成一张路线图,让研究人员能够可视化发育过程。该计算机程序产生一个分支结构,让研究人员了解哪些细胞类型会产生其他细胞、哪些最密切相关以及发生什么样的遗传变化导致小鼠和人类视网膜中发现超过100种细胞类型。“该路线图为我们提供了一种方式,让我们可以了解个体基因和基因网络对发育中的中枢神经系统的影响”,Blackshaw说道。在一项原理验证实验中,研究人员接下来选择仔细研究三种基因,即核因子1(NFI)a、b和x,这些基因已知对于帮助祖细胞确定其年龄以及可以产生的视网膜细胞类型必不可少。研究人员对小鼠进行了基因工程改造,使它们大量表达这三种基因或者完全不表达,并通过跟踪在计算机程序中的任何给定时间“开启”何种基因来观察它们的视网膜细胞生命周期如何改变。研究人员发现,NFI基因表达水平升高的细胞表现得比实际年龄更老,并且比正常眼睛视网膜祖细胞产生更多相应的细胞类型(神经胶质细胞)。相比之下,没有NFI基因的祖细胞继续产生早期的细胞类型(如视杆细胞),并像年轻的祖细胞一样继续进行分裂。研究人员表示,他们最终希望将描绘技术应用于其他细胞类型,以更好地了解哪些基因影响身体其他组织中的疾病发展。“如果我们确切地知道祖细胞是如何从未定型干细胞群发育成成熟组织,我们就可以使用这个路线图将它们重定向,以沿特定的其他路径发育”,约翰霍普金斯大学医学院神经科学助理教授兼McKusick-Nathans遗传医学研究所成员Loyal Goff博士说道。
厂商
2019.05.27
大连医科大学最新文章:慢性压力促进癌症发展
大连医科大学肿瘤干细胞研究院刘强教授课题组取得重要研究进展,发现慢性压力能够促进肾上腺素水平异常升高,通过改变乳腺癌的糖酵解水平引起肿瘤微环境的酸性增强从而促进乳腺癌肿瘤干细胞的干性特征,揭示乳腺癌发生发展的新机制。这一研究发现公布在国际医学领域权威期刊《Journal of Clinical Investigation》(《临床调查》),大连医科大学为第一完成单位,刘强教授作为唯一通讯作者,实验师崔柏、硕士研究生罗圆媛、讲师彭飞等为共同第一作者。癌症现已成为严重威胁人类生命健康的疾病之一,而癌症患者通常伴有焦虑、绝望、恐惧等不良情绪,这往往加速病人病程的进展,影响患者的预后。但是,由不良情绪导致的慢性精神压力的致癌作用和具体机制尚不清楚。在这篇文章中,研究人员发现慢性压力能够促进肾上腺素水平异常升高,通过改变乳腺癌的糖酵解水平引起肿瘤微环境的酸性增强从而促进乳腺癌肿瘤干细胞的干性特征,揭示乳腺癌发生发展的新机制。另外,为了进一步找到有效的治疗药物,刘强教授课题组利用美国FDA批准药物的筛选系统,筛选出靶向LDHA的潜在治疗药物维生素C(Vitamin C),通过一系列实验发现,Vitamin C能够显著逆转肾上腺素对乳腺癌的致癌作用,为今后肿瘤患者的临床治疗提供了崭新的思路。刘强教授课题组长期从事肿瘤干细胞的动态调控以及社会心理行为影响肿瘤发生发展的机制研究,该研究由国家自然科学基金重点项目、大连市高层次人才创新支持计划等项目共同资助。
厂商
2019.05.24
《Neuron》健康的大脑发育是一项人权
我们知道儿童和青年人的成长环境影响着大脑发育健康。现在,耶鲁大学的一位心理学家正致力于反对她后院一个特别恶劣的环境——美国监狱系统。 在5月22日发表在《Neuron》杂志上的一篇论文中,作者宣称,每个人,包括年轻的罪犯,都应该得到健康的大脑发育——她说,美国监狱经常侵犯这一权利。耶鲁大学的心理学教授、跨部门神经科学项目和司法合作者B.J. Casey说:“健康的心理大脑发展不是精英们的特权,而是所有人的权利。”她认为,美国的法律制度经常侵犯这项权利,因为美国监禁的青少年比其他任何国家都多,但却没有为他们提供使他们具备成为一个在社会中发挥良好作用的人所必需技能的机会。为此,对最终进入法律体系的年轻人需要更多的保护,以确保他们能够有健康的心理发育。具体来说,Casey认为保释改革是必要的。事实上,在纽约臭名昭著的严苛惩教所Rikers,80%的被拘留者没有被定罪,他们中的许多人仅仅因为无力保释而被拘留。在押人员中,近15%是青少年。Casey认为,“首先需要实施改革,以防止许许多多无辜孩子入狱。”此外,她建议改革少年犯转移系统。她指出,许多美国州没有向成人法院移交的最低年龄。最后,关闭严格纪律的设施和缺乏康复部分也至关重要。Casey说,司法系统的这些重大失败造成了Kalief Browder的例子。Kalief Browder是一名16岁的少年,他从未被定罪,但因家人无法保释而被关押在Rikers三年,其中两年被单独监禁。两年后,Browder自杀了。Casey说:“通常,当我们想到年轻的罪犯时,我们想到的仅仅是青少年,但研究表明,大脑功能的显著变化一直延伸到20岁出头,司法政策定制与实际情况并不相符。”她报告说,政策制定者开始认识到“年轻人阶段”与其他年龄阶段的显著不同,全国各都需要年轻年成人法院(young adult courts),以及更多康复而非严格惩罚性措施的试点项目,试点已经显现出了缓慢的转变,但她说,还需要更多的工作。“大象席地而坐,”她说:“当我们谈到与法律接触的年轻人或被移交到成人法庭的年轻人时,我们知道他们中有不成比例的人是有色人种的年轻人。”Casey指出,她未来的研究将涉及与有色人种人接触会如何影响行为和感知。“作为发育科学家,我们需要继续进行客观、实证的研究,以负责任地为政策提供信息。我觉得必须努力回答这些难题,”她说。
厂商
2019.05.24
麻省总医院研究发现:患肠癌的风险与每天久坐成正相关
久坐不动的生活方式是患结直肠癌的一个新兴危险因素。而患肠癌风险较低的人群每天会进行更多低强度运动,如站立或行走。这些发现也进一步证明了保持积极生活方式的重要性。 结直肠癌是世界第三高发恶性肿瘤,近十年来在我国发病率要逐年上升。有数据显示,我国结直肠癌发病率、死亡率在全部恶性肿瘤中均位居第5位。而到2030年,全球结直肠癌病例数预计将增加60%,每年将有超过220万新发病例且每年约110万患者会因该病死亡。 因此,预防、早诊早治结直肠癌显得刻不容缓。过去,结直肠癌患者主要是50岁以上的人群,但近年来患者呈年轻化趋势,研究人员对影响年轻患者发病的因素尚不清楚。近期,一项由美国麻省总医院和哈佛医学院Long Nguyen博士领导的研究揭示,每天看电视超过两个小时的人,患直肠癌的风险会增加约70%。这项研究结果首次将久坐行为列为50岁以下肠癌患者数量急剧上升的诱因之一。 该研究对89278名年龄25至42岁的美国女性护士进行追踪调查。在二十年的随访中,共有118例研究对象被确诊为结直肠癌(包括结肠癌和直肠癌)。与看电视较少的人相比,每天看电视超过一小时会使患病风险增加12%,超过两个小时,则患病风险会增加约70%。该研究结果与体质指数(BMI)和运动水平无关,这表明久坐可能是导致早发性结肠癌的唯一风险因素。但目前尚无证据显示用餐或办公室工作等其它室内活动会增加结直肠癌的患病风险。 久坐不动的生活方式是患结直肠癌的一个新兴危险因素。而患肠癌风险较低的人群每天会进行更多低强度运动,如站立或行走。这些发现也进一步证明了保持积极生活方式的重要性。 这项研究也可以帮助识别潜在的高风险患病人群,并帮助他们尽早筛查, 从而获益更多。结直肠癌若能早期发现,及时治疗,患者5年生存率可达80%以上,可基本实现治愈。 关于麻省总医院麻省总医院成立于1811年,是哈佛医学院最初设立的且规模最大的教学医院。麻省总医院研究所是全美最大的以医院为基础的研究机构,下设艾滋病毒/艾滋病、心血管研究、癌症、计算及整合生物学、皮肤生物学、基因组医学、医学成像、神经退行性疾病、再生医学,生殖生物学、系统生物学、光学医学和移植生物学等主要研究中心。据2015年自然指数(Nature Index)发布的数据,麻省总医院是在顶尖科学期刊上发表论文最多的医疗机构。2018年8月,麻省总医院再次荣登美国新闻与世界报道“美国最佳医院”排行榜中的荣誉榜(全美共20家医院进入荣誉榜)。
厂商
2019.05.24