【飞诺美色谱】ADC药物的DAR值分析——反相色谱法
概述
小分子毒素抗体比DAR(drug-to-antibody ratio) 是ADC药物独特的重要质量属性,它代表抗体偶联小分 子毒性药物的平均数量。
DAR值分析常见的模式为HIC,该模式下根据分子 疏水性逐渐增加的顺序洗脱。荷载小分子药物最多的分 子由于疏水性最强最后洗脱,分离过程类似于反相色谱, 但是随着ADC药物的payload不断发展,近期科研工作 者发现对于偶联较强亲水性payload的ADC药物而言, 不同荷载分子之间的疏水性差异不是特别明显,HIC模 式下无法很好的分离不同载药数量的ADC分子。
此时反相色谱在就成为一种适合的替代方案,该方 法特别适合基于半胱氨酸偶联的ADC。通过对ADC药物 进行还原,使抗体还原为轻链和重链,含不同数量小分 子载药数的轻链和重链依据载药数量从少到多依次洗脱。 再通过计算各轻、重链的峰面积百分比,并结合每个峰 偶联小分子药物的个数,计算加权平均DAR值。
Trastuzumab deruxtecan(DS-8201;ENHERTU®) 是由第一三共和阿斯利康合作开发的新型HER2靶向 ADC。Deruxtecan是毒性药物DX-8951 的衍生物 (Dxd) 和连接子马来酰亚胺-GGFG 肽的偶联物,是一种较为 亲水性的payload。
本应用使用Biozen 的400A孔径的WidePore C4色谱 柱对 DTT还原后的Trastuzumab- deruxtecan供试品进行 分析,并计算其平均DAR值。
关键词
平均DAR值;DS-8201;反相;Biozen WidePore C4; BioTi;核壳柱
化合物信息

实验部分
3.1仪器、试剂与材料
3.1.1主要仪器设备
Thermo U3000高效液相色谱仪
3.1.2试剂材料
三氟乙酸,乙腈为色谱纯,屈臣氏蒸馏水
3.1.3样品
Trastuzumab- deruxtecan对照品购自第一三共, DAR值为8。用纯水稀释为浓度为1.0 mg/mL;
Trastuzumab- deruxtecan供试品,由客户慷慨 赠送,先用纯水稀释为浓度为1.0 mg/mL;再用 1M DTT还原后上样。
Trastuzumab购自MCE;先用纯水稀释为浓度为1.0 mg/mL;再用1M DTT还原后上样。
3.2色谱条件
色谱柱:Biozen WidePore C4(2.6um,400A 150*4.6mm);P/N: 00F-4786-E0;
流动相A:0.1%TFA水;
流动相B:0.1%TFA乙腈;
流 速:0.5 mL/min;
柱 温:60 ℃;
波 长:280nm;
进样量:10 μL
梯度程序见表2:
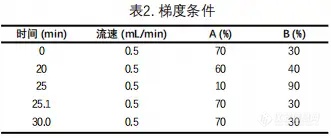
3.3结果与讨论
通过对Trastuzumab- deruxtecan供试品,Trastuzumab单抗和Trastuzumab- deruxtecan对照品 进行还原(100ug蛋白中加入5uL 1M DTT,37°C分 别孵育半小时和一小时),我们可以在反相色谱上 通过梯度优化,清晰的分离轻链和重链以及荷载不 同小分子数量的轻重链。
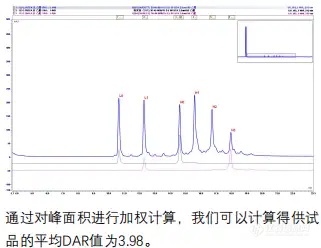
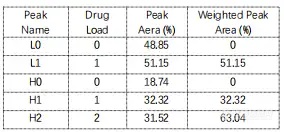

结论
在本应用使用Biozen 的400A孔径的WidePore C4色谱柱对 DTT还原后的Trastuzumab- deruxtecan 供试品进行DAR值分析。该柱采用核壳技术结合丁基 的键合相,可以大幅减少蛋白与固定相的次级作用, 改善蛋白回收率,峰形和残留的问题,三键键合技 术的C4固定相能够耐受90度的高温;Bio Ti生物惰性 的钛合金柱硬件也最大程度的减少了对生物基质样 品的干扰,保证分析结果的稳健可靠。
更多![]()
【飞诺美色谱】莽草酸色谱柱筛选
厂商
2024.09.12
【飞诺美色谱】9-亚甲基-9H-芴和9-甲基-9H-芴的分析方法
厂商
2024.09.12
【飞诺美色谱】莽草酸色谱柱筛选
厂商
2024.09.12
【飞诺美色谱】吡啶-3-磺酰氯的分析方法
厂商
2024.09.12








