好文推荐 | 基于AQbD理念的吡罗昔康凝胶体外释放研究
2024/03/13 16:59
阅读:60
分享:方案摘要:
产品配置单:
华溶自动透皮扩散系统TD-12AT
型号: TD-12AT
产地: 广东
品牌: 华溶仪器
¥50万 - 80万
参考报价
联系电话
方案详情:

目的:基于分析方法质量源于设计(AQbD)理念,建立并优化吡罗昔康凝胶体外释放实验(IVRT)
方法:建立分析目标、确定关键分析属性[体外释放速率(IVRR)、初始采样时间累积释放量(Q0)、释放度];基于先前的知识与经验,从分析目标中推导出有影响的方法变量,并利用石川图进行系统总结,对影响的变量进行风险等级评估,筛选出关键方法变量(膜的种类、释放介质的种类、上样量);对2种上样量(150、300mg)、3种释放介质(0.9% NaCl 溶液、pH 5.5 的磷酸盐缓冲液和pH7.2 的磷酸盐缓冲液)和3种膜[混合纤维素膜(MCE)、聚醚砜膜(PES)、聚四氟乙烯膜(PTFE)]进行2×3×3全析因实验设计,采用扩散池法进行IVRT,将各时间点样品进行HPLC定量分析,进一步计算Q0、释放度和IVRR。利用JMP Pro 软件对实验结果进行建模分析,筛选最优参数。参考美国食品药品监督管理局(FDA)、欧洲药品管理局(EMA)要求对建立的IVRT进行膜惰性验证,释放介质验证,线性、精密度和重复性考察,敏感性和特异性考察及耐用性考察。
结果:吡罗昔康凝胶IVRT采用静态垂直扩散池(扩散面积1.767cm2,接收池体积12 mL),温度32 ℃,转速600 r·min−1,释放介质为pH7.2磷酸盐缓冲液、膜为MCE、上样量为300mg,取样时间为0.5、1.0、2.0、3.0、4.0、5.0、6.0h,取样方式为全部取样。方法学验证均符合要求。
结论:所建立的吡罗昔康凝胶IVRT可靠、耐用、具有区分力。

一、简 介
体外释放实验(IVRT)目的是测定药物从制剂中释放的速度和程度。口服固体制剂IVRT 可以建立生物药剂学分类系统(BCS)1和3类药物生物等效性,从而实现临床试验生物豁免。皮肤外用半固体制剂如软膏剂、凝胶剂、乳膏剂等的IVRT 亦是评价半固体制剂性能的有效手段,其测定的体外释放速率(IVRR)受原料药溶解度、粒径、剂型流变性、处方工艺等多方面影响,是制剂微观结构(Q3)的反映,是药品的关键质量属。欧洲药品管理局(EMA)、美国食品药品监督管理局(FDA)等监管机构已发布相关文件表示IVRT 可以作为生物等效性的评估工具替代临床试验,因此需要科学合理开发出可靠、耐用且具有区分力的IVRT方法。目前半固体制剂体外释放方法主要有流通池法、浸没池法和扩散池法。《美国药典》对这3 种方法均有收载,日本药局方收载了扩散池法,《中国药典》仅收载了流通池法且不是用来测定半固体制剂体外释放。其中扩散池因测定简便、重现性好被广泛使用。FDA发布的半固体制剂品种指南中,大部分亦推荐使用扩散池法进行IVRT研究。
分析方法质量源于设计(AQbD)是质量源于设(QbD)理念的延伸,其理念是通过设计而获得稳健且经济效益高的分析方法,目前已在高效液相色谱(HPLC)、超高性能液相色谱或快速分辨液相色谱等色谱方法开发中取得成功,该理念同样可以应用到IVRT方法的开发。
吡罗昔康作为非甾体抗炎药,具有解热、镇痛、抗炎作用。吡罗昔康对胃肠道有较大刺激性,而吡罗昔康凝胶经皮给药,可规避口服制剂引起的一系列胃肠道不良反应,具有局部药物吸收好、释药快等优点,临床主要用来缓解局部疼痛。目前尚无关于吡罗昔康凝胶体外释放研究的相关报道。因此,本研究以国内外半固体制剂、透皮制剂指导原则为依据,应用AQbD理念按以步骤利用扩散池建立吡罗昔康凝胶体外释放方法:建立分析目标、确定关键分析属性(CAA)、进行风险评估、识别关键方法变量(CMV)、实验设计、建模分析、方法验证。
二、材 料
2.1药物及主要试剂
吡罗昔康凝胶(黑龙江天辰药业有限公司,批号20220502,规格每支20 g);吡罗昔康对照品(中国食品药品检定研究院,批号100177-201704,质量分数99.5%);磷酸二氢钾、氢氧化钠、磷酸(分析纯,国药集团化学试剂有限公司);甲醇、乙腈(色谱纯,Merck 公司);混合纤维素膜(MCE)、聚醚砜膜(PES)、聚四氟乙烯膜(PTFE)(0.45 μm,天津市津腾实验设备有限公司)。
2.2主要仪器
岛津高效液相色谱仪(配备DGU-403在线脱气机、LC-40D二元泵、SIL-40C自动进样器、CTO-40S柱温箱、SPD-M40 PDA 紫外检测器),色谱柱为Waters SunFire C18(150mm×4.6mm,3.5μm);干加热自动透皮系统(推荐使用华溶TD-12AT PLUS 透皮扩散系统);CPX8800H-C 超声波清洗仪(美国Emerson 公司);XA205 十万分之一天平(梅特勒托利多公司);Milli-QIQ7000 纯水(MILLIPORE公司);JMP Pro16.0 软件。
三、方法与结果
3.1建立分析目标和确定CAA
分析目标即分析方法要达到的目标,是分析方法建立的基础,只有确定了分析目标,才能建立有效、耐用、风险可控的分析方法。CAA来源于分析目标,是分析方法质量优劣的表征,表1、2 列出了本实验的分析目标和CAA。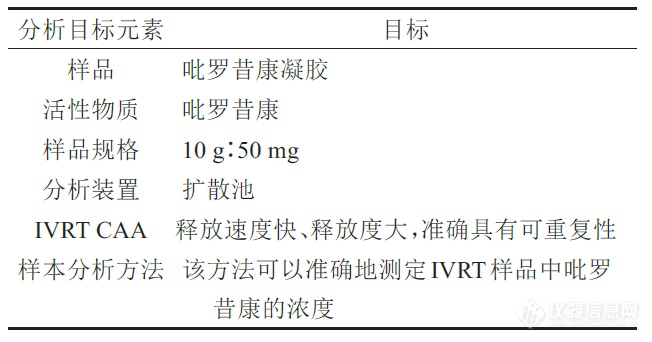

3.2 风险评估
基于先前的知识与经验,从分析目标中推导出有影响的方法变量,并利用石川图进行系统总结。对影响的变量进行风险等级评估,筛选出CMV。影响因素石川图见图1,风险等级评估见表3,上样量、释放介质类型、膜的类型是CMV。
3.3 实验设计
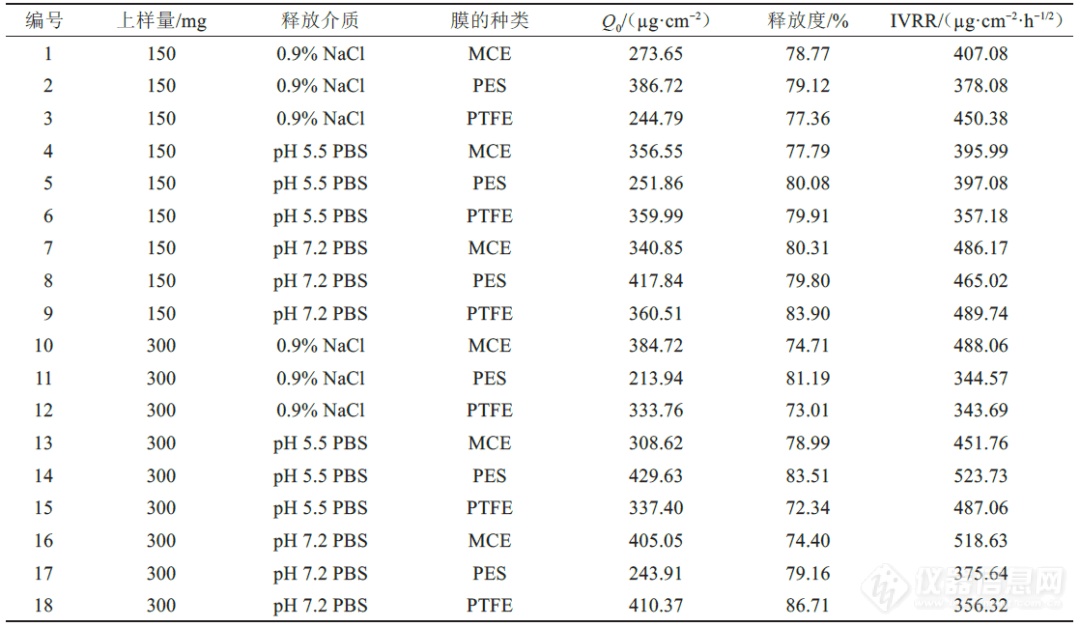
使用JMP 软件对筛选出的CMV 进行实验设计,包括2 种上样量(150、300 mg)、3 种释放介质(0.9% NaCl 溶液、pH 5.5 的磷酸盐缓冲液和pH7.2 的磷酸盐缓冲液)和3 种膜(MCE、PES、PTFE),实验设计结果见表4。
3.4 IVRT实验
IVRT采用静态垂直扩散池,温度32 ℃,转速600 r·min−1,取样模式采用全部取样,取样时间为30 min 及1、2、3、4、5、6 h。
将IVRT 实验中各时间点样品进行HPLC 定量分析,具体方法见“2.5”项,进一步计算Q0、释放度和IVRR(表4)。凝胶释放符合Hugichi 方程,即单位面积累积释放量(Q)与时间的平方根(√t)成正比,IVRR为Q和√t 的斜率。
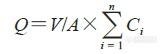
V为释放介质体积,A为释放面积,Ci为取样时间为i 时样品浓度,将i=30 min 代入上述公式即为Q0释放度=Q/( A×上样量×0.5%)
3.5 吡罗昔康分析方法及验证
3.5.1 色谱条件
Waters Sunfire C18 色谱柱( 150 mm×4.6 mm,3.5 μm);流动相0.1%磷酸-乙腈(65∶35);检测波长352 nm;进样量10 μL;柱温30 ℃;体积流量1 mL·min−1。
3.5.2 溶液配制
稀释剂:pH 7.2磷酸盐缓冲液;对照品储备液:精密称取10mg吡罗昔康对照品至10 mL 量瓶中,用甲醇稀释并定容;对照品溶液:将对照品储备液稀释至30 μg·mL−1。供试品溶液为IVRT实验的样品。
3.5.3 专属性考察
精密量取对照品溶液、释放1h样品溶液、释放介质溶液进样测定,记录色谱图,见图2。结果表明,在该色谱条件下,理论板数为13 205,目标峰与相邻峰能达到基线分离,分离度大于1.5,本方法满足检测的需要。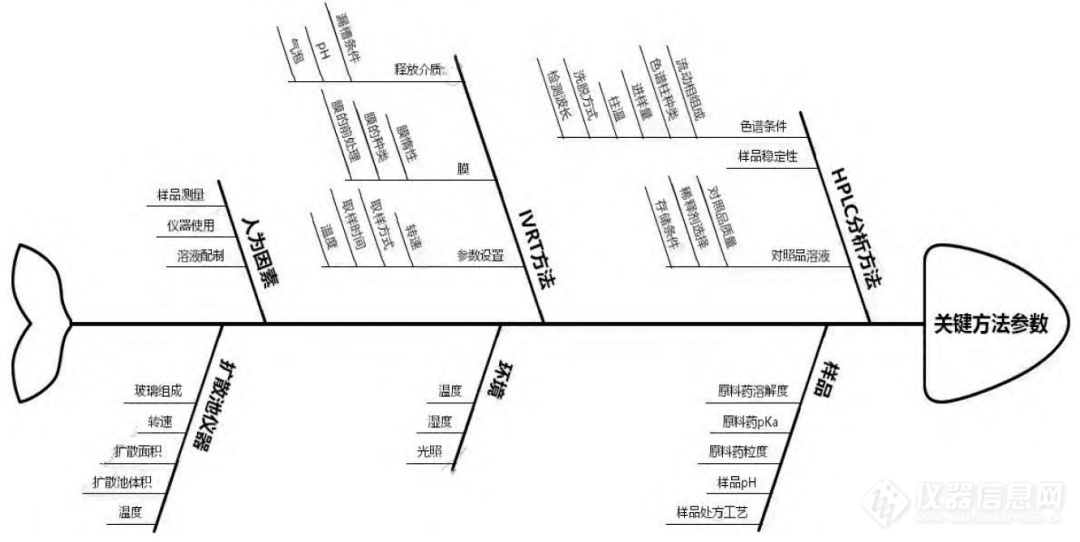

3.5.4 进样精密度考察
取对照品溶液,连续进样6次,吡罗昔康峰的保留时间和峰面积的RSD均小于2%,表明仪器精密度良好。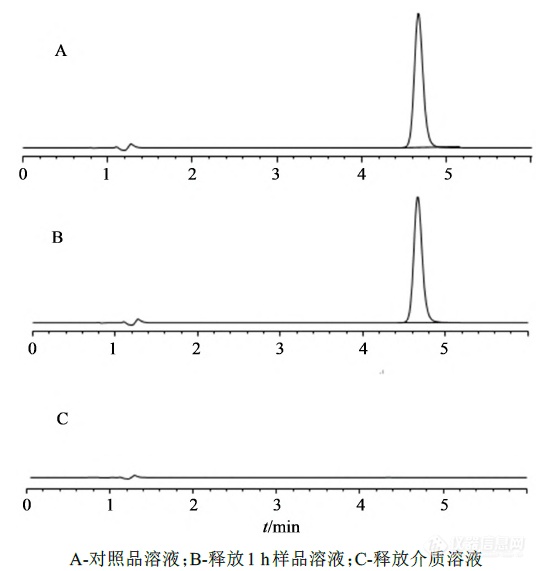
3.5.5 线性关系考察
取对照品储备液适量,用稀释剂定量稀释制成质量浓度分别为1、5、10、20、30、40、50、60 μg·mL−1的系列对照品溶液。取上述系列对照品溶液适量,按“2.5.1”项下色谱条件进样测定,记录峰面积。以质量浓度为横坐标、峰面积为纵坐标进行线性回归,得回归方程为y=31 290 x-4 394.1(r=0.999 7)。结果表明,吡罗昔康质量浓度与峰面积在1~60 μg·mL−1线性关系良好。
3.5.6 检测限和定量限考察
取对照品溶液适量,倍比稀释,注入液相色谱仪,按信噪比10∶1 确定定量限,信噪比为3∶1 确定检测限。经计算,吡罗昔康定量限为0.10 μg·mL−1,检测限为0.03 μg·mL−1。
3.5.7 稳定性考察
取样品溶液,分别在0、4、8、24h测定。吡罗昔康峰面积RSD均小于2.0%,说明溶液稳定性良好。
3.5.8 回收率考察
精密量取0.5 h 取样时间样品1 mL 置10mL 量瓶中,加入定量对照品储备液0.1、0.3、0.5mL,制成低、中、高3 个质量浓度加标供试品溶液,平行制备3份。取上述系列待测溶液适量,按色谱条件进样测定,记录峰面积并计算回收率。回收率为98.98%~101.88%,RSD均小于1.6%。
3.5.9 重复性考察
称取样品600 mg,置于10 mL量瓶,加稀释剂定容,平行配制6 份,分别进样,计算含量。样品含量的RSD为0.4%,表明该方法重复性良好。
3.6 建模及方法优化
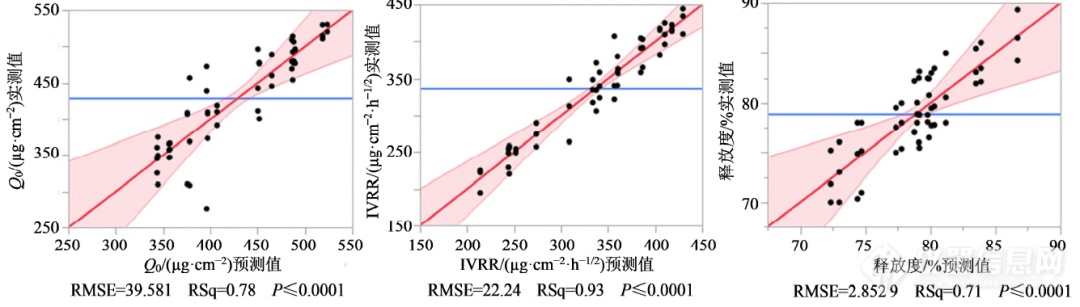
通过建模的方式评价CMV对CAA的影响及协同影响。利用JMP Pro 软件对实验结果(表4)进行建模分析,进行实验设计和多项式模型求解,对所建模型进行统计学检验。模型预测表达式见图3,表达式中的系数表明了CMV 对CVA 的影响程度,系数越大影响越大,系数为正表明有积极影响,系数为负,表明有消极影响。t 检验、方差分析表明所建模型合理,见图4。
为使IVRT 响应最大化,采用意愿函数对CMV进行优化,意愿函数越接近1,响应值越接近目标值。使用JMP Pro 进行预测值刻画,意愿函数最大为0.83,见图5,此时CMV为上样量为300 mg、释放介质为pH 7.2 的PBS、膜为MCE,该参数为最优参数。
3.7 IVRT方法学验证
3.7.1 膜惰性验证
将MCE置于30 μg·mL−1 的对照品溶液中(32±1)℃ 、600 r·min−1 孵育6 h,重复3次,测定对照品溶液质量浓度前后变化,计算回收率。
3.7.2 释放介质验证
释放介质需要满足漏槽条件,测定pH 7.2 磷酸盐缓冲液中吡罗昔康饱和溶解度。
3.7.3 线性、精密度和重复性考察
连续3 d 进行3组IVRT 实验,每组6个,Q与√t 成线性,计算IVRR以表征IVRT方法的精密度和重现性。
3.7.4 敏感性和特异性
以市售吡罗昔康凝胶为原料,制备质量分数0.25%、0.375% 的吡罗昔康凝胶,进行IVRR 测定,评估IVRT 方法的敏感性和特异性。
3.7.5 耐用性考察
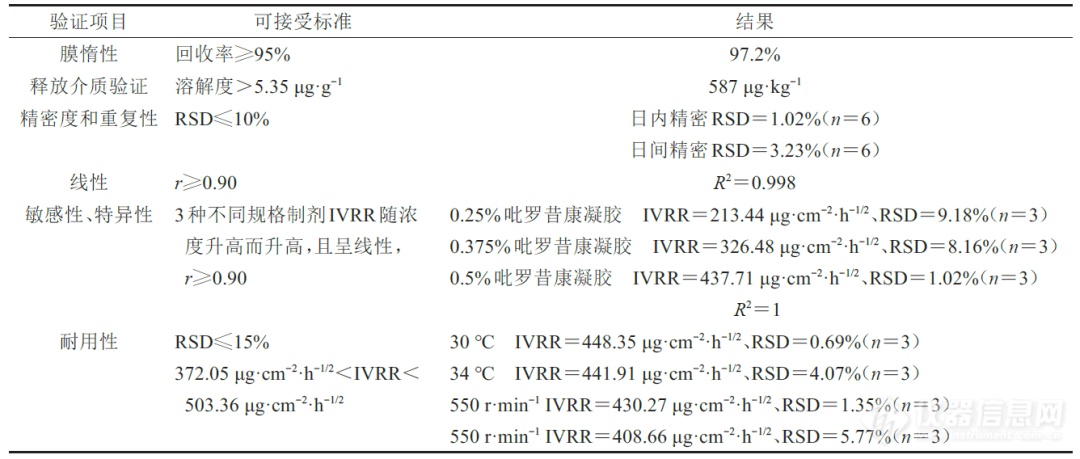
IVRT 温度为(32±2)℃,转速为(600±50)r·min−1时,考察方法的耐用性。IVRT方法学验证可接受标准及结果见表5。
四、讨 论
4.1 CMV选择
吡罗昔康昔康凝胶属于无限剂量样品,上样量选择150、300 mg;0.9%氯化钠水溶液比较接近人体皮肤生理状态,人体皮肤表面呈弱酸性,因此选择0.9%氯化钠溶液、pH 5.5 磷酸盐缓冲液和pH 7.2磷酸盐缓冲液作为释放介质。不同膜结构性能不同,选择具有亲水性的MCE、PES 和具有疏水性的PTFE。
4.2 CAA分析
通过绘制Q与√t 的关系得到的回归线的斜率,即IVRR。IVRR 是IVRT 的CAA,也是评价半固体制剂质量一致性的重要工具之一。建模结果表明CMV中上样量对IVRR的影响最大,其次是膜和释放介质,膜与上样量、介质的交互影响作用显著,其余交互影响作用不显著。Q0为30 min 时累积释放量,旨在排除剂量倾倒的可能性,建模结果表明CMV 中膜、释放介质和膜与释放介质的交互影响具有显著性。释放度旨在评价释放过程中质量守恒,表达式中释放度的各项系数相对较小,表明该CAA受影响较小。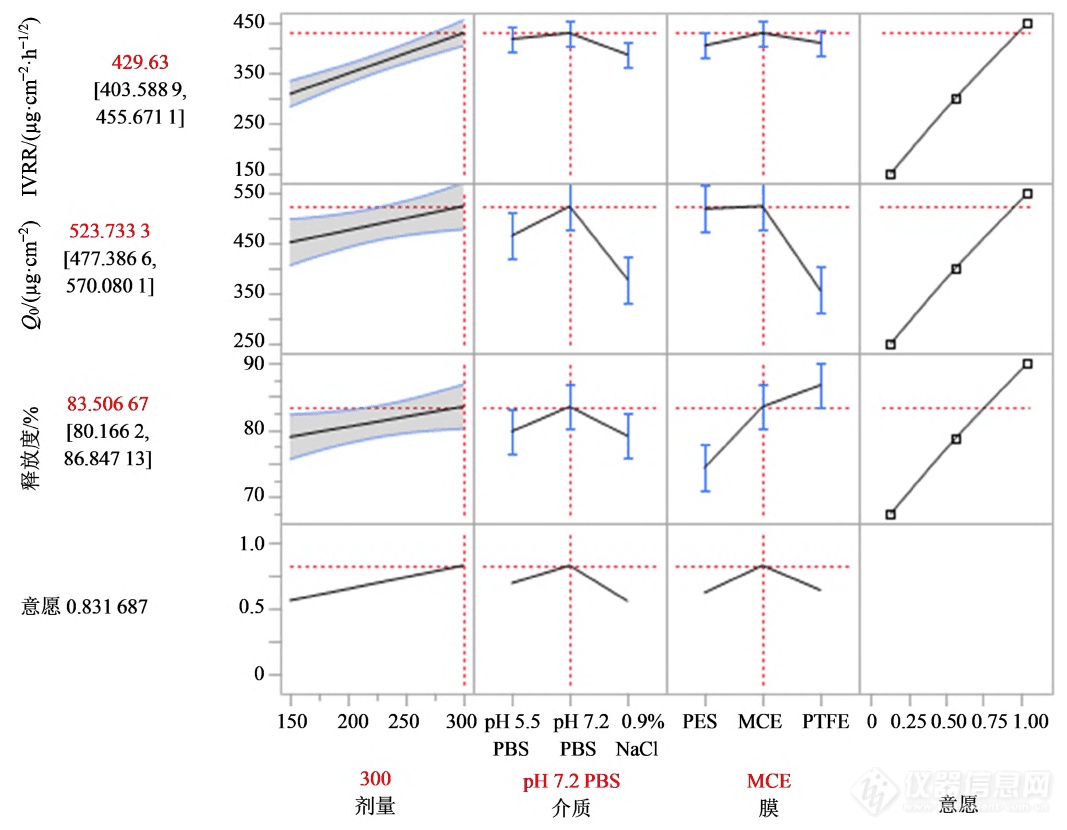
本研究以AQbD理念作为IVRT 方法开发的框架,从定义分析目标入手,确定CMA后,将IVRT 的影响因素进行全面剖析,并进行风险评估,确定CMV,采用2×3×3 全因子设计实验,评估上样量、膜的种类和释放介质对CAA(IVRR、Q0和释放度)的影响。对这些影响进行建模并通过t 检验和方差分析验证所建模型。利用所建模型的预测功能,得到IVRT 释放最大化的参数MCE、pH 7.2 磷酸盐缓冲液和300 mg 的上样量。根据欧洲和美国监管机构的最新指南,对优化后的IVRT 条件进行了膜惰性、线性、精度、耐用性性和区分力指标的评估,同时对HPLC法进行了验证,证明该方法可靠、耐用具有区分力。
五、参考文献
略 如需原文,请联系小编(代老师)
下载本篇解决方案:
更多![]()
好文推荐 |依匹哌唑原位凝胶植入剂的体外释放研究
目的 建立一种依匹哌唑原位凝胶植入剂的体外释放方法,研究处方在体外的释放行为和缓释机制。 方法 以抗精神病依匹哌唑为模型药物,制备以聚乳酸⁃羟基乙酸共聚物( polylactide gly⁃ colic acid,PLGA)/醋酸异丁酸蔗糖酯( sucrose acetate isobutyrate,SAIB)为基质的原位凝胶植入剂。开发体外释放检测方法,采用多种体外释放装置研究依匹哌唑原位凝胶植入剂的释放差异, 考察体外释放的影响因素。
制药/生物制药
2024/06/24
好文推荐 | 水杨酸片在流池法溶出仪性能验证试验中的应用
流池法溶出仪是控释剂型、难溶性药物和许多特殊剂型(如混悬液、软胶囊、植入剂、微球和脂质体)溶出度测试的首选仪器。虽然流池法溶出仪已列入药典多年,但一直没有正式的性能验证试验(PVT)方法。在这项研究中,水杨酸片被用来开发流池法的PVT。水杨酸片在篮法和桨法装置上相同的溶蚀和零级释放机制,可作为流池法装置中PVT的潜在参考标准品。在第一阶段,采用实验设计法(DoE)系统考察了四个参数对水杨酸片溶出度的影响。片剂装载方式是影响溶出度的最重要参数;流速和池体内径(ID)也有显著影响,温度对溶出的影响可以忽略不计。在第二阶段,由四名不同的分析人员在不同的流池法装置上(即四名合作者)进行溶出试验,以进行重复性和重现性评估,并确定PVT的初步可接收标准。第二阶段的实验条件是将片剂放置在带有玻璃珠的片剂支架上,池体ID为12 mm,流速为16 mL/min,温度为37℃,90分钟采集样品。第五个合作者的数据证实了PVT的可重复性。
制药/生物制药
2024/06/14
介质脱气小能手 | 华溶DGU-900在线溶媒脱气机,只为溶出仪而生
在进行溶出实验过程中,介质中溶解气体的释放是影响溶出结果的主要变动因素之一。因此,对溶出介质进行脱气处理变得尤为重要,并应将具体脱气程序写入溶出检测操作的标准操作规程。
制药/生物制药
2024/04/15
好文推荐 | 奈帕芬胺眼用混悬液的体外释放试验方法
体外释放试验(IVRT)方法对于监测制药生产过程中批次间的质量变化以及表现仿制药与原研药的药物等效性非常重要。为了满足批准眼用混悬液仿制药的监管要求,需要进行体外释放研究。目前尚无药典或非药典方法用于奈帕芬胺眼用混悬液的体外释放研究。 目前的研究旨在筛选使用不同的常规和非常规的各种方法,以建立最合适的奈帕芬胺眼用混悬液的技术,然后优化方法参数并进行验证。试验使用带透析袋的桨法装置(USP 2型)、流通池装置(USP 4型)、水浴转瓶装置和Franz扩散池装置。使用USP 4型装置,在pH 7.4的模拟泪液(STF)中,药物在120分钟内的释放度约为83%,添加表面活性剂月桂醇硫酸酯钠(SLS)后,释放度增加到约97%。使用USP 2型和Franz扩散池装置,药物释放缓慢或未接近完全释放。然而,在水浴转瓶装置的情况下,观察到了突释曲线。药物释放量的估计是通过HPLC方法进行的,所有方法验证参数,如专属性、准确度、线性和精密度都在可接受标准范围内。
制药/生物制药
2024/04/02










