推荐厂家
暂无
暂无



 400-883-7896
400-883-7896
 留言咨询
留言咨询

 400-860-8560
400-860-8560
 留言咨询
留言咨询

 400-860-5168转2623
400-860-5168转2623
 留言咨询
留言咨询



[size=15px][font=&][font=宋体]对乙酰氨基酚([/font][font=&]APAP[/font][font=宋体])过量是药物性肝损伤的主要原因。[/font][font=&]Sirtuins 5[/font][font=宋体]([/font][font=&]SIRT5[/font][font=宋体])与各种肝脏疾病的发展有关。然而,其在[/font][font=&] APAP [/font][font=宋体]诱发的急性肝损伤([/font][font=&]AILI[/font][font=宋体])中的作用仍不清楚。[/font]SIRT5[/font][font=宋体]在[/font][font=&]AILI[/font][font=宋体]中显著下调,并且[/font][font=&]SIRT5[/font][font=宋体]耗竭加剧了体内和体外的线粒体氧化应激。从机制上讲,[/font][font=&]SIRT5[/font][font=宋体]在对乙醛脱氢酶[/font][font=&]2[/font][font=宋体]([/font][font=&]ALDH2[/font][font=宋体])的[/font][font=&]K385[/font][font=宋体]位点进行去琥珀酰化,从而保持[/font][font=&]ALDH2[/font][font=宋体]的酶活性,进而抑制炎症和线粒体氧化应激。此外,[/font][/size][font=宋体][size=15px]研究发现葛根素([/size][/font][font=&][size=15px]puerarin[/size][/font][font=宋体][size=15px])可促[/size][/font][size=15px][font=宋体]进[/font][font=&]SIRT5[/font][font=宋体]去琥珀酰化酶活性并缓解[/font][font=&]AILI[/font][font=宋体]。 [size=15px][b]1、AILI 中肝细胞SIRT5表达显著下调[/b][/size] [size=15px]作者首先通过RNA测序发现APAP[/size][font=宋体]处理[/font][size=15px]后,肝脏组织中 SIRT5 表达显著下调。进一步验证SIRT5参与AILI,发现APAP处理的小鼠血清ALT和AST水平均不同程度升高,且q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]、Western blott和免疫组化检测显示APAP处理后肝脏中SIRT5下调,表明SIRT5是AILI发展的关键介质 [/size][/font][/size][b][font=&][color=#0070c0]2[/color][/font][font=宋体][color=#0070c0]、[/color][/font][font=&][color=#0070c0]SIRT5 [/color][/font][font=宋体][color=#0070c0]改善[/color][/font][font=&][color=#0070c0]APAP[/color][/font][font=宋体][color=#0070c0]诱导的肝毒性[/color][/font][/b][size=15px][font=宋体][size=15px] [/size] [size=15px]作者构建了SIRT5-KO小鼠和AAV介导的肝脏特异性SIRT5过表达小鼠,以进一步研究SIRT5在AILI中的作用。结果显示APAP处理后WT小鼠血清ALT和AST水平显著升高,且SIRT5-KO小鼠的血清ALT和AST水平升高更为明显,肝脏坏死显著加重,肝细胞死亡率更高,而SIRT5过表达显著改善APAP引起的肝脏损伤,肝细胞死亡率显著降低,结果表明 SIRT5 可减轻 APAP 诱导的肝毒性 [/size] [size=15px][b]3、SIRT5抑制APAP诱导的肝脏炎症[/b][/size] [size=15px]多项研究表明APAP 引起的肝毒性与炎症密切相关。作者发现接受APAP处理的SIRT5-KO小鼠CD11b和Ly6g阳性炎症细胞数量显著增加,肝脏中炎症细胞因子的水平显著升高,且NF-κB 信号的激活增加,而肝脏特异性SIRT5过表达小鼠则相反,这些结果表明SIRT5可抑制APAP诱导的AILI肝脏炎症 [/size] [size=15px][b]4、SIRT5 抑制AILI 中APAP诱导的线粒体氧化应激[/b][/size] [size=15px]在AILI过程中,细胞色素P450酶产生过量的毒性反应代谢物NAPQI,消耗GSH并与线粒体蛋白共价结合形成APAP加合物,导致线粒体功能障碍、ROS产生和线粒体细胞死亡因子的释放,最终导致肝细胞死亡。作者研究了SIRT5 KO或过表达对APAP诱导的线粒体氧化应激的影响,体内和体外实验结果表明SIRT5抑制了AILI期间的线粒体氧化应激 [/size] [size=15px][b]5、SIRT5缺乏导致AILI中蛋白质琥珀酰化全面增加[/b][/size] [size=15px]鉴于SIRT5在去琥珀酰化中的作用明确,作者采用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析了APAP处理的WT和SIRT5-KO小鼠肝脏中的琥珀酰化。结果显示共有465种蛋白质中的953个位点表现出差异琥珀酰化,其中359种蛋白质中的802个位点显示琥珀酰化水平增加,而106种蛋白质中的151个位点显示琥珀酰化水平降低,结果表明SIRT5缺陷导致AILI中蛋白质琥珀酰化整体增加,这在体内和体外得到了进一步的验证 [/size] [size=15px][b]6、SIRT5在K385残基处使ALDH2去琥珀酰化[/b][/size] [size=15px]SIRT5缺乏导致参与线粒体氧化应激的关键酶ALDH2的琥珀酰化显著上调。进一步探索SIRT5调控ALDH2琥珀酰化的具体分子机制,免疫荧光发现SIRT5与ALDH2共定位,免疫共沉淀实验表明SIRT5与ALDH2互作,且SIRT5敲除显著上调了体内和体外ALDH2的琥珀酰化水平,但对ALDH2的总蛋白浓度没有影响,相反SIRT5过表达显著降低ALDH2的琥珀酰化水平。进一步检测发现SIRT5缺乏会抑制ALDH2的酶活性,而SIRT5过表达会增加ALDH2的活性。[/size] [size=15px][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS显示ALDH2中三个位点(K370、K377、K385)琥珀酰化显著增加,其中K370和K385在不同物种中高度保守,作者通过将赖氨酸(K)突变为谷氨酸(E)模拟琥珀酰化,将K突变为精氨酸(R)模拟去琥珀酰化,发现K385是ALDH2上的关键琥珀酰化位点,且K385而非K370的琥珀酰化影响ALDH2的酶活性。此外,SIRT5主要通过对ALDH2在K385残基上的去琥珀酰化来减轻AILI [/size] [size=15px][b]7、ALDH2在K385残基处的去琥珀酰化可保护小鼠免受 AILI的侵害[/b][/size] [size=15px]为了研究ALDH2-K385去琥珀酰化在AILI中的作用,作者建立了AAV-GFP、AAV-ALDH2-WT和AAV-ALDH2-385K-E过表达转染小鼠,并对其进行APAP处理。结果显示APAP 给药增加ALDH2的琥珀酰化,而ALDH2-385K-E小鼠肝脏中ALDH2的琥珀酰化程度低于ALDH2-WT小鼠。此外,在APAP给药后,ALDH2-385K-E小鼠的转氨酶水平、肝坏死面积和肝细胞死亡增加,线粒体氧化应激和炎症加重。数据表明ALDH2在K385的去琥珀酰化可保护小鼠免受AILI的侵害 [/size] [size=15px][b]8、[/b][/size][size=15px][b]K385 [/b][/size][size=15px][b]位点ALDH2去琥珀酰化介导SIRT5对AILI的保护作用[/b][/size] [size=15px]为了研究SIRT5对ALDH2去琥珀酰化在体内AILI中的作用,作者通过尾静脉注射表达 AAV-GFP、AAV-ALDH2-WT或AAV-ALDH2-385K-E的相关AAV,在SIRT5-KO小鼠中过表达各种形式的ALDH2,这些小鼠随后接受APAP治疗。结果显示SIRT5缺乏显著升高血清转氨酶水平,在APAP处理后引起坏死和肝细胞死亡,而 ALDH2-WT的过表达显著改善了肝损伤。此外,ALDH2-WT小鼠的肝脏氧化和炎症明显减少,但ALDH2-385KE小鼠的肝脏氧化和炎症没有减少,数据表明ALDH2在K385处的去琥珀酰化介导了SIRT5对AILI的保护作用 [/size][size=15px][b]9、葛根素促进SIRT5减轻AILI[/b][/size] [size=15px]为探究SIRT5激动剂对AILI的治疗作用,作者通过虚拟筛选寻找能与SIRT5结合的天然化合物。根据对接结果筛选出10个亲和能最低的化合物,进一步考察其对SIRT5去琥珀酰化酶活性的影响,其中葛根素对SIRT5去琥珀酰化酶活性的提高最为显著。分子对接分析显示SIRT5能与葛根素结合,分子动力学模拟在原子水平上证实了SIRT5-葛根素复合物的结合稳定性和动力学。接着在体内验证了葛根素对APAP诱导的肝损伤的影响,发现葛根素组在APAP刺激后血清AST和ALT水平降低,肝脏坏死和肝细胞死亡减少,APAP 诱导的氧化应激和炎症明显被抑制。结果表明葛根素通过药理学激活SIRT5减轻AILI,提示葛根素是临床治疗AILI的一种有前途的药物[/size][/font][/size]
[font=宋体]肝纤维化是指持续性肝损伤后,肝内结缔组织异常增生进行自我修复而引起的可逆性病理现象,且在严重情况下可发展成肝硬化和肝癌。肝纤维化的发病机制复杂,其中细胞外基质沉积和慢性肝损伤导致的肝星状细胞([/font][font='Times New Roman',serif]HSC[/font][font=宋体])持续活化是主要的发展进程。目前仍然没有确定的药物可以用于逆转肝纤维化并在临床中发挥肝保护作用。甘草酸被报道具有肝脏解毒、抗炎、抗氧化和抗病毒活性,但甘草酸在[/font][font='Times New Roman',serif]CCl[sub]4[/sub][/font][font=宋体]诱导的肝纤维化模型的靶蛋白尚未被确定。[/font][font=宋体]中国中医科学院西苑医院王培利联合中国中医科学院中药研究所青蒿素研究中心的王继刚等团队在[/font][font='Times New Roman',serif]Phytomedicine[/font][font=宋体](中科院[/font][font='Times New Roman',serif]1[/font][font=宋体]区,[/font][font='Times New Roman',serif]IF=6.7[/font][font=宋体])发表题为[/font][font='Times New Roman',serif]“Glycyrrhizic acid ameliorates hepatic fibrosis byinhibiting oxidative stress via AKR7A2”[/font][font=宋体]的文章,发现甘草酸可通过[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]抑制活化[/font][font='Times New Roman',serif]HSC[/font][font=宋体]中[/font][font='Times New Roman',serif]ROS[/font][font=宋体]介导的氧化应激,可显著逆转肝纤维化。[/font] [font=宋体]在该研究,与模型组比较,血生化和病理切片结果均显示甘草酸组可改善四氯化碳诱导的小鼠肝纤维化。体外实验表明,甘草酸对正常肝细胞没有影响,但对肝癌细胞[/font][font='Times New Roman',serif]HepG 2[/font][font=宋体]和肝星状细胞[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]都有抑制作用,且流式细胞术表明甘草酸可清除[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞内活性氧,维持活化[/font][font='Times New Roman',serif]HSC[/font][font=宋体]的稳态。接下来作者用基于活性的蛋白质组分析[/font][font='Times New Roman',serif](ABPP)[/font][font=宋体]鉴定[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞中甘草酸的蛋白质靶标(图[/font][font='Times New Roman',serif]1[/font][font=宋体])。凝胶扫描图的结果显示甘草酸([/font][font='Times New Roman',serif]GA[/font][font=宋体])减弱了[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]探针的荧光信号,表明[/font][font='Times New Roman',serif]GA[/font][font=宋体]与[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]标记的蛋白质竞争性结合(图[/font][font='Times New Roman',serif]1B[/font][font=宋体])。对各组差异蛋白进行[/font][font='Times New Roman',serif]MS[/font][font=宋体]分析,并选择在[/font][font='Times New Roman',serif]GA[/font][font=宋体]结合蛋白中具有最大丰度比的[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]用于进一步研究(图[/font][font='Times New Roman',serif]1C[/font][font=宋体])。纯化的重组[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]蛋白的荧光标记与上述一致(图[/font][font='Times New Roman',serif]1D[/font][font=宋体])。此外,[/font][font='Times New Roman',serif]CETSA[/font][font=宋体]表明[/font][font='Times New Roman',serif]GA[/font][font=宋体]给药最初增加[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞中的[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]表达,且与[/font][font='Times New Roman',serif]DMSO[/font][font=宋体]相比,其结合热稳定性显著提高(图[/font][font='Times New Roman',serif]1E[/font][font=宋体])。荧光共定位法观察到[/font][font='Times New Roman',serif]GA[/font][font=宋体]和[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]在[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞中竞争性占据的蛋白荧光。核[/font][font='Times New Roman',serif]Hoechst[/font][font=宋体]、[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]([/font][font='Times New Roman',serif]Click[/font][font=宋体]荧光试剂)和[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]蛋白分别显示蓝色、红色和黄色荧光(图[/font][font='Times New Roman',serif]1F[/font][font=宋体])。在[/font][font='Times New Roman',serif]DMSO[/font][font=宋体]处理的细胞中,仅添加具有[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]的荧光二抗的[/font][font='Times New Roman',serif]Hoechst[/font][font=宋体]。与[/font][font='Times New Roman',serif]DMSO[/font][font=宋体]组相比,[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]组显示出强烈的红色荧光,表明该蛋白在[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞中与[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]高度结合。与[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]组相比,[/font][font='Times New Roman',serif]GA[/font][font=宋体]和[/font][font='Times New Roman',serif]IAA-yne[/font][font=宋体]竞争性地占据[/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞中的[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体],表现为[/font][font='Times New Roman',serif]GA + IAA-yne[/font][font=宋体]组的红色荧光强度显著降低,黄色荧光增强。通过分子对接进一步预测[/font][font='Times New Roman',serif]GA[/font][font=宋体]与[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]的结合位点,模拟分析显示[/font][font='Times New Roman',serif]GA[/font][font=宋体]与[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]的氨基酸残基[/font][font='Times New Roman',serif]ARG-264[/font][font=宋体]、[/font][font='Times New Roman',serif]LYS-267[/font][font=宋体]、[/font][font='Times New Roman',serif]CYS-355[/font][font=宋体]、[/font][font='Times New Roman',serif]GLU-345[/font][font=宋体]和[/font][font='Times New Roman',serif]GLN-207[/font][font=宋体]结合,结合能为[/font][font='Times New Roman',serif]-5.47 kJ/mol[/font][font=宋体](图[/font][font='Times New Roman',serif]1G[/font][font=宋体])。此外,[/font][font='Times New Roman',serif]SPR[/font][font=宋体]分析验证了计算机分子对接方法的结果。结果显示[/font][font='Times New Roman',serif]GA[/font][font=宋体]显著结合[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体],[/font][font='Times New Roman',serif]K[sub]d[/sub][/font][font=宋体]值为[/font][font='Times New Roman',serif]21.76 μM[/font][font=宋体](图[/font][font='Times New Roman',serif]1H[/font][font=宋体])。这些实验表明[/font][font='Times New Roman',serif]GA[/font][font=宋体]直接结合[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]。并且在[/font][font='Times New Roman',serif]WB[/font][font=宋体]实验,[/font][font='Times New Roman',serif] GA[/font][font=宋体]给药后[/font][font='Times New Roman',serif]α-SMA[/font][font=宋体]([/font][font='Times New Roman',serif]α-SMA[/font][font=宋体]是肝纤维化的标志物之一)水平显著降低,[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]和[/font][font='Times New Roman',serif]CYGB[/font][font=宋体](有研究表明,[/font][font='Times New Roman',serif]cygb[/font][font=宋体]具有预防纤维化和实现纤维化逆转的功能)都在一定程度上增加(图[/font][font='Times New Roman',serif]5I[/font][font=宋体])。这些结果进一步证实[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]是[/font][font='Times New Roman',serif]GA[/font][font=宋体]作用的靶标。 [img=,690,954]https://ng1.17img.cn/bbsfiles/images/2024/09/202409091641582775_4564_6541583_3.png!w690x954.jpg[/img] [img=,690,425]https://ng1.17img.cn/bbsfiles/images/2024/09/202409091641194830_405_6541583_3.png!w690x425.jpg[/img] [/font] [font=宋体]作者通过观察[/font][font='Times New Roman',serif]GA[/font][font=宋体]对[/font][font='Times New Roman',serif]CCl[sub]4[/sub][/font][font=宋体]诱导的小鼠肝纤维化及激活的肝星状细胞([/font][font='Times New Roman',serif]LX-2[/font][font=宋体]细胞)的影响,发现[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]参与了这一过程。其他研究表明[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]是醛[/font][font='Times New Roman',serif]/[/font][font=宋体]酮还原酶超家族的成员,其依赖于[/font][font='Times New Roman',serif]NADP[/font][font=宋体]([/font][font='Times New Roman',serif]H[/font][font=宋体])将醛和酮还原成醇,主要存在于组织如肝和肾中,对脂质过氧化产生的醛具有催化活性,因此在防御活性氧以逆转氧化应激中发挥作用。由于[/font][font='Times New Roman',serif]GA[/font][font=宋体]不仅在活化的[/font][font='Times New Roman',serif]HSC[/font][font=宋体]中增加[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]的表达,而且在整个肝脏中也增加[/font][font='Times New Roman',serif]AKR7A2[/font][font=宋体]的表达,因此[/font][font='Times New Roman',serif]GA[/font][font=宋体]可显著改善肝纤维化。 [/font]
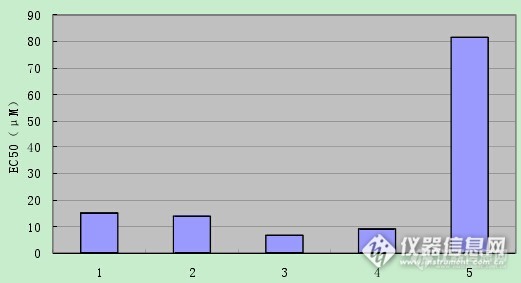
九味中药的抗氧化能力活性筛选 衰老的自由基学说最早1956年提出, 并逐步发展为自由基一氧化应激学说。此学说认为在生命活动过程中产生的自由基对生物大分子、细胞器、细胞等累积性氧化损伤,导致组织损伤和器官功能衰退,诱导及加速机体衰老。在病理条件下或随着年龄的增加,各种内外因素导致自由基大量、过多产生,超过了机体的抗氧化能力,便产生氧化应激,过多自由基通过损伤细胞核及线粒体DNA、生物膜脂质过氧化、蛋白质交联变性等多种方式引起细胞损伤,氧化损伤逐渐累积,最后导致各种老年性疾病的发生和发展。 本实验室通过大量调研文献,筛选出具有潜在抗氧化作用的中药,只在通过实验最终筛选出具有抗氧化作用比较强的药味,进一步开发利用! DPPH(二苯基苦味酰基自由基,)在有机溶剂中是一种稳定的以氮为中心的自由基,其单电子在517 nm附近有最大吸收。甲醇溶液呈紫色,其浓度与吸光度呈线性关系。当甲醇溶液中有自由基清除剂存在时,的单电子被配对而使ESR信号减弱,溶液颜色变浅,直至达到稳定。因此,可以通过在517nm波长处检测不同待测样品对自由基的清除效果,从而评价样品的抗氧化能力。本实验参照相关文献用紫外分光光度计筛选了九味中药的DPPH自由基清除活性,并测定了半效应浓度(EC50)。一、试剂与仪器二苯代苦味酰自由基(DPPH)、2,6-二叔丁基-4-甲基苯酚;氯仿、甲醇均为分析纯;紫外可见分光光度计为上海产S54A型分光光度计。二、实验方法2.1样品的制备 待测样品:九味中药分别采用水煎煮的方法提取浓缩成每1g提取液相对于10g原药材。每份提取液以最适溶剂溶解后,配成1μg/ml、5μg/ml、10μg/ml、25μg/ml、50μg/ml、100μg/ml六个浓度的溶液待测。2.2 DPPH标准曲线的制备 精密称取DPPH标准品12.62 mg,加入200 ml无水甲醇,配制成浓度为0.16 mmol/L的储液。分别精密移取1.00 mL各个样品的六个浓度的待测溶液,依次迅速加入1.00 mL DPPH甲醇溶液。在选定最大吸收波长(517 nm)的条件下,分别测定其吸光度。2.3样品的自由基清除能力测定 DPPH[


