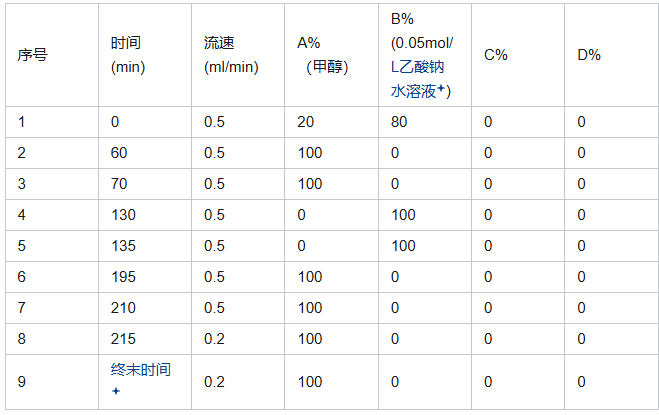
岛津LC-20AT常见8大故障是什么?解析具体原因及正确解决方法
一、泵不送液1、泵头中有气泡解决方法:将流动相用超声波清洗器进行脱气;打开排液阀,按PURGE功能键排除气泡;打开排液阀,用注射器从泵的排液管中抽液排除气泡。2、单向阀堵塞,污染,磨损造成单向阀工作不正常。解决方法: LC-20AT是双泵头串联泵,在主泵头和辅泵头的下端分别装有入口单向阀,当送液泵出现压力波动超过0.3MP或者送液压力达不到正常压力值时,排除气泡干扰的因素后,初步判断单向阀被污染导致上述现象发生,可用下面两种方法清洗。第一种方法是在线清洗:打开仪器电源,确认键盘在开启状态,拆下泵的出口管,连接阻尼管,阻尼管的出口直接接入废液瓶,将流动相换成异丙醇,打开排液阀,按PURGE键更换流动相,等待其运行结束后关闭排液阀,按FUNC键将流速设为1mL/min,按PUMP键送液清洗,需要清洗一个小时以上。第二种方法是超声波清洗:拧松并取下单向阀的管路用扳手分别松开两个泵头的入口单向阀,用手取下单向阀,用镊子将单向阀放入装有异丙醇的烧杯中,用超声波清洗15分钟,清洗完毕后将单向阀用镊子取出,装到泵头上,用扳手拧紧,将单向阀连接管路装好并拧紧,重新送液测试,如果压力正常则清洗完毕,如果故障依然存在,可能需要更换单向阀。3、吸滤头堵塞。解决方法:吸滤头清洗或者更换。清洗时将吸滤头从送液管中拔出,用镊子放入装有异丙醇的烧杯中,超声波清洗15分钟,清洗完毕后将吸滤头用镊子取出,用滤纸擦干后插入送液管,放入装有流动相的瓶中,送液测试,确认吸滤头没有气泡产生,否则应更换新的吸滤头。二、泵压力偏高1、泵的管路过滤器堵塞。断开泵的出口管路,以1mL/min送液压力高于0.3MP,说明管路过滤器堵塞。管路过滤器位于泵的出口处,用于清除由泵输送的流动相试剂中的机械杂质或柱塞密封垫磨损的碎屑。长期使用或使用含机械杂质较多的流动相时容易引起堵塞,此时需要清洗或更换过滤器上的过滤片。操作如下:拧松并取下过滤器连接管路,拧松并取下管路过滤器,用镊子将管路过滤器放入装有异丙醇的烧杯中,用超声波清洗15分钟,清洗完毕后用镊子取出过滤器,用手将过滤器拧入连接口,用手拧紧,用扳手拧紧60°~90°即可,打开泵电源开关,用纯水做流动相,以1mL/min送液,如压力值超过0.3MP,应更换新的管路过滤片。用镊子将过滤器前端的过滤片取下,把新的过滤片用纯水或异丙醇浸湿,放在过滤器座上,用手将过滤器拧入连接口,用手拧紧并用扳手拧紧60°~90°即可,连接上泵出口管路,更换完毕。2、预混合室过滤片堵塞。断开混合室出口管路,以1mL/min送液压力高于1MP,说明预混合室过滤片堵塞。当混合室压力过高时,可能是由于混合室的过滤片污染所造成。解决方法:用扳手拧开预混合室的管路,用扳手取下预混合室,取出过滤片,取下的过滤片放在装有5﹪稀硝酸溶液的烧杯中,用超声波清洗15分钟,再用纯水清洗5分钟,将清洗后的滤片安装到预混合室中,拧紧预混合室,装好连接管路,清洗完毕。如果管路压力依然偏高需要更换过滤片。3、进样器堵塞。断开进样器出口,以1mL/min送液压力高于1MP, 说明进样器流路堵塞,建议使用清洗液洗进样器流路。4、色谱柱堵塞或污染。断开色谱柱出口,送液压力仍高,说明色谱柱堵塞或污染,建议按色谱柱使用说明书清洗或者更换色谱柱。5、检测池堵塞。断开检测池出口,送液压力仍高,说明检测池堵塞。SPD-20A紫外检测器和SPD-M20A二极管阵列检测器的清洗:打开并取下检测器前面板,拧下检测器出口和入口管路接头,断开连接,再拧松两个连接头的固定螺丝,拔掉检测池加热线,拧松检测池固定螺丝,取下检测池,将适配器连接到检测池的入口并拧紧螺丝,用注射器吸取50mL异丙醇缓缓地把溶剂推入检测池中,清洗完毕后拆下适配器,观察检测池中是否留有异物,如果清洗不彻底,应分解清洗检测池,用螺丝刀拧下检测池一侧的透镜固定螺丝,用镊子取下透镜和垫片,注意镊子不要划伤透镜表面,用螺丝刀拧下检测池另一侧的透镜固定螺丝,用镊子取下透镜和垫片,将透镜放入装有异丙醇的烧杯中,用超声波清洗10分钟。同时观察检测池内是否还有异物,如有异物,先将保温罩拆下,将检测池朝下放入装有异丙醇的100毫升烧杯中,注意液面刚好没过检测池孔即可,不益使用过大烧杯,以致溶剂接触到加热线,用超声波清洗10分钟,清洗完毕后,取出检测池和透镜放在滤纸上,将池体表面的液体擦干,装回保温罩,将新的垫片装入检测池左侧池孔中,再将凸透镜放在垫片上面,注意垫片和透镜应放在检测池的凹槽中,透镜的凸面应朝上,拧上透镜固定螺丝,将新的垫片放入检测池右侧池孔中,将平面透镜放在垫片上面,拧上透镜固定螺丝,螺丝的紧固程度应该以检测池不漏液为准,过紧可能会损坏透镜,将检测池装到检测器上,检测池上的箭头方向应朝上,拧紧固定螺丝,将连接头固定在检测器上,插入检测池加热线,分别连接好检测池的入口和出口连接管路,装上前面板,检测池清洗完毕。三、泵压不稳1、泵头中有气泡。解决方法:将流动相用超声波清洗器进行脱气;打开排液阀,按PURGE功能键排除气泡;打开排液阀,用注射器从泵的排液管中抽液排除气泡。2、单向阀堵塞,污染,磨损造成单向阀工作不正常。清洗单向阀或者更换。参见在线清洗或超声波清洗单向阀操作步骤。3、吸滤头堵塞。超声波清洗吸滤头或更换。4、柱塞密封垫漏液。检查泵头是否漏液,如果漏液需更换柱塞密封垫。操作如下:柱塞密封垫磨损时密封性减弱,就会发生漏液,密封垫漏液会产生以下现象:泵头后面的清洗管路有流动相流出,如果连接泵头自动清洗装置时,装清洗液的瓶内清洗液会增加,此时需要更换新的柱塞密封垫。下面以更换左泵头密封垫为例,打开仪器电源,确认键盘在开启状态,重复按FUNC键到屏幕显示CONTROL,按ENTER键进入P-SET,输入数字“1”,按ENTER键确认,泵运行指示灯亮,等待指示灯熄灭,此时柱塞回到初始位置,用扳手拧松并取下左泵头上的连接管路,用手拧下泵头下的进液管接头,然后用内六角扳手交替拧松并取下两个泵头固定螺栓,将泵头平行取出,平放在桌面上,将密封垫装卸工具有突起的一端插入柱塞密封垫中,拉出密封垫,注意密封垫的下面还有一个小垫片,取出柱塞密封垫时应避免小垫片掉出,此时检查泵头内部,如有异物可用超声波将其清洗干净。新的密封垫先用异丙醇或乙醇浸泡5分钟,再将新密封垫套入装卸工具平直的一端,插入泵头并顶紧,将密封垫装卸工具从密封垫中拉出,再将泵头边上的凹槽与泵头座上的销钉对齐,将泵头安装到泵头固定座上,使销钉滑入槽中,将两个内六角螺栓放入泵头的螺栓孔中,先用手拧紧,再用内六角扳手将螺栓交替均匀的拧紧,将泵头上下的管路装好并拧紧,然后将左泵头的送液量清零。操作如下:按“CE”键直到屏幕回到初始画面,重复按“VP”键直到屏幕显示MAINTENANCE,重复按FUNC键直到屏幕显示“L SEAL DELIVERED”输入数字“0”,按ENTER键确认,将左泵头的送液量记录归零。注意右泵头密封垫送液量清零选择“R SEAL DELIVERED”按同样方法可更换右泵头密封垫。四、基线漂移1、色谱柱污染。用洗脱力强的溶剂长时间清洗色谱柱或更换色谱柱。2、管路污染。用清洗液清洗流路或更换被污染的部件。3、流动相污染或纯度不够。流动相重新配置,净化处理或更换纯度 高的流动相。4、检测池污染。清洗检测池,参见检测池清洗操作步骤。5、环境温度变化大。6、泵压力不稳。参见泵压不稳故障诊断。五、基线噪音大 1、检测池有气泡。参见检测池清洗操作步骤。2、流动相纯度不够,或流动相在使用波长下吸收大。更换纯度高的 流动相或更 换流动相种类。3、检测池能量低。更换光源或光路部件。4、仪器接地不良。重新连接地线,确定接地。六、峰面积重现性差1、手动进样器污染。手动进样阀的清洗:峰面积重现性差或出杂峰时,有可能进样阀受到污染,在日常清洗不能解决问题时,需分解进样阀进行清洗,如果出现漏夜现象,通常需要更换进样阀转子密封垫。首先用附带扳手拧下进样阀2号口和3号口连接管,再拧下5号口和6号口废液管,用附带内六角扳手拧松手柄的两个固定螺丝,取下进样阀,用附带的内六角扳手交替拧松进样阀后盖的三个固定螺丝,取下固定螺丝,取下进样阀后盖,取出转子密封垫和定子,放入烧杯中,分别用水和异丙醇超声清洗10分钟。清洗完毕后将定子和转子密封垫取出,放到干净的滤纸上,查看转子密封垫的表面是否有划痕,如有划痕需更换,将转子密封垫晾干后,装入进样阀,注意安装的正反面,导针孔要对应好,将定子装入后盖中,再将后盖装到进样阀上,注意定位销要对准,将三个固定螺丝放到进样阀后盖螺孔中,用扳手交替并均匀拧紧,将进样阀装回拧紧固定螺丝,将5号口和6号口废液管连接好,将2号口和3号口连接管恢复,装上进样阀手柄,拧紧固定螺丝,进样阀清洗完毕。2、手动进样器的进样口漏液。更换转子密封垫。3、自动进样器清洗液流路有气泡。选择合适的清洗液并脱气,使用PURGE功能冲洗进样阀,排除气泡。4、自动进样器进样口漏液。在流路中进样口发生漏液时,通常是进样口密封垫损坏造成,这时需要更换进样口密封垫。操作如下:打开电源开关,仪器开始自检结束后,确认键盘在开启状态,重复按FUNC键,直到屏幕显示CONTROL,按ENTER键进入,重复按FUNC键,直到屏幕显示ZHOME,按ENTER键执行,这时进样针提起并移到ZHOME位置,关闭仪器电源,打开进样器门,取出样品架,拧下挡板螺丝,取出挡板,用手拧松进样口密封垫并取下,将新的进样口密封垫插入高压阀中并用手拧紧即可,安装挡板,拧上固定螺丝,放回样品架,并关紧进样器门,打开仪器电源,仪器开始自检,自检结束后,确认键盘在开启状态,按VP键直到屏幕显示MAINTENANCE,按FUNC键直到屏幕显示NDL SEAL USED,输入“0”,按ENTER键确认,将密封垫的使用计数归零,按“CE”键两次回到初始画面,进样口密封垫更换完毕。进样口位置校正:进样针在进样口的位置发生偏移时,可能造成进样口漏液或损坏进样口密封垫,这时需要调整进样针位置。操作如下:打开仪器电源,仪器开始自检,自检结束后,确认键盘在开启状态,重复按VP键直到屏幕显示CALIBRATION,按FUNC键,输入密码,初始密码是五个零,按ENTER键进入,重复按FUNC键,直到屏幕显示ADJUST INJ PORT,按ENTER键进入,打开自动进样器门拆下挡板,按ENTER键开始调整进样器位置,依次用键盘上的上下箭头调整针的上下位置,依次用左右箭头调整针的左右位置,用FUNC和BACK键调整针的前后位置,直到进样器的针尖调整到密封垫的水平面并在密封垫的孔的中间,按ENTER键仪器自动测试调整后的位置,安装挡板,关上进样器门,输入数值“1”保存调整好的位置,输入数值“1”按ENTER键磨合进样口密封垫,进样口位置调整完毕,按CE键两次,回到初始画面,将仪器恢复。5、自动进样器流路污染。使用清洗液清洗进样器管路。6、色谱柱污染或劣化。用洗脱力强的溶剂长时间清洗色谱柱或更换色谱柱。七、保留时间重现性差1、泵压力不稳。参见泵的故障诊断。2、环境温度变化大。3、色谱柱未充分平衡好。充分平衡色谱柱。4、梯度洗脱时流动相混合比例异常。确认各流路的流速是否正确。八、峰形异常1、色谱柱污染或劣化。用洗脱力强的溶剂长时间清洗色谱柱或更换色谱柱。2、流路污染。使用清洗液清洗流路。3、流路死体积大。检查管路连接处,正确连接管路,消除死体积
操作维护
2024.09.13
超高效液相色谱质谱UPLC-q-tof-MS步骤
一、开机1.打开电脑,输入用户名:waters密码: administrator 进入电脑系统桌面;2.打开液相各个模块的电源(没有顺序);3.打开氮气发生器的电源(或液氮瓶的开关),确证压力指示在100 psi或0.7 MPa;打开氩气减压阀确证压力指示在7 psi或0.05 MPa(如果是HDMS, 还需要打开氦气减压阀确证压力指示在7 psi);4.打开质谱电源开关(在质谱背面板右侧位置有四个黑色的可以上下搬动的开关,按照从下向上的顺序依次将这四个开关搬到向上的位置,质谱 电源就打开了);5.等待5分钟(或是进入桌面的hyperterminal文件夹,双击其中的的hypertrm 图标,在name处输入epc并点击OK,接着在弹出的窗口中在Connect using 中选择com1并点击OK,在弹出的窗口中将Bits per second设为9600并点 击OK,在弹出的窗口中直至出现Done executing startup script 'script.txt' 的信息,表明质谱启动完毕);6.双击桌面上的Masslynx V4.1 图标,打开Masslynx 软件,等待在Masslynx 的主窗口状态栏中部偏右的位置出现“Not Scanning”的信息;7.打开MS Console窗口,左边栏依次选中/Synapt G2 QTOF/Intellistart,在右 侧窗口中点击operate快捷图标;注意:在点击operate 图标后应该能听到外置真空泵发出很大的噪音,随后声音逐渐变小;8.打开MS tune 窗口,单击氩气的控制开关,使氩气关闭。然后等待直至 右下角红色的方块变为绿色,表明仪器可以工作了; 注意:通常这个过程需要7-8个小时,长时间不用则需要两天左右。也可以从MS tune/view/vacuum中观察真空度得变化,当TOF位置的真空度小1.2×10-6时,右下角红色方块会变成绿色;9.开机结束。二、每天开始试验流程1.打开MS tune窗口,点击右下角operate 图标,右侧方块变绿色后仪器可以 使用;2.在Inlet Method窗口中编辑液相方法并保存;3.在Inlet Method窗口中,使用Start up System功能平衡液相系统;4.在MS tune窗口中设置质谱的参数,主要是MS tune/ESI 界面中各种电压,气体和温度;5.在MS Console\Synapt G2\Intellistart窗口中完成:Create calibration和Lockspray Setup两项内容,结果均应为Pass;注意:(1)Create Calibration,温度恒定的前提下一个星期做一次,若温度波动 大,则测试样品前做一次;(2)Lock Spray Source Setup,2-3天校一次;(3)Detector Setup第一年一个月做一次,2500-4000V,以保证灵敏度,若 3-4个月未做,仪器会自动提醒并强制进行Detector Setup;(4)Detector Setup的Positive与Negative都是单独做,不能同时做。6.在MS method窗口中编辑质谱方法,确保调用最新的Lockspray方法和 Enable MS event;7.在Masslynx的主界面上编辑进样序列,确保Sample name,MS method,Inlet method,Bottle position and Injection volume 都选择相应的参数;8.点击进样按钮开始进样。三、重启仪器过程1.关闭所有的软件,并重启电脑,直至显示windows桌面;2.在质谱背面板右侧位置有一个银色的可以上下搬动的按钮,将其搬至向 下的位置(向上的位置为Auto,向下的位置为Pump Override,在搬动过 程中,需要将按钮向外稍微用力才可以上下搬动);3.从上向下依次关闭质谱背面板右侧除了Vacuum位置的其它三个黑色的 开关;4.等待15分钟;5.从下向上依次将质谱背面板右侧除了Vacuum 位置的其它三个黑色的开 关搬到向上的位置;6.等待5分钟(或是进入桌面的hyperterminal 文件夹,双击其中的的hypertrm 图标,在name处输入epc并点击OK,接着在弹出的窗口中在Connect using 中选择com1并点击OK,在弹出的窗口中将Bits per second设为9600并点 击OK,在弹出的窗口中直至出现Done executing startup script 'script.txt' 的信息,表明质谱启动完毕);7.双击桌面上的Masslynx V4.1 图标,打开Masslynx 软件,等待在Masslynx 的主窗口状态栏中部偏右的位置出现“Not Scanning”的信息;8.打开MS tune 窗口,单击氩气的控制开关,使氩气关闭。看到MS tune左 下角出现“Pump Override Activated”信息后,找到质谱背面板右侧位置 的一个银色的可以上下搬动的按钮,将其搬至向上的位置。这时“Pump Override Activated”信息将会消失;9.点击MS tune窗口右下角的operate按钮,看到右下角红色方块变成绿色后 完成;10. 重启完毕。四、关机过程1.打开MS tune窗口,点击Vacuum/Vent,在弹出的对话框中选择Yes;2.等待约5 分钟(在这个过程中应该能听到分子泵降速的声音,也可以观察MStune\View\Vacuum, 六个Turbo speed 会逐渐下降,直至六个分子泵 的转速均降至5以下,表明真空已经关闭);3.关闭所有软件和电脑;注意关闭软件顺序:先关闭子程序,最后关主软件程序;4.关闭液相所有模块的电源;5.关闭质谱的电源(在质谱背面板右侧位置有四个黑色的可以上下搬动的 开关,按照从上向下的顺序依次将这四个开关搬到向下的位置);6.关闭氮气发生器的电源或是液氮罐的开关;7.关闭氩气减压阀(如果是HDMS 还需要关闭氦气减压阀);8.关机结束。五、日常维护及注意事项1.流动相流动相:(1)水相:2-3天换一次;(2)有机相:一般不用换;2.更换缓冲液后,需要重新校准体积;3.更换进样针后,需要重新校准针体积、针坐标并清洗泵头;4.样品盘更换:更换后一定要用软件设定好并传送至仪器硬件,以免进样出错:48孔2mL盘,蓝色;96孔2mL盘,白色;5.液相方法相关快捷键:方法编辑完毕并保存后,需要点击快捷栏最后一个“Load”,将方法的初始条件传送至液相,以便后续运行进样程序;6.注意监察使用不同流动相(有机相及是否加缓冲液等)柱压的正常范围,以 便今后判断问题之所在;7.更换新柱子:断开所有(任何检测器);用纯甲醇或纯乙腈冲柱子1小时以上(试剂流向Waste);8.编辑液相方法:未知样品可以先跑一个大梯度:90%水至100%乙腈,然后再调整;9. Standby:(1)3-4天不用:Source Standby;(2)一星期不用:Instrument Standby;10.MS Tune在3-4天不用或一星期不用时,将Source温度降至60℃或80℃;11.清洗离子源:(1)先降温,再清洗;(2)若不是很脏,则50%甲醇+50%水清洗;(3)若很脏,清洗试剂依次为:45%甲醇+45%水+10%甲酸;100%水;100%甲醇;d. N2吹干;12.样品制备:(1)用流动相溶样;(2)用0.22μm样品过滤膜过滤;(3)放入Waters UPLC适用的样品瓶;13.色谱柱保存:(1)在室温条件下,如果超过四天不使用反相ACQUITY UPLC色谱柱 及ACQUITY UPLC BEH Amide色谱柱,请将柱子保存在100%乙腈 中;(2)对于高温条件下的应用,在工作结束后即快速将色谱柱保存在100%乙腈 中以延长色谱柱的使用寿命;(3)不要将色谱柱保存在缓冲盐流动相条件下;(4)如果流动相中含有缓冲盐,先用10倍柱体积的液相色谱级水(大比例)冲洗色谱柱,之后用100%乙腈替换保存。如果没有进行这一中间步骤直接换成100%乙 腈将会导致缓冲盐析出;14.在使用时应当严格按要求操作,注意保养维护,每次使用、维护完毕后,应 当详细填写使用记录。
操作维护
2024.09.13
什么是UPLC?和HPLC有什么区别?
UPLC:超高效液相色谱(Ultra Performance Liquid Chromatography)色谱理论认为提高色谱柱的效能(efficiency)就能增加仪器的解析度(resolution),而运用粒径低于2μm的小颗粒无疑是增加效能的好方法。但减小固定相的粒度以增加色谱柱效能一直的色谱仪器科学的瓶颈,因为小颗粒不仅要求系统能承受高于目前极限压力(比如9000psi),需要更小的系统体积(死体积),并且需要能适应可能只有几秒峰宽的高速检测器。UHPLC:超高效液相色谱 (Ultra-High Performance Liquid Chromatography)特点是工作压力超过6000 psi或工作温度超过环境温度的应用。由于 UHPLC 应用中使用的硬件通常可以承受 9000 psi或更高的系统压力,因此色谱工作人员可以使用由更高级固相(其颗粒远远小于传统的5 μm直径硅胶)填充的色谱柱。采用颗粒更小的固相不仅可以实现更高的分辨率,同时还能缩短整体分析时间。HPLC:高效液相色谱(High Performance Liquid Chromatography)又称“高压液相色谱”、“高速液相色谱”等。高效液相色谱是色谱法的一个重要分支,以液体为流动相,采用高压输液系统,将具有不同极性的单一溶剂或不同比例的混合溶剂、缓冲液等流动相泵入装有固定相的色谱柱,在柱内各成分被分离后,进入检测器进行检测,从而实现对试样的分析。该方法已成为化学、医学、工业、农学、商检和法检等学科领域中重要的分离分析技术。UPLC和HPLC的区别与传统的高效液相色谱(HPLC)相比,UPLC具有高分离度(ultra resolution)、高速度(ultra speed)、高灵敏度(sensitivity)等优势。在全面提升HPLC的速度、灵敏度和分离度诸品质的同时,保留其原有的实用性及原理。其最显著的优势是可以缩短分析时间,提高工作效率。使用UPLC确实能明显缩短分析时间,提高效率(如某有关物质分析方法,使用HPLC运行一针是75分钟,UPLC完全可以在10分钟内搞定),分析效率提高将近7.5倍。当然了,分析效率提高这么多,其配套设备肯定也不是闹着玩的。UPLC需要小颗粒杂化填料(1.7um)的色谱柱、更高耐压(达15000Psi)、低系统体积的输液单元。学会正确维护UPLC,避免被领导骂。溶液的制备很关键在色谱系统中,溶液是一个更重要的部分,那么UPLC中溶液的制备应该是怎样的呢?样品溶液的制备样品的制备同样是过滤和离心两种方法。过滤:根据样品溶液的极性,选择不同材质的0.22um滤膜过滤。滤膜的选择,要进行分析方法确证,滤膜的相容性实验。此处强调一下,必须是0.22um,千万不要用错。离心:采用高速离心的方式(大于10000转/分钟)。离心的方法一般适用于过滤较困难的溶液,为了保护UPLC的系统,离心完毕后建议再次进行过滤。流动相的制备所用有机相应是进口的色谱级别。使用的水应为超纯水,MILLI-Q纯水机生产的即可。配制缓冲盐溶液应该有效期的规定,根据各实验室SOP规定。所有的流动相用前必须使用0.22um的微孔滤膜过滤。有很多同仁在平衡色谱柱时,因为使用的是甲醇/水或是乙腈/水系统,因为不涉及到缓冲盐溶液,经常把过滤这一步省略,再次提醒大家:UPLC系统使用的所有流动相均必须经过0.22um的微孔滤膜过滤。色谱柱的使用若柱效不佳,将会浪费样品分析时间,问题排查时间,更是浪费宝贵样品。所以色谱柱的使用操作的规范性,直接决定UPLC的分析效率与数据可靠性。首先,应与色谱柱的供应商沟通,充分了解色谱柱的性能,如反相柱、正相柱、氰基柱、亲水柱、离子交换柱等。再次,建立色谱柱的管理SOP,在SOP中规定色谱柱的登记、启用、使用及报废记录,便于色谱柱整个生命周期的管理。色谱柱的启用色谱柱包装开启后一定要阅读说明书,关注说明书中的注意事项,如pH的适用范围、流动相中能否采用水、平衡时的流速,保留溶剂等。对于正相色谱柱来说,最重点的是注意初始流速一定要小,一般0.2ml/min。反相柱就比较麻烦一点了,先用小流速0.2ml/min的甲醇冲洗2小时,再用10%甲醇冲洗2小时,最后过渡到检品的流动相,流速由低逐步增加到目标流速。柱子开始使用前,必须确认系统适用性测试是否满足要求,主要关注理论板数、分离度、拖尾因子等关键分离参数,验收合格后才能使用。色谱柱的清洗和保存正相色谱柱进样后一般无需刻意清洗,但是需要保存时,必须按照说明书要求选择溶剂,以免长时间引起固定相干涸。反相色谱柱清洗过程:高水相等度洗脱保证缓冲盐冲洗干净后,梯度洗脱的方式过渡到纯有机相,等度洗脱10~30柱体积,柱温可适当提高2~5度,方法运行完及时关闭柱温。对于亲水作用色谱柱:最后保存尽量避免使用纯有机相,应包含少量的水,比如95%的乙腈。色谱柱的使用使用色谱柱,应轻拿轻放,安装零死体积。切忌由大流速变化引起的压力变化对色谱柱造成机械损伤,应使用逐渐提高流速的方法达到目标流速。建立色谱柱的使用记录,记录中体现出理论板数、分离度拖尾因子、柱压、保留时间、流动相体系、保存溶剂等信息,一旦发现参数异常,以便展开调查,避免偏差发生。色谱柱使用过程中,应关注其柱压、柱效,使用完毕后填写“色谱使用记录”。色谱柱最好是专用,带保护柱。并且使用过缓冲盐的色谱柱最好不要用于新项目的方法开发。低紫外区的检测,为了避免“鬼峰”的出现,可以使用捕集柱,色谱柱使用完毕后一定要按SOP及时清洗。对于鬼峰捕集柱的使用,很多科研单位觉得不可行,不知道如何在标准中进行表达。其实在方法建立过程中,如果鬼峰无法避免,可以在“发展报告”中说明使用鬼峰捕集柱的理由,并在标准中如实描述,以便与厂家或是QC进行方法转移。有关亲水性色谱柱,小编也有些提议:以HILIK色谱柱为例,使用更少或是较弱的极性溶剂可以增加极性化合物的保留。样品溶解的溶液尽可能接近流动相条件的初始条件,然而,极性大的分析物经常在有机溶液中存在溶解度较低的现象,可以先用水溶解样品,再用乙腈/水溶液进行稀释,需要平衡溶解度和峰形之间的关系,根据化合物性质,具体情况具体分析。色谱柱的报废要素1.色谱柱堵塞,压力升高1000psi。2.色谱柱污染出现鬼峰、噪音增加、检测限增大时。3.填料塌陷或污染引起色谱图前沿、拖尾、分叉时。4.理论板数、分离度、拖尾因子按各检品质量标准规定执行,未规定的按各国药典通则规定执行,不符合上述规定时。UPLC使用常见问题液相基线噪音干扰如果出现基线噪音较大的情况,首先应该排除检测器的问题。排查流动相问题时,需要重点考虑流动相的组成及检测波长是否发生了改变?一定要确定您所用仪器上最后使用的流动相是什么?为了避免这个问题,在接上个人用仪器之前,要连接两通,用超纯水将仪器管路全部清洗一遍。此外还需要考虑流动相的互溶性的问题。不相混溶的溶剂不能用作梯度洗脱的流动相。有些溶剂在一定比例内混溶,超出范围后就不互溶,使用时更要引起注意。当有机溶剂和缓冲液混合时,还可能析出盐的晶体,尤其使用磷酸盐时需特别小心。梯度洗脱所用的溶剂纯度要求更高,为了保证良好的重现性。进行样品分析前必须进行空白梯度洗脱,以辩证溶剂杂质峰。分析弱酸性样品时,通常在流动相中加入少量弱酸,常用50mmol/L磷酸盐缓冲液和1%醋酸溶液;分析弱碱样品时,通常在流动相中加入少量弱碱,常用50mmol/L磷酸盐缓冲液和30mmol/L三乙胺溶液。流动相中加入有机胺可以减弱弱碱性样品和残余硅醇基的强相互作用,减轻或消除峰拖尾现象。所以在此使用的有机胺也成为减尾剂。要确保所使用流动相不改变填料的任何性质。低交联度的离子交换树脂和排阻色谱填料有时遇到某些有机相会溶胀或收缩,从而改变色谱柱填床的性质。碱性流动相不能用于硅胶柱系统。酸性流动相不能用于氧化铝、氧化镁等吸附剂的柱系统。即使经过0.22um滤膜过滤,在保质期时间内,有的流动相仍会存在长菌、沉淀、结晶等现象。流动相不干净,进入液相系统是非常危险的,尤其是缓冲盐。在此有一个小窍门:用激光笔测试,不干净的缓冲盐溶液在激光笔照射时,里面会看到一条红线。最后,还有滤膜的相容性问题,有的滤膜可以引起基线及噪音的波动,遇到这种情况,需要进行滤膜筛选。液相压力波动最常见原因是泵内有气泡。其他还有:溶剂进口过滤芯堵塞(最好更换新的过滤芯,一旦长菌,是不可逆的)、未充分混匀(尤其是有机相和水相相差比例悬殊时)、溶剂未脱气、泵的密封垫老化、出口单向阀实效、主动阀失效等。液相压力过低包含原因首先想到的是连接管路泄露或其他设备不密封,如泵头密封垫。还会存在溶剂进口过滤芯堵塞,溶剂无法通过、溶剂或流速改变、主/被动阀失灵、四元比例阀失灵、单向出口阀失灵、色谱柱固定相流失等原因。液相压力过高包含原因这个原因各位同仁应该都很熟悉,如:色谱柱污染、柱子进口过滤芯被污染、PURGE阀过滤芯污染、连接管路堵塞、进样器旋转密封阀被堵塞或进样针或针座被堵塞等。系统优化时所需过度溶剂1.反相和正相相互转换:所用溶剂为异丙醇,原因:排除系统中空气的最好溶剂。2.使用缓冲液后冲洗系统:所用溶剂为二次蒸馏水,原因:再溶解缓冲液结晶的最好溶剂。3.更换溶剂后:所用溶剂为二次蒸馏水,原因:再溶解缓冲液结晶的最好溶剂。选择UPLC 还是HPLC?某网友:“由于所在实验室即将添置一台新质谱,质谱已经选好了,但是在液相的选择上很是犹豫,不知是否该买一台UPLC。因为经常是一次分析几百个样品,高速液相的速度会快一些。但是,生物样品的前处理要求也相应提高。而且价格也比较贵。是否需要买UPLC?还是买HPLC?想了解一下大家的使用经验和看法。”相信这是很多实验室小伙伴会面临的选择,那么到底该从哪些方面来衡量仪器的选型?有人说,能用HPLC就用,多数情况下,HPLC都能hold住。UPLC肯定是大势所趋。就像很多人所说的一样,UPLC就像是鸦片,用过了就上瘾摆脱不了。这个说法虽然极端,但是话糙理不糙,你觉得有理吗?网友支招网友A:如你所说,使用UPLC肯定能提高你分析的速度,但是不知道目前你选好的质谱是什么型号的?这里存在一个质谱工作站能否兼容你的液相色谱的问题,所以还请考虑仔细。个人觉得UPLC类的快速液相是大势所趋。网友B:个人感觉UPLC不错,最直观的感觉是分析时间大大缩短,这也是UPLC鼓吹的一点。但UPLC对流动相,色谱柱,样品前处理,质谱接口,数据采集系统都提出了更严格的要求,同时带来的液氮、乙腈等耗材的使用量下降,这个是很明显的。至于所用的试剂、耗材等等比HPLC高级多少,我倒没看出来。无非是要求过下0.22μm的膜。个人认为短期内还无法完全替代普通LC。普通液相采用细径色谱柱是目前最成熟和经济的LC-MS方案。网友C: UPLC在分析速度、分离度等方面确实有优势,但对样品的前处理、试剂等提出了更高的要求,样品分析成本也高了。我们知道,影响分析速度快慢的主要步骤是样本的前处理,而仪器分析速度的快慢不是主要因素,现在仪器都是自动进样加24小时开机,测定一个样品多花点时间能有多大影响,很多人那UPLC分析速度快来说事是不合适的。我的行业测定的是食品样品,从我的经验来看,我更喜欢用普通的HPLC。网友D:我是做中药成分的,个人觉得还是uplc更好一些。因为是与质谱联用,日常分析中的样品如果成分比较复杂的话,普通液相的色谱条件就不太好找,必然会经常遇到需要加酸、碱或缓冲盐的情况,尤其是缓冲盐的选择受质谱的限制较大。而uplc由于柱效高,分离效果要比普通液相高的多,在很多时候普通液相上加缓冲盐也很难分离的成分,在uplc上什么都不用加就可以分开,而且效果很好。所以觉得uplc在联用时更方便一些。网友E:个人认为,如果追求分析速度的话可以选用UPLC,如果考虑的是分析成本的话,还是用HPLC。如果样品量大,分离简单,则可以配UPLC。UPLC配质谱的好处主要在于处理量大,不要把希望寄托在它分离效果好上。一种又快又好又稳定的仪器太难找了。网友F:高通量生物分析如果样品量大或食品类样品比较多,建议你不要配UPLC,否则会后悔的。UPLC一般适用于研究性质的实验或样品基质比较干净的实验。网友G:各人觉得你要是做生物样品或者医药方面的UPLC还是有优势的,但是你如果是做残留分析,比如农残,兽残什么的就买HPLC就好,UPLC的确是快,但是食品蔬菜什么的基质比较复杂的你就甭想分离的很好,分离效果差很多的。网友H:个人意见,如果做生物样品分析,而且每天分析样品量比较大,不建议使用UPLC。UPLC的优点是分离度高,峰形尖锐。但是其填料粒径太小,在高通量生物分析时很容易堵柱子(UPLC柱价格比较贵),使用寿命比HPLC柱少很多。另外其峰形尖锐,与扫描型质谱联用会降低分析物的灵敏度。网友I:如果条件允许的话还是买UPLC吧,我们也是样品量很大,如果用hplc可能的跑上一天也不一定打完全部样品,但是用uplc三个小时左右就能打35-40针,还能让仪器休息一下,好好的冲洗系统,如果是用hplc的话估计向我们这么大的样品量,仪器早晚的罢工。再有就是用uplc同时降低了开发方法的时间,提高了工作效率,同时还能省下不少的溶剂,正如waters的广告所说的,在乙腈比较昂贵的时候确实能省不少钱,我们500ml的乙腈能走大约上百针样品(梯度洗脱)。主要是效率高,也提高了灵敏度,峰形好,当然仪器也贵些,好东西,贵点也值得,等你用熟了再用hplc,你就会感觉很不爽,原因我就不说了!这么多网友支招,大家是否在面对选择UPLC还是HPLC时,不再犹豫了呢,其实,小编认为,选择哪种仪器,最主要还是要看需求和预算,总的来说,HPLC相比UPLC更加经济,不管是仪器本身的价格,还是使用耗材的价格,而且能够满足多数实验室的一般检测需求。至于UPLC其使用体验的确好过HPLC,关于使用要求来说,其实没那么多问题,只要养成良好的使用维护习惯,也没啥大不了。套用一句话:UPLC可以干HPLC的活儿,但是反过来咋办?
操作维护
2024.09.13
waters UPLC HPLC色谱系统管理使用教程
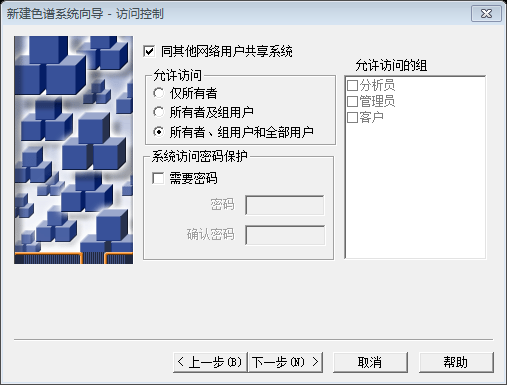
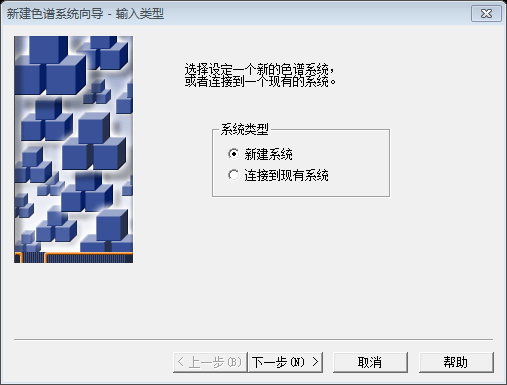
1、新建色谱系统根据仪器所需的控制连接类型(Waters busLAC/E 卡、8 口串行卡、网络接口卡 (NIC)、网络交换机或通讯端口)确定仪器的连接方式。Empower 通过连接检测到仪器时,便将该仪器输入 Empower 节点属性的“仪器”选项卡,并将其用作色谱系统的一个组件。配置色谱仪器的步骤为:在下图1左侧“Empower 3配置”点击其项下的“系统”,在右侧空白处单击鼠标右键。点击弹出窗口中的“新建(N)”,即弹出“新建色谱系统向导”窗口(图2)。2、在图2中选择系统类型,点击“下一步”即弹出“选择系统”窗口(如图3所示)。在“选择系统”窗口中“可用仪器”一栏双击需要配置的仪器型号,则在“新系统”中显示已添加的仪器。选择仪器完毕后点击“下一步”弹出“访问控制”窗口如图4所示。3、在“访问控制”窗口中设置“允许访问”选项以及“允许访问的组”,必要时可勾选“系统访问密码保护”。点击“下一步”,即弹出“选择名称”窗口,如图 5所示。4、在“选择名称”窗口输入“系统名”,必要时勾选“在线”或输入“系统注释”。点击“完成”则此色谱系统建立。2、删除色谱系统删除色谱系统的步骤为:在下图6左侧“Empower 3配置”点击其项下的“系统”,在右侧选中需要删除色谱系统(例如Acchrom S6000),然后点击右键,点击右键菜单里的“删除”,即 弹出“确认删除”窗口(图7所示),点击“是”即弹出“删除色谱系统”窗口(如图8所示)。在色谱系统中选择“删除全部”或“删除”后即可删除此色谱系统。注意:“删除全部”是指从色谱软件数据库、工作站和数据库上的所有用户帐户中删除选定色谱系统。此物理系统不再进行配置时,请使用此选项。“删除”是指从此数据库上的所有用户帐号中删除所选色谱系统,但该系统仍配置在采集服务器上。工作站继续运行该系统,可于稍后重新与其连接。当您不再需要该系统而其他用户仍需要它时,请使用此选项3、修改色谱系统属性及色谱系统的访问权创建色谱系统时,可以定义对系统的以下三种类型的用户访问权:选择是否允许网络用户访问色谱系统;同其他用户共享色谱系统;要求用户输入密码才能访问色谱系统。对已建立的色谱系统也可以随时查看和修改这些权限。修改色谱系统属性及访问权限的步骤为:在下图9所示的“Empower 3配置”项下的“系统”一栏选择需要修改的色谱系统,单击鼠标右键并点击“系统属性”。在弹出的“色谱系统属性”窗口(如图10所示)中对此色谱系统进行修改,如访问权等。
参数原理
2024.09.13
一文读懂液相色谱(HPLC)
在色谱法中存在两相,一相是固定不动的,我们把它叫做固定相;另一相则不断流过固定相,我们把它叫做流动相。色谱法的分离原理就是利用待分离的各种物质在两相中的分配系数、吸附能力等亲和能力的不同来进行分离的。使用外力使含有样品的流动相(气体、液体)通过一固定于柱中或平板上、与流动相互不相溶的固定相表面。当流动相中携带的混合物流经固定相时,混合物中的各组分与固定相发生相互作用。由于混合物中各组分在性质和结构上的差异,与固定相之间产生的作用力的大小、强弱不同,随着流动相的移动,混合物在两相间经过反复多次的分配平衡,使得各组分被固定相保留的时间不同,从而按一定次序由固定相中先后流出。与适当的柱后检测方法结合,实现混合物中各组分的分离与检测。应用一、在食品研究中的分析应用1.食品中的天然成分碳水化合物类脂化合物、甘油三酸酯、胆固醇脂肪酸和有机酸蛋白、肽、氨基酸2.食品添加剂酸味剂、甜味剂、香精、乳化剂抗氧化剂、防腐剂颜料和染料(色素〕维生素3.污染物霉菌(黄曲霉毒素)农药和兽药残留多环芳烃(PAHS)和亚硝酸二、在兽药研究中分析应用1.在医药研究中分析应用药物分析有USP、BP、CP等标准常用药物研究中的应用:解热镇痛药、镇静药、安定药、心血管药、磺胺类消炎药等。甾体药物研究中的应用:肾上腺皮质激素、雄性激素、雌性激素和孕激素等。抗菌素类药物研究中的应用:青霉素、头孢菌素、庆大毒素、四环素、氯霉素、诺氟沙星等。中草药研究中的应用:生物碱、甙类(皂甙、强心甙、黄酮甙等)、萜类手性药物研究中的应用:光学异构体的拆分(如解毒剂D-青霉胺毒性小,L-异构体毒性很强)医疗药物的检测、新药研究、药物代谢、药代动力学研究。三、在生物化学和生物工程中的应用1.氨基酸、多肽和蛋白质的分析研究核碱、核苷、核苷酸和核酸的分析研究生物胺的分析研究(儿茶酚胺类)在精细化工分析中的应用1.醇、醛和酮、醚的分离分析2.酸和酯的分离分析表面活性剂的分析聚合物的分析研究3.药物、农药、染料、炸药等工业产品在无机离子分析中应用4.饮用水、酸雨、土壤中阴离子和阳离子分析四、在公安、刑警破案工作需要分析等1.在环境污染分析中的应用2.废气、废水、废渣中多环芳烃、多氯联苯、农药残留酚类和胺类的检测液相色谱图相关术语色谱峰-Peak1.色谱柱流出组分通过检测器时产生的响应信号的微分曲线峰底-Peak Base峰的起点与终点之间连接的直线峰高 - Peak Height峰最大值到峰底的距离峰宽-Peak Width在峰两侧拐点处所作切线与峰底相交两点之间的距离半(高)峰宽-Peak Width at Half Height通过峰高的中点作平行于峰底的直线,其与峰两侧相交两点之间的距离峰面积-Peak Area峰与峰底之间的面积,又称响应值标准偏差;σ-Standard Error0.607倍峰高处所对应峰宽的一半拖尾峰 - Tailing Peak后沿较前沿平缓的不对称峰前伸峰- Leading Peak前沿较后沿平缓的不对称峰鬼峰- Ghost Peak并非由试样所产生的峰;亦称假峰基线-Baseline在正常操作条件下,仅由流动相所产生的响应信号的曲线基线飘移-Baseline Drift基线随时间定向的缓慢变化基线噪声:N-Baseline Noise由各种因素所引起的基线波动谱带扩展- Band Broadening由于纵向扩散,传质阻力等因素的影响,使组分在色谱柱内移动过程中谱带宽度增加的现象死时间to-Dead time不被固定相滞留的组分,从进样到出现峰最大值所需的时间保留时间,tR-Retention time组分从进样到出现峰最大值所需的时间死体积,Vo-Dead volume不被固定相滞留的组分,从进样到出现峰最大值所需的流动相体积保留体积,VR-Retention volume组分从进样到出现峰最大值所需的流动相体积
参数原理
2024.09.06
安捷伦和赛默飞世尔的离心机,哪家比较好?
知名品牌有艾本德,赛默飞,贝克曼,日立,sigma离心机大致分为台式微量,台式高速,落地高速,落地大容量。艾本德只有台式机。艾本德优势,皮实,耐用缺点,参数较低,只能满足一般生物实验需求,艾本德似乎也不打走高端,怎么说,艾本德优点像日本车,好用,耐用,维护成本低。赛默飞具备全系列产品。赛默飞很有传承,集索福,贺立式,捷安等技术优势于一身。优势在大容量冷冻离心机,血站和生物制药占有绝对比重,最近推出的落地高速机反响也不错。在中国市场,赛默飞的装机量应该在前两名。赛默飞的缺点是集团太大,全球采购后品质有时候不稳定,一般会出现在台式机上。赛默飞有点像宝马车,很多性能的领导者,比如碳纤维转头,转头自锁,16L超大容量离心机。贝克曼具备全系列产品。品牌很有传承,现在在丹纳赫集团。优势产品是超速离心机,落地高速离心机,高速机现场面临赛默飞的挑战,不容乐观。他的台式机除了少数12,15之外都是sigma代工,质量么,也就那样。贝克曼一直以来都是超速离心机的技术领导者,这也是他们的优势,落地高速机现在没啥优势,买他台式机就是买sigma。贝克曼和索福(现在的赛默飞)书写了离心机的历史。日立,具备所有机型。头几年跟贝克曼拼超速离心机拼的很厉害,这几年比较被动,因为它们不是日立直销,所以在基因技术应用支持上太少。至于台式机,我每次看到都要合影,因为太少了。日立虽然再中国销量不行,服务也不太好,产品参数也不出彩,但这些不耽误他是个好品牌。因为在日本人家销量大的很。Sigma只有台式机。70年代被贺立式收购,过了专利期有开门营业。乡镇家族企业,部分机器在上海生产。在欧洲其实不如海蒂诗和贺墨,但是名字很讨巧,不信你问外行sigma,他们都觉得很高大尚。它们并不能一言蔽之,每个品牌也有优秀的机器和垃圾的机器。比如,艾本德,5424很优秀,可是5804和5810参数就太低了。贝克曼j30比j26参数好,但他们的销售只卖j26赛默飞的primo就是笑话日立么……是在装机太少sigma在欧洲市场4系列还有的卖,在中国却是1系列和3系列卖的好,阿弥陀佛。另外,工业品,都会出问题,做为使用者,你看到坏了就是这个品牌100%有问题,而我看的是整合行业。
参数原理
2024.09.06
赛默飞高效液相色谱仪HPLC的使用说明
1. 开机(软件):双击“控制器”,点击“启动仪器控制”,待仪器显示“运行空闲”,双击“变色龙软件7”进入色谱工作站,工作站左上角“模块状态”显示“Connected”,表示连接成功。2. 排气:打开输液泵的盖子,找到输液泵的排气阀,拧松排气阀(逆时针)拧松一圈半到两圈,将A流动比例设为100%,泵流速设为3ml/min(具体自己定),点击冲洗按钮,在排气阀打开的情况下忽略警告执行。重复上述操作,分别进行b、c、d流路的排气操作,一般排气60s。在此期间观察各流路软管内是否有气泡,确保气泡完全排除。结束后再次点击冲洗按钮,停止排气,拧紧排气阀。(此处要注意,在拧紧排气阀之前,一定要将流速降低,确保压力在正常范围小于150bar)在加样前,选择自动进样器选项,依次进行灌注注射器、清洗缓冲环、外部清洗针。3 创建仪器方法:点击创建 → 选择仪器方法 → 设定运行时间() → 取消选择所有通道 → 点击下一步 → 编写各瓶溶剂名称 → 下一步 → 删除平衡阶段 → 编写仪器方法(每一个时间不代表区间,仅代表着该时间点的流速以及各相比例) → 下一步 → 采用默认的进样针参数 → 下一步 → 采用默认的进样模式 → 下一步 → 进行温度控制(具体自己设,本实验条件为30℃) → 下一步 → 设置波长信号 → 直至完成,在方法界面里,左上角保存改仪器方法。4. 平衡基线:流速设为1ml/min,有机相:流动相比例设置为(自己设),点击马达,启动输液泵;点击UV选项,设置波长,点击紫外灯,点灯成功会有打钩。 有机相与流动相比例不断进行调整,直到进样需要的条件,本实验从100%有机相到20%有机相。5 处理方法的创建:选择创建菜单下的处理方法,选择基本定量 → 下一步 → 命名处理方法并保存 → 打开 → 完成。 采用仪器的默认数据处理方法。6 样品检测:序列创建:创建菜单 → 序列 → 编写相关信息 → 下一步 → 浏览 → 选择建好的仪器方法和处理方法 → 下一步直至完成,命名序列并完成。待到基线平衡后,在数据点击开始运行。可以在仪器操作界面看到当前情况。(此处要注意队列中前面的队列已完成)7 清洗柱子(清洗色谱仪先水洗,后醇洗,柱子需要保存在100%有机相中,分为快洗和慢洗,此处描写快洗方法,需要时刻注意压力值):快洗:先将调到100%醇:0%水 → 0%醇:100%水 → 100%醇0%水进行柱子保存。(打开UV界面的紫外灯,再打开位于界面最上方的基线监视)慢洗:创建仪器方法同上,运行时间尽可能大,在编写仪器方法时,可尝试如下编写。(0min时各相比例应与HPLC工作时的比例相同;需确保各相试剂充足;具体流速需根据A:B=1:1时进行调整,此比例下柱压最大)
参数原理
2024.09.06
为什么安捷伦的气相色谱会在国内实验室里处于一种统治状态?
分析仪器的灵敏度稳定性主要取决于做什么,怎么做。而A家的产品设计思路明显广于其他各厂 (对需求精度的用户,有还说的过去的精度;对长时间使用/样品污染严重的用户,有良好的耐用性;对操作人员水平不足的用户,有很好的人机对话)核心的竞争力-应用,A家有强大的应用团队支持市场销售,实践经验基本涵盖了所有使用分析仪器的行业。用户在提出仪器需求时也当然会选择有成熟应用支持的厂家。同时也如其他答友所说,专业的应用开发团队能够快速的相应各种标准并参与新标准制定因为产品的高附加值,Agilent有充足的资源吸引并组建一支汇聚中国乃至世界行业精英的销售、售后服务团队。市场队伍水平高+ 稳定的仪器品质+完善的应用方案就相当于一支强力军队+后勤支援给力+尖端武器,体现出的竞争力自然更强中国市场的特殊性,A家进入中国市场时间远早于其他各厂,且在刚进入时就投入了大量资源进行推广宣传,抢占到了市场先机,用户最先开始接触的就是A家仪器,使用的就是A家工作软件,形成了长久的信任。其实在北美市场,PE的占有率是高于A家的安捷伦的优势并不是一招鲜,而是富有远见的R&D,质量过硬的生产质控,跟进时代的应用部门,汇聚精英的营销部门,不遗余力的市场宣传部门共同造就了今日的一家独大。究其根本就在于——底蕴1、安捷伦的气相色谱仪和气相色谱柱种类丰富,特别是气相色谱柱种类较全(第二列为安捷伦气相色谱柱的产品)。2、安捷伦的仪器和气相色谱柱性价比是真的可以,中等偏上一点点。3、安捷伦的推广很成功,就是很贵的手性气相柱,他们也会舍得本让你免费试用,试用后能分开你的化合物,你再购买。4、安捷伦可以做得到开发很多案例(解决方案),这个需要人力物力去做实验室,如果有现成的解决方案,为何不买现成能解决问题的产品呢,5、安捷伦气相色谱仪的软件操作起来不复杂,很实用,就是新手容易上路的那种。5、安捷伦的销售专业性匹配性比较强,销售一般有分析背景,这样更能和客户有效沟通,解决客户问题,就连安捷伦代理商的销售也如此。6、安捷伦的体量说大不小,但安捷伦生命科学绝对占它的主体业务,不像有些公司虽然世界500强内,但气相这块不占产品主要。7、安捷伦乐意与高校合作,sci文献上,仪器和色谱柱很多被引用到文献。
参数原理
2024.09.06
安捷伦1200型液相色谱仪使用及维护保养标准操作规程
1 目的本SOP规定了安捷伦1200型液相色谱仪的操作、维护清洁及注意事项,以达到操作者正确操作及维护的目的。2 范围本SOP适用安捷伦1200型液相色谱仪的操作、维护清洁及注意事项。3 职责仪器操作人员执行本SOP。4 内容4.1 仪器描述安捷伦1200型液相色谱仪由安捷伦科技有限公司生产,主要由工作站、高效液相色谱仪单元泵(G1310A)、手动进样器(7725i)、可变波长紫外检测器(G1314B)等部件组成。4.2 操作方法4.2.1 开机准备:①启动计算机:打开计算机电源,登陆windows操作系统。②启动液相:打开Agilent 1200各模块电源。待Agilent 1200各模块自检完成后(各模块右上角指示灯为黄色或者无色),双击“仪器1联机”图标,或者“开始->所有程序->Agilent Chemstation->仪器1联机”。③开启工作站:工作站打开,点击“方法和运行控制”或者在“视图”中选择“方法和运行控制”。打开仪器控制视图:选择“视图->系统视图”,即可显示仪器控制视图,选择“视图->样品视图”,即可显示样品信息视图。模块右上角状态灯颜色说明工作站图形颜色说明指示灯颜色情况说明指示灯颜色情况说明无色未开电源或模块准备就绪绿色模块准备就绪黄色模块未准备就绪黄色模块未准备就绪绿色正在进样分析蓝色正在进样分析红色模块出错红色出错或者不能联机所有模块红色仪器有漏液灰色此模块没启用④配置流动相:将流动相装入溶剂瓶中。设置溶剂瓶参数,在溶剂瓶图形上单击鼠标左键,点击“溶剂瓶填充量”设置溶剂瓶中流动相实际体积。⑤冲洗流动相管路:旋开溶液排空阀,左键单击泵图标,点击“设置泵”,设置“流速”为5ml/min,冲洗通道即可。⑥开启模块:单击每个模块右下角的按钮,可以单独启动模块、或者单击检测器按钮灯未点亮,检测器图形为黄色或者单击“启动”按钮,启动全部模块,检测器灯也将点亮。⑦监视基线:点击按钮或者“视图->在线信号”打开“在线图谱”。点击“改变”按钮,选择“可选信号”中需要监视的信号,“添加”到“选定信号中”。调整“窗口”中“X周范围”,如需要画“0”点基线,请选择“画零线”。调整Y轴“Y轴范围”与“偏移量”或者选择“Y轴自动调整”来选择合适的监视图形。⑧平衡色谱柱、进样分析:关闭溶液排空阀(确认泵流量为1ml/min),监视压力基线等待平稳后,可以进样采集分析。4.2.2数据采集方法编辑:①设置泵:左键单击泵图标,点击“设置泵”或者点击“仪器”的下拉菜单中选取“设置泵”后进入泵的参数设置菜单。a.流速---设置泵的流速,在“压力限-上限”>200时,流速设置范围为:0-5.00ml/min;在“压力限-上限”b.停止时间---设置泵停止分析的时间,时间范围为:0.0-99999.00min或“无限制”。c.后运行时间---泵在后运行时间保持后运行状态,从而延迟下一个分析的开始。在溶剂成分改变后(例如:在梯度洗脱后),可以使用“后运行时间”使色谱柱达到平衡,时间范围为:0.0-99999.00min或“无限制”。d.压力限---“上/下限”是最大/小压力限制,达到“上限”或者“下限”值时,泵将自动关闭,从而防止分析系统压力超限。e.时间表---通过在“时间”字段中输入时间并在时间表的以下字段中输入适当的值,可以使用时间表对分析过程中参数进行设置。泵时间表中的值随时间从初始值到时间表中定义的时间所对应的值发生线性变化(例如,溶剂梯度)。②控制:左键单击泵图标,点击“控制”或者点击“仪器”的下拉菜单“更多泵”中选取“控制”后进入泵的控制菜单,控制泵的“启动”,“关闭”或者“待机”状态。③手动进样器:在设置“运行控制->样品信息”后,将手动进样阀扳至“load”状态进样(将样品装入到定量环内)。对于7725i手动进样阀,样品进样量为定量环体积的50%以下或者满定量环进样,否则进样量不准确。进样后,将手动进样器扳至“inject”状态,工作站自动开始记录采集数据。分析完成后,将手动进样阀扳至“load”状态,用定量环的5倍体积左右的甲醇清洗定量环,再在“inject”状态下清洗排空管路。清洗进样口,防止残留样品污染下次进样。④设置可变波长紫外检测器:左键单击可变波长紫外检测器图标,点击“设置VWD信号”或者点击“仪器”的下拉菜单“设置 VWD 设置信号”后进入可变波长紫外检测器的参数设置菜单:a.波长---设置VWD检测波长。b.峰宽---设置为色谱图中的预期的最窄峰。峰检测器将忽略比峰宽设置窄很多或者宽很多的所有峰。c.停止时间---设置VWD停止分析时间。一般设置为“与泵一致”即可。当VWD与其他检测器一起工作时,关闭检测器的灯,分析将停止。如果希望关闭检测器的灯时也能进行分析,请在“设置 VWD 信号->更多信息->特殊设置值(设置)”中选择“当灯关闭时也进行分析”。⑤控制:左键单击可变波长紫外检测器图标,点击“控制”或者点击“仪器”的下拉菜单“更多 VWD”中选取“控制”后进入可变波长紫外检测器的控制菜单:a.灯---控制检测器灯的开关。b.开灯---选择,则在打开电源的同时也点灯。为了延长灯的寿命,建议不选此项,以便在冲洗系统或者其他不需要检测器工作的情况下节省灯的消耗。4.2.3数据分析方法编辑:从“视图”菜单中,点击“数据分析”进入数据分析画面从“文件”菜单中选择“调用信号”选项,选中您的数据文件名,点击确定,数据被调出。①谱图优化:a.从“图形”菜单中选择“信号选项”;b.从“范围”中选择“全量程”或“自动量程”及合适的显示时间或选择“自定义量程”手动输入X、Y坐标范围进行调整,点击“确定”。反复进行,直到图的显示比例合适为止。选中化合物的名称前的空白框c.选择“图形->新建标注”,在工作站窗口右边打开图形编辑菜单,可以在色图谱中任意位置添加文字、图形等内容;d.选择“图形->信号选项”中选择“化合物名称”即可将命名的化合物名称添加到当前的色谱图中。②积分参数优化:a.自动积分方法:从“积分”菜单中选择“积分事件”选项,选择合适的“斜率灵敏度”,“峰宽”,“最小峰面积”,“最小峰高”。从“积分”菜单中选择“积分”选项,则数据被积分。如积分结果不理想,则修改相应的积分参数,直到满意为止。4.2.4建立全新完整方法向导:①新建完整方法:选择“方法->新建方法”后,点击“方法->编辑完整方法”编辑新方法。选择“方法信息”、“仪器/采集”、“数据分析”,“数据分析”也可以在“数据采集后”后再加入方法中。写入方法注释,而后按照数据采集方法编辑与数据分析方法编辑中所述内容,根据具体的仪器配置完成下面步骤的设置。a.设置泵参数。b.设置自动进样器参数。c.设置检测器参数。d.信号细节可以留空不选。e.设置积分方法。f.设置报告方法②保存方法:选择“方法->保存方法/方法另存为”。③保存即时改变的方法:通过在线改变数据采集或者在线/离线改变数据分析参数而变更方法,可以通过选择“方法->保存方法/方法另存为”或者保存新的参数到现在的方法中或另存为新方法。④调用方法:通过选择“方法->调用方法”或调用已有的方法。方法一经调用便立即生效。4.2.4进样:选择“运行控制->样品信息”。查看单针,点击a.路径---选择数据文件存储路径。b.选择手动或者前缀/计数器---命名数据文件名。c.样品位置---设置样品位置,直接填写数字即可,不需要写“样品瓶”。d.运行方法---保存样品信息并运行方法。e.确定---保存样品信息,后“运行控制->运行方法”。4.2.5 关机①关闭检测器的灯:G1314B(可变波长紫外检测器),关闭检测器的灯后冲洗系统,可以延长检测器灯的寿命。②冲洗系统:a.没有盐缓冲溶液的流动相:(反相系统)用85%~90%有机相+15%~10%水相冲洗系统和反相色谱柱或者适宜的流动相冲洗系统和反相色谱柱;b.有盐缓冲溶液的流动相,(反相系统)用85%~90%水相+15%~10%有机相冲洗系统和反相色谱柱(反相系统),除去反相色谱柱与系统中的盐溶液。然后用85%~90%有机相+15%~10%水相冲洗系统和反相色谱柱。③封存色谱柱:(反相系统)用90%~95%有机相+10%~5%水相封存反相色谱柱,两端封死。(如长时间存放可将柱子完全侵泡有机相内,以防用纯有机相封存反相色谱柱,如果长期保存有机相会挥发)。④关闭电脑:将泵流速逐步降至0ml/min,单击“关闭”按钮关闭所有模块,退出化学工作站,关闭电脑。⑤关闭模块:关闭所有模块电源开关。4.3常见问题解决方法4.3.1 工作站无法联机:确认打开Agilent 1200所有模块电源:①查看Agilent 1200网卡地址,如果使用bootp程序,请查看仪器配置中IP设置,如果未使用bootp程序,通常仪器默认地址为:192.168.254.11。②查看电脑网卡地址,“开始->控制面板->网络连接”,双击“本地连接”,单击“属性”,双击“Internet协议(TCP/IP)”,选择“使用下面得IP地址”,填入“地址”:192.168.254.10,“子网掩码”:255.255.255.0。如使用bootp程序,请将IP地址与Agilent 1200的IP地址前9个数字设为一样,后一位设为1~254之间,但不与Agilent 1200网卡地址相重复即可。③配置工作站,打开配置编辑器“配置->仪器”,选择“Modular LC System”或者“Modular 3D LC System”,选择“1100/1200 ACCESS->添加”,在“通过IP地址识别”输入192.168.254.11或者bootp中配置的地址,保存,退出。4.3.2 菜单显示不完全:选择“视图->全部菜单”。4.3.3 如何调整峰纯度报告样式:选择“光谱->光谱选项”,打开“光谱选项”菜单,选择“纯度->高级”,在“纯度计算”里面根据需要选择“类似曲线显示为”:Ln(相似性和阈值);相似性/阈值;纯度比率,将显示不同的纯度报告样式。4.3.4 如何将“峰纯度”和“库检索”结果自动生成报告:选择“视图->报告版面设计”或者,进入报告版面设计界面。选择“文件->打开模板”或者,打开“LIBRARY_CHS”模板,选择“文件->添加到报告模式中”,输入报告格式名称后,将“库检索”和“峰纯度”模板添加到“数据分析->报告->设定报告”中。选择“报告->自动检索谱库”,设定需要检索的谱库以及检索参数以及峰纯度阈值后“确定”保存退出。选择需要的色谱数据,选择报告类型为刚添加入“报告格式”中的名字,打印报告即可。5 注意事项5.1设备运行时禁止拔插接头。5.2禁止用水对设备进行喷淋清洗。6 清洁与维护清洁仪器,清理工作现场,拔掉电源。
操作维护
2024.09.06
什么是仪器检测限 (IDL)?
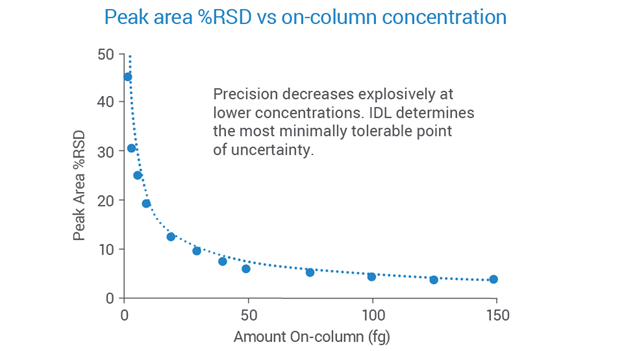
大多数分析仪器在分析空白(单独基质或溶剂)时会产生信号。空白处生成的信号称为仪器背景电平和基线噪声,定义为背景电平的波动。 仪器检测限 (IDL) 是分析灵敏度的统计测量方法,考虑了测量的精密度。它表征了要使测量信号为真实信号(而不是基线噪音)为 99% 可信度所需的分析物量(样品浓度或柱上量)。 当分析物的水平接近方法检测限时,测量的不确定度会急剧增加(精密度开始降低)。IDL 以数学方式确定最可容忍的不确定点,以确保您能够区分非常低的、可重复观察到的信号或基线噪声。为什么使用 IDL 而不是信噪比?信噪比 (S/N) 是一种常用的质谱灵敏度指标,在易于测量噪音时非常有用。然而,随着技术的发展以提高测量特异性,由于超低噪声水平,使用 S/N 比较高灵敏度检测系统变得越来越困难。S/N 可以使用可以夸大指标的算法来计算。每种算法略有不同,即使样本相同,也会生成不同的结果。许多算法也被设置为在较短的时间窗口内搜索噪声尽可能低的区域,并应用人工平滑,从而使指标产生偏差。此外,信噪比由单次进样确定,表示采样 n=1。在本例中,同一数据文件中使用了不同的噪声定义,表明 S/N 比发生了显著变化,而质谱检测限没有实际变化1 pg 利血平或氯霉素是确定系统灵敏度的常用性能标准品。但是,在质谱分析中没有计算信噪比的标准方法。这种缺乏严谨性或定义标准会导致根据不切实际的噪声定义报告的误导性 S/N 值,与实际分析没有实际相关性。IDL 是使用样品的重复测量来确定的;确保分析物在一系列进样中能够得到可靠检测。在仪器基线附近测量测试样品的响应,从而提供可靠、统计合理的仪器在低水平下的性能特征。
参数原理
2024.08.30
气质原理分析
基本原理介绍:气相色谱法是利用气体作流动相的色层分离分析方法。汽化的试样被载气(流动相)带入色谱柱中,柱中的固定相与试样中各组份分子作用力不同,各组份从色谱柱中流出时间不同,组份彼此分离。采用适当的鉴别和记录系统,制作标出各组份流出色谱柱的时间和浓度的色谱图。根据图中表明的出峰时间和顺序,可对化合物进行定性分析;根据峰的高低和面积大小,可对化合物进行定量分析。具有效能高、灵敏度高、选择性强、分析速度快、应用广泛、操作简便等特点。适用于易挥发有机化合物的定性、定量分析。对非挥发性的液体和固体物质,可通过高温裂解,气化后进行分析。可与红光及收光谱法或质谱法配合使用,以色谱法做为分离复杂样品的手段,达到较高的准确度,是司法鉴定中检测有机化合物的重要分析手段。色谱法:利用组分在两相间分配系数不同而进行分离的技术流动相:携带样品流过整个系统的流体固定相:静止不动的一相(色谱柱)定性:根据样品到检测器的时间(保留时间)多长可以进行定性定量:根据组分的峰面积和峰高度多少进行定量(和标准样品曲线进行对比)结构与功能:主要结构组成:自动进样器、柱温箱、色谱柱、检测器、(载气)阀门:六通阀、十通阀基本示意图检测器:氢火焰离子(FID):载气可用氦气和氮气,检测浓度为ppm以上,主要用于检测有机化合物电子捕获(ECD):载气可用氮气,检测浓度为ppb以上,主要用于检测有机卤素的化合物火焰光度(FPD):载气可为氦气和氮气,检测浓度约0.1ppm,主要用于检测硫、磷化合物火焰热离子(FTD):载气可为氦气和氮气,检测浓度为ppm以上,主要用于检测氮、磷化合物热导(TCD):载气可为氦气、氢气、氮气和氩气,检测浓度为50ppm以上,主要用于检测无极气体和有机化合物应用行业:典型应用:化工行业天然气解决方案炼厂气分析解决方案煤气分析解决方案油品分析解决方案微量硫化物解决方案微量CO、CO2分析解决方案痕量杂质分析系统各大行业一、室内环境检测行业包装厂,涂料厂,建材产品质量检测中心,室内空气检测公司,建筑工程质量检验测试站,环境检测站等需要气相色谱仪分析空气质量、材料质量等。二、烟酒食品行业香烟厂,酒厂,白酒厂,啤酒厂,酿酒公司,食品厂,饮料厂,蜂蜜厂等需要用气相色谱仪分析不同食品中指定组成的含量。三、科研及事业单位产品质量监督检验所,研究所,设计院,技术学院,大学化学系,农业质量监测中心,白蚁防治研究所,燃气公司,有机化学所,自来水厂,公安系统,等同样需要气相色谱仪分析、检测、研究。四、石油化工行业农药厂,制药厂、农化公司,精细化工,生物化工,石油化工,液化器厂、燃气厂,气体厂,煤炭工业,日用化工,粮油公司等用气相色谱仪分析检测。五、医药卫生行业司法鉴定中心,制药厂,医院,疾病控制中心等也需要用上气相色谱仪。气相色谱仪的用途:环境保护:大气水源等污染地的痕量毒物分析、监测和研究;生物化学:临床应用,病理和毒理研究;食品发酵:徽生物饮料中微量组分的分析研究;中西药物:原料中间体及成品分析;石油加工:石油化工,石油地质,油质组成等分析控制和控矿研究;有机化学:有机合成领域内的成分研究和生产控制;卫生检查:劳动保护公害检测的分析和研究;尖端科学:军事检测控制和研究.应用领域: 1、石油和石油化工分析:油气田勘探中的化学分析、原油分析、炼厂气分析、模拟蒸馏、油料分析、单质烃分析、含硫/含氮/含氧化合物分析、汽油添加剂分析、脂肪烃分析、芳烃分析。2、环境分析:大气污染物分析、水分析、土壤分析、固体废弃物分析。3、食品分析:农药残留分析、香精香料分析、添加剂分析、脂肪酸甲酯分析、食品包装材料分析。4、药物和临床分析:雌三醇分析、儿茶酚胺代谢产物分析、尿中孕二醇和孕三醇分析、血浆中睾丸激素分析、血液中乙醇/麻醉剂及氨基酸衍生物分析。5、农药残留物分析:有机氯农药残留分析、有机磷农药残留分析、杀虫剂残留分析、除草剂残留分析等。6、精细化工分析:添加剂分析、催化剂分析、原材料分析、产品质量控制。7、聚合物分析:单体分析、添加剂分析、共聚物组成分析、聚合物结构表征/聚合物中的杂质分析、热稳定性研究。8、合成工业:方法研究、质量监控、过程分析。检测样品:样品:沸点低于500℃有机物气相色谱仪分离要求在最短的时间内以塞子形式进入一定量的试样样品,然后进入色谱柱分离,试样样品进样方法的几种形式,即气体试样、液体试样、固体试样:1、气体试样的进样方法有四种:使用气密性注射器进样,使用阀定量管进样,定体积进样和气体自动进样。一般经常使用注射器进样与气体自动进样。使用注射器进样的优点是简便
参数原理
2024.08.30
一文教你读懂顶空进样!
顶空进样器是气相色谱法中一种方便快捷的样品前处理方法,其原理是将待测样品置入一密闭的容器中,通过加热升温使挥发性组分从样品基体中挥发出来,在气液(或气固)两相中达到平衡,直接抽取顶部气体进行色谱分析,从而检验样品中挥发性组分的成分和含量。使用顶空进样技术可以免除冗长繁琐的样品前处理过程,避免有机溶剂对分析造成的干扰、减少对色谱柱及进样口的污染。基本原理顶空进样分为溶液顶空和固体顶空。前者是将样品溶解于适当溶剂中,置顶空瓶中保温一定时间,使残留溶剂在两相中达到气液平衡 , 定量取气体进样测定。固体顶空就是直接将固体样品置顶空瓶中,置于一定温度下保温一定时间,使残留溶剂在两相中达到气固平衡,定量取气体进样测定。平衡顶空分析目前,顶空分析方法有手工方式、气密针进样方式、平衡式加压系统、定量环加压系统、静态-动态补偿式这五种进样方式。下面就是这几种进样方式各自的特点。01手工方式(烘箱或水浴法)Manual Injection(1)样品加热后达到热平衡状态(2)用注射器将样品抽出(3)迅速拿到气相上进样分析02气密针进样方式Gas-Tight Syringe Injection(1)样品加热后达到热平衡状态(2)通过可加热气密针将样品抽出(3)移动到气相进样分析03平衡式加压系统Balanced-Pressure System(1)样品加热后达到热平衡状态(2)用导管通入载气加压(3)样品随载气一起进样04定量环加压系统Pressure-Loop System(1)样品加热后达到热平衡状态(2)加压将样品引入定量环(3)阀将样品打入传输通道进样顶空优势(1)方便快捷的样品前处理:顶空进样器将待测样品置入一密闭的容器中,通过加热升温使挥发性组分从样品基体中挥发出来,在气液(或气固)两相中达到平衡,直接抽取顶部气体进行色谱分析,从而检验样品中挥发性组分的成分和含量。这种方法免除了冗长繁琐的样品前处理过程,避免有机溶剂对分析造成干扰,减少对色谱柱及进样口的污染。(2)样品中挥发性组分的成分和含量:顶空进样技术特别适用于对挥发性有机物进行定性和定量分析。它可以直接抽取并分析顶部气体,提供一种方便、快速、无损的分析方法。(3)连接各种型号的气相色谱仪:顶空进样器系列可以与国内外各种型号的气相色谱仪相连接,使其应用范围更加广泛。顶空进样技术的局限性(1)样品前处理过程相对繁琐,操作起来需要一定技巧,对于新手来说可能会有一定的学习难度。(2)顶空进样器的使用需要熟练的技术人员,对于一些小型实验室来说,可能需要额外的人员培训和操作技能的提升。(3)顶空进样技术的价格相对较高,对于一些需要大量使用的实验室来说,成本可能会较高。(4)顶空进样技术的灵敏度相对较低,对于一些低浓度的挥发性有机物的分析可能存在一定的难度。(5)顶空进样技术对于样品中不同组分的吸附和解吸动力学研究不够准确,这可能会对分析结果产生一定的影响。因此,在使用顶空进样技术时需要根据实际需要和实验室条件来选择是否使用该技术。怎么清洗顶空进样器无特殊情况下,清洗顶空进样器主要用纯水、甲醇或无水乙醇等冲洗或超声清洗,污染严重可用棉签轻轻擦拭,不可用力过度,避免破坏内表面产生活性点,然后放置到烘箱70℃烘干后干燥冷却密封存放即可。01清洗步骤如下:(1)设置传送带温度为60℃,设置样品定量管和传送管温度为Off。(2)一旦样品定量管和传送管温度冷却到低于60℃,关闭通往顶空进样器的气体,拆下出口端的放空管线。(3)在传送带中插入一个空的样品瓶。(4)用手提起样品瓶。(5)用一次性注射器抽取约6ml的纯净水注射进HSS放空管。(6)降低样品瓶然后取出来。重复步骤3到5(注射两到三次将清洗彻底)。(7)再设置一个空样品瓶并提起,然后使用一次性注射器注射足够的空气将水吹扫出来。(8)将传送管一端插入一个烧杯或类似容器中,并使用一次性注射器从HSS气体管出口注入约10ml水,然后注入约10ml甲醇。(9)使用一次性注射器注射足够的空气以吹扫出水。(10)重新安装好管线并打开气流。然后,切换样品瓶到Load-INJ反复几十次以将水和甲醇全部吹出样品阀和管线。顶空进样器操作过程中的注意事项(1)样品制备:在进行顶空进样之前,必须对样品进行适当的制备。如果样品过于粘稠或含有杂质,可能会影响仪器性能甚至导致故障。因此,在使用进样器之前,应该确保样品已经被预处理和净化。(2)压力控制:在进行顶空进样时,需要适当地控制系统内的压力。过高或者过低的压力都会对样品的分析结果产生不利的影响。因此,应该严格按照仪器说明书上的要求进行调节。(3)选择适当的针头:顶空进样器通常需要使用特殊的针头进行操作。在选择针头时,需要根据样品的性质和容器大小来确定。如果针头太大或太小,可能会影响样品的输送速度和分析结果的准确性。
参数原理
2024.08.30
分析仪器租赁是买还是租?
如何在租赁和购买仪器之间做出选择,已不再是简单的财务问题,而是关系到公司长远发展的战略决策。以下是我对这一问题的一些分析和建议,希望能为面临类似选择的企业提供一些有价值的参考。 成本效益:精打细算,撬动更多资源购买的优点在于一次性投入后,长期来看设备的平均使用成本可能较低,且设备成为公司固定资产。缺点是初期资金压力大,影响公司现金流。租赁的优点是初期投入小,可以分散成本,保持财务灵活性。缺点是长期租赁的总费用可能超过购买成本。在当今快速变化的商业环境中,资金的灵活运用至关重要。购买仪器意味着一次性的大额支出,这不仅会压缩公司的现金流,也会限制其他领域的投资潜力。而租赁则能将资金使用效率最大化,将原本用于购买仪器的资金,投入到市场拓展、研发创新等更具回报的项目中。换句话说,租赁可以帮助我们以更低的初始成本撬动更多的资源和机会。仪器利用率:切记盲目购买如果仪器的使用频率不高或只是短期项目的需求,租赁能够避免因设备闲置而浪费资源。购买更适合那些使用频率高、长期需要的设备,能够在长时间内摊薄成本。互联网时代,业务模式和需求波动加剧,不确定性成为常态。在这种环境下,固定资产的灵活配置显得尤为重要。如果仪器的使用频率不稳定,或仅在特定项目中需要,租赁无疑是更明智的选择。它允许我们根据实际需求灵活调整设备配置,避免因设备闲置而造成的资源浪费。技术更新:紧跟技术,保持竞争力技术迭代的速度让人应接不暇,作为行业先锋,必须时刻保持对最新技术的敏锐嗅觉。租赁仪器的好处在于我们可以在技术更新时轻松升级设备,始终保持技术的前沿地位,而不必担心设备贬值。反之,购买设备意味着我们要承担设备过时的风险,这在科技更新如此迅速的今天,可能会成为一种负担。维护与维修:省心省力专注核心业务购买设备意味着我们需要承担所有的维护和维修责任,增加管理成本。而租赁的优点是大多数情况下,维护和维修都由租赁公司负责,这让我们可以更加专注于业务本身,而不是后勤管理。维护和维修问题往往是购买设备后的隐形成本。购买仪器后,我们不仅要承担高昂的维修费用,还要投入大量精力管理设备的日常维护。这无疑会分散我们对核心业务的关注。而租赁仪器通常包括全面的维护和维修服务,这不仅节省了我们的人力和物力成本,还能确保设备始终处于最佳状态,助力我们专注于业务创新和客户服务。财务灵活性:优化资金配置资金流动性是企业运营的生命线。通过租赁,我们可以将大额资金支出转化为可控的运营费用,这种安排灵活性高,转化在财务报表上表现为更加健康的现金流和更好的资本效率。购买产生大额支出后可能影响公司的资金流动性,增加财务压力尤其是在当前不确定性加剧的市场环境中,保持财务灵活性尤为重要,它能让我们更从容地应对市场变化和突发状况。折旧资产管理:灵活应对市场购买仪器后,设备会随着时间的推移而折旧,这会直接影响公司的资产负债表。而租赁则让我们可以轻装上阵,避免固定资产过多导致的财务压力。特别是在资产管理和财务优化方面,租赁更有助于我们维持一个灵活、可持续的财务结构,让公司在市场竞争中更具优势。但在考虑长期投资时,租赁和购买的总成本比较至关重要。如果某台仪器将在未来几年内频繁使用,购买可能会更具成本效益。但从战略角度出发,如果我们预见到技术的快速变化或市场需求的波动,租赁可能是更为审慎的选择。它让我们能够随时调整战略,避免长期资产固定化带来的束缚。在这个数字化和技术驱动的时代,企业必须从全局战略出发,灵活配置资源。租赁和购买的选择,不仅仅是成本的对比,更是对未来发展的布局和思考。如果公司当前的资金状况需要保持灵活性,且面对快速变化的技术和市场,租赁无疑是一个更具智慧的选择。而对于那些确定将长期使用、且稳定性较高的设备,购买仍然是值得考虑的长期投资。无论如何,关键在于权衡利弊,做出符合企业长远发展的明智决策。
操作维护
2024.08.30
怎么为实验室挑选合适的质谱仪?
为实验室选择最合适的质谱仪是很有挑战性的,因为决定中涉及到许多因素,这里绝不可能把所有的因素都总结出来。然而,我在这里建议了几个关键的考虑因素,他们在临床实验室领域是比较重要的。➤ 确定你的需求是否需要高通量(筛查),每天对许多样品进行特定的测定?如果是,这就需要一个强大的、经过确认的仪器。此外,备用仪器或快速服务支持也是必不可少的。是否需要一个多功能的仪器,用于生物医学研究实验室或临床研究,每天需要许多不同类型的测定/分析?感兴趣的分析物是什么?例如,小分子、挥发性代谢物、生物聚合物和元素都有不同的仪器要求。测定需要更多的定量(诊断)结果,还是定性分析(筛查)就足够了?➤ 确定分析物和研究替代分析方法确定分析物:确定关键化合物、代谢物和蛋白质;开发或获得一个测试化合物。调查竞争测定:确定替代方法;获得替代方法的关键规格,例如,定量限(LOQ)、分析范围和精密度。➤确定质谱仪和相关部件确定能够测试关键化合物的质谱仪:电离模式;所需的分辨率;流动注射,HPLC,GC。➤化合物测试演示由特定供应商进行操作演示:测试关键代谢物;评估灵敏度、精密度、优化的难易程度和数据处理软件;将结果与平行分析进行比较:两个准备相同的样品,一个用有效方法分析,另一个用考虑中的仪器分析。仪器间的比较也应在相同的来源和相同的条件下制备的样品上进行。如果可行的话,用一套生物标准品来校准质谱仪,并将真实样品上得到的结果与目前内部方法得到的结果进行比较。➤如果可能的话,要求提供仪器进行现场评估。➤最终评估:软件;数据处理;解释数据链(数据库,数据接口方式);价格、稳健性、技术支持(响应时间)、运营成本;从拥有当前或类似型号的实验室获得相关支持性资料。诊断科学编辑团队收集、整理和编撰,如需更多资讯,请关注公众号诊断科学(DiagnosticsScience)。
参数原理
2024.08.24
国际巨头占近90%市场份额,国产质谱仪如何“突围”?
质谱仪,是一种分析仪器,可以将待测的物质电离成不同质荷比的离子,并且利用电磁学原理使离子按照质荷比分离并测定离子流强度。包括飞行时间质谱仪、四级杆质谱仪、离子阱质谱仪和串联质谱仪四种类型。基于质谱技术高灵敏度、高分辨率、分析速度快等优势,质谱仪在医疗健康、食品安全、环境监测、工业分析、国家安全等领域具有不可替代的作用和举足轻重的地位。国际巨头占近90%市场份额目前质谱仪尚未完成国产替代化进程,国内专门从事研发、生产和销售的质谱仪公司也不多。禾信仪器虽然成立以来就牵头承担数项与质谱仪相关的“国家重大科技专项项目”,但其产品结构相当单一,主要应用与环境监测,服务的客户也主要为各级生态环境部门、环境监测站或者科研中心,市场拓展高度依赖环保政策和财政预算安排。据SDI的数据,目前全球质谱仪市场基本被国际巨头所占据,市场主要参与者为沃特世、丹纳赫、布鲁克、安捷伦、赛默飞、岛津等公司,这些公司占据了全球近90%的质谱仪市场份额。目前质谱仪的主要销售市场也不在亚洲,而是集中在欧美地区,其中美国是全球最大的质谱仪销售市场。随着亚洲地区国家的发展,未来亚洲有可能成为全球质谱仪市场增速最快的地区,我国有望成为亚洲地区增速最快的质谱仪应用市场。但是,我国质谱仪市场基本被国际巨头占据。据中国海关的数据,2018年,我国进口了12426台质谱仪,质谱仪的进口金额达到95.81亿元,其中4成左右的进口质谱仪来自美国。据智研咨询的数据,如果不算进口质谱仪的关税、流通渠道费用、技术服务费用等环节,2018 年中国质谱仪市场规模为111.93亿元,换言之,国外厂商在中国质谱仪市场的占有率为85.6%,留给国内厂商的市占率仅为15%左右。前景可期,国产质谱仪当奋力“突围”随着我国经济的不断发展,质谱仪因其高特异性、高灵敏度的优势将会不断得到市场认可,应用领域涉及国民经济各个环节,其作为采集信息的重要源头,对其他产业的发展具有巨大的带动作用,在各大检测领域都将会有越来越广泛地运用。根据中国海关进口数据统计,2018年国内质谱仪市场规模约为100亿元。在此基础上,如进一步考虑进口后相关税费、国内市场渠道流通、提供技术服务等环节,初步测算2018年国内质谱仪市场规模约为130亿元。如保守以国际市场年均复合增长率7.70%为基础进行测算,我国2026年质谱仪市场规模将会至少达到235亿元,未来市场前景可期。面对质谱仪进口数量不断攀升的现状,我国要进一步加强对质谱技术的重视程度,制定合理、有效的发展计划,加大研发投入和支持力度,加快推进产业化进程,从而缩短国产质谱仪器与进口产品之间的差距,实现国产质谱仪的“突围”。
参数原理
2024.08.24
关于质谱仪的使用,这篇文章都全了!
质谱分析法是通过对被测样品离子的质荷比的测定来进行分析的一种分析方法。被分析的样品首先要进行离子化,然后利用不同离子在电场或磁场运动行为的不同,把离子按质荷比(m/z)分开而得到质谱,通过样品的质谱和相关信息,可以得到样品的定性、定量结果。质谱仪是如何构成的?典型的质谱仪,一般由样品导入系统、离子源、质量分析器和检测器组成,此外,还含有真空系统和控制及数据处理系统等辅助设备。看下图质谱仪的分类有机质谱仪:由于应用特点不同又分为:(1) 气相色谱-质谱联用仪(GC-MS)。在这类仪器中,由于质谱仪质谱仪工作原理不同,又有气相色谱-四极质谱仪、气相色谱-飞行时间质谱仪、气相色谱-离子阱质谱仪等。(2) 液相色谱-质谱联用仪(LC-MS)。同样,有液相色谱-四器极质谱仪、液相色谱-离子阱质谱仪、液相色谱-飞行时间质谱仪,以及各种各样的液相色谱-质谱-质谱联用仪。(3) 其他有机质谱仪。主要有:基质辅助激光解吸飞行时间质谱仪(MALDI-TOFMS)、傅里叶变换质谱仪(FT-MS)。2.无机质谱仪:包括:火花源双聚焦质谱仪(SSMS)、感应耦合等离子体质谱仪(ICP-MS)、二次离子质谱仪(SIMS)等。3.同位素质谱仪:包括:进行轻元素(H、C、S)同位素分析的小型低分辨率同位素质谱仪和进行重元素(U、Pu、Pb)同位素分析的具有较高分辨率的大型同位素质谱仪。4.气体分析质谱仪:主要有:呼气质谱仪、氦质谱检漏仪等。质谱仪的样品导入系统现代商品质谱仪一般配备以下进样系统,供测定不同样品时选用。1.直接进样(1)探头进样:单组分、挥发性较低的液体或固体样品,可在高真空条件下,用进样杆把样品通过真空闭锁装置送入离子源中被加热气化,并被离子源离子化。(2)储罐进样:低沸点的样品,将其气化并导入抽真空的加热气罐中,以恒定的流速由储罐通过一个小孔(分子漏孔)导入离子源。2.色谱联用进样:对于复杂多组分的样品,采用质谱仪与色谱仪联用的方式,色谱先将多组分分离成单一组分,再通过“接口”(interface)导入质谱进行分析。高效液相色谱质谱仪日常维护计划目的:指导化验员正确的维护和保养高效液相色谱质谱仪,提高仪器使用寿命,使仪器稳定的工作得到稳定可靠的数据。液相色谱仪部分:一、流动相的制备要求:高效液相级色谱醇,二次蒸馏水,缓冲盐一定要过滤;流动相脱气至关重要(可采用抽滤,超声波脱气等方法。二、高压恒流泵的维护和保养1.高压恒流泵为整个色谱系统提供稳定均衡的流动相流速,保证系统的稳定运行和系统的重现性。高压输液泵由步进电机和柱塞等组成,高压力长时间的运行回逐渐磨损泵的内部结构。在升高流速的时候应梯度势升高,Z好每次升高0.2mL/min当压力稳定时再升高,如此反复直到升高到所需流速。2.特殊情况下可拆下滤头抽取以判断其中是否堵塞;亦可用注射器吸取流动相通过吸滤头打出以判断其是否堵塞。若有堵塞情况可用异丙醇超声波清洗;清洗不成功则需要更换3.在仪器使用完了以后,要及时清晰管路冲洗泵,保证泵的良好运转环境,保证泵的正常使用寿命。三、色谱柱的维护和保养1.所使用的流动相均应为HPLC级或相当于该级别的,在配置过程中所有非HPLC级的试剂或溶液均经0.45um薄膜过滤。而且流动相使用前都经过超声仪超声脱气后才使用。2.所使用的水必须是经过蒸馏纯化后再经过0.45um水膜过滤后使用,所有试液均新用新配。并且在进样的样品都必须经过0.45um薄膜针筒过滤后进样。3.所使用到的Z大流速为1.0mL/min,所以流速提升过程应是梯度提升,不存在流速的突升突降。4.仪器检测完,均使用水:甲醇=90:10清洗了管路和色谱柱1小时以上,使用水:甲醇=90:10保存管路和色谱柱40分钟以上。四、工作站的维护出现死机可重启计算机;不正常运行时,首先可更换电脑测试其硬件故障;或在本机上重新插拔接口、重新安装软件。五、常见故障及日常维护下表中列出了液相色谱常见的一些问题,右侧中则列出了的日常维护的方法可以减少问题出现的频率。液相质谱仪质谱部分:一、分子泵的维护和保养1.喷口离orifice位置尽可能远。2.样品尽可能干净。3.机械泵油经常更换。4.分子泵的散热尽量充分。二、不定期做质量校正:仪器只有在质量正确的条件下才能保征分析结果可靠:1.负离子:PPG300010ul/min。2.正离子:1/10PPG 5ul/min (API3000)1/50 PPG 5ul/min(API4000)。3.每次重新开机,不关机时,每三个月。三、清洗Curtain Plate, Orifice, Skimmer和Q0:1.清洗 Curtain Plate:用无尘纸加甲醇擦洗。2.清洗 Orifice 外部:拆卸Curtain Plate后,用无尘纸加50水/50甲醇擦洗。3.停API主机15分钟后,停机械泵拆卸Curtain Plate拆开Interface,拆卸skimmer用200ul加样枪头,加50水/50甲醇擦洗Orifice内部用无尘纸加甲醇擦洗Skimmer和Q0。四、堵的判断及处理方法:1.进样管及spray tube堵塞。2.用Syringe推:直线喷出—没有堵塞。3.若堵,取下用50水/50甲醇超声。4.超声仍无效,更换进样管及spray tube。5.Orifice堵塞,灵敏度下降或真空度异常的好,应用50水/50甲醇清洗orifice 外部,不能解决问题时再清洗orifice内部。五、机械泵维护:1.每三个月更换机械泵油。2.不同公司的油不可混合使用:会损坏机械泵。3.更换不同公司的油时:必须用新油先冲洗一次。六、常见故障及日常维护七、死机处理的9个步骤1.Analyst软件中Hardware configure重新deactive,再active。2.用CTRL-ALT-DEL,Windows任务管理器结束任务,关掉Analyst软件,然后重新打开Analyst。3.关掉Analyst软件,Stop Service后重新打开Analyst软件。4.重新启动控制仪器的电脑,HPLC重新启动,再active。5.Stop Service后进入Scu21.exe中,clear GPIB Bus。6.Stop Service后进入Scu21.exe中,Reset System controller。7.同时按下电源旁边的两个按扭reset。8.重新开关仪器总电源。9.Stop Service后进入Scu21.exe中。※说明:一步不行,再使用下一步,不一定7步都需要做完
参数原理
2024.08.24
质谱仪的原理是什么?
目前越来越多的环境监测、排放源监测、工业控制方面运用到了在线质谱技术。这一技术以高特异性和高灵敏度得到了广泛的认可。那么什么是在线质谱技术?其内涵有哪些分类可以选择呢?以下就来简单介绍一下:质谱分析法是测量离子质荷比的分析方法,离子质荷比即质量-电荷比。其遵循样品导入→离子源→分析器→检测器的方式,将样品导入离子源中发生电离,生成带电荷离子,然后运用加速电场将离子束引入分析器中,再利用电场和磁场使其发生相反的速度色散,再将它们聚焦起来而得到质谱图,从而确定其质量。而在线质谱则是在这之后增加了数据处理和控制系统、并可以将有效数据上传至云服务器,达到远程、实时查看及数据分析的目的。质谱技术根据样品导入、离子源、分析器、检测器等均有着不同的分类和组合方式,可谓种类繁多。按样品导入可分为:1)直接引入,将低挥发性、热稳定性好的样品直接装在探针上进行电流极具加热,样品在高温下挥发形成蒸汽,蒸汽被引至离子源中离子化。2)间接引入,色谱引入和膜进样。色谱引入是将样品通过毛细管导入至离子源。而膜进样则是采用硅聚合半透膜,阻挡基体和溶剂,并使小分子有机物通过膜壁。按电离技术主要包含:1)等离子体解吸[PD-MS]2)快原子轰击[FAB]3)电喷雾[ESI]4)基质辅助激光解吸[MALDI]按离子源主要包含:1)电子电离[EI],其离子化试剂为电子,适宜气态样品2)化学电离[CI],其离子化试剂为气体离子,适宜气态样品3)解吸电离[DI],其离子化试剂为光子、高能粒子,适宜固态样品4)喷雾电离[SI],其离子化试剂为高能电场,适宜热溶液按分析器主要包含:1)双聚焦质谱仪2)四极杆质谱仪3)飞行时间质谱仪[TOF-MS]4)离子阱质谱仪[IT-MS]5)傅立叶变换质谱仪[FT-MS]按检测器主要包含:1)电子倍增管2)离子计数器3)感应电荷检测器4)法拉第收集器按属性组合主要包含:1)气相色谱质谱仪[GC-MS]2)液相色谱质谱仪[LC-MS]3)基质辅助激光解吸飞行时间质谱仪[MALDI-TOFMS]4)傅里叶变换质谱仪[FT-MS]5)火花源双聚焦质谱仪。6)感应耦合等离子体质谱仪[ICP-MS]。7)二次离子质谱仪[SIMS]这些分类只是目前质谱分析的主要分类,根据分析样品和目的的不同,运用不同的技术和组合会衍生更多的应用分类。在线质谱设备专业性相对较强,针对客户不同的要求、检测环境和检测物质等都有着不同的仪器配置方案。故在项目购置时则需要寻找行业内较为资深的企业和相关专业人士进行详细了解和配置方案的制定,从而得出性价比更高的解决方案。
参数原理
2024.08.24
制备型SFC介绍
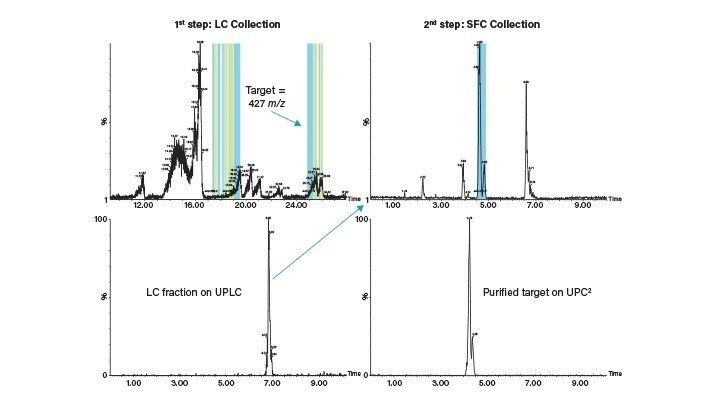
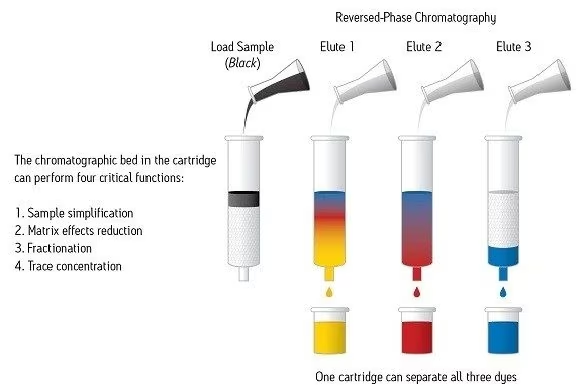
纯化的目的是去除所有会影响产品品质、造成环境污染、引入掺杂物或导致产品受到污染的物质。化学意义上的纯化是指分离物质中的各组分并去除杂质。从古到今,为了提高生活质量,人们运用各种方法来分离和纯化化学物质。从药物发现到化工材料、天然产物和食品生产,纯化都是必不可少的。总体而言,纯化的目的是分离物质、改变混合物组成或去除干扰物。具体而言,研究人员进行纯化的目的多种多样,包括结构解析、活性研究、产品配方和产物富集、杂质分析等等。面对纯化挑战,市面上有许多复杂程度和效果各不相同的解决方案。然而,如何实现化合物的高通量分离通常是提升效率的瓶颈。因此,人们迫切需要更快、更高效的纯化工具。超临界流体技术(SFx)包括一系列基于CO2的技术,专为精简纯化工作流程而设计,制备型超临界流体色谱(Prep SFC)就是其中之一。本初学者指南将介绍Prep SFC用作纯化技术的原理、应用、仪器和工作流程。SFx技术简介SFC纯化的基础是超临界流体技术(SFx)。沃特世SFx技术包括超临界流体萃取(SFE)、分析型色谱(UPC2)和制备型色谱(Prep SFC),它们都以亚临界或超临界状态的CO2为主要溶剂。SFx技术采用CO2替代液态有机溶剂和水性溶剂,是液相纯化技术的正交技术,而且更加环保和经济有效。之所以说SFx是一项“绿色”技术,是因为它不产生有机废液,可减少环境影响。相较于LC纯化,SFx在速度和选择性方面均有显著提升,这意味着从复杂原料到终产物所需的时间和成本大大降低。随着仪器技术的发展,各种纯化应用越来越明显地体现出SFx技术带来的分离能力优势。以CO2为溶剂超临界流体是流体压力和温度超过临界值的产物。在临界点处,气液两相间的界面消失,此时高度压缩气体的密度与液体密度相近。超临界流体还具有类似于气体的高扩散性和低粘度。其溶解能力主要与密度相关,而密度可通过控制压力和温度进行调节。一般来说,密度越大溶解能力越强,降低温度或增大压力均可增大密度。另一方面,升高温度或减小压力则会使密度变小。图1所示为CO2的相图,展示了它从一种状态到另一种状态的物理变化及其临界点。很多物质在极端条件下才能转变为超临界状态,而且在该状态下会表现出某些不良特性。表1所示为几种物质转变为超临界流体的条件及其在此状态下的特性。不同于其他超临界物质,CO2不可燃、无爆炸危险、无毒性或腐蚀性,因此通常被认为是一种十分安全的物质。此外,CO2很容易达到超临界状态(在31 °C和74 bar下),因此人们能够在可接受的温度和压力范围内控制其密度。不仅如此,由于临界温度相对温和,它还适用于处理热不稳定样品。CO2还易于通过其他工业工艺回收,因而价格相对低廉;这意味着它对环境CO2水平的影响是中性影响。上述所有优势使得CO2成为了超临界流体技术最常用的物质。SFx纯化工作流程纯化工作流程由多个步骤组成,其复杂性和必要性根据应用要求而异。最基本的SFx纯化工作流程包括以下方面:原料或样品:样品可能很复杂(例如天然的植物性样品),也可能相对简单(例如经过准确表征的候选药物),这将决定需要进行何种程度的样品制备(如果需要)以及纯化的规模。尽可能收集有关样品和最终产品的信息(例如热稳定性、极性、溶解度和反应性)也很重要,这些信息将决定样品的处理方式。样品制备:纯化的第一步需要根据原料状态和应用的目的或适用范围正确地制备样品。样品制备可能包括研磨、干燥、提取和过滤等多个步骤,也可能只需溶解样品将其制成溶液。超临界流体萃取(SFE)是SFx工作流程的第一步(即样品制备)。该技术通常用于涉及工业粗制品、植物性材料或天然产物的应用。样品纯化:纯化的作用是降低样品复杂性,或者分离出纯度达到指定范围的终产物进行分析或用于产品配方。通过SFE制备的样品通常是含有目标化合物和杂质的复杂混合物。作为SFx工作流程的第二个步骤(纯化),制备型超临界流体色谱(Prep SFC)会从提取物中纯化出一种或多种目标物质。Prep SFC还可应用于多种其他方法制备的样品,而不仅仅局限于SFE法制备的样品。终产物:获得终产物是工作流程的最终目标。它可以是分析得到的数据和信息、某种工艺所需的精炼原料,或者是可直接使用的终产物。终产物决定了成功的工作流程所需的仪器和方法。在SFx工作流程中,提取(SFE)和纯化(Prep SFC)之前及之后的样品分析由超高效合相色谱(UPC2)完成。上述SFx技术中的任何一种都可以根据需要用于非SFx工作流程中的样品制备、纯化或分析步骤。制备型色谱:HPLC到SFC的沿革过去20年来,制备型高效液相色谱(Prep HPLC)一直都是较常用的纯化技术之一。具体而言,该技术是精细化学品、制药和生物技术行业普遍使用的一种分离工艺,广泛应用于产品纯化。在这期间,Prep HPLC已发展成为一种非常高效且适用性极广的技术,尤其是在非手性纯化领域。反相液相色谱(RPLC)的优势是采用几乎通用的固定相(C18),以及由水和乙腈组成的通用混合流动相。RPLC兼容质谱(MS)分析,它与MS联用(RPLC-MS)已成为许多研究环境下的标准纯化方法。尽管应用广泛,Prep HPLC也存在诸多缺点。相较于处理的总样品量,纯化一定质量化合物的流动相用量相当大。典型的Prep HPLC馏分含有大量溶剂(包括有机溶剂和水性溶剂),分析人员需要花费大量时间和精力来干燥和获取终产物,这极大限制了纯化效率。LC所用的溶剂会污染局部环境(通过蒸发或接触)和大气环境(通过化学废弃物焚烧)。正相液相色谱(NPLC)对环境的危害更大,因为其流动相通常是纯有机溶剂。鉴于上述环境问题,购买和处置LC流动相溶剂的成本越来越高;因此人们迫切需要一种对溶剂依赖程度更低或更环保的纯化方法。SFC正是这样一种替代方案,它有助于突破效率瓶颈,同时可带来缩短用时、减少废液和降低成本等好处。最近,SFC仪器方面的进展使得该技术作为手性和非手性纯化的一种有用工具再次成为人们的关注焦点。在分析和纯化领域,SFC是比HPLC更加环保的一种替代方法。SFC也是色谱超临界流体色谱(SFC)是一种色谱技术,其使用亚临界(液态)和超临界CO2作为流动相的主要溶剂,通常还需搭配有机溶剂使用。和所有色谱技术一样,SFC技术也基于分析物在固定相(色谱柱)和流动相(溶剂)之间的分配来分离各组分。HPLC与SFC有许多相似之处,例如:SFC可在等度和梯度方法条件下运行,并且兼容所有标准检测技术,如紫外(UV)检测、光电二极管阵列(PDA)检测、蒸发光散射(ELS)检测和质谱(MS)检测。常规Prep SFC工作流程与HPLC的相同,包括方法开发、放大、馏分收集,以及对收集到的馏分进行纯度分析(图3)。SFC的回收率和样品纯度可媲美RPLC,在某些应用中SFC的回收率较高,而对于其他应用,HPLC是更好的解决方案。SFC一般采用正相色谱分离原理。SFC与HPLC的不同之处在于,SFC采用CO2替代非极性液态组分(例如正己烷和庚烷)作为流动相的主要组分。由于超临界CO2是可压缩流体,因此压力和温度是控制溶剂强度,进而影响色谱保留时间和选择性的重要参数。超临界CO2是色谱纯化的理想之选,因为其不可燃、无毒并且具有高扩散性、低粘度和出色的溶解能力。近年来,得益于节省溶剂和高效率的优势,SFC备受纯化实验室青睐。Prep SFC优势:节省溶剂由于采用CO2替代了大部分流动相,Prep SFC的主要优势之一是溶剂用量少。这一优势在分析级分离中也许并不明显,但在制备级分离中效果相当显著。许多纯化实验室都需要花费相当多的时间从馏分中去除溶剂,这极大制约了化合物纯化完成后获得目标产物或结果的效率。在Prep SFC中,流动相中的CO2通过降压即可除去,只剩下少量助溶剂。所得馏分中的产物浓度也更高,缩短了去除溶剂和产物分离所需的时间。馏分还可以直接用于分析,无需进行样品富集或浓缩。对于那些在普通长时间干燥条件下会发生降解的化合物而言,这一点至关重要。SFC有机溶剂用量较低带来的其他优势还包括节约成本、更安全(就可燃性和毒性角度而言),以及对环境影响更小等等。在溶剂购买和处置方面,SFC的成本优势相当可观;除此之外,由于去除溶剂所需的能耗更低,还能进一步节省成本。SFC还可避免使用有毒溶剂,例如RPLC使用的乙腈以及NPLC使用的脂肪烃和氯化物溶剂。作为其他工业工艺的副产物,CO2价格相对低廉,而且可以循环使用。Prep SFC优势:提高工作效率SFC效率的提升得益于流动相的低粘度和高扩散性对色谱分析速度和效率的提升。图4比较了HPLC、UPLC、SFC和UPC2的Van Deemter曲线。在色谱分析中,分离速度部分取决于溶质在流动相中的扩散速度及其进出固定相的速度。SFC的Van Deemter曲线比HPLC更宽更平,这表示SFC在流速(线性流速)增大的情况下仍能保持较高的色谱效率(低塔板高度)。SFC的高扩散系数直接转化成了更快的色谱分析速度。由于流动相粘度较低,色谱柱和系统压力也较低,因此可采用高达HPLC流速3~4倍的线性流速以及粒径更小的色谱柱。此外,低粘度还能缩短平衡时间。这样一来,运行时间缩短,分离效率提高,进而可增大载样量并缩短进样周期;这些对于任何制备型色谱分离而言都是提高效率的关键参数。因此,SFC得以在更短的时间内获得纯化合物,从而提高总体工作效率。表2给出了SFC相较于HPLC更省时、更高效的示例。Prep SFC是反相液相色谱(RPLC)的正交技术利用SFC与RPLC的正交关系可提高多种应用的产物质量。采用C18色谱柱的RPLC是一种几乎通用的解决方案,能够极大简化方法开发过程,但由于其使用水性流动相,溶剂兼容性和化合物溶解性非常有限。另一方面,SFC可配合多种有机稀释剂使用,对溶剂和化合物的兼容范围更广。此外,SFC可选用的固定相也非常丰富。之所以说SFC是RPLC的正交检测技术,是因为SFC一般被视为正相色谱,并且可提供多种易于操作的色谱分离选项。由于兼具正相选择性和高分离效率,SFC在立体异构体、位置异构体和结构相似化合物分离方面的优势尤其明显。对于非极性化合物,SFC的灵活性允许分析人员采用反相色谱柱(例如C18),同时以水作为添加剂,将应用扩大到极性更强的范围。对于化合物易降解的应用,SFC纯化更是理想的替代解决方案,因为SFC方法分离速度快、不使用水,并且馏分干燥步骤能在低温条件下快速完成。Prep SFC的回收率和纯度可媲美RPLC,某些应用采用SFC和RPLC均可。一项研究筛查了SFC和LC纯化对某制药化合物数据库中化合物的适用性,所得结果如图5所示。约82%的化合物可通过两种纯化技术中的任意一种进行纯化。但除此之外,该研究还证明了这两种纯化平台的互补性。部分化合物只能通过SFC法纯化(4%),还有一部分化合物只能通过LC法纯化(8%)。两种纯化平台联用所带来的灵活性为优化分离和纯化方案提供了更多可能性。SFC的选择性与RPLC互补,因此我们可在方法开发过程中引入正交技术用于分离复杂的棘手样品。采用跨平台多步纯化方案或使用正交技术进行馏分分析,可获取纯度更高的产物和更丰富的信息。图6所示为采用正交的LC和SFC分离方法纯化某复杂基质中所含化合物的示例。
参数原理
2024.08.16
SPE - 固相萃取教程
分析科学家在确定最好使用哪些工具来获得所需的结果时面临许多挑战。确定样品前处理工具和方法是可能显著影响成败的重要考虑因素。如果不必进行任何样品前处理工作,就再好不过了。但在现实中,样品前处理往往是不可或缺的一环。您可能需要针对现有样品优化方法,以提高通量或降低每次分析的成本。或者,您可能需要分析各种不同类型的样品以报告新的目标化合物。每种新的样品类型都会带来不同的分析挑战。此外,当今的科学家需要分析比以往浓度更低的物质,并且不能牺牲准确度和精密度,面临着巨大挑战。本书旨在帮助您认识和了解样品前处理技术领域一项非常强大的工具:固相萃取[SPE]。这项技术使用了装有色谱填料的装置,本书将说明这项技术如何帮助您应对分析挑战。固相萃取的定义SPE是一项样品前处理技术,采用固体颗粒色谱填料(通常装于小柱型装置中)对样品的不同组分进行化学分离。样品几乎总是处于液态[尽管一些特殊应用可能会使用一些气相样品]。图1所示为使用SPE装置处理一个黑色样品,以便对组成该样品的各染料化合物进行色谱分离。可以使用色谱床分离样品中的不同化合物,提高后续分析检测的成功率。例如,SPE常用于选择性去除干扰物。严格来讲,这项技术的正确名称是“液-固相萃取”(Liquid-Solid Phase Extraction),因为色谱颗粒是固体,而样品处于液态。这里使用的液相色谱基本原理也与HPLC所用相同,但形式不同,原因也不同。这里使用色谱法是为了更好地制备样品,然后提交进行分析检测。在样品前处理中,样品来源可能很广泛,包括生物体液,例如血浆、唾液或尿液;环境样品,例如水、空气或土壤;食品,例如谷物、肉和海鲜;药物;保健品;饮料;或工业产品。甚至蚊子头部也可以作为样品!当科学家需要分析从蚊子脑部提取的神经肽时,SPE是首选的样品前处理方法[沃特世应用数据库,1983年]。SPE的四大优势使用SPE有诸多优势,其中有四大优势值得特别关注。1. 复杂样品基质的简化以及化合物纯化对于分析化学家而言,最棘手的问题之一,就是目标化合物包含在复杂的样品基质中,例如谷物中的真菌毒素、虾中的抗生素残留,或者血浆、血清或尿液中的药物代谢物。样品基质中的大量干扰成分或物质和目标化合物在一起,导致分析极其困难。首先要解决的问题是分析本身的复杂性,因为存在如此之多的成分,必须分离之后才能鉴定和定量目标化合物。请参见图2。分析的稳定性可能不足,因为任何细微变化都可能影响一对关键分析物的分离度。另一个考虑因素是,原始样品基质中存在的所有干扰物都有可能导致仪器停机,因为每次进样都会积聚污染。如果在样品前处理过程中去除了干扰物,则可以使用更简单、更稳定的方法来分析目标化合物。如图3所示,图中比较了原始样品(上图)与使用SPE方法制备的新样品(下图)。简化样品基质的另一个优势是提高了定量准确度。图4中化合物1的顶部蓝色迹线起初看起来可以接受。但与正下方红色的空白样品基质迹线相比,它实际受到了来自样品基质的一些污染。经过适当的SPE方案处理后,下方迹线显示了不存在干扰问题的同一化合物,使定量更加准确。另一个示例如图5所示。上方迹线显示,样品基质对化合物1和2均存在显著干扰。下方迹线显示,由于使用SPE进行了适当的样品前处理,结果得到大幅改善[干净的基线]。请注意,更干净的基线有助于提高分析结果准确度。此外,如果样品需要对该化合物进行分离和纯化,则可以获得更纯净的提取物。2. 减弱MS应用中的离子抑制效应或离子增强效应复杂样品基质带来的第二个问题体现在质谱仪输出[LC-MS或LC/MS/MS]上。为获得适当的MS信号响应[灵敏度],必须形成合适的化合物离子。如果化合物离子的形成受到样品基质中干扰物的抑制,信号强度将大幅下降。可以在图6中看到这种效应。上图是注入用生理盐水制备的目标化合物溶液的信号。下方迹线显示,当分析人血浆中所含的这些相同化合物时,信号响应显著下降[抑制率 > 90%]。对于下方迹线,仅执行了常规蛋白沉淀步骤。该技术无法清除引起离子抑制的基质干扰物,导致信号响应不佳。这种抑制效应另一个很好的示例可参见图7。在MS输出的上方迹线中,血浆样品只经过蛋白沉淀步骤处理,可以看出特非那定峰受到80%的抑制。在下方迹线中,同样的样品使用SPE方法进行了处理,可以看出离子抑制效应非常小。由于去除了样品基质中的干扰物,因此能够形成合适的化合物离子,从而获得更出色的信号。有时,样品基质中的干扰物会人为增加化合物信号的报告值。这种现象称为离子增强效应,会导致误报偏高的信号值。适当的SPE方法可以清除化合物中的干扰物,尽可能减弱该效应,从而得到更准确的报告值。3. 按类别分馏样品基质以分析化合物的能力分析人员要处理的样品可能包含许多化合物,需要按不同类别分离这些化合物,以便更有效地完成进一步分析。例如,软饮料的配方中包含多种化合物。可以开发一种SPE方法来分离不同类别的化合物,例如按极性分离。极性化合物与较为非极性的化合物可以作为分离馏分收集,然后就能以更有效的方式分别分析这两种馏分,因为它们的化合物相似度较高。图8的示例说明了SPE的分馏能力。在这里,一种复杂的干粉样品[紫葡萄饮料混合物]轻松分离成四种馏分:一个仅含极性化合物的馏分、一个纯化的红色化合物、一个纯化的蓝色化合物,最后一个馏分包含所有剩余的非极性极强的化合物。本书其他地方会介绍这种能力的强大之处。4. 痕量目标物的浓缩(富集)如今,分析人员经常需要报告浓度水平远低于以往的化合物,可能低至万亿分之一[ppt]甚至更低。在纯样品中,这些浓度通常低于分析仪器的灵敏度。分析环境样品中的痕量污染物或生物体液中随时间推移形成的代谢物就是一个很好的例子。图9中的上方迹线显示,原始纯样品中目标化合物的信号响应不佳。上方迹线使用相同的分析条件,但样品是通过痕量浓缩策略中所用的SPE方法制备的,可以看到该化合物的信号强度明显增加。利用这个结果,即可准确计算出纯样品中的原始化合物浓度。如果没有SPE中色谱填料的保留能力,使用其他样品前处理方法就算可行,也很难对特定化合物进行痕量浓缩。总结正如我们所看到的,带有色谱床的SPE装置可以执行四项关键功能,从而提高样品分析的成功率。请参见图10
参数原理
2024.08.16
多肽分离的实用方法
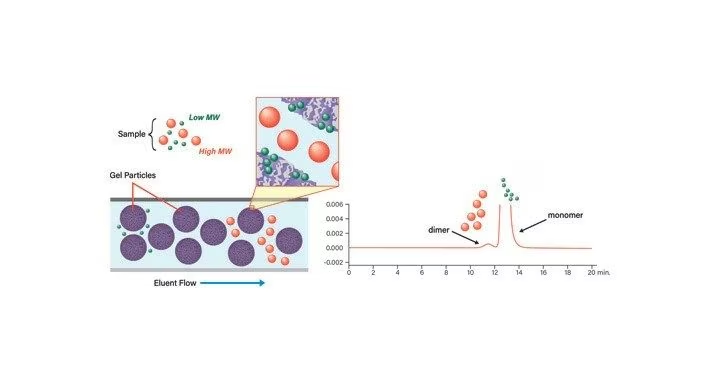
肽在新型候选药物的开发中发挥着独特作用,填补了传统小分子治疗药物与大分子蛋白质治疗药物之间的专业技术空白。肽类药物的疗效和安全性均优于小分子药物,在人体内的耐受性也更高,此外,其工艺复杂性和生产成本低于蛋白质类生物药物,作为一种有望应用于治疗多种疾病的候选药物,肽类药物受到越来越多的关注。合成肽可用于研究细胞基质间的结构-活性关系,其本身也是具有疗效的药物。无论是采用固相肽合成工艺、溶液相肽合成工艺,还是从天然产物中分离,几乎所有粗制肽混合物都相当复杂且需要进行纯化。即使小心控制合成反应,也会不可避免地形成杂质,产物中还可能含有结构缺失、截断或序列经过化学改性的变体(如裂解加合物或处理过程中形成的其他副产物)。近年来,分析方法方面的技术进步对肽作为诊断技术和新兴治疗药物的应用起到了推动作用。采用先进仪器运行分析方法可有效提高灵敏度和分离度并缩短运行时间,这些优势均有助于我们在生产过程中节省大量时间。有关合成肽的一大棘手问题是分离方法的开发。对于未来研究,纯度和目标肽产率是影响实验结果的关键因素。如前文所述,合成肽在合成、裂解和去保护过程中可能会产生数量相当多的杂质。应用分析级HPLC的方法开发原理可改善肽产物的分离效果。开发制备级纯化方法运用的分离机制与开发小规模方法时需遵循的原则相同。色谱柱和流动相改性剂的选择、温度控制以及梯度优化是开发任何分离方法时都必须考察的内容。通过系统方法开发流程开发肽分离方法可显著提高产物纯度和收率。传统的肽分离通常采用UV引导的色谱方法,而将质谱引导的分离方法与严谨的方法开发流程相结合,可以更加明确地区分目标肽与合成及裂解过程中形成的污染物,从而使纯化过程变得更加轻松。肽纯化过程的要求任何分离策略的目标都是在尽可能短的时间内纯化尽可能多的样品,同时达到后续实验所要求的纯度。对于需要合成多种肽的典型实验室而言,制定适用于大部分样品并且可根据需要进行简单优化的标准纯化方案将十分有用。若能在改变流动相组成、改性剂或柱温时确保运行间的性能保持一致,将省去设置多组色谱柱的时间。这种提高收率和纯度的方式既经济又直接,且易于实施。理想的肽纯化方案还会使用能兼顾分析级和制备级分离的稳定仪器。对于流速范围较广的通用型仪器,仅通过改用直径匹配分离目标的色谱柱就能提高纯化效率。综合考量上述各因素可降低肽纯化的整体成本。肽分离工作流程肽分离标准方案(图1)的第一步是确定后续实验要求达到的肽纯度。通过粗制肽分析可合理估算样品纯度,结合该结果与后续研究所需的纯肽量即可估算出载样量。载样量将决定制备色谱柱的规格,继而会决定选定LC仪器的流速。粗制肽分析完成之后的步骤是将方法几何放大至具有相同填料的大规格色谱柱上用于分离。图2中的放大公式展示了在不同规格色谱柱之间转换分离方法时,色谱柱直径、柱长、载样量和流速之间的关系。梯度斜率表示为单位柱体积对应的溶剂变化百分比,而非单位时间内溶剂变化的百分比,可确保梯度方法从初始条件到最终条件的各个步骤输送的柱体积数量始终相同,从而保持分离度一致。制备级方法必须包括一段用于模拟系统延迟的起始条件保持时间,具体将通过小规模分离确定,同样以柱体积数量表示。制备型色谱分离完成后,将对收集到的馏分进行分析评估。纯肽的后续处理应遵循用户指南。肽分离完全可以采用配备泵、进样器、UV检测器和馏分收集器的简单液相色谱系统进行(图3)。虽然并不是肽分离必须采用的技术,但质谱检测可鉴定目标肽并减少分离之后需要进行分析的馏分数量。无法电离或难电离的化合物通常采用短波长UV检测。相反,UV吸光性极差的肽通常可由MS轻松检出。纯化过程注意事项分离模式由于不同肽的特性各异,分离可用的色谱模式也有许多选择。尽管反相色谱是目前应用最广的肽分离模式,但使用离子交换色谱或体积排阻色谱等替代选择方法来分离某些肽会更加高效。这些替代技术也可与反相色谱联用,制定专用于棘手样品的两步分离方案。反相色谱反相色谱因其重现性好、适用性广的优势被广泛应用于多种类型化合物的分离,其中也包括肽的分离。非极性的C18-键合硅胶是相当常用的一类反相色谱柱填料。反相色谱流动相通常由水和可与水混溶的极性有机溶剂(例如乙腈或甲醇)组成,这种流动相会根据化合物极性从C18色谱柱上洗脱化合物。因此,肽本身的疏水性越强,它在C18色谱柱上的保留性就越好。虽然C18是相当常用的反相填料,但其他一些键合相(C4、C8、RP18、苯基等)也可与基质颗粒键合,为优化化合物分离提供替代选择性。硅胶是最早问世的反相色谱柱填料之一,但硅胶基质填料会限制分离速度、分离度、pH、温度耐受性以及色谱柱载样量。采用获专利的*杂化颗粒技术开发的新型色谱柱基质颗粒能够在更高的流速、温度和pH下运行,同时提高选择性、分离度、重现性并延长色谱柱寿命。*美国专利号6,686,035 B2离子交换离子交换色谱从很早开始就被用于蛋白质及其他生物制剂的分离。由于组成肽的氨基酸带有正电或负电,因此可采用离子交换色谱进行肽分离。经过官能化的天然聚合物树脂(如琼脂糖)和合成聚合物(如聚甲基丙烯酸甲酯(MMA),或苯乙烯-二乙烯苯共聚物)是大分子分离的常用介质,因为这些填料可承受大规模生物处理的工艺周期和批次之间极为严苛的清洁处理。上述工艺采用的氢氧化钠溶液会损坏小分子和小规模肽分离常用的硅胶基质填料。离子交换剂可分为四种:弱阴离子交换剂、弱阳离子交换剂、强阴离子交换剂和强阳离子交换剂。阳离子交换模式用于保留并分离带负电表面上的正电荷离子,而阴离子交换模式则用于保留并分离带正电表面上的负电荷离子。强阴离子和强阳离子交换色谱柱可在较宽的pH范围内(2–12)完全离子化,而弱离子交换色谱柱只能在较窄的pH范围内(9.5–5.5)离子化。相较于阴离子交换模式,阳离子交换模式更常用于肽分离,但具体选用哪种模式取决于肽序列。在pH小于3的条件下进行肽分离时,氨基酸侧链羧基上的负电将被中和,同时N-端基团质子化,使得肽带上正电荷,进而被吸引至阳离子交换色谱柱上的负电位点(图4)。反之,对于适合在pH 6-10的条件下进行分离的肽,应采用阴离子交换模式。在较高pH条件下进行阴离子交换时,肽上的羧基带负电,因此会被吸引至阴离子交换色谱柱上的正电位点(图5)。为应用离子交换技术的肽分离方法选择色谱柱和进行方法开发时,应遵循几条一般建议。阴离子和阳离子交换模式均可使用,基本原则是:分离酸性肽采用阴离子交换模式,分离碱性肽采用阳离子交换模式。对于某些肽,可能需要反向运用该原则(尤其是分子量较大的肽),但必须通过调节pH使肽所带的净电荷与填料所带的电荷相反。无论极性如何,强交换剂都是肽色谱分离的首选。肽的带电情况是序列和带电侧链所处微环境共同作用的结果。针对具体的肽序列,可通过小幅调整流动相pH来调节分离的选择性。选择性的小幅调整不会影响强离子交换剂的结合能力。离子交换分离是作为两步纯化方案中的第一步还是作为单步分离方案用于制备实验材料,会影响流动相和操作条件的选择。如果离子交换分离的产物将通过反相色谱进一步纯化,则可以采用蛋白质离子交换方案常用的缓冲液和洗脱条件,例如使用磷酸盐或Tris缓冲液并采用氯化钠梯度进行洗脱。产物中的盐将通过后续步骤去除。如果要通过离子交换法一步得到可用的肽,应谨慎选择可通过冻干去除的挥发性缓冲液。甲酸铵是理想选择,因为它具有分别对应铵盐和甲酸盐pK值的两个缓冲区域。甲酸铵既可在pH 3-4的条件下用于碱性肽的阳离子交换色谱分离,又可在pH 9.25-10.25的条件下用于酸性肽的阴离子交换色谱分离。在pH恒定的条件下,可利用甲酸铵浓度逐渐升高的离子强度梯度来洗脱目标肽。另一方面,利用pH梯度进行洗脱则能够省去通过冻干去除高离子强度缓冲液的耗时操作。同样地,甲酸铵缓冲液是很好的起始缓冲液。采用阴离子交换剂分离酸性肽时的洗脱梯度为pH从高到低,采用阳离子交换剂分离碱性肽时的洗脱梯度则为pH从低到高。体积排阻色谱根据分子大小进行色谱分离的技术如今被称为体积排阻色谱(SEC),该技术可追溯至20世纪50年代。这种分离技术基于分子大小进行色谱分离,而非基于分子的带电情况或极性等化学特性,过去也被称作凝胶过滤或凝胶渗透色谱(GPC)。具有特定孔径分布的固定相颗粒可阻止大于柱床孔穴的样品分子进入,从而使其快速洗脱出来,小分子则会进入孔穴中并深入更复杂的结构,洗脱速度较慢。因此,大分子最先洗脱,小分子则根据其在溶液中的大小以降序顺序洗脱出来(图6)。SEC是一种低分离度技术,采用等度方法且运行之间无需进行平衡。色谱柱载样量取决于样品体积和浓度,而这两个因素都会影响分离度。SEC有时会作为初始净化步骤用于去除截断序列、去保护不彻底的肽以及其他杂质。随着合成肽的序列长度增加,上述污染物的数量也会大幅增加。在反相分离之前执行任何简单的初始纯化步骤都有助于简化色谱分离。SEC还可用于缓冲液更换,也就是将当前溶解肽的缓冲液更换为更适合后续实验或纯化步骤的其他缓冲液或溶液。总结肽分析和分离可采用多种不同的色谱技术,包括反相色谱、离子交换色谱和体积排阻色谱。半制备级分离(分离量为几毫克至几百毫克)通常采用反相色谱技术。本文后续部分将围绕肽分离展开,重点介绍可利用哪些相关因素和技术对应用反相色谱分析和纯化肽的方法进行优化。
参数原理
2024.08.16
什么是质谱?质谱是怎样工作的?
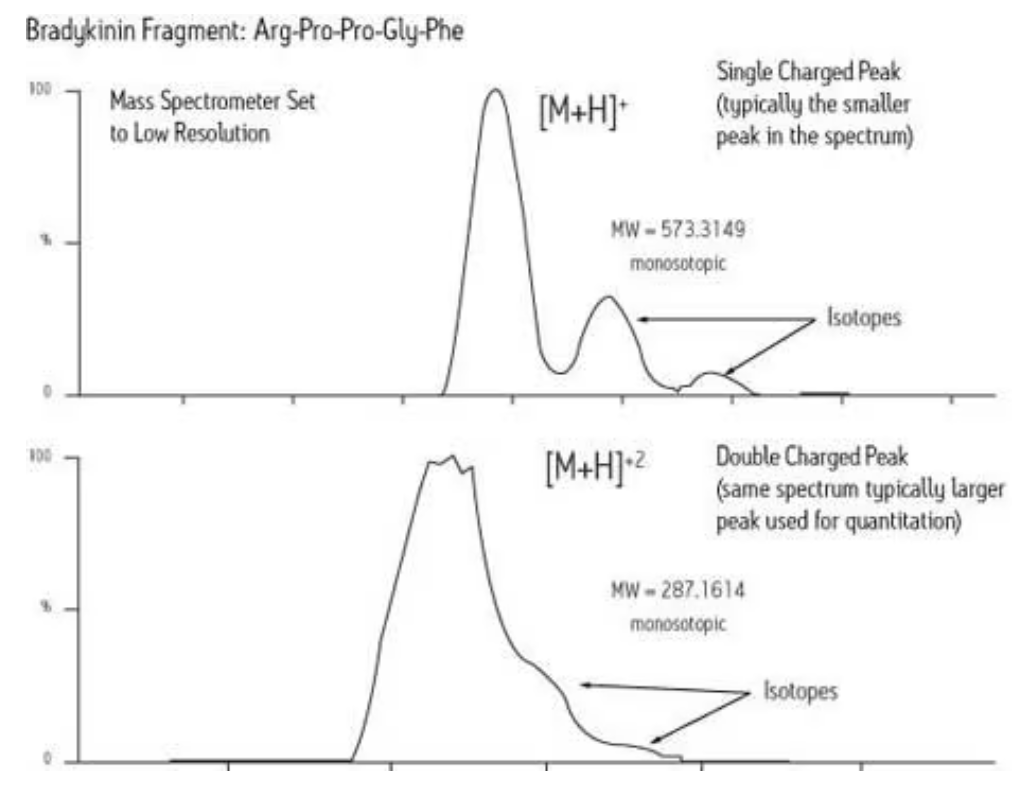
质谱仪可能小如一枚硬币,也可能占据一个非常大的房间。尽管各种仪器类型用于截然不同的应用,但它们的一部分工作原理仍是相同的。现已采用道尔顿(Da)取代其他术语(例如amu)作为质谱测量单位。1 Da = 一个碳12 (12C)同位素原子质量的1/12。过去质谱仪只用作辅助化合物鉴定的定性设备,人们一度认为它不能准确定量。但近年来,质谱仪已被证实是一种集定性和定量能力于一体的仪器。使用质谱仪测定分子的质量时必须先将分子转化为气相离子。为此,质谱仪会向分子传递电荷,并将由此产生的带电离子流转换为成比例的电流,然后通过数据系统读取该电流。数据系统将电流转换为数字信息,以质谱图的形式呈现。a)以类似色谱图的形式呈现出不断增大的总离子流(TIC)丰度随时间推移而发生的变化。b)峰的每个数字切片都代表当时构成离子流的离子,这通常被称为轮廓图或连续采集。此时x轴(或“时间”轴)是质荷比(m/z),很明显可以看出分辨谱图中相邻离子(如同位素)的能力。c)轮廓图质谱图通常又可简化为“棒状图”,棒状图由从每个峰顶点处绘制的质心表示,能够减少存储文件的大小,有利于增加分辨率信息。可以通过多种适合目标分析物的方式生成离子:将溶于基质的化合物上样至平坦表面进行激光烧蚀,例如MALDI让化合物与高能粒子或电子相互作用,例如电子轰击电离(EI)将电离作为传输过程本身的一部分,例如我们已经了解的电喷雾电离(ESI)技术会对液相色谱仪的洗脱液施加高压,从而在气溶胶中生成离子质谱仪将根据离子的质荷比(m/z)对离子进行分离、检测和测定。绘制相对离子流(信号)与m/z的关系图,生成质谱图。小分子通常只带一个电荷:因此m/z是质量(m)除以1的值。“1”代表电离过程中添加的质子[表示为M+H+,如果通过失去质子形成离子,则为M-H-],如果离子是通过失去电子形成的,则表示为自由基正离子[M+.]。不同质谱仪的准确度或实际测定真实质量的能力可能会有所不同,相关内容请参阅本入门指南的后面部分。较大的分子在其结构内的多个位置捕获电荷。小分子肽通常可带两个电荷(M+2H+),而非常大的分子有许多位点,因此可以通过简单的算法来推断谱图出现的离子的质量。经正确校准后,低分辨率仪器可以提供非常准确的质量数,但由于分辨率空间有限,随着数据堆集,可提供的有关谱图的信息也逐渐减少。缓激肽(一种9氨基酸肽)的常见代谢片段BK1-5(即Arg-Pro-Pro-Gly-Phe,是一种ACE(血管紧张素转化酶)抑制剂,用于扩张血管)可携带两个电荷(单电荷(M+H)产生单同位素质量数573.3149,而双电荷版本(M+2H)的质量数为287.1614)。同位素带双电荷,也开始填充可用的分辨率空间。可分析的分子大小上限是多少?解吸方法(已在本入门指南中介绍)扩展了分析大分子、非挥发性、易碎分子的能力。在40,000 Da范围内以0.01%的准确度(或4 Da以内)进行常规检测可以确定微小的变化,例如翻译后修饰。多电荷态使质谱仪远远超出其设计范围上限,包括1,000,000 Da及以上的质量。同位素和元素质谱天然同位素丰度已得到充分表征。尽管通常认为该参数较稳定,但它仍然可以显示出显著的特征差异。同位素比测定被用于代谢研究(使用富含同位素的元素作为示踪剂)以及气候研究(测定与温度相关的氧和碳变化)。在实际应用中,使用高精度功能(如扇形磁场仪器上的功能)分析复杂分子之前要先将其碎裂为简单的分子组分(请参阅下一节)。元素分析通常用于分析无机材料 - 旨在确定元素组成,而非结构 - 在某些情况下使用固体金属样品。在使用放电装置(或低功率辉光放电装置)来电离样品的应用中,电感耦合等离子体(ICP)离子源很常用。使用专用仪器在ppt水平行检测的应用并不少见。
操作维护
2024.08.16
十四大质谱常见问题及处理方法
1、质谱不出峰的可能原因?答:1)进样系统与离子源没连接或有漏液2)六通阀漏液3)雾化气没开4)喷雾电压没有5)离子进入分析器的离子通道堵塞6)喷雾毛细管堵塞2、如何根据样品选择离子源?答:可根据分子量的大小、极性。APCI适合小分子,极性小的化合物;ESI适合分析的分子量范围较大、分子要求带有一定极性。一般先考虑用ESI分析,如果极性实在太小,才想到用APCI。3、等度还是梯度洗脱如何选择?答:其实只做一两个化合物,是等度洗脱好,速度快,但也并非越快越好,特别在分析生物样品时,考虑到基质效应,保留因子控制在2-3左右较好。梯度洗脱适合分析多个结构不同的物质,如化合物与代谢产物一同鉴定的时候,比如苷和苷元的一同测定。另外很多做合成化学的分析实验室用的也是一通用的梯度洗脱方法,一个方法搞定大部分样品。一般来说对于组成简单的样品可以采用等度洗脱,而对于那些复杂的样品分离通常需要进行梯度洗脱。4、气质和液质系统对比?答:除了采用的分离手段不同(气相和液相)外主要的区别在于真空系统和电离方式。气质的真空系统比较简单,只要一个小的机械泵和一个分子涡轮泵就可以了。液质的机械泵要比气质大,需要两个分子涡轮泵。气质的电离方式有电子电离(EI)和化学电离(CI)。液质的电离方式有电喷雾电离(ESI)、大气压化学电离(APCI)和大气压光电离(APPI)。5、APCI和ESI的不同点?答:1)离子产生的方式不同。APCI利用电晕放电离子化,气相离子化。ESI利用离子蒸发,液相离子化。2)能被分析的化合物类型不同。APCI适合弱极性,小分子化合物,且具有一定的挥发性;ESI 极性化合物和生物大分子。3)流速不同。ESI一般流速较小,约0.001到0.25 mL/min,APCI 相对较大,约0.2到2 mL/min。4)多电荷。APCI不能生成一系列多电荷离子,所以不适合分析大分子;ESI 能生成一系列多电荷离子,特别适用于蛋白,多肽类等生物分子。6、CID和CAD区别?答:CID,碰撞诱导解离。通常在真空接口处调节电压发生CID现象,一般是去除溶剂,如果电压增大,也会产生碎片离子。这是一级质谱的原理。CAD碰撞活化解离。做二级质谱时,选择的母离子进入Q2后,碰撞活化产生子离子,这个过程称为 CAD。以API3200谱仪为例,CID指的是Q0里面的诱导碰撞的气体,CAD指的是Q3里面的诱导碰撞气体。也就是说,在这里的CID&CAD都是指氮气。7、氮气发生器该使用吗?答:氮气发生器的工作原理是分离空气,电解膜的负极侧发生氧化反应,“吃掉”空气中的氧化性气体,在正极侧还原,空气流过电解池后就只剩下氮气和惰性气体。故国内发生器的纯度大多标有“相对含氧量”。氮气的纯度和空气流速、有效分解面的长度、电解电势的强弱都有关系。这种分离方法也决定了氮气的纯度不可能做的很高。加入电解质的作用就是提高水的导电率,使电化学反应能顺利进行。发生器对质谱的影响有一点常常被忽略,就是发生器内的开关电源工作时会对电网电压造成一定的干扰(压缩机的启动和停止也会)。8、串联质谱如何定量?答:串联质谱定量时,是以后面产生的碎片峰(子离子)定量。但是这一子离子是由母离子在碰撞室产生的特征性碎片,所以用MRM定量灵敏度会比用SIM定量好很多。建立方法的步骤是:用一定溶度的标准品溶液(1-10 ug/mL)调谐化合物的一级质谱条件,找到母离子的最佳质谱条件。然后对母离子进行打碎,优化碰撞能量,得到其特征性的子离子。最后利用该质谱条件和该母离子->子离子对进行定量。9、质量偏差怎么办?答:质谱的质量数偏了,说明你的仪器该校正了,一般3个月就要校一次机。一般每个厂家都会随机带有校正液。10、如何更换机械泵油?答:一般3个月到半年更换一次泵油,可同时停机对仪器进行一次清洗。更换泵油的时候,先开启振气阀5-10分钟,待将泵内沉淀振起后,关闭振气阀,同时关闭电源。打开泵下的泵油排放阀门,放掉旧油。如果泵油已经很脏,则可取少许新油清洗泵后放掉再注入新油。11、产生碰装室离子交互影响(Collision Cell Cross Talk)的原因及消除?答:多通道扫描(MRM)时,如果两个离子扫描通道的碎片离子一样(或类似如相差1-2分子量单位),前一个离子通道扫描结束后,碰装室里的离子来不及清除,影响下一个离子通道反应的定量(如果色谱分离完全则无此影响)。可能的消除方法:1)选择特异的子离子(特别是在用稳定同位素内标时)2)增加离子通道扫描反应之间的时间间隔(如100 ms→300 ms)3)可设置额外的“无用的离子扫描通道(dummy MRM)”12、排除色谱柱流失问题的最佳方法是什么?答:诊断色谱柱是否存在流失问题的方法是第一次在方法条件下安装色谱柱时,做一次空白色谱图,然后将最近的运行和空白运行色谱图对比。如果在空白运行中产生了很多峰,则色谱柱性能改变,这可能是由于载气中含有氧气,也可能是由于样品残留。如果有 GC-MS,则低极性色谱柱的典型流失离子(例如 DB/HP-1或5)质/荷比m/z 将为 207、73、281、355 等,大多数为环硅氧烷。13、谱图为什么只有溶剂峰?答:可能有以下原因1)进样针损坏2)载气流速太低3)样品浓度太低4)样品被柱或进样器衬套吸附14、质谱基线高是什么原因?答:质谱的基线其实跟液相的紫外检测器和荧光检测器一样,基线高的原因不外乎内部和外部的原因。1)选择的流动相在质谱的响应比较高,比如水相比较多的时候,噪音比较大些;还有如果盐含量比较大的时候,噪音更大些。2)检测器的灵敏度越高的时候,噪音应该越高。如果质谱的污染比较严重时,基线肯定比较高。比如离子阱检测器,用得久了,阱中的离子就会增多,一方面降低了质谱的灵敏度,另一方面增加了基线噪音。3)质谱的基线很多时候还跟你选择的离子宽度有关。比如作选择离子扫描的时候,基线就低些。作选择反应扫描的时候,离子宽度不要选得太宽,太宽噪音就高些。4)多级质谱一般做二级或三级质谱,基线噪音就低很多。
操作维护
2024.08.02
Agilent 6890 气相色谱仪色谱柱维护
色谱柱在不使用时要安全保存起来。 安全保存中有两大要点: 1. 保存柱子切勿划伤。划伤后的柱子可能由于高温加热而足以使之 从划痕处断裂。 2. 堵上柱子两端以保护柱子中的固定液不被氧气和其它污染物所污 染。 当使用熔凝硅柱时,记住这是一种玻璃材质,一定注意保护眼睛。固定相(交联的硅氧相)允许我们使用溶剂淋洗柱来溶 掉或移走柱上的沉积物,这样可以避免峰拖尾。 毛细管柱淋洗贮罐 进样口石墨垫作用 石墨垫的作用 色谱柱与色谱系统的连接处靠密封垫密封.理想的密封垫 提供无泄漏的密封效果,适合各种外径的色谱柱,不用过 分拧紧,与色谱柱或接头不粘连,且耐温度变化。为什么要更换石墨垫?石墨垫损坏会造成:水,空气渗入系统,破坏色谱柱, 样品损失, 出鬼峰, 污染质谱仪 如何避免出现问题 先用手拧紧柱帽,再用扳手拧紧. •保持清洁,避免手印,油的污染. •用放大镜检查是否有破损,裂纹.自动进样器常见故障及解决方法日常维护 、经常检查进样口隔垫 、清洗检查进样针 、清洗样品盘、机械臂上的灰尘、 清除样品盘周围的异物- 常见故障 1. 重现性不好:样品粘度,抽样速度,排汽泡 2. 样品残留: 增加洗针的次数(溶剂洗针,样品洗针) 3. 污染和鬼峰:彻底清洗进样针,更换进样垫和衬管 4. 注射器故障:换针日常维护-GC系统推荐的维护时间表
操作维护
2024.08.01
Agilent 6890 进样口详解
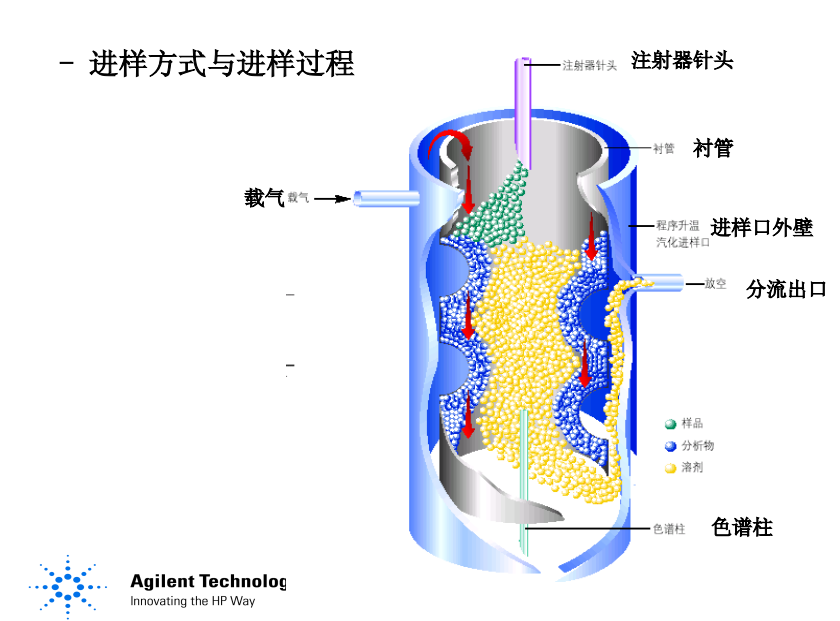
进样口结构进样方式与进样过程为了保证分流比的概念真实有效, 样品(溶剂+被分析物)必须与载 气充分混合,形成一个均匀的混合 物。 这一混合物的一小部分将会从进样 口的底部进入色谱柱,而大部分的 混合物则会从分流出口流出。如果进样量过大,溶剂会膨胀为 很大的体积,致使进样口衬管过 载。 其结果必将导致样品从吹扫出口 流出而造成样品损失,同时也会 造成载气输入管路的污染。
参数原理
2024.08.01
waters UPLC HPLC使用方法
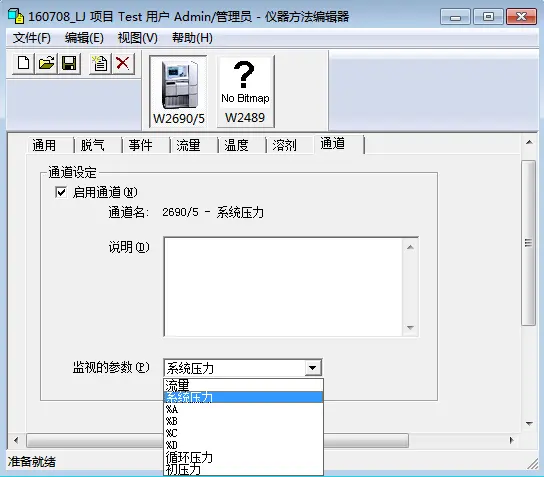
1、在图1所示的“仪器方法编辑器”界面上部列出色谱系统的配置,通过点击不同的仪器模块可对其进行仪器方法编辑。仪器方法编辑主要是:分离模块的方法编辑和检测器的方法编辑。分离模块的方法编辑主要包括:通用、脱气、时间、流量、温度、溶剂和通道。在“通用”界面中可根据实验方法要求的流速来设置“输送体积”的大小(如图2所示),例如流速为1.0ml/min时将“输送体积”的大小设为50微升。也可根据不同的样品性质更改自动进样器的“注射器吸取速度”(如图3所示)以及进样针“针头的清洗时间”(如图4所示)。注意:当使用玻璃内衬管时,需要将进样针的“针头深度”进行调整,此时需要将“针头深度”调整为2(如图4所示)。正常:2.5ul/s缓慢:1ul/s快速:5ul/s正常:13 s双:26 s延长:52 s如系统配备氦气脱气装置,可在“脱气”一栏的“喷射”中设置每一路溶剂的氦气通入流量。如配备在线脱气机可在“脱气”中选择“脱气模式”为开或关如图5所示。如下图所示,在“流量”界面可设置此方法运行的“压力限制”,超出此压力范围则系统会报错停止运行。在“设定的流量”一栏可选择“泵模式”为“等度”(如图6所示)或是“梯度”(如图7所示),也可设定相应的泵流速以及各相的比例等。在“泵模式”为“梯度”(如图7所示)时,可设置某一时间段内流动相梯度变化的曲线,具体的曲线模式如图8所示。在如下图9所示的“温度”选项卡中勾选“柱温”则可设置柱温箱的设定温度,“柱温范围”是指柱温箱的温度控制在目标温度上下浮动柱温范围之内。如配备样品盘控温模块亦可设置“样品目标温度”。Empower在运行样品采集数据时也可设置其他“监视的参数”,如“系统压力”。一般而言,通过观察色谱系统的系统压力可以判断样品在运行期间仪器状态是否正常,因此可在方法编辑的时候勾选通道内的“启用通道”,在“监视的参数”中选择“系统压力”,如下图10所示。
操作维护
2024.07.31
光谱仪的工作原理是什么,都有哪些种类?
光谱学是一个广泛的领域,包括几个不同的子学科和广泛的技术,每一个都会使用高度专业化的设备。对应光谱仪的分类,是一个很大的话题,有按照原理来分类的,也有按应用分类的,同一原理可以做成不同的应用,不同的应用领域,也有可能由不同的原理来制成。光谱仪的应用是涉及天文、地理的,了解它的人也必须要上知天文,下知地理,我相信没有人能单独言尽其详。我按照自己的认知分类如下:1、光学吸收型光谱仪这类光谱仪是我们最常见的一种光谱仪类型,也是我们常规意义上理解的光谱仪。通常这类光谱仪可以通过棱镜色散原理或者光栅分光原理,将光源发出的光(由连续光谱、发射光谱(亮线)或吸收光谱(暗线)组成)按照波长(或频率)分离得到横轴为波长(或频率)纵向为强度的谱线图2、光学发射型光谱仪光学发射光谱仪(通常称为“OES或火花放电光谱仪”),可以得到非常高精度地确定金属物质的化学成分,通常用于评价金属。电火花通过高压施加在表面,使粒子汽化成等离子体。粒子和离子发出的辐射由探测器(光电倍增管)以不同的特征波长测量。3、电子光谱学光谱仪有些形式的光谱学分析的是电子能量而不是光子能量。x射线光电子能谱就是一个例子4、质谱仪质谱仪是一种分析仪器,通过测量气相离子的质荷比和丰度来确定样品中存在的化学物质的数量和类型5、飞行时间光谱仪已知质量的粒子的能谱可以通过飞行时间光谱仪测试两个探测器之间的飞行时间(得到速度)来确定。另外,如果速度已知,则可以用飞行时间质谱仪测定质量。6、磁谱仪当一个快速带电粒子(电荷q,质量m)以直角进入恒定磁场B时,由于洛伦兹力,它被偏转到半径为r的圆形路径。粒子的动量p由其中m和v是质点的质量和速度;下图所示是最古老、最简单的磁谱仪,由J. K. Danisz发明的半圆磁谱仪。其中,恒定的磁场垂直于页面。动量为p的带电粒子通过狭缝,偏转成半径为r = p/qB的圆形路径。结果是它们都在几乎相同的地方,也就是焦点处碰到了水平线;在焦点处放置一个粒子计数器,改变不同的磁场B,用α粒子谱仪测量得到α粒子的能谱,β粒子能谱用β粒子谱仪来测。
参数原理
2024.07.31
质谱是怎样做到定量的?
1. 质谱信号强度与待分析物含量的关系任何定量分析方法都需要建立实验测量信号与待分析物的量的关系。很幸运的是,在质谱中,通常也可以建立这样的关系,因此质谱信号是可以用于定量的。从题主的说明来看,Ta的疑惑主要在这里。既然问题是“质谱是怎样做到定量的?”,我们不妨把质谱信号的产生按时间顺序粗略分为三个步骤,即离子的产生,传输与检测。产生离子时,不同样品分子的电离通常是相互独立的。因此样品量越多,其产生的离子也就越多。目前常用的各种离子化方法(EI、ICP、ESI、MALDI等)在实验中(严格来说仅在一定浓度范围内——术语是动态范围,dynamic range)都至少满足样品量与产生离子量的正相关,一般情况下也可以进一步近似成线性相关。传输离子时,简单来说可以认为传输效率与被传输离子的量无关;(严格地说,被传输的离子太多时,相同电荷的互相排斥会造成离子束的“体积”变大,导致传输效率下降。这种影响在空间有限的离子阱中表现得更加明显,因此在离子阱质谱中一个重要的技术就是适当控制进入仪器的离子数量,使其既不太少也不太多。)检测离子时,不论是使用光电倍增管的检测器,还是检测镜像电流的检测器(ICR/Oribtrap),其信号强度(在一定范围内)均与离子数量大致线性相关。废话几句,可能会使题主感觉质谱不能定量的原因之一是,我们看到的质谱图常用相对强度作为纵坐标,即0-100%最强峰,而不展示信号的绝对强度。但在做质谱的时候,仪器记录的当然是绝对强度(相对强度也是通过绝对强度换算出来的)。我们需要用绝对强度来定量时,就需要这部分平时不常看的信息了。另外,在谈到色谱-质谱联用方法时,待分析物与实验测量信号的关系之中又多了一层色谱,即待分析物含量->色谱流出物中样品含量->质谱信号。与EI谱图分析以相对强度为主不同,在色谱-质谱联用时,信号的绝对强度就成了我们天天都要关心的内容,因为质谱信号强度随时间的变化就是实验的色谱图,通常以总离子强度或者某一特定质荷比离子的强度作图2. 定量的两种方法说过了为什么质谱可以定量,下面我们来看看具体的定量方法。常用的定量方法有两种,外标法与内标法。外标法用已知量的标准样品A和未知量的待测样品A分别进行实验;我们会得到以下三个信息:标准样品的量(已知);标准样品的信号强度;待测样品的信号强度。(假设样品的响应=常数*浓度,从这三个信息即可算出待测样品的量。)为了更加精确地测定未知量的样品,我们希望标准样品的信号强度与待测样品的信号强度尽量接近(以减少非线性响应的影响)。因此常用的外标法会测量一系列已知量的标准样品,绘制一条工作曲线,再用拟合的方法确定未知样的量。内标法外标法主要有以下两方面的局限:1标样和待测样是独立进行实验的,实验间的偶然误差无法消除;2标样和待测样的基质(即除待分析物外的其它成分)不同,基质有可能会带来不同的影响,也会产生误差。那么,如果我们把已知量的标准样品B直接加入待测样品A,就可以把标准样品和未知样品的测定在同一次实验和同样基质中完成,也就消除了两次实验和基质不同造成的误差,这就是内标法。(如果加入的标准样品和待测样品是同种物质A,那么由于它们不可区分,只通过一次实验是不能定量待测样的,这时我们在加入标样前后分别进行两次测量,即测量待测样及待测样+标样的信号,即可计算出待测样的量。)3. 质谱相关的特殊定量细节同位素稀释前面内标法的介绍中我们可以发现,最理想的内标物既要和待测样相同(具有相同的响应系数)又要不同(仪器可以区分二者的信号),这对矛盾的集合体就是同位素内标。由于不同同位素的化合物具有近似相同的物理化学性质,离子化时的响应通常也是相同的,而它们具有不同的质荷比m/z,即可在质谱中被区分出来。因此同位素标准品是最理想的内标物。另外,由于某些元素的天然同位素分布有一定的比例,当我们加入一定量的同位素内标时,可以把对信号绝对强度的测量转化为对信号相对比例的测量,从而提高实验的准确性。选择反应监测在不太复杂的体系中,我们只要按照分子量就可以定性某种化合物了。但对于复杂混合物(如石油产品/生物样品)而言,很多化合物具有相同或相近的质量(同分异构体质量完全相同,有些化合物分子量非常接近,如CO和N2,要考虑仪器的质量分辨率是否能区分二者),此时仅靠测量质量就不能确定这个化合物是否就是我们关心的“the one”了。在串联质谱 (Tandem MS) 仪器中,我们不仅可以把质谱仪理解为一个称量离子的“天平”,它还具有了离子“镊子”(选择某个特定的离子把它分离出来)和“剪刀”(把某个/某些离子激活并打成碎片)的功能。通过母离子和子离子的两步选择,我们可以在复杂体系中精确定位到我们关心的化合物,同时,两次离子选择还可减少复杂基质的干扰,降低背景噪声(获得更低的检出限)并提高方法的动态范围。因此选择反应监测是目前色谱(气相色谱/液相色谱)-质谱联用中最常用的定量方法。
参数原理
2024.07.23
浅谈离子色谱仪的结构、常见故障及处理方法
离子色谱是分析阴离子和阳离子的一种色谱方法,广泛应用于化工、医药、环保、半导体制造等各个领域。在使用离子色谱实际测定工作中会遇到的各类异常现象,需要实验人员能够快速的识别排查各类异常现象并即时做出处理,从而确保分析数据准确可靠,因此具体探讨国高材分析测试中心中的离子色谱仪的基本结构,常见故障及对应的处理方法,方便大家在使用离子色谱测定过程中遇到相同的故障情况时可参照此方法来排除故障,从而提高实验室的工作质量和工作效率。一、原理及基本结构:原理:离子色谱采用离子交换的原理,借助薄壳型离子色谱柱快速分离多种离子,由串联在分离柱后的自再生抑制器除去淋洗液中的强电解质以扣除其背景电导,再用电导检测器连续检测流出液的电导值,得到各种离子的色谱峰,达到分离、定性、定量分析的目的。结构:离子色谱仪一般由图1所示的各部分组成。其中输液系统主要由贮液罐、高压输液泵组成;进样系统分为手动进样和自动进样;分离系统主要由离子色谱柱(阴、阳柱)组成,主要起分离作用;检测系统主要由抑制器、检测器组成。离子色谱仪的组成示意图二、常见故障及解决办法:离子相色谱仪在使用的过程中难免会出现一些故障,有一些相对简单的故障,只要我们知道原理,使用逻辑推理的方法,逐—排查,寻找问题所在,然后根据故障的类别、大小,采取相应的解决措施,就可以自己进行维修,从而缩短仪器的故障周期提高使用效率。下面主要针对离子色谱仪日常分析工作中一些简单故障的排除进行说明。2.1压力问题2.1.1压力增高通常以下情况会导致系统压力增高:一是保护柱压力高。二是色谱柱压力高。三是流速设定过高。四是进样阀损坏或堵塞。五是泵的单向阀堵塞。排查方法:通常按照以下方法进行排查哪个原因引起的压力增高:①在1.0流速下先记录仪器总压力P;②先断开保护柱入口,记录压力P1;③接上保护柱入口,断开保护柱出口,记录压力P2;④连接保护柱出口,断开色谱柱出口记录压力P3;⑤连接色谱柱出口,断开抑制器淋洗液出口记录压力P4;⑥连接抑制器淋洗液出口,断开抑制器再生液入口,记录压力P5。按照上述进行排查记录压力后,用总压力P分别减去P1、P2、P3、P4的压力后和各个组件部位正常的压力进行比对,就能排查出哪个组件引起的系统压力高。2.1.2压力降低通常以下情况会导致系统压力降低:一是流动相气泡干扰。处理方法:流动相要经过脱气处理。二是系统漏液。处理方法:详细处理方法见3.2进行处理。三是流速设定过低。处理方法:按照色谱柱分析报告设置流速。四是柱温过高。处理方法:按照色谱柱分析报告设置柱温。2.2漏液问题常见漏液处:一是接头处漏液。处理方法:①接头处有卡痕松动,切掉前段部分,再将其重新连接上;②接头磨损,要进行更换。二是泵漏液。处理方法:①泵密封损坏,密封圈漏液,进行更换密封圈;②排气阀漏液,需要重新拧紧。三是检测器手紧接头处漏液。处理方法:重新拧紧。四是:抑制器漏液。处理方法:①接头漏液,重新拧紧;②侧边漏液,更换抑制器。2.3背景电导偏高问题通常以下情况会导致背景电导偏高:一是淋洗液基体中有高电导的物质。处理方法:将纯水重新处理并更换淋洗液。二是抑制器损坏,无法起到抑制背景电导的作用。处理方法:更换抑制器。三是电导池中结晶有固体电解质。处理方法:将电导池取下,滴加一滴1:1的硝酸,再用去离子水冲洗干净,在重新装上去。2.4基线漂移大问题分析原因:一是温度波动。处理方法:尽量使室温保持恒定,采用恒温装置,使柱温恒定约30-60min;二是流动相不均匀。处理方法:进行脱气处理,使用纯度更高的试剂。三是流动相配比不当或流速变化。处理方法:检查流动相的组分及流速是否按照色谱柱分析报告进行配置。2.5基线噪声大问题分析其原因:一是流动相污染、变质或由低质溶剂配成。处理方法:更换流动相,使用纯度更高的试剂。二是系统内有气泡。处理方法:打开排气阀门,增大流量排净液缸中的气泡,逐级断开连接口,排掉流路中的气泡。三、使用与维护离子色谱使用维护可以从长期未使用及日常使用进行展开。3.1仪器长时间未开机通常情况下仪器长时间未开机按照以下操作对仪器进行使用维护:①使用去离子水按照抑制器活化步骤进行活化;②按色谱柱要求配置淋洗液;③换上淋洗液,将泵开启,接上保护柱和色谱柱;④用0.3ml/min流速运行1-2h;⑤将泵流速逐渐调至色谱柱的要求流速;⑥采集基线,看一下仪器基线噪声和漂移;⑦基线噪声和漂移合格后,可进行样品检测。3.2日常使用维护通常情况下仪器日常使用按照以下操作对仪器进行使用维护:①做样结束后,需继续冲洗30min,清洗进样口;②流速需逐步降低,关泵之前,先关电流;③泵关闭之前“后冲洗”需用去离子水清洗;⑤淋洗液必须经过脱气处理,且现用现配;⑥样品须经过0.22μm滤膜过滤后再进样;⑦淋洗液瓶、砂芯过滤装置等需要定期清洗⑧所用器皿禁止接触酸。
操作维护
2024.07.18
HPLC高效液相色谱常见故障及解决方法
高效液相色谱(HPLC)是近30年发展起来的一种具有高灵敏度、高选择性的高效快速分离分析技术。它既能用于微量组分的分析测定,又能用于大量的制备分离,灵活多样,其应用范围已超过其他各种分离方法,尤其在中药样品的分析分离方面更充分发挥它的特长,为推动该领域的进步和发展作出了巨大贡献。高效液相色谱在使用过程中常会出现一些影响分析结果的问题,如果使用人员了解常见问题及其成因和相关解决方法,就能做到早预防勤维护,使分析结果保持较好的稳定性与较高的精确性。高效液相色谱仪系统组成:液相色谱仪主要由贮液瓶、泵、进样器、柱子、柱温箱、检测器、数据处理系统组成。对于整个系统而言,柱子、泵和检测器是核心部件同时也是易出问题的主要部位。高效液相作为一种高精密仪器,如果在使用过程中不按照正确操作的话,就容易导致一些问题。其中最常见的就是柱压问题、漂移问题、峰型异常问题。柱压问题柱压问题是使用高效液相色谱仪过程中需要密切注意的地方,柱压的稳定与色谱图峰形的好坏、柱效、分离效果及保留时间等密切相关。所谓柱压稳定并不是指压力值稳定于一个恒定值而是指压力波动范围在50 PSI(3.3 Bar)之间(在使用梯度洗脱时,柱压平稳缓慢的变化是允许的)。压力过高、过低都属于柱压问题。压力过高这是高效液相色谱仪在使用中最常见的问题,指的是压力突然升高,一般都是由于流路中有堵塞的原因。此时,我们应该分段进行检查。1)首先断开真空泵的入口处,此时PEEK管里充满液体,使PEEK管低于溶剂瓶,看液体是否自由滴下,如果液体不滴或缓慢滴下,则是溶剂过滤头堵塞。处理方法:用30%的硝酸浸泡半个小时,在用超纯水冲洗干净。如果液体自由滴下,溶剂过滤头正常,再检查;2)打开Purge阀,使流动相不经过柱子,如果压力没有明显下降,则是过滤白头堵塞。处理方法:将过滤白头取出,用10%的异丙醇超声半个小时。如果压力降至100 PSI(6.7 Bar)以下,过滤白头正常,再检查;3)把色谱柱出口端取下,如果压力不下降,则是柱子堵塞。处理方法:如果是缓冲盐堵塞,则用95%的水冲至压力正常。如果是一些强保留的物质导致堵塞,则要用比现在流动相更强的流动相冲至压力正常。假如按上面的方法长时间冲洗压力都不下降,则可考虑将柱子的进出口反过来接在仪器上,用流动相冲洗柱子。这时,如果柱压仍不下降,只有换柱子入口筛板,但一旦操作不甚,很容易造成柱效下降,所以尽量少用。压力过低1)压力过低的现象一般是由于系统泄漏,处理方法:寻找各个接口处,特别是色谱柱两端的接口,把泄漏的地方旋紧即可;2)当然还有一个原因就是泵里进了空气,但此时表现的往往是压力不稳,忽高忽低,更严重一点会导致泵无法吸上液体。处理方法:打开Purge阀,用3~5 ml/min的流速冲洗,如果不行,则要用专用针筒在排空阀处借住外力将气泡吸出。漂移问题主要包括基线漂移和保留时间漂移。基线漂移一般说来,机器刚起动时,基线容易漂移,大概要半个小时的平衡时间,如果你用了缓冲溶液或缓冲盐,还有就是在低波长下(220 nm)平衡时间相对会比较长,但如果你在实验过程中发现基线漂移,则你要考虑下面的原因:1)柱温波动。解决方法:控制好柱子和流动相的温度,检查是否有打开的窗户或空调对着柱温箱;2)流通池被污染或有气体。解决方法:用甲醇或其他强极性溶剂冲洗流通池(最好断开柱子)。如有需要,可以用1N的硝酸(不要用盐酸);3)紫外灯能量不足。解决方法:更换新的紫外灯;4)流动相污染、变质或由低品质溶剂配成。解决方法:检查流动相的组成,使用高品质的化学试剂及HPLC级的溶剂;5)样品中有强保留的物质(高K’值)以馒头峰样被洗脱出,从而表现出一个逐步升高的基线。解决方法:使用保护柱,如有必要,在进样之间。在分析过程中,定期用强溶剂冲洗柱子;6)检测器没有设定在最大吸收波长处。解决方法:将波长调整至最大吸收波长处;7)流动相的PH值没有调节好。解决方法:加适量的酸或碱调至最佳PH值。保留时间漂移保留时间重现是液相性能好坏的一个重要标志,同一种东西,两次的保留时间相差不要超过15 s,超过了半分钟可看做保留时间漂移,就无法进行定性,你要考虑以下原因:1)温控不当。解决方法:调好柱温,检查是否有打开的窗户或空调对着柱温箱;2)流动相比例变化。解决方法:检查四元泵的比例阀是否有故障;3)色谱柱没有平衡。解决方法:在每一次运行之前给予足够的时间平衡色谱柱;4)流速变化。解决方法:重新设定流速 ;5)泵中有气泡。解决方法:从泵中除去气泡 。峰形异常问题峰型问题是液相的主要问题,在做液相过程中,我们就是要变换不同的条件来改善不好的峰型,对于各种各样的异常峰,要区别对待,从主要问题出发,一个一个加以解决。1)色谱图中未出峰。解决方法:系统未进样或样品分解;泵未输液或流动相使用不正确;检测器设置不正确;针对以上情况成因作相应调整即可。2)一个峰或几个峰是负峰。解决方法:流动相吸收本底高;进样过程中进入空气;样品组分的吸收低于流动相。3)所有峰均为负峰。解决方法:信号电缆接反或检测器输出极性设置颠倒;光学装置尚未达到平衡。4)所有峰均为宽峰。解决方法:系统未达到平衡;溶解样品的溶剂极性比流动相差很多;色谱柱尺寸及类型选择不正确;色谱柱或保护柱被污染或柱效降低;温度变化造成的影响。5)所出峰比预想的小。解决方法:样品黏度过大;进样品故障或进样体积误差;检测器设置不正确;定量环体积不正确;检测池污染;检测器灯出现问题。6)出现双峰或肩峰。解决方法:进样量过大;样品浓度过高;保护柱或色谱柱柱头堵塞;保护拄或色谱柱污染或失效;柱塌陷或形成短通道。7)前伸峰。解决方法:进样量或样品浓度高;溶解样品的溶剂较流动相极性强;保护柱或色谱柱污染或失效。8)拖尾峰。解决方法:柱超载,降低样品量;增加柱直径采用较高容量的固定相;峰干扰,对样品进行清洁过滤;调整流动相;硅羟基作用,加入三乙胺,用碱致钝化柱增加缓冲液或盐的浓度降低流动相pH值;柱内烧结不锈钢失效,更换烧结不锈钢;加在线过滤器,对样品进行过滤;死体积或柱外体积过大,将连接点降至最低;尽可能使用内径较细的连接管;柱效下降,更换柱子;采用保护柱,对柱子进行再生。9)出现平头峰。解决方法:检测器设置不正确;进样体积太大或样品浓度太高。10)出现鬼峰。解决方法:进样阀残余峰,在每次进完样后用充足的时间来平衡和清洗系统;样品中存在未知物,改进样品的预处理;流动相污染,更换新流动相,尽可能现配现用,隔夜的流动相再次使用时要过滤;尽可能使用HPLC级试剂;流路中有小的气泡,打开Purge阀,加大流速排除。以上内容只是对液相色谱中出现的常见的问题进行了分析,在故障排除时要遵守以下原则:(1)一次只改变一个因素,确定假定因素与问题之间的联系;(2)如果通过更换组件来排查故障时要注意将拆下的完好组件装回原位,避免浪费;(3)养成良好的记录习惯,这是成功进行故障排除的关键。总之,在使用高效液相色谱时一定要注意样品的前处理与仪器的正确操作和保养。在日常的使用过程中,仪器条件经常变化,色谱柱经常拆卸,因此需要对色谱仪经常检定以发现仪器性能的变化。但有不少实验人员因为不熟悉仪器的结构原理,不甚了解仪器的技术指标对分析测定结果的影响,而不能将仪器调整到最佳状态,从而直接影响到所测定数据的准确性。如果实验人员能注意检定液相色谱仪的一些问题,则会大大延长仪器的使用寿命,并使仪器的性能得到最大限度的发挥。下面,我们重点讨论液相色谱仪检定中常见的几个影响因素以及解决问题的方法:气泡由于HPLC系统中气泡的存在,会造成色谱图上出现尖锐的噪声峰,严重时会造成分析灵敏度下降;气泡变大进入流路或色谱柱时会使流动相的流速变慢或不稳定,使基线起伏。造成上述现象的主要原因有三条:一是流动相溶液中往往因溶解有氧气或混入了空气而形成气泡;二是系统开始工作时未能将流路中的空气驱赶干净;三是在注入样品时不注意混入了空气。为了避免这类问题的出现,HPLC实际分析过程中必须重视对流动相进行脱气处理;在HPLC系统开始工作前,可以用注射器连接恒流泵的排空阀,抽入流动相,将流路中的空气驱赶干净;在注入样品前注意排出样品注射器中的空气。柱温在操作HPLC时,色谱柱是在室温环境下工作的。大多数的工作环境温度是不断变化的,温度的差别就会引起较复杂的问题。温度的影响在所有的色谱分析方式中都是存在的,HPLC方法中的洗脱方式受温度的影响。1)等度洗脱时温度会影响保留时间。当温度升高时所有的色谱峰都前移了,等度洗脱时一般温度每升高1℃,保留时间会缩短(1~3)%。2)温度变化对梯度洗脱和等度洗脱的影响趋势是一样的,但是对梯度洗脱的影响要小于对等度洗脱的影响。即便如此,若梯度洗脱时不控制温度的话,保留值一般也会有较大的变化。3)温度变化还可能引起选择性显著变化。正如柱子不能完全平衡将导致保留时间的重现性差一样,柱温不平衡也会导致不理想的后果,这个问题在峰宽上的影响尤其明显。当温度变化时除了选择性和保留时间的变化之外,峰宽也会发生变化。升高温度通常会使理论塔板数升高,峰宽变窄,由于峰面积不变,峰越窄就会越高,因此升高温度可以达到更小的检测限。4)柱子里的温度变化也会影响峰形。当流动相和柱子之间的温差增大时,由温度不平衡而导致的峰变形就会加剧。为了获得一致的结果我们必须要控制柱温,使用柱温箱是最好的办法。如果没有柱温箱,最有效的办法就是将色谱柱隔绝在一个温度波动最小的地方。色谱柱污染色谱柱污染会引起保留时间漂移。HPLC色谱柱是非常有效的吸附性过滤器,它可以过滤并吸附流动相携带的任何物质。污染源可能是:流动相本身,流动相容器,连接管、泵、进样器和仪器密封垫,以及样品等。样品中如果存在色谱柱上保留很强的组分,就可能使保留时间漂移。通常样品中的强保留组分具有较高的分子量,在此情况下,保留时间漂移的同时或其后会有反压的增加。可以通过使用固相提取等样品前处理方法来去除样品基质的影响。避免色谱柱污染最简单的方法是防患于未然。相比之下,找到问题的所在并设计有效的清洗步骤以去除污染物要困难的多。通常使用在给定色谱条件下的强溶剂,但并非所有污染物都可以在流动相中溶解。使用保护柱是个非常有效的方法。反冲色谱柱仅是不得已时采用的办法。色谱柱平衡如果我们观察到保留时间漂移,首先应考虑色谱柱是否已用流动相完全平衡。通常平衡需要10~20个柱体积的流动相。但如果在流动相中加入少量添加剂则需要相当长的时间来平衡色谱柱。需要柱子的充分平衡,然后才能对HPLC进行检定。流动相有机溶剂流动相有机溶剂可能影响HPLC的检测限。分析中要求使用HPLC纯的试剂,关键是两点:纯度高、紫外吸收小。纯度高,是希望没有杂质干扰HPLC分析;不会有金属离子损害纯度为99.99%以上的高纯度硅胶基质。可以通过重蒸分析纯溶剂;或滤膜过滤,并定期把前置的过滤头取下,放稀硝酸里清洗,再用纯水洗至中性。柱压柱压过高是HPLC分析中常碰到的问题。其原因有多方面,而且常常并不是柱子本身的问题。1)溶剂或样品含有颗粒杂质,这些杂质将筛板堵塞引起压力上升,应更换柱子入口筛板;2)泵内有空气,解决的办法是清除泵内空气,对溶剂进行脱气处理;3)比例阀失效,应更换比例阀;泵密封垫损坏,应更换密封垫;系统检漏,则找出漏点,密封即可。HPLC分析中,在色谱柱正常,样品灵敏度足够,分析方法合适,色谱峰在出峰时间较短的条件下,峰形应对称而尖锐。充分考虑到可能影响分析结果的因素,可以科学地进行液相色谱仪的检定。
操作维护
2024.07.17
新手必看,超详细的Waters2695液相色谱仪操作规程
一、开机前的准备工作:1.检查设备电源、流路、信号连接是否完好;2.流动相:配制相应的流动相,经0.22mm微孔滤膜抽真空过滤后,或检查是否需要添加。适当选择滤膜,水系/有机系(反光面朝上)。3.样品溶液:按方法取样或配制标准样品溶液,0.22mm滤膜过滤。二、开机平衡系统:1.开机自检:打开电源开关,仪器开始自检(4-5min),待屏幕上方出现“Idle”自检完成。2.脱气:按面板右下方“Menu/Status”键进入“Status”界面,移动光标至“Degasser Mode”,按Enter选择“On”,打开在线脱气。一般默认是开的。3.设定柱温:在“Status”界面,光标至“Col Htr Set”,输入目标温按Enter。4.清洗柱塞杆:按“Menu/Status”键回到“Menu”界面,按下排功能键“Diag”,然后再按下排功能键“Prime Seal Wsh”,“Start”,冲洗1~2min后,“HALT”,“CLOSE”。5.Wet Prime:在“Status”界面中“Composition”下,选择将用到的溶剂通道为“100%”,按液晶屏幕右下角“Direct Function”键,移动光标选择“Wet Prime”,“OK”,流速及时间可使用默认值,也可自行设定(如:5ml/min,3min),“OK”即可。将每一个会用到的溶剂通道按照上述操作一次。(也可各通道选25%v 5ml/min,3min)。6.注射器排气泡及清洗:进入“Direct Function”界面后,选择“Purge Injector”,“OK”,默认数值为6,“OK”。7.清洗注射针:进入“Diagnostics”界面,按下排功能键之“Prime Ndl Wsh”,“Start”,默认30秒钟,“Close”,即可返回“Diagnostics”界面。注:以上4-7为溶剂系统前处理过程,建议每天开机后依次进行。若发现注射器中有气泡,则可重复6)直至排除。8.平衡柱子:在“Status”界面上,按流动相比例设定各通道溶剂比例后,再Wet Prime操作一次,然后设置流速,平衡色谱柱30-60min。三、编辑仪器方法和方法组:1.打开电脑双击桌面上的Empower,输入用户名system、密码manager选择项目和系统。2.新建方法与方法组新建方法:单击监视区方法组编辑向导—新建—2695的参数:单次输送体积(建议130)、针头深度0、脱气设置开、泵模式(等度/梯度)、柱温。2489配置:通用(灯开启、波长)—文件—另存为(输入方法名XX)-保存-退出。新建方法组:选择所需的方法名称,点击下一步—输入方法组名(与方法名一致)。四、进样:1.待“监视基线”稳定后,点击“中断样品组”开关,进入“进样”阶段。2.当进行单进样时,在“运行样品”的“单进样”界面中输入“样品名”“功能”“方法组”“进样体积”“运行时间”等;“单进样”就是单次进样,完成分析后即停止检测(流动相正常走动);3.当多进样时,在“运行样品”的“样品”界面点击“样品瓶”输入所有样品分别所在位置(输入所在编号),“进样体积”、“进样数”、“功能”、“方法组”、“运行时间”等。4.开启绿色“运行”-“运行样品”开关。五、关机:1.清洗注射器、针、柱塞杆:方法同开机平衡系统中的4-7。如果流动相中含有盐类,则实验结束后必须用水清洗柱塞杆。2.如果流动相使用了盐,注意不要让有机溶剂直接和缓冲盐接触,中间要使用水过渡一下。先用水/甲醇(或乙腈)=95/5在1ml/min流速下清洗色谱柱和系统30分钟,再用甲醇或乙腈清洗30分钟;如果流动相中没有使用盐,则用甲醇或乙腈清洗色谱柱和系统30分钟。3.降低流速至0,待系统压力回零后,退出Empower软件系统,关闭HPLC系统。最后,关闭计算机及显示器电源。六、仪器使用注意事项:1.水性流动相使用不要超过二天,最好每天新鲜配制以免微生物的生长。2.样品组方法里的“功能”一项,有“平衡”及“平衡色谱柱”两个选项,其功能不同。若仪器方法选用梯度,用“平衡色谱柱”可以在进样前运行梯度来平衡柱子;而如果选用“平衡”则只是按照初始梯度条件等度平衡柱子。(当然,如果用等度的流动相条件,则两者没有区别)。3.清洗柱塞杆的溶剂可以用水,或5%-10%甲醇(抑菌)。4.清洗针的溶剂可以根据样品溶解性选择,如甲醇,或异丙醇-水(1:1)。5.“实验结束后要注射器排气泡及清洗(purge injector)”,1次即可,包括了“purge sample loop”。6.在线脱气机打开后,开始时运行加速,压力很快降到1.0psi以下,然后维持0.5psi左右。7.怀疑管路堵塞可卸下单向阀和在线过滤器进行清洗。单向阀安装注意方向(箭头朝上)。8.注射器中的气泡快速有效排除方法:可以小心的卸下注射器抽吸甲醇排除气泡后,注射器中保留少量溶剂,做“purge injector”小心安装上,再做几次“purge injector”观察没有气泡即可。其他方法,可以在“purge injector”开始后、注射器杆向上时,拧掉下边螺丝,上下抽推排除气泡,但手动排泡过程要在purge injector结束前完成。溶剂用甲醇较好,不用同时拧掉上方注射器。9.当有多个“仪器方法”和“方法组”存在时要注意选择当前需要使用的“仪器方法”和“方法组”;当“仪器方法”改变时尤其是流动相组成等发生变化时,必须对系统重建平衡,也就是在新的“仪器方法”流动相条件下平衡系统30分钟以上,使得基线重新稳定。10.长期不使用HPLC,应该将色谱柱从系统拆除,拆除前应该充分平衡色谱柱,一般为用甲醇或乙腈冲洗色谱柱40分钟以上。11.若色谱柱长期保存未使用,则刚装入HPLC系统时应以流量0.2mL/min平衡过夜(注意断开检测器避免不必要的检测器耗损),然后再以0.8mL/min流量平衡30分钟以上。以低流量缓慢的提高流速直到获得稳定的基线,这样可以保证色谱柱的使用寿命。当然在分析结束时冲洗色谱柱及系统后停止流量时也应该从高流量逐步过渡到低流量直到流量为0。12.系统短期不使用,应该在每次使用后冲洗系统30分钟以上。
操作维护
2024.07.17