【阿拉丁】新型抗菌利器——抗菌肽
新型抗菌利器——抗菌肽 随着全球细菌耐药性的日益增加以及新型传染病的频繁出现,核糖体合成抗菌肽(RAMPs)在抗生素研究领域中逐渐崭露头角,成为一大研究热点。抗菌肽根据其合成途径可分为非核糖体合成肽和核糖体合成肽。非核糖体合成的肽主要存在于细菌和真菌中,这些肽是由肽合成酶组装而成,而非通过核糖体合成。短杆菌肽、杆菌肽、多粘菌素B和万古霉素是此类非核糖体合成抗菌肽的典型例子。这些抗生素在科学研究中已被证明具有很高的有效性,但由于新型细菌耐药性(如耐万古霉素的金黄色葡萄球菌和肠球菌)的出现,使其在新应用方面受到了限制。 一、 核糖体合成抗菌肽的来源及特性 RAMPs来源广泛,遍布从原核生物到人类的各种物种。作为宿主抵御每天暴露于数百万潜在病原体的天然防御机制,抗微生物肽不仅具有抗菌活性,还可能展示出抗病毒、抗寄生虫和抗肿瘤的多功能性。据文献报道,已有超过500种RAMPs被鉴定和描述。其独特的抗生素谱是由氨基酸序列和结构构象共同决定的。RAMPs是由12至50个氨基酸组成的基因编码肽,具有很少的遗传重叠。缺乏序列同源性反映了这些肽在不同物种环境中的形态和功能优化进化。通常,RAMPs是阳离子肽,至少一半的氨基酸残基是疏水的,并且含有少量中性或带负电的残基。其具有相对的疏水和亲脂面的两亲结构,能够有效干扰细菌细胞壁。 二、 RAMPs的作用机制 RAMPs的作用机制包括以下几个关键步骤:1. 肽与细菌细胞表面的结合:RAMPs首先通过静电作用与带负电荷的细菌细胞表面的成分(如革兰氏阴性细菌的脂多糖或革兰氏阳性细菌的酸性多糖)结合。2. 肽的构象改变:在结合过程中,肽发生构象变化,这种变化促进了肽的嵌入和聚集。3. 多个肽单体的聚集:多个肽分子在细菌细胞膜上聚集,形成孔道或破坏膜的完整性。4. 通过细菌细胞壁形成孔:这种聚集最终导致细菌细胞膜的渗透性增加,形成瞬时孔隙,导致细胞成分泄漏和细胞死亡。 针对细菌细胞膜的渗透机制,RAMPs主要有三种理论模型:桶壁模型、胸廓模型和地毯模型。桶壁模型认为肽在细胞膜上形成桶状结构;胸廓模型则认为肽在膜上形成胸廓状孔道;地毯模型则描述肽像地毯一样覆盖在细胞膜表面,导致膜的破裂和细菌死亡。 三、 RAMPs的临床应用前景 RAMPs在临床抗菌药物中的应用前景非常广阔,主要有以下几个优点: 1. 对耐药菌株的有效性:RAMPs对多种耐药菌株表现出显著的抗菌活性。 2. 不易选择出耐药突变体:RAMPs不容易选择出耐药突变体,并且其天然细菌耐药性较低。 3. 与常规抗生素协同作用:RAMPs能与常规抗生素协同作用,特别是对抗耐药突变体。 4. 动物模型中的有效性:在动物模型中,RAMPs被证明能够有效杀死细菌。 5. 快速杀灭细菌:RAMPs能够迅速杀灭细菌,减少感染的严重程度。 6. 补充作用:RAMPs还具有抑制脓毒症等补充作用。 尽管RAMPs在临床上具备理想的候选药物特性,但其结构的多样性使得预测其体内活性存在挑战。设计功能性合成仿生体是一项复杂的任务,微小的肽序列或构象变化可导致体内抗菌和细胞毒性水平的显著差异。为了获得MIC、特异性、稳定性和毒性信息,研究人员利用生物信息学数据库设计了新的合成抗菌肽。 四、 抗菌肽的研究进展 近年来,抗菌肽研究取得了显著进展。研究者们利用现代生物技术手段,如高通量筛选和计算机模拟,发现和优化了多种新的抗菌肽。这些新型抗菌肽在临床前研究中表现出良好的抗菌活性和低毒性,为未来的临床应用奠定了基础。例如: 1. Pexiganan:一种用于治疗糖尿病足感染的抗菌肽。Pexiganan在临床试验中展示了良好的抗菌效果,特别是对抗耐甲氧西林金黄色葡萄球菌(MRSA)。 2. Lantibiotics:如Nisin,这些抗菌肽主要用于食品保鲜,但研究表明它们在抗药性病原体的治疗中也具有潜在应用。 3. Defensins:这些是哺乳动物中常见的一类抗菌肽,研究发现它们不仅具有广谱抗菌活性,还能够调节免疫系统,提高机体对病毒和肿瘤的抵抗能力。 4. LL-37:一种人类源的抗菌肽,展示了广谱抗菌活性,并在慢性伤口愈合和抗炎治疗中展现出潜力。 此外,研究人员还探索了抗菌肽在抗病毒、抗肿瘤和免疫调节中的潜在应用。最新的研究表明,某些抗菌肽可以通过调节免疫系统,提高机体对病毒和肿瘤的抵抗能力。例如,LL-37不仅具有抗菌活性,还能通过抑制炎症反应来加速伤口愈合。 结语 选择合适的转染技术取决于实验目的、细胞类型、期望的效率和基因表达的持续时间。化学方法如脂质转染和磷酸钙转染操作简便、成本低廉,而物理方法如电穿孔和微量注射则具有高效率和精确度。病毒转导技术,尤其是腺病毒和慢病毒转导,提供了高效率和稳定的基因表达能力。每种方法都有其独特的优势和局限性,因此,根据研究的具体需求定制方法至关重要。 随着转染技术的发展,它们不仅加深了我们对细胞过程的理解,还推动了新治疗策略的发展,凸显了这些技术在现代生物学研究中的核心作用。欢迎咨询阿拉丁,寻找发现细胞转染相关实验试剂,推动研究进展。 阿拉丁:https://www.aladdin-e.com
应用实例
2024.07.22
【阿拉丁】细胞内ELISA实验方案
细胞内ELISA实验方案 细胞内ELISA(也称为基于细胞的ELISA、细胞蛋白质印迹或细胞印迹)是一种使用比色或荧光读数对培养细胞进行定量的广为接受的免疫细胞化学测定方法,用于量化培养细胞中的靶蛋白或靶蛋白的翻译后修饰。 这里我们提供了96孔微孔板的通用方案。大致流程包括:培养细胞(根据需要进行处理)并将其接种到包被的96孔微孔板中;固定和透化后,将一抗添加到孔中并孵育,然后添加标记的二抗,最后进行检测和分析。 一、准备细胞 粘附细胞可以在推荐的分析微孔板中生长,或直接接种到分析微孔板中并允许其附着贴壁几个小时或过夜。 所需材料 - 96孔微孔板:底部透明(荧光抗体需要黑色壁),最好用胺/胶原蛋白等进行包被,以实现最佳细胞培养条件 - 多通道移液器(推荐) - 蒸馏水或去离子水 - 10×磷酸盐缓冲液(PBS)(80 mM Na2HPO4、14 mM KH2PO4、1.4 M NaCl、27 mM KCl,用NaOH调节p至7.4) - 1× PBS:实验开始时准备。将45 mL 10× PBS稀释于405 mL蒸馏水或去离子水中并充分混合。室温保存。 - 400× Tween-20(20%水溶液) - 1×洗涤缓冲液:实验开始时准备。将625 µL 400× Tween-20稀释于250 mL 1× PBS中并混合均匀。室温保存。 实验步骤 1.将细胞以所需密度接种到96孔微孔板中。对于384孔微孔板,以96孔板密度的四分之一进行接种。 注意:最佳细胞接种密度取决于细胞类型,应根据每个实验确定。例如,在96孔微孔板中,每孔应接种25,000 - 50,000个HeLa细胞。 2.让细胞粘附数小时或过夜。 3.按需要处理附着的细胞,96孔板培养基总体积为100 µL(384孔板体积为96孔板体积的四分之一)。培养基中可接受高达10%的血清。 注意:您应该确定细胞处理的持续时间。当使用目标药物处理细胞时,我们建议包括未处理的细胞和用药物溶剂处理的细胞。 二、将细胞固定至微孔板 所需材料 - 10×磷酸盐缓冲液(PBS):80 mM Na2HPO4、14 mM KH2PO4、1.4 M NaCl、27 mM KCl,用NaOH调节pH至7.4。 - 20%多聚甲醛 - 蒸馏水或去离子水 - 8%多聚甲醛:使用前立即配制。将6.25 mL蒸馏水或去离子水与1.25 mL 10× PBS和5.0 mL 20%多聚甲醛混合。注意:多聚甲醛有毒,应在通风橱中配制和使用。根据当地法规处理多聚甲醛。 - 实验开始时准备的1× PBS - 96孔微孔板。底部透明(荧光抗体需要黑色壁),最好涂层(胺/胶原蛋白)以实现最佳细胞培养 - 多通道移液器(推荐) 实验步骤 1.立即向含有培养基的孔中加入等体积(100 μL)的8%多聚甲醛溶液。孵育15分钟。 警告:多聚甲醛有毒,应在通风橱中配制和使用。根据当地法规处理多聚甲醛。 2.轻轻吸出微孔板中的多聚甲醛溶液,并用300 μL 1× PBS每孔清洗微孔板3次。 3.在孔中加入100 μL 1× PBS。用密封件盖住微孔板。 提示:此时可以将微孔板在4°C下保存几天。如需长期保存,可在PBS中添加0.02%叠氮化钠。 警告:多聚甲醛和叠氮化钠均有毒,应小心处理并根据当地法规进行处置。 注意:在检测期间或检测前的任何时候都不应让微孔板干燥。 三、细胞通透 建议在孵育步骤中使用板振荡器(~300 rpm)。任何涉及去除缓冲液或溶液的步骤之后,都应在纸巾上轻轻叩击培养板以去除孔中的所有溶液。 所需材料 - 100× Triton X-100(10%水溶液) - 1×PBS - 1×透化缓冲液:使用前立即配制。将250 µL Triton X-100稀释于24.75 mL 1× PBS中并混匀。 - 10×封闭缓冲液 - 2×封闭液:使用前立即配制。将5 mL 10×封闭液稀释于20 mL 1× PBS中。 - 多通道移液器(推荐) - 平板摇床 实验步骤 1.除去PBS,每孔加入200 μL新鲜配制的1×透膜缓冲液。 2.孵育30分钟。 提示:建议在孵育步骤中使用平板振荡器(~300 rpm)。 任何涉及去除缓冲液或溶液的步骤之后都应在纸巾上轻轻敲击培养板以去除孔中的所有溶液。 3.除去1×通透缓冲液并向每孔中加入200 μL 2×封闭溶液。 4.孵育2小时。 注意:建议在孵育步骤中使用平板摇床(~300 rpm)。 任何涉及去除缓冲液或溶液的步骤之后都应在纸巾上轻轻敲击培养板以去除孔中的所有溶液。 四、一抗孵育 我们必须至少在一个孔中省略一抗,以确定实验的背景信号,该背景信号可以从所有测量数据中减去。应针对每个实验条件和每个检测抗体执行此操作。 所需材料 - 细胞内ELISA鉴定的一抗 - 10×封闭缓冲液 - 1×PBS - 1×孵育缓冲液:使用前立即配制。将2.5 mL 10×封闭液稀释于22.5 mL 1× PBS中。 - 多通道移液器(推荐) 实验步骤 1.将提供的抗体储备液稀释于1×孵育缓冲液中,配制成1×一抗溶液。 2 .除去2×封闭液,每孔加入100 µL稀释的一抗溶液,4°C孵育过夜。 提示:为了确定背景信号,请从每个实验条件和所用检测抗体所含细胞的至少一个孔中省略一抗。 五、二抗孵育 所需材料 - 实验开始时准备的1×洗涤缓冲液 - 合适的荧光或HRP标记的二抗 - 10×封闭液 - 1×PBS - 1×孵育缓冲液:使用前立即配制。将 2.5 mL 10×封闭液稀释于 22.5 mL 1× PBS中。 - 多通道移液器(推荐) 实验步骤 1.按照试剂盒使用说明(或抗体数据表)中的指示,在1×孵育缓冲液中稀释,制备1×二抗溶液。 注意 :保护荧光标记抗体免受光照。 2.除去一抗溶液,用250 μL 1×洗涤缓冲液/孔洗涤微孔板3次。 3 .除去1×洗涤缓冲液,每孔加入100 µL 1×二抗溶液,孵育2小时。 4 .弃去二抗溶液,用250 µL 1×洗涤缓冲液/孔洗涤4次。 注意:不要移除最后一次清洗的缓冲液。 六、检测信号 所需材料 - 70%乙醇 - 合适的微孔板读数仪:对于HRP检测,使用能够测量650 nm(最好在动力学模式下)或450 nm吸光度的微孔板读数仪。对于荧光标记抗体,使用相应的成像系统(如LI-COR® Odyssey®或Aerius®的近红外成像系统)。 - 对于HRP检测,HRP底物溶液 - 0.5 M盐酸 实验步骤 1.如果使用荧光偶联二抗,请用70%乙醇擦拭微孔板底部和扫描仪表面,然后在LI-COR® Odyssey®系统上扫描微孔板。 提示:根据制造商的说明使用700 nm和800 nm通道(建议强度范围为 5-7)。 2.对于HRP标记的二抗,移除最后一次清洗液并将微孔板面朝下擦干以去除多余的液体。并添加100 µL HRP底物。 戳破所有气泡,如下设置微孔板读数仪参数,并记录蓝色变化: - 模式:动能 - 波长:650nm - 时间:30分钟 - 间隔:20秒至1分钟 - 摇动:读数之间摇动 - 替代方案:代替动力学读数,在用户定义的时间,记录640 nm处的终点OD,或通过添加100 µL 0.5M HCl来停止反应并记录450 nm处的OD。 3.保存数据并将原始数据导出到Excel。 提示:使用LI-COR® ICW软件或其他合适的数据分析软件(例如 Microsoft Excel 或 GraphPad Prism)分析数据。 细胞内ELISA的提示和技巧总结: 1.关于细胞 -细胞接种密度、培养基和其他生长条件是实验成功且可重复的关键。 -用户应定义特定于细胞类型的参数。 2.细胞附着和固定 -粘附细胞可以在分析微孔板中直接生长和处理。 -可以用显微镜检查细胞附着情况。 -当细胞完全附着时,可以去除培养基并替换为含有处理试剂的培养基。 -含有高达10%胎儿血清的培养基不会干扰细胞固定和与微板的交联,但可能会干扰处理试剂。 3.细胞处理 -使用药物(抑制剂或激活剂)时,实验中应同时包括未处理的细胞和仅用药物溶剂处理的细胞。 4.细胞接种密度 -检测微孔板的细胞接种密度取决于细胞类型。它取决于细胞大小(对于粘附细胞,则为直径)和目标蛋白的丰度。 -一般建议使用单层以获得稳健的信号。 -可以通过显微镜观察连续稀释细胞的细胞密度来确定细胞接种的数量。 -对于粘附细胞,在微孔板(孔尺寸相似)中制备细胞的连续稀释液,并在显微镜下观察细胞密度。在合适的细胞密度范围内,取更大数值的细胞密度将产生更强的整体信号并增加微小信号的检出率。例如,HeLa和HepG2细胞应每孔接种25,000至50,000个细胞,而人类成纤维细胞(HdFN)-每孔接种15,000至 25,000个细胞。 5.对照设置 至少在一个孔中省略一抗,以便为实验提供背景信号,该背景信号可以从所有测量数据中减去。应针对每个实验条件和每个检测抗体执行此操作。 6.高通量 该检测也可采用384孔微孔板形式进行,使用四分之一体积的试剂和细胞。 如需了解更多产品详情,请前往阿拉丁官网查询。https://www.aladdin-e.com
企业动态
2024.07.08
【阿拉丁】使用ICP OES评价碳酸锂和氢氧化锂的纯度等级
使用ICP OES评价碳酸锂和氢氧化锂的纯度等级简介 近年来,全球对锂盐的需求大幅增长,这主要归因于锂离子电池(LIB)市场的迅速扩张,特别是汽车行业。在全球交易的关键锂化合物中,碳酸锂(Li2CO3)和氢氧化锂(LiOH)占据重要地位。这些化合物是从地质矿石和地下卤水等自然资源中提取的,随后被用于各种锂离子电池组件(图1)。虽然碳酸锂的提取成本效益较高,但由于氢氧化锂具有低温分解的特性,更有利于实现更可持续的电池阴极制造过程并提高最终产品的耐久性,因此更受欢迎。图1. 从矿石到电池组件的锂提取简化示意图 电池和原材料制造商需要确保用于生产电池组件的所有物质都经过元素杂质的检测,如碱金属和碱土金属以及过渡金属,以确保最终产品的性能不会受到影响。纯度是增加材料价值和最终盈利能力的一个关键区别因素,因此严格和定期的质量控制至关重要。电池级锂盐中元素杂质的分析通常基于中国标准GB/T-11064.16-2013和国际电工委员会(IEC)62321标准中描述的方法,其中电感耦合等离子体发射光谱法(ICP-OES)是两者都推荐的技术。ICP-OES被认为是电池材料分析测试的关键技术,因为它可以在短时间内进行完整的多元素分析,并且能够处理各种潜在的样本类型。 实验部分 仪器参数和实验条件 本实验采用iCAP PRO XP ICP OES Duo仪器来评估Li2CO3和LiOH中的45种痕量元素,旨在确定这些化合物及其盐组成中的总杂质浓度。仪器在智能全范围(iFR)模式下运行,采用轴向等离子体观察,能够在单次曝光中同时实现紫外和可见光谱范围内的高灵敏度测量。这显著减少了样品周转时间,加快了结果交付,并为实验室节省了成本。样品引入系统按常规配置用于水溶液分析,但火炬除外,火炬特别选择了陶瓷D型火炬。这一选择是为了提高样品基质的耐受性并减少维护需求,因为高纯度石英火炬在长时间暴露于这些特定样品类型后可能会出现损坏和失透现象,需要频繁更换。陶瓷D型火炬可以轻松有效地处理这两种样品类型,始终产生稳健可靠的数据。 表1概述了样品引入设置的具体细节和典型的仪器参数。iCAP PRO系列ICP-OES同时测量整个波长范围的能力使得无论分析物或波长的数量如何,都能实现快速样品分析。在本实验中,实现了对45种分析物的全面定量分析,每个样品的总运行时间为144秒。表1. 仪器配置和典型操作参数 样品制备 分析包括两个Li2CO3样品,一个纯度等级为99.9%,另一个为99.998%,还有一个纯度为98%的LiOH(一水合物)样品。从每个样品中准确称取250±2mg的精确等分试样,放入指定的样品管中。随后,谨慎地向每个样品中加入1mL HNO3(微量金属等级)。之后让样品静置15分钟,以确保中和反应完成。之后,使用超纯水进一步稀释样品,直到达到50mL的最终体积。 标品或参考物质 利用单元素标准品对每个分析物进行校准,在2%(v/v)HNO3中制备了校准空白和一系列跨越三个数量级浓度范围的校准标准品。这些标准品的特定浓度分别为50、200、500、1,000和2,000 µg·L-1。 为了减轻由于样品中高锂含量导致的易电离元素(EIE)的干扰,校准标准品和校准空白都进行了基质匹配和强化,确保溶液中最终的锂浓度为1,000 mg·L-1。 此外,为了在整个实验过程中持续监测和调整任何物理干扰,在整个实验过程中,通过T型接头在线引入了一种含有5 mg·L-1钇的内部标准溶液。 质量控制和方法验证 为了验证本研究中的校准质量,我们使用了包含所有分析物200 µg·L-1的标准溶液作为质量控制(QC)标准。此外,我们还通过向选定样品中添加50 µg·L-1和1 mg·L-1的浓度来增强方法的准确性。加标样品和原始样品都经过了超过10小时的连续测量,以确保所提出方法的稳健性。 结果和讨论选择性、灵敏度和线性 表2全面概述了本研究中考察的分析物,包括基于相对灵敏度和无干扰条件选择的波长,以及获得的分析性能指标。如图1中的校准曲线所示,在整个校准范围内,所有分析物波长的确定系数(R2)均超过0.9996。此外,表格还包含了仪器检测限(IDL),该检测限来自空白和低浓度校准标准的三次重复测量,以及原始固体样品中的方法检测限(MDL),后者通过将IDL乘以样品制备过程中应用的稀释因子来计算。值得注意的是,45个目标元素中有43个的MDL明显低于1 mg·L-1,表明整个分析物系列都具有出色的灵敏度。 此外,如果需要,还可以使用相同的方法监测样品中的总锂含量,只需使用不同的非基质匹配标准和包含在单独校准块中的空白即可。表2. 各元素的适宜波长、最低检测限(LOD)、R2值和方法检测限(MDL)列表 准确性 如前所述,我们向样品中添加了不同浓度的特定分析物,以评估该方法在预期这些杂质相似浓度下的准确性。值得注意的是,所有加标回收率都保持在预期浓度±20%的范围内。表3. Li2CO3和LiOH样品中50 µg·L-1和1 mg·L-1加标的回收率(N=8)。如果未给出结果(在表中以“-”表示),则由于样品中发现的浓度水平而未进行加标回收率测试。 易电离元素(EIE)效应 样品中存在的易电离元素(EIE),如钠、钾或锂等,以其低电离势为特征,可能破坏等离子体中的电离平衡。这些EIE释放出的电子随后被等离子体中的其他元素所利用,从而改变了离子和原子之间的平衡。因此,这导致原子发射线的强度增加,离子发射线的强度减少,进而改变了特定分析物的表观浓度。当使用非基质匹配的标准时,这种现象被归类为化学干扰,可能导致错误的结果(如图2所示)。然而,本研究中实施的基质匹配措施防止了不准确结果的出现。图2. 当校准溶液和实际样品基质不匹配时,易电离元素可能导致内标回收率差且不一致。表示100%回收率的数据点代表间歇运行的校准空白。随着序列延长数小时,回收率预计会进一步恶化。然而,本研究通过采用基质匹配来缓解这一问题,显著提高了数据的稳定性。 Li2CO3和LiOH原材料的真实样品组成/纯度检查 本研究中调查的三种锂盐的定量分析结果汇总在表4中。结果表明,这些盐中的总杂质水平与声明的纯度声明相吻合。在所有样品中检测到的主要杂质是碱性和碱土元素,如钠、钾、镁和钙,尽管也存在一些常见的过渡金属,如铬、铁或锌。然而,值得注意的是,即使具有相同纯度等级的样品,其杂质组成也可能存在显著差异。例如,整体纯度超过98%的LiOH样品中的钙和硅含量显著低于整体纯度超过99%的Li2CO3样品,但铝和硫的含量较高。这种差异可能会影响这些原材料的进一步加工流程。对于广泛的分析物来说,杂质水平低于ICP-OES的检测限,表明需要一种灵敏度更高的分析技术,如电感耦合等离子体质谱(ICP-MS)。表4. 本研究中测量的原材料样品的痕量元素组成 典型工作周期内的稳健性验证 所开发的方法通过进行为期十二小时的稳健性测试以进行连续测量,在较长一段时间内对准确性进行了严格的测试和验证。这种模拟反映了现实工业场景,其中需要不间断地监测数百个此类样品,以保证产品的一致质量和均一性。稳健性测试涵盖了Li2CO3和LiOH的所有三个样品,包括其原始状态和加标等分试样。实验序列以校准块开始,包括空白和标准品,随后进行初始质量控制检查(ICV = 初始校准验证)。之后,每20个未知样品后分析一次QC样品以确保一致性。 结果表明,在整个实验过程中没有显著的信号漂移或QC失败。内标的回收率、QC样品浓度回收率和加标浓度回收率在整个分析过程中保持稳定。具体而言,内标回收率保持在90-100%的范围内(图3)。同样,所有分析物的QC回收率均在可接受的80-110%范围内,其中大多数集中在更窄的85-100%范围内(图4)。图3. 在12小时稳健性测试分析中,内标回收率表现优异,校准溶液与真实样品基质匹配 图4. 稳健性测试分析期间的QC回收率。红色双线标记的是80-120 ± 5%的区间。 结论 本应用说明介绍了一种快速、灵敏、精确且稳健的方法,用于分析各种常见的锂离子电池原材料,特别是Li2CO3和LiOH。iCAP PRO XP ICP-OES Duo仪器能够同时测量和表征两种样品类型中的45种痕量分析物,为终端用户提供了一种优雅且高效的方法,用于可靠地日常测量数百个样本。• 在本研究中,使用统一的方法分析了Li2CO3和LiOH盐,该方法通过iCAP PRO XP ICP-OES Duo同时覆盖了45种元素。对于19种元素,方法检测限(MDL)低于0.01 mg·L-1;对于23种元素,低于0.1 mg·L-1;剩余2种元素的MDL略高于1 mg·L-1。• 由于单次曝光中对所有分析物的数据同时采集,多元素分析得以迅速完成,每个样本仅需2分24秒(包括三次重复、进样和清洗)。• 该方法的准确性和精确性通过真实样本基质的精确加标回收率、出色的QC回收率和在12小时稳健性测试期间稳定的内标回收率得到证明。由于校准标准和空白样本与实际样本基质匹配,因此基质中高锂浓度引起的增强电离效应(EIE)并未降低数据质量。• 跨越十二小时的不间断分析突显了iCAP PRO XP ICP-OES Duo在处理不同组成的锂盐方面的卓越稳健性。 阿拉丁官网:https://www.aladdin-e.com/
企业动态
2024.07.05
【阿拉丁】靶点药物发现:数量稀缺,效率低下,其有效性究竟几何?
靶点药物发现:数量稀缺,效率低下,其有效性究竟几何?尽管基于靶点的药物发现是当前药物研发的主流方法,但最新的全面评估显示,其成果并不尽如人意。该方法所发现的药物数量相对较少,且其治疗效果在很大程度上依赖于非靶点机制。这让人不禁对这种方法产生疑问:它真的如我们所期望的那样有效吗?还是只是一个外表华丽但实际价值有限的“金箔”?本文将依托Arash Sadri的研究,对基于靶点的药物发现的效率及其与非靶点机制的关系进行深入探讨。 药物发现背后的挑战与困境回顾过去150年的文献,我们发现,仅有大约9.4%的小分子药物是通过基于靶点的检测手段得以发现的。尽管获得批准的候选药物与进入临床研究的候选药物之间的比率约为13%,但在更为复杂的中枢神经系统疾病和癌症领域,这一比例竟低至0.4%。此外,新药研发还面临着效率低下、成本高昂以及制药公司纷纷撤退等重重困难。针对这些问题,研究者指出,当前主流的基于靶点的药物发现方法带有明显的还原论倾向。这种方法过分聚焦于寻找能够调节单一或少数几个蛋白质的药物,却忽视了细胞内和细胞外复杂的网络结构及其反馈机制。这种方法的盛行已经持续了数十年,恰好与药物研发生产力的下降相吻合。因此,我们需要重新审视并改进现有的药物研发策略,以应对当前的挑战。 靶向药物研发效率低下:现状反思与未来挑战尽管基于靶点的药物发现方法一直备受瞩目,但其效率和效果却饱受争议。在此背景下,研究者提出了一个大胆的假设:药物发现效率的下降可能与过度依赖基于靶点的还原论药物发现方法有关。该方法主要聚焦于药物与少数预设“靶点”蛋白的结合,并以此为基础进行分子的选择和优化,通常仅在最后阶段才考虑体内和人体数据。为了验证这一假设,研究者采用了人工手段,对美国FDA在2020年底前批准的所有药物进行了详尽的调查,重点收集了关于药物发现起源的信息。为了确保研究的客观性和准确性,他们提出了以下几个关键定义:• “发现起源”:指的是首次观察到某种治疗类别与治疗效果之间存在相关性的时刻。• “治疗类别”:指与某一先导分子相关的一组在化学或药理学上具有相似性的物质。• “基于靶点的药物”:指的是那些发现过程主要依赖于观察分子对蛋白质影响的药物。• “基于表型的药物”:指的是那些发现过程主要依赖于观察分子对生物体表型影响的药物。通过深入的调查和分析,他们发现,与传统的基于靶点的药物发现方法不同,传统方法更加经验主义。这种方法依赖于分子对人类和其他生物(如动物、真菌和细菌)的治疗效果来选择和优化分子,因为它缺乏评估药物对单一蛋白质效果的工具。为了得出更加全面和准确的结论,研究者决定进一步扩大研究范围,涵盖所有已批准的药物,并增强分析的精确性和客观性。 表型药物的新路径:超越“靶向”机制,探索“非靶向”替代法与以特定靶点为核心的药物研发方法形成鲜明对比的是“非靶向”机制,这种方法更加关注药物与多个蛋白质之间的复杂交互。尽管基于靶点的还原论药物发现在当前仍占据主流地位,但为了提升药物研发的整体效率,这种反还原论、以证据为基础的方法可能会展现出更大的潜力。借助人工智能和机器学习等先进工具,我们可以优先关注更高层次的表型观察结果,这些结果更接近于患者的实际治疗反应。这种方法的优点在于能够更全面地考虑药物的各种作用机制,避免过度聚焦于单一的靶点,从而为药物研发提供更全面、更综合的方案。研究数据显示,基于表型的药物在所有已获批药物中占据了相当大的比例。这些药物的发现主要源于对非人类或体外表型的观察、对人类表型的观察、对内源分子表型效应的观察,以及受历史上使用过的化合物和作用机制启发的表型观察。这表明基于表型的药物发现方法在药物研发中具有不可替代的重要作用,而且其并不局限于对单一蛋白质的调节。在对比基于表型和基于靶点的两类药物在所有已获批药物以及1995年后获批药物中的比例时,我们发现一个有趣的现象:1995年,即首个“基于靶点”的药物——沙奎那韦(S126514)获得批准的年份,成为了这两种方法发展历程中的一个重要分水岭。图1. 药物发现起源中不同方法的占比。(a)所有已批准的药物;(b)1995年后批准的药物。虽然靶向药物研发在历年获批药物中的占比呈现出逐年增长的态势,但始终未能超越表型药物研发所占的比例。事实上,众多所谓的“靶向”药物都展现出多种“非靶向”治疗机制。以多奈哌齐(D332795)为例,这款药物最初是作为乙酰胆碱酯酶抑制剂被研发出来的,然而后续的研究却发现它具备高达40种独立的治疗机制,包括抗炎、免疫调节、神经保护等多种功能。除此之外,我们还观察到许多已获批准的药物与其治疗“靶点”的亲和力并不强,但它们大多倾向于处于高亲和力百分位数等级。这意味着与高亲和力“靶点”的结合与治疗效果之间存在某种关联。然而,与单一“治疗靶点”的高亲和力结合仅仅是影响药物治疗效果众多因素中的一个。图2. 获批准药物相对于其治疗目标所有ChEMBL配体的亲和力百分位数等级。总的来说,基于靶点的药物研发方法可能过于简化了生物系统的复杂性。相比之下,高层次的表型观察药物提供了一种更为有效的研究和治疗疾病的方法,因为它直接针对治疗效果,并且具有更高的预测性。这种方法将人体的复杂性视为一个“黑箱”,不深入探究低层次的机制,而是直接关注最终的治疗效果。 基于靶点的药物发现:其不可忽视的价值与意义在药物研发的漫长历程中,基于靶点的药物发现始终占据着举足轻重的地位。计算化学、高通量筛选和组合化学等技术,初期备受研发界的瞩目与追捧,然而随着科技进步与研究的深入,它们的局限性逐渐浮出水面。尽管如此,这些技术依然是当前药物研发过程中不可或缺的核心要素。针对特定的疾病,如单基因孟德尔疾病,基于靶点的药物研发方法充分展现了其独特的价值,这一点得到了单克隆抗体成功研发案例的进一步验证。同时,在寻找类似物的药物研发过程中,基于靶点的策略同样发挥了至关重要的作用,尤其是在优化和改进药物结构方面。然而,在针对某些复杂疾病的研发过程中,收集高级数据可能既昂贵又繁琐,此时基于靶点的药物研发方法则能够为研发工作提供坚实的基石。尽管如此,单纯依赖单一靶点的方法也存在明显的局限性。为了克服这些挑战,研究人员开始探索多药理学的概念,希望通过同时针对多个靶点来提升药物的疗效。与此同时,系统药理学和网络药理学等新颖方法与传统方法形成鲜明对比,它们从整体角度出发,为治疗复杂疾病提供更全面的解决方案,能够涵盖疾病的多种潜在因素。尽管基于靶点的药物研发方法在某些情况下具有显著优势,尤其是当疾病与特定蛋白质的亲和力密切相关时,未来的药物研发仍需从更宏观的视角来审视疾病的复杂性。为了真正提升药物研发的效率和疗效,我们必须结合循证研究,充分利用新技术和方法来深入探索疾病的多重机制。只有这样,我们才能为药物研发领域带来更加全面和创新的解决方案。 小结总体而言,基于靶点的药物发现仍然是药物研发领域的核心。然而,未来的研发趋势将更加注重整合多种技术和方法,以更全面、更具预测性的视角来审视药物研发问题。结合现代科技的进步,我们需要对疾病进行更加全面和深入的理解,从而更好地满足公众健康的需求,并应对制药行业所面临的挑战。这一转变将推动药物研发领域不断进步,为人类的健康事业做出更大的贡献。 阿拉丁中文官网链接:https://www.aladdin-e.com/
应用实例
2024.07.04
【阿拉丁】EBL-3183的工艺之路:从吲哚到临床前抑制剂
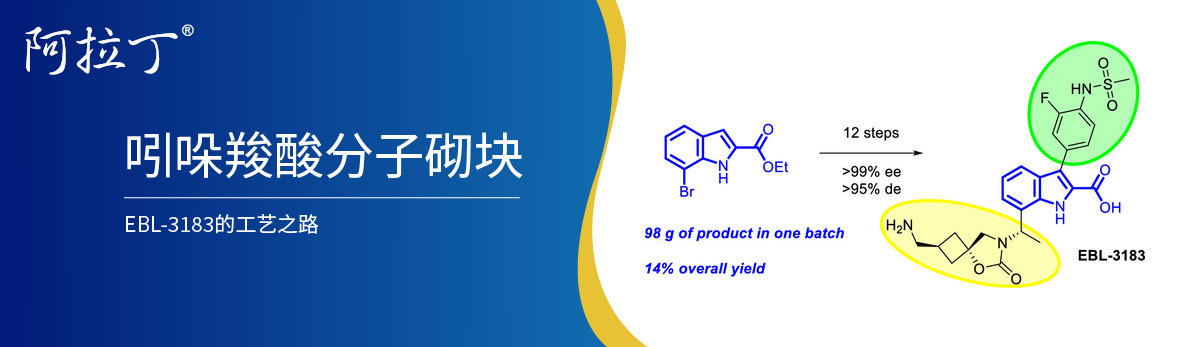
EBL-3183的工艺之路:从吲哚到临床前抑制剂背景金属β-内酰胺酶(MBLs)被视为决定碳青霉烯抗生素抗药性的主要因素。因此,寻找新的MBL抑制剂成为当前的紧迫任务。近期,Andrei Baran教授及其团队在Org. Process Res. Dev杂志上发表了一篇文章,详细介绍了MBL抑制剂“EBL-3183”的合成路径,以及如何通过优化合成工艺来提高产量和纯度,以满足临床前研究的需要。 关于EBL-3183EBL-3183作为一种新型的金属-β-内酰胺酶(MBLs)抑制剂,能有效干扰MBL的活性,提升抗生素的治疗效果。目前已进入临床前研究阶段。 EBL-3183是含有吲哚羧酸(InC)支架的新型化合物,具备优异的活性。尽管之前的候选化合物InC 1在体内外展现出卓越的抑制活性,但在安全性方面表现欠佳。因此,研究团队转向了类似物InC 2的研究,这类似物相较于InC 1在体内显示出更好的安全性,并且对碳青霉烯药物也表现出良好的增效作用。 图1. 吲哚羧酸金属-β-内酰胺酶抑制剂 InC 1(EBL-2915)和 InC 2(EBL-3183)的结构。 合成策略研究团队通过一项新的合成路线成功合成了候选化合物EBL-3183,并且已经在公斤级规模上实现了生产。这一合成工艺是以吲哚-2-羧酸酯为起始原料,通过埃尔曼辅助方法和钌催化的立体选择性还原引入手性。关键的螺环环丁烷基团则是通过精巧地组装环氧化物结构单元而来,这种结构单元能够以非对映纯形式获得,从而为合成过程提供了便利。图 2. InC 2(EBL-3183)的药物化学路线 在合成过程中,(S)-7的制备是至关重要的一步,需要极具选择性的还原条件。通过选择性更好的还原剂和催化条件,能够有效地避免异构体的分离问题,同时提升产物的结晶性,进而简化了后续的纯化操作。此外,为了确保(S)-7的合成成功,必须严格把控钛试剂的质量,以防止杂质的生成。图3. Ti(OEt)4促进亚磺酰亚胺(S)-7a 的合成 实现目标化合物InC 2的大规模合成的关键之一是能够可扩展地实现立体选择性,以制备关键的螺环并联环丁烷-环氧化物trans-16。通过对易得的烯烃13进行环氧化反应,然后利用结晶和蒸馏分离目标异构体,成功地制备了环丁烷构建块trans-16'。这个过程采用了3个并行批次,平均产率为39%,得到了23克的trans-16'。图 4.替代环丁烷结构分子砌块-氰基环氧化物反式-16' 制备中间体11'对于合成EBL-3183同样至关重要。通过环化反应可大量获得中间体11'(单批次可达160克)。该过程采用Suzuki-Miyaura交叉偶联反应完成。图 5.分子砌块反式-16′和中间体 11′的合成另外,成功实施了腈还原步骤,确认了11'作为备用C3类似物合成的合适分子砌块。通过pH控制沉淀法进行可扩展的精制,使得目标化合物2(EBL-3183)的整体纯度提高到95.3-95.5%的充分水平,满足了临床前研究对高纯度的需求。总结总的来说,该合成路线是以吲哚3为起始物,经过六个关键步骤制备了手性结构分子砌块9,总产率达到了47%。通过结晶和蒸馏的手段成功分离出目标异构体,制备了高度立体选择性的环丁烷结构单元反式-16′。最终,通过五个步骤,总产率达到了29%,满足了足够规模和纯度的要求,获得了新型MBL抑制剂候选化合物(EBL-3183)。参考文献1.Andrei Baran,Jevgenijs Kuzmins. et al. Optimized Synthesis of Indole Carboxylate Metallo-β-Lactamase Inhibitor EBL-3183. Org. Process Res. Dev. 2023, 27, 4, 692–706. https://doi.org/10.1021/acs.oprd.3c00002 阿拉丁:https://www.aladdin-e.com
应用实例
2024.05.21
【阿拉丁】基于1,3,4-噁二唑衍生物的生物活性化合物和材料
基于1,3,4-噁二唑衍生物的生物活性化合物和材料简介众所周知,1,3,4-噁二唑(1,3,4-Oxadiazoles)是一类重要的杂环化合物,也是药物分子以及有机合成中常见的杂环砌块。[1] 1,3,4-噁二唑杂环是呋喃的衍生物,其中两个亚甲基被两个氮原子取代。用两个氮原子取代这两个亚甲基会降低环的芳香性,市得到的噁二唑环表现出共轭二烯的性质。另一个杂原子由于诱导作用对噁二唑形成弱碱。在亲核取代反应中,氢原子被亲核试剂取代。合成1,3,4-噁二唑的常用合成路线包括酸肼(或肼)与酰氯/羧酸的反应,以及使用各种脱水剂如三氯氧化磷、亚硫酰氯、五氧化二磷、三氟甲酸酐、多磷酸直接环化二酰基肼,以及酸与(N-异氰氨基)三苯基磷烷的直接反应。应用药物化学许多1,3,4-噁二唑衍生物因其良好的生物和药理活性[2]广泛地存在于药物分子中,例如抗癌活性[3]、各种酶抑制剂[4]、除草剂[5]、抗真菌活性[6]等。已经上市的艾滋病抗病毒药物雷特格韦(Raltegravir)1,对 HIV 整合酶催化的链转移过程具有强效抑制作用,以最大限度地提高它们作为 HIV 整合酶抑制剂对野生型病毒和一些突变体的抑制作用,并优化其在临床前物种中的选择性、药代动力学和代谢特征。[7] Zibotentan 2 是一种特异性 ETA 受体拮抗剂,目前正处于治疗激素耐药前列腺癌(HRPC)的临床开发阶段。[8] 以及已上市的除草剂Methoxydiazone 3(图1)的化学结构中都具有1,3,4-噁二唑的结构单元,这很好地说明了1,3,4-噁二唑杂环在药物研发和农业化学中的应用潜力。材料化学除此之外,1,3,4-噁二唑也被广泛用于制造新型材料。例如,基于1,3,4-噁二唑结构的耐热聚合物[9],采用四唑路线或Suzuki偶联反应制备的9,9-二辛基芴和噁二唑的交替共聚物,可用作电子传输和蓝光发射聚合物(例如图1中的聚合物4)[10],由1,3,4-噁二唑重复单元组成树枝状聚合物[11],高效激光染料[12]和金属液晶[13]。图1. 基于1,3,4-噁二唑结构的生物活性化合物和材料的实例有机化学1,3,4-噁二唑早已广泛应用于有机化学合成之中,用于生成与亲电官能团反应的高活性卡宾中间体[14]。2,5-二氢-1,3,4-噁二唑由于其易于制备且相当稳定,还是双(杂原子)烯碳的热原来源,因此在有机合成中发挥着重要作用。此类烯碳化合物会与各种亲电官能团发生反应,通常会导致初始产物发生重排。这些产物可用作其他合成目标的起始原料,同时其热分解的副产品主要是N2和酮,因此从反应中分离产物相对比较简单。1,3,4-噁二唑的另一个有前途的合成应用是它们的分子内[4+2]/[3+2]交叉环加成反应[15]。图2. 1,3,4-噁二唑参与分子间反应级联的实例参考文献 1. J. Suwiński, J.; Szczepankiewicz, W. in Comprehensive Heterocyclic Chemistry, 3rd edition, eds. A.R. Katritzky, C.A. Ramsden, E.F.V. Scriven, and R. J.K. Taylor, Pergamon, Oxford, 2008. Vol. 5, p. 398.2. Yogesh, M.; Senthilkumar, G. P. World J. Pharmaceut. Res. 2019, 8, 1406-1428.3. Glomb, T.; Szymankiewicz, K.; Swiatek, P. Molecules 2018, 23, 3361/1-3361/16. https://doi.org/10.1021/acsomega.2c015864. Boström, J.; Hogner, A.; Llinàs, Wellner, E.; Plowright, A.T. J. Med. Chem. 2012, 55, 1817. https://doi.org/10.1016/j.bmcl.2015.11.0465. Das, A.C.; Debnath, A.; Mukherjee, D. Chemosphere 2003, 53, 217. https://doi.org/10.1016/s0045-6535(03)00440-56. Zou, X.-J.; Lai, L.-H.; Jin, G.-Y.; Zhang, Z.-X. J. Agric. Food Chem. 2002, 50, 3757. https://doi.org/10.1107/S241431462200342X7. Summa, V.; Petrocchi, A.; Bonelli, F.; Crescenzi, B.; Donghi, M. et al. J. Med. Chem. 2008, 51, 5843. https://doi.org/10.1021/jm800245z8. James, N. D.; Growcott, J. W. Drugs Future 2009, 34, 624.9. Hill, J. in Comprehensive Heterocyclic Chemistry, 2nd edition, eds. A. R. Katritzky, C. W. Rees, and E. F. V. Scriven, Pergamon, Oxford, 1996, vol. 4, p. 268.10. Ding, J.; Day, M.; Robertson, G.; Roovers, J. Macromolecules 2002, 35, 3474. https://doi.org/10.1021/ma011093n11. Verheyde, B.; Dehaen, W. J. Org. Chem. 2001, 66, 4062. https://doi.org/10.1002/pola.2133312. Nijegorodov, N.; Mabbs, R. Spectrochim. Acta, Part A, 2002, 58, 349. https://doi.org/10.1016/s1386-1425(01)00544-313.Wen, C.-R.; Wang, Y.-J.; Wang, H.-C.; Sheu, H.-S.; Lee, G.-H.; Lai, C.K. Chem. Mater. 2005, 17, 1646.14. Warkentin, J.; Acc. Chem. Res. 2009, 42, 205. https://doi.org/10.1021/ar800072h15. Elliott, G.I.; Fuchs, J.R.; Blagg, B.S.J.; Ishikawa, H.; Tao, H.; Yuan, Z.-Q.; Boger, D.L. J. Am. Chem. Soc. 2006, 128, 10589. https://doi.org/10.1021/ja0612549阿拉丁:https://www.aladdin-e.com
企业动态
2024.05.16
【阿拉丁】蛋白质印迹的上样对照
蛋白质印迹的上样对照自从1979年第一篇描述蛋白质印迹的出版物以来,这种免疫检测技术已经被广泛用于事变从细胞或组织中提取的复杂混合物中的特定蛋白质。蛋白质印迹具有三个基本要素:1按大小分离蛋白质,2转移到固相支持物上,3使用适当的一抗标记目标蛋白质,然后进行可视化(通常使用偶联的二抗)。随后工具和技术的改进,以及高灵敏度荧光标记的开发,有效地提高了检测极限,并使科学家能够探测组织特异性的正常和疾病。然而,科学家在使用定量蛋白质印迹法来识别蛋白质水平的变化时通常会遇到一些困难。这是由于许多蛋白质在不用组织和不同生理和病理条件下表现出不同的表达模式。蛋白质印迹:一项并不简单的常规技术尽管蛋白质印迹可能是最常用的免疫应用,单仍然存在一些可能长期被忽视的关键技术问题。例如,分离或分离方案是否会影响蛋白质或其翻译后修饰的完整性?能否区分蛋白质的讲解或聚集以及生物过程的相关产物?当结果是多个条带时,如何确定哪些是结果、变异、伪影? 定量蛋白质印迹可用于比较一组样品中靶蛋白的相对量,所述样品可代表不同的个体、治疗条件、疾病状态或其他生物学变量。为了准确识别和测量多个样品的总蛋白水平,科学家可以使用“上扬对照”作为内部标准。该对照是指添加针对假定存在于所有样品中的蛋白质的一抗,并且其相对丰度不受到生物变异或实验条件的影响。蛋白质靶标通常是上样对照的良好候选者,它们是普遍表达的“管家”基因产物。假设不同样品泳道之间的上样对照相同,使用上样对照可以对所有孔中的样品上样进行定量,以使结果标准化。使用上样对照还可以防止“边缘效应”,这是使用大量泳道时常见的情况,并且外侧泳道中的蛋白质转移到抹上更靠近框架的位置,从而导致在泳道上产生更强烈的染色。上样对照可用于显示蛋白质上样量是否发生变化,并可解释观察到的目标条带的变化。如果正确使用,上样对照可确保蛋白质得到正确定量,尽管蛋白质印迹所有泳道上的上样量存在细微差异。选择上样对照抗体β-肌动蛋白和β-微管蛋白一直被用作加载对照,因为它们的表达在大多数模型系统中是相对组成型的。然而,一些出版刊物质疑使用β-肌动蛋白作为标准负荷对照,理由是β-肌动蛋白和β-微管蛋白水平组织之间存在差异,并且它们的表达可能受到病理条件的影响。这些作者建议将总蛋白分析作为定量蛋白印迹中的替代技术,并建议在研究所研究基因的表达模式后应谨慎使用“管家”基因产品。尽管如此,β-肌动蛋白和β-微管蛋白作为内参抗体还是具有一定的优势:它们高度保守,表达水平高,在大多数实验条件下表现出较好稳定性。值得注意的是,必须根据所研究的特定组织或细胞类型选择对照,并且可能需要进行经验测试来验证上样对照的均匀性。通过上样对照抗体获得有效结果的技巧为了克服蛋白质印迹的变异性并减少数据解释中的错误,以下一些预防措施可能会有所帮助。 使用稳定表达且受实验条件影响最小的内部上样对照。 选择针对已知在样品中组成行表达的蛋白质的上样对照抗体。 利用第二个上样对照来证实第一个对照获得的结果。对于新的或新颖的样品来说,可能特别有价值。 上样对照应涵盖较宽的分子量范围,以便选择的对照与目标蛋白的分子量相似。这确保了可以在印迹上轻松的区分目标条带和对照条带。 上样对照抗体通常检测大量表达的管家蛋白,导致信号饱和,特别是在使用化学发光检测方法时,过饱和可能会导致上样对照条带无法用于参考,可能会隐藏目标蛋白质量的样品间差异。参考文献1. Renart J, Reiser J, Stark GR. 1979. Transfer of proteins from gels to diazobenzyloxymethyl-paper and detection with antisera: a method for studying antibody specificity and antigen structure.. Proceedings of the National Academy of Sciences. 76(7):3116-3120. https://doi.org/10.1073/pnas.76.7.31162. Dittmer A, Dittmer J. 2006. β-Actin is not a reliable loading control in Western blot analysis. Electrophoresis. 27(14):2844-2845. https://doi.org/10.1002/elps.2005007853. Eaton SL, Roche SL, Llavero, Hurtado M, et al. Total Protein Analysis as a Reliable Loading Control for Quantitative Fluorescent Western Blotting. PLoS ONE. 8(8):e72457. https://doi.org/10.1371/journal.pone.00724574. Li R, Shen Y. 2013. An old method facing a new challenge: Re-visiting housekeeping proteins as internal reference control for neuroscience research. Life Sciences. 92(13):747-751. https://doi.org/10.1016/j.lfs.2013.02.0145. Gorr TA, Vogel J. 2015. Western blotting revisited: Critical perusal of underappreciated technical issues. Prot. Clin. Appl.. 9(3-4):396-405. https://doi.org/10.1002/prca.201400118阿拉丁:https://www.aladdin-e.com
应用实例
2024.05.14
【阿拉丁】ROS1 融合抑制剂NVL-520与MGAT2 抑制剂 BMS-963272
ROS1 融合抑制剂NVL-520与MGAT2 抑制剂 BMS-9632721.NVL-520NVL-520(CAS: 2739829-00-4)是一种具有选择性抑制作用的药物,针对ROS1融合和次生抗性突变,同时具有TRK保护性和良好的脑穿透性。其设计合理,通过大环结构,对98%的激酶组中ROS1的选择性超过50倍。1.1 NVL-520的设计与结构NVL-520是一种大环小分子化合物(见图1A)。计算模型显示,NVL-520与ROS1结合的方式与劳拉替尼相似。NVL-520中的氨基吡啶基团与铰链区的Glu2027和Met2029形成两个氢键(见图1B)。图 1.NVL-520 的设计和生化活性NVL-520的临床前特性包括对ROS1及其多种耐药突变的强效靶向作用,以及对ROS1 G2032R的高度选择性,而非TRK。此外,它还具有良好的脑穿透性。这些特性标志着一种独特的ROS1酪氨酸激酶抑制剂的开发,有可能克服早期一代酪氨酸激酶抑制剂在ROS1融合阳性患者治疗中的局限性。1.2 NVL-520的合成路线NVL-520的合成中一个关键的步骤是合成中间体6(CAS号:2921961-52-4),其结构为4-((1-乙基-1H-吡唑-4-基)甲基)-5-碘-2-甲基-2H-1,2,3-三唑。 (S) -5-氟-3-甲基苯并[c][1,2]氧杂硼烷-1(3H)-醇的合成: 目标产物NVL-520的合成:2.BMS-963272近期,研究人员发现了一种高度有效且具有较高选择性的MGAT2抑制剂BMS-963272(CAS号:1441057-15-3)。作为首选的临床候选药物,该药物已经在一期临床试验中进行了评估。BMS-963272能够以较低的剂量在人体中实现靶向有效的暴露,可用于治疗代谢性疾病。经过进一步的小鼠模型测试发现,所选的类似物能够显著减少小鼠的食物摄入量和体重。随后,在MGAT2基因剔除小鼠中对主要候选药物12(BMS-986172)进行的研究表明,该药物具有靶向和基于机制的药理作用。2.1 BMS-963272的合成路线 利用埃尔曼化学(方案1)开发了一种用于合成必需的(S)-β-亚砜胺19-20的立体选择性方法,并通过对相关类似物进行X射线分析,确定了C6处的绝对立体化学结构。 在碱性条件下,1-(1-(环丙基甲基)-1H-吡唑-3-基)乙酮26与(溴甲基)环丙烷发生了烷基化反应,合成了1-(1-(环丙基甲基)-1H-吡唑-3-基)乙酮27。合成目标类似物所需的大多数杂环乙酸都很容易获得。四唑酮乙酸30a-b的合成详见方案2。 对于方案3中的四唑酮类似物12-14,可以使用PMB和SEM保护酸30a和30b来生成酮酰胺47-49。经过环化后,再进行一个额外的脱保护步骤(使用CAN脱保护PMB,使用TFA脱保护SEM),就可以以适度的产率生成12-14。 阿拉丁:https://www.aladdin-e.com 参考文献1. Alexander Drilon. et al. NVL-520 Is a Selective, TRK-Sparing, and Brain-Penetrant Inhibitor of ROS1 Fusions and Secondary Resistance Mutations. Cancer Discov (2023) 13 (3): 598-615. https://doi.org/10.1158/2159-8290.CD-22-09682.Wei Meng,Robert Brigance. et al. Discovery of 12 (BMS-986172) as a Highly Potent MGAT2 Inhibitor that Achieved Targeted Efficacious Exposures at a Low Human Dose for the Treatment of Metabolic Disorders. J. Med. Chem. 2023, 66, 18, 13135–13147. https://doi.org/10.1021/acs.jmedchem.3c01147
企业动态
2024.05.13
【阿拉丁】纳米颗粒用于共振成像造影剂
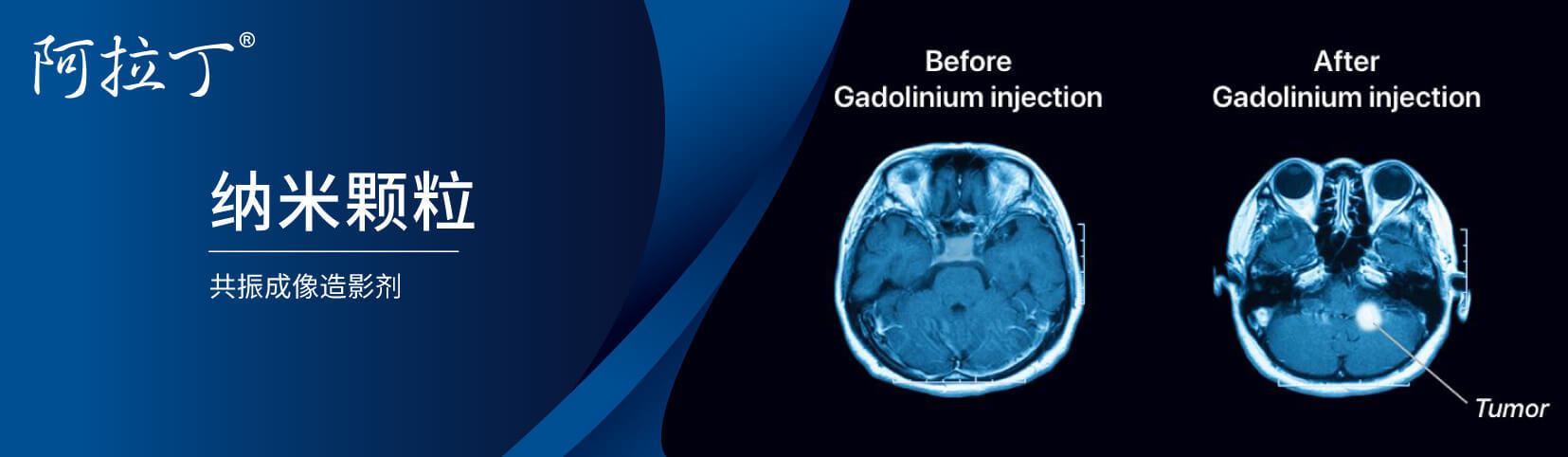
纳米颗粒用于共振成像造影剂磁共振成像(MRI)是利用核磁共振(NMR)原理加上梯度磁场来探测发射的电磁波并绘制物体内部结构图像的技术。MRI的原理可以简单概括为:根据需要将样品分成几层薄层。每一层都可以分成一个小体积,称为体素。为每个体素校准一个标记,这个过程称为编码或空间定位。对某一层施加射频脉冲后,接收并解码该层的NMR信号,得到各体素的核磁共振信号。最后,根据体素与编码体素之间的对应关系,得到体素信号的大小,并显示在屏幕的相应像素上。其中,信号大小用不同的灰度级别表示。信号大的像素亮度高,信号小的像素亮度低。这样,就可以得到反映每个体素NMR信号大小的图像,即MRI图像。MRI是近年来发展迅速的一项医学诊断技术,已广泛应用于各种疾病的发现和早期诊断。其中,磁共振成像造影剂是这一技术的重要组成部分。MR中的对比取决于质子自旋密度,以及纵向(T1)和横向(T2)弛豫时间(图1),对比剂可以显著增强T1加权或T2加权图像。临床上使用的钆螯合物缩短T1,从而增加了浓度依赖性的弛豫度r1(T1的倒数),从而在MR中产生增亮效果。或者,超顺磁性氧化铁纳米颗粒可以缩短T2(增加r2),导致信号减少,从而产生变暗效果。另外还有一种来自磁场不均匀性的减相效应,称为T2,通常比T1短。图 1. 钆配合物与水的相互作用,导致水质子松弛磁共振成像造影剂常用的MRI造影剂及其基本分类的总结如下:• 钆基造影剂基于钆(III)的造影剂分为三大类:细胞外液(ECF)造影剂、血池造影剂(BPCAs)和器官特异性造影剂。• 锰基造影剂锰增强MRI(MEMRI)使用锰离子(Mn2+),这种造影剂在动物实验中有应用。Mn2+通过钙(Ca2+)通道进入细胞,因此,这组造影剂可用于功能性脑成像。先前的一项MRI研究表明,氧化石墨烯纳米片和氧化石墨烯纳米带的Mn2+碳纳米结构复合物是非常有效的MRI造影剂。• 氧化铁造影剂氧化铁造影剂有两种:超顺磁性氧化铁(SPIO)和超小超顺磁性氧化铁(USPIO)。超顺磁造影剂由氧化铁纳米颗粒的悬浮胶体组成。在成像过程中应用时,它们会降低吸收造影剂的组织中T2信号的强度。SPIO和USPIO在一些肝脏肿瘤的诊断中取得了成功的结果。这组造影剂的纳米尺寸和颗粒形状允许不同的生物分布和应用,这是其他造影剂所无法观察到的。目前,纳米颗粒氧化铁是临床实践中使用的一种流行且独特的纳米颗粒剂。然而,由于复杂的现代分子和细胞成像技术,使疾病特异性生物标志物在微观和分子水平上可见,其他纳米颗粒作为潜在的MRI造影剂也得到了更多的关注。由于纳米技术的巨大进步,新型纳米颗粒MRI造影剂已被开发出来,其造影剂的造影剂能力以及其他功能得到了进一步提高。• 铁铂造影剂与氧化铁纳米粒子相比,超顺磁性铁铂粒子(SIPPs)具有显著改善的T2弛豫特性。SIPP已被磷脂包裹,以创建多功能SIPP隐形免疫胶束,以特异性靶向人类前列腺癌细胞。据我们所知,这些造影剂仍在研究中,尚未在人体中进行研究。一般来说,MRI造影剂有三种基本类型,根据不同的标准进行分类。1. 根据MRI造影剂的磁性中心,MRI造影剂可分为顺磁性物质、超顺磁性物质和铁磁性物质三大类。2. 根据药代动力学特点,MRI造影剂可分为以下三类:非特异性细胞外造影剂、细胞结合及细胞内造影剂、血池造影剂。3. 根据造影剂是否带电荷,顺磁共振成像造影剂可分为以下两种:非离子造影剂和离子造影剂。 参考文献1. Colombo, M. , Carregalromero, S. , Casula, M. F. , Gutiérrez L, Morales, M. P. , & Böhm IB, et al. (2012). Biological applications of magnetic nanoparticles. Pharmaceutical Research, 41(11), 4306. https://doi.org/10.1039/C2CS15337H2. Meng, X., Seton, H. C., Lu, L. T., Prior, I. A., Thanh, N. T. K., & Song, B. . (2011). Magnetic copt nanoparticles as MRI contrast agent for transplanted neural stem cells detection. NANOSCALE, 3(3), 977-0.https://doi.org/10.1039/C0NR00846J3. Pablico-Lansigan, M. H., Hickling, W. J., Japp, E. A., Rodriguez, O. C., Ghosh, A., Albanese, C., ... & Stoll, S. L. (2013). Magnetic nanobeads as potential contrast agents for magnetic resonance imaging. ACS nano, 7(10), 9040-9048.https://doi.org/10.1021/nn403647t4. Xiao, Y. D., Paudel, R., Liu, J., Ma, C., Zhang, Z. S., & Zhou, S. K. (2016). MRI contrast agents: classification and application (review). International Journal of Molecular Medicine, 38(5). https://doi.org/10.3892/ijmm.2016.2744阿拉丁:https://www.aladdin-e.com
应用实例
2024.05.11
【阿拉丁】胶体金在电子显微镜领域的应用
胶体金在电子显微镜领域的应用在研究细胞和细胞器的复杂结构以及研究细胞生物过程时,电子显微镜是必不可少的。胶体金及其各种衍生物一直是生物电子显微镜中应用最广泛的抗原标记物。这些颗粒可以附着在包括抗体、凝集素、超抗原、聚糖、核酸和受体等许多传统的生物探针上。由于大小不同,这些颗粒在电子显微镜下很容易区分,从而允许同时进行多次标记实验。1971年,胶体金作为一种特殊的标记物首次被引入透射电子显微镜(TEM)。然后在1975年,Horisberger和他的同事开发了用于扫描电子显微镜(SEM)的胶体金法,并于1979年用于荧光显微镜。1979年报道了用X射线绘制金粒子图。在SEM中,胶体金法已被用于标记许多细胞,包括酵母、红细胞、血小板、肝细胞和乳脂球。SEM的一个优点是人们可以观察到相对较大的区域的细节(图 1)。与其他传统的SEM标记不同,金标记是二次电子的良好发射器,这使得观察者能够在没有金属涂层的细胞表面定位金颗粒。目前最方便的金标记物尺寸约为50 nm,不过也发现了小到Au22的颗粒。图 1 :SKBR3细胞中HER2纳米免疫金标的预包埋SEM。无论(A)是否与抗HER2纳米体(B, D)或抗HER2抗体曲妥珠单抗(C)一起孵育,SKBR3细胞都被固定。在冷鱼明胶和乙酰化牛血清白蛋白的混合物中进行免疫标记。随后,用二抗和15 nm的蛋白A偶联金颗粒孵育细胞。按照材料和方法中描述的方法,对样品进行临界点干燥和电子显微镜检查。刻度:左图:A:1µm,B, C:0.5µm,D:0.2µm;右面板:A:250 nm,B-D:100 nm。在TEM中,由于它们对电子的不透明性和它们的特征形状,可以很容易地识别金标记物。此外,粒径的选择取决于所使用的放大倍率和考虑结合位点的位阻不可达性。Au5和 Au20颗粒是最常用于标记病毒、细菌、酵母、植物细胞和各种动物细胞的颗粒(图 2)。图 2:SKBR3细胞中HER2免疫金标的预包埋纳米体TEM。SKBR3或MDA- MB-231细胞用4%(w/v)甲醛固定,并进行免疫标记处理。作为阴性对照,省略一抗(A)或使用缺乏HER2表达的MDA-MB-231细胞(B)。SKBR3细胞在(C, E)或(D, F)甲醛固定后与抗HER2纳米体11A4(VHH)(C, D)或曲妥珠单抗(mAb)(E, F)孵育。尺度= 500 nm。免疫电子显微镜是检测和定位细胞和组织中蛋白质的最佳方法之一。这种方法几乎可以应用于每一种单细胞和多细胞生物,通常可以在结构和功能的关联之间提供意想不到的见解。结合金颗粒的一抗的应用允许对细胞上和细胞内的多种抗原进行高分辨率的检测和定位。但免疫电镜的成功应用是由以下因素决定的:1)蛋白质抗原性的保存;2)抗体浸润整个细胞的能力;3)抗原和一抗之间识别的特异性。此外,需要对生物样品进行适当的处理,例如固定,这涉及到适当选择包埋树脂和针对目标分子的特异性抗体。虽然传统的电子显微镜不能提供关于特定分子的信息,但免疫金标记可以在可见结构与特定的原位定位和分子分布之间建立高分辨率的联系。如此看来,毫无疑问,胶体金颗粒的应用代表了免疫化学方法改进中的一个重大事件。在将胶体金引入免疫细胞化学的过程中,开发了许多方案。一般来说,它们是基于TEM的, 包括在树脂包埋后的免疫标记或在此过程之前的免疫染色。虽然胶体金在组织化学中有几种用途,但它的主要应用是在细胞化学中使用扫描电镜和透射电镜。这种方法很常见,它依赖于各种各样的大分子,这些大分子可以附着在金颗粒上。此外,金标记物可以快速廉价地制备,同时几乎没有非特异性吸附,并且可以通过各种方法对其进行量化。它们也是多次标记实验的理想选择。最后,通过在电子显微镜下使用胶体金,可以清楚地识别细胞内抗原。参考文献1. Horisberger, M. (1981). Colloidal gold as a cytochemical marker in electron microscopy. Gold Bulletin, 14(3), 90-94.https://link.springer.com/article/10.1007/BF032167352. De Paul, A. L., Mukdsi, J. H., Petiti, J. P., Gutiérrez, S., Quintar, A. A., Maldonado, C. A., & Torres, A. I. (2012). Immunoelectron microscopy: a reliable tool for the analysis of cellular processes. In Applications of Immunocytochemistry. IntechOpen. https://sc.panda321.com/#google_vignette3. Horisberger, M., Rosset, J., & Bauer, H. (1975). Colloidal gold granules as markers for cell surface receptors in the scanning electron microscope. Experientia, 31(10), 1147-1149. https://link.springer.com/article/10.1007/BF023267614. Kijanka, M., van Donselaar, E. G., Müller, W. H., Dorresteijn, B., Popov-Čeleketić, D., El Khattabi, M., & Post, J. A. (2017). A novel immuno-gold labeling protocol for nanobody-based detection of HER2 in breast cancer cells using immuno-electron microscopy. Journal of structural biology, 199(1), 1-11.https://doi.org/10.1016/j.jsb.2017.05.008阿拉丁:https://www.aladdin-e.com
应用实例
2024.05.10
【阿拉丁】新药研发中的点击化学
新药研发中的点击化学在点击化学反应家族中,最受关注的可能莫过于Cu(I)催化末端炔烃与有机叠氮化物发生1,3-偶极环加成反应(Huisgen反应)生成1,4-二取代1,2,3-三唑(方案1)。1 作为一种“好”的点击反应,该反应可靠、产量高、易于进行、不受空气或湿气的影响,并可兼容多种官能团。在许多情况下,水是理想的反应溶剂,可提供最佳产率和最快反应速率。通常情况下,环加成产物是固体,无需进行色谱纯化。1,2,3-三唑环化学性质稳定,不易水解、氧化、还原或以其他方式裂解。以上这些特性使得Cu(I)催化的叠氮-炔环化成为新药研发过程中药物分子库开发的重要手段。2方案1在抗坏血酸作为还原剂的条件下使用Cu(II)盐形成具有催化活性的Cu(I)一直是制备合成1,2,3-三唑的常选方法,但可能在生物偶联应用当中存在问题。Cu(I)盐,如[Cu(CH3CN)4]PF6可在稳定配体三[(1-苯甲基-1H-1,2,3-三唑-4-基)甲基]胺(TBTA)存在下直接使用(图1)。3 TBTA已被证明可以有效地增强铜催化的环加成反应,同时还不会破坏生物支架。图1.TBTA(T162437) 尽管Cu(I)催化的点击反应提供了获得1,4-二取代三唑的途径,但过渡金属变体获会得互补的1,5-二取代三唑异构体。在催化剂Cp*RuCl(PPh3)2的存在下,用叠氮化物处理末端或内部炔烃提供了具有完全控制区域特异性的高收率的环加合物(方案2)。4方案2 在市面上,许多有机叠氮化物是不易获得的。Carreira及其同事最近报道了Co(II)催化未活化烯烃与对甲苯磺酰基叠氮化物(TsN3)的加氢叠氮化反应,得到烷基叠氮化物(方案3)。5该催化剂很容易由Co(BF4)2·6H2O和Schiff碱配体原位制备。在加氢叠氮化反应中可以兼容单取代、二取代和三取代的烯烃,并且完全体现出马氏规则的选择性。此外,反应可以与夏普莱斯三唑环加成偶联,在一锅法中得到1,4-三唑。方案3 阿拉丁可为您的点击化学研究需求提供各种试剂、催化剂和配体。 参考文献 1.Rostovtsev V. 2002. Angew. Chem.. Int. Ed.. 412596.2.Tornøe CW, Christensen C, Meldal M. 2002. Peptidotriazoles on Solid Phase: [1,2,3]-Triazoles by Regiospecific Copper(I)-Catalyzed 1,3-Dipolar Cycloadditions of Terminal Alkynes to Azides. J. Org. Chem.. 67(9):3057-3064. https://doi.org/10.1021/jo011148j3.Kolb H. 2001. Angew. Chem.,. Int. Ed. 402004.4.Kolb HC, Sharpless K. 2003. The growing impact of click chemistry on drug discovery. Drug Discovery Today. 8(24):1128-1137. https://doi.org/10.1016/s1359-6446(03)02933-75.Manetsch R, Krasi?ski A, Radi? Z, Raushel J, Taylor P, Sharpless KB, Kolb HC. 2004. In Situ Click Chemistry: Enzyme Inhibitors Made to Their Own Specifications. J. Am. Chem. Soc.. 126(40):12809-12818. https://doi.org/10.1021/ja046382g阿拉丁:https://www.aladdin-e.com
应用实例
2024.04.23
【阿拉丁】免疫细胞化学染色实验方案
免疫细胞化学染色实验方案第1阶段 样品制备和固定样品的固定是 ICC 实验和储存过程中维持细胞形态的重要步骤。对于盖玻片上培养的细胞在此过程中,细胞在固定前直接培养在盖玻片上。所需材料− 标准盖玻片或多孔板− 无菌PBS− 用于包被的蛋白质(例如聚-L-赖氨酸)− 无菌水步骤1. 制备包被溶液并过滤——必要时灭菌。提示 :不同的样品类型可能需要不同的蛋白质来帮助粘附。典型的包被溶液是在 PBS 中添加聚-L-赖氨酸 (PLL)、聚-D-赖氨酸 (PDL) 或明胶制备而成。请参阅文献了解您感兴趣的细胞类型和推荐的包被蛋白浓度。2. 用包被溶液覆盖玻片或平板。室温下孵育时间通常为1小时至24 时。提示: 将盖玻片放入组织培养板的孔中,并用包被液覆盖。3. 用无菌 PBS冲洗盖玻片3次。提示: 这是为了确保去除盖玻片上的游离蛋白质。4. 让盖玻片完全干燥。如果需要,在紫外线下消毒至少4小时。警告:或者,盖玻片可以在包被之前用 70% 乙醇清洗,并在整个过程中使用无菌溶液。5. 在包被的盖玻片或平板上培养细胞。6. 确定细胞总数并检查细胞活力。一般来说,存活率应为 90 - 95%。7. 准备固定剂,并用选定的固定剂孵育细胞。固定剂时间4% 多聚甲醛(PFA)的PBS溶液室温孵育 10-20 分钟甲醇(95-100%)-20°C 孵育 5 - 10 分钟乙醇(95-100%)-20°C 孵育 5 - 10 分钟丙酮-20°C 孵育 5 - 10 分钟提示:乙醇、甲醇和丙酮会使细胞透化,因此使用这些固定剂前通常不需要另外透化。较长的孵育时间通常会导致较高程度的固定,直至表位可能过度固定。孵育时间短可能会导致表位保存不良和样品固定不足。最佳固定时间需要凭经验确定。8. 用洗涤缓冲液清洗细胞 3 次。提示:理想情况下,固定后尽快进行染色。但样品可以保存在 0.1% 叠氮化钠/PBS 中,在 4°C下保存 1-2 周。较长的储存时间可能会缓慢地逆转固定,导致形态较差和表位保存不良。对于悬浮细胞对于悬浮细胞,可以在将悬浮液培养到载玻片上之前洗涤并固定细胞。 所需材料− 细胞悬液− 聚苯乙烯圆底 12 × 75 mm 2 个Falcon 管/96 孔板(或任何与您的离心机兼容的容器)− 悬浮液/洗涤缓冲液(例如PBS)步骤1. 根据厂商的指导收获和洗涤细胞。2. 确定细胞总数,并检查细胞活力。一般来说,存活率应为90 - 95%。3. 离心,并在冰冷的悬浮缓冲液中重悬细胞样品。3.1. 在4°C下以约 200 xg 离心5分钟。提示:旋转时间和速度可能需要优化。4. 准备固定剂,并用选定的固定剂孵育细胞。固定剂时间4% 多聚甲醛(PFA)的PBS溶液室温孵育 10-20 分钟甲醇(95-100%)-20°C 孵育 5 - 10 分钟乙醇(95-100%)-20°C 孵育 5 - 10 分钟丙酮-20°C 孵育 5 - 10 分钟提示:乙醇、甲醇和丙酮会使细胞透化,因此使用这些固定剂前通常不需要另外透化。较长的孵育时间通常会导致较高程度的固定,直至表位可能过度固定。孵育时间短可能会导致表位保存不良和样品固定不足。最佳固定时间需要根据经验确定。5. 用洗涤缓冲液清洗细胞3次。5.1. 将细胞离心成沉淀(200 xg,5分钟,4°C)。5.2. 每次洗涤后去除上清液并重新悬浮沉淀。提示:理想情况下,固定后尽快进行染色。但样品可以保存在 0.1% 叠氮化钠/PBS 中,在4°C下保存 1-2 周。较长的储存时间可能会缓慢地逆转固定,导致形态较差和表位保存不良。6. 将约10 µL悬浮细胞移至载玻片上。使用的最佳细胞密度取决于所使用的细胞系和实验要求。此时的典型密度为 10 6 - 10 7 个细胞/mL。 第 2 阶段 透化(可选)透化作用将部分溶解细胞膜,使抗体能够到达细胞内表位。如果 PFA 用作固定剂,则尤其需要这样做。甲醇等有机溶剂通常会同时透化和固定细胞,因此使用有机溶剂作为固定剂时并不严格要求透化。 所需材料− 经过相关固定步骤的样品− PBS− 洗涤剂(见表1)− 疏水屏障笔(可选)步骤所需时间约20分钟。1. 根据以下步骤,用 PBS 稀释洗涤剂来制备透化溶液:表 1:透化用洗涤剂洗涤剂建议浓度时间刺激性清洁剂:Triton X-100、NP-40PBS 中 0.1- 0.2%孵育2-5分钟温和清洁剂:Tween 20、皂苷、毛地黄皂苷、leucopermPBS 中 0.2 - 0.5%孵育2-5分钟警告: Triton X-100 是最常用的用于提高抗体渗透性的去污剂。然而,它通常不太适合膜相关抗原,因为它溶解膜及其相关蛋白。最佳的去垢剂取决于蛋白质及其定位。应针对所使用的样品优化去污剂的浓度和孵育时间。如果样品在载玻片上,您可以用PAP笔圈出细胞样品,以帮助汇集试剂。2. 用透化溶液覆盖细胞并在室温下孵育 2-5 分钟。提示:如果样品位于载玻片上,您可以用 PAP笔圈出细胞样品,以帮助汇集试剂。3. 用 PBS 洗涤细胞 3 次。 第三阶段 封闭在 ICC 中,封闭步骤对于防止图像中的高背景染色特别重要。典型的封闭剂是与二抗宿主物种或BSA相对应的2-10%血清蛋白溶液,其物种依赖性较小,但封闭效率可能较低。封闭液不应含有一抗宿主动物的血清,因为这可能会导致高背景。 所需材料− 已经历相关固定和透化步骤的样品− 蛋白封闭剂− 二抗宿主物种的正常血清− 牛血清白蛋白(例如,B265991)− PBS(例如P492453)− 甘氨酸步骤所需时间约2小时。1. 准备封闭缓冲液。1.1. 将所选的蛋白质封闭剂溶解在PBS中至2-10 % w/v。1.2. 加入浓度为0.1 M的甘氨酸(可选)。封闭剂何时使用山羊血清如果用于检测的二抗是在山羊体内产生的驴血清如果用于检测的二抗是在驴体内产生的牛血清白蛋白通常与多种抗体兼容2. 通过在封闭缓冲液中孵育细胞来封闭细胞。室温孵育1-2 h警告:如果样品位于载玻片上,您可以用PAP笔圈出细胞样品,以帮助汇集试剂。3. 继续抗体孵育。 第4阶段 抗体孵化执行必要的封闭步骤后,您现在就可以用抗体对细胞进行染色了。通常有两个原则:(i) 直接 ICC,其中一抗直接与荧光团缀合,以及 (ii) 间接 ICC,其中使用合适的荧光标记二抗检测一抗。两种方法都有优点和缺点,这里将更详细地讨论。间接 ICC 是最常用的协议。 多色 ICC 涉及使用两组或多组抗体对细胞进行染色,以揭示两种或多种感兴趣蛋白质的分布或共定位。下面给出的间接和直接协议均可适用于多色 ICC。如果间接 ICC 用于多色,强烈建议使用预吸附二抗。这些抗体针对其他物种进行了预吸附,从而最大限度地减少了所用二抗与来自不同物种的一抗发生交叉反应的机会。间接法所需材料− 已经历相关透化/封闭步骤的细胞− 抗体稀释缓冲液 PBS(例如 P492453)或 PBS-T(含有 0.1% Tween-20 的 PBS,例如 T434505、P196391)− 洗涤缓冲液 PBS(例如 P492453)或 PBS-T(含 0.1% Tween-20 的 PBS,例如T434505、P196391)− 一抗− 偶联二抗− 疏水性屏障笔——可选用于载玻片或盖玻片上的小细胞体积步骤所需时间约13小时30分钟。1. 确定要使用的最佳抗体稀释度。然后用抗体稀释缓冲液稀释抗体。抗体数据表上通常会建议最佳稀释度。警告:您应该进行稀释以确定最有效的抗体浓度。抗体稀释缓冲液可以仅为PBS。稀释缓冲液还可能含有 0.1% Tween(以降低表面张力)和 1% BSA(作为额外的封闭剂以减少非特异性结合)。2. 将样品在预稀释的一抗中孵育。室温孵育 2 小时,或4°C过夜警告:孵育时间和温度可能需要优化。提示 1:抗体溶液需要完全覆盖您的样品。提示 2:使用疏水性屏障笔有助于容纳小体积。3. 用 PBS 或 PBS-T 清洗载玻片3次。4. 在抗体稀释缓冲液中制备二抗,并将样品浸入预稀释的二抗中。室温孵育1小时。提示 :可能需要优化孵育时间和抗体浓度。典型的二抗稀释度为 1:1000 或 1:2000 或 0.1-2 µg/mL。对于多色实验,通常可以稀释不同的二抗并一起孵育。如果使用荧光团,则必须在黑暗中孵育以避免光漂白。5. 用 PBS 或 PBS-T 清洗样品 3 次。6. 继续复染、封片和成像。直接法所需材料− 已经历相关透化/封闭步骤的细胞− 抗体稀释缓冲液 PBS(例如 P492453)或 PBS-T(含有 0.1% Tween-20 的 PBS,例如 T434505、P196391)− 洗涤缓冲液 PBS(例如 P492453)或 PBS-T(含 0.1% Tween-20 的 PBS,例如 T434505、P196391)− 偶联一抗− 疏水性屏障笔——可选用于载玻片或盖玻片上的小细胞体积步骤所需时间约12小时15分钟。1. 确定要使用的最佳抗体稀释度。然后在抗体稀释缓冲液中稀释抗体。提示:抗体数据表上通常会建议最佳稀释度。如果没有,您可能需要进行稀释以找到最有效的抗体浓度。抗体稀释缓冲液可以仅为PBS。我们还建议添加 0.1% Tween(以降低表面张力)和 1% BSA(作为额外的封闭剂以减少非特异性结合)。2. 将样品浸入预稀释的一抗中。室温孵育2小时,或4°C过夜。警告:孵化时间可能需要优化。提示 1:抗体溶液需要完全覆盖您的样品。提示2: 使用疏水性屏障笔可以帮助容纳小体积。3. 用 PBS 或 PBS-T 清洗样品3次。4. 按照制造商推荐的方案完成任何适当的复染。 第 5 阶段 复染和检测ICC 过程的最后一步是样品封片并检测信号。这涉及将盖玻片添加到载玻片上(用于盖玻片上的细胞培养物),或将盖玻片覆盖到样本上,以实现成像。 典型的细胞核复染剂是 DAPI (D598342)、HOECHST 33342 (H288601) 或 DRAQ7 (D266297)。还有一些细胞器或细胞骨架复染剂可用(P287444) 。 所需材料− 用荧光团偶联抗体染色的细胞− 荧光复染剂(可选,例如:DAPI D598342)− 适用于荧光检测的封固剂(适用于盖玻片或载玻片上的细胞)− 密封剂(用于盖玻片或载玻片上的细胞,例如:指甲油)− PBS(适用于孔中的细胞,例如 P492453)− 荧光显微镜步骤1. 如果需要,将样品浸入复染溶液中。1.1. 根据制造商的指导在室温下孵育,或直至观察到所需的颜色。提示:某些封固剂含有荧光复染剂(参见 H288601)。这样就无需单独对载玻片进行复染以添加封固剂。2. 封固您的样品。样本格式程序盖玻片或显微镜载玻片上的细胞1,在载玻片上添加几滴封固剂并在室温下静置。2,使用镊子将盖玻片放在载玻片上。如果使用水性封固剂,请用柠檬烯或指甲油密封。3,密封后,将载玻片放在荧光显微镜上。细胞在孔中生长1,用 PBS 或存储缓冲液(PBS 中的 0.1% 叠氮化钠)覆盖样品。2,将样品直接置于倒置显微镜下。提示:封片剂通常含有抗淬灭剂,有助于更长时间地保存荧光。3. 使用适当的激发/发射滤光片组和/或激光器对样品进行成像。如需了解更多产品详情,请前往阿拉丁官网查询。阿拉丁:https://www.aladdin-e.com/
应用实例
2024.04.22
【阿拉丁】1,3-噻唑砌块在天然产物和合成材料中的应用
1,3-噻唑砌块在天然产物和合成材料中的应用噻唑(thiazole),也称1,3-噻唑,是一种同时含有硫和氮的五元杂环化合物。“噻唑”也指一大类衍生物。噻唑本身是一种具有吡啶类气味的淡黄色液体,分子式为C3H3NS。[1,2] 噻唑环是维生素硫胺素(B1)的重要组成成分之一。分子和电子结构噻唑是唑类化合物中的一员,除此之外还有咪唑和恶唑。噻唑环是平面的且具有芳香性。噻唑的特征在于比相应的恶唑具有更大的π电子离域,因此具有更大的芳香性。在HNMR光谱中,氢的化学位移(在7.27和8.77ppm之间)也证明了这种芳香性,显著地表明出了强的抗磁性环电流。计算的π电子密度将C5标记为亲电取代的主要位点,将C2标记为亲核取代的位点。噻唑及其盐噻唑官能团是维生素B1和埃博霉素的一个重要的组成结构。其他比较重要的噻唑化合物包括其与苯的稠环衍生物,即苯并噻唑,存在于萤火虫的化学荧光素中。当噻唑中的氮原子被烷基化后,就形成了一个噻唑盐。在施泰特尔反应和安息香缩合中,噻唑盐可以当作催化剂。噻唑染料也被用来染棉花。噻唑类化合物在生物大分子中的含量很高,而氧原子替代硫原子的恶唑类化合物则不然。它存在于天然存在的肽中,并被用于开发拟肽分子(即模仿肽的功能和结构的分子)[3]。应用取代的1,3-噻唑结构在天然产品和合成材料的应用中无处不在。[4]图 1. 天然产品和人工合成分子中出现的噻唑化合物 从不同海洋生物的蓝藻中分离出的含噻唑的天然产物包括小分子线性肽(例如图1中的Nordysidenin 1)、线性寡肽(称为Apramidas)、环肽(例如图1中所示的Tenuecyclamide A 2)和生物碱。[5] 此外,在一些土壤细菌提取物中还发现了一些含有噻唑环的大环类化合物和环状内酯。[6] 1,3-噻唑是药物发现阶段中的一种特殊分子砌块。许多基于噻唑的化合物被证实具有抗肿瘤、抗真菌和酶抑制活性;[7] 其中一些是目前批准的药物。[8] 1,3-噻唑在有机合成中也是不可或缺的,在不对称反应中可作为甲酰基官能团的固定基团和手性助剂。[9,10] 1,3-噻唑衍生作为荧光染料(如噻唑橙 3)已在细胞学中作为DNA的“发光”探针得到重要应用。该技术受益于含有噻唑的半导电共轭聚合物[11] 以及催化剂,如图1中的化合物4 [12]。参考文献1. Zoltewicz, J. A.; Deady, L. W. (1978). Quaternization of Heteroaromatic Compounds. Quantitative Aspects. Advances in Heterocyclic Chemistry. Vol. 22. pp. 71-121. doi:10.1016/S0065-2725(08)60103-8. ISBN 9780120206223.2. Eicher, T.; Hauptmann, S. (2003). The Chemistry of Heterocycles: Structure, Reactions, Syntheses, and Applications. ISBN 978-3-527-30720-3.3. Mak, Jeffrey Y. W.; Xu, Weijun; Fairlie, David P. (2015-01-01). Peptidomimetics I (PDF). Topics in Heterocyclic Chemistry. Vol. 48. Springer Berlin Heidelberg. pp. 235–266. doi:10.1007/7081_2015_176. ISBN 978-3-319-49117-2.4. Chen B.; Heal, W. In Comprehensive Heterocyclic Chemistry, 3rd edition, eds. A.R. Katritzky, C.A. Ramsden, E.F.V. Scriven, and R. J.K. Taylor Pergamon, Oxford, 2008. Vol. 4, p. 635.5. König, G.M.; Kehraus, S.; Seibert, S.F.; Abdel-Lateff, A.; Müller, D. ChemBioChem 2006, 7, 229.6. Hofle, G.H.; Bedorf, N.; Steinmetz, H.; Schomburg, D.; Gerth, K.; Reichenbach, H. Angew. Chem. Int. Ed. 1996, 35, 1567.7. (a) Kumar, S.; Patil, M. T.; Kataria, R.; Salunke, D. B. Eds. Gupta, G. K.; Vinod, K. Chem. Drug Design 2016, 243-281. (b) Thorat, B. R.; Joshi, V.; Thorat, V. B. Heterocycl. Lett. 2016, 6, 389-409.8. According to www.drugbank.ca as of September 2019 there are 28 thiazole-containing marketed drugs. These drugs include natural products, natural-product-based architectures, and purely synthetic compounds.9. Dondoni, A.; Marra, A. Chem. Rev. 2004, 104, 2557.10. Velazquez, F.; Olivo, H.F. Curr. Org. Chem. 2002, 6, 303.11. (a) Subramaniyan, S.; Kim, F.S.; Ren, G.; Li, H.; Jenekhe, S.A. Macromolecules 2012, 45, 9029. (b) Hussain, S.; De, S.; Iyer, P.K. ACS Appl. Mater. Interfaces 2013, 5, 2234.12. (a) Luo, Q.-L.; Tan, J.-P.; Li, Z.-F.; Nan, W.-H.; Xiao, D.-R. J. Org. Chem. 2012, 77, 8332. (b) Frija, L. M. T.; Pombeiro, A. J. L.; Kopylovich, M. N. Coord. Chem. Rev. 2016, 308, 32-55.阿拉丁:https://www.aladdin-e.com
应用实例
2024.04.22
【阿拉丁试剂】免疫沉淀(IP)裂解液和试剂
免疫沉淀(IP)裂解液和试剂 免疫沉淀是一种能够纯化蛋白质的方法。将目标蛋白质的抗体与细胞提取物一起孵育,抗体会与溶液中的蛋白质结合。通过使用蛋白A/G偶联的琼脂糖珠将抗体/抗原复合物从样品中提取出来 。这可以将目标蛋白质与样品的其余部分分离。然后通过SDS-PAGE分离样品进行蛋白质印迹分析。裂解缓冲液理想的裂解缓冲液将最大限度地减少蛋白质变性,同时从样品中释放足够量的蛋白质。NP-40和Triton X-100等非离子型去污剂的刺激性低于SDS和脱氧胆酸钠等离子型去污剂。其他可能影响免疫沉淀成功的变量包括了盐浓度、二价阳离子浓度和pH值等。为了优化变量,应在以下范围内测试它们:-盐:0-1 M-非离子洗涤剂:0.1-2%-离子洗涤剂:0.01-0.5%-二价阳离子:0-10 mM-EDTA:0-5 mM-酸碱度:6-9非变性裂解缓冲液用于可溶于去污剂且可被抗体以天然形式识别的抗原。Triton X-100可以替代NP-40。-20 mM Tris HCl pH 8-137 mM 氯化钠-1% Nonidet P-40 (NP-40)-2 mM EDTA4°C下最多可保存6个月,使用前立即添加蛋白酶抑制剂。为方便起见可配制10%脱氧胆酸钠储备液(5g加入50mL),必须避光。不含去垢剂的可溶性蛋白裂解缓冲液一些可溶性蛋白质可能不需要使用洗涤剂。此缓冲液用于机械细胞裂解,例如使用杜恩斯匀浆器进行匀浆。PBS含有:-5mM EDTA-0.02%叠氮化钠4°C下最多可保存6个月,使用前立即添加蛋白酶抑制剂。非去污剂可溶性抗原的变性裂解缓冲液仅识别变性蛋白质的抗体无法接近天然蛋白质的表位。收获和裂解细胞时,在变性裂解缓冲液中加热细胞。该方法也可用于无法用非离子去污剂从细胞中提取的抗原。使用蛋白酶抑制剂将有助于从染色质中提取蛋白质。1% SDS5mM EDTA室温下最多可保存1周。使用前立即添加10 mM二硫苏糖醇或β-巯基乙醇蛋白酶抑制剂15 U/mL洗涤缓冲液-10mM Tris;调节pH至7.4-1mM EDTA-1mM EGTA;pH8.0-150mM氯化钠-1% Triton X-100-0.2mM原钒酸钠-蛋白酶抑制剂混合物4°C下最多可保存6个月。使用前立即添加蛋白酶抑制剂。其他试剂蛋白酶抑制剂细胞裂解后,蛋白水解、去磷酸化和变性过程就开始了。将样品放在冰上会减慢这些过程,但也可以使用蛋白酶和磷酸酶抑制剂混合物。如果不使用混合物,PMSF(50 μg/mL)和抑肽酶(1 μg/mL)是常用于免疫沉淀的蛋白酶抑制剂。其他试剂-无菌PBS pH 7.4-无菌PBS-BSA 1% w/v(过滤)-TBST缓冲液-用于蛋白质印迹的上样/样品缓冲液-VeriBlot用于免疫沉淀二抗,在蛋白质印迹过程中优先检测未还原、未变性 的一抗。-100mM EDTA库存溶液由1.86gEDTA溶解在40mL H2O中制成。添加NaOH 将pH调节至7.4。最后将总体积调整至50 mL。制备裂解物细胞培养物裂解物(非变性)1,将细胞培养皿置于冰上,并用冰冷的PBS清洗细胞。2,排干PBS,然后添加冰冷的裂解缓冲液(1mL每107个细胞/100mm2培养皿 /150cm2烧瓶;0.5 mL每5×106个细胞/60mm2培养皿或75cm2烧瓶)。3,使用冷塑料细胞刮刀将贴壁细胞从培养皿上刮下,然后将细胞悬浮液轻轻转 移至预冷的微量离心管中。4,在4°C下保持恒定搅拌30分钟。5,在4°C的微量离心机中离心。您可能需要根据细胞类型改变离心力和时间。原则是12,000 rpm,20分钟, 但您应该针对您的特定实验进行优化(例如,白细胞需要非常轻微的离心)。6,轻轻地从离心机中取出管子并置于冰上。吸出上清液并置于冰上的新管中, 并丢弃沉淀。 细胞培养物裂解物(变性)1,将100μL变性裂解缓冲液添加到0.5-2×107个细胞中。2,以最大速度剧烈涡旋2-3秒充分混合。将细胞悬液转移至微量离心管中。由 于DNA的释放,溶液在此阶段可能会变得粘稠。3,将样品加热至95°C,5分钟使其变性。4,用0.9 mL非变性裂解缓冲液稀释悬浮液,轻轻混合。非变性裂解缓冲液中过量1% Triton X-100会淬灭原始变性缓冲液中的SDS。5,将裂解的悬浮液通过连接到1 mL注射器的针头5-10次,从而打碎DNA。通过重复机械破坏,直到粘度降低。如果 DNA存在未完全消化和片段化, 可能会干扰离心后沉淀与上清液的分离。6,在冰上孵育5分钟。7,继续进行免疫沉淀。组织裂解物1,用干净的工具尽快解剖组织。如果可能,请在冰上进行以防止蛋白酶降解。2,将组织放入圆底微量离心管中,浸入液氮中快速冷冻。将样品储存在-80°C 下供以后使用或保存在冰上以便立即均质化。3,对于约5 mg的组织片,将约300 μL裂解缓冲液快速添加到管中,并用电动 匀浆器匀浆。4,每次冲洗时用另外300 μL裂解缓冲液冲洗刀片两次,然后在4°C下保持恒 定搅拌2小时(例如置于冰箱中的定轨摇床上)。裂解缓冲液的体积必须根据存在的组织量来确定。蛋白质提取物不应太稀,以避免蛋白质损失并尽量减少上样到凝胶上的样品体积。最低浓度0.1mg/mL;最佳浓度为1–5mg/mL。如果需要变性样品,使用变性裂解缓冲液并执行上述变性方案中的步骤2-5。5,在微量离心机中于4°C下以12,000 rpm离心20分钟。轻轻地将管从离心机 中取出并置于冰上,吸出上清液并置于冰上保存的新管中丢弃沉淀。预清除裂解物预清除裂解物有助于减少非特异性结合并降低背景。但如果蛋白质的最终检测是通过蛋白质印迹法进行,则不需要预清除,除非污染蛋白质干扰了目标蛋白质的可视化。1,将50 μL与免疫沉淀抗体相同种类和同种型的脱靶抗体或正常血清(通常首 选兔)添加到1 mL裂解液中。在冰上孵育1小时。2,将100 μL珠浆添加到裂解液中。3,在 4°C下孵育10–30分钟,并轻轻搅拌。4,在微量离心机中于4°C以14,000 g旋转10分钟。5,丢弃珠粒并保留上清液用于免疫沉淀。为了提高产量,可以在裂解缓冲液中将珠子洗涤1或2次以上,并将上清液 收集在一起。 重要的是要确保尽可能多地去除正常血清。为了确保这一点,可以使用裂解缓冲液代替样品进行测试,并执行上述所有预清除步骤。将所得上清液进行凝胶电泳并用考马斯染色显示血清Ig是否被有效去除。如果血清未充分去除,重链和轻链将出现50和25kDa的条带;它的存在可能会导致免疫沉淀反应较弱。考虑减少血清量或增加预澄清步骤中与样品一起孵育的珠子量。 参考文献1.Bonifacino, Juan S. et al. Current Protocols in Immunology 8.3.1 -8.3.28, New York: John Wiley, 2001.2.Harlow, Ed, and David Lane. Using Antibodies. Cold Spring Harbor, New York: Cold Spring Harbor Laboratory Press, 1999. 阿拉丁: https://www.aladdin-e.com/
应用实例
2024.04.07
【阿拉丁试剂】创新镍催化反应:探索硼酸(酯)与新型镍试剂的合成新路径
创新镍催化反应:探索硼酸(酯)与新型镍试剂的合成新路径 硼酸(酯)在分子合成中扮演着至关重要的角色,尤其是那些特殊的硼酸(酯),如杂环、烯丙基、饱和烃以及含有双官能团的底物,它们在合成化学中备受青睐。2019年,JACS杂志发表了Melanie S. Sanford教授的一篇重要文章,她为我们介绍了一种全新的方法,可以直接从酸合成硼酸(酯)。这一方法的具体合成步骤如下:JACS 2019 Oct 16. doi: 10.1021/jacs.9b08961 该方法的优势镍催化羧酸氟化物的脱羰硼化反应•无碱条件,对硼化高度选择性•通用,与各种硼酯和硼酰胺兼容•丰富的羧酸作为底物•反金属活性中间体作为空气稳定催化剂•机制研究提出了Ar-Ni-F配合物与有机硼和二硼试剂的反金属化反应的趋势 实验方法以下是脱羰硼酸反应的一般步骤:1. 在一个充满氮气的手套箱中,将羧酸(0.3 mmol,1当量)、TFFH(0.3 mmol,1当量)和双二甲氨基萘(0.3 mmol,1当量)精确称重到一个10 mL反应瓶中。2. 加入THF(0.5 mL)作为溶剂,室温下搅拌15~30分钟,使反应物充分混合。3. 加入催化剂B(0.03 mmol,0.1当量)和二硼试剂(0.6 mmol,2当量),继续搅拌。4. 将反应瓶密封后从手套箱中取出。5. 将反应混合物在115℃下加热搅拌16小时,使反应进行完全。6. 冷却至室温后,加入Et2O(10 mL)和饱和NaHCO3(10 mL),以分离有机层和水层。7. 收集有机层,用Et2O(2×10 mL)进一步萃取水溶液,以去除残留的水。8. 对提取的所有有机层进行干燥处理,用Na2SO4去除水分。9. 对干燥后的有机层进行真空浓缩,以减少体积。10. 最后,用正己烷和乙酸乙酯的混合流动相在硅胶上进行闪柱层析纯化,得到纯化的脱羰硼酸产物。 反应示例 可能适用该方法的分子砌块 参考文献1. Christian A. Malapit, James R. Bour, Simon R. Laursen, and Melanie S. Sanford, J. Am. Chem. Soc. 2019, 141, 43, 17322–17330. https://doi.org/10.1021/jacs.9b08961
应用实例
2024.04.03
【阿拉丁】量子点在电子和能源领域的应用
什么是量子点?量子点(QDs)是一种纳米级(约2-10纳米)的半导体材料。由于尺寸较小,量子点表现出量子约束效应以及与尺寸相关的电学和光学特性。自20世纪 80年代发现镉基QDs以来,人们已经合成并研究了多种镉基和非镉基QDs。通过调整QDs的形状和尺寸,QDs的电学和光学特性得到了显著改善,并已成为一类重要的材料,其应用范围从发光二极管(LED)扩展到光伏、光电探测器、激光器和场效应晶体管。本篇技术文章总结了一些新型非镉基QDs的特性以及QDs的不同应用。钙钛矿量子点 最近发现的通用分子式为 APbX3 [A = Cs、MA(甲胺)、FA(甲脒),X = Cl、Br、I]的钙钛矿量子点引起了人们极大的研究兴趣。这主要是因为它们具有很高的光致发光量子效率(PLQY,高达95%)和很窄的发射带宽(FWHM 图1展示了各种钙钛矿量子点在紫外光照射下的颜色。CsPbCl3 QD发出蓝光,随着Cl部分被Br取代,产生混合卤化物包晶CsPb(Cl/Br)3(图 2),发射波长转移到可见光谱的绿色区域。成分为CsPbBr3的QD会发出绿光,CsPb(Br/I)3的发射波长转向黄色,CsPbI3的发射波长则变为红色。在各种包晶型QDs中,CsPbX3(X = Cl、Br)组成的QDs最为稳定,其发射波长在450-510 nm之间,这些QDs具有更强的光学特性和化学稳定性,因此在光电应用中很有前景。这些低铅含量的无镉QDs可应用于LED、LCD背光和光电探测器。图1. 各种钙钛矿量子点在紫外线照射下的颜色。图2. 钙钛矿量子点CsPbX3(X- Cl和Br)的发射波长PbS量子点硫化铅量子点的发射波长可根据其尺寸(2.5-8纳米之间)在900-1600 纳米之间调整,这属于电磁波谱的红外(IR)波段。通常,硫化铅量子点具有较宽的吸收光谱范围和较窄的荧光带(图 3)。这些特性使PbS QDs适合用作太阳能电池、光电探测器和红外线LED中的光吸收器或红外线(IR)发射器。量子点具有宽吸收光谱(从近红外延伸到红外)、高峰谷比(大于4)、窄带发射(FWHM 图3. ~4 nm PbS量子点的吸收和发射波长量子点的应用发光二极管 (LEDs)量子点在LED器件的发光层中具有很好的应用前景。窄幅的发射宽度(由窄幅的半高宽(FWHM)定义)和发射波长的可调谐性使得量子点在尺寸和成分上的简单变化对LED具有吸引力。此外,通过卷对卷印刷制造具有量子点基LED的光电器件的可能性,以及大多数量子点与轻质、柔性塑料基板的兼容性,为制造低成本、大面积柔性器件开辟了新的应用前景。可见量子点LED(Visible quantum dot -based LED)具有色彩纯度高、亮度高、功耗低等优点,被认为是继OLED显示器之后的新一代显示技术。图4展示了基于量子点的LED器件的原理图。首先,在以玻璃或高分子材料为基片的氧化铟锡(ITO)上旋转涂覆空穴传输层(HTL),然后用旋涂法制备量子点。对于可见LED,使用钙钛矿、CdSe或InP基的量子点,PbS量子点可用于红外LED。沉积量子点之后是沉积电子传输层(ETL)和电极。电极通常用金属制备,如银、金或铝,并通过热蒸发系统沉积[1-6]。图4. 基于量子点的结构草图照明A)液晶显示(LCD)背光在传统的液晶显示器中,背光源使用的是LED发出的白色光源。然而,在新一代液晶显示器中,背光系统由蓝色发光二极管和量子点滤光片组成。滤光片包含绿色和红色量子点,可将部分蓝光转换成绿色和红色。由于红光、绿光和蓝光的FWHM很窄,因此色域很宽,从而使液晶显示器上的图像更明亮、对比度更高。此外,这种排列方式还能显著降低能耗。基于QD的滤光片可以设计成三种配置:“片上”、“边缘”和“表面”。在“片上”的配置中,绿色和红色量子点混合放置在LED封装内蓝色芯片的顶部;在“边缘”配置中,混合物被置于封装中靠近LED的玻璃导轨内;在“表面”配置中,聚合物薄膜中的混合量子点集成在蓝色 LED 和 LCD 矩阵之间(图 5)[7-11]。钙钛矿、基于CdSe和InP的量子点在可见的电磁光谱范围内发射,可在背光中有着广泛的应用。图5. 量子点液晶背光在“表面”配置的原理图B)荧光粉量子点可以作为荧光粉用于白色照明或园艺照明(图6)。在这些应用中,最高效、最便宜的蓝光LED被用作主光源,与液晶显示器类似,QD被用作荧光粉,可以将部分蓝光转换成另一种光。照明设备的可能配置有“片内”和“远程荧光粉”两种。在“片内”配置中,QDs混合物被置于LED封装内蓝色芯片的顶部,而在“远程荧光粉”配置中,QDs混合物被置于蓝色LED之后的聚合物薄膜中。在白光照明中,混合物由绿色和红色QDs组成。在白光照明中使用QDs的主要优点是可以获得较高的显色指数(CRI)和相关色温(CCT)。与自然光源相比,这些参数是衡量光源再现各种物体颜色能力的指标。红色量子点聚合物复合材料有望用于温室植物高效生长的园艺LED。植物叶绿素通常最有效地捕获红色(600-700纳米)和蓝色(400-500纳米)光波,绿色光波被反射。因此,具有蓝色LED和带有红色量子点的聚合物复合材料的设备可以向植物提供更多的光合有效辐射,而不会使它们过热。量子点的使用也能够有效降低能耗成本。图6. QD基础设备(a)白色照明和(b)园艺照明的卡通示意图太阳能电池PbS量子点在太阳能光伏应用中特别有趣。PbS是一种具有大玻尔激子半径的半导体材料,可以在广泛的太阳光谱范围内实现量子尺寸效应调节。此外,这种材料通过尺寸效应带隙可调谐性,为单材料的串联和多结太阳能电池提供了途径。图7展示了带有量子点的太阳能电池装置的示意图。PbS量子点可以有不同的带隙,通常,P型PbS量子点薄膜是通过自旋涂覆在ETL/ITO/玻璃基片层上逐层沉积的,然后沉积由银或金组成的HTL和上电极,典型的电极沉积是通过加热或电子束蒸发来实现的[12-16]。图7. 量子点太阳能电池结构示意图光电探测器量子点可用于探测红外和可见光的光电探测器。红外光探测器在夜视相机、大气光谱气体检测、生物医学成像、质量控制和产品检验等领域均有着广泛的应用。可见光光电探测器用于图像传感器,用于将入射光转换为电子信号。量子点还可以用于监控、机器视觉、工业检测、光谱和荧光生物医学成像,使用量子点的优点是易于与硅电子器件或柔性有机衬底集成。此外,量子点还可以通过喷墨打印、溶液铸造和低温蒸发等简单方法沉积在衬底的预制电极上。通过量子尺寸效应可调谐的光学吸收和发射光谱是量子点提供的另一个重要优点。图8描绘了基于量子点的光电探测器的原理图。典型的制备方法是通过蒸发将电极沉积在玻璃或陶瓷衬底上,然后将胶体量子点或聚合物中的量子点混合物自旋涂覆在衬底上,从而在电极之间形成固体量子点膜或量子点聚合物复合材料[17-18]。PbS量子点可用于红外光谱的光电探测器,而基于钙钛矿、CdSe和InP的量子点则更多的被用于紫外-可见光谱上。图8. 量子点光电探测器结构示意图生物医学成像量子点作为生物医学成像的发光探针有几个优点。这些特性包括高的光稳定性、宽的吸收光谱、大的消光系数和可调谐的发射波长。此外,已有研究表明,量子点的表面可以通过修饰使其附着羧基和胺等表面基团,从而与抗体、多糖和多肽等生物分子结合(图9)。生物偶联量子点已被用作DNA杂交、受体介导的内吞作用、寄生虫代谢监测、组织和细胞结构实时可视化以及诊断应用的探针[19-21]。图9. 表面功能化量子点的示意图:(a)羧基功能化(b)氨基功能化(c)抗体连接参考文献1. Gong X, Yang Z, Walters G, Comin R, Ning Z, Beauregard E, Adinolfi V, Voznyy O, Sargent EH. 2016. Highly efficient quantum dot near-infrared light-emitting diodes. Nature Photon. 10(4):253-257. https://doi.org/10.1038/nphoton.2016.112. Supran GJ, Song KW, Hwang GW, Correa RE, Scherer J, Dauler EA, Shirasaki Y, Bawendi MG, Bulović V. 2015. High-Performance Shortwave-Infrared Light-Emitting Devices Using Core-Shell (PbS-CdS) Colloidal Quantum Dots. Adv. Mater.. 27(8):1437-1442. https://doi.org/10.1002/adma.2014046363. Veldhuis SA, Boix PP, Yantara N, Li M, Sum TC, Mathews N, Mhaisalkar SG. 2016. Perovskite Materials for Light-Emitting Diodes and Lasers. Adv. Mater.. 28(32):6804-6834. https://doi.org/10.1002/adma.2016006694. Song J, Li J, Li X, Xu L, Dong Y, Zeng H. 2015. Quantum Dot Light-Emitting Diodes Based on Inorganic Perovskite Cesium Lead Halides (CsPbX3). Adv. Mater.. 27(44):7162-7167. https://doi.org/10.1002/adma.2015025675. Dai X, Zhang Z, Jin Y, Niu Y, Cao H, Liang X, Chen L, Wang J, Peng X. 2014. Solution-processed, high-performance light-emitting diodes based on quantum dots. Nature. 515(7525):96-99. https://doi.org/10.1038/nature138296. Chen O, Zhao J, Chauhan VP, Cui J, Wong C, Harris DK, Wei H, Han H, Fukumura D, Jain RK, et al. 2013. Compact high-quality CdSe-CdS core-shell nanocrystals with narrow emission linewidths and suppressed blinking. Nature Mater. 12(5):445-451. https://doi.org/10.1038/nmat35397. Protesescu L, Yakunin S, Bodnarchuk MI, Krieg F, Caputo R, Hendon CH, Yang RX, Walsh A, Kovalenko MV. 2015. Nanocrystals of Cesium Lead Halide Perovskites (CsPbX3, X = Cl, Br, and I): Novel Optoelectronic Materials Showing Bright Emission with Wide Color Gamut. Nano Lett.. 15(6):3692-3696. https://doi.org/10.1021/nl50487798. Li X, Wu Y, Zhang S, Cai B, Gu Y, Song J, Zeng H. 2016. CsPbX3Quantum Dots for Lighting and Displays: Room-Temperature Synthesis, Photoluminescence Superiorities, Underlying Origins and White Light-Emitting Diodes. Adv. Funct. Mater.. 26(15):2435-2445. https://doi.org/10.1002/adfm.2016001099. Kim T, Jun S, Cho K, Choi BL, Jang E. 2013. Bright and stable quantum dots and their applications in full-color displays. MRS Bull.. 38(9):712-720. https://doi.org/10.1557/mrs.2013.18410. Huang B, Xu R, Zhuo N, Zhang L, Wang H, Cui Y, Zhang J. 2016. “Giant” red and green core/shell quantum dots with high color purity and photostability. Superlattices and Microstructures. 91201-207. https://doi.org/10.1016/j.spmi.2016.01.01511. Supran GJ, Shirasaki Y, Song KW, Caruge J, Kazlas PT, Coe-Sullivan S, Andrew TL, Bawendi MG, Bulović V. 2013. QLEDs for displays and solid-state lighting. MRS Bull.. 38(9):703-711. https://doi.org/10.1557/mrs.2013.18112. Lan X, Voznyy O, Kiani A, García de Arquer FP, Abbas AS, Kim G, Liu M, Yang Z, Walters G, Xu J, et al. 2016. Passivation Using Molecular Halides Increases Quantum Dot Solar Cell Performance. Adv. Mater.. 28(2):299-304. https://doi.org/10.1002/adma.20150365713. Ning Z, Voznyy O, Pan J, Hoogland S, Adinolfi V, Xu J, Li M, Kirmani AR, Sun J, Minor J, et al. 2014. Air-stable n-type colloidal quantum dot solids. Nature Mater. 13(8):822-828. https://doi.org/10.1038/nmat400714. Chuang CM, Brown PR, Bulović V, Bawendi MG. 2014. Improved performance and stability in quantum dot solar cells through band alignment engineering. Nature Mater. 13(8):796-801. https://doi.org/10.1038/nmat398415. Pan J, El-Ballouli AO, Rollny L, Voznyy O, Burlakov VM, Goriely A, Sargent EH, Bakr OM. 2013. Automated Synthesis of Photovoltaic-Quality Colloidal Quantum Dots Using Separate Nucleation and Growth Stages. ACS Nano. 7(11):10158-10166. https://doi.org/10.1021/nn404397d16. Wang X, Koleilat GI, Tang J, Liu H, Kramer IJ, Debnath R, Brzozowski L, Barkhouse DAR, Levina L, Hoogland S, et al. 2011. Tandem colloidal quantum dot solar cells employing a graded recombination layer. Nature Photon. 5(8):480-484. https://doi.org/10.1038/nphoton.2011.12317. Konstantatos G, Sargent EH. 2013. Colloidal Quantum Dot Optoelectronics and Photovoltaics. https://doi.org/10.1017/cbo978113902275018. Konstantatos G, Sargent EH. 2010. Nanostructured materials for photon detection. Nature Nanotech. 5(6):391-400. https://doi.org/10.1038/nnano.2010.7819. Michalet X. 2005. Quantum Dots for Live Cells, in Vivo Imaging, and Diagnostics. Science. 307(5709):538-544. https://doi.org/10.1126/science.110427420. Jamieson T, Bakhshi R, Petrova D, Pocock R, Imani M, Seifalian AM. 2007. Biological applications of quantum dots. Biomaterials. 28(31):4717-4732. https://doi.org/10.1016/j.biomaterials.2007.07.01421. Yu WW, Chang E, Drezek R, Colvin VL. 2006. Water-soluble quantum dots for biomedical applications. Biochemical and Biophysical Research Communications. 348(3):781-786. https://doi.org/10.1016/j.bbrc.2006.07.160阿拉丁:https://www.aladdin-e.com
应用实例
2024.03.29
【阿拉丁】在有机发光半导体中实现高效率
在有机发光半导体中实现高效率前言50多年来,有机分子的电致发光效应一直都是一种众所周知的现象。1,2 然而,直到20世纪80年代末,它才有了实际应用的前景。有机发光在发光器件中的成功应用需要克服与有机材料的高电阻率相关的问题的器件结构,同时还需要实现从电极到有机物的良好平衡的电荷注入。Tang和van Slyke3用有机发光半导体(OLEDs)的薄膜异质结构概念解决了以上这两个问题。图1显示了由夹在电极之间的三个有机层组成的双异质结构OLED的示意图。与阴极和阳极相邻的有机层分别是电子传输层(ETL)和空穴传输层(HTL)。图1.由空穴传输层(HTL)、电子传输层(ETL)、发射层(EML)和电极组成的双异质结构OLED的示意图。在OLED操作期间,从相对电极注入的空穴和电子被传输到发射层(EML),在那里它们复合形成激子。500Å或更小的膜厚度将驱动电压降低到5-10 V水平,并且分离的空穴和电子导电层提供了有效的电荷注入和载流子复合。这导致激子的形成,并最终随着激子衰变到基态而发射。在引入基于薄膜异质结构的OLED后不久,经证明具有掺杂到适当的基质中的发射极分子的双组分发射层通过提高发射层中的电荷复合和激子约束水平来提高器件效率。这也消除了发射掺杂剂的自猝灭。4利用磷光提高OLEDs的效率OLED中的空穴和电子是奇电子物种,具有ms=±½的相等分布。因此,当空穴和电子复合形成激子时,会产生单重态和三重态激子的统计混合物。5,6这导致了25%的单重态激子和75%的三重态的激子群体,并对OLED效率产生了重大影响。20世纪90年代末之前为OLED开发的大多数发射掺杂剂都是从荧光态发射的,这些荧光态只利用形成的激子的单线态部分。7这将基于荧光的器件的内部量子效率限制在25%,对应于仅约5%的外部效率(正面)。在20世纪90年代末,一种新的发射掺杂剂家族被引入,显著提高了OLED的效率。这种效率提高的关键是认识到三重态激子分数比单线态更重要。三重态激子的有效捕获需要磷光掺杂剂,其将捕获单重态和三重态的激子。磷光掺杂剂的附加要求是其具有与OLED的RC时间常数相当的辐射寿命,该RC时间常数通常在微秒时间范围内。实现高磷光效率和微秒级辐射寿命的最佳方法是将重金属原子掺入掺杂剂中,其自旋轨道耦合将有效促进单线态和三线态之间的系统间交叉。用于此目的的最常用的金属是Ir,然而,也已经开始使用其他重金属制备有效的磷光掺杂剂,包括Pt、Ru、Re、Au和Os。 图2显示了一些基于Ir的有机金属掺杂剂的结构和CIE色度坐标。其中,已经用四种圈出的掺杂剂制备了OLED;它们的CIE坐标已分别用彩色箭头标记。自1999年在OLED中引入Ir基磷光体以来,8近200种不同的Ir配合物已被掺入OLED中,大多数的外部效率为8%或者更高。9几个小组报告称,在优化的设备中使用Ir基材料可以获得>20%的外部效率,对应于接近100%的内部效率。10-12图2.有机发光二极管的化学结构、CIE色度坐标和铱环金属化配合物的磷光光谱。有机金属磷光体的发射能量与有机配体的结构密切相关,这使得设计一系列覆盖大部分可见光谱的高效磷光发射器成为可能。13,14 配合物的金属中心也可以应用于微调其发射能量。过渡金属配合物的发射源于其最低能量的三重态激发态。光谱分析结果表明,这种状态主要集中在环金属化配体上,具有单线态金属支持和电荷转移(1MLCT)特性。辅助(“非发射”)配体的修饰影响金属轨道的能量,从而影响激发态中1MLCT特征的量。以1MLCT为中心的配体比例的变化直接影响混合激发态的能量。13因此,通过修饰(F2ppy)2Ir(L^X)配合物中的辅助配体(L^X=辅助配体),可以将配合物的发射能量从458 nm转移到512 nm。该系列的深蓝色配合物之一[(F2ppy)2Ir(pz2Bpz2)]已被用于制造外部效率>11%的OLED。15OLEDS在照明中的应用LED的一个重要的潜在应用是照明。对用作照明源的器件的要求与上述单色OLED的要求有些不同。以RGB显示器为目标的OLED必须给出以峰值波长为中心的具有相对窄的线形的电致发光光谱。另一方面,照明源旨在近似黑体太阳光谱,并且需要在整个可见光谱中具有大致相等强度的宽线形。因此,为了实现整个可见光谱的完全覆盖,用于照明目的的OLED通常采用多个发射器,这些发射器要么共同沉积到单个发射层中,要么分布到器件的不同层或区域中。已经报道了许多不同的器件结构来实现高效的白色电致发光。 大多数白光有机发光二极管(WOLEDs)利用来自几种不同颜色发射器的发光,使得组合输出均匀地覆盖可见光谱。虽然已经报道了具有少于三个不同发射器的WOLEDs,但WOLEDs中最常见的方法是使用三个,即蓝色、绿色和红色。最简单的器件架构之一包括将蓝色、绿色、红色掺杂剂混合到单个发射层中,使得三个发射光谱的总和覆盖可见光谱。16-18在三重掺杂的发射层中使用磷光发射器可以产生高效的器件。然而,在单层中使用三种掺杂剂还是存在问题的,因为能量容易从较高能量的蓝色掺杂剂转移到绿色掺杂剂以及从绿色掺杂剂转移至红色掺杂剂。因此,需要仔细调整每种掺杂剂的浓度,以实现良好平衡的发射颜色,掺杂水平为蓝色>绿色 >> 红色。为了获得良好平衡的白色发射,红色掺杂剂的掺杂水平通常需要远低于1%。 掺杂剂间能量转移问题的一种解决方案是将染料分离成不同的层。高效的WOLEDs已经使用这种堆叠概念与荧光或磷光发射极一起制备。18-21还描述了使用掺杂到单独层中的双组分荧光蓝色和橙色发射极的更简化的结构。19,22虽然将发射极堆叠在单独层中消除了这些能量转移问题,由于难以在每个发射层内实现平衡的载流子复合和激子局域化,器件结构可能变得明显更复杂。 平面铂基掺杂剂的使用使得可以制备仅具有单一掺杂剂的宽带发射(白色)OLED,这与上述使用两个或三个不同发射器的方法相反。图3显示了白色是如何通过将同一有机金属铂络合物的单体(蓝色)和聚集体(黄色到红色)的发射相结合来实现的,给出了覆盖整个可见波长范围的发射光谱。单体与聚集体发射的比例由掺杂浓度和掺杂剂的立体体积控制。23增加掺杂剂的空间体积会阻碍聚集体的形成,而增加掺杂剂浓度则有利于聚集体的产生。最大限度地减少掺杂剂的数量可显着降低器件的复杂性。最近的研究表明,基于单聚体宽带发射方法的设备可以用于实现15-20%的外部效率。24,25图3. F2 -ppyPt(acac)掺杂薄膜的光致发光光谱,显示光谱线形与掺杂水平的相关性。光谱由聚集体和单体发射成分组成。在5.6%的掺杂浓度下,膜中的F2-ppyPt(acac)单体与聚集体的比例平衡以产生白光。F2-ppyPt(acac)及其二聚体的化学结构如右图所示。 白光由大约25%的蓝色组成,平衡覆盖了绿色和红色之间的能量。OLED中空穴和电子复合形成的激子也以25%的单重态对75%的三重态的比例形成。白光的蓝色部分和单线态部分的相似性表明了实现高效白光发射的另一种方法:将单线态激子耦合到蓝色荧光掺杂剂,并将三重态耦合到覆盖光谱的绿色和红色部分的磷光体。这种组合荧光和磷光发射的实施方式已被证明具有许多优点。引入稳定的荧光蓝有望缓解WOLED的蓝色组件的操作寿命有限的众所周知的问题。磷光三组分WOLED的量子效率-电流密度图的形状通常显示在效率达到其最大值后不久在更高的电流密度下效率曲线的急剧下降。26在组合荧光/磷光器件中,由于三重态在发射层中间的浓度低于它们形成的ETL或HTL界面附近的浓度,因此在高电流下导致不必要的效率降低的三重态-三重态湮灭减少。 最近已经报道了基于磷光的WOLEDs的重大进展。Nakayama等人已经制备了一种WOLED,其中蓝色、绿色和红色磷光体用于产生广谱白色OLED。27他们的器件在1000 cd/m2的亮度下提供了64 lm/W的效率。这种效率超过了紧凑型荧光源,接近荧光管光源(约75–90 lm/W)。此外,该器件在该亮度下的器件寿命超过10000小时。这些数值比OLED之前的记录高出两倍多,清楚地表明OLED在照明方面有着光明的前景。 结论OLED有望在全彩显示器和照明应用中产生显著影响。这两类器件都需要高效率和长寿命,以及低成本的制造、宽范围的器件组和高色彩饱和度。OLED已经展示了所有这些特性;然而,大面积制造仍然是一个重大挑战,使得制造成本相当高。另一项技术挑战是深蓝色器件的器件寿命。有大量稳定的红色和绿色磷光发射器,使器件寿命接近106小时。相反,基于蓝色磷光体的OLED的操作稳定性通常明显更短,最佳值在15000和20000小时之间。这些蓝色设备的不稳定性增强的来源仍然是一个悬而未决的问题。尽管许多荧光和磷光OLED已经在小面积移动显示器中商业化,但仍有足够的科学研究空间来更好地理解控制和限制有机电致发光的参数。参考文献1. Pope M, Kallmann HP, Magnante P. 1963. Electroluminescence in Organic Crystals. The Journal of Chemical Physics. 38(8):2042-2043. https://doi.org/10.1063/1.17339292. Bernanose A, Comte M, Vouaux P. 1953. Sur un nouveau mode d'émission lumineuse chez certains composés organiques. J. Chim. Phys.. 5064-68. https://doi.org/10.1051/jcp/19535000643. Tang CW, VanSlyke SA. 1987. Organic electroluminescent diodes. Appl. Phys. Lett.. 51(12):913-915. https://doi.org/10.1063/1.987994. Tang CW, VanSlyke SA, Chen CH. 1989. Electroluminescence of doped organic thin films. Journal of Applied Physics. 65(9):3610-3616. https://doi.org/10.1063/1.3434095. Segal M, Baldo MA, Holmes RJ, Forrest SR, Soos ZG. Excitonic singlet-triplet ratios in molecular and polymeric organic materials. Phys. Rev. B. 68(7): https://doi.org/10.1103/physrevb.68.0752116. Baldo MA, O?Brien DF, Thompson ME, Forrest SR. Excitonic singlet-triplet ratio in a semiconducting organic thin film. Phys. Rev. B. 60(20):14422-14428. https://doi.org/10.1103/physrevb.60.144227. Shoustikov A, Yujian You, Thompson M. 1998. Electroluminescence color tuning by dye doping in organic light-emitting diodes. IEEE J. Select. Topics Quantum Electron.. 4(1):3-13. https://doi.org/10.1109/2944.6694548. Baldo MA, Lamansky S, Burrows PE, Thompson ME, Forrest SR. 1999. Very high-efficiency green organic light-emitting devices based on electrophosphorescence. Appl. Phys. Lett.. 75(1):4-6. https://doi.org/10.1063/1.1242589. Crabtree R, Mingos D. 2007. Comprehensive Organometallic Chemistry III. 12. Oxford, UK: Elsevier.10. Tsuboyama A, Iwawaki H, Furugori M, Mukaide T, Kamatani J, Igawa S, Moriyama T, Miura S, Takiguchi T, Okada S, et al. 2003. Homoleptic Cyclometalated Iridium Complexes with Highly Efficient Red Phosphorescence and Application to Organic Light-Emitting Diode. J. Am. Chem. Soc.. 125(42):12971-12979. https://doi.org/10.1021/ja034732d11. Soichi W, Yuya A, Daisaku T, Junji K. 2005. High-Efficiency Phosphorescent OLEDs using Chemically Doped Layers. J. Photopol. Sci. Technol.. 18(1):83-86. https://doi.org/10.2494/photopolymer.18.8312. Meerheim R, Walzer K, Pfeiffer M, Leo K. 2006. Ultrastable and efficient red organic light emitting diodes with doped transport layers. Appl. Phys. Lett.. 89(6):061111. https://doi.org/10.1063/1.226835413. Li J, Djurovich PI, Alleyne BD, Yousufuddin M, Ho NN, Thomas JC, Peters JC, Bau R, Thompson ME. 2005. Synthetic Control of Excited-State Properties in Cyclometalated Ir(III) Complexes Using Ancillary Ligands. Inorg. Chem.. 44(6):1713-1727. https://doi.org/10.1021/ic048599h14. Brooks J, Babayan Y, Lamansky S, Djurovich PI, Tsyba I, Bau R, Thompson ME. 2002. Synthesis and Characterization of Phosphorescent Cyclometalated Platinum Complexes. Inorg. Chem.. 41(12):3055-3066. https://doi.org/10.1021/ic025550815. Holmes RJ, D?Andrade BW, Forrest SR, Ren X, Li J, Thompson ME. 2003. Efficient, deep-blue organic electrophosphorescence by guest charge trapping. Appl. Phys. Lett.. 83(18):3818-3820. https://doi.org/10.1063/1.162463916. Kawamura Y, Yanagida S, Forrest SR. 2002. Energy transfer in polymer electrophosphorescent light emitting devices with single and multiple doped luminescent layers. Journal of Applied Physics. 92(1):87-93. https://doi.org/10.1063/1.147975117. Tasch S, List EJW, Ekström O, Graupner W, Leising G, Schlichting P, Rohr U, Geerts Y, Scherf U, Müllen K. 1997. Efficient white light-emitting diodes realized with new processable blends of conjugated polymers. Appl. Phys. Lett.. 71(20):2883-2885. https://doi.org/10.1063/1.12020518. Kido J, Shionoya H, Nagai K. 1995. Single?layer white light?emitting organic electroluminescent devices based on dye?dispersed poly(N?vinylcarbazole). Appl. Phys. Lett.. 67(16):2281-2283. https://doi.org/10.1063/1.11512619. Jiang X, Zhang Z, Zhao W, Zhu W, Zhang B, Xu S. 2000. White-emitting organic diode with a doped blocking layer between hole- and electron-transporting layers. J. Phys. D: Appl. Phys.. 33(5):473-476. https://doi.org/10.1088/0022-3727/33/5/30120. Ko CW, Tao YT. 2001. Bright white organic light-emitting diode. Appl. Phys. Lett.. 79(25):4234-4236. https://doi.org/10.1063/1.142545421. D’Andrade B, Thompson ME, Forrest S. 2002. Controlling Exciton Diffusion in Multilayer White Phosphorescent Organic Light Emitting Devices. Advanced Materials. 14147.22. Yang J, Jin Y, Heremans P, Hoefnagels R, Dieltiens P, Blockhuys F, Geise H, Van der Auweraer M, Borghs G. 2000. White light emission from a single layer organic light emitting diode fabricated by spincoating. Chemical Physics Letters. 325(1-3):251-256. https://doi.org/10.1016/s0009-2614(00)00619-923. Adamovich V, Brooks J, Tamayo A, Alexander AM, Djurovich PI, D'Andrade BW, Adachi C, Forrest SR, Thompson ME. 2002. High efficiency single dopant white electrophosphorescent light emitting diodesElectronic supplementary information (ESI) available: emission spectra as a function of doping concentration for 3 in CBP, as well as the absorption and emission spectra of Irppz, CBP and mCP. See http://www.rsc.org/suppdata/nj/b2/b204301g/. New J. Chem.. 26(9):1171-1178. https://doi.org/10.1039/b204301g24. Cocchi M, Kalinowski J, Virgili D, Fattori V, Develay S, Williams JAG. 2007. Single-dopant organic white electrophosphorescent diodes with very high efficiency and its reduced current density roll-off. Appl. Phys. Lett.. 90(16):163508. https://doi.org/10.1063/1.272267525. Williams E, Haavisto K, Li J, Jabbour G. 2007. Excimer-Based White Phosphorescent Organic Light-Emitting Diodes with Nearly 100?% Internal Quantum Efficiency. Adv. Mater.. 19(2):197-202. https://doi.org/10.1002/adma.20060217426. Sun Y, Giebink NC, Kanno H, Ma B, Thompson ME, Forrest SR. 2006. Management of singlet and triplet excitons for efficient white organic light-emitting devices. Nature. 440(7086):908-912. https://doi.org/10.1038/nature0464527. Nakayama T, Hiyama K, Furukawa K, Ohtani H. 2007. 19.1:Invited Paper: Development of Phosphorescent White OLED with Extremely High Power Efficiency and Long Lifetime. 38(1):1018-1021. https://doi.org/10.1889/1.2785478阿拉丁:https://www.aladdin-e.com
应用实例
2024.03.29
【阿拉丁】与源叶:共同开启新篇章
我们很高兴地宣布阿拉丁和源叶旅程中的一个重要里程碑——双方的合作旨在创新、激励和引领生命科学领域。阿拉丁拟收购源叶51%的股份,此举标志着我们公司、团队和尊贵客户合作与变革之旅的开始。 战略联盟 此次拟收购不仅仅是一次商业交易,它也是两家愿景一致、优势互补公司的战略联盟。阿拉丁以其在化学、材料科学和生命科学领域的开创性工作而闻名,与生化试剂的开拓者源叶强强联手,源叶非常注重创新和质量。我们的目标是共同创建一个处于科学研究和产品开发前沿的平台。 为什么是源叶? 源叶已成为生化试剂卓越的提供商。他们致力于推进科学研究,加上他们的创新产品,使他们成为阿拉丁的理想合作伙伴。这种合作关系使我们能够扩大我们的产品组合,增强我们的研发能力,并巩固我们在全国乃至国际市场的地位。 这对我们的客户和利益相关者意味着什么? 1、增强产品供应:客户可以期待更广泛的高质量产品和服务,以满足科学界不断变化的需求。2、创新解决方案:通过研发的共同努力,我们将加速创新,向市场推出新的解决方案,以促进科学发现和研究效率。3、扩大全球影响力:我们的合并网络将使我们能够更有效地为客户提供服务,确保我们的产品和服务在全球范围内可用。4、追求卓越:阿拉丁和源叶都致力于在我们所做的一切中保持最高的质量标准和卓越性。当我们共同前进时,这一点将保持不变。 展望未来 当我们开启这一激动人心的新篇章时,我们对未来充满乐观。这种伙伴关系开启了一个充满创新、增长和成功可能性的世界。我们致力于无缝整合我们的运营和团队,确保阿拉丁和源叶的价值观、文化和使命得到保留和加强。 我们衷心感谢我们的员工、客户和利益相关者对我们的持续支持和信任。您对我们使命的信念激发了我们在生命科学领域树立新标杆的决心。我们将共同致力于科学、创新和可持续发展,继续为世界带来改变。 随着我们在这一充满希望的旅程中前进,请继续关注更新。这是一个充满突破、成长和协作的未来。欢迎来到阿拉丁和源叶的新时代,我们共同创新,共创美好明天!
企业动态
2024.03.21
1.81亿元!阿拉丁拟收购源叶生物51%股权
18日晚间,阿拉丁(688179.SH)对外宣布,拟使用银行贷款和自筹资金合计1.81亿元收购“上海源叶生物科技有限公司”(下称“源叶生物”)51%股权,收购完成后,源叶生物将成为阿拉丁合并报表范围内的控股子公司。 值得注意的是,此番交易,源叶生物100%的股权交易价格为3.55亿元,相对于其2023年的净资产增值413.68%。截至2023年9月底,阿拉丁拥有账面货币资金4.89亿元,阿拉丁表示总体资金较充裕。 不过,针对此次交易,阿拉丁也与源叶生物的原股东崔媛媛和谭小勇约定了业绩承诺和业绩补偿条款。崔、谭二人作为乙方承诺,源叶生物2024-2026年间的扣非“经审计净利润”不低于3300万元、4000万元和4700万元,如累计实际净利润低于承诺数的90%,乙方需向阿拉丁进行业绩补偿。 有媒体分析,阿拉丁之所以愿意高溢价收购源叶生物,既是看中了后者业务上的优势及成长潜力,更是出于提振自身经营业绩的迫切需求。 据披露,源叶生物主要从事科研试剂的研发、生产及销售,在生化试剂、标准品、小分子抑制剂、液体试剂等相关产品方面优势明显,“源叶”试剂品牌不仅在行业内具有一定知名度,且业务遍布全国,客户涵盖各地大专院校科研院所和制药、食品卫生、电子、石化、生物工程等工业领域。 近年来,源叶生物业绩亮眼,2023年实现营收1.05亿元,净利润3682.13万元,2024年1月营收1036.79万元,净利润392.44万元。 相比之下,近年来阿拉丁经营业绩承压明显。 2022年,阿拉丁实现营收3.78亿元,同比增长31.44%,归母净利润9233.15万元,同比微增3.32%,增速较2021年下滑近17个百分点。2023年,阿拉丁实现营收4.03亿元,同比微增6.60%,归母净利润8328.19万元,同比下降9.80%。 阿拉丁经营上的承压,还体现在其核心业务毛利率的下降,以及公司营运能力的下滑。 资料显示,阿拉丁是一家集研发、生产及销售为一体的科研试剂制造商,产品应用于高等院校、科研院所以及生物医药、新材料、新能源、节能环保、航空航天等高新技术产业和战略性新兴产业相关企业的研发机构。 目前,囊括了高端化学、生命科学、分析色谱、材料科学等领域在内的“科研试剂业务”是阿拉丁的核心业务,占比超过95%。 但星矿数据显示,2020-2022年间,阿拉丁科研试剂的毛利率为62.35%、63.04%、58.99%,整体上不升反降。与此同时,阿拉丁的营业周期从2021年的493.86天增加至2022年的673.17天,对应的存货周转天数由467.47天增加至639.89天。 经营的承压,甚至还影响到阿拉丁募投项目的进展。本月初,阿拉丁表示,考虑复杂的内外部宏观环境,结合所处的行业发展状况和未来的发展规划,募投项目投入进度不及预期。 因此,包括“阿拉丁高纯度科研试剂研发中心建设及其配套项目”“高纯度科研试剂生产基地项目”“张江生物试剂研发实验室项目”在内的3个项目,预定可使用状态均从2024年3月延期一年至2025年3月。 而收购源叶生物,对阿拉丁的业绩或将起到立竿见影的“润色”作用。以2023年的财务数据估算,阿拉丁合并源叶生物后的营收及利润水平将分别增长25.93%、44.21%。 不过,从更长远的角度来看,阿拉丁也表示,公司的试剂产品中高端化学试剂占比较高,与源叶生物的产品线有一定的差异性,通过此次并购可以丰富公司生化试剂产品线,补足了公司在这方面的短板,与源叶生物形成良好的协同关系。
媒体关注
2024.03.20
【阿拉丁】买试剂赠耗材,全面装备你的实验室!
其中:X为单笔订单金额 活动时间:2024年3月18日-2023年3月31日活动规则:1、用户在活动期间通过官网(www.aladdin-e.com)下单,当499元≤单笔订单金额2、用户在活动期间通过官网下单,当999元≤单笔订单金额3、用户在活动期间通过官网下单,当1,699元≤单笔订单金额4、用户在活动期间通过官网下单,当2,699元≤单笔订单金额5、用户在活动期间通过官网下单,当4,099元≤单笔订单金额6、用户在活动期间通过官网下单,当8,999元≤单笔订单金额7、用户在活动期间通过官网下单,当单笔订单金额≥16,999 元时,可享阿拉丁高端好礼三选一:索爱(soaiy) SH16 蓝牙音箱或者阿拉丁定制logo黑色商务双肩背包亦或是蓝牙人体工程学鼠标,根据您的喜好自由选择(礼品限量,先到先得)。 注:1、赠品领取方式:活动满额赠品(耗材或者礼品)将在活动期间/结束后,单独进行发放(不随下单订单一同发货,同时,阿拉丁默认用户下单收货地址为礼品派发地址)。2、本活动仅针对官网下单的积分用户,未在官网下单的及非积分用户不在本次活动范围内。3、阿拉丁官网全部试剂及耗材将参与本次活动,积分礼品及检测服务不在本次活动范围内。4、本次活动礼品限量赠送且颜色随机,按照下单时间进行审核,审核通过后先到先得,送完即止。5、若符合活动规则的订单在指定耗材/礼品派送完后,阿拉丁有权决定用活动其他同等价值的耗材/礼品代替,但将尽量提前通知用户(客服联系)。6、用户承诺并保证其完全有权将个人及单位信息提供给阿拉丁保存记录,用户应保证其所填信息的真实性、完整性和合法性,并且保证不会侵犯任何的合法权利。如因用户违反本承诺,将赔偿阿拉丁由此产生的全部损失。7、礼品/耗材发放前阿拉丁需要核实用户有无超账期欠款,结清超期欠款后才可发放礼品。8、上海阿拉丁生化科技股份有限公司享有对本活动的最终解释权。
企业动态
2024.03.20
【限时免费!】领取阿拉丁生物产品试用装,超值体验蛋白和抗体!
阿拉丁一直致力于提供最优质的生物产品,包括蛋白和抗体。我们的产品严格遵循科学标准,并经过严密的质量控制,以确保您获得准确、可靠的实验结果。 现在,阿拉丁为了推广我们优质的生物产品线,隆重推出了【生物产品试用装免费领取】的全新活动!通过参与此活动,您将有机会亲身体验我们的生物产品,并亲眼见证其优质和高效。 试用装将提供给您完整的产品体验,让您深入了解产品的质量和性能。我们相信,只有亲身体验过的用户才能真正感受到阿拉丁产品的卓越之处。为了满足您多元化的选择需求,我们精心准备了多种不同类型的生物产品供您申请试用。无论您对蛋白质还是抗体感兴趣,我们都会确保为您提供最适合您需求的产品。在接下来的1年内,您有机会免费申请试用我司一次生物产品的试用装,且先到先得,现货送完即止(请参考官网一级目录:部分药靶配体/蛋白质/抗体)。 1、首先,您需要登录您的企业或个人账号。如果您还没有账号,可以通过我们的官方网站进行注册。2、登录后,浏览我们的生物产品(蛋白质和抗体目录),找到您所感兴趣的产品。在产品详情页上,您会看到一个特殊标识,上面写着“试用装”。请点击该标识下方的金色字体,以申请试用装(详见下图)。3、点击后,系统将自动跳转至申请页面。在此页面上,您需要填写一些详细的信息,以便我们能更好地了解您的需求和情况。请您认真填写,并确保提供准确无误的联系方式。4、提交申请后,我们的专业客服团队将对您的申请进行审核。一旦您的申请通过审核,我们将向您发放优惠券(优惠券使用有效期:1周),用于金额抵扣。有了这个优惠券,您将能够在购买时享受该指定产品的免费试用装!5、请您耐心等待审核结果,我们会及时通知您审核是否通过并发送优惠券到您的账户。6、如果您有任何疑问或需要帮助,请联系我们的客户服务团队。我们将竭诚为您提供支持和解答您的问题。 Q1:申请的免费试用装产品有数量限制吗?A1:每个客户有且仅有一次免费申请机会,且每次申请只可获得一种试用装产品,超过限制的需自行进行购买。 Q2:需要为试用装产品支付任何费用吗?A2:使用阿拉丁提供的折扣券即可免费获得该产品,但需自行承担该笔订单所产生的固定运费20元;同时,如果订单中包含其他产品,同样也需承担其他产品的送货费用。 Q3:什么条件的产品可以申请免费生物试用装产品?A3:当阿拉丁官网正装产品显示为现货时即可申请符合该活动产品的试用装。 本次【生物产品试用装免费领取】活动是我们阿拉丁回馈长期支持客户的一份心意,同时,也为更多客户提供了方便、高品质的生物产品体验机会。我们始终坚信,客户的满意和信任是我们不断追求卓越的原动力。现在就点击产品链接报名参加活动,轻松领取您感兴趣的生物试用装,让您尽情享受顶级生物科技的魅力吧! 阿拉丁期待为您提供卓越的生物产品和无与伦比的服务体验。让我们携手共创科研未来,开启科学奇迹! 备注:活动最终解释权归上海阿拉丁生化科技股份有限公司所有。
企业动态
2024.02.02
抗体的结构和亚型----阿拉丁试剂
抗体结构抗体也称为免疫球蛋白(Ig),是B细胞产生的大型Y型糖蛋白,作为主要免疫防御。抗体特异性结合称为抗原的独特病原体分子。抗体以有四条多肽组成的Y型单元的一个或多个拷贝存在(图1)。每个Y单元包含两个相同的重链(H)和两个相同的轻链(L);重链和轻链的序列和长度不同。Y型的顶部包含可变区(V),也称为片段抗原结合(F(ab))区。该区域与抗原的特定部分(称为表位)紧密结合。抗体碱基由恒定结构域(C)组成,并形成Fc片段(Fragment Crystallization Region)。该区域对于免疫反应期间抗体的功能至关重要。图1:抗体结构。Y型抗体通过柔性铰链区链接在中间。抗原结合发生在可变域(V),由免疫球蛋白重链(H)和轻链(L)组成。抗体的碱基包括恒定结构域(C)。VH为重链可变结构域,VL为轻链可变结构域,CH为重联恒定结构域,CL为轻链恒定结构域。F(ab)和Fc片段Y型的抗体可以被胃蛋白酶切割成三个片段:两个F(ab)区和一个Fc区。F(ab)区包含与同源(特异性)抗原结合的可变结构域。Fc片段为淋巴细胞和二抗表面上的内源性Fc受体提供结合位点。此外,染料和酶可以与抗体的Fc部分共价连接,以实现实验可视化。重链重链的类型定义了抗体的总体类别或亚型。哺乳动物Ig重链有五种类型,用希腊字母表示:α、δ、ε、γ和μ。这些链分别存在于IgA、IgD、IgE、IgG和IgM抗体中。重链的大小和成分不同,α和γ含有大约450个氨基酸,而μ和ε含有大约550个氨基酸。每条重链都有两个区域:恒定区(CH)和可变区(VH)。恒定区在所有相同同种型抗体中是相同的,但在不同同种型抗体中是不同的。重链γ、α和δ具有由三个串联Ig结构域(CH1,CH2,CH3)组成的恒定区和用于增加灵活性的铰链区。重链μ和ε具有由四个免疫球蛋白结构域组成的恒定区。重链的可变区(VH)根据产生它的B细胞而有所不同,但对于单个B细胞或B细胞克隆产生的所有抗体来说是相同的。每条重链的可变区长约110个氨基酸,由单个Ig结构域组成。轻链哺乳动物只有两种类型的轻链,即lambda(λ)和kappa(κ),它们的多肽序列差异很小。轻链具有两个连续的结构域:恒定结构域(CL)和可变结构域(VL)。轻链的大约长度为211-217个氨基酸。每个抗体都包含两条始终相同的轻链。其他类型的轻链,例如iota(ι)链,存在于软骨鱼和硬骨动物等低等脊椎动物中。抗体亚型在哺乳动物中,抗体分为物种亚型IgA、IgD、IgE、IgG和IgM。每种亚型都有独特的结构,如图2所示。亚型根据数量和重链类型而变化。它们的生物学特性,功能位置和处理不同抗原的能力也有所不同(表1)。图2:抗体结构和亚型。表1:不同抗体同种型的结构和功能。抗原-抗体相互作用:抗体如何以及在何处结合F(ab)抗体区域包含称为互补位的抗原结合位点。互补位与抗原的特定部分(称为表位)结合,表位是抗原的一小部分,有时只有几个氨基酸长(图3)。 互补位和表位通过互补的形状和分子间相互作用(例如范德华力、氢键、静电和疏水相互作用)结合在一起;这些力的强度决定了抗体的亲和力。图3:抗原-抗体相互作用的示意图。参考文献1. Alberts B, Johnson A, Lewis J, et al. Molecular Biology of the Cell. 4th edition. New York: Garland Science; 2002. Chapter 24, The Adaptive Immune System. https://www.ncbi.nlm.nih.gov/books/NBK26830/2. Murphy K, Weaver C. Janeway's Immunobiology. 9th edition. New York: Garland Science; 2016. Chapter 5, Antibodies and Antigens. https://www.ncbi.nlm.nih.gov/books/NBK27125/Janeway CA, Travers P, Walport M, et al. Immunobiology: The Immune System in Health and Disease. 5th edition. New York: Garland Science; 2001. Chapter 5, Antibodies and Antigens. https://www.ncbi.nlm.nih.gov/books/NBK27101/阿拉丁提供相关产品,详情请见阿拉丁官网:https://www.aladdin-e.com
应用实例
2024.01.16
饮料中添加剂含量的测定----阿拉丁试剂
简介饮料,如常见的苏打水和能量饮料,可能含有许多极性成分,很容易溶解在饮料的水溶液基质中。这些成分包括甜味剂(糖或代糖)、咖啡因、维生素补充剂、氨基酸、有机酸和植物提取物。因为需要被分析的样品已经处于溶液状态,所以不需要额外的样品制备过程,而是将溶液稀释后直接注入到高效液相色谱(HPLC)中即可。在本篇技术文章中,我们介绍了两种饮料用快速高效液相色谱柱的应用。这类色谱柱适用于各类HPLC系统,其中的一个优势是它们能够达到UHPLC系统上使用亚2微米柱相关的分辨率、效率和速度,而不会产生高背压。本篇技术文章选择的为化学柱(RP-酰胺和HILIC),因为它们与C18相比具有更强的极性化合物特征。 无糖汽水的分析人工甜味剂通常以特定的组合在饮料中使用,以模拟天然糖的甜度。它们所含的能量比糖少,添加它们是为了保持口感而不额外增加热量。除了甜味剂,苏打水还可能含有防腐剂,添加防腐剂是为了抑制微生物生长,以延长饮料的保质期。因为人造甜味剂和防腐剂都被认为是添加剂,所以它们经常受到管制;因此,必须确定它们的性质和添加浓度。图1展示了三种人工甜味剂(安赛蜜、阿斯巴甜和纽甜)、两种防腐剂(苯甲酸和山梨酸)咖啡因的高效液相色谱分离。在这个例子中,使用快速RP-酰胺柱。酰胺柱中的酰胺官能团提供了不同于烷基纯相(如C18)的选择性。极性化合物的选择性差异最明显,如本应用中的化合物。在快速RP-酰胺柱上,所有主要成分的分离能够在1分钟内实现,使用的是可接受背压(3200 psi/220 bar)的传统HPLC系统。图1. 用高效液相色谱分析无糖汽水中的人工甜味剂,防腐剂和咖啡因 HPLC条件色谱柱: 快速RP-酰胺柱,3 cm x 4.6 mm I.D., 2.7 µm粒径;流动相:(A)100 mM 醋酸铵溶液,pH = 5.6,用乙酸滴定标定浓度;(B)水;(C) 乙腈;梯度:20%恒速的A,1分钟内C由5到60% C,并保持60% C持续0.1分钟;流速:3 mL/分钟;柱温:40 °C;检测器:214 nm处UV;注射容量:1 µL;样品:缓冲溶液中的无糖汽水,浓度为100-500 µg/mL。 咖啡因能量饮料分析能量饮料含有多种可营销的组分,如糖、维生素和咖啡因,和苏打水一样,它们通常也含有防腐剂,在快速 HILIC色谱柱上分析能量饮料的色谱图如图2所示。选择HILIC色谱法是因为它适用于保留和分离基于极性差异的亲水化合物,无论这些分析物是酸性、碱性、带电的还是中性的。采用紫外分光光度法和ELSD法能够检测不同类型的化合物;ELSD可以检测不吸收紫外线的糖。分析使用的是MS友好型流动相,分析速度快(2分钟以内),背压低(815 psi)。由于这些优势的存在,HILIC色谱柱可以被用分析饮料成分。图2. 用HPLC分析能量饮料中的糖、维生素、防腐剂和咖啡因 HPLC条件色谱柱: 快速HILIC柱,10 cm x 3.0 mm I.D., 2.7 µm粒径;流动相:(A)100 mM 醋酸铵溶液,pH = 5.0;(B)水;(C) 乙腈;(A: B: C = 9:1:90);流速:0.6 mL/分钟;柱压:815 psi;柱温:35 °C;检测器:254 nm处UV或ELSD,55 °C,3.5 bar氮气;注射容量:2 µL;样品:用乙腈1:9稀释的商品化功能饮料。 结论 这些简单的例子展示了两个快速色谱柱在饮料分析中的应用,这类色谱柱都适用于极性化合物的分析,能够成功地用于分析几种饮料成分,包括糖类、维生素、甜味剂、防腐剂和咖啡因。快速柱提供了传统高效液相色谱系统的快速分离方法,而与亚2微米柱相关的背压没有显著增加。两柱之间的选择性差异可以进一步用于改变洗脱顺序和化合物保留时间。阿拉丁提供相关产品,详情请见阿拉丁官网:https://www.aladdin-e.com
应用实例
2024.01.15
Cannizzaro反应---阿拉丁试剂
Cannizzaro反应 Cannizzaro反应简介Cannizzaro反应,译作坎尼扎罗反应、康尼查罗反应、康尼扎罗反应,是无α-活泼氢的醛在强碱作用下发生分子间氧化还原反应,生成一分子羧酸和一分子醇的有机歧化反应。[1,2] 意大利化学家斯坦尼斯劳·坎尼扎罗在使用用草木灰处理苯甲醛时,同时得到了苯甲酸和苯甲醇,首次发现了这个反应,该反应名称也因此而来。[3]图1. Cannizzaro反应Cannizzaro反应中适用的醛一般为芳香醛(如苯甲醛)和甲醛。如果醛中含有α -活泼氢,碱则会夺取其α -活泼氢,进而发生羟醛缩合反应,导致Cannizzaro反应的收率降低。[4]分子内也可以发生Cannizzaro反应,有些情况下产物羟基酸还会进一步失水环化生成内酯。Cannizzaro反应机理图2. Cannizzaro反应机理反应起始于亲核试剂(如氢氧根离子)对羰基碳的攻击,引发歧化反应并去质子化产生携带两个负电荷的二价阴离子。生成的中间体现在可以起到氢化物还原剂的作用。由于其不稳定的性质,中间体会释放出一种氢化物阴离子。这个氢化物阴离子继续攻击另一个醛分子。在此过程中,二价阴离子转化为羧酸根阴离子,醛转化为醇盐阴离子。在最后一步中,水向醇盐阴离子提供质子,从而产生最终的醇产物。由于醇盐比水碱性更强,反应可以进行。当使用酸后处理时,羧酸根离子产生最终的羧酸产物(需要酸后处理,因为羧酸根的碱性比水弱,因此不能从水中获得质子)。交叉Cannizzaro反应交叉Cannizzaro反应是Cannizzaro反应的一种类型:混合不同的两种不含α -活泼氢的醛作为底物,在碱性条件下使其发生交叉氧化还原反应,则该反应为交叉Cannizzaro反应。[4] 该反应常会产生多种产物,没有制备价值。但可以牺牲醛与更有价值的化学物质结合,如果其中一个醛为甲醛,则其总是自身被氧化为甲酸(因为甲醛还原性最强),而醇是从另一种醛化学物质的还原中获得的,这样的反应有制备价值。由于两种不同的醛可以完全转化为各自所需的产物,因此具有价值的目标产物的产量也大大增加。例如,工业制备季戊四醇就是采取的该方法。图3. 工业制备季戊四醇总而言之,Cannizzaro反应可以用来控制不可烯醇化的醛的歧化。而交叉Cannizzaro反应可以用于提高高附加值化学品的产量。Cannizzaro反应研究进展溴化锂作为一种温和且可回收的试剂,可与三乙胺共同作用于室温无溶剂的Cannizzaro反应。[5]在TOX配体与Cu(II)催化下,芳基和烷基乙二醛与醇的不对称分子内Cannizzaro反应表现出了前所未有的高对映选择性。初步结果表明,除了半缩醛中间体的动态动力学拆分外,醇与乙二醛的对映选择性加成对立体选择性贡献最大。[6]以一系列简单的2-酰基苯甲醛作为反应底物,海洋天然产物pestalone衍生物中2-甲酰基芳烯酮可在亲核催化(NaCN)下的Cannizaro反应中,或在光化学条件下(DMSO,350 nm)便捷的转化(异构化)为3-取代的邻苯二甲酸酯。[7]参考文献1. Cannizzaro, S. Ueber den der Benzoësäure entsprechenden Alkohol. Liebigs Annalen. 1853, 88: 129–130. https://doi.org/10.1002/jlac.185308801142. 2. List, K.; Limpricht, H. Ueber das sogenannte Benzoëoxyd und einige andere gepaarte Verbindungen. Liebigs Annalen. 1854, 90: 190–210. https://doi.org/10.1002/jlac.185409002113. Geissman, T. A. "The Cannizzaro Reaction" Org. React. 1944, 2, 94. https://doi.org/10.1002/04712641804. Kürti, L., Czakó, B. (2005). Strategic Applications of Named Reactions in Organic Synthesis; Background and Detailed Mechanisms. Burlington, MA: Elsevier Academic Press.5. Mohammad M. Mojtahedi,Elahe Akbarzadeh,Roholah Sharifi and,M. Saeed Abaee. Lithium Bromide as a Flexible, Mild, and Recyclable Reagent for Solvent-Free Cannizzaro, Tishchenko, and Meerwein−Ponndorf−Verley Reactions[J]. Org. Lett.,2007,9(15). https://doi.org/10.1021/ol070894t6. Wang Pan,Tao Wen-Jie,Sun Xiu-Li,Liao Saihu,Tang Yong. A highly efficient and enantioselective intramolecular Cannizzaro reaction under TOX/Cu(II) catalysis.[J]. Journal of the American Chemical Society,2013,135(45). https://doi.org/10.1021/ja409859xGerbino Dario C,Augner Daniel,Slavov Nikolay,Schmalz Hans-Günther. Nucleophile- or light-induced synthesis of 3-substituted phthalides from 2-formylarylketones.[J]. Organic letters,2012,14(9). https://doi.org/10.1021/ol300757m阿拉丁提供相关产品,详情请见阿拉丁官网:Cannizzaro Reaction (aladdin-e.com)
应用实例
2023.11.29
论文有奖征集,来【阿拉丁】领取您的100元优惠券!
阿拉丁论文奖励活动是一个旨在鼓励学术交流和知识分享的活动。通过这个活动,我们希望能够给参与者提供一些实实在在的福利,并为你们的文章提供更多的曝光机会。参与者将有机会获得总金额为¥100的优惠券,包括四张¥25的优惠券,每张优惠券有效期为一年,可以用于购买阿拉丁平台的任何产品或兑换积分商城的礼品。此外,参与者们的文章也有可能被展示在阿拉丁平台上,面向我们的全球社区。注:本次活动仅适用于已发表的文章。 I. 参与条件 A. 文章发表的要求和限制: a) 只要文章中使用了 Aladdin的产品且文章已正式发布,您就可以提交任意数量的文章。 b) 我们对研究领域或文章类型没有任何限制。 B. 参与者资格的界定: a) 每位参与者每篇文章只能获得总计¥100的奖励一次。 b) 如果一篇文章的多位作者申请该活动奖励,奖励将授予首次有效提交的人。 II. 奖励细则 A. ¥100优惠券的使用方式和有效期: a) 本次活动的¥100优惠券不会一次性获得一张,而是获得四张独立的¥25优惠券。 b) 每张¥25优惠券的有效期为一年,每张优惠券上都会清楚地标明具体的过期日期。 c) 每张¥25优惠券可以给别人使用,允许在合作者或同事之间灵活分配。 B. 文章在阿拉丁平台上的展示机会: a) 我们确保您所提供的文章如果符合我们的展示规则将在我们的平台上得到充分的曝光和推广,让更多的读者能够品味到其中的精华和魅力。 b) 无论是在国内还是国际上,我们都将积极地推广您已发表的作品,让更多的人了解您的才华和见解。 c) 我们将继续努力提供最好的服务和最佳的展示机会,帮助您的文章获得更大的关注度和认可度。 III. 注意事项 A. 活动仅适用于已发表的文章: a) 成功提交您的文章信息后,您将收到一条确认消息,内容为:“感谢您的提交!验证后,我们将把您的四张¥25优惠券发送到提供的电子邮件地址。” b) 一旦我们验证通过了您提交的文章信息,您将在5个工作日内收到四张¥25的优惠券。 B. 隐私声明: a) 所有参与者提供的信息仅用于此次活动,并将严格保密。 b) 任何参与者提供的数据都将仅用于此次活动没,并且不会与第三方实体共享。 点击进入论文奖励活动申请页面(用户登录)
企业动态
2023.11.17
流式抗体新时代:阿拉丁多款靶标抗体震撼上市!
流式抗体的重要性流式抗体是流式细胞术中的关键组成部分,在科研中扮演着重要角色。它们可用于分析细胞表面标记物,帮助科研人员识别不同类型的细胞,分离和纯化细胞群,诊断疾病,以及在免疫学和药物研发中发挥作用。流式抗体为科研人员提供了强大的工具和技术支持,对细胞生物学、免疫学和临床诊断等领域具有重要意义。 阿拉丁流式抗体涵盖多种热销靶标阿拉丁致力于持续推出各种新型靶标流式抗体。高质量阿拉丁生产的流式抗体经过严格的质量控制,具有高特异性、高灵敏性和高再现性的特点,能够帮助您得到可靠的实验结果。采用重组抗体CD20抗体(FITC)进行流式实验结果(黑色代表未标记样品,绿色代表细胞被重组蛋白CD20抗体(FITC)染色)专业支持阿拉丁公司拥有专业的科研团队,能够为客户提供流式抗体选择方面的专业建议和支持。 阿拉丁相关产品 了解更多产品详情可进入阿拉丁官网(https://www.aladdin-e.com),搜索“流式抗体”。
企业动态
2023.11.17
【阿拉丁】连接子 - 抗体与药物结合的关键因素
连接子 - 抗体与药物结合的关键因素抗体-药物偶联物(Antibody-drug conjugate, ADC)结合了抗体的高特异性和小分子药物的强细胞毒性。这种组合结合了抗体的独特和非常敏感的目标能力,可以区分健康组织和癌组织。它还具有细胞毒性药物的细胞杀伤能力,可能最大限度地减少剂量限制性毒性,同时最大限度地提高所需的治疗效果。ADC的主要优点是可以在体循环中作为药物使用,最终在靶肿瘤细胞中释放游离药物。在这一过程中,连接子在释放有效药物靶向肿瘤细胞,决定ADC的药代动力学特性、治疗指标和选择性,甚至整体成功方面发挥着关键作用。目前使用的连接子可分为可切割连接子和不可切割连接子两大类,它们之间的区别在于它们在细胞内是否会被降解。一、用于连接的可切割连接ADC连接子的主要类别是可切割连接子。可切割连接子被设计为对细胞外和细胞内环境差异(pH、氧化还原电位等)表现出化学不稳定性,或者可以被特定的溶酶体酶切割。在大多数情况下,这种连接子被设计成在键断裂后释放有效载荷分子。这种无迹可循的药物释放机制使研究人员能够根据已知的游离有效载荷的药理学参数估计共轭有效载荷的细胞毒性。2.1 可切割接头的类型可裂解接头腙是一种酸不稳定基团,当ADC被转运到核内体(pH 5.0-6.0)和溶酶体(pH约4.8)时,它被用作可切割的连接子,通过水解释放游离药物。组织蛋白酶B响应连接子组织蛋白酶B是一种溶酶体蛋白酶,在多种癌细胞中过表达,参与人类许多致癌过程。组织蛋白酶B的底物范围相对较广,但它优先识别某些序列,如苯丙氨酸-赖氨酸(Phe-Lys)和缬氨酸-瓜氨酸(Val-Cit)。这种序列的c端切割肽键。Val-Cit和Val-Ala连接物偶联p -氨基苄氧羰基(Val-Cit- pabc和Val-Ala- pabc)是adc最成功的可切割连接物。PABC片段使自由有效载荷分子以无迹方式释放。双硫键连接子谷胱甘肽敏感连接子是另一种常见的裂解连接子,其策略依赖于细胞质中较高浓度的还原分子(如谷胱甘肽)(1-10 mmol/L)。二硫键嵌入在连接子中,在循环中抵抗还原性裂解。然而,内化后,大量细胞内谷胱甘肽减少二硫键,释放自由有效载荷分子。为了进一步提高循环中的稳定性,通常在二硫键旁边安装一个甲基。焦磷酸二酯连接子该阴离子连接子具有比传统连接子更高的水溶性和优良的循环稳定性。此外,在内化后,焦磷酸二酯通过内核体-溶酶体途径快速裂解,释放未修饰的有效载荷分子。图1. 可切割连接子。(Kyoji Tsuchikama & Zhiqiang An. 2018)二、不可切割的连接子不可切割连接子由稳定的键组成,抵抗蛋白质水解降解,确保比可切割连接子更高的稳定性。不可切割连接子依赖于细胞质和溶酶体蛋白酶对ADC抗体成分的完全降解,并最终释放与降解抗体衍生的氨基酸残基连接的有效载荷分子。与可切割连接子相比,不可切割连接子的最大优点是其等离子体稳定性增强,与可切割连接子相比,这可能提供更大的治疗窗口。此外,与可切割的偶联物相比,它有望降低脱靶毒性,因为不可切割的adc可以提供更大的稳定性和耐受性。图2. 不可切割的连接子。不可切割连接的化学稳定性可以承受蛋白质水解降解。单抗的细胞质/溶酶体降解可以释放与降解的单抗衍生氨基酸残基相连的有效载荷分子。(Kyoji Tsuchikama & Zhiqiang An. 2018)三、总结结论保证游离药物在肿瘤细胞内的特异性释放是选择Linker的最终目的。该连接子对ADC的稳定性、毒性、PK特性和药效学等具有重要意义。每个环节都有其优点和缺点。在选择连接子时,必须考虑许多因素,包括单克隆抗体和细胞毒性药物中的现有基团、反应性基团和衍生功能基团。最后,需要通过个案分析确定如何优化选择合适的连接物、靶点和毒性分子,平衡ADC药物的有效性和毒性。表1. 连接子类型及优缺点比较参考文献1. Kyoji Tsuchikama & Zhiqiang An. Antibody-drug conjugates: recent advances in conjugation and linker chemistries. Protein & Cell. 2018; 9:33-46.2. Jun Lu. Feng Jiang. Aiping Lu. and Ge Zhang. Linkers Having a Crucial Role in Antibody–Drug Conjugates. Int J Mol Sci. 2016 Apr; 17(4):561.3. Monteiro Ide P, Madureira P, de Vasconscelos A, Pozza DH, de Mello RA. Targeting HER family in HER2-positive metastatic breast cancer: potential biomarkers and novel targeted therapies. Pharmacogenomics. 2015; 16(3):257-71.阿拉丁提供相关产品,详情请见阿拉丁官网:Linkers - A Crucial Factor in Antibody–Drug Conjugates (aladdin-e.com)
应用实例
2023.11.13
【阿拉丁】双十一盛宴!感恩回馈,满赠三重好礼!
敬请进入阿拉丁官网参与活动!点击进入官网 立即选购! 活动时间:2023年11月8日-2023年11月22日活动规则:1、用户在活动期间(2023年11月8日-2023年11月22日)通过官网下单,当1,199元≤单笔订单金额时,可享阿拉丁定制周边好礼:精美玻璃杯一个(礼品限量,先到先得)。2、用户在活动期间(2023年11月8日-2023年11月22日)通过官网下单,当3,299元≤单笔订单金额时,可享阿拉丁定制周边好礼:全能移动电源一个(颜色随机配发,礼品限量,先到先得)。3、用户在活动期间(2023年11月8日-2023年11月22日)通过官网下单,当单笔订单金额≥5,299 元时,可享阿拉丁定制周边好礼:小米联名无线蓝牙鼠标一个(礼品限量,先到先得)。 注:1、礼品领取方式:当订单为现货时,活动礼品将在活动期间随货发放;如存在期货产品,将于活动结束后统一确认信息并告知客户礼品配送时间,再进行派送(阿拉丁默认用户下单收货地址为礼品派发地址)。2、本活动仅针对官网下单的积分用户,未在官网下单的及非积分用户不在本次活动范围内。3、阿拉丁官网全部试剂及耗材将参与本次活动,积分礼品及检测服务不在本次活动范围内。4、本次活动礼品限量赠送且颜色随机,按照下单时间进行审核,审核通过后先到先得,送完即止。5、若符合活动规则的订单在指定礼品派送完后,阿拉丁有权决定用活动其他礼品代替,但将尽量提前通知用户(客服联系)。6、用户承诺并保证其完全有权将个人及单位信息提供给阿拉丁保存记录,用户应保证其所填信息的真实性、完整性和合法性,并且保证不会侵犯任何的合法权利。如因用户违反本承诺,将赔偿阿拉丁由此产生的全部损失。7、礼品发放前阿拉丁需要核实用户有无超账期欠款,结清超期欠款后才可发放礼品。8、上海阿拉丁生化科技股份有限公司享有对本活动的最终解释权。
企业动态
2023.11.07
【阿拉丁】量子点技术在癌症检测和治疗中的应用
癌症的早期筛查是必要的,因为大多数肿瘤只有当它们含有数百万可能已经转移的细胞、达到一定的大小时才能被检测到。目前采用的诊断技术,如医学成像、组织活检和酶联免疫吸附试验(ELISA)对体液的生物分析所具有的敏感性和特异性不足以检测大多数类型的早期癌症。此外,这些分析是劳动密集型、耗时、昂贵的,且没有能够反复利用结果的能力。另一方面,基于量子点的检测是快速、简单和经济的,可以实现癌症标志物的快速护理点筛查。量子点具有独特的特性,使其成为检测肿瘤的理想选择,包括长时间的强而稳定的荧光、耐光漂白性[1-5]、大的摩尔消光系数、高灵敏度的检测,因为它们具备在吸收和发射光上均非常高效的能力。由于量子点具有较大的表面积体积比,单个量子点可以与多种分子结合,因此量子点在设计更复杂的多功能纳米结构方面具有很大的应用价值。各种类型的生物标记物,如蛋白质,特定的DNA或mRNA序列和循环肿瘤细胞,已经可以从血清样本中确定用于癌症诊断。因此,基于量子点(QD)的多路复用方法[1]可以同时识别多个生物标志物,从而可以实现更有效的癌症诊断。量子点已被共价连接到各种生物分子,如抗体、多肽、核酸和其他配体,用于荧光探测[6-19]。其在生物学中的一些应用[20-32]以及它们在体内分子成像方面的巨大潜力[33-37]正在一一被揭开。 无机量子点相对于有机荧光团的优势与生物实验中用于荧光标记的传统有机荧光团相比,无机量子点由于其对光漂白的高抗性,使生物材料的可视化时间更长,应用范围更广。由于荧光团对周围环境非常敏感,可以进行光漂白,这是一种不可逆的光氧化过程,使它们成为非荧光体,是所有需要长时间观察荧光团标记结构的研究的主要限制。荧光团只能在很窄的波长范围内被光学激发,荧光发射也被限制在一定的波长范围内。而量子点可以用波长比荧光波长短的单一光源激发。量子点的荧光光谱较窄、对称,在荧光团中没有红尾,各种颜色都可以被观察和区分,没有任何光谱重叠。因此,用不同颜色的量子点对不同结构进行多色标记成为可能。这种多路复用的方法[3, 38-40]在疾病诊断和药物输送等场景中具有广阔的应用前景。量子点是一个跨学科的研究领域,经过化学、物理、生物和医学等不同学科的人员共同努力,有利于发现它的最大价值,将它们用于癌症的检测和治疗就是一种极为重要的应用。 量子点技术量子点是一种具有独特发光特性的无机半导体纳米晶体,其典型直径在2-8nm之间。它们通常由元素周期表中的II和VI族元素(例如CdSe和CdTe)或III和V族元素(例如InP和InAs)的原子组成。它们的物理尺寸小于导致量子限制效应的波尔半径[1]激子,这就是它们具有独特的光学和电子特性的原因。 量子点的合成高质量的量子点已经可以通过各种方法合成[41-43],但通常它们的合成是在有机溶剂中进行的,如甲苯或氯仿,并且会添加表面活性剂,反应温度较高。但表面活性剂包覆的颗粒不溶于水,其极性表面活性剂头基会附着在量子点(QD)的无机核心上,疏水链则会凸出到有机溶剂中,而一般来说,所有细胞实验都涉及水溶性物质。因此,为了使表面活性剂具有水溶性,人们制定了各种策略,要么替换表面活性剂层,要么涂上额外的保护层,如亲水或两亲聚合物[44-45]。表面活性剂的疏水涂层被配体分子所取代,配体分子一端携带官能团与量子点表面结合,另一端携带亲水性基团使量子点可溶于水。也有报道使用两亲性聚合物作为QD表面的附加涂层[38, 46-48]。聚合物的疏水尾部与QD表面的疏水表面活性剂层发生反应,而聚合物的亲水基团在外端产生水溶性。量子点还被包裹在磷脂胶束[8]中,使其可溶于水。 量子点的性质及应用最常用的量子点系统是CdSe的内半导体核包覆ZnS的外壳。ZnS壳层负责保障CdSe核的化学和光学稳定性。只需改变量子点的大小,就可以使其发出从紫外线到红外光谱中所有波长的荧光。量子点的荧光波长取决于它的能隙(即激发态和基态之间的差),这是由量子点的大小决定的[49-52]。量子点具有光谱线宽窄、亮度高、宽光谱范围内吸收系数大、高光稳定性和多路探测能力等特点,即使在复杂的体内条件下,它们也非常明亮和稳定,这使它们适用于先进的分子和细胞成像、药物传递以及高灵敏度的生物测定和诊断的应用[53-54],QD生物偶联物使具有更高分辨率的高灵敏度实时成像,和对活细胞表面单个受体分子的跟踪成为可能[13,55]。量子点的各种应用如图1所示。在大多数情况下,用于癌症检测的功能QD共轭物由半导体核心(CdSe, CdTe)组成;在CdSe作为量子点的情况下,会增加一个额外的壳层,如ZnS,因其具有比CdSe更高的能带隙,能够提高量子产率,同时可作为水溶亲水性涂层,以及作为功能化抗体或其他生物分子在肿瘤位点的补充靶向癌症标记物。图1. 量子点的应用 克服量子点的毒害性由半导体纳米粒子组成的天然量子点在自然界中是有毒的。已经观察到,CdSe量子点对暴露在紫外线下较长时间的细胞有很高的毒性,因为紫外线会溶解CdSe,从而释放出有毒的镉离子。然而,在体内研究[48]表明,聚合物涂层量子点在没有紫外线的情况下是无毒的。研究还表明,将胶束包裹的量子点注射到青蛙胚胎中并不影响其发育[8]。因此,量子点通常被封装在两亲性聚合物的外壳涂层内[57-58],使其具有水溶性,并能抵抗化学或酶降解。它们通常在有机溶剂中合成,如三-正辛基-氧化磷化氢(TOPO)[59-62]和十六烷基胺,它们具有长烷基链和高沸点,从而可以防止形成聚集体。近年来,对量子点进行表面化学修饰使其具有水溶性的研究取得了很大的进展[63-64]。最为常见的是,量子点与聚乙二醇(PEG)或类似的配体连接,以使它们具有生物相容性并减少非特异性结合。通过使用不同的策略将它们与各种生物亲和配体(如多肽、抗体、寡核苷酸等)结合,使它们对目标位点具有特异性。用于检测肿瘤细胞生物标记物的QD生物偶联物的可能示意图如图2所示。图3则简要描述了QD技术用于癌症体内诊断的各个步骤。图2. 多功能量子点通常用于靶向肿瘤细胞。QDs与各种亲和配体(肽、抗体、抑制剂、药物等)结合,这些配体对肿瘤细胞的生物标志物具有特异性。 图3. 量子点用于癌症体内诊断的步骤。(a)QD生物偶联物的形成,(b)将QD生物偶联物静脉注射到小鼠体内,(c)QD生物偶联物能有效靶向肿瘤细胞。 量子点的闪烁行为Nirmal等人[65]首次发现,量子点在连续激发下会表现出闪烁行为,即间歇性开关发射,这归因于俄歇电离[65-66]。即使在今天,这种行为的原理也没有得到很好的解释。但是,只有在分析过程中需要单个QD的信号时(如流式细胞术应用程序),它才需要被重点关注到。在这种情况下,单个量子点的发射可能由于“闪烁”而关闭,从而导致探测器的信号丢失。但通常在大多数应用中,如在基于细胞的分析中,涉及多个量子点,即使一些量子点闪烁,其他量子点也会发出信号供最终检测,因此,检测器不会遗漏任何信号。一种抵消闪烁导致的量子产率降低的方法是在量子点核心的顶部组装一个由几层具有更大能带隙的材料原子层组成的壳层。 表面功能化对量子点光学性质的影响一些基础研究表明,量子点的发光对表面功能化过程非常敏感,因为分子与量子点表面的相互作用会改变量子点表面的电荷[67],但许多基于量子点的探测应用是基于目标分析物分子与量子点表面功能化的生物分子相互作用后量子点荧光的变化而衍生的。量子点的表面功能化改善了其溶解度,但它也会降低量子效率。这在经巯基乙酸处理的量子点中得到了证明,量子效率大大降低[7, 63],但是蛋白质功能化的量子点倾向于保持它们的量子效率,并提供更长的保质期,它们还可以在不降低量子效率的情况下被多个官能团[7]进一步功能化。 用于观察和追踪量子点的测量系统使用共聚焦显微镜、全内反射显微镜或外荧光显微镜可以对单个量子点进行更长时间的观测和追踪,最长可达数小时。Gao等人[68]和So等人[69]介绍了利用量子点作为标签进行荧光成像及其测量的方案:Gao等人采用了波长分辨光谱成像的全身宏观照明系统,可对体内分子靶标进行高灵敏度检测;So等人也采用了波长分辨光谱成像系统,其软件可将自发荧光与量子点信号分离。 主动和被动量子点靶向技术QD生物偶联物可以通过主动靶向和被动靶向两种机制在体内传递给肿瘤,尽管被动靶向比主动靶向慢得多,效率也低得多。在被动靶向机制中,由于增强的通透性和保留作用,QD生物偶联物优先聚集在肿瘤部位[70-72]。这种效应可以归因于血管生成肿瘤(i)产生血管内皮生长因子,负责增强渗透性,(ii)缺乏有效的淋巴引流系统,这导致QD生物偶联物积累。另一方面,在主动靶向机制中,抗体偶联QD将抗体与肿瘤细胞上存在的前列腺特异性膜抗原等特异性肿瘤生物标记物结合在靶向部位。 深层组织成像要求研究表明,深层组织成像需要使用远红外线和近红外线[73],这就需要使用近红外发光的QD来提高肿瘤成像的灵敏度,因为血液和水[74]的主要吸收峰在这一区域不会产生干扰。 去除活细胞中的量子点在将该技术用于人类的癌症诊断和治疗之前,需要对QD从活体动物体内的清除及其新陈代谢进行更加重点的关注和深入研究,受保护的QD从体内清除的唯一途径是通过肾脏缓慢过滤和排泄,因为通过化学或酶分解的可能性很小。 量子点在疾病诊断和治疗中的潜在应用基于量子点技术的最新进展和研究人员对此的浓厚兴趣,在不久的将来,量子点在疾病诊断和治疗领域将会有诸多潜在的应用。 生物分子与量子点的结合目前已开发出各种共价和非共价策略(如图4所示),用于将蛋白质和抗体等生物大分子与量子点结合。生物大分子可以利用交联剂[1, 6, 8, 17, 38, 44, 64, 75-77]进行共价结合,交联剂将量子点表面的-COOH、-NH2或 -SH等官能团与生物大分子上的官能团交联。如今,有各种共轭化学方法可用于修饰生物大分子,使其具有所需的官能团。图4. 将抗体/蛋白质与量子点连接的各种策略 修饰生物分子的策略其中一种策略采用N-乙基-N′-(3-二乙基氨基丙基)碳二亚胺(EDC)作为杂交连接剂,将量子点的羧基与蛋白质的氨基交联。这种方法不需要对蛋白质进行任何化学修饰,因为大多数蛋白质都含有伯胺。另一种策略是基于活性酯马来酰亚胺介导的胺和巯基偶联。但这种方法有一个局限性,即游离的巯基在氧气存在下不稳定,在原生生物大分子中很少发现。最近,Pellegrino等人[46]采用了含有多个酸酐单元的预活化两亲聚合物将蛋白质与量子点结合。由于聚酐是可生物降解的聚合物,因此这种方法有可能应用于制造持续给药系统,但将生物大分子与量子点精确控制和定向结合的策略尚未被深入研究。Goldman等人[78]利用一种融合蛋白将免疫球蛋白G(IgG)与量子点结合,该融合蛋白具有一个带正电的亮氨酸拉链结构域,可与带负电的量子点发生静电结合,而蛋白G结构域可与IgG的恒定Fc区域结合,从而使F(ab′)2区域可自由用于抗原结合。镍-氮三乙酸(Ni-NTA)作为螯合剂,可用于将六组氨酸标记的生物大分子与量子点结合。Gao和他在美国埃默里大学的研究小组正在开发这种技术,它在生物分子的可控定向结合、探针体积小和生产成本低等方面具有优势。链霉亲和素-生物素结合策略也可用于将生物大分子与量子点结合,因为链霉亲和素涂层的量子点可在市场上买到,而且很容易与生物素化的生物大分子结合[13, 38, 55, 59, 80]。图4展示了量子点的各种生物共轭策略。 量子点对生物分子生物学功能的影响研究表明,在许多情况下,生物大分子与量子点的共轭不会改变生物大分子与其特定受体的结合能力[6, 8-9, 13, 17, 38, 55, 58-59 64, 76-77, 80-81]及其生物功能。Kloepfer等人[77]发现,将量子点与转铁蛋白共轭不会影响蛋白质的功能。Dahan等人[82] 也观察到,量子点与膜结合受体的结合对受体在膜中的扩散行为没有影响。不过,也有少数报道称量子点可能会影响生物大分子的生物功能,如神经递质血清素与血清素转运蛋白的结合亲和力[14]。这可能是由于量子点的立体阻碍作用,要确认量子点对生物大分子的生物功能可能产生的影响,还需要进行详细的研究。 量子点技术在癌症诊断中的应用进展在早期阶段,量子点被用于几种成像应用,以取代有机染料,但当观察到这些材料持续发射强荧光数周后,这些材料的巨大应用潜力才得以实现。这是显微成像技术的重大进步,有助于揭示许多细胞过程。在随后的发展阶段,研究人员对量子点技术产生了浓厚的兴趣,并开始探索其在不同领域的应用。制备了由相同材料组成但尺寸不同的量子点,其经单一波长的光激活后可以产生不同的颜色。实验证明,标记有生物分子(如抗体、多肽等)的量子点可用于检测细胞表面或细胞内部的特定分子。 量子点-多肽偶联物可靶向肿瘤细胞Akerman和同事[58]发表了使用量子点-多肽偶联物在体内靶向肿瘤血管的研究。他们采用了ZnS封装的CdSe量子点,并展示了涂覆有不同多肽的量子点的靶向能力。通过静脉注射后,涂有肺靶向肽的量子点在小鼠肺部聚集,该多肽与肺血管内皮细胞上的膜二肽酶结合;第二种情况是,涂覆有靶向肽的量子点与某些肿瘤的血管和肿瘤细胞结合;第三种情况,涂有靶向肽的量子点会与淋巴管和肿瘤细胞结合。该研究小组还表明,在量子点外涂层中添加PEG可防止其在网状内皮组织中的非选择性聚集。 量子点识别活体乳腺癌细胞的能力量子点公司(Quantum Dot Corporation)和基因泰克公司(Genentech)的研究小组证明了量子点在识别可能对抗癌药物产生反应的活体乳腺癌细胞方面的潜力[38]。他们采用与免疫球蛋白G(IgG)和链霉亲和素相连的量子点来标记活体乳腺癌细胞表面的Her2癌症标记物,并探索了同时标记细胞表面和细胞核中 Her2的量子点技术。研究人员用单一激发波长同时检测了两个细胞靶标,从而表明不同颜色的量子点(即尺寸不同但材料相同的量子点)可用于区分单个细胞的不同部分,从而实现多重靶标检测。 多功能量子点同时靶向和成像活体动物的肿瘤Gao和同事报道了多功能量子点同时靶向和成像活体动物的肿瘤的研究[68]。高度稳定的量子点共轭物由两亲性三嵌段共聚物(用于体内保护)、靶向配体(用于肿瘤抗原识别)和多个PEG分子(用于改善生物相容性和循环)组成。通过组织切片显微镜和全动物光谱成像监测量子点探针的体内行为,QD结合物通过静脉注射小鼠,我们观察到它们会通过被动靶向机制(由于肿瘤血管的渗漏)和主动靶向机制(由于包被肿瘤特异性抗体的QD偶联物与肿瘤标记物相互作用)在靶向肿瘤部位聚集。Gao和同事还使用量子点标记培养中的特定细胞,观察到在很短的一段时间内,量子点在细胞核中积累。因此,具有量子点的细胞在注射后,可以借助其荧光在活体动物体内进行跟踪。 近红外量子点用于前哨淋巴结绘图Kim和团队[34]探索了利用发射波长为850 nm的近红外量子点进行前哨淋巴结绘图的实用性,这是在最靠近受影响器官的淋巴结中检测游离癌细胞的主要途径。将量子点经皮内注射到活体小鼠体内后,甚至在皮肤下1厘米处的前哨淋巴结也能得到实时跟踪。这一进展是一项重大突破,因为在不使用放射性标记的情况下,切除前哨淋巴结所需的切口面积减小了。研究人员正在尝试使用量子点技术来治疗癌症,一种可能性是用X射线/红外光照射注射后的量子点,这将为肿瘤提供热能并引发细胞凋亡/程序性细胞死亡的过程。 用于多路复用的量子点Goldman和同事[83]在使用单一激发光源的夹心免疫测定中使用了四种具有不同发射波长的量子点,证明了量子点对四种毒素进行多重分析的能力。同样地,Makrides和同事[84]在蛋白质印迹检测中使用了两种光谱不同的量子点来检测两种蛋白质。在需要检测的目标肿瘤部位存在的各种癌症生物标记物时,多路复用的方法具有极其重要的意义。 用于体内成像的自发光量子点最近,斯坦福大学的Jianghong Rao研究小组证明,自发光QD共轭物(QD-Luc8)具有体内成像的潜在应用价值[69]。该研究小组开发了一种雷尼拉肾形荧光素酶(Luc8)的八次突变变体,它在血清中更稳定,催化效率更高。利用 1-乙基-3-(3-二甲基氨基丙基)盐酸碳二亚胺(EDC)交联剂,将Luc8与聚合物包覆的镉/锌核壳QD 655共轭,制成自发光 QD共轭,它们在没有外部激发的情况下通过生物发光共振能量转移(BRET)发光。BRET是一个能量从发光供体蛋白(如R. reniformis 荧光素酶)向附近的受体荧光蛋白进行非辐射性转移的过程[69, 85-87],与现有的QD相比,它大大提高了小动物成像的灵敏度。用于体内成像的QD的最大优势之一是,通过调整其尺寸,可在整个近红外光谱范围内调整其发射波长,从而产生在生物缓冲液中高度稳定的光稳定性荧光团。这是因为深层组织光学成像在近红外光谱中效果最佳,因为瑞利散射随波长增加而减少,而且动物体内的主要发色团(即血红蛋白和水)在该光谱中具有局部吸收最小值。使用EDC将检测癌症生物标志物的抗体与QD-Luc8复合物结合。将形成的QD-Luc8抗体复合物通过尾静脉注射到患癌小鼠体内,以检测癌症生物标志物。然后将小鼠麻醉并转移到光密室中。几分钟后,静脉注射Luc8的底物——腔肠素,并拍摄体内生物发光图像。 基于量子点的靶向癌症药物传递系统Shuming Nie及其同事[35]用一层防水的聚合物涂层改造了原始的镉硒QD,防止了剧毒镉离子从QD共轭物中渗出,并提供了一种将肿瘤靶向分子和给药功能化学附着到QD共轭物上的方法,该研究小组正在开发一种针对癌细胞的给药系统。开发的与肽或抗体结合的 量子点,用于靶向在小鼠体内生长的人类肿瘤细胞,QD将被调整为在红外区域辐射,以防止能量发射对组织造成损害。与针对目标癌细胞表面癌症标志物的特异性肽/抗体结合的量子点只有在受到激光照射时才会释放药物,这样就可以控制接受毒素的细胞,从而将副作用降到最低。同时他们还在努力将量子点的荧光波长扩展到900 nm以上,因为几乎没有任何生物分子的荧光波长超过这一数值。 该技术的现状如今,在量子点技术的帮助下,癌症研究人员能够观察到肿瘤细胞中发生的基本分子事件。这是通过荧光显微镜在体内跟踪不同大小、不同颜色的QD(标记有多种不同的生物分子)来实现的,量子点技术在纳米生物技术和医疗诊断等领域具有巨大的应用潜力,可被用作标签。但要在人体中使用它们,仍需要进行广泛的研究,以确定使用的长期影响。 量子点在癌症诊断和治疗中的应用前景研究人员对量子点的探索始于最近二十年。虽然这一领域仍处于起步阶段,但由于其独特的光学和电子特性,它已深深吸引了科学家和工程师的关注。量子点已经彻底改变了分子成像领域,在未来几年,它们将在不同领域得到不同程度的发展,影响最大的领域之一肯定是活细胞的细胞内成像,这项技术将为了解癌症的病理生理学以及肿瘤成像和筛查提供新的见解。量子点在未来肯定会成为所设想的多功能纳米设备的组成部分之一,这种设备可以检测病变组织、提供治疗并实时报告进展情况。 阿拉丁提供相关产品,详情请见阿拉丁官网:Applications of Quantum Dot Technologies in Cancer Detection and Treatment (aladdin-e.com)
应用实例
2023.11.03
吖丁啶在药物化学、有机合成和生物化学中的应用----阿拉丁试剂
简介吖丁啶(Azetidine),也称氮杂环丁烷,是一种饱和杂环有机化合物,含有三个碳原子和一个氮原子。它在室温下呈液态,有强烈的氨味,与大多数仲胺相比其具有强碱性。图1. 吖丁啶(Azetidine) 吖丁啶及其衍生物由于具有较高的刚性和环张力,很少出现在自然界的天然分子结构中。几乎未被探索的四元杂环——氮杂环丁烷是饱和氮杂环家族中一类特别的存在。尽管合成取代氮杂环丁烷往往非常具有挑战性,但由于其在催化、立体选择性合成和药物化学中的重要作用依然受到化学家的极大关注。近年来,由于对提高候选药物分子的饱和度和三维性需求的不断增加,如何有效获得取代杂环衍生物变得愈加重要。[1]合成和制备吖丁啶可以通过氢化铝锂还原2-氮杂环丁酮(β-内酰胺)制得。更有效的方法是使用氢化铝锂和三氯化铝的混合物,三氯化铝是“AlClH2”和“AlCl2H”的来源。[2] 吖丁啶也可以以3-氨基-1-丙醇为原料通过多步反应制得。[3] 2-芳基氮杂环丁烷的区域选择性和非对映选择性合成可以通过适当取代的环氧乙烷经由环转化进行。它遵从鲍德温规则(Baldwin's rules),具有显著的官能团耐受性。 吖丁啶及其衍生物是天然产物中相对罕见的化学骨架。它们是木根酸和Penaresidin的成分之一。氮杂环丁烷-2-羧酸是最丰富的含有氮杂环丁烷的天然产物,是脯氨酸的非蛋白原氨基酸同系物,可以错误地掺入蛋白质中代替脯氨酸。[4]应用药物化学:在过去的十年里,基于片段的药物设计(FBDD)已经成为一种极具潜力的新药研发方法。由于大多数有机小分子缺乏固有的分子刚性,这似乎成为了这种有前景的方法的一个严重障碍(图2)。在利用计算机筛选方法的时,构象受限的刚性分子显示出更高的结果再现性。通过引入环或环系统改变分子构象柔性是最常用的方法之一。小的单环骨架优选于其他构象受限的骨架,原因是它们对分子的总分子量和亲脂性的影响较小。而氮杂环丁烷是最小的含氮饱和杂环,具有合理的化学稳定性。一段时间以来,含有吖丁啶的分子砌块已被广泛用于药物设计之中;其中最著名且成功的一个例子是高血压治疗药阿折地平(Azelnidipine),属于钙离子通道阻滞剂。图2. 含有氮杂环丁烷结构的具有生物活性的药物先导化合物和天然产物有机合成:与其他氮杂环如氮杂环、吡咯烷或哌啶相比,关于氮杂环丁烷的研究和进展要少得多,可能是因为它们的可用性有限。最近已经开发了从容易获得的对映体纯起始化合物开始的这些应变杂环的合成路线。这些杂环中的环应变使它们成为亲核开环或扩环反应的优秀候选化合物,从而合成更高的环系或高度取代的无环胺。生物化学:新型氨基酸合成备受瞩目,其中难点在于保持氨基酸部分的氮杂环,如脯氨酸、哌啶酸和谷氨酸类似物的许多合成方法也都显示出来这一点。相反,四元杂环氨基酸的合成却鲜有报道,这可能是由于缺乏有效的合成方法来制备官能化的氮杂环丁烷,尤其是对映体纯形式的氮杂环丁烷。Rabassoa课题组报道了一种合成具有一般结构的氮杂环丁烷氨基酸的新路线,如图3所示。其中位于C-4的R基团的性质来源于对映体纯的β-氨基醇。[5]图3. 氮杂环丁烷氨基酸参考文献1. Recent advances in the Chemistry of Metallated Azetidines, J. Name., 2013, 00, 1-3 https://doi.org/10.1039/C6OB01665K2. Alcaide, Benito; Almendros, Pedro; Aragoncillo, Cristina (2007). "Β-Lactams: Versatile Building Blocks for the Stereoselective Synthesis of Non-β-Lactam Products". Chemical Reviews. 107 (11): 4437–4492. https://doi.org/10.1021/cr03073003. Donald H. Wadsworth (1973). "Azetidine". Organic Syntheses. 53: 13. https://doi.org/10.15227/orgsyn.053.00134. Kovács, Ervin; Ferenc, Faigl; Zoltan, Mucsi (Aug 10, 2020). "Regio- and Diastereoselective Synthesis of 2-Arylazetidines. Quantum Chemical Explanation of Baldwin's Rules for the Ring-formation Reactions of Oxiranes". Journal of Organic Chemistry. 85 (17): 11226–11239. https://doi.org/10.1021/acs.joc.0c01310Azetidinic amino acids: stereocontrolled synthesis and pharmacological characterization as ligands for glutamate receptors and transporters, Org. Biomol. Chem. , 2005, 3 , 3926–3936 https://doi.org/10.1039/B509514J阿拉丁提供相关产品,详情请见阿拉丁官网:Substituted Azetidines in pharmaceutical chemistry, organic synthesis, and biochemistry (aladdin-e.com)
应用实例
2023.10.31