









《机智的医生生活》中,新生儿由于先天性心脏病而延迟关胸,手术之后小朋友心脏不再需要借助仪器辅助,开始健康地跳动,“李子一样大小的心脏,跳动起来异常有力”震撼的场面让实习医生们决定加入胸外科的道路。心脏的跳动是生命的信号,血液流过的地方与心跳一起带给了心内膜细胞(Endocardial cells,ECs)流体剪切机械应力以及牵拉力。在发育过程中机械力帮助心血管系统逐渐成型,但这些力量如何指导局部心肌细胞的细胞命运的刻画的仍不清楚。
为此,法国国家健康与医学研究院Julien Vermot研究组在Science发文题为Bioelectric signaling and the control of cardiac cell identity in response to mechanical forces,通过在体内操纵机械应力揭开了机械力在促进心血管瓣膜形成以及特定细胞命运决定中的关键作用。
以斑马鱼作为模式生物可以实现高分辨率的时空机械应力参数在体内的控制,作者们首先通过的荧光标记的Ca2+感受器蛋白GCaMP7a在心内膜细胞中的表达监测Ca2+的动态变化【1】作者们惊讶地发现Ca2+振荡几乎只会在房室瓣的房室管区域形成(图1)。这一现象引发的了作者们的兴趣,作者们想知道Ca2+的振荡是否与血管瓣膜形成分化过程相关,所以作者们想找到Ca2+信号在体内的解码器以及效应因子。也就是说,什么因子能够读取Ca2+振荡事件所带来的信息呢?先前的研究表明,Nfatc1(Nuclear factor of activated T cells 1)是一个对Ca2+通道非常敏感的转录因子,能够调节心内膜细胞向间充质细胞的转化以及心脏瓣膜形态发生过程【2,3】。因此,作者们构建了一个Nfat结合元件报告品系,可以反映Nfat蛋白的结合。作者们确认了Ca2+信号通路的时空调控与Nfat激活是相耦连的,是瓣膜形成过程中心内膜细胞中的特征。
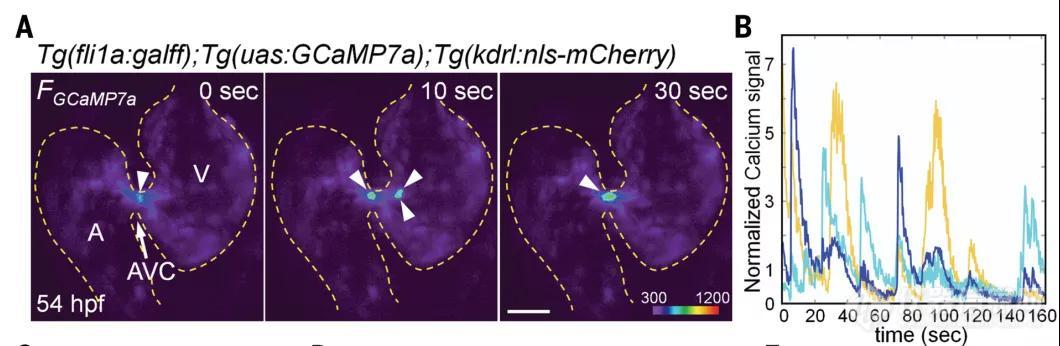
图1 Ca2+振荡只出现在瓣膜形成区域
进一步地,作者们想知道所观察的Ca2+振荡是否与心内膜细胞中对于应力的响应有关,所以作者们使用抑制剂处理使得心脏跳动停止,然后观察此时Ca2+信号的变化。作者们发现心脏跳动停止后,Ca2+振荡消失,与此同时Nfat的激活也消失。另外,在斑马鱼的缺血性突变体中Ca2+的振荡也会显著减少,并且Nfat的活性也同步降低。这些现象表明Ca2+振荡以及Nfat的激活对于机械应力具有响应。
进一步地,作者们希望通过操纵血管瓣膜边界处的机械应力对机械力改变所带来的效应进行检测。作者们想到了一个很巧妙地方式,将一个30-60μm的琼脂磁珠插入到心血管腔中,通过精妙地微型外科手术确保不会影响心脏的正常功能。作者们通过磁镊(Magnetic tweezers)精确调控可以施加在磁珠上的机械应力。通过Ca2+的流量对心内膜细胞中对机械力的响应,作者们发现心肌细胞机械应力的与Ca2+振荡有关。
那么当应力发生错误的时候,是否对瓣膜形态形成和发育有影响呢?为此,作者们通过对磁珠移植的局部反应进行检测,发现移植的磁珠会导致心脏瓣膜定位异常并伸入心胶质中,同也会导致心脏瓣膜相关基因的异常表达。另外,通过Nfat的抑制剂处理,作者们发现Nfatc1的核定位会被增加的机械力所促进,并且是以一种Nfatc1中Ser/Thr去磷酸化依赖的方式进行的。除此之外,作者们发现Ca2+-Nfat信号通路并不是通过通常认为的klf2a机械转导信号进行的,而是通过一个机械力敏感的基因egr1实现的。
为了找到机械力依赖的Ca2+-Nfat信号通路激活的具体因子,作者们对一些已知对机械力敏感的通道蛋白以及纤毛发生相关的突变体品系进行检测,比如Trp通道以及Piezo等。但是作者们发现这些突变体中Ca2+激活都是正常的,而且对胚胎使用非特异性应力敏感通道阻滞剂钆离子处理后的胚胎Ca2+的激活也是正常的。这说明可能有其他的因素参与其中。先前的研究表明,这体外培养的心内膜细胞对于机械力在响应的时候会产生ATP水平的变化【4】,ATP会通过嘌呤受体P2X通道激活Ca2+信号。通过拮抗剂以及转录本、过表达等实验,作者们确认在心内膜细胞中Ca2+内流是由P2X通道调节,以响应胞外ATP水平的变化。
随后作者们对激活以及抑制P2X介导的ATP信号通路对瓣膜形成的影响进行鉴定,发现P2X受体调节Nfat活性,但该调节作用并不依赖于VEGF信号通路。P2X介导的ATP信号通路发生异常时,心脏瓣膜结构异常,瓣膜形态不完全。因此,P2X作为Nfat活性上游发挥作用,控制心脏瓣膜发育以响应机械力的刺激。
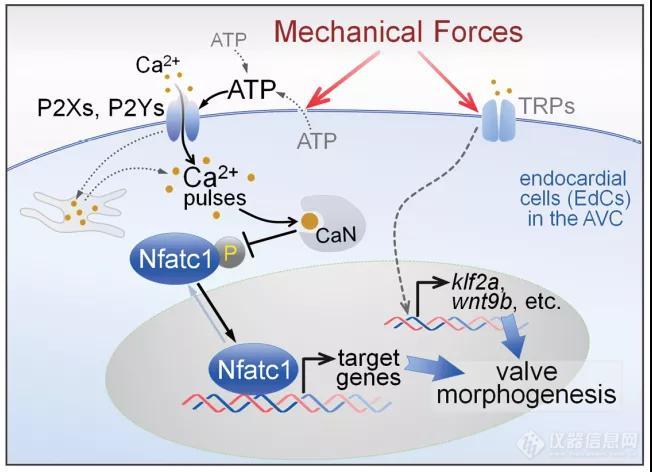
图2 工作模型
总的来说,该工作揭开了心内膜细胞“破译”机械力信息的奥秘(图2),并且发现ATP作为一种附加的机械敏感旁分泌信号,通过它血流动力学力量可以指导心脏瓣膜的发育,可能可以作为未来帮助心脏瓣膜在体外的生长以及对先天性心脏瓣膜缺陷的治疗方案。
由于该工作对于心脏瓣膜发育与机械力之间关系的揭示,同期刊发了观点文章对其进行了高度评价,题为Not all stress is bad for your heart。适当的机械应力对于心内膜细胞感受刺激并在正确位置产生心脏瓣膜具有非常重要的意义。斑马鱼中的研究并非终点,如何将机械应力在哺乳动物例如小鼠或者人类中瓣膜形成与特化过程相联系,能否用于三维类器官培养以造福病人等该领域未来的发展方向。不过,看来有点儿“小压力”对心脏也并非坏事,小压力,才有强心脏!
原文链接:
https://www.science.org/doi/abs/10.1126/science.abc6229
[来源: BioArt]

2024.07.16

2024.07.16

2024.07.16

超23亿!北京首批医疗设备购置项目公布,涉及CT、DR、基因序列仪等
2024.07.16


2024.07.16
版权与免责声明:
① 凡本网注明"来源:仪器信息网"的所有作品,版权均属于仪器信息网,未经本网授权不得转载、摘编或利用其它方式使用。已获本网授权的作品,应在授权范围内使用,并注明"来源:仪器信息网"。违者本网将追究相关法律责任。
② 本网凡注明"来源:xxx(非本网)"的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责,且不承担此类作品侵权行为的直接责任及连带责任。如其他媒体、网站或个人从本网下载使用,必须保留本网注明的"稿件来源",并自负版权等法律责任。
③ 如涉及作品内容、版权等问题,请在作品发表之日起两周内与本网联系,否则视为默认仪器信息网有权转载。
![]() 谢谢您的赞赏,您的鼓励是我前进的动力~
谢谢您的赞赏,您的鼓励是我前进的动力~
打赏失败了~
评论成功+4积分
评论成功,积分获取达到限制
![]() 投票成功~
投票成功~
投票失败了~