【设备更新】精选案例 | PR系列蛋白稳定性分析仪
2023/06/16 13:22
阅读:71
分享:方案摘要:
产品配置单:
NanoTemper PR Panta+机械臂自动上样器 全自动多功能蛋白稳定性分析仪
型号: Panta+Robotic Autosampler
产地: 德国
品牌: NanoTemper
面议
参考报价
联系电话
PR-C002 | PR NT.48 系列标准毛细管
型号:
产地:
品牌: NanoTemper
面议
参考报价
联系电话
方案详情:
精选案例 | PR系列蛋白稳定性分析仪
过去,很多生物制药企业主要基于生物学活性来筛选生物药候选分子,却极少在研发前期考量其可生产性等因素。致使很多前期给予厚望的候选分子在后期生产工艺开发阶段时,遇到稳定性等技术方面的困难,使其无法顺利商业化,从而导致大量资源消耗及低效研发回报率。近来,越来越多的研发机构开始将生物药尤其是抗体稳定性纳入前期开发流程中以便及早降低其开发风险。
今天小编将和大家分享并一起学习Merck、Janssen、Amgen等知名药企在以下3个研究领域中的应用案例:
1) 抗体可开发性评估;
2) 制剂开发;
3) 等效验收标准建立的工作流程。
抗体可开发性评估
01
通过早期发现筛选预测抗体可开发性

doi:10.1080/19420862.2020.1743053IF: 6.440 Q2

2020年3月,Merck的研发人员在mAbs杂志发表了抗体可开发性评估流程(图1)。在早期筛选阶段,使用高通量分析方法对152个单克隆抗体进行表征(如纯度、热稳定性、结合活性等),后将大量实验数据上传至数据管理系统,进行关联分析排序,从而有效选择出最小风险的抗体进行下游开发(图2)。
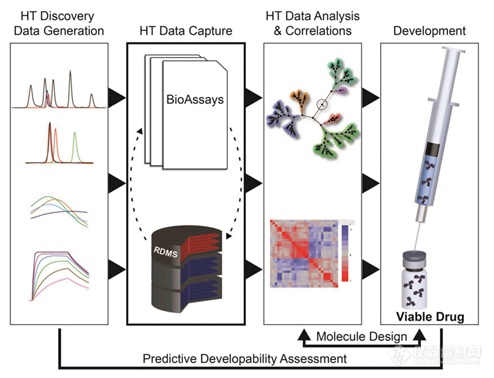
图1. 高通量分析表征,可开发性数据管理系统
制作关联分析热图,根据关联性强弱进行分群(图2)。相关系数为1,红色区域为强烈的正相关;相关系数为0,灰色区域无相关性;相关系数为-1,蓝色区域为强烈的负相关。
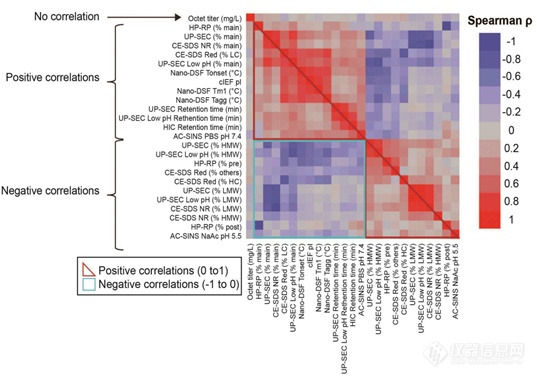
图2. spearman相关系数热图
表1为相关性最高的实验结果(如spearman相关系数ρ>0.5,p<0.001),解链起始温度Tonset,解链温度Tm以及聚集起始温度Tagg有很高的相关性,并且Tonset,Tm及Tagg与高等电点,抵抗聚集体形成之间呈现非常强的关联,接下来研究人员将这些指标应用到抗体的筛选中。
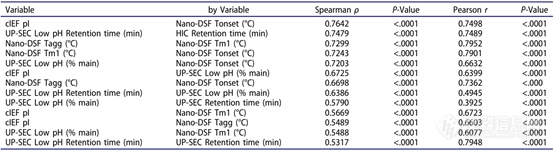
表1. 相关性最强的实验结果
mAb87,由低pH调节到7时出现白色沉淀,造成20%的蛋白损失并出现2%可溶性聚集,可能是因为pI较低造成。随后研究人员generate了9个variants以提高pI。根据10种抗体的热稳定性Tm,SEC,毛细管电泳等检测结果(图3),发现mAb107(红框处)的纯度、热稳定性、聚集倾向以及等电点均有明显的提升。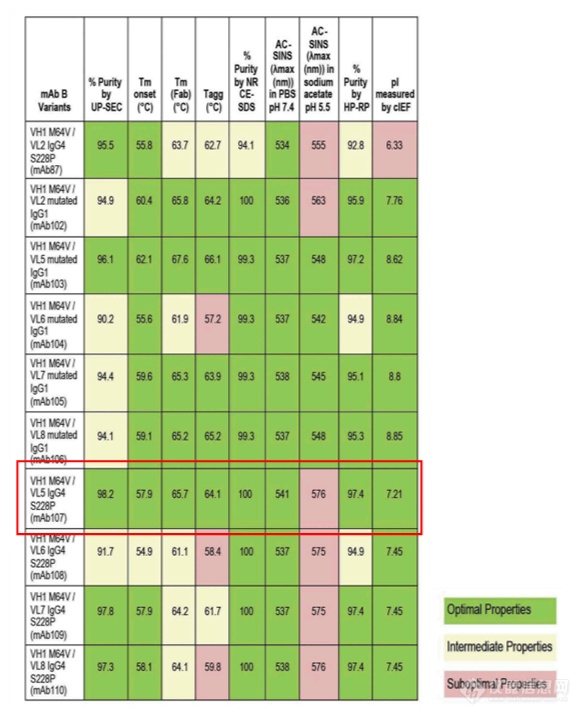
图3. mAb87及其variants可开发性比较
选取mAb87,mAb107及其突变体mAb111进行纯化检测,研究人员发现mAb107及其突变体mAb111几乎所有的下游工艺开发属性均得到了提升,如溶解度提升,自相互作用变弱。50 ℃放置10天后,流式细胞仪计算颗粒数量,从mAb87的8053个降低至不到2000个(详细信息见原文)。结果表明通过SEC、热稳定性Tonset、Tm、胶体稳定性Tagg进行早期的可开发性属性评估,可以快速锁定有效的候选分子。在进行早期可开发性评估时,通常可用于检测的样品量较少并且需要检测结合活性、稳定性等多种参数。PR只需10 μL样品,一次运行可检测48个样品并同时得到解链起始温度Tonset、解链温度Tm、聚集起始温度Tagg三种关键参数,帮助用户降低成本,提升筛选效率,快速发现最合适的候选抗体。
02
提高前列腺癌靶向抗体的稳定性

doi:10.1038/s41598-020-66636-zIF: 4.996 Q2

Janssen使用转基因鼠生产靶向前列腺癌抗原的抗体PCa75,PCa75表现出良好的功能属性,与靶标的亲和力为247 pM。但Fab片段的Tm仅有61.8 ℃(图4),其热稳定性与胶体稳定性并不理想。因此研究人员generate了10个突变抗体,对其稳定性、结合活性及免疫原性进行了对比。其中PCa62 Fab Tm及Tagg显著提升。EpiMatrix score结果(表2)也显示PCa62免疫原性风险较低(EpiMatrix score>20更易产生免疫原性,score<-20则倾向免疫惰性)。综合以上结果,研究人员认为PCa62是最有希望成药的分子。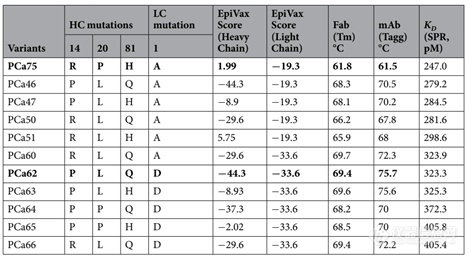
表2. 抗体EpiVax scores,Fab Tm,Tagg检测结果
为了更加全面评估抗体的构象稳定性,研究人员进行化学变性实验。将抗体用梯度稀释的盐酸胍孵育12小时后上机检测,PCa62出现两个transition,并且第二个ΔG是PCa75的2.5倍,表明PCa62比PCa75稳定。
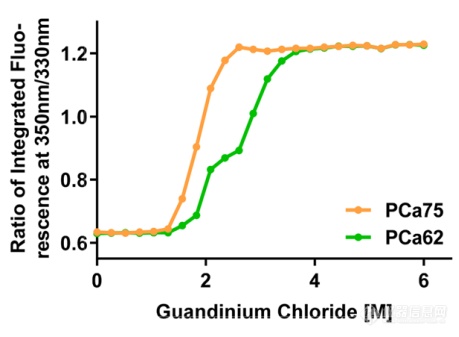
图4. PCa75与Pca62化学变性检测结果
加速实验也呈现出同样的结果。将PCa62与Pca75在4 ℃和40 ℃放置28天,在第0天,第14天,第28天通过SEC监测降解情况。最终,Pca62在4 ℃形成的聚集体小于0.3%,40 ℃下形成的聚集体小于1%。而Pca75在4 ℃形成的聚集体为0.5%,40 ℃下形成的聚集体增加至3%。基于以上结果,研究人员将PCa62锁定为候选抗体。
除了Tm,Tagg之外,PR还可轻松完成化学变性实验。使用变性剂孵育抗体后上机,PR可以在十几秒内得到化学变性曲线,并自动计算ΔG,无需自行分析。此外,您还可以在PR上自定义升温程序(如在25 ℃和80 ℃之间循环切换)对抗体进行复性分析。
制剂开发
03
HIV疫苗多参数制剂筛选

doi:10.1101/2020.11.30.403873

据统计,有约60%的公司遭遇过制剂开发问题导致的项目延迟甚至失败,尽早启动制剂开发能够帮助企业降低药物研发风险。近期2bind公司借助NanoTemper今年刚上市的PR Panta完成了HIV-1疫苗BG505-SOSIP的制剂开发,预印本已发布于bioRxiv。
2bind的研究人员使用FORMOscreen® buffer筛选试剂盒与NanoTemper的Panta仪器寻找能够提升HIV-1疫苗BG505-SOSIP热稳定性,均一性及耐受性的制剂条件。
Step 1: 检测BG505-SOSIP在96中buffer中的解链温度,与BG505-SOSIP在PBS中的Tm(65.7 ℃)进行对比(表3), buffer 9中其Tm增加了6.8 ℃,而buffer 16中Tm降低了10.5 ℃。
Step 2:通过Panta的DLS模块测定了Tm排序前10和后10样品的流体力学半径和多分散性指数PDI。buffer 9中Tm最高,但其流体力学半径和标准偏差都是Tm排序前10中最大的, PDI为0.28表明样品是不均一的*。buffer 57的Tm比buffer 9低2.25℃,但57的流体力学半径为7.18 nm,PDI仅有0.09,表明样品高度均一。因此,buffer 57是目前最佳的制剂条件。
* Note:
PDI<0.1表示样品高度均一0.1<PDI<0.25表示样品均一性较好
PDI>0.25表明样品不均一,出现聚集
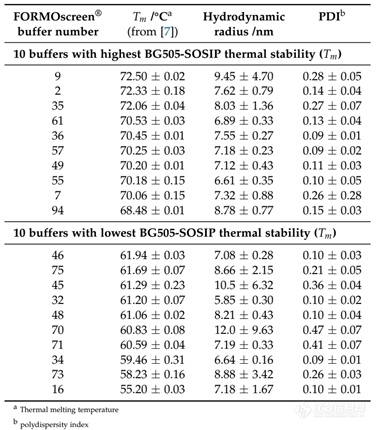
表3. 前10和后10位buffer中Tm及DLS参数
Step 3:加速降解实验。buffer 57对BG505-SOSIP长期稳定性的影响:(1) Thermal Stress: 25,40,60 ℃放置14天;(2) Thermal + Oxidative Stress:过氧化氢处理下25,40,60 ℃放置14天;(3) Mechanical:振荡;(4) Freeze-Stress:冻融。25、40 ℃包括加入过氧化氢放置14天后,BG505-SOSIP的流体力学半径及PDI均无明显变化。仅在60 ℃放置14天后流体力学半径增加一倍,PDI增加至0.3,表明部分样品发生了去折叠。振荡20 min以及5次冻融均未造成影响。结果表明buffer 57非常适合BG505-SOSIP的长期存储(详细信息见原文)。
Panta先通过Tm,Tturbidity进行初筛,缩小制剂范围。随后通过DLS检测选取合适的缓冲液并开展加速降解实验(表4),极大提升了制剂开发效率,降低成本(样品及时间消耗如下图蓝色高亮部分所示)。
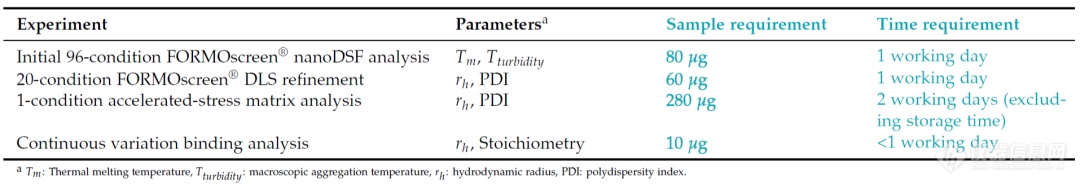
表4. PR Panta制剂筛选消耗样品量及时间
等效验收标准建立
04
蛋白药物可比性研究

doi:10.1016/j.ab.2020.113581IF: 3.191 Q3

Amgen的研究人员使用各种类型的Biologics对PR产品进行了评估,并于今年1月发表在Analytical Biochemistry杂志上。在本文中Amgen的研究人员使用PR建立了等效验收标准,将其定义为重复性的三倍。对在Site1生产和转移到site2之后生产的抗体进行了对比。蓝色曲线为转移后生产的抗体,红色曲线为转移前生产的抗体(图5)。可以看到不同地点生产的抗体的热变性曲线几乎是相同的,并且相同样品的重复性也非常好。
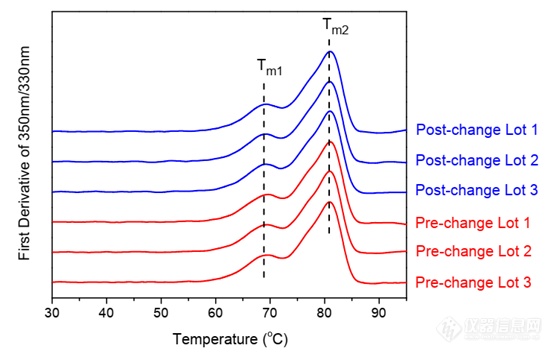
图5. 转移前后抗体热变性曲线
统计学分析结果显示转移前后的抗体的热稳定性是相同的(表5)。之前我们提到等效验收标准EAC是重复性的三倍,这里使用的EAC是0.6 ℃,表明Amgen用PR检测到该样品的重复性为0.2 ℃。
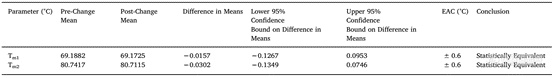
表5. 转移前后抗体统计分析结果
等效验收标准的建立对所用技术的准确性和重复性要求非常高。在本文中Amgen的研究人员使用7种单抗,4种双抗以及2种细胞因子对PR与业内比较认可的金标准DSC进行了对比,结果显示PR检测结果的特异性和准确度完全媲美DSC(图6)。
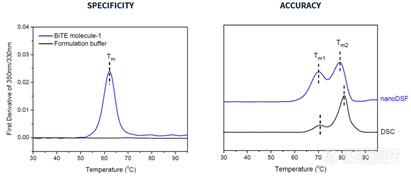
图6. DSC与nanoDSF单抗,双抗检测结果
PR的重复性以及浓度范围则超越了DSC。不同类型或者不同浓度的抗体重复性均在0.2℃以内(图7)。DSC通常检测浓度为0.2-2mg/mL,Amgen在这项研究中使用的样品浓度跨度为0.05mg/mL-74mg/mL,PR的IgG实际测试结果是5 µg/mL to 250 mg/mL。
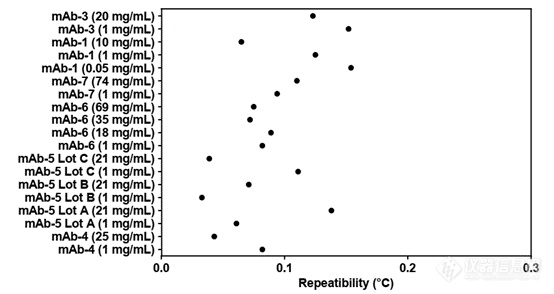
图7. 抗体Fab结构域重复检测结果
PR系列单品单次运行可检测48个样品,每个样品仅需10 μL,70 min完成检测,并且最多能同时获得解链温度Tm,聚集起始温度Tturbidity, 实时流体力学半径rH多种参数。相比于传统DSC技术几百μl样品,近2个小时检测时间,可以极大提升检测效率,降低检测成本。
— PR在生物制剂开发中的贡献 —

— 参考文献 —

Bailly M , Mieczkowski C , Juan V , et al. Predicting Antibody Developability Profiles Through Early

Stage Discovery Screening. mAbs, 2020, 12(1):1743053. Venkataramani S , Ernst R , Derebe M G , et al. In Pursuit of Stability Enhancement of a Prostate Cancer Targeting Antibody Derived from a
Transgenic Animal Platform. Scientific Reports, 2020, 10.

Corinna P, et al. Multi-parameter formulation development for an HIV-vaccine protein with direct validation of epitope binding integrity and stoichiometry. bioRxiv, 2020.

Wen J , Lord H , Knutson N , et al. Nano differential scanning fluorimetry for comparability studies of therapeutic proteins. Analytical Biochemistry, 2020, 593:113581.
下载本篇解决方案:
更多![]()
【设备更新】NanoTemper抗体药物开发实验指南
我们将介绍用于检测生物治疗药物稳定性的各种技术,阐明单克隆抗体配方的来龙去脉,介绍新药临床试验申请(IND)和新药上市申请(NDA)的典型时间线,并深入研究存储条件如何影响单抗稳定性。
制药/生物制药
2023/07/14
【设备更新】生物制剂研究人员必备宝典-DLS动态光散射技术指南
动态光散射(DLS)是一种强大的技术,是一种测量颗粒大小、低聚化和分散性,以及环境变化(如药物偶联物的添加或储存缓冲液的变化)对它们的影响的方法。可提供有关生物制剂制备物的纯度和聚集状态的信息,并增加对候选物稳定性的更深入了解。 阅读DLS技术指南电子书,了解其工作原理,以及它如何帮助您优化候选药物的筛选过程。 我们介绍了在整个生物制药流程中,DLS技术如何帮助您改善每一个决策,同时也提供了一些设计DLS实验的实用技巧。
制药/生物制药
2023/04/06
【设备更新】MST 技术在中药成分靶点检测中的解决方案
中药成分及天然产物的药效是通过与多个靶点的相互作用来实现的,它们与靶蛋白瞬时、弱亲和力相互作用,这种作用机制的复杂性为其靶点鉴定带来很大挑战。 传统的基于亲和力的靶点垂钓方法取决于小分子化合物和靶点蛋白质的亲和力,这种结合需要足够强,以便从整个蛋白质组中分离目标蛋白质,而NanoTemper的微量热泳动技术(MST)检测结合亲和力的范围非常广,可发现从皮摩尔级 (pM) 到毫摩尔级 (mM) 的极强和极弱结合分子。
制药/生物制药
2023/06/25
【设备更新】MST技术在纳米颗粒检测中的解决方案
纳米抗体具有分子小、水溶性好、亲和性和稳定性高、特异性强、易于表达生产且能进一步修饰等优点,在多个领域内都有极大的应用前景。但不同表面特性的纳米粒子与蛋白质之间的相互作用的亲和力等指标,仍然缺乏相关研究。MST 技术是通过激光在溶液中产生精确而短暂的温度变化从而检测配体结合引起的荧光强度变化,结合检测不受由配体结合引起的粒径和分子量变化限制。 对于纳米颗粒与蛋白间的亲和力检测也能轻松应对!
制药/生物制药
2023/06/25














