推荐厂家
暂无
暂无
 留言咨询
留言咨询
 银牌1年
银牌1年
 400-860-5168转6112
400-860-5168转6112
 留言咨询
留言咨询
 留言咨询
留言咨询
 400-860-5168转4076
400-860-5168转4076
 留言咨询
留言咨询
 400-629-8889
400-629-8889
 留言咨询
留言咨询

 400-860-5168转4076
400-860-5168转4076
 留言咨询
留言咨询
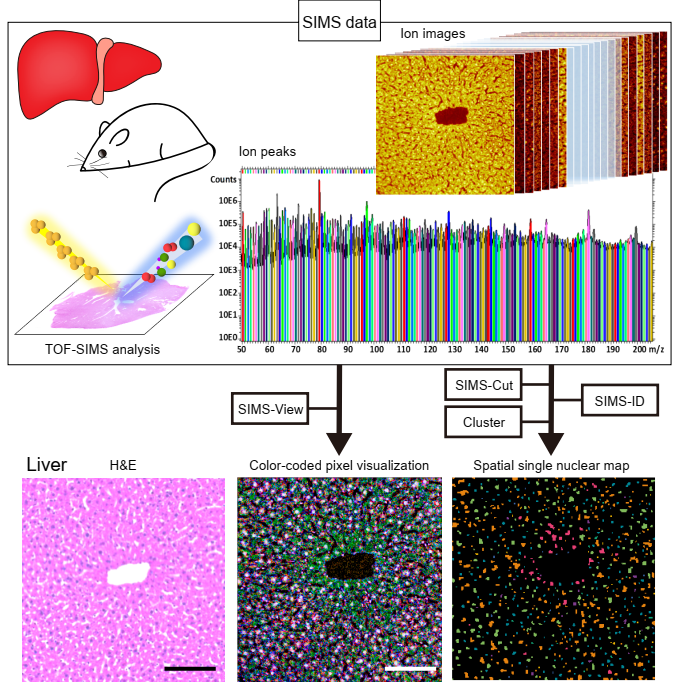



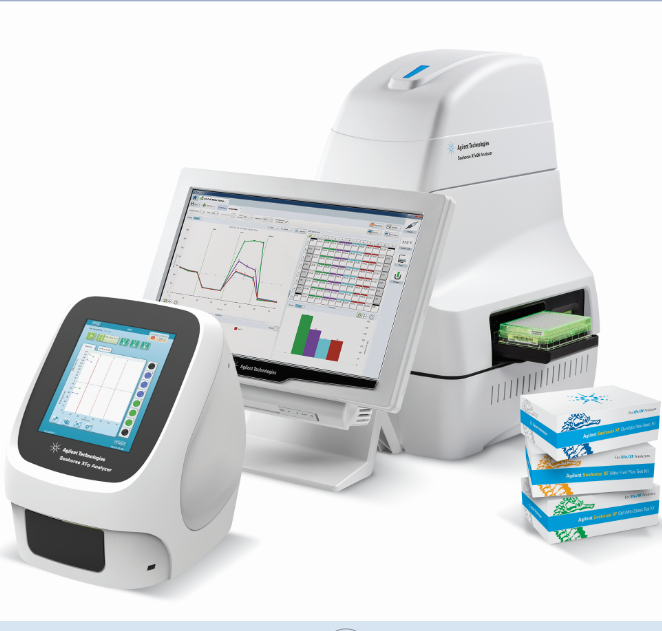
该文该文汇总了单细胞代谢的研究方法,包括质谱 (MS),质谱成像( MS imaging), 毛细管电泳(CE)(其中主要是chip ce), 光谱学(optical spectroscopy),和荧光生物传感器等多种技术手段分析了几百个单细胞,对单细胞进行大分子层面上的表征,以此阐述细胞代谢的表型异质性(phenotypic heteroge-neity)。大概就这个意思吧,大牛的东西,读起来反正就是半懂不懂。
生物质谱技术在细胞生物学中的应用桑志红 王红霞 综述 概 论 蛋白分离与显色 蛋白质鉴定 数据库查寻 灵敏度 具体示例 展望未来(相关文献)摘 要 基因组计划的飞速发展使我们提早进入"后基因组时代",而质谱技术的重要进展使得通过酶解、质量分析、序列分析及其数据库检索对蛋白质进行高通量快速鉴定的技术方法应运而生,并成为"后基因组时代"的关键核心技术。这种技术的应用范围已经从细胞,组织以及整个有机体中蛋白质的表达到蛋白质翻译后修饰等等方面。本文简要综述生物质谱技术在细胞生物学等学科中的应用。 过去的十年经历并见证了生命科学革命性的变化. 大规模基因组测序技术的问世使人类基因组计划最终目标的实现比预期一再提前。与此同时,近几年间已有10余种模式生物的基因组序列测定告罄,3年内还将有40种左右生物的基因组全序列问世。因此大多数人同意我们现在已经提早进入"后基因组时代"(post-genome era), 目前我们所面临的挑战是如何破解基因组计划已获得的大量序列信息并加以应用。这个问题的关键是基因的生物学功能不能只通过对核酸一级结构(序列)的检测来确定。研判一个未知基因的功能、与其他基因产物及其亚细胞结构之间的功能联系, 最终都必须通过在蛋白水平对基因产物的研究才能确定。蛋白质组这个名词是近几年才提出来的,它用来描述一个细胞的全部蛋白质,而在蛋白水平上进行大规模的研究引出了新的术语蛋白质组学。蛋白质表达图谱是依靠蛋白质显示技术和精确定量技术对细胞或组织中蛋白质表达总况进行比较(2), 这个领域最近已有综述(11)。细胞图谱蛋白质组学是指应用生物质谱技术鉴定蛋白质及其相互作用并确定在亚细胞中的定位。本文的目的是 简要综述生物质谱技术在细胞生物学领域中越来越多的应用,并为该领域正考虑应用这种技术的研究者提供一些的有用的信息。 作为一个新的研究领域,蛋白质组学发展的关键是近年来质谱技术的革新。这种革新极大地促进了质谱技术在生命科学研究中的应用。质谱现在可以作为将各种蛋白质与序列数据库联系起来的桥梁。生物质谱根据质量数和所载电荷数不同的多肽片断在磁场中产生不同轨道而以质荷比(m/z)方式来分离它们。80年代末,随着两种崭新的尤其适合蛋白质研究的软电离方式ESI(电喷雾电离)和MALDI(基质辅助激光解吸附电离)的出现,质谱成为现代蛋白质科学中最重要和不可缺少的组成部分。 生物质谱最强大的应用功能之一是能够鉴定蛋白质复合物的组成成分(19)。细胞中一些最重要的生命过程都是通过多蛋白质复合体来执行和调节的,但由于蛋白质鉴定的困难,大多数上述蛋白复合体都是未知的。生物质谱灵敏度的不断提高显著地促进了对具有生物学功能和治疗潜力的蛋白复合体的鉴定,例如,NF-k B信号通路,CD95(FAS/APO-1)介导的细胞死亡途径,和核受体介导的转录信号传导过程中形成的蛋白复合体。在某些情况下,复合物可通过常规蛋白纯化的方法进行纯化,如剪接体复合(25),酵母纺锤体复合物(29)及VHL肿瘤抑制复合物(18)。然而,更常见的是,复合物中的组成成分通过一步免疫沉淀或免疫亲和步骤后就可纯化,这种方法甚至可以用于鉴定那些用常规蛋白纯化和鉴定技术所不及的一些过渡态或不稳定的复合物。因为生物质谱技术的介入,现在已经不再需要通过抗体进行免疫印迹实验,而是通过生物质谱技术对免疫沉淀获得的蛋白复合体组分直接进行蛋白序列分析。以酵母P24复合物鉴定为例,应用上游表位标签策略有可能不需制备抗目标蛋白的抗体就能对蛋白质复合物进行鉴定(13)。这种方法(36)对于基因组序列已完全清楚和遗传稳定的生物(如芽殖酵母,啤酒酵母)尤为简便, 例如对RENT复合物和促有丝分裂后期复合物(49)。因为这种方法的成功应用,使人们对上游表位标签策略-蛋白纯化-生物质谱分析的方法兴趣倍增。值得一提的是,将能被特殊蛋白酶切除的连接子(接头)掺入表位标签是尤为有利的(如下所述)。 上述方法是通过识别蛋白复合物中相互作用和配对的各组分而达到对蛋白鉴定的目的,另一种策略则是通过对分离纯化的细胞器蛋白组成进行鉴定而在亚细胞水平对蛋白质定位. 用这种方法确定蛋白质位置, 对评价蛋白质潜在的功能将是大有帮助的. 应用这种方法,我们称为细胞器蛋白质组学, 已经发现正常工作状态下的细胞器含有比我们以前所知道的数量多得多的蛋白种类。然而实际上,由于质谱极高的分辨率和灵敏度,纯化后的细胞器组分即使只有微量的混杂,也能被质谱分辨并误认为是细胞器的组成部分。因此,如何充分的纯化以保证至少绝大多数被鉴定的蛋白质都来自同一种细胞器,成为制约上述工作的瓶颈。 蛋白质翻译后修饰也是蛋白鉴定工作中的一个重要方面。根据DNA序列信息并不能可靠预测或推导出蛋白质翻译后的修饰。而质谱技术已经被证明对研究蛋白质翻译后的修饰(例如磷酸化和糖基化)是极为有用的,特别是对序列已知的蛋白的鉴定。例如:Betts等人(1a)用这种方法成功地鉴定了从小鼠大脑中分离的神经纤维蛋白体内磷酸化位点。同样方法, Wong等人(45)确定了钙联蛋白质(calnexin)C未端的磷酸化位点。在糖基化的例子中, Carr等人(5)采用液相色谱与质谱联用技术选择性地鉴定了糖蛋白中N- 和O-联接的寡糖. 稍后, 本文将会通过对E-选择素中糖基化位点的鉴定来进一步说明这种方法.
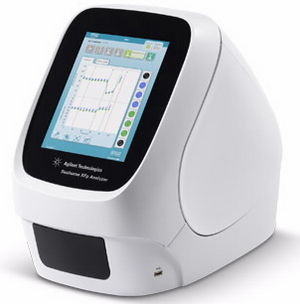
北京华威中仪科技代理的由美国Seahorse Bioscience 公司最新研发的XF生物能量测定仪(细胞代谢呼吸动态分析仪)XF extracellular analyzer是世界首创使用24孔及96孔微孔盘为平台,采用无损伤专利固态探针侦测技术即时同步侦测有氧呼吸O2(OCR)以及糖酵解作H+(OCAR)、 CO2产率(CDPR)的动态分析仪,透过此系统的协助,研究者得以更快的速度、更简易的设计了解细胞以及线粒体如何运用不同的受质作为能量的来源、评估疾病与氧代谢及线粒体运作状态之交互作用、分析代谢调节药物对于生理的效应、建立细胞品管系统、快速筛选出具开发潜力之药物及药物毒性评估等多种不同应用。此系统现已被广泛应用于免疫学、药物筛选、肝脏及外源性毒理、糖尿病及肥胖症、老化、干细胞、细胞生理、药物转化等各个领域,哈佛大学等名校已借助该系统在nature、cell上发表文章几十篇,其他SCI高影响因子文章200多篇,现在就拥有Seahorse Bioscience 公司的细胞代谢呼吸动态分析仪,领先下一个细胞与线粒体研究的黄金十年。